È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Immagini dal vivo di Drosophila melanogaster Migrazioni Hemocyte embrionali
In questo articolo
Riepilogo
Ematociti concentrati Drosophila disperdere sulla totalità dello sviluppo dell'embrione. Questo protocollo dimostra come montare e immagine queste migrazioni uso di embrioni con ematociti concentrati fluorescente.
Abstract
Molti studi sulle cellule migrazione indirizzo utilizzando
Protocollo
Preparazione
- Ottenere adeguate linee di Drosophila contenente un hemocyte specifico GAL4 driver (ad esempio SRP-GAL4 2) e un giornalista geneticamente codificato fluorescenti SUP sotto controllo (ad esempio UAS-GFP). Vola omozigoti per SRP-GAL4, UAS-GMA 3 o CRQ-GAL4, UAS-GFP 4, 5 sono particolarmente utili per scopi di imaging (nb GMA è fuso con la GFP actina dominio di legame moesina), vedi sotto per una discussione di la gamma di GAL4 driver e SUP costruisce disponibili (il Bloomington Archivi Centro contiene una grande varietà).
- Incroci genetici sono tipicamente svolta in modo tale alleli mutanti sono equilibrati con fluorescenti bilanciatori CTG o TTG 6, con GAL4 driver e uas costruisce svolta alternativa cromosomi omologhi. In questo modo è possibile selezionare mutanti omozigoti sulla base di assenza di CTG / TTG associata fluorescenza GFP (questo è avvenuto nella fase 2.11).
- Amplifica le scorte e vola posto in una gabbia che con una piastra di agar succo di mela 7. Le mosche sono necessari almeno due giorni per acclimatarsi alla gabbia che gli embrioni prima di iniziare a sufficienza per essere gettate. In generale twenty vola di ogni sesso dovrebbe essere sufficiente per generare embrioni a sufficienza per l'imaging, ma va notato che le linee differenti hanno differenti gradi di fertilità. Utilizziamo 55 millimetri piastre di Petri che si inseriscono nel fondo di un bicchiere di plastica, forato alla base per consentire il flusso d'aria. I mezzi esatto del prelievo degli embrioni non è importante, ma i tempi sono fondamentali al fine di raccogliere correttamente messo in scena embrioni.
- Raccogliere embrioni da un giorno all'altro piastra di agar succo di mela mantenuta a 25 ° C o da un piatto a tempo. Per questi ultimi ci permettono di solito le mosche porre su una piastra preriscaldata per 4 ore, prima di rimuovere la placca ea metterla a 18 ° C per 15-16 ore prima del montaggio degli embrioni: questo fornisce embrioni da stadio avanzato dal 12 al alla fase 15 di sviluppo. Una piastra durante la notte contiene una maggiore diversità di fasi, ma offre il vantaggio di alti livelli di espressione giornalista fluorescenti ematociti concentrati a causa di un periodo di tempo più lungo a 25 ° C come GAL4-UAS sistema è sensibile alla temperatura.
Procedura
- Sloggiare embrioni dalla piastra di agar succo di mela con una piccola quantità di acqua e una punta morbida pennello. Embrioni sloggiato può essere visto facilmente ad occhio nudo.
- Trasferimento degli embrioni a un filtro cella (Fisher) o fatti in casa basket 7 versando acqua dalla piastra di agar succo di mela nel cesto rinviato un bicchiere per la raccolta acque reflue.
- Ripetere il passo 2,2 finché non siete soddisfatti avete abbastanza embrioni trasferiti dalla piastra di agar succo di mela.
- Lavare gli embrioni in cella di filtro / cestino con acqua.
- Luogo cellula filtro / basket nel coperchio capsula di Petri della piastra di agar succo di mela e aggiungere candeggina abbastanza pulito per sospendere gli embrioni nel filtro cellule / basket.
- Seguire dechorionation degli embrioni in un microscopio dissezione sotto campo chiaro: dechorionation è completa quando le appendici dorsali si sono dissolti, che dovrebbe avvenire entro due minuti.
- Rimuovere celle filtro / cestino embrioni contenenti da la candeggina e lavare con acqua residuo di candeggina. Tutte le tracce di candeggina deve essere rimosso prima di procedere alla fase 2.8. Un trucco per valutare se tutte le candeggina è stato rimosso è quello di cancellare l'acqua residua di colore blu tessuti laboratorio - se non vi è residuo di candeggina il colore blu sarà sbiancato bianco / rosa.
- Asciugare l'acqua residua utilizzando tessuti di laboratorio / mediwipes applicata alla parte inferiore della cellula filtro / basket.
- Mettere una goccia d'acqua in un coperchio di piastra di Petri. Con un pennello fine, raccogliere tutti gli embrioni dechorionated dal cestello embrione e risospendere in la goccia. Accanto a secco gli embrioni aspirando l'acqua con una micropipetta o accuratamente con un panno assorbente laboratorio / mediwipes.
- Una volta che gli embrioni sono stati essiccati, aggiungere una goccia di olio voltalef per coprire tutti gli embrioni. Mettere una seconda goccia d'olio adiacente la goccia contenente gli embrioni. NB: non siamo stati capaci di trovare una sede nel Regno Unito fornitore di olio voltalef; Halocarbon 700 (Sigma), possono essere usati.
- Sotto un microscopio a fluorescenza dissezione selezionare opportunamente messo in scena gli embrioni del genotipo desiderato utilizzando un paio di pinze orologiai (numero 5) da la goccia d'olio. Queste pinze devono essere piegati verso l'interno (Figura 1) al fine di raccogliere gli embrioni senza pungere loro membrana vitellina. Trasferimento degli embrioni selezionati per la goccia d'olio secondo. E 'importante che si è in grado di vedere ematociti concentrati fluorescente del microscopio da dissezione in modo da essere in grado di raccogliere buone immagini al microscopio confocale (Figura 2). Noi di solito montare embrioni fase 13/14 alla migrazione immagine laterale ematociti concentrati sulla linea mediana ventrale o stadio 15 embrioniper l'immagine della motilità di ematociti concentrati seguenti dispersione oltre l'embrione.
- Stick due coprioggetti (18x18mm, spessore 1) alla parte inferiore di un Petriperm / Lumox piatto (Sarstedt), con 2 gocce di olio voltalef, lasciando circa 1 cm tra loro (Figura 3), che saranno utilizzati per sostenere un copri posto sopra gli embrioni, per non schiacciarli. Petriperm piatti (diametro 50mm) contengono un idrofobo, gas-permeabile membrana. Troviamo che i piatti diventano più facili da usare una volta che sono stati usati più volte (piatti possono essere puliti con etanolo al 70% e riutilizzati).
- In campo chiaro sul microscopio dissezione, raccogliere gli embrioni selezionati uno ad uno con la pinza piegate e allinearli lato ventrale e parallelamente al bordo del coprioggetto (Figura 3). E 'possibile allineare fino a 15 embrioni in questo modo, a seconda della destrezza e la vostra pazienza. E 'importante per manipolare gli embrioni delicatamente sia gli embrioni e piatto membrana Petriperm sono fragili e possono essere facilmente rotto.
- Una volta che gli embrioni sono allineati aggiungere una piccola goccia di olio e lasciar diffondere per formare uno strato omogeneo tra le due lamelle. Dopo che l'olio si è diffuso (l'operazione potrebbe richiedere alcuni minuti) verificare che gli embrioni sono ancora in alto lato ventrale. Se gli embrioni sono rotolato leggermente, li riposizionare di nuovo con le pinze.
- Infine, utilizzando una pinzetta (numero 3) posto un coprioggetto (18x18mm, spessore 1) nel corso degli embrioni, che poggiano su due coprioggetto precedentemente aderito. Colla questo coprioggetto al coprioggetto supporta l'utilizzo di smalti per unghie (Figura 3).
- Prendete il piatto Petriperm con embrioni montato al microscopio confocale o grande campo e montare il piatto Petriperm sul palco utilizzando un apposito adattatore. Sia un microscopio in posizione verticale o invertito può essere utilizzato, con l'obiettivo obiettivo di messa a fuoco attraverso il coprioggetto (al contrario attraverso la membrana).
Rappresentante dei risultati:
Questo protocollo descrive come montare embrioni di Drosophila per l'imaging dal vivo di ematociti concentrati sul lato ventrale dell'embrione. Se fatto correttamente sarà facile per generare sia alambicchi o film di ematociti concentrati. Il fattore determinante è il microscopio usato per l'immagine del ematociti concentrati (in particolare la lente obiettiva), ma la natura delle immagini acquisite dipenderà anche dalle fase di sviluppo, la temperatura gli embrioni sono state sollevate in e le linee GAL4 e scuole universitarie professionali utilizzati.
Alti livelli di espressione della proteina fluorescente permetterà ematociti concentrati per essere ripreso con maggiore facilità, quindi è importante essere in grado di vedere ematociti concentrati quando gli embrioni sono in fase di 2,11 del protocollo (figura 2 contiene esempi di ematociti concentrati chiaro all'interno embrioni, scattate con una telecamera montato su un microscopio a dissezione). Numeri quindi aumentato di GAL4 e costrutti UAS permettere un maggiore rapporto segnale-rumore. Inoltre questo riduce la necessità di laser ad alta intensità o tempi di esposizione aumentata quando imaging, che a sua volta permette hemocyte comportamento da seguire per lunghi periodi di tempo.
Livelli molto elevati di espressione GFP apparirà dettagli della morfologia hemocyte, in particolare il sottile foglio-come lamelle che circondano il corpo circolare cella (Figura 4A-B). Regioni circolare esclusi GFP rappresentano fagosomi (Figura 4A-C). Simili a dita filopodia può essere visto anche che emergono dal lamelle (Figura 4B). GAL4 due piloti rimangono sufficiente a vedere questi processi (Figura 4C), soprattutto se uno o più è SRP-GAL4 (vedi la discussione), comunque più lenta velocità di scansione o potenza del laser più grande del microscopio confocale può essere richiesto. Come diminuire i livelli di espressione diventa più difficile per l'immagine del sporgenze di ematociti concentrati, tuttavia esso è ancora possibile seguire la migrazione di ematociti concentrati in queste condizioni, come il corpo cellulare resta evidente anche quando sporgenze sono meno chiare (Fig. 4D).
Nei primi stadi di sviluppo (fino alla fase 13) ematociti concentrati migrare a stretto contatto l'uno all'altro ed è spesso difficile distinguere le singole celle. Entro la fine della fase 13 ematociti concentrati hanno formato una sola linea lungo la linea mediana ventrale (Figura 5A), quindi, diventando sempre più mobili, migrano lateralmente ai bordi del cordone nervoso ventrale (Figura 5B). Il citoscheletro di actina all'interno della dinamica di sporgenze ematociti concentrati può essere direttamente osservata attraverso l'espressione del GMA (Figura 5C) o ciliegio moesina.
Montaggio degli embrioni in questo modo consente lo scambio di gas e previene la disidratazione e gli embrioni rimangono vitali immagini seguenti. Se l'embrione è danneggiato durante il montaggio in genere è ovvio che il contenuto embrione fuga attraverso la sua membrana vitellina. Se un embrione si avvia a disidratarsi allora questo può spesso stato visto da deformazioni della membrana vitellina. Occasionalmente un embrione rotolerà nel corso di un film Timelapse, però questo tende solo ad essere problematico per i film più lunghi tempi. Lastly, montaggio embrioni contemporaneamente dà la sperimentalista le migliori possibilità di ottenere un embrione con l'orientamento ideale per il loro esperimento.

Figura 1. Pinza per la manipolazione di embrioni dechorionated.
Le punte delle pinze orologiai (dimensione numero 5) devono essere piegati verso l'interno al fine di moda uno strumento per raccogliere gli embrioni come mostrato qui. La superficie esterna della regione piegata è utile anche per manipolare gli embrioni quando si posiziona sulla membrana Petriperm in quanto non in possesso di spigoli vivi che potrebbero perforare l'embrione.
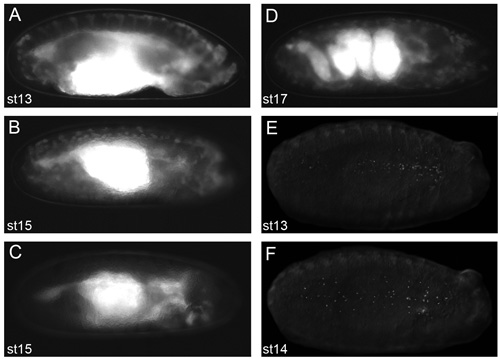
Figura 2. Immagini rappresentative di embrioni che darà buoni risultati di immagini dal vivo.
Immagini di embrioni dechorionated in olio voltalef (al 2,11 del protocollo) assunto un microscopio a fluorescenza dissezione. Vista laterale dello stadio 13 (A) e lo stadio 15 (B) SRP-GAL4, UAS-GFP; CRQ-GAL4, UAS-GFP embrioni. Vista laterale di uno stadio 15 SRP-GAL4, UAS-GFP / +; CRQ-GAL4, embrione uas-GFP/uas-N17Rac (C) in cui ematociti concentrati non sono riusciti a migrare fuori dalla testa, dimostrando che gli embrioni simile a quando ematociti concentrati non sono evidenti lungo le loro rotte migratorie. Vista laterale di uno stadio 17 SRP-GAL4, UAS-GFP; CRQ-GAL4, UAS-GFP embrione mostra la struttura contorto dell'intestino in questa fase di sviluppo (D), la comparsa di contrazione muscolare impedisce immagini dal vivo di embrioni al di là di questo stadio di sviluppo. Vista ventrale della fase 13 (E) e lo stadio 14 (F) SRP-GAL4, UAS-rosso embrioni stinger che mostra la dispersione di ematociti concentrati con nuclei fluorescente. Osservazione dei ematociti concentrati per fluorescenza in fase 2.11 del protocollo è un prerequisito per ottenere immagini eccellenti; anteriore è a destra per tutte le immagini.

Figura 3. Montaggio degli embrioni su un Petriperm / Lumox piatto.
Due coprioggetto 18x18mm (spessore 1) sono attaccati alla faccia inferiore del piatto Petriperm utilizzando una piccola goccia d'olio, separate da circa 1 cm, come mostrato. Gli embrioni vengono poi allineati lato ventrale con il loro asse parallelo lungo (antero-posteriore) ai bordi del coprioggetto e coperto con una piccola goccia di olio. Una volta che l'olio si è diffusa di colmare il divario tra le due coprioggetto un coprioggetto terzo (18x18mm spessore 1) si posa delicatamente sulla parte superiore del petrolio coperta di embrioni utilizzando le due coprioggetto precedentemente aderito come un ponte per evitare che gli embrioni vengano schiacciati. Questo vetrino viene poi incollata ai due ponti coprioggetto utilizzando due piccole gocce di smalto. Una volta impostato, gli embrioni possono essere esposte su un microscopio in posizione verticale o invertita con la lente obiettivo di messa a fuoco attraverso i coprioggetti (anziché attraverso la membrana Petriperm).
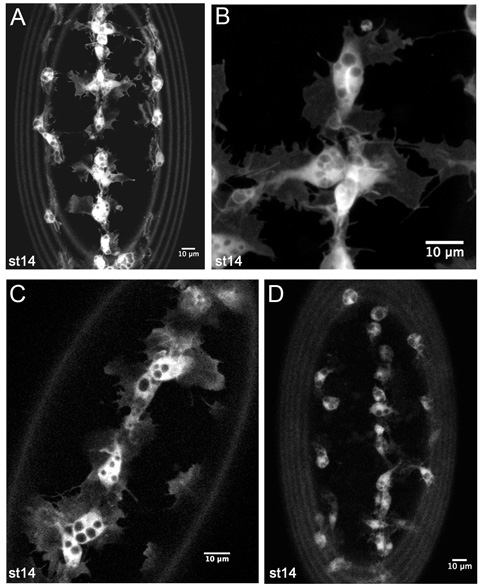
Figura 4. Risultati rappresentativi di immagini dal vivo di ematociti concentrati GFP etichettati.
Z-proiezioni di ematociti concentrati sul lato ventrale di un palcoscenico 14 SRP-GAL4, UAS-GFP; CRQ-GAL4, UAS-GFP embrione (AB). (A) è un'immagine ingrandimento inferiore, come utilizzato per monitorare hemocyte migrazioni di sviluppo nei film Timelapse. (B) è un ingrandimento maggiore ancora di ematociti concentrati sulla linea mediana ventrale, che mostrano dettagli della loro morfologia. (C) è un singolo 1 fetta m ematociti concentrati sulla linea mediana ventrale in uno stadio 14 SRP-GAL4, UAS-GFP / +; CRQ-GAL4, UAS-GFP / + embrione, rivelando che il numero di copie inferiore GAL4 driver e SUP costrutti sono anche sufficienti a generare buone immagini. (D) mostra una proiezione-z ematociti concentrati in uno stadio 14 CRQ-GAL4, UAS-GFP embrione. Qui sporgenze hemocyte sono meno evidenti a causa della minore espressione di GFP, ma è ancora possibile fare film e tenere traccia della migrazione hemocyte con questa combinazione di driver e GAL4 UAS costruire. Le immagini sono state scattate in un microscopio confocale Leica LSM510; anteriore è in tutte le immagini, gli anelli alla periferia di immagini sono causati da autofluorescenza membrana vitellina.

Figura 5. Risultati rappresentativi di immagini dal vivo di ematociti concentrati GMA esprimere.
Z-proiezioni di ematociti concentrati sulla linea mediana ventrale dello stadio 13 (A) e lo stadio 14 (B) SRP-GAL4, UAS-GMA embrioni, presi dai film Timelapse per mostrare le migrazioni di sviluppo di ematociti concentrati. Informazioni dettagliate sulle dinamiche actina può essere ottenuta con l'imaging ingrandimento maggiore di ematociti concentrati GMA esprimere (C). GMA consiste GFP fusa al dominio di legame actina-di filamenti di actina moesina ed etichette. Anteriore è in tutte le immagini, le immagini sono state scattate in un microscopio confocale.
Discussione
Gli elementi più importanti di questa procedura sono la selezione di embrioni sani con ematociti concentrati etichettati in modo chiaro e montare con cura senza danneggiarli. Una volta che gli embrioni sono l'olio alocarburi sono resistenti alla disidratazione e una volta montata può essere ripreso per diverse ore. Nelle nostre mani possiamo ematociti concentrati immagine per tre ore, con disidratazione trascurabile dell'embrione o del foto-danno evidente, prendendo un z-pila di immagini ogni tre minuti sul no...
Riconoscimenti
Questo protocollo è stato sviluppato attraverso il nostro lavoro all'interno e in collaborazione con i laboratori di Paul Martin e Antonio Jacinto. Ringraziamo il Centro archivi Bloomington per il suo servizio eccellente e la comunità Drosophila per continuare a condividere linee di volare. BS è attualmente finanziata da una sovvenzione BBSRC progetto. WW è finanziato da una borsa di studio Career Development Wellcome Trust.
Materiali
| Name | Company | Catalog Number | Comments |
| Cell strainer | BD Biosciences | 352350 | 70μm pores |
| Halcarbon oil 700 | Sigma-Aldrich | H8898 | |
| Lumox/Petriperm dish | Sarstedt Ltd | 96077305 |
Riferimenti
- Brand, A. H., Perrimon, N. Targeted gene expression as a means of altering cell fates and generating dominant phenotypes. Development. 118, 401-415 (1993).
- Bruckner, K. The PDGF/VEGF receptor controls blood cell survival in Drosophila. Dev Cell. 7, 73-84 (2004).
- Dutta, D., Bloor, J. W., Ruiz-Gomez, M., VijayRaghavan, K., Kiehart, D. P. Real-time imaging of morphogenetic movements in Drosophila using Gal4-UAS-driven expression of GFP fused to the actin-binding domain of moesin. Genesis. 34, 146-151 (2002).
- Stramer, B. Live imaging of wound inflammation in Drosophila embryos reveals key roles for small GTPases during in vivo cell migration. J Cell Biol. 168, 567-573 (2005).
- Wood, W., Jacinto, A. Drosophila melanogaster embryonic haemocytes: masters of multitasking. Nat Rev Mol Cell Biol. 8, 542-551 (2007).
- Halfon, M. S. New fluorescent protein reporters for use with the Drosophila Gal4 expression system and for vital detection of balancer chromosomes. Genesis. 34, 135-138 (2002).
- Sullivan, W., Ashburner, M., Hawley, R. S. . Drosophila protocols. , (2000).
- Tepass, U., Fessler, L. I., Aziz, A., Hartenstein, V. Embryonic origin of hemocytes and their relationship to cell death in Drosophila. Development. 120, 1829-1837 (1994).
- Millard, T. H., Martin, P. Dynamic analysis of filopodial interactions during the zippering phase of Drosophila dorsal closure. Development. 135, 621-626 (2008).
- Doerflinger, H., Benton, R., Shulman, J. M., St Johnston, D. The role of PAR-1 in regulating the polarised microtubule cytoskeleton in the Drosophila follicular epithelium. Development. 130, 3965-3975 (2003).
- Olofsson, B., Page, D. T. Condensation of the central nervous system in embryonic Drosophila is inhibited by blocking hemocyte migration or neural activity. Dev Biol. 279, 233-243 (2005).
- Paladi, M., Tepass, U. Function of Rho GTPases in embryonic blood cell migration in Drosophila. J Cell Sci. 117, 6313-6326 (2004).
- Vlisidou, I. Drosophila embryos as model systems for monitoring bacterial infection in real time. PLoS Pathog. 5, e1000518-e1000518 (2009).
- Jacinto, A. Dynamic actin-based epithelial adhesion and cell matching during Drosophila dorsal closure. Curr Biol. 10, 1420-1426 (2000).
- Wood, W., Jacinto, A. Imaging cell movement during dorsal closure in Drosophila embryos. Methods Mol Biol. 294, 203-210 (2005).
- Kunwar, P. S. Tre1 GPCR initiates germ cell transepithelial migration by regulating Drosophila melanogaster E-cadherin. J Cell Biol. 183, 157-168 (2008).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon