Method Article
Consegna dei geni e trasfezione in cellule umane di cancro al pancreas con Epidermal Growth Factor Receptor mirati Nanovectors Progettato a base di gelatina
In questo articolo
Riepilogo
Di tipo B a base di gelatina sistema progettato nanovectors (GENS) è stato sviluppato per la consegna del gene sistemica e trasfezione nel trattamento del cancro al pancreas. Modificato con recettore per l'epidermal growth factor (EGFR), peptide specifico sulla superficie del nanparticles, potrebbero bersaglio sul recettore EGFR e rilasciare plasmide sotto riducendo l'ambiente, come ad esempio elevate concentrazioni di glutatione intracellulare.
Abstract
Più di 32.000 pazienti con diagnosi di cancro al pancreas negli Stati Uniti ogni anno e la malattia è associata a mortalità molto alto 1. Urgente bisogno esiste di sviluppare nuove strategie clinico-terapeutiche traducibile in grado di migliorare le statistiche di sopravvivenza triste dei malati di cancro al pancreas. Anche se la terapia genica nel cancro ha dimostrato un formidabile potenziale, la sfida maggiore è nello sviluppo del sistema di distribuzione sicuro ed efficace, che può portare a espressione del transgene sostenuta.
La gelatina è una delle più versatili biopolimero naturale, ampiamente utilizzati nei prodotti alimentari e farmaceutici. Studi precedenti del nostro laboratorio hanno dimostrato che il tipo B gelatina potrebbe incapsulare fisica del DNA, che ha conservato la struttura superavvolto dell'efficienza di trasfezione plasmide e migliorata al momento della consegna intracellulare. Con thiolation di gelatina, i gruppi sulfidrilici potrebbero essere introdotte nel polimero e si fdisolfuro legame orm all'interno nanoparticelle, che stabilizza il legame disolfuro intero complesso e, una volta è rotto a causa della presenza di glutatione nel citosol, carico utile sarebbe stato rilasciato 2-5. Poli (etilene glicole) (PEG)-GENS modificato, se somministrato nella circolazione sistemica, fornisce la circolazione lungo i tempi e gli obiettivi di preferenza per la massa tumorale a causa della iper-permeabilità della neovascolarizzazione dalla permeabilità maggiore e l'effetto di ritenzione 6. Gli studi hanno dimostrato iper-espressione del recettore del fattore di crescita epidermico (EGFR) su Panc-1 le cellule umane di adenocarcinoma del pancreas 7. Al fine di indirizzare attivamente il cancro del pancreas linea cellulare, peptide specifico EGFR è stato coniugato sulla superficie delle particelle attraverso un distanziale PEG 8.
La maggior parte delle terapie anti-tumorali geni si concentrano sulla gestione dei geni soppressori tumorali, come ad esempio p53 wild-type (WT-p53), per ripristinare la funzione pro-apoptotico nelle cellule 9 10. Nel cancro del pancreas, la maggior parte delle cellule sono le mutazioni nella proteina p53, causando la perdita di attività apoptotica. Con l'introduzione della wt-p53, l'apoptosi potrebbe essere riparato e innesca ulteriormente la morte delle cellule in cellule tumorali 11.
Sulla base delle motivazioni di cui sopra, abbiamo progettato EGFR targeting peptide modificati nanoparticelle tiolati gelatina per wt-p53 consegna del gene e l'efficienza di consegna valutati e trasfezione in Panc-1 le cellule.
Protocollo
1. Estrazione di DNA plasmidi incapsulato rivolti contro l'EGFR Nanoparticelle gelatina
- Sintesi di gelatina tiolati
- Tiolati gelatina sono stati sintetizzati come metodo precedente 2-5, per coniugazione covalente con 2-iminothiolane su gruppi amminici primari di tipo B gelatina. 1 grammo di gelatina è stato sciolto in 100 ml di acqua deionizzata e incubate con 20 mg 2-iminothiolane cloridrato a temperatura ambiente per 15 ore.
- Reagente non reagito è stato rimosso con la dialisi contro 5 mM HCl soluzione, seguita dalla soluzione 1 mM HCl per 3 ore ciascuno. Purificato tiolati gelatina era liofilizzati e conservati a 4 ° C per un ulteriore uso.
- Preparazione di DNA contenenti nanoparticelle
- 200 mg tiolati gelatina è stato dissolto in acqua e pH della soluzione è stata regolata a 7 con l'aggiunta di 0,2 M di NaOH soluzione. 1mg di DNA è stato aggiunto e delicatamente mescolato con una soluzione di gelatina.
- Etanolo refrigerata è stato aggiunto lentamente nella miscela, mentresoluzione mescolando ad alta velocità. Le nanoparticelle sono formate quando composizione del solvente cambiato al 75% soluzione idroalcolica.
- Le nanoparticelle sono state ulteriormente reticolato con aggiunta lenta di 0,1 ml di soluzione 8% (v / v) gliossale. I reagenti sono stati temprati reagito con 0,5 ml di soluzione 0,2 M glicina.
- Nanoparticelle sono stati ultra centrifugati a 16.000 rpm per 30 minuti. I pellet sono stati lavati con acqua deionizzata due volte e nanoparticelle sono state purificate liofilizzati e conservati a 4 ° C.
- Della superficie delle nanoparticelle
- Le nanoparticelle sono stati sospesi in tampone fosfato 0,1 M (pH 7,4) con una concentrazione di 10 mg / ml e incubate con 2 volte il peso di metossi-PEG-succinimidile carbossi metil estere (MPEG-SCM, 2.000 MW Da) o maleimmide-PEG-succinimidile carbossi metilestere (MAL-PEG-SCM, 2.000 MW Da) per 2 ore a temperatura ambiente mescolando lentamente.
- Nanoparticelle pegilato sono stati raccolti con ultra-centrifugazione a 16.000 rpm per 30 minutis. I pellet sono stati lavati con acqua deionizzata due volte e nanoparticelle sono state purificate liofilizzati e conservati a 4 ° C.
- MAL-PEG-SCM nanoparticelle modificate sono state sospese in 0.1M tampone fosfato (pH 6,5) con concentrazione di 10mg/ml e incubate con il 10% del peso del peptide specifico EGFR (YHWYGYTPQNVI-GGGGC) per 6 ore a temperatura ambiente mescolando lentamente.
- Peptide nanoparticelle modificate sono stati raccolti con ultra-centrifugazione a 16.000 rpm per 30 minuti. I pellet sono stati lavati con acqua deionizzata due volte e nanoparticelle sono state purificate liofilizzati e conservati a 4 ° C.
2. Caratterizzazione di EGFR-Target Nanoparticelle
- Dimensione delle particelle e la misura potenziale zeta
Le nanoparticelle sono state sospese in acqua con concentrazione di 1mg/ml. Sospensione è stata analizzata usando Zetasizer Nano (Malvern Inc). Analisi granulometrica è stata effettuata presso un angolo di dispersione di 90 ° a 25 °C. potenziale Zeta è stata misurata a parametri di default di costante dielettrica, indice di rifrazione e la viscosità dell'acqua a 25 ° C. - Microscopia Elettronica a Scansione
Nanoparticelle liofilizzato sono stati montati su supporto in alluminio campione e sputtering rivestite con palladio per migliorare la conducibilità e ridurre anche l'accumulo di cariche. I campioni sono stati osservati per la morfologia della superficie con un emissione di campo 4800 Hitachi microscopio elettronico a scansione a 3 kV. - Spettroscopio di elettroni per l'analisi chimica (ESCA)
Liofilizzati formulazione di controllo, le nanoparticelle modificate pegilato e peptide sono stati analizzati da ESCA. E 'stata eseguita al ESCA Nazionale e Centro di analisi di superficie per i Problemi Biomedici (NESAC / BIO), University of Washington (Seattle, WA).- I campioni sono stati posti nel vuoto ad altissima ed esposto a bassa energia fascio di raggi X, che ha indotto un emissione di fotoelettroni secondari dalla superficie.
- Tracciando numero di elettroni rilevati in funzione di binding di energia, i picchi dello spettro osservato è stato assegnato a ciascuna componenti chimici.
- Analisi ad alta risoluzione di C1s spettri è stato effettuato per determinare l'esatta composizione chimica da idrocarburi (CC o CH a 285mV), etere (CO) presso 286.4mV) e carbonile (C = O a 288,1 mV), e la composizione relativa di ogni funzionalità è stata determinata area sotto la curva.
- Stabilità del plasmide incapsulato
La stabilità del DNA plasmidico incapsulato è stato confermato eseguendo il DNA estratto su gel pre-cast. Le nanoparticelle sono stati digeriti con 0,2 mg / ml proteasi contenenti PBS (30 min a 37 ° C) e 0,2 U / ml di DNAsi (10 minuti a temperatura ambiente) separatamente, simultanea o sequenziale. I campioni sono stati poi caricati su 1,2% gel (GP) (E-Gel, Invitrogen, CA) ad una concentrazione di 100ng/well in un volume 18μL per pozzetto. Nudo plasmide è stato caricato come il controllo e il gel è stato eseguito a 75 V per 30 minuti. Kodak digitale a raggi X del campione (DXS) sistema è stato utilizzato per visualizzare i Bands con transluminescence UV. - Determinazione del carico plasmide
Plasmidi nanoparticelle incapsulato sono stati sospesi a 1mg/ml e digerite con proteasi 0.2mg/ml a 37 ° C per 30 minuti. Soluzione è stata centrifugata a 13.000 rpm per 10 minuti e il surnatante è stato raccolto e testato per la concentrazione plasmide con PicoGreen saggio (Invitrogen). Rapporto di incapsulamento è stato calcolato dividendo la concentrazione incapsulato plasmide con il caricamento iniziale 0,5% (w / w).
3. Studi in vitro Transfection Panc-1 in cellule del pancreas Cancro
- Condizioni di coltura cellulare
Panc-1 e Capan-1 linee cellulari di adenocarcinoma del pancreas, l'adenocarcinoma SKOV3 linea di cellule ovariche e NIH-3T3 murini linea cellulare di fibroblasti sono stati ottenuti da ATCC. Panc-1 e NIH-3T3 sono stati coltivati con DMEM fornito con L-glutamina, Pen-streptococco e il 10% di siero fetale bovino a 37 ° C e 5% di CO 2, mentre Capan-1 in dotazione necessaria DMEM 20% di siero fetale bovino.SKOV3 è stato coltivato in RPMI-1640 in dotazione con il 10% di siero fetale bovino. - Analisi Western blot per l'espressione di EGFR
- Lisati cellulari sono stati raccolti da 2 milioni di cellule e analizzati per la concentrazione di proteine totali con BCA saggio (Pierce). NIH-3T3 è stato utilizzato come controllo negativo e SKOV3 è stato utilizzato come controllo positivo per l'espressione di EGFR.
- 10 mg di estratto proteico totale è stato eseguito su prefabbricati di sodio dodecil solfato-poliacrilammide gel elettroforesi (SDS-PAGE) sistema a 135V per 90 minuti.
- Successivamente, gel è stato trasferito su membrana di PVDF dal Sistema iBlot secco Blotting (Invitrogen).
- Membrana è stata bloccata con il 5% senza grassi del latte contenente Tween-tampone Tris salino (TBS-T) per 1 ora a temperatura ambiente.
- Membrana è stata tagliata e incubato con diluizione 1:1000 di primaria coniglio beta-actina anticorpi e 1:1000 diluizione di anticorpi primari EGFR coniglio separatamente notte a 4 ° C.
- Membrana è stata poi lavato due volte conTBS-t e incubate con 1:2.000 diluizioni di secondario anti-coniglio rafano-perossidasi coniugato IgG in TBS-t per 1 ora a temperatura ambiente.
- Dopo aver sciacquato gli anticorpi in eccesso con TBS-t e acqua, 4 ml di substrato ECL (Pierce, Rockford, IL, USA) è stato aggiunto e incubato con membrane per 5 minuti.
- Bande chemiluminescente sono stati poi visualizzati utilizzando Kodak digitale a raggi X del campione (DXS) del sistema.
- Vitalità studi sulle cellule con formulazioni differenti
- Panc-1 le cellule sono state coltivate in piastre da 96 pozzetti a 10.000 cellule per pozzetto in 200μL di DMEM integrato durante la notte.
- Terreno di coltura è stato sostituito con siero media liberi contenenti diverse concentrazioni di nanoparticelle con 0, 0,5, 1, 2, 4, 6 mg / ml. 1mg/ml PEI, un noto polimero cationico citotossici, è stato utilizzato come controllo positivo.
- Le cellule sono state trattate con nanoparticelle 200μL per 6 ore e poi sostituito con il reagente 20μL MTS e completa 100μLcultura dei media.
- Dopo l'incubazione post per 3 ore a 37 ° C in 5% CO 2, l'estinzione del prodotto formazano è stata misurata a 490nm con Biotek SynergyHT piastra lettore (Winooski, VT).
- La vitalità per cento delle cellule è stato espresso come il rapporto tra assorbanza delle cellule trattate polimero rispetto al controllo negativo (0mg/ml) moltiplicato per 100 e tracciati in funzione delle concentrazioni di polimero.
- Cellula traffico studi
- Rodamina B isotiocianato (RBITC) è stato utilizzato per coniugare il tiolati gelatina per reazione con il gruppo amminico. Dopo la dialisi e liofilizzazione, RBITC etichettati tiolati gelatina è stata utilizzata per la preparazione delle nanoparticelle.
- Prima desolvatazione, 25μL PicoGreen è stato mescolato con 1mg plasmide per 1 minuto e plasmidi etichettati sono stati aggiunti alla soluzione di gelatina. Diverse formulazioni sono state fatte seguendo il metodo precedente.
- Panc-1 le cellule sono state coltivate in 6 pozzetti contenenti vetro di copertura scivola con 200.000 cellule per bene. Dopo una crescita durante la notte, 2 ml di nanoparticelle etichettati sono stati trattati in ciascun pozzetto con una concentrazione nel siero di 1mg/ml media liberi.
- Dopo diversi tempi, da 15 minuti a 6 ore, di media è stato sostituito con terreno di coltura contenente 1μg/ml di Hoest 33342 (Invitrogen) per 15 minuti di incubazione a temperatura ambiente. 2 ml di soluzione di paraformaldeide al 4% è stato sostituito in ogni pozzetto per fissare cellule. Le cellule sono state poi lavate con PBS due volte.
- Coversilps sono stati montati su vetrini. Microscopia confocale a scansione laser a fluorescenza è stato utilizzato per ottenere immagini di cellule fisso.
- Determinazione qualitativa di efficienza trasfezione al microscopio a fluorescenza con pEGFP-N1 incapsulato nanoparticelle
- pEGFP-N1 plasmidi sono stati incapsulati in nanoparticelle e sospeso nel siero media liberi con concentrazione pari a 10μg plasmidi per ml per ulteriori trattamenti.
- Panc-1 le cellule sono state coltivate pernottamento in 6 pozzetti conteNing copertura in vetro-scivola con 200.000 cellule per pozzetto. 2 ml di pEGFP-N1 plasmidi nanoparticelle incapsulato sono stati trattati in ciascun pozzetto. 20μg di plasmidi sono stati mescolati con Lipofectin 20μl, cationici reagenti di trasfezione di lipidi, ed è stato utilizzato come controllo positivo, mentre le cellule non trattate sono state usate come controllo negativo.
- Le cellule sono state incubate con diverse formulazioni per 6 ore.
- Medio è stato sostituito con terreno di coltura e le cellule sono state post-trasfettate per 24, 48, 72 e 96.
- Dopo post-trasfezione, medio è stato sostituito con terreno di coltura contenente 1μg/ml di Hoest 33342 (Invitrogen) e incubati con le cellule per 15 minuti a temperatura ambiente.
- Coprioggetto sono state montate su vetrini ed espressione della GFP nelle cellule è stato osservato al microscopio a fluorescenza. Contrasto interferenziale differenziale (DIC) e le immagini acquisite utilizzando la fluorescenza Olympus BX61 microscopio e le immagini digitali sono state elaborate con software Image J.
- Determinazione quantitativa di efficienza trasfezione mediante ELISA con pEGFP-N1 incapsulato nanoparticelle
- pEGFP-N1 plasmidi sono stati incapsulati in nanoparticelle e sospeso nel siero media liberi con concentrazione pari a 10μg plasmidi per ml per ulteriori trattamenti.
- Panc-1 le cellule sono state coltivate pernottamento in 6 pozzetti con 200.000 cellule per pozzetto. 2 ml di pEGFP-N1 plasmidi nanoparticelle incapsulato sono stati trattati in ciascun pozzetto. 20μg di plasmidi sono stati mescolati con Lipofectin 20μl, cationici reagenti di transfezione lipidi, che è stato utilizzato come controllo positivo e le cellule non trattate sono state usate come controllo negativo.
- Le cellule sono state incubate con diverse formulazioni per 6 ore.
- Medio è stato sostituito con terreno di coltura e le cellule sono state incubate per post-24, 48, 72 e 96.
- Dopo post-trasfezione, lisati di cellule sono stati raccolti da ogni pozzetto e analizzati per la concentrazione di proteine totali con BCA saggio (Pierce).
- pozzetti è stato coaTed con 100μl di 1:1000 diluizioni di anticorpi monoclonali anti-GFP anticorpi in ciascun pozzetto. Dopo incubazione 2 ore, piastra è stato lavato con PBS-0.5% (w / v) di Tween-80 per 4 volte.
- 300μl buffer TBS il blocco sono stati aggiunti in ogni pozzetto e incubare per 2 ore. Poi piastra è stata poi lavata con PBS-0.5% (w / v) di Tween-80 per 4 volte.
- 30 mcg di proteine di ogni gruppo sono stati aggiunti nella piastra ed incubato overnight a 4 °. Poi piastra è stata poi lavata con PBS-0.5% (w / v) di Tween-80 per 4 volte.
- 100μl di diluizioni di 1:2400 secondario anti-GFP anticorpi rispetto alla fosfatasi alcalina sono stati aggiunti a ciascun pozzetto e incubare per 1 ora. Poi piastra è stata poi lavata con PBS-0.5% (w / v) di Tween-80 per 4 volte.
- 100μl substrati fosfatasi alcalina sono stati aggiunti a ciascun pozzetto e incubare per 30 minuti a 1 ora. Piastra è stata misurata con lettore Biotek piastra Synergy HT per assorbanza a 405 nm.
- Concentrazione GFP espresso è stato segnalato come nanogrammi per milligrams delle proteine totali.
- Determinazione qualitativa di efficienza trasfezione mediante RT-PCR con wt-p53 nanoparticelle plasmide incapsulato
- Wt-p53 plasmidi sono stati incapsulati in nanoparticelle e sospeso nel siero media liberi, con pari concentrazione di 10μg ml plasmide per per ulteriori trattamenti.
- Panc-1 le cellule sono state coltivate pernottamento in 6 pozzetti con 200.000 cellule per pozzetto. 2 ml di WT-p53 plasmidi nanoparticelle incapsulato sono stati trattati in ciascun pozzetto. 20μg di plasmidi sono stati mescolati con Lipofectin 20μl, cationici reagenti di transfezione lipidi, che è stato utilizzato come controllo positivo e le cellule non trattate sono state usate come controllo negativo.
- Le cellule sono state incubate con diverse formulazioni per 6 ore.
- Medio è stato sostituito con terreno di coltura e le cellule sono state incubate per post-48 ore.
- mRNA sono stati estratti da ciascun pozzetto utilizzando Alta Pure RNA Kit di isolamento (Roche, Indianapolis, IN) e misurati con NanoDrop 2000 (Thermo scientifico, Wilminton, DE).
- RT-PCR è stata eseguita utilizzando QIAGEN One-step RT-PCR Kit (Qiagen, Valencia, CA). Primer per p53, Bax, Bcl-2, beta-actina, DR5, Apaf-1, PUMA, Survivin sono stati sintetizzati da Eurofins MWG Operon (Huntsville, AL).
- I prodotti di PCR sono stati valutati con elettroforesi su gel e il pixel di bande cDNA sono stati analizzati con il software ImageJ.
- Determinazione quantitativa di efficacia terapeutica con wt-p53 palsmid nanoparticelle incapsulato
- Wt-p53 plasmide è stato incapsulato in nanoparticelle e sospeso nel siero media liberi, con pari concentrazione plasmidi 10μg per ml per un ulteriore trattamento.
- Panc-1 le cellule sono state coltivate pernottamento in 6 pozzetti con 200.000 cellule per pozzetto. 2 ml di WT-p53 plasmidi nanoparticelle incapsulato sono stati trattati in ciascun pozzetto. 20μg di plasmidi sono stati mescolati con Lipofectin 20μl, cationici reagenti di transfezione lipidi, che è stato utilizzato come controllo positivo e le cellule non trattate sono stateutilizzato come controllo negativo.
- Le cellule sono state incubate con diverse formulazioni per 6 ore.
- Medio è stato sostituito con terreno di coltura e le cellule sono state incubate per post-24, 48, 72 e 96.
- La condensazione della cromatina / permeabilità della membrana / Dead Kit apoptosi delle cellule (Invitrogen, Carlsbad, CA) è stato utilizzato per etichettare le cellule apoptotiche, le cellule necrotiche e cellule vive con coloranti diversi.
- iCys Imaging Research Citometro da CompuCyte (Westwood, MA) è stato utilizzato per analizzare e confrontare i livelli di apoptosi dopo il trattamento. Sulla base delle immagini di fluorescenza microscopica, le intensità di tutti i colori è stato registrato e riportato in funzione del conteggio e le percentuali per le diverse popolazioni sono stati calcolati.
- Rispetto al controllo negativo, il che significa che non c'era nessun trattamento per le cellule, le cellule apoptotiche cambiamenti volte sono stati calcolati fuori ed elencati nel grafico.
- Kit di analisi 3.8.8 Apo-ONE omogenea caspasi-3 / 7 (Promega, Madison, WI) è stato utilizzato per esaminare la pro-apoptotici attività dopo la transfezione di wt-p53 plasmide. 1mg/ml PEI è stato utilizzato come controllo negativo per eliminare tutta l'attività apoptotica. Dopo post-trasfezione, le cellule sono state trattate con rodamina 110, bis-(N-CBZL-aspartil-L-glutamil-L-valilico-L-acido aspartico amide; Z-DEVD-R110), che è un substrato della caspasi 3 / 7, per un massimo di 18 ore.
- Piastra è stata misurata con lettore Biotek piastra Synergy HT per fluorescenza a 490/520 nm. Sulla base della intensità di fluorescenza verde, pro-apoptotici attività può essere valutato.
4. Rappresentante Risultati
1. Sintesi e Chatacterization di nanoparticelle EGFR mirate
EGFR targeting peptide modificati nanoparticelle sono stati sintetizzati in cui il regime ha mostrato in figura 1. Le nanoparticelle preparato da desolvatazione sono stati caratterizzati per la dimensione delle particelle e potenziale zeta. La tariffa media grandezza e superficie delle particelle preparati con gelatine tiolaticon diversi gradi di thiolation sono elencati nella Tabella 1. I diametri media delle particelle differenti nanoparticelle sono stati tra i 150-250 nm. Tiolati nanoparticelle più piccole dimensioni rispetto alle nanoparticelle gelatina, potrebbe a causa della formazione disolfuro ponte all'interno particelle. Con modifiche superficie diversa, la dimensione delle nanoparticelle sono aumentati. I potenziali zeta di diverse formulazioni erano circa -20 mV. Con l'analisi SEM, le dimensioni, la morfologia della superficie e la forma sferica di nanoparticelle sono state osservate e corrispondenti al risultato Zetasizer. L'efficienza di carico del DNA in nanoparticelle gelatina e gelatina tiolati nanoparticelle sono stati superiori del 95% (Tabella 1).
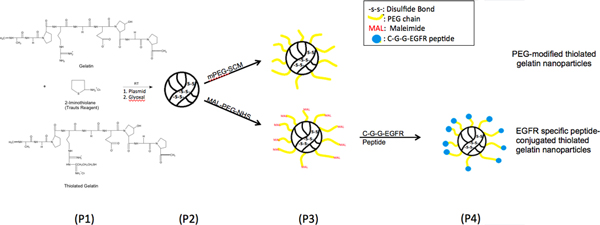
Figura 1. Schema di reazione chimica, la modifica della superficie di illustrare tiolati nanoparticelle gelatina con una crescita epidermico di fattor recettore (EGFR) attraverso un legame peptidico (glicole etilenico) poli (PEG) spacer.
Caratterizzazione di nanoparticelle
| Formulazione | Nanoparticelle Diametro (nm) | Zeta potenziale (mV) | Plasmide Caricamento Efficienza DNA (%) |
| Gel NP | 151,4 ± 23,5 | -17,1 ± 5,23 | 95,6 ± 2,2 |
| SH-Gel NP | 132,6 ± 17,9 | -24,6 ± 5,16 | 97,0 ± 3,8 |
| SH-Gel-PEG | 179,0 ± 30,9 | -22,3 ± 9,50 | 95,8 ± 6,5 |
| SH-Gel PEG Peptide | 230,8 ± 41,5 | -18,1 ± 4,02 | 94,8 ± 5,1 |
TaTavola 1. dimensione delle particelle, carica di superficie, l'efficienza e plasmide DNA incapsulamento di controllo e rivolti contro l'EGFR nanoparticelle tiolati gelatina e gelatina.
Ad alta risoluzione C 1S scansioni di spettroscopia di elettroni per l'analisi chimica (ESCA) è stato utilizzato per analizzare componente superficie di tiolati gelatina (SH-Gel NP), PEG-modificato tiolati gelatina (SH-Gel PEG) ed EGFR-targeting peptide modificato gelatina tiolati nanoparticelle (SH-Gel PEG Peptide). I risultati in tabella 2 ha mostrato intensità di picco della CH (idrocarburi), CO (etere) e C = O (carbonile) gruppi a 285,0, 286,3 e 288,1 eV, rispettivamente. Il segnale CO etere è aumentata dopo la modifica PEG e diminuito dopo coniugazione peptide. Mentre la composizione di azoto è diminuito dopo PEG modifica e l'aumento dopo la modifica del peptide, che ha confermato la presenza di EGFR-targeting peptide sul nanoparticelle. Analisi ESCA ha ulteriormente confermato PEG e la modifica della superficie peptide.
Spettroscopia di elettroni per l'analisi chimica di superficie composizione nanoparticelle
| Formulazione | C 1s (%) | O 1s (%) | N 1s (%) |
| SH-Gel NP | 59,3 ± 0,8 | 22,9 ± 0,5 | 12,9 ± 0,1 |
| SH-Gel-PEG | 58,2 ± 0,6 | 28,0 ± 1,2 | 9,5 ± 0,7 |
| SH-Gel PEG Peptide | 56,7 ± 0,8 | 25,9 ± 0,7 | 12,3 ± 0,6 |
| Formulazione | CC (%) | CO, N (%) | C = O (% ) |
| SH-Gel NP | 51,5 | 26,6 | 21,9 |
| SH-Gel-PEG | 17,1 | 63,1 | 19,8 |
| SH-Gel PEG Peptide | 33,1 | 42,8 | 24,1 |
Tabella 2. C 1S scansioni ad alta risoluzione della spettroscopia di elettroni per l'analisi chimica (ESCA)
Al fine di esaminare la stabilità del plasmide incapsulato, le nanoparticelle sono stati trattati con proteasi o DNAsi separatamente, simuntaneously o sequenziale. Dopo l'elettroforesi, i risultati in figura 2 hanno dimostrato che il DNA plasmide incapsulato in tutte le nanoparticelle sono protetti da nanoparticelle e stabile, paragonabile a nudo il DNA plasmide. Questi studi hanno dimostrato che tutte queste nanoparticelle potrebbero incapsulare e preservare la struttura del plasmide dopo l'incapsulamento.
/ Files/ftp_upload/3612/3612fig2.jpg "/>
Figura 2. Stabilità del DNA plasmidico incapsulato in tiolati gelatina, PEG-modificato tiolati gelatina, EGFR e peptidi modificati tiolati nanoparticelle gelatina mediante elettroforesi su gel di agarosio. Le nanoparticelle sono stati trattati con 0,2 mg / ml di proteasi per dimostrare l'incapsulamento plasmide DNA all'interno della matrice di nanoparticelle
2. Baseline espressione di EGFR nelle cellule tumorali del pancreas
Due linee cellulari umane di adenocarcinoma del pancreas (Panc-1 e Capan-1) sono stati analizzati mediante western blot per l'espressione di EGFR. Adenocarcinoma ovarico umano (SKOV3) e fibroblasti murini ((NIH-3T3) le cellule sono state scelte come controlli positivi e negativi, rispettivamente. Beta-actina è stato analizzato come controllo di caricamento delle proteine. Panc-1 le cellule hanno mostrato l'espressione di EGFR superiore rispetto a Capan-1 e questa linea cellulare è stato poi utilizzato per i successivi studi in vitro
3. Citotossicità di controllo e Surface-Modified tiolati Nanoparticelle Gelatina
Al fine di valutare l'interazione cellulare delle nanoparticelle, test di citotossicità sono state effettuate dopo il trattamento con le nanoparticelle. Sulla base dei risultati in Figura 3, sia il controllo e la superficie modificati nanoparticelle erano relativamente sicuri e biocompatibili in Panc-1 le cellule anche a concentrazioni elevate, con rispetto al PEI. I seguenti studi sono stati condotti con nanoparticelle 1mg/ml.
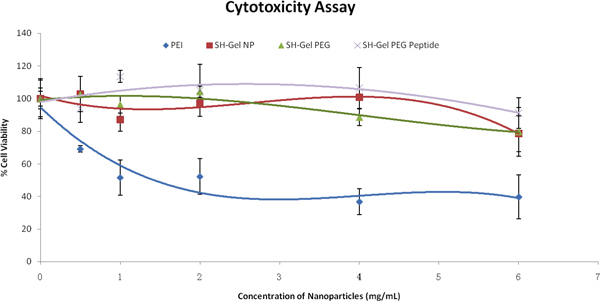
Figura 3. Vitalità cellulare percentuale in funzione delle concentrazioni di formulazione di nanoparticelle in Panc-1 le cellule, come valutato dal colorante tetrazolio (MTS) test
4. Recettore cellulare mediata assorbimento in Panc-1 Cellule
Per confermare l'accessibilità superficie del bersaglio l'EGFR peptide e mediata dai recettori assorbimento intracellulare di nanoparticelle, un sistema di etichettatura è stato progettato da ciascun component con fluorescenza diversi per la visualizzazione di assorbimento di nanoparticelle e il traffico di cellule. Con questo sistema di etichettatura, DNA plasmidico, nanoparticelle e nucleo della cellula è stato possibile identificare. Microscopia confocale a scansione laser a fluorescenza è stato utilizzato per prendere le immagini in diversi momenti, da 15 minuti a 6 ore. Confrontando le immagini di diverse formulazioni, peptide nanoparticelle coniugate gelatina ha mostrato l'assorbimento rapido e il rilascio plasmide entro 30 minuti. Questo ulteriore risultato ha dimostrato che EGFR-peptide coniugato nanoparticelle sono stati sottoposti endocitosi facilitato con interazione rapida tra il peptide specifico EGFR e recettori EGFR sulla superficie delle cellule, che era molto più veloce, rispetto ad altre nanoparticelle, che sono stati sottoposti non specifici endocitosi.
La tratta delle cellule di studio
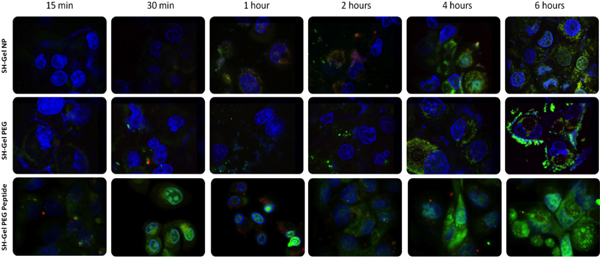
Figura 4. Microscopia confocale a fluorescenza unoANALISI DELLA DNA incapsulato l'assorbimento delle nanoparticelle e il traffico di Panc-1 le cellule. (Rosso = rodamina marcato nanoparticelle, verde = PicoGreen marcato DNA plasmidico e blu = DAPI marcato nucleo). La potenza del laser è stato 7 volte meno negli ultimi quattro figure del pannello inferiore.
5. Qualitativa e quantitativa in Transfection Vitro con Enhanced Green Fluorescent Protein
ELISA nella Figura 5 e analisi al microscopio a fluorescenza in Figura 6 sono stati utilizzati per misurare l'efficienza qualitativa e quantitativa tranfection GFP in Panc-1 dopo somministrazione di cellule modificate, PEG-modificato e EGFR-peptide modificato nanoparticelle tiolati gelatina. Plasmidi forniti da rivolti contro l'EGFR nanoparticelle provocato il più alto livello di espressione della GFP dopo 48 ore rispetto ad altri controlli, tra cui Lipofectin-complessati DNA.
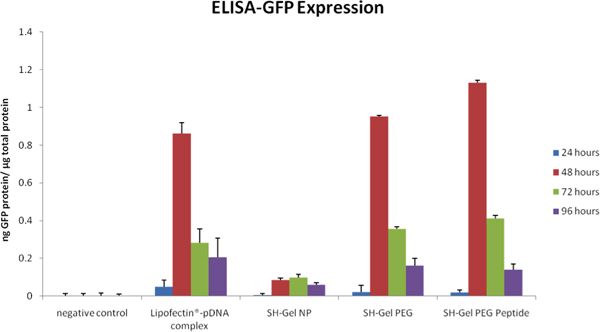
Figura 5. Espressione GFP unonalyzed da ELISA un grafico in funzione del tempo post-somministrazione di DNA plasmidico di controllo e rivolti contro l'EGFR nanoparticelle.
Fluoresence analisi microscopica per la trasfezione GFP
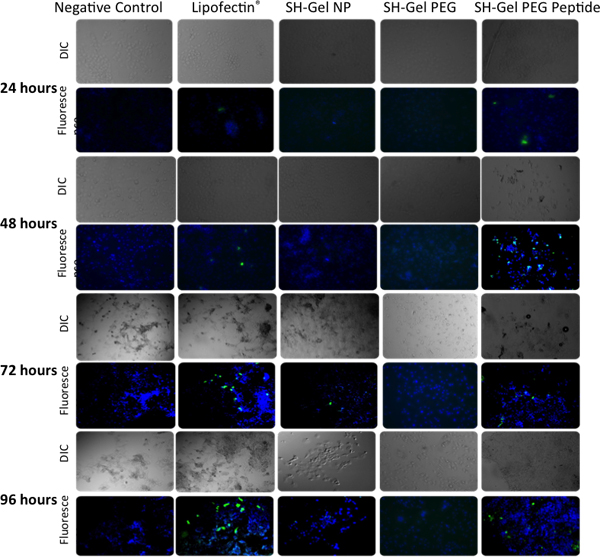
Figura 6. Analisi qualitativa di espressione della proteina verde fluorescente in Panc-1 le cellule al microscopio epifluoresence dopo 24, 48, 72 e 96 ore dopo la trasfezione con EGFP-N1. Lipofectin-DNA complesso è stato utilizzato come controllo positivo.
6. Tranfection In Vitro con wild-type p53 plasmidi in Panc-1 Cellule
Wild-type plasmidi p53 pORF-hp53, con obiettivo EF-1α / HTLV promotore ibrido sono stati estratti da E. coli e incapsulati in nanoparticelle per studiare l'effetto apoptotico terapeutico. Panc-1 le cellule sono state trattate con particelle per 6 ore e post-transfettate per ulteriori 24, 48, 72, e 96 ore.
Dato che p53 può indurre l'apoptosi nelle cellule e per realizzare questa funzione, molti fattori di trascrizione a valle sarebbe coinvolto e direttamente regolata da un'espressione di wt-p53. Tra questi, Bax, caspasi-3, caspasi-9, DR5, PUMA e Apaf-1 sarebbero up-regolati da espressione di p53 e mentre Bcl-2, survivina sarebbe down-regolato. Al fine di esaminare i livelli di questi fattori di trascrizione, mRNA è stato estratto da Panc-1 le cellule dopo 48 ore dopo la trasfezione e utilizzati per RT-PCR. I prodotti sono stati valutati con elettroforesi su gel e fasce sono stati analizzati con ImageJ. Sulla base dei risultati ha mostrato in Figura 7, survivina è diminuito in modo significativo con il trattamento di EGFR mirati nanoparticelle tiolati gelatina rispetto ad altri trattamenti, nessun cambiamento evidente è stato osservato in Bcl-2, Bax e l'espressione della caspasi-3, caspasi-9, DR5, PUMA e Apaf-1increased con trattamento mirato nanoparticelle.
les/ftp_upload/3612/3612fig7.jpg "/>
Figura 7. I livelli di mRNA di fattori a valle della wt-p53 espressione sono stati confrontati mediante RT-PCR dopo 48 ore dopo la trasfezione.
Dopo wt-p53 transfezione, cromatina condensa / permeabilità della membrana / Dead Kit di apoptosi delle cellule è stata utilizzata per differenziare le cellule apoptotiche, le cellule necrotiche e cellule vive con coloranti diversi. iCys Imaging Research Citometro da CompuCyte (Westwood, MA) è stato utilizzato per analizzare e confrontare i livelli di apoptosi dopo il trattamento. Rispetto al controllo negativo, le cellule apoptotiche cambiamenti volte sono stati calcolati fuori ed elencati nella Figura 8. EGFR mirati nanopaticles tiolati gelatina hanno mostrato la più alta popolazione apoptotica delle cellule dopo la post-trasfezione. Analisi delle caspasi 3 / 7 ha anche mostrato che l'attività rivolti contro l'EGFR nanoparticelle aveva internazionalizzazione rapida e più alto livello di attività apoptotica in Panc-1 le cellule.
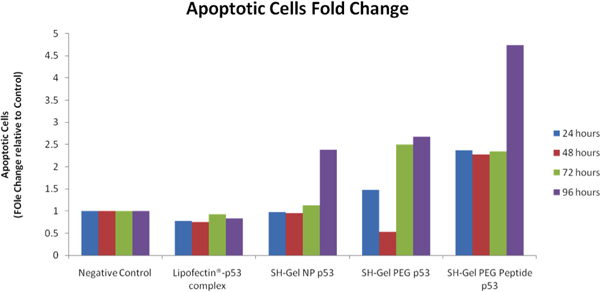
Figura 8. Analisi in citometria di pro-apoptotici in attività di controllo wt-p53 transfettate Panc-1 le cellule utilizzando iCys ° Imaging Citometro
Discussione
Controllo e EGFR mirati nanoparticelle tiolati gelatina sono stati preparati con l'incapsulamento di DNA efficiente e stabilità. Le dimensioni delle particelle di tutti questi sistemi sono stati nel range di 150-250 nm di diametro. Potenziale zeta ha dimostrato che questo sistema è un sistema leggermente negativo. Con l'analisi SEM, le dimensioni delle nanoparticelle sono stati lo stesso con risultato Zetasizer. Analisi ESCA potrebbe confermare PEG e la modifica della superficie peptide.
Analisi Western blot ha mostrato che le cellule Panc-1 ha avuto un alto livelli di espressione di EGFR e questa linea cellulare è stata utilizzata per l'studi in vitro. Sia il controllo e la superficie modificati nanoparticelle sono stati relativamente meno citotossico in Panc-1 le cellule rispetto al PEI.
Studi traffico di cellule ha mostrato un assorbimento rapido e il rilascio di plasmide rivolti contro l'EGFR nanoparticelle in Panc-1 le cellule. Consegna del DNA giornalista plasmidi che esprimono l'EGFR con mirati nanoparticelle portato a più alti livelli diGFP espressione rispetto ad altri controlli, tra cui Lipofectin-complessati DNA. Con lo stesso sistema, trasfezione con wt-p53 plasmide attivato il percorso a valle apoptotico indotto apoptosi e rapido Panc-1 le cellule.
Questi risultati preliminari suggeriscono che le nanoparticelle tiolati rivolti contro l'EGFR gelatina può essere utilizzato come sistema DNA sicura ed efficiente consegna per la terapia genica come trattamento per il cancro al pancreas.
Divulgazioni
Nessun conflitto di interessi dichiarati.
Riconoscimenti
Questo studio è stato sostenuto da Alleanza del National Cancer Institute in Nanotecnologie per Cancer Center per il Cancer Nanotechnology Excellence (CCNE) concedere U54-CA151881.
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente | Azienda | Numero di catalogo | Commenti |
| Tipo B gelatina, Bloom 225 | Sigma-Aldrich | G9391 | |
| 2-iminothiolane cloridrato | Sigma-Aldrich | I6256 | |
| pEGFP-N1 plasmide | Elim Biopharm | N / A | |
| pORF-hp53 E. coli | Invivogen | porf-hp53 | |
| Soluzione gliossale (40wt.% in H 2 O) | Sigma-Aldrich | 128465 | |
| Glicina | Sigma-Aldrich | 410225-250G | |
| QIA filtro plasmidi kit Mega | Qiagen | 12281 | |
| Beckman LE 80K Ultracentrifuga | Beckman | N / A | |
| FreeZone 6 litri Console Fermo Sistemi a secco | Labconco | 7753020 | |
| MPEG-SCM, 2.000 MW Da | Laysan | MPEG-SCM-2K-1g | |
| MAL-PEG-SCM, 2.000 MW Da | Jenkem Tecnologia | A5001-1 | |
| Zetasizer Nano | Malvern | Zetasizer Nano ZS | |
| Hitachi 4800 emissione di campo microscopio elettronico a scansione | Hitachi | S-4800 FE-SEM UHR | |
| Quant-iT PicoGreen dsDNA reagenti e kit | Invitrogen | P7589 | |
| Transfection Reagent Lipofectin | Invitrogen | 18292011 | |
| DMEM | Mediatech cellgro | 10 013 CM | |
| RPMI | Mediatech cellgro | 50 020 PB | |
| Pierce BCA Protein Assay Kit | Thermo Scientific | 23225 | |
| iBlot sistema a secco blotting | Invitrogen | IB1001 | |
| XCell SureLock Mini-Cell e XCell II Blot Module Kit CE Mark | Invitrogen | EI0002 | |
| Pierce ECL Western Blotting Substrato | Thermo Scientific | 32109 | |
| Kodak digitale a raggi X del campione (DXS) Sistema | Kodak | N / A | ; |
| CellTiter 96 AQ ueous Una soluzione Proliferation Assay cellulare (MTS) | Promega | G3580 | |
| Biotek SynergyHT piastra lettore | Biotek | N / A | |
| NanoDrop 2000 | Thermo Scientific | N / A | |
| One-step RT-PCR kit | Qiagen | 210212 | |
| La condensazione della cromatina / permeabilità della membrana / Dead Kit apoptosi delle cellule | Invitrogen | V23201 | |
| Apo-ONE omogenea caspasi-3 / 7 Assay Kit | Promega | G7790 | |
| Hybaid PCR Thermal Cycler Sprint | Thermo Scientific | N / A | |
| EGF Receptor anticorpi | Cellulasegnalazione | 2232 | |
| β-actina anticorpi | Segnalazione cellulare | 4967 | |
| Anti-IgG di coniglio, HRP-linked anticorpi | Segnalazione cellulare | 7074 | |
| Topo anticorpo monoclonale GFP | Novus Biologicals | NB600-597 | |
| Anticorpi policlonali di capra GFP (fosfatasi alcalina) | Novus Biologicals | NB600-1502 | |
| Kit substrato della fosfatasi | Thermo Scientific | 37620 |
Riferimenti
- Vimalachandran, D. Genetics and prevention of pancreatic cancer. Cancer. Control. 11, 6-14 (2004).
- Kommareddy, S., Amiji, M. Preparation and evaluation of thiol-modified gelatin nanoparticles for intracellular DNA delivery in response to glutathione. Bioconjug. Chem. 16, 1423-1432 (2005).
- Kommareddy, S., Amiji, M. Poly(ethylene glycol)-modified thiolated gelatin nanoparticles for glutathione-responsive intracellular DNA delivery. Nanomedicine. 3, 32-42 (2007).
- Kommareddy, S., Amiji, M. Antiangiogenic gene therapy with systemically administered sFlt-1 plasmid DNA in engineered gelatin-based nanovectors. Cancer. Gene. Ther. 14, 488-498 (2007).
- Kommareddy, S., Amiji, M. Biodistribution and pharmacokinetic analysis of long-circulating thiolated gelatin nanoparticles following systemic administration in breast cancer-bearing mice. J. Pharm. Sci. 96, 397-407 (2007).
- Kaul, G., Amiji, M. Tumor-targeted gene delivery using poly(ethylene glycol)-modified gelatin nanoparticles: in vitro and in vivo studies. Pharm. Res. 22, 951-961 (2005).
- Bardeesy, N., DePinho, R. A. Pancreatic cancer biology and genetics. Nat. Rev. Cancer. 2, 897-909 (2002).
- Li, Z. Identification and characterization of a novel peptide ligand of epidermal growth factor receptor for targeted delivery of therapeutics. FASEB. J. 19, 1978-1985 (2005).
- McCormick, F. Cancer gene therapy: fringe or cutting edge. Nat. Rev. Cancer. 1, 130-141 (2001).
- Green, D. R., Kroemer, G. Cytoplasmic functions of the tumour suppressor p53. Nature. 458, 1127-1130 (2009).
- Barton, C. M. Abnormalities of the p53 tumour suppressor gene in human pancreatic cancer. Br. J. Cancer. 64, 1076-1082 (1991).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon