È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Un modello di topi di danno peritoneale indotto da clorexidina gluconato
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Il presente protocollo stabilisce un modello murino di dialisi peritoneale (PD) di fibrosi peritoneale indotta da clorexidina gluconato (CG). Il modello attuale è semplice e facile da usare rispetto ad altri modelli animali PD.
Abstract
La fibrosi peritoneale è un'importante complicanza della dialisi peritoneale (PD). Per indagare e affrontare questo problema, è necessario un modello animale appropriato di PD. Il presente protocollo stabilisce un modello di fibrosi peritoneale indotta da clorexidina gluconato (CG) che imita la condizione di un paziente con PD. La fibrosi peritoneale è stata indotta mediante iniezione intraperitoneale dello 0,1% di CG in etanolo al 15% per 3 settimane (somministrato a giorni alterni), per un totale di nove volte nei topi maschi C57BL / 6. I test funzionali peritoneali sono stati quindi eseguiti il giorno 22. Dopo che i topi sono stati sacrificati, sono stati raccolti il peritoneo parietale della parete addominale e il peritoneo viscerale del fegato. Erano più spessi e più fibrotici se analizzati al microscopio dopo la colorazione tricromatica di Masson. La velocità di ultrafiltrazione è diminuita e il trasporto di massa di glucosio ha indicato un aumento della permeabilità peritoneale indotto da CG. Il modello PD così stabilito può avere applicazioni nel miglioramento della tecnologia PD, nell'efficacia della dialisi e nel prolungamento della sopravvivenza del paziente.
Introduzione
La dialisi peritoneale (PD) è un tipo di terapia sostitutiva renale. Tuttavia, il PD ha problemi che non possono essere risolti. Ad esempio, il trattamento a lungo termine della malattia di Parkinson può causare danni peritoneali, portando infine al fallimento dell'ultrafiltrazione e alla sospensione del trattamento 1,2,3,4,5,6. La fibrosi peritoneale è una delle complicanze più gravi 7,8. La fibrosi peritoneale è caratterizzata dalla deposizione e dall'accumulo di matrice extracellulare all'interno dell'interstizio e dalla neoangiogenesi e vasculopatia del peritoneo 9,10.
Le cause principali di questi cambiamenti peritoneali sono la peritonite ricorrente e la non biocompatibilità del dializzato, che sono iperosmotiche, alto glucosio, basso pH e accumulo di prodotti di degradazione del glucosio11,12. Pertanto, modelli sperimentali animali adatti possono aiutare i ricercatori a studiare meglio i cambiamenti fisiologici e patologici del peritoneo durante la terapia con PD. Pertanto, stabilire un modello animale di PD è importante per migliorare la tecnologia PD e l'efficacia della dialisi e prolungare la sopravvivenza del paziente. Questo studio mirava a generare un modello murino PD mediante iniezione intraperitoneale (i.p.) di clorexidina gluconato (CG), come descritto in precedenza13,14. Questo modello di topo PD è semplice, facile da usare e fattibile rispetto ad altri modelli animali PD.
Protocollo
Tutti gli esperimenti sui topi sono stati approvati dal Laboratory Animal Center dell'E-DA Hospital / I-Shou University e sono stati gestiti secondo la "Guida per la cura e l'uso degli animali da laboratorio" (NRC, USA 2011). Per il presente studio sono stati utilizzati topi maschi C57BL/6, di 7-8 settimane.
1. Preparazione chimica
- Preparare l'irritante chimico diluendo lo 0,1% di clorexidina gluconato (CG, vedi Tabella dei materiali) in etanolo al 15%.
2. Trattamento degli animali
- Assegnare tre topi come gruppo di controllo. Eseguire l'iniezione intraperitoneale (i.p.) di 1 ml/kg di soluzione salina normale allo 0,9% (NS) a giorni alterni per 3 settimane, per un totale di nove volte.
- Assegnare tre topi al gruppo di fibrosi peritoneale. Indurre la fibrosi peritoneale utilizzando clorexidina gluconato (CG) somministrando iniezioni i.p. dello 0,1% di CG in etanolo al 15% (fase 1.1) alla dose di 12,5 μL/g di peso corporeo. Eseguilo a giorni alterni per 3 settimane, per un totale di nove volte.
3. Test di funzionalità peritoneale (test di equilibrio peritoneale modificato)
- Preparare una soluzione di dialisi contenente glucosio al 4,25%. Prelevare 0,5 ml di campione di dializzato con una siringa, quindi controllare la concentrazione di glucosio nel campione di dializzato.
NOTA: La concentrazione di glucosio è determinata secondo il metodo esochinasi/G6PD. I campioni di dializzato sono stati sottoposti al test Glu 2 di tipo L e sono stati studiati con un analizzatore biochimico (vedi Tabella dei materiali). Questa è la concentrazione iniziale di glucosio dializzato. - Anestetizzare i topi mediante iniezione intramuscolare di Zoletil e Xilazina (preparati in un rapporto di 1:2 in volume, vedere Tabella dei materiali) alla dose di 20 μL/20 gw. Inoltre, utilizzare un unguento veterinario sugli occhi per prevenire la secchezza in anestesia.
- Eseguire l'instillazione i.p. della soluzione di dialisi (2 ml/20 g di peso corporeo).
- Dopo 30 minuti, valutare e verificare la profondità dell'anestesia con mancanza di riflesso del pizzico della punta. Quindi, eseguire un'incisione verticale nella linea mediana dell'addome (sotto il processo xifoideo), quindi aprire l'addome dei topi e raccogliere il liquido intraperitoneale con una siringa (definita come "volume 1"). Quindi, misurare il peso di un cotone pulito e asciutto e mettere il cotone nella cavità addominale dei topi per assorbire il liquido intraperitoneale residuo. Infine, misurare nuovamente il peso del cotone.
NOTA: L'aumento di peso del cotone è uguale al peso del liquido intraperitoneale residuo. Quindi, convertire nel volume ottenuto (peso specifico: 1 g / cm3; definito come "volume 2"). Il volume finale del dializzato è il volume 1 più il volume 2. - Utilizzare 0,5 ml di campione di dializzato (dializzato finale) per misurare la concentrazione di glucosio. Questa è la concentrazione finale di glucosio dializzato.
- Calcolare l'ultrafiltrazione netta utilizzando la formula15:
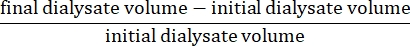
- Calcolare la permeabilità peritoneale utilizzando la seguente formula15:
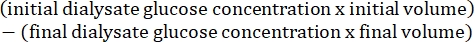
4. Preparazione tissutale del muscolo della parete addominale e del fegato e analisi istologica
- Sacrificare i topi mediante puntura cardiaca (flebotomia)3,16.
- Tagliare la parete addominale (1 cm x 1 cm) ed epatectomia totale. Fissare la parete addominale dei topi e i tessuti del fegato durante la notte in formalina tamponata neutra al 10%.
- Preparare sezioni di paraffina spesse 3 μm del muscolo della parete addominale e del fegato ed eseguire l'analisi istologica seguendo il rapporto17 precedentemente pubblicato.
- Valutare il peritoneo parietale della parete addominale e il peritoneo viscerale delle superfici epatiche dei topi usando la morfometria18.
- Eseguire analisi statistiche utilizzando software di statistica e grafici (vedi Tabella dei materiali). Esprimere tutti i dati come media ± SD e analizzare la significatività statistica utilizzando un t-test19. Definire valori con P < 0,05 come risultati significativi.
Risultati
Nella Figura 1A,B, il peritoneo parietale della parete addominale era marcatamente più spesso e più fibrotico sotto la colorazione tricromatica di Masson17, indicando che nel gruppo esposto a CG, la fibrosi peritoneale è più grave rispetto al gruppo salino di controllo (NS). Nella Figura 2A,B, il peritoneo viscerale delle superfici epatiche era anche marcatamente più spesso e più fibrotico, dimostrando così che nel...
Discussione
In questo studio, un modello di PD murino è presentato mediante iniezione i.p. di CG e i risultati hanno mostrato fibrosi peritoneale e deterioramento funzionale in questo modello, che imitava le condizioni del paziente PD.
Ci sono diversi passaggi critici nel protocollo. In primo luogo, per eseguire un'iniezione i.p. di CG o NS, la pelle della parete addominale del topo deve essere prelevata usando una pinza per prevenire danni agli organi intraperitoneali indotti dalla puntura. In secondo l...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Ringraziamo sinceramente Shin-Han Tseng per la discussione critica e l'esecuzione parziale dello studio. Questo studio è stato supportato da EDAHP110003 e NCKUEDA110002 della Research Foundation dell'E-DA Hospital e della National Cheng Kung University, Taiwan.
Materiali
| Name | Company | Catalog Number | Comments |
| 0.9% Normal Saline | Y F CHEMICAL CORP., New Taipei City, Taiwan | - | |
| 10% neutral buffered formalin | Taiwan Burnett International Co., Ltd., Taipei City, Taiwan | 00002A | |
| Automatic biochemical analyzer | Hitachi Ltd., Tokyo, Japan | Labospect Series 008 | for determining glucose concentration |
| Chlorhexidine digluconate solution, 20% in H2O | Sigma-Aldrich, MO, USA | C9394 | diluted to 0.1% with 15% ethanol for injection |
| Ethanol | Avantor Performance Materials, LLC, PA, USA | BAKR8006-05 | diluted to 15% with normal saline for working concentration |
| Glucose (Dianeal) | Baxter International, Inc., IL, USA | FNB9896 | Commercial dialysis solution (4.25%) |
| GraphPad Prism 8.0 | GraphPad Software, Inc., CA, US | ||
| L-type Glu 2 assay | FUJIFILM Wako, Japan | 461-32403 | |
| Xylazine 20 | Juily Pharmaceutical Co., Ltd., New Taipei City, Taiwan | - | |
| Zoletil 50 | Virbac Laboratories, Carros, France | - |
Riferimenti
- Han, S. H., et al. Improving outcome of CAPD: twenty-five years' experience in a single Korean center. Peritoneal Dialysis International. 27 (4), 432-440 (2007).
- Kawaguchi, Y., Hasegawa, T., Nakayama, M., Kubo, H., Shigematu, T. Issues affecting the longevity of the continuous peritoneal dialysis therapy. Kidney International Supplements. 62, 105-107 (1997).
- Lee, Y. C., et al. Vitamin D can ameliorate chlorhexidine gluconate-induced peritoneal fibrosis and functional deterioration through the inhibition of epithelial-to-mesenchymal transition of mesothelial cells. BioMed Research International. 2015, 595030 (2015).
- Nakamoto, H., Kawaguchi, Y., Suzuki, H. Is technique survival on peritoneal dialysis better in Japan. Peritoneal Dialysis International. 26 (2), 136-143 (2006).
- Schaefer, F., Klaus, G., Muller-Wiefel, D. E., Mehls, O. Current practice of peritoneal dialysis in children: results of a longitudinal survey. Mid European Pediatric Peritoneal Dialysis Study Group (MEPPS). Peritoneal Dialysis International. 19, 445-449 (1999).
- Woodrow, G., Turney, J. H., Brownjohn, A. M. Technique failure in peritoneal dialysis and its impact on patient survival. Peritoneal Dialysis International. 17 (4), 360-364 (1997).
- Schmidt, D. W., Flessner, M. F. Pathogenesis and treatment of encapsulating peritoneal sclerosis: basic and translational research. Peritoneal Dialysis International. 28, 10-15 (2008).
- Augustine, T., Brown, P. W., Davies, S. D., Summers, A. M., Wilkie, M. E. Encapsulating peritoneal sclerosis: clinical significance and implications. Nephron Clinical Practice. 111 (2), 149-154 (2009).
- Di Paolo, N., Nicolai, G. A., Garosi, G. The peritoneum: from histological studies to mesothelial transplant through animal experimentation. Peritoneal Dialysis International. 28, 5-9 (2008).
- Fusshoeller, A. Histomorphological and functional changes of the peritoneal membrane during long-term peritoneal dialysis. Pediatric Nephrology. 23 (1), 19-25 (2008).
- Goffin, E. Peritoneal membrane structural and functional changes during peritoneal dialysis. Seminars in Dialysis. 21 (3), 258-265 (2008).
- Ito, T., Yorioka, N. Peritoneal damage by peritoneal dialysis solutions. Clinical and Experimental Nephrology. 12 (4), 243-249 (2008).
- Io, K., et al. SAHA suppresses peritoneal fibrosis in mice. Peritoneal Dialysis International. 35 (3), 246-258 (2015).
- Yoh, K., Ojima, M., Takahashi, S. Th2-biased GATA-3 transgenic mice developed severe experimental peritoneal fibrosis compared with Th1-biased T-bet and Th17-biased RORgammat transgenic mice. Experimental Animals. 64 (4), 353-362 (2015).
- Karl, Z. J. T., et al. Peritoneal Equilibration Test. Peritoneal Dialysis International. 7 (3), 138-148 (1987).
- Lee, Y. C., et al. The clinical implication of vitamin D nanomedicine for peritoneal dialysis-related peritoneal damage. International Journal of Nanomedicine. 14, 9665-9675 (2019).
- Goldner, J. A. Modification of the masson trichrome technique for routine laboratory purposes. The American Journal of Pathology. 14 (2), 237-243 (1938).
- Cheng, F. Y., et al. Novel application of magnetite nanoparticle-mediated vitamin D3 delivery for peritoneal dialysis-related peritoneal damage. International Journal of Nanomedicine. 16, 2137-2146 (2021).
- Ross, A., Willson, V. L. . Basic and Advanced Statistical Tests: Writing Results Sections and Creating Tables and Figures. , 13-16 (2017).
- Suga, H., et al. Preventive effect of pirfenidone against experimental sclerosing peritonitis in rats. Experimental and Toxicologic Pathology. 47 (4), 287-291 (1995).
- Ishii, Y., et al. An experimental sclerosing encapsulating peritonitis model in mice. Nephrology Dialysis Transplantation. 16 (6), 1262-1266 (2001).
- Nishino, T., et al. Antisense oligonucleotides against collagen-binding stress protein HSP47 suppress peritoneal fibrosis in rats. Kidney International. 64 (3), 887-896 (2003).
- Mishima, Y., et al. Enhanced expression of heat shock protein 47 in rat model of peritoneal fibrosis. Peritoneal Dialysis International. 23 (1), 14-22 (2003).
- Kushiyama, T., et al. Effects of liposome-encapsulated clodronate on chlorhexidine gluconate-induced peritoneal fibrosis in rats. Nephrology Dialysis Transplantation. 26 (10), 3143-3154 (2011).
- Nishino, T., et al. Involvement of lymphocyte infiltration in the progression of mouse peritoneal fibrosis model. Renal Failure. 34 (6), 760-766 (2012).
- Lua, I., Li, Y., Pappoe, L. S., Asahina, K. Myofibroblastic conversion and regeneration of mesothelial cells in peritoneal and liver fibrosis. The American Journal of Pathology. 185 (12), 3258-3273 (2015).
- Kitamura, M., et al. Epigallocatechin gallate suppresses peritoneal fibrosis in mice. Chemico-Biological Interactions. 195 (1), 95-104 (2012).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon