Case Report
Gastrectomia prossimale laparoscopica a singola incisione più una porta con anastomosi a doppio canale per il trattamento del cancro gastrico
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
La gastrectomia prossimale laparoscopica a singola incisione più una porta con anastomosi a doppio canale è stata inizialmente impiegata per la resezione radicale del carcinoma gastrico prossimale. Questo studio ha dimostrato la fattibilità della procedura e ha gettato le basi per ulteriori ricerche.
Abstract
La gastrectomia prossimale laparoscopica a singola incisione più una porta con anastomosi a doppio canale (SILT-DT) è un approccio chirurgico minimamente invasivo per il trattamento del carcinoma gastrico prossimale. Questa tecnica comprende la resezione laparoscopica completa dello stomaco prossimale, la dissezione linfonodale e l'anastomosi a doppio tratto. Integrando la chirurgia laparoscopica a porta singola con un foro operatorio ausiliario, SILT-DT riduce le difficoltà procedurali facilitando il posizionamento di un tubo di drenaggio addominale. Rispetto alla tradizionale gastrectomia laparoscopica a cinque vie, la SILT-DT richiede un minor numero di porte e comporta una lunghezza delle incisioni più breve, contribuendo a ridurre il dolore postoperatorio e a un recupero più rapido. È stata condotta un'approfondita valutazione preoperatoria per garantire il successo della procedura, con fattori quali le dimensioni del tumore, lo stadio, la posizione e l'IMC del paziente. Questa valutazione completa ha permesso una selezione ottimale dei pazienti e una pianificazione chirurgica. Il follow-up postoperatorio non ha dimostrato complicanze significative, sottolineando la sicurezza e l'efficacia di SILT-DT. Questa tecnica innovativa offre una promettente alternativa minimamente invasiva per la gestione del carcinoma gastrico prossimale, mantenendo al contempo eccellenti risultati clinici.
Introduzione
Le tecniche laparoscopiche sono recentemente diventate una delle principali direzioni per il trattamento chirurgico del cancro gastrico 1,2. La chirurgia laparoscopica di routine per il cancro gastrico viene eseguita principalmente con il metodo a 5 fori. Con i progressi delle tecniche chirurgiche e i continui miglioramenti dei dispositivi medici, la chirurgia laparoscopica del cancro gastrico a porta ridotta si è gradualmente sviluppata per ridurre ulteriormente il trauma chirurgico, minimizzare il disturbo della cavità addominale e accelerare il recupero postoperatorio 3,4,5,6.
Omori7 ha riportato per la prima volta un intervento chirurgico laparoscopico laparoscopico per carcinoma gastrico distale nel 2011. La gastrectomia radicale laparoscopica pura a porta singola per il cancro gastrico è più difficile della tradizionale gastrectomia laparoscopica a cinque vie. Per risolvere questo problema, alla procedura laparoscopica a porta singola viene aggiunto un foro operativo ausiliario, che riduce la difficoltà dell'operazione e facilita il posizionamento di un tubo di drenaggio addominale 8,9. La chirurgia laparoscopica a singola incisione più una porta (SILS+1), una tecnica minimamente invasiva per i pazienti con carcinoma gastrico, ha guadagnato popolarità negli ultimi anni grazie al numero ridotto di porte e alle lunghezze di incisione più brevi.
Attualmente, la chirurgia laparoscopica a porta singola o SILS+1 per carcinoma gastrico è relativamente comune nella gastrectomia distale, mentre la sua applicazione nella gastrectomia totale è rara. Inoltre, non è stato riportato l'uso dell'anastomosi totale laparoscopica del carcinoma gastrico del doppio tratto.
Sulla base di ciò, abbiamo prima tentato la gastrectomia prossimale laparoscopica totale a porta singola più una porta con anastomosi a doppio tratto (SILT-DT). La porta transombelicale è stata utilizzata come porta operativa principale e la porta di drenaggio addominale superiore sinistro è stata utilizzata come porta operativa ausiliaria. Questa tecnica è stata impiegata per eseguire la gastrectomia prossimale, la dissezione linfonodale D2 e l'anastomosi del doppio tratto per la ricostruzione del tratto digestivo.
PRESENTAZIONE DEL CASO:
Il paziente, un uomo di 63 anni, è stato ricoverato in ospedale dopo che un tumore è stato scoperto alla giunzione esofagogastrica durante una gastroscopia (Figura 1). I risultati della biopsia del gastroscopio hanno suggerito un adenocarcinoma moderatamente differenziato (Figura 2). Le scansioni TC avanzate del torace e dell'addome preoperatorie non hanno rivelato alcuna evidenza di metastasi a distanza (Figura 3). Il paziente era precedentemente sano e non aveva una storia di chirurgia addominale.
Selezione dei pazienti
I pazienti erano idonei a partecipare se avevano adenocarcinoma della giunzione gastroesofagea di Siewert di tipo II o III istologicamente confermato, con TC addominale preoperatoria che non mostrava linfonodi ingrossati intorno allo stomaco o metastasi a distanza. Il diametro massimo del tumore doveva essere inferiore a 3 cm e la distanza tra il polo inferiore del tumore e l'angolo gastrico doveva superare i 5 cm. I criteri di esclusione includevano i pazienti che avevano precedentemente subito un intervento chirurgico addominale, quelli con un diametro del tumore preoperatorio superiore a 3 cm e/o che necessitavano di resezione multiviscerale, i pazienti che erano stati sottoposti a discussioni di gruppo multidisciplinare (MDT) in merito alla chemioradioterapia neoadiuvante o quelli che avevano ricevuto chemioradioterapia neoadiuvante e i pazienti con intolleranza alla chirurgia laparoscopica.
Protocollo
L'operazione ha seguito le procedure standard e ha ricevuto l'approvazione etica. Questo studio è stato autorizzato dal Comitato Etico dell'Ospedale Centrale di Xiangyang, affiliato all'Università delle Arti e delle Scienze di Hubei. Il consenso informato scritto è stato ottenuto dal paziente. I contenuti e i metodi della ricerca hanno aderito alle norme e ai requisiti di etica medica. I reagenti e le attrezzature utilizzate nello studio sono elencati nella Tabella dei materiali.
1. Passaggi pre-chirurgici
- Il paziente è stato istruito ad assumere sale di fosfato di sodio orale per la preparazione intestinale un giorno prima dell'intervento chirurgico. Il paziente ha digiunato per 8 ore e gli è stata consentita l'assunzione di acqua fino a 2 ore prima dell'intervento. Prima di entrare in sala operatoria è stato inserito un sondino gastrico superiore.
- Il paziente è stato posizionato in posizione supina a gamba divisa con la testa sollevata e leggermente inclinata a destra.
- È stata eseguita l'intubazione endotracheale e l'anestesia generale è stata somministrata secondo i protocolli approvati istituzionalmente.
2. Procedura chirurgica
- Intorno all'ombelico è stata creata un'incisione trasversale di 3,0-3,5 cm per inserire la porta SILS dotata di quattro trocar integrati (Figura 4A). Un ulteriore trocar da 12 mm è stato inserito nel quadrante superiore sinistro per fungere da porta operativa per gli strumenti chirurgici, tra cui il taglio a ultrasuoni, la suturatrice lineare endoscopica e il tubo di drenaggio postoperatorio.
- Un coltello a ultrasuoni è stato utilizzato per sezionare il tessuto linfoide adiposo dei gruppi 1, 2, 3, 4, 7, 8a, 9 e 11p (Figura 5A, B). È stata assicurata una lunghezza inferiore del segmento esofageo di circa 5-7 cm (Figura 5C) ed è stata mantenuta la libertà della curvatura maggiore e minore dello stomaco.
NOTA: La procedura SILT-DT è illustrata nella Figura 5. La dissezione dello stomaco e dei linfonodi è stata eseguita in conformità con le Linee Guida per la Chirurgia Laparoscopica per il Cancro Gastrico (edizione 2023)10. Sono state completate una linfoadenectomia D2 e una gastrectomia prossimale. - È stata stabilita l'anastomosi esofago-digiuno (EJ). Il sito dell'anastomosi EJ è stato identificato sul digiuno, 20 cm distalmente al legamento di Treitz e vicino all'esofago inferiore. L'anastomosi EJ è stata eseguita attraverso la porta da 12 mm nel quadrante superiore sinistro utilizzando una suturatrice lineare endoscopica da 60 mm (Figura 5D).
NOTA: Il diagramma schematico che illustra la ricostruzione del tubo digerente è mostrato nella Figura 4B. - Una suturatrice lineare endoscopica da 60 mm è stata utilizzata per resecare campioni dell'esofago e chiudere l'apertura anastomotica tra il digiuno e l'esofago (Figura 5E).
- È stata creata l'anastomosi gastrodigiunale (GJ), con il sito segnato sul digiuno 8-15 cm distale all'anastomosi EJ e sulla parete posteriore della curvatura maggiore dello stomaco rimanente (Figura 5F).
- L'anastomosi digiuno-digiunale è stata stabilita. L'anastomosi digiunodigiunale è stata praticata attraverso l'incisione di 3,5 cm all'ombelico utilizzando una suturatrice lineare endoscopica da 60 mm, segnando 5 cm distalmente al sito dell'anastomosi GJ (Figura 5G).
- Le singole anastomosi sono state chiuse e rafforzate. Entrambe le aperture comuni dell'anastomosi GJ e dell'anastomosi digiunodigiunale sono state chiuse utilizzando un filo micro Joe 3-0. Lo iato mesangiale era chiuso con una sutura continua.
- Un tubo di drenaggio è stato posizionato dietro l'anastomosi EJ ed è uscito dall'addome superiore sinistro (Figura 5H).
3. Gestione postoperatoria
- È stato implementato il digiuno postoperatorio con acqua e il sondino gastrico è stato drenato con una sacca a permanenza.
- Il sondino gastrico è stato rimosso dopo 48 ore di osservazione, garantendo l'assenza di presenza evidente di liquido di drenaggio sanguinolento.
- L'infusione di liquidi è stata somministrata per mantenere l'equilibrio di acqua, elettroliti e acido-base, insieme alla soppressione acida. La durata degli antibiotici profilattici è stata limitata a un massimo di 48 ore.
- La mobilizzazione precoce è stata promossa attivamente entro 6-24 ore dopo l'intervento. Durante il recupero è stata avviata una dieta liquida per 2-3 giorni.
- È stata valutata la perdita anastomotica e lo sviluppo dello stomaco residuo è stato valutato attraverso la radiografia del tratto gastrointestinale superiore il giorno 7.
- Il tubo di drenaggio della cavità addominale è stato rimosso entro 5-7 giorni dalla dimissione dall'ospedale.
Risultati
L'intervento chirurgico è stato completato entro 150 minuti, con un sanguinamento intraoperatorio minimo di 5 ml. Non ci sono state complicanze a breve termine e il recupero postoperatorio del paziente è stato positivo. Sono stati recuperati un totale di 24 linfonodi e non sono state riscontrate metastasi linfonodali. Il tempo operatorio è stato di 150 minuti e la perdita di sangue stimata è stata di 5 ml. Il paziente è rimasto a letto per 2 giorni. Il tempo per il primo flatulenza è stato di 70 ore e il paziente ha iniziato a consumare cibi e bevande liquidi dopo 3 giorni. Il tubo gastrico è stato rimosso il 4° giorno e il tubo di drenaggio è stato rimosso entro 7 giorni. Il mezzo di contrasto è persistito nello stomaco residuo per 30-50 minuti senza reflusso nell'esofago (Figura 6). L'esito estetico delle incisioni addominali postoperatorie è stato soddisfacente (Figura 4C). Il dolore è stato valutato da una scala di valutazione numerica (NRS) a 11 punti, dove 0 è nessun dolore e 10 è il peggior dolore immaginabile,11. I dati dettagliati per il paziente sono presentati in Table 1.
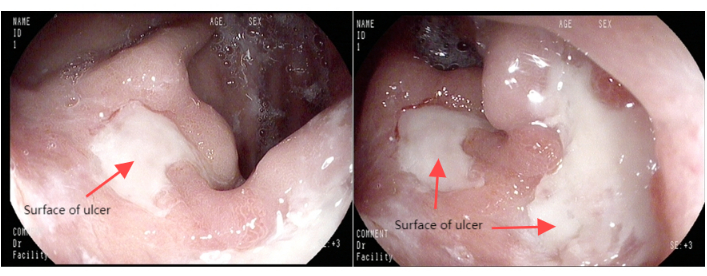
Figura 1: Immagini gastroscopiche. Clicca qui per visualizzare una versione più grande di questa figura.
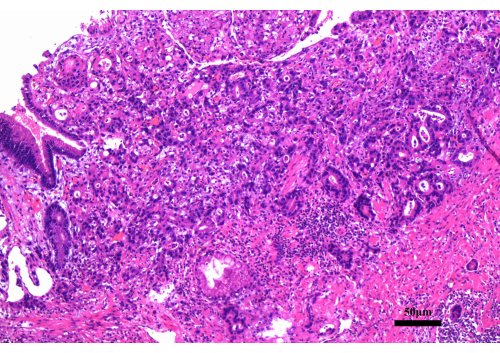
Figura 2: I risultati della biopsia gastroscopica. La biopsia gastroscopica ha rivelato un adenocarcinoma moderatamente differenziato. Barra di scala: 50 μm; ingrandimento: 200x. Clicca qui per visualizzare una versione più grande di questa figura.
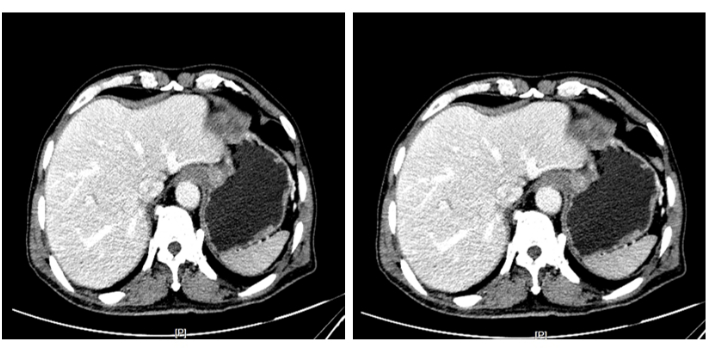
Figura 3: TAC addominali migliorate. Un enhancement eterogeneo è stato osservato nel cardias, che è stato considerato una lesione neoplastica, e il tumore non ha invaso lo strato muscolare. Clicca qui per visualizzare una versione più grande di questa figura.
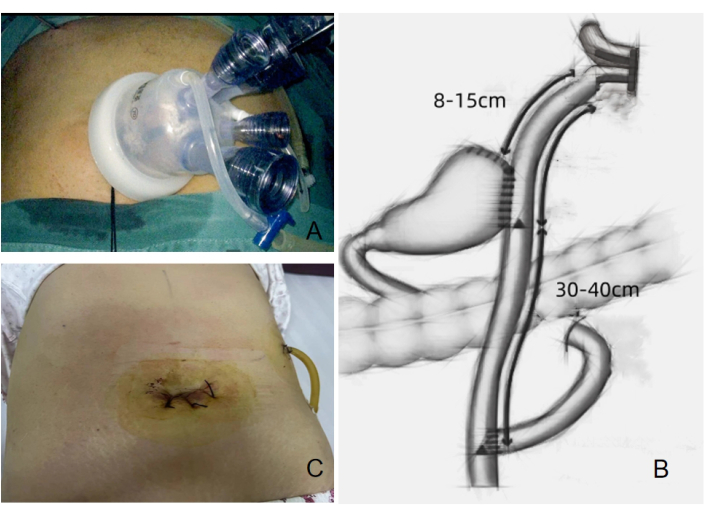
Figura 4: Impostazione chirurgica e condizione della ferita postoperatoria. (A) Quattro trocar incorporati utilizzati nella procedura. (B) Anastomosi del doppio tratto eseguita durante l'intervento chirurgico. (C) Condizioni postoperatorie della ferita mostrate dopo la procedura. Clicca qui per visualizzare una versione più grande di questa figura.
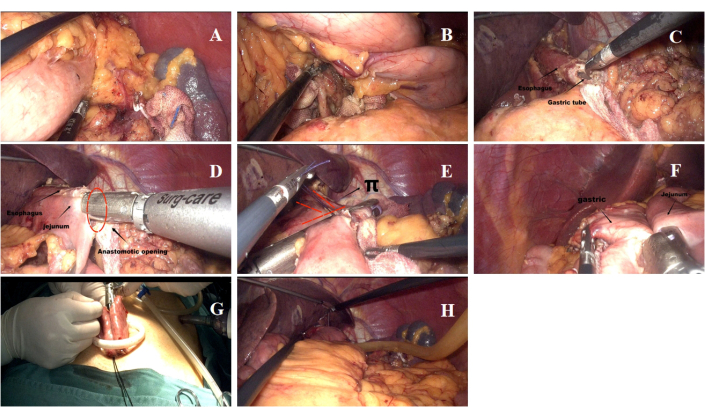
Figura 5: Dettagli della procedura chirurgica. (A,B) Il processo di pulizia dei linfonodi durante l'intervento chirurgico. (C) Transezione dell'esofago e apertura dell'estremità esofagea inferiore. (D) Esofagodigiunostomia laterale eseguita come parte dell'anastomosi. (E) Chiusura dell'apertura comune nel sito di anastomosi esofagodigiuno. (F) Gastrodigiunostomia residua completata. (G) Anastomosi entero-intestinale da lato a lato eseguita attraverso l'incisione ombelicale. (H) Posizione del tubo di drenaggio. Clicca qui per visualizzare una versione più grande di questa figura.
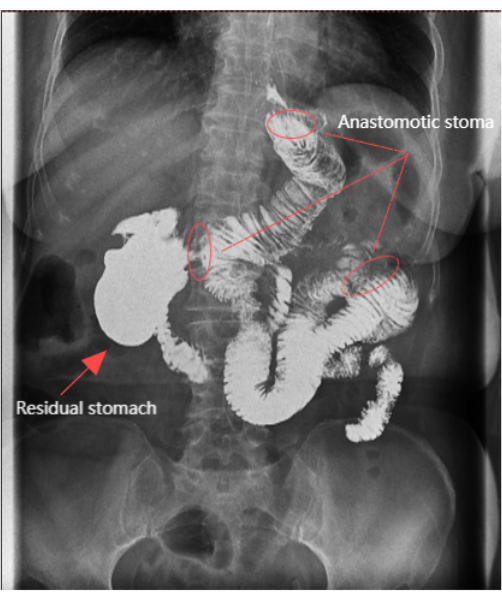
Figura 6: Radiografia del tratto gastrointestinale superiore. La radiografia del tratto gastrointestinale superiore ha mostrato che l'anastomosi era aperta e lo stomaco rimanente era chiaramente visibile. Clicca qui per visualizzare una versione più grande di questa figura.
| Elementi | Risultato |
| Genere | Maschio |
| Anno | 63 |
| BMI (kg/m2) | 23.5 |
| Grado di anestesia | III |
| Stadiazione TNM preoperatoria | cT1N0M0 |
| Tempo di funzionamento (min) | 150 |
| Lunghezza dell'incisione (cm) | 2.8 |
| Volume di sanguinamento intraoperatorio (mL) | 5 |
| Patologia | adenocarcinoma moderatamente differenziato |
| La distanza del margine prossimale (cm) | 3.4 |
| La distanza del margine distale (cm) | 5.5 |
| Dimensione del tumore (cm) | 1.5*2*1.2 |
| Il numero di linfonodi recuperati | 24 |
| Messa in scena TNM | pT2N0M0 |
| La durata della rimozione del sondino gastrico dopo l'intervento chirurgico (d) | 4 |
| La durata fino al pasto iniziale | 3 |
| La durata dell'attività a letto | 2 |
| La durata alla flatulenza (h) | 70 |
| Il tempo per la evacuazione (d) | 6 |
| La durata del tubo di drenaggio (d) | 7 |
| Punteggio del dolore il primo giorno dopo l'intervento chirurgico | 2 |
| Degenza ospedaliera postoperatoria (giorno) | 8 |
| Complicazioni | Nessuno |
Tabella 1: Dati perioperatori del paziente. Dettagli relativi ai dati perioperatori per il paziente, comprese le misurazioni e gli esiti chiave.
Discussione
La gastrectomia radicale laparoscopica a porta singola e ridotta è diventata un approccio innovativo per il trattamento del cancro gastrico e sta guadagnando costantemente accettazione. Queste tecniche stanno ricevendo maggiore attenzione per i loro vantaggi, tra cui migliori risultati estetici, riduzione del dolore postoperatorio, minor rischio di infezioni del sito chirurgico e tempi di recupero più rapidi.
I risultati di 12 studi che hanno coinvolto 343 casi hanno dimostrato che la chirurgia laparoscopica a porta singola e a porta ridotta era efficace nel trattamento del carcinoma gastrico distale, rappresentando la maggior parte dei casi 3,4,12,13,14,15,16,17,18,19,20,21 . Tuttavia, solo quattro studi si sono concentrati sulla resezione gastrica totale 22,23,24,25. Questi risultati suggeriscono che la ricerca clinica e l'applicazione della chirurgia del cancro gastrico a porta singola, in particolare la gastrectomia totale, sono limitate a causa dell'elevata difficoltà chirurgica, dell'ampia dissezione e rimozione dei linfonodi richieste e della complessa tecnica di ricostruzione endoscopica del tratto digestivo.
Abbiamo eseguito con successo la prima gastrectomia prossimale laparoscopica con anastomosi a doppio tratto utilizzando una singola incisione più una porta per il trattamento del carcinoma gastrico prossimale. Rispetto ai metodi chirurgici tradizionali, la chirurgia a singola incisione più una porta è più minimamente invasiva. Rispetto alla tecnica a porta singola, l'aggiunta della porta addominale superiore sinistra migliora la praticità durante l'operazione e consente il posizionamento razionale di un tubo di drenaggio attraverso un'incisione nell'addome superiore sinistro.
Lee et al.26 hanno riportato il primo caso di gastrectomia prossimale laparoscopica a porta singola con ricostruzione a doppio tratto per carcinoma gastrico precoce nel 2016. Rispetto alla SILS, la chirurgia a singola incisione più una porta include un'ulteriore porta addominale superiore sinistra, creando una struttura triangolare composta dalla regione ombelicale, dall'addome superiore sinistro e dall'area chirurgica. Questo approccio innovativo affronta efficacemente i limiti della chirurgia a singola incisione pura, come l'inadeguata anti-trazione e la visualizzazione lineare. Inoltre, migliora la flessibilità dello strumento della mano destra del chirurgo, portando a miglioramenti significativi nell'efficienza operativa e a una riduzione della complessità durante ogni anastomosi in laparoscopia totale.
Inoltre, diverse strategie possono migliorare l'efficienza operativa e ridurre la durata della procedura. Il chirurgo può prendere in considerazione la possibilità di modificare il loro posizionamento durante la dissezione linfonodale e la ricostruzione del tratto digestivo, come posizionarsi sul lato sinistro del paziente o tra le gambe del paziente, per ottimizzare l'esposizione dell'area chirurgica. Per procedure come l'esofagodigiunostomia e la gastrodigiunostomia, si raccomanda che un assistente o il capo chirurgo mantenga una posizione stabile mentre un altro esegue l'aggancio, migliorando così l'efficienza dell'anastomosi e riducendo al minimo il rischio di avulsione dei tessuti. Inoltre, si consiglia l'utilizzo di strumenti laparoscopici integrati per ridurre al minimo l'interferenza tra le fibre ottiche e altri strumenti.
In sintesi, la gastrectomia prossimale laparoscopica a singola incisione più una porta con anastomosi a doppio canale è fattibile per il trattamento del carcinoma gastrico prossimale. In questo caso, il paziente ha sperimentato un recupero di successo. L'operazione è minimamente invasiva e il recupero è più rapido. Tuttavia, i limiti di questo protocollo includono la necessità di cancro gastrico in fase iniziale o tumori gastrici benigni, con un BMI del paziente non eccessivamente alto. L'applicazione di questo protocollo non è raccomandata per i pazienti con malattia localmente avanzata o BMI elevato a causa del potenziale rischio di margini tumorali positivi e di una maggiore complessità chirurgica. Questo protocollo è ancora in fase di esplorazione tecnica, senza linee guida stabilite e dati clinici insufficienti per convalidare pienamente la sua efficacia a lungo termine. Lo sviluppo di questo protocollo richiede l'approvazione etica da parte delle istituzioni mediche e il rigoroso rispetto delle indicazioni chirurgiche. Sono necessarie ulteriori ricerche ed esplorazioni cliniche per determinare l'applicabilità clinica della tecnica SILT-DT.
Divulgazioni
Gli autori non hanno conflitti di interesse o legami finanziari da divulgare.
Riconoscimenti
Questo lavoro è stato sostenuto da sovvenzioni del Progetto di ricerca scientifica della Commissione sanitaria della provincia di Hubei e del Progetto chiave di Xiangyang per la scienza e la tecnologia in campo medico e sanitario (2021YL15).
Materiali
| Name | Company | Catalog Number | Comments |
| 3D laparoscope | KARL STORZ SE & Co. KG | 26605BA | |
| Absorbability surgical sutures | Johnson & Johnson | TLBJXZ | |
| Absorbable ligature clip | Hangzhou KANGJI Medical Instrument co., LTD | KJ-JZJ02ML | |
| Disposable puncture device | Hangzhou KANGJI Medical Instrument co., LTD | Type IV sets F | |
| Disposable step type endoscopic cutting stapler and nail bin | Nanjing Maidixin Medical Device Co.,Ltd | MLCR-Mb,MLCNC-60b-purple, MLCNC-45b-white | |
| laparoscopic instruments | Hangzhou KANGJI Medical Instrument co., LTD | ||
| Ultrasound knife | INNOLCON, Medical Science and Technology (suzhou) co., LTD |
Riferimenti
- Bray, F., et al. Global cancer statistics 2018: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 68 (6), 394-424 (2018).
- Chevallay, M., et al. Cancer of the gastroesophageal junction: A diagnosis, classification, and management review. Ann N Y Acad Sci. 1434 (1), 132-138 (2018).
- Omori, T., et al. A randomized controlled trial of single-port versus multi-port laparoscopic distal gastrectomy for gastric cancer. Surg Endosc. 35 (8), 4485-4493 (2021).
- Kang, S. H., et al. Postoperative pain and quality of life after single-incision distal gastrectomy versus multiport laparoscopic distal gastrectomy for early gastric cancer - a randomized controlled trial. Surg Endosc. 37 (3), 2095-2103 (2023).
- Teng, W., et al. Short-term outcomes of reduced-port laparoscopic surgery versus conventional laparoscopic surgery for total gastrectomy: A single-institute experience. BMC Surg. 23 (1), 75 (2023).
- Podda, M., Saba, A., Porru, F., Pisanu, A. Systematic review with meta-analysis of studies comparing single-incision laparoscopic colectomy and multiport laparoscopic colectomy. Surg Endosc. 30 (11), 4697-4720 (2016).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surg Endosc. 25 (7), 2400-2404 (2011).
- Teng, W., et al. Comparison of short-term outcomes between single-incision plus one-port laparoscopic surgery and conventional laparoscopic surgery for distal gastric cancer: A randomized controlled trial. Transl Cancer Res. 11 (2), 358-366 (2022).
- Du, G. S., et al. Single-incision plus one-port laparoscopic gastrectomy versus conventional multi-port laparoscopy-assisted gastrectomy for gastric cancer: A retrospective study. Surg Endosc. 36 (5), 3298-3307 (2022).
- Chinese Society of Laparoscopic and Endoscopic Surgery, C. S. S., Chinese Medical Association, Association, R. a. L. S. C. O. C. R. H., Endoscopic and Robotic Surgical Society, C. a.-C. A., Endoscopy and Minimally Invasive Technology Society, C. a. O. M. E. Guideline for laparoscopic gastrectomy for gastric cancer (2023 edition). Chinese J Digest Surg. 22 (4), 425-436 (2023).
- Hjermstad, M. J., et al. Studies comparing numerical rating scales, verbal rating scales, and visual analogue scales for assessment of pain intensity in adults: A systematic literature review. J Pain Symptom Manage. 41 (6), 1073-1093 (2011).
- Park, D. J., Lee, J. H., Ahn, S. H., Eng, A. K., Kim, H. H. Single-port laparoscopic distal gastrectomy with d1+β lymph node dissection for gastric cancers: Report of 2 cases. Surg Laparosc Endosc Percutan Tech. 22 (4), e214-e216 (2012).
- Ahn, S. H., Jung, D. H., Son, S. Y., Park, D. J., Kim, H. H. Pure single-incision laparoscopic d2 lymphadenectomy for gastric cancer: A novel approach to 11p lymph node dissection (midpancreas mobilization). Ann Surg Treat Res. 87 (5), 279-283 (2014).
- Ahn, S. H., Son, S. Y., Jung, D. H., Park, D. J., Kim, H. H. Pure single-port laparoscopic distal gastrectomy for early gastric cancer: Comparative study with multi-port laparoscopic distal gastrectomy. J Am Coll Surg. 219 (5), 933-943 (2014).
- Kim, S. M., et al. Techniques of the single-port totally laparoscopic distal gastrectomy. Ann Surg Oncol. 22 (Suppl 3), S341 (2015).
- Jeong, O., Park, Y. K., Ryu, S. Y. Early experience of duet laparoscopic distal gastrectomy (duet-ldg) using three abdominal ports for gastric carcinoma: Surgical technique and comparison with conventional laparoscopic distal gastrectomy. Surg Endosc. 30 (8), 3559-3566 (2016).
- Kim, S. M., et al. Comparison of single-port and reduced-port totally laparoscopic distal gastrectomy for patients with early gastric cancer. Surg Endosc. 30 (9), 3950-3957 (2016).
- Lee, B., et al. Learning curve of pure single-port laparoscopic distal gastrectomy for gastric cancer. J Gastric Cancer. 18 (2), 182-188 (2018).
- Omori, T., et al. The safety and feasibility of single-port laparoscopic gastrectomy for advanced gastric cancer. J Gastrointest Surg. 23 (7), 1329-1339 (2019).
- Kang, S. H., et al. Long-term outcomes of single-incision distal gastrectomy compared with conventional laparoscopic distal gastrectomy: A propensity score-matched analysis. J Am Coll Surg. 234 (3), 340-351 (2022).
- Lee, S., et al. Intracorporeal modified delta-shaped gastroduodenostomy during 2-port distal gastrectomy: Technical aspects and short-term outcomes. Ann Surg Treat Res. 105 (3), 172-177 (2023).
- Ahn, S. H., Park, D. J., Son, S. Y., Lee, C. M., Kim, H. H. Single-incision laparoscopic total gastrectomy with d1+beta lymph node dissection for proximal early gastric cancer. Gastric Cancer. 17 (2), 392-396 (2014).
- Ertem, M., Ozveri, E., Gok, H., Ozben, V. Single incision laparoscopic total gastrectomy and d2 lymph node dissection for gastric cancer using a four-access single port: The first experience. Case Rep Surg. 2013, 504549 (2013).
- Lee, I. Y., Lee, D., Lee, C. M. Case report: Single-port laparoscopic total gastrectomy for gastric cancer in patient with situs inversus totalis. Front Oncol. 13, 1094053 (2023).
- Luo, Y., et al. A novel single-port robot for total gastrectomy to treat gastric cancer: A case report (with video). Asian J Endosc Surg. 17 (2), e13292 (2024).
- Lee, C. M., et al. Single-port laparoscopic proximal gastrectomy with double tract reconstruction for early gastric cancer: Report of a case. J Gastric Cancer. 16 (3), 200-206 (2016).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon