Method Article
薬物過敏症におけるIgEが介在する機序の解明のための好塩基球の活性化試験
要約
好塩基球の活性化の試験は、IgE依存性のアレルギーを検出するための強力なツールです。 in vitroで。ここでは、好塩基球の活性化のテスト用に最適化されたプロトコルは、薬物過敏症を調査するために使用されます。共有結合薬剤 - タンパク質複合体とその物理化学的特性評価の効率的な製造方法について説明する。
要約
propyphenazone(PP)とジクロフェナクのような非ステロイド性抗炎症薬(NSAIDs)(DF)に対する過敏性反応は、アレルギー反応1 I -のような形として現れることができます。臨床の現場では、薬剤過敏症の診断は、主に皮膚テストは信頼性と経口誘発試験患者2の生命を脅かすリスクを負担ではないとして、患者の病歴によって実行されます。したがって、基本的なIgEを介する病態のための証拠を得るのは難しいです。
ここで、我々は、in vivoでのアレルギーエフェクター反応を模倣する薬剤過敏患者由来のヒト好塩基球の使用に基づいて、in vitroの方法に存在する。薬剤アレルギー患者の好塩基球は、犯人の薬剤のためのIgE分子が特定運ぶように、彼らは、IgE受容体の架橋によって活性化され、アレルギーのエフェクター分子をリリースとなる。好塩基球の活性化は、フローサイトメトリー3を使用してCD63の表面発現のアップレギュレーションの測定によりモニターすることができます。
低分子量の薬物の場合には、複合体は、好塩基球のIgEレセプターの架橋を可能にするように設計されています。 図1に示すように、非ステロイド性抗炎症薬の代表2名、PPとDFは、共有結合リジン残基の一級アミノ基と反応カルボキシル基を介してヒト血清アルブミン(HSA)にバインドされています。カルボキシル基含有PPの誘導体はorganochemically事前調査1に合成されなければならなかったのに対し、DFは、このように、直接4に使用できる固有のカルボキシル基とを、運びます。
蛋白質の担体分子の低分子量化合物とその空間分布の結合度は、2つのIgE受容体分子の架橋を保証することが重要です。ここで説明するプロトコルは、シーケンシャルな屈折率(RI)と結合度の測定のための紫外線(UV)検出システムを搭載した高性能サイズ排除クロマトグラフィー(HPSEC)が適用されます。
説明される方法は他の薬に適用される場合がありますので、好塩基球活性化テスト(BAT)は、薬物過敏症におけるIgE媒介機構の決定に使用される可能性を負いません。 BATによる非IgE媒介としてここでは、IgEを介するとDF過敏症としてPPの過敏症を決定する。
プロトコル
1。薬物コンジュゲートの調製
- 1.5 mlの反応チューブに10 mgのDF 1ミリリットルのdH 2 Oに溶解する。さらに先に進むには、このDFのソリューションの95μlを使用してください。 HSAにPPコンジュゲートするには、500μlの0.3 Mの水酸化ナトリウム(NaOH)の30.4 mgをPP誘導体(304 g /モル)を溶解する。
- (N -モルホリノ)エタンスルホン酸(MES)緩衝液に溶解したDFの6.5から95μlを- 430.6μLのdH 2 Oと100μlの0.5Mの2を追加。 PPのサンプルに33.1μLのdH 2 Oおよび2 M MES緩衝液pH 2.9の140μlを添加する。
- 新しく調製したN -エチル- N'の57.5μlを加え、 - DFのサンプル〜100 mg / mlの、またはに10μlのEDC溶液の濃度とOのdH 2に溶解した(3 -ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC)ストック溶液PPのサンプル。ボルテックスで1分間のサンプル。
- 各サンプル〜118 mg / mlの濃度でHSA溶液の16.9μlを加え。
- 300ラウンド/分で振とうしながら室温で2時間サンプルをインキュベートする。
- 数時間ごとにDFとPPのサンプルをリン酸緩衝生理食塩水(PBS)pH7.4の2リットルに対して3回透析。 4℃で、すべての透析の手順を実行します。
- 14,000 xgでサンプル10分間遠心し、上清を含むDFまたはHSAに結合したPPを収集する。
- 12%ゲルを用いて、SDS - PAGEを行うことにより、タンパク質の上清を確認してください。 oneゲルのスロットにHSA抱合体の約12μgをロードします。
2。薬物複合体の結合率を決定する(図2)
- HPSECでDFとPPの複合体の結合率の分析のために150mMのNaCl及び0.05%アジ化ナトリウムを含む100mMリン酸ナトリウム緩衝液pH6.5を使用してください。 7.8 × 300ミリメートルTSK - GEL - G2000 SWXLの列を使用してください。
- オンライン結合RIとUV検出器システムを使用して信号の検出を行います。
- のdH 2 O中に1 mg / mlの濃度でHSAの標準サンプルを準備する検出器のキャリブレーションのために50μlのHSAの標準溶液を注入する。
- RI定数kのRIおよび検出器のためのUV定数kのUVを計算する。式の領域のRIを使用= k個のRI * [(DN / DC)HSA * C(HSA)]とエリアUV = K UV * [(DA / DC)HSA * C(HSA)]と(DN / DC)HSA = 0.185と(DA / DC)HSA = 0.518 5。
- DFとの両方の規格の5、10、および30 nmol収量を容易に注入できることをHPSEC用PP派生規格を準備します。
- 薬と両方の規格のための(DA / DC) 薬 (DN / DC)の値を平均計算する。 DFの場合は、39.000の0.235の(DN / DC)± 0.010と(DA / DC)± 0.493を決定した。 PPの場合は、53.155の0.328の(DN / DC)± 0.016と(DA / DC)± 2.464を決定した。
- HPSECの薬物複合体を注入し、それらのRIとUVピーク面積を決定する。
- = kのRI * [(DN / DC) 薬 * C(薬)+(DN / DC)HSA * C(HSA)]とエリアのUV二つの方程式の領域のRIを解くことによってDF、PP誘導体、およびHSAの濃度を計算する= K UV * [(DA / DC) 薬 * C(薬)+(DA / DC)HSA * C(HSA)]未知数のため。
3。薬物複合体を使用してBAT
- sevenフローサイトメトリーのバイアルを準備し、その内容に応じて、それらにラベルを付ける:未染色のコントロール、ネガティブコントロール、ポジティブコントロール、および薬物複合体を。
- ピペット染色およびネガティブコントロール用に予約されたバイアルにB - CCR - STBの刺激バッファー(Flow2 CAST、Bühlmann研究所、Schönenbuch、CH)の50μlの。ポジティブコントロールとして、Flow2 CASTキットで提供される抗FcεRI溶液50μlを使用してください。 0.02 -20μg/ mlのDF共役とPP共役(200μlのアッセイ体積中の最終濃度)から1:10希釈系列を作成することにより、薬物複合体のために予約バイアルに共役ソリューションの適切な量を追加。これらの滴定実験は、各患者サンプルに対して最適な好塩基球活性化の濃度を決定するために実行する必要があります。
- 各チューブに、50μlの患者のEDTA全血に100μlの刺激のバッファを追加。慎重にサンプルを混ぜる。
- ピペット20μlのFlow2 CAST染色コエリスリン(PE)と各チューブにフルオレセインイソチオシアネート(FITC)で標識した抗CD63抗体で標識した抗CCR3抗体を含む試薬、再度混ぜる。未染色標本に染色試薬をピペッティングしないでください!
- 37℃の水浴中で45分間サンプルをインキュベートする。
- 5分間氷上で反応を停止します。
- 静かに各バイアルおよび渦に試薬を溶解し2.0ミリリットルFlow2のCASTを追加することにより、赤血球を溶解する。室温で10分間暗所でサンプルをインキュベートする。
- 5 500 × gで分間、注意深く上清をデカントのためにサンプルを遠心する。
- フローサイトメトリーするまで氷上で500μlのFlow2 CASTの洗浄バッファーとストア内の細胞を再懸濁する。
- フローサイトメーターの電圧sを調整する前方および側方散乱光(FSC、SSC)のためのettings未染色標本を獲得しながら。
- ゲートのセルは、SSC - FSCのプロットからSSC - PEのプロットへのリンパ球として予測。好塩基球は、CCR3 ハイ SSC LOとゲートそれらのFITC - PEのプロットになど、PE標識抗CCR3抗体によって識別されます。活性化好塩基球を検出する抗CD63抗体は、FITCで標識されている。
- ネガティブコントロールにおけるCD63 HIと好塩基球の最大カットオフ2.5%を設定します。 > 5%の好塩基球は、CD63 hiおよびネガティブコントロールのMFIで割ったサンプルの平均蛍光インデックス(MFI)2を超える(図3)である場合、サンプルは、好塩基球活性化のために正とみなされます。
4。代表的な結果:
この実験では、IgE依存性の薬物過敏症を検出するために有益なツールとしてBATを評価します。非ステロイド性抗炎症薬の蛋白質複合体は、好塩基球の活性化のために使用されています。 RIとUV検出の凝集状態、結合度、および結合体の効果的な利回りとHPSECによって決定されます。 図4に示すように、DFの複合体の43.5%、5.0 DF / HSAの結合度を持つ単量体であった。凝集体のために9.5の結合度を決定した。 propyphenazone複合体は、21.2の結合度と68.5%のモノマーから成ることが示された。凝集体の結合度は27.9であった。合計では、DFの複合体の決定結合度は7.6 DFとPPの複合体のそれは23.2であった。
BATはNSAID過敏症におけるIgE依存性反応の調査を許可されて最適化された条件下での抱合体(抱合体の濃度、刺激時間)で行う。好塩基球の20.6%が活性化された蛍光強度の対数変化によって特徴づけ: 図5に示すように、唯一のPP複合体は、好塩基球活性化はCD63の表面発現のアップレギュレーションにより視覚誘発することができた。 MFIは1893年に386(ネガティブコントロール)から4.9倍増加した。対照的に、好塩基球のDF共役を使用すると、は3.1%が5%未満にオフカットされた活性化した。また、MFIは197(ネガティブコントロール)から210に係数1.1(上限2.0)でのみ増加した。アッセイの妥当性は、<好塩基球の亜集団の蛍光強度の(ⅱ)ログシフト、および(iii)、陰性対照の5%好塩基球の活性化> 50%活性化好塩基球(陽性対照)(i)で与えられる。
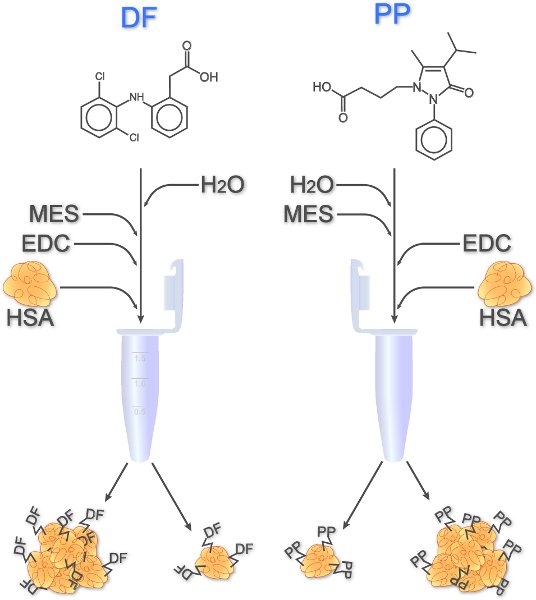
図1。HSAにDFとPP誘導体のカップリング。溶解後の薬剤、水、MES緩衝液、およびEDC(カップリング試薬)が追加されます。 HSAは、薬剤のソリューションにピペッティングする前にサンプルを1分間ボルテックスしている。室温で振盪しながら2時間以内に薬は共有結合HSAに結合する。モノマーと同様に凝集が発生する可能性があります。

図2。結合度の計算。最初に、RIとK UV K定数が決定されます。したがって、既知の濃度のHSAの標準は、HPSECシステムに注入される。 (DN / DC)とHSAの(DA / DC)がそれぞれ5、0.185と0.518の値が与えられます。ピーク面積は、定数を計算するために使用されています。第二に、各薬物のための3つの基準は、薬物と濃度固有のRIとUV領域を決定するために注入されています。 k個のRIとK UVの定数は上記の手順から知られているので、薬剤固有の(DN / DC)と(DA / DC)の誘導体は、計算することができます。第三に、薬剤HSAコンジュゲートは、HPSECに注入されています。結果として得られるピーク面積は、2つの未知変数を持つ2つの方程式を解くことにより、ピークあたりの薬剤とHSAの濃度を計算するために使用されています。
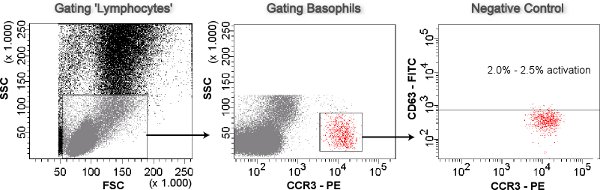
図3。好塩基球のゲーティング。リンパ球は前方散乱対ゲート側方散乱(SSC - FSCプロット)であるため、細胞が予測している。好塩基球は、ゲートリンパ球(SSC - CCR3 - PEプロット)からCCR3 ハイ SSC LOとして識別されます。好塩基球は、CD63 - FITC - CCR3 - PEのプロットの活性化(CD63 HI)について分析する。ネガティブコントロールは、CD63 hiを残りの最大2.5%の好塩基球のカットオフを設定するために使用されます。
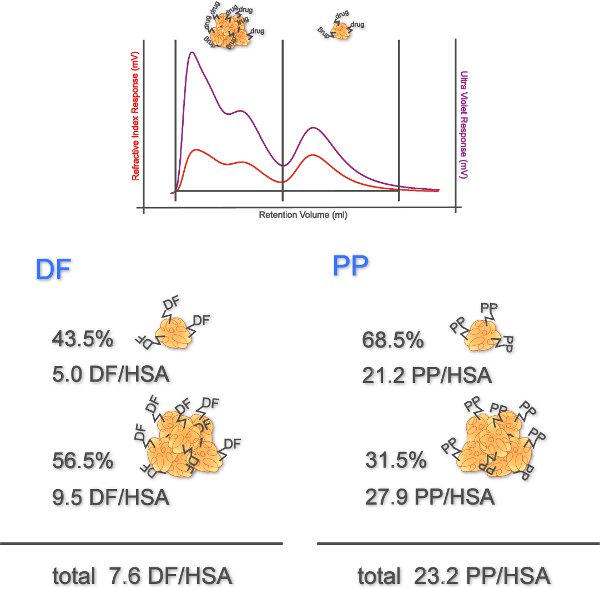
図4。薬物複合体の決定結合度。 RIとUVの信号は、薬物 - HSA複合体の凝集体(低保持容量で溶出)および単量体を(高い保持容量で溶出)を表す2つのピークを示す。単量体と凝集体(RIシグナルから決定)とそれらの結合度のパーセンテージは、(N = 1)描かれています。
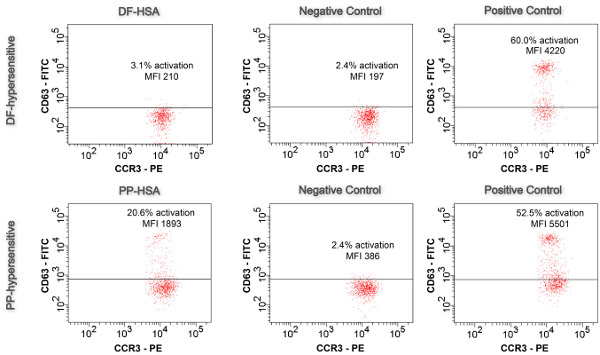
図5。好塩基球activatiテストで。薬物複合体活性化サンプル、ネガティブコントロール、ポジティブコントロールの結果は、CD63 - FITC - CCR3 - PEのプロット(N = 1)で示されています。
ディスカッション
BATは、IgE介在アレルギー性疾患6,7の診断のための十分に確立さまだ日常的に使用されていないが方法です。低分子量化合物が架橋IgE受容体、好塩基球の活性化8の前提条件にできないとして、薬物過敏症の場合は、しかし、その適用性が損なわれます。したがって、調査中の薬は、共有結合適当な担体タンパク質(例えばHSA)に結合する必要があります。重要なことは、結合度(担体タンパクあたりの薬物分子の数など)が抱合体( すなわち、IgE受容体架橋)免疫学的活性を保証するために制御する必要がある。理論的には、担体分子当たり2つのハプテンは、IgE受容体架橋とHSAあたり5 DFの分子は細胞ベースのアッセイ4のメディエーター遊離を誘発することが示されている限り少ないために十分なはずです。両方の複合体、PP - HSAとDF - HSAは、十分に高い結合度(HPSEC)を表示し、それらのBATの使用に適した試薬making免疫学的にアクティブになるように決定されている。もう一つの問題は、代わりに親薬物の代謝物として、過敏反応を引き起こす可能性、薬物代謝物の役割を果たしていることがあります。 DFの場合には、この可能性は、以前は次の5つの主要なフェーズI代謝一リンケージバリアント4を用いて詳細に評価されている。マスタリング説明する手法のための重要な要因は、血液サンプル(<採血、検出された好塩基球の数から12時間> 500)と刺激条件の最適化(時間、投与量)の質が含まれています。さらに、さらに、ポジティブコントロールと反応しない、いわゆる非応答(IgEレセプターに対する抗体)が同定されている。したがって、検証の基準は、ポジティブコントロールとして抗FcεRI抗体を含める必要があります。薬物複合体を使用しての重要な利点は、彼らがBAT 4の抗FcεRI抗体との共刺激により、DF - HSA抱合体のために示される純粋な薬、とは対照的に非毒性の現れるという事実です。純粋なDFは、対照的に、BAT 9の解釈性の問題を引き起こして1.25 mg / mlの濃度で細胞毒性効果を表示します。一般的に、潜在的な細胞毒性のためのテストを実施することを強くあらゆる新たに生成される薬物複合体のために推奨されます。
ここでは、IgE媒介過敏症を明らかにするためにBATで使用されているPP - HSA抱合体の可能性を示している。対照的に、DF過敏症は、DF - HSA抱合体に反応して好塩基球活性化の欠如によって示されるIgEと関連付けられていません。重要なことは、IgE媒介メカニズムに関する不確実性の場合には、コンジュゲートはDF 4に示されているようにin vitroでの細胞ベースのアッセイシステムでによって免疫学的活性について評価する必要があります。
適切なタンパク質担体分子に共有結合抗生物質、他の非ステロイド性抗炎症薬、造影メディア、筋弛緩薬、麻酔薬等を含む薬剤に対する過敏反応の数を低分子量の薬物を結合の説明に従ってセットアップを使用することを介するIgEの関与を調査することができるメカニズム。したがって、BATは、診断のための既存の方法(皮膚テスト、経口誘発試験)に加えて、として機能することができる。
開示事項
利害の衝突は宣言されません。
謝辞
この作品は、オーストリア科学基金(FWF)助成P18820 - B13によって賄われていた。
倫理のステートメント:
調査は1983年に改訂し、参加しているすべての患者が彼らの書面によるインフォームドコンセントを与えたとして、ヘルシンキのDeclaractionを遵守するザルツブルクの大学のヒトおよび/または動物を伴う実験のために倫理委員会(PLUS_Ethik_090514)承認された。
資料
| Name | Company | Catalog Number | Comments |
| 試薬/装置の名前 | 会社 | カタログ番号 | コメント |
|---|---|---|---|
| 2 - (N -モルホリノ)エタンスルホン酸 | シグマ | M3671 | - |
| 7.8 × 300 mmのゲルを、TSK - G2000SWXLコラム | バイオサイエンス東ソー | 08540 | - |
| BD FACSCanto II | ベクトンディッキンソン | 338962 | - |
| ベンチトップ遠心機 | シグマ | - | - |
| ジクロフェナクナトリウム塩 | シグマ | D6899 | - |
| EDTA -バキュテイナ | ベクトンディッキンソン | 368589 | - |
| Flow2 CASTキット | Bühlmann研究所 | FK - CCR | 効果的な2011年6月14日Flow2 CASTキットは現在、フローCASTです。 |
| HP1100 HPLCシステム | ヒューレットパッカード | - | - |
| ヒト血清アルブミン | シグマ | A9511 | - |
| 実験室の遠心機 | エッペンドルフ | - | - |
| N -エチル- N' - (3 - ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC) | シグマ | E6383 | - |
| PBSの錠剤 | AppliChem | A9199 | - |
| Propyphenazone誘導体 | 分子生物学科、ザルツブルク大学、オーストリア | - | - |
| シェーカー | エッペンドルフ | - | - |
| アジ化ナトリウム | シグマ | S8032 | - |
| 塩化ナトリウム(NaCl) | シグマ | S1679 | - |
| ナトリウム炭酸水素 | シグマ | 90421C | - |
| ナトリウムhydroxid | シグマ | S5881 | - |
| リン酸ナトリウム | シグマ | 342483 | - |
| トリプル検出器アレイ | Viscotek | TDA302 | - |
| 個人BioVortex V - 1プラス | Peqlab | 90 - V - 1 | - |
| 水浴1012 | GFL | 1012 | - |
参考文献
- Himly, M. IgE-mediated immediate-type hypersensitivity to the pyrazolone drug propyphenazone. J Allergy Clin Immunol. 111, 882-888 (2003).
- Demoly, P., Pichler, W., Pirmohamed, M., Romano, A. Important questions in Allergy: 1--drug allergy/hypersensitivity. Allergy. 63, 616-619 (2008).
- Ebo, D. G., Hagendorens, M. M., Bridts, C. H., Schuerwegh, A. J., Clerck, L. S., Stevens, W. J. Flow cytometric analysis of in vitro activated basophils, specific IgE and skin tests in the diagnosis of pollen-associated food allergy. Cytometry Part B (Clinical Cytometry). 64B, (2005).
- Harrer, A. Diclofenac hypersensitivity: antibody responses to the parent drug and relevant metabolites. PLoS One. 5, e13707-e13707 (2010).
- Wen, J., Arakawa, T., Philo, J. S. Size-exclusion chromatography with on-line light-scattering, absorbance, and refractive index detectors for studying proteins and their interactions. Anal Biochem. 240, 155-166 (1996).
- De Weck, A. L., Sanz, M. L., Gamboa, P. M., Aberer, W., Bienvenu, J., Blanca, M., Demoly, P., Ebo, D. G., Mayorga, L., Monneret, G., Sainte Laudy, J. Diagnostic tests based on human basophils: more potentials and perspectives than pitfalls. II. Technical issues. J Investig Allergol Clin Immunol. 18, 143-155 (2008).
- Ebo, D. G. Flow-assisted allergy diagnosis: current applications and future perspectives. Allergy. 61, 1028-1039 (2006).
- Poulsen, L. K., Quan, S., Kragh, C., Platzer, M. H., Skov, P. S. The basophil granulocyte in allergic reactions: experimental models and their use for the identification of drugs with effects or side effects on basophils. Curr Med Chem - Anti-inflammatory & Anti-Allergy Agents. 3, 167-180 (2004).
- Sanz, M. L., Gamboa, P., de Weck, A. L. A new combined test with flowcytometric basophil activation and determination of sulfidoleukotrienes is useful for in vitro diagnosis of hypersensitivity to aspirin and other nonsteroidal anti-inflammatory drugs. Int Arch Allergy Immunol. 136, 58-72 (2005).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved