このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
タンパク質吸着とポリマー力学の石英結晶マイクロバランス測定におけるサンプル調製
要約
石英結晶マイクロバランスは、バイオメディカルおよび環境センシング、コーティング、ポリマー科学の調査に関連するミクロンまたはサブミクロンの範囲のフィルムに正確な質量および粘弾性特性を提供することができます。サンプルの厚さは、センサーに接触する材料から得られる情報に影響を与えます。
要約
本研究では、石英結晶マイクロバランス実験の薄膜調製がデータの適切なモデリングを知らせ、フィルムのどの特性を定量できるかを決定する方法の種々の例を提示する。石英結晶マイクロバランスは、高周波で振動する石英結晶の機械的共振の変化を観察することにより、応用フィルムの質量や機械的特性の微細な変化を測定するための独自の感度の高いプラットフォームを提供します。このアプローチの利点は、その実験的な汎用性、実験時間の長さの広い範囲にわたる特性の変化を研究する能力、および小さなサンプルサイズの使用が含まれます。我々は、センサーに堆積した層の厚さとせん断弾性率に基づいて、材料から異なる情報を得ることができることを実証する。ここで、この概念は、塩濃度の関数として膨潤中に金および多電解質複合体上に吸着したコラーゲンの質量および粘弾性計算をもたらす実験パラメータを表示するために特に利用される。
概要
石英結晶マイクロバランス(QCM)は、石英結晶の圧電効果を利用して、表面に付着した質量に依存する共振周波数を監視します。この技術は、ATカット石英結晶センサの共振周波数と帯域幅(通常は5MHzの範囲)1を空気中または流体と、フィルムの堆積後のセンサの周波数と帯域幅と比較します。QCM を使用して薄膜の特性と界面を調べるための利点には、質量に対する感度が高く、粘弾性特性の変化に対する可能性がある(サンプルの均一性と厚さによって異なります)、situ2での研究を実行する機能、従来のせん断リロジーや動的機械解析 (DMA) よりもはるかに短いレオロジー タイムスケールをプローブする機能など、いくつかの利点があります。短いレオロジータイムスケールを調査すると、このタイムスケールでの応答が非常に短い(ms)3と長い(年)期間4の両方でどのように変化するかを観察することができます。この能力は、様々な運動過程の研究に有益であり、また、従来のレオメトリック技術の有用な拡張である5、6。
QCMの高感度はまた、非常に小さな生体分子の基本的な相互作用を研究する生物学的用途での重い使用につながっています。コーティングされていないまたは機能化されていないセンサー表面は、タンパク質の吸着を調査するために使用することができます。さらに、酵素、抗体、およびアプタマー間の複雑な結合事象を介したバイオセンシングは、質量7、8、9の変化に基づいて調べることができる。例えば、この技術は、周波数および粘弾性10の相関変化を観察することによって、流体含有小胞を剛体構造に吸着する二相プロセスとして、平面脂質二重層への小胞の形質転換を理解するために用いられてきた。近年、QCMはさらに、小胞またはナノ粒子11による薬物送達を監視する堅牢なプラットフォームを提供している。材料工学と分子細胞生物学の交差点では、QCMを使用して、タンパク質、核酸、リポソーム、細胞などの材料と生理活性成分との間の主要な相互作用を解明することができます。例えば、生体材料へのタンパク質吸着は、炎症などの下流の細胞応答を媒介し、生体適合性の肯定的な指標としてしばしば使用されるが、他の例では、血液と界面性のコーティングへの細胞外タンパク質付着は、血管12、13において危険な凝固を誘発し得る。したがって、QCMは、さまざまなニーズに最適な候補を選択するためのツールとして使用できます。
QCM実験を行うための2つの一般的なアプローチは、実験から類似したデータを収集します:最初のアプローチは、周波数シフトと伝導ピークの半分の帯域幅(Γ)を記録します。2番目のアプローチは、散逸を伴うQCM(QCM-D)、周波数シフトと散逸係数を記録し、これは式1、14を通してΓに正比例する
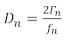 (1)
(1)
ここで、Dは散逸係数、ƒ は周波数です。DとΓはどちらも、フィルムがセンサーに与える減衰効果に関連しており、フィルムの剛性を示します。下付けnは、クォーツセンサーの奇数共振周波数である周波数の倍音または高調波を示します (n = 1, 3, 5, 7...)。フィルムの質量および粘弾性特性を得るために複数の高調波を用いたモデルのさらなる議論は、ヨハンスマン14およびShullグループ15、16、17、18からの以前の論文によるレビューで見つけることができます。
QCMサンプルを調製するための重要な考慮事項の1つは、センサー表面に薄膜を塗布する方法です。いくつかの一般的な方法は、スピンコーティング、ディップコーティング、ドロップコーティング、または実験中のセンサ表面へのフィルムの吸着を含む、20。QCMサンプルには、ザウアーブリー限界、粘弾性体制、バルク政権、過剰な体制の4つの地域があります。十分に薄いフィルムの場合、ザウアーブリー限界が適用され、ここで周波数シフト(Δƒ)はフィルムの表面質量密度を提供する。ザウアーブリー限界内では、周波数シフトは共振高調波、n、減衰因子(DまたはΓ)の変化に伴って直線的にスケーリングされますが、一般的に小さくなります。この体制では、追加の仮定を行わずに層のレオロジー特性を一意に決定するのに十分な情報は利用できません。この体制のデータは、フィルムの表面質量密度(密度が事前に知られている場合は厚さ)を計算するために使用されます。結晶に接触する媒体が十分に厚いバルク体制では、エバネッセントせん断波は完全に湿らせる前に培地中に伝播する。ここで、Δƒを用いて質量情報を得ることができない。しかしながら、この領域では、粘弾性特性はΔƒとΔΓ15,18の組み合わせを用いて確実に決定される。バルク体制では、媒体が硬すぎると、フィルムはセンサーの共振を湿し、QCMからの信頼性の高いデータの収集を防ぎます。粘弾性体制は、フィルムがフィルムを通して完全に伝播し、減衰因子の信頼性の高い値を持つほど薄い中間体制です。減衰係数とΔƒを使用して、フィルムの粘弾性特性とその質量を決定することができます。ここでは、粘弾性特性は、複雑なせん断弾性率の密度と大きさの積によって与えられます |G*|pとΦ=アークタン(G"/G')で与えられる位相角)フィルムがザウアーブリー限界で調製される場合、単位面積当たりの質量は、21の下に示すザウアーブリー方程式に基づいて直接計算することができます。
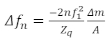 (2)
(2)
ここでΔƒnは共振周波数の変化、nは目的の倍音、ƒ1はセンサの共振周波数、Δm/Aはフィルムの面積当たりの質量、Zqは石英の音響インピーダンスであり、ATカットクォーツの場合はZq=8.84 x 106 kg/m2sである。粘弾性体制は、ポリマーフィルムの研究に最も適しており、バルクリミットは粘性ポリマー22またはタンパク質溶液16を研究するのに有用である。異なる体制は、完全粘弾性および質量特性評価のための最適な厚さが一般的にフィルム剛性に伴って増加して、対象材料の特性に依存する。図1は、フィルムの実質密度、複雑なせん断弾性率、位相角に関する4つの領域を示し、このタイプの材料に関連することが示されている位相角とフィルム剛性との間に特定の関係を仮定した。実用的に興味のある多くのフィルムは、厚さが数十〜数百ミクロンの順序である特定のバイオフィルムのようなQCMで粘弾性特性を研究するには厚すぎます。このような厚膜は、一般にQCMを用いた研究には適さないが、はるかに低周波共振器(ねじり用共振器など)23を用いて測定してもよいし、せん断波をフィルムにさらに伝播することを可能にする。
どの体制が所定のQCMサンプルに関連しているかを決定するには、石英結晶センサの機械的振動のせん断波長に対する膜厚(d)の比であるd/λnパラメータを理解することが重要である(λn)15、16、18。 理想的な粘弾性体制はd / λn = 0.05 - 0.218で、0.05未満の値はザウアーブリー限界内にあり、0.2を超える値はバルク体制に近づきます。d/λnのより厳密な記述は、15、18の他の場所で提供されるが、それはザウアーブリー限界および粘弾性限界を描写する定量的パラメータである。 以下で使用する分析プログラムは、このパラメーターを直接提供します。
QCM を使用した薄膜の分析には、いくつかの追加の制限があります。ザウアーブリーと粘弾性の計算では、フィルムの厚さとQCMの電極表面全体の横面の両方で均質であると仮定します。この仮定は、空隙または充填剤が存在するフィルムを研究することは困難であるが、移植されたナノ粒子6からなるフィルムにいくつかのQCM調査が行われてきた。均一性が全体的な膜厚に比べて小さい場合でも、複合系の信頼性の高い粘弾性特性が得られる。より異種システムの場合、粘弾性解析から得られる値は常に細心の注意を払って見る必要があります。理想的には、不均一性が不明なシステムから得られた結果は、均質であることが知られているシステムに対して検証されるべきである。これは、このホワイト ペーパーで説明したシステム例で行ったアプローチです。
本論文で示す重要な点は、周波数領域(Γが報告される場所)と時間領域実験(Dが報告される場所)で行われたQCM測定値との正確な対応である。2つの異なるQCM実験(1つの時間領域と1つの周波数領域)からの結果が記載され、それぞれが異なるが概念的に関連するモデルシステムを含む。最初のシステムは、時間領域(QCM-D)測定中の経時の代表的な結合動態および吸着の平衡を例示するために、センサへのコラーゲン付着の簡単な例である。コラーゲンは体内で最も豊富なタンパク質で、結合行動や形態の多様性で知られています。ここで使用されるコラーゲン溶液は、吸着9を誘導するためにセンサの金表面の追加機能化を必要としない。第2の実験系は、アニオン性ポリスチレンスルホン酸(PSS)およびカチオン性ポリ(透析液メチルアンモニウム)(PDADMA)と同様に調製されたポリ電解質錯体(PEC)をSadmanら(22)と同様に調製したものである。これらの材料は膨らみ、塩(この場合はKBr)溶液で柔らかくなり、周波数領域アプローチ(QCM-Z)を用いてポリマー力学を研究するためのシンプルなプラットフォームを提供します。各プロトコルについて、測定値の準備、取り、分析のプロセスを図2に示します。この概略図は、QCM-Z アプローチと QCM-D アプローチの主な違いが、データ収集ステップと実験で使用される計測器にあることを示しています。前述のすべてのサンプル調製手法は両方のアプローチと互換性があり、各アプローチは図 1に示す 3 つの領域のサンプルを分析できます。
当社のデータは、測定前または測定中にセンサーコーティングによってサンプルの調製がシステムの粘弾性特性を抽出する能力を決定することを示しています。実験の初期段階を適切に設計することで、解析ステップ中に正確に収集できる情報を特定できます。
Access restricted. Please log in or start a trial to view this content.
プロトコル
QCM-Dコラーゲン吸着
1. サンプル調製とセンサープリクリーニング
- 0.1 M酢酸緩衝液の20mLを調製し、必要に応じてHClとNaOHでpHを調整し、pH=5.6を達成する。
- 滅菌条件下の酢酸緩衝液20mLにラットテールコラーゲン溶液を10μg/mLの最終濃度に加えます。
- 金被覆の石英センサーを洗浄して、有機および生物学的材料25、26を除去する。
- センサーのアクティブな側面をUV/オゾンチャンバーに上に置き、表面を約10分間処理します。
- 脱イオン水(dH2O)、アンモニア(25%)の5:1:1混合物を加熱する過酸化水素(30%)75 °C に変更します。センサーを溶液に5分間入れ込む。
- dH2Oでセンサーをすすいで、窒素ガスの流れで乾燥させます。
- センサーのアクティブな側面をUV/オゾンチャンバーに置き、表面を10分間処理します。
メモ:洗浄手順は、センサー表面の環境汚染を最小限に抑えるために、測定の直前に実行する必要があります。
2. QCM-D測定データ取得
- ポンプ、エレクトロニクスユニット、コンピュータソフトウェアなどの測定に必要なすべての機器をオンにします。
- チャンバープラットフォームからフローモジュールを取り外し、大きなサムネジを外してモジュールを開きます。
- センサーが最初の洗浄後に取り残されている場合(ステップ1.3.1-1.3.4)、センサーを脱イオン水(dH2O)ですすいで窒素ガスの流れで乾燥させ、表面に汚染物質がないことを確認します。
- 露出したOリングのフローモジュールにセンサーを取り付け、まず窒素ガスの流れでエリアを乾燥させ、Oリングが平らに横たわっていることを確認します。センサーは、フローモジュール内のマーカーに向かってアクティブな表面側とアンカー状の電極を配置する必要があります。
- サムネジを回してフローモジュールを密閉し、チャンバープラットフォームで交換します。必要なPTFEポンプチューブをフローモジュールと外部ポンプに取り付けます。
- 適切なコンピュータソフトウェアを使用して、フローモジュールの温度を37°Cに設定します。変化する温度を10~15分間監視し、目的の値で平衡状態に保たれるようにします。
- センサーの初期共振周波数を見つけます。ソフトウェアで共振周波数が見つからない場合は、フローモジュールがチャンバプラットフォームに正しく配置されていることを確認するか、フローモジュールにセンサーを再マウントして、中央に配置され、適切な電気的接触が行われていることを確認します。
- 1xリン酸緩衝生理食塩水(PBS)溶液に入口ポンプチューブを入れます。25°L/minで外部ポンプの流れを開始し、チューブを目視で検査して、流体がチューブを流れていることを確認します。
注: 流体流量は、流体流量を一時的に100μL/min以上に増やすことで見やすくなります。流体がチューブ内を移動していないように見える場合は、フローモジュールの2つの部分が適切なシールを作成していない可能性が最も高いです。サムネジを締め付けたり、チューブの入口とコンセントにコネクタを締めたり、センサーを取り付け直してOリングが平らで中央に配置されていることを確認してください。 - フローモジュールを通る1x PBSの流体フローを少なくとも15分間、適切に平衡化できるようにします。
- コンピュータソフトウェアで測定を開始し、データ収集を開始します。頻度と散逸値を少なくとも5分間監視して、安定したベースラインを確保します。
- ポンプを停止し、入口チューブをコラーゲン酢酸緩衝液溶液に移動させ、流体の流れを再開します。後で分析するために、このイベントの時刻に注意してください。
- 新しい周波数と散逸値を安定した値に平衡化できるようにします。ここでは、この安定化が8-12時間後に起こることを期待する。
- ポンプを停止し、入口チューブを1x PBS溶液に戻し、流体の流れを再開します。後で分析するために、このイベントの時刻に注意してください。
- 新しい周波数と散逸値を安定した値に平衡化できるようにします。ここで、この安定化は30分後に生じる。
注: ステップ 2.13 および 2.14 は、より多くのステージを持つより厳格な実験で、流体の流れの新しい期間ごとに繰り返すことができます。 - 測定のデータ取得を終了し、データを保存します。
- QCM機器を清掃し、解体します。
- 外部ポンプの流体流量を500μL/min以上に増やし、入口チューブを2%ヘルマネックス洗浄液の溶液に20分以上入れます。
メモ:その他の実験では、センサーのさらなる分析が必要な場合は、ステップ2.16.1の前にセンサーを取り外し、モジュールに別のクリーニングセンサーを配置します。 - ポンプを停止し、入口チューブをdH2Oに移動し、流体の流れを再開して、少なくとも20分間システムをさらにフラッシュします。
- 流体フローを停止し、フローモジュールからセンサーを取り外します。センサーを乾燥させ、流れモジュールの内部を窒素ガスの流れで乾燥させます。コンピュータソフトウェア、エレクトロニクスユニット、およびペリスタリックポンプの電源を切ります。
メモ:金被覆センサーは、手順1.3.1-1.3.4で詳しく説明されているように適切に洗浄し、いくつかの測定に再利用することができます。センサーが信頼性の高い測定に再利用できなくなったという兆候には、初期共振周波数の大きな変動や、バッファフローによるベースライン測定の大きなドリフトが含まれますが、これらに限定されません。データは、QCM-D機器を専門とする企業が提供するソフトウェアを含め、好みのソフトウェアで開いて分析することができます。
- 外部ポンプの流体流量を500μL/min以上に増やし、入口チューブを2%ヘルマネックス洗浄液の溶液に20分以上入れます。
QCMポリ電解質複合体腫脹
3. サンプル調製
注:この実験は、Shull研究グループ内でデータ収集と分析のために開発されたMATLABプログラムを使用して行われました。
- まず、ベクターネットワークアナライザとコンピュータに接続されたサンプルホルダーにベアクォーツ結晶センサを配置します。アナライザの電源を入れ、振動電圧をセンサに印加し、空気中のセンサの基準伝導スペクトルを収集します。
- 蒸留水で満たされたリップレス100 mLビーカーにサンプルホルダーを沈め、水中の裸センサーの基準導電スペクトルを収集します。
- 臭化カリウム(KBr)の0.5M溶液を調製する。
- 30mLの蒸留水にKBrの1.79gを溶解する。溶け込むまで振る。
- 小さなシリコンウエハを角度でKBrソリューションに挿入し、アニーリングステップ中にクォーツセンサーのスライドを作成し、フィルムがセンサーから外れるのを防ぎます。
- スピンコーティング用のセンサーを準備します。
- スピン コートパラメータを 10,000 rpm、8,000 加速度、および 5 s に設定します。
- センサーをスピンコーターに差し込み、真空をオンにします。
- センサーの表面をエタノールで覆い、スピンコーターを実行してセンサー表面を清掃します。
- PEC (PSS:PDADMA は、サドマンらの詳細と同じ方法で準備されています。22)をセンサの表面に。
- 複合体が2相(ポリマーリッチおよびポリマー不良)にある場合は、ゆっくりとピペットを溶液に挿入する。より密度の高いポリマーリッチな位相にピペットを移動しながら、気泡を吹くことによってピペットを避難させます。
- ポリマーリッチ相でカップルの気泡を放出した後、ポリマーリッチ溶液の0.5〜0.75 mLをピペットに引き上げます。ピペットバルブの圧力を維持して、ポリマーの不良相がピペットに入ることを許さないので、ピペットを溶液から引き出します。
- キムワイプを使用してピペットの外側を拭きます。表面を完全に覆うために、石英センサーの表面に落とすだけの十分な溶液を追加します。センサー表面の溶液に目に見える泡がないことを確認します。
- PECサンプルをスピンコートし、すぐに0.5 M KBr溶液にセンサを沈下させ、フィルム上の塩分結晶化を防ぎます。
注: この手順は調整が困難な場合があります。最良の結果を得るには、KBr ソリューションのすぐ上にあるセンサーを解放します。 - フィルムを少なくとも12時間アニールにします。
注:実験を容易にするために、夕方にステップ4を準備し、フィルムが一晩アニールするようにしてください。
4. 空気中および水中のフィルムの測定
- センサーを蒸留水で満たされたビーカーに移して、センサーのフィルムと背面から余分なKBrを取り除きます。センサーは30~60分間溶液の中に入れたままにしておきます。
- 空気中のフィルムの測定を取ります。空気中の裸センサーへの参照。フィルムデータを平衡化できるようにします。
- 乾燥硫酸カルシウムを100mLのリップレスビーカーに挿入し、完全に乾燥したフィルムの厚さを測定します。ビーカーから硫酸カルシウムを取り出し、蒸留水でビーカーをすすすします。
- 100 mL のリップレス ビーカーに 30 mL の蒸留水を充填します。攪拌バーを挿入して、フィルムの周りを水が循環していることを確認します。約30〜45分間、またはフィルムデータが平衡化されるまで、水中でフィルムを測定します。水中の裸センサーへの参照。
- 蒸留水に3M KBrの15 mL溶液を調製します。KBrの5.35 gを等級シリンダーに測定し、蒸留水で15 mLまで充填します。溶解するまで旋回する。
- 0.1M刻みで蒸留水でビーカーにKBr溶液を追加します。表 1に、3 M KBr 溶液の mL 単位で 0.1 M 刻みフィルムが溶けないように、KBr溶液が水に添加されている場所からフィルムを向きます。KBr ソリューションを追加する前に、システムが平衡状態になっていることを確認してください。
- すべてのデータが取得されたら、ホルダーからフィルムを取り出し、蒸留水のビーカーに入れます。塩がフィルム(30-60分)を残し、フィルムを空気乾燥させます。
- センサーからPECフィルムをきれいにするには、ビーカーにKBrを追加し、溶液をゆっくりと旋回します。5~10分間座らせます。このプロセスを2~3回繰り返し、蒸留水でセンサーをすすいでください。
メモ:センサーからの応答がまだ良好な場合は、センサーをクリーニングして再利用できます。これは、対象の高調波(<100 Hz)のための小さな絶対帯域幅の読み取り値を持つセンサーによって確認することができます。
5. データ分析
- サドマン (https://github.com/sadmankazi/QCM-D-Analysis-GUI)27によって作成された QCM-D データ分析 MATLAB GUI を開きます。「QCM をロード」を選択して、フィルムをエアデータファイルで開きます。
注: Shull グループは、QCM ( https://github.com/shullgroup/rheoQCM ) のデータ収集と分析用に同様の Python GUIを開発しました。分析コードの一部は、データの分析と本稿の数値の生成の両方の補足情報に記載されています。 - 目的の計算(3,5,3または3,5,5)、ガンマ、およびフィルムを空気アイコンで選択します。[プロット QCM] をクリックします。
- 実験の最も平衡化されたデータポイント(通常は最後のデータポイント)を使用して、ドライフィルムの厚さを決定します。この値を記録します。
- フィルムを水データファイルで開きます。空気中のフィルムの代わりに水中のフィルムを除き、ステップ5.2と同じパラメータを選択します。
- 膨潤実験の各平衡工程の後、膜厚、複雑なせん断弾性率、および粘弾性相角を決定する。これらの値をイオン強度と共に記録します(0.1 M 単位で 0 ~ 1 M の範囲)。
- 次のように腫脹率を決定する
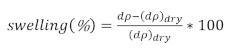 (3)
(3)
ここで、dpは溶液からの膜厚で、dpドライは乾燥膜の厚さです。
Access restricted. Please log in or start a trial to view this content.
結果
タンパク質吸着時の周波数の変化は、図3A-Bに示す特徴的な曲線および高原を示す。裸のセンサー表面全体の1x PBSの最初の緩衝洗浄は、周波数のごくわずかな変化のみを誘発し、将来のデータポイントの参照として機能する安定したベースラインを提供します。コラーゲン溶液の導入は、タンパク質吸着を開始させ、時間の経過とともに周波数の着実な減少?...
Access restricted. Please log in or start a trial to view this content.
ディスカッション
コラーゲン吸着結果はザウアーブリーと粘弾性体制に及ぶ。周波数シフトを対応する高調波数に正規化してプロットすることにより、測定の最初の2時間程度にザウアーブリー限界が当てはまることが観察されます。しかし、センサに付着する質量が増加すると、第3高調波と第5の高調波の正規化周波数シフトが互いに逸脱し始め(t>2時間)、吸着フィルムの粘弾性特性を決定する能力を?...
Access restricted. Please log in or start a trial to view this content.
開示事項
著者たちは何も開示する必要はない。
謝辞
この作業は NSF (DMR-1710491、OISE-1743748) によってサポートされました。J.R. および E.S. は NSF(DMR-1751308)からのサポートを確認します。
Access restricted. Please log in or start a trial to view this content.
資料
| Name | Company | Catalog Number | Comments |
| Acetic acid | Sigma-Aldrich | A6283 | For collagen adsorption |
| Ammonium hydroxide solution | Sigma-Aldrich | 221228 | For collagen adsorption |
| Aqueous QCM probe | AWSensors | CLS 00050 A | For polyelectrolyte swelling |
| Collagen I Rat Protein, Tail | Thermo Fisher Scientific | A1048301 | For collagen adsorption |
| Distilled water | Sigma-Aldrich | EM3234 | For polyelectrolyte swelling; generally easy to acquire in research labs, but there is a catalog number in case it is not accessible |
| Ethanol | Sigma-Aldrich | 793175-1GA-PB | For polyelectrolyte swelling |
| Gibco Phosphate Buffered Saline | Thermo Fisher Scientific | 20012-027 | For collagen adsorption |
| Hellmanex III | Sigma-Aldrich | Z805939 | For collagen adsorption |
| Hydrogen peroxide solution | Sigma-Aldrich | 216763 | For collagen adsorption |
| Kimberly-Clark Professional Kimtech Science Kimwipes Delicate Task Wipers, 1-Ply | Fisher Scientific | 06-666A | For polyelectrolyte swelling |
| NP2K VNA | Makarov Instruments | For polyelectrolyte swelling | |
| Poly(diallyldimethylammonium chloride), MW 200,000 | Sigma-Aldrich | 409022 | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Poly(styrene-sulfonate) sodium salt 30% weight in water | Sigma-Aldrich | 561967-500G | For polyelectrolyte swelling; for full synthesis procedure see Sadman et al. |
| Potassium Bromide | Sigma-Aldrich | 793604-1KG | For polyelectrolyte swelling |
| QSense QCM Explorer System | Biolin Scientific | For collagen adsorption | |
| Sodium acetate, anhydrous | Sigma-Aldrich | S2889 | For collagen adsorption |
| Spin coater, Model WS-650MZ-23NPP | Laurell technologies | For polyelectrolyte swelling |
参考文献
- Marx, K. A. Quartz crystal microbalance: A useful tool for studying thin polymer films and complex biomolecular systems at the solution - Surface interface. Biomacromolecules. 4 (5), 1099-1120 (2003).
- Kleber, C., Hilfrich, U., Schreiner, M. In situ QCM and TM-AFM investigations of the early stages of degradation of silver and copper surfaces. Applied Surface Science. 253 (7), 3712-3721 (2007).
- Yeh, C. J., Hu, M., Shull, K. R. Oxygen Inhibition of Radical Polymerizations Investigated with the Rheometric Quartz Crystal Microbalance. Macromolecules. 51 (15), 5511-5518 (2018).
- Sturdy, L. F., Yee, A., Casadio, F., Shull, K. R. Quantitative characterization of alkyd cure kinetics with the quartz crystal microbalance. Polymer. 103, 387-396 (2016).
- Delgado, D. E., Sturdy, L. F., Burkhart, C. W., Shull, K. R. Validation of quartz crystal rheometry in the megahertz frequency regime. Journal of Polymer Science, Part B: Polymer Physics. , 1-9 (2019).
- Bilchak, C. R., Huang, Y., Benicewicz, B. C., Durning, C. J., Kumar, S. K. High-Frequency Mechanical Behavior of Pure Polymer-Grafted Nanoparticle Constructs. ACS Macro Letters. 8 (3), 294-298 (2019).
- Hook, F., Rodahl, M., Brzezinski, P., Kasemo, B. Energy dissipation kinetics for protein and antibody-antigen adsorption under shear oscillation on a quartz crystal microbalance. Langmuir. 14, 729-734 (1998).
- Liss, M., Petersen, B., Wolf, H., Prohaska, E. An aptamer-based quartz crystal protein biosensor. Analytical Chemistry. 74 (17), 4488-4495 (2002).
- Felgueiras, H. P., Murthy, N. S., Sommerfeld, S. D., Brás, M. M., Migonney, V., Kohn, J. Competitive Adsorption of Plasma Proteins Using a Quartz Crystal Microbalance. ACS Applied Materials and Interfaces. 8 (21), 13207-13217 (2016).
- Keller, C. A., Kasemo, B. Surface specific kinetics of lipid vesicle adsorption measured with a quartz crystal microbalance. Biophysical Journal. 75, 1397-1402 (1998).
- Olsson, A. L. J., Quevedo, I. R., He, D., Basnet, M., Tufenkji, N. Using the quartz crystal microbalance with dissipation monitoring to evaluate the size of nanoparticles deposited on surfaces. ACS Nano. 7 (9), 7833-7843 (2013).
- Xu, X., Zhang, C., Zhou, Y., Cheng, Q. L. J., Yao, K., Chen, Q. Quartz crystal microbalance study of protein adsorption on chitosan, chitosan/poly(vinyl pyrrolidone) blends and chitosan-graft-poly(vinyl pyrrolidone) surfaces. Journal of Bioactive and Compatible Polymers. 22, 195-206 (2007).
- Weber, N., Pesnell, A., Bolikal, D., Zeltinger, J., Kohn, J. Viscoelastic properties of fibrinogen adsorbed to the surface of biomaterials used in blood-contacting medical devices. Langmuir. 23, 3298-3304 (2007).
- Johannsmann, D. Viscoelastic, mechanical, and dielectric measurements on complex samples with the quartz crystal microbalance. Physical Chemistry Chemical Physics. 10 (31), 4516-4534 (2008).
- Denolf, G. C., Sturdy, L. F., Shull, K. R. High-frequency rheological characterization of homogeneous polymer films with the quartz crystal microbalance. Langmuir. 30 (32), 9731-9740 (2014).
- Martin, E. J., Mathew, M. T., Shull, K. R. Viscoelastic properties of electrochemically deposited protein/metal complexes. Langmuir. 31 (13), 4008-4017 (2015).
- Sturdy, L., Casadio, F., Kokkori, M., Muir, K., Shull, K. R. Quartz crystal rheometry: A quantitative technique for studying curing and aging in artists' paints. Polymer Degradation and Stability. 107, 348-355 (2014).
- Sadman, K., Wiener, C. G., Weiss, R. A., White, C. C., Shull, K. R., Vogt, B. D. Quantitative Rheometry of Thin Soft Materials Using the Quartz Crystal Microbalance with Dissipation. Analytical Chemistry. 90 (6), 4079-4088 (2018).
- Wasilewski, T., Szulczyński, B., Kamysz, W., Gębicki, J., Namieśnik, J. Evaluation of three peptide immobilization techniques on a qcm surface related to acetaldehyde responses in the gas phase. Sensors (Switzerland). 18 (11), 1-15 (2018).
- Lvov, Y., Ariga, K., Kunitake, T., Ichinose, I. Assembly of Multicomponent Protein Films by Means of Electrostatic Layer-by-Layer Adsorption. Journal of the American Chemical Society. 117 (22), 6117-6123 (1995).
- Sauerbrey, G. Verwendung von Schwingquarzen zur Wägung dünner Schichten und zur Mikrowägung. Zeitschrift für Physik. 155 (2), 206-222 (1959).
- Sadman, K., Wang, Q., Chen, Y., Keshavarz, B., Jiang, Z., Shull, K. R. Influence of Hydrophobicity on Polyelectrolyte Complexation. Macromolecules. 50 (23), 9417-9426 (2017).
- Sievers, P., Moß, C., Schröder, U., Johannsmann, D. Use of torsional resonators to monitor electroactive biofilms. Biosensors and Bioelectronics. 110, 225-232 (2018).
- Ringberg, J. Q-Sense Explorer Operator Manual. Biolin Scientific. , Stockholm, Sweden. (2017).
- Ringberg, J. Q-Sense User Guide: Instrument care and sensor pre-cleaning. Biolin Scientific. , Stockholm, Sweden. (2015).
- Kern, W. The Evolution of Silicon Wafer Cleaning Technology. Journal of The Electrochemical Society. 137 (6), 1887(1990).
- Sadman, K. sadmankazi/QCM-D-Analysis-GUI: QCMD-Analyze. , (2018).
Access restricted. Please log in or start a trial to view this content.
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved