침전 반응에서 수용성 염의 수성 용액은 불용성 이온 화합물인 침전을 제공하기 위해 반응합니다. 반응은 용액의 반대로 충전 된 이온이 물에 대한 매력을 극복하고 서로 결합하여 용액과 분리되는 침전을 형성 할 때 발생합니다. 이러한 반응은 수성 용액에서 이온 화합물 사이의 이온교환을 수반하기 때문에 이중 변위, 이중 교체, 교환 반응 또는 메타염 반응("전이"에 대한 그리스어)이라고도 합니다. 침전 반응은 물질의 조성을 결정하기 위한 화합물 및 중력 방법에서 금속 이온을 식별하는 분석 기술로 사용된다.
물질이 물에 용해될 수 있는 범위, 또는 임의의 용매는, 지정된 조건하에서 달성될 수 있는 물질의 최대 농도로 정의된 용해도로 정량적으로 표현된다. 상대적으로 큰 수용성을 가진 물질은 용해성이라고 합니다. 용액 조건이 그 농축액이 용해도를 초과할 때 물질은 침전됩니다. 상대적으로 낮은 수용성을 가진 물질은 불용성이라고 합니다, 이들은 용액에서 쉽게 침전하는 물질입니다.
예를 들어, 강수량은 요오드 칼륨과 납 질산염의 용액이 혼합되어 고체 납 요오드의 형성을 초래할 때 관찰됩니다.

이 관찰은 용해도 지침과 일치합니다: 관련된 모든 사람들 중 유일하게 불용성 화합물은 요오드 염의 일반적인 용해도에 대한 예외 중 하나인 납 요오드제입니다.
이 반응을 나타내는 순 이온 방정식은 다음과 같은 것입니다.
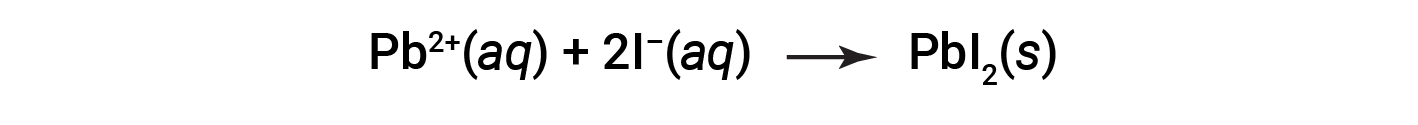
수용성 지침은 수용성 이온 화합물의 용액이 함께 혼합될 때 강수 반응이 발생할지 여부를 예측하는 데 사용될 수 있다. 하나는 단지 용액에 존재하는 모든 이온을 식별하고 가능한 양이온 음이온 페어링이 불용성 화합물을 초래할 수 있는지 고려해야합니다.
예를 들어, 은 질산염 과 나트륨 불소의 혼합 용액은 Ag+, NO3-, Na+및 F- 이온을 포함하는 솔루션을 산출합니다. 이외에도 원래 솔루션에 존재하는 두 개의 이온 화합물에서, AgNO3 및 NaF, 두 개의 추가 이온 화합물은 이온의이 컬렉션에서 파생 될 수있다: NaNO3 및 AgF. 용해도 지침은 모든 질산염이 용해적이지만 AgF는 불소 염의 일반적인 용해도에 대한 예외 중 하나임을 나타냅니다. 강수 반응은, 따라서, 다음 방정식에 의해 설명된 대로, 일어날 것으로 예상됩니다:


Copyright © 2025 MyJoVE Corporation. 판권 소유