JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
밀러 - 유리의 실험을 실시
요약
밀러 - 유리의 실험은 생명의 기원에 가능한 관련 유기 화합물의 비 생물 적 합성에 관한 선구적인 연구했다. 기본 가스는 유리 용기에 넣고 원시 지구의 대기 해양 시스템에서 낙뢰의 영향을 시뮬레이션 방전을 실시 하였다. 실험은 그것으로부터 수집 샘플 삶의 화학적 빌딩 블록을 분석 하였다, 그 후, 일주일 동안 실시 하였다.
초록
1953 년, 스탠리 밀러 (Stanley Miller)는 원시 지구의 대기 - 해양 시스템을 시뮬레이션하기 위해 구성된 장치를 사용하여, 간단한 가스 원료로부터 생체 분자의 생산을 보도했다. 물이 동시에 동안 밀러는 다음 주를위한 전기 방전, 환류,이 혼합물을 실시하고, 장치에 물 200 ㎖, H 2의 100 mmHg로, CH 4의 200 mmHg로하고, NH 3의 200 mmHg로 소개 가열. 이 원고의 목적은 간략화 된 3 L 반응 플라스크를 사용하여, 밀러 - 유리의 분류 스파크 방전 실험을 수행하는 데 사용할 수있는 일반적인 실험 프로토콜로 리더를 제공하는 것이다. 실험 고전압 방전에 가연성 가스를 노광 수반하기 때문에, 폭발의 위험을 줄이는 중요한 단계를 강조 가치가있다. 이 연구에서 설명 된 일반적인 절차 방전 실험의 다양한 설계 및 실시 외삽 될 수있다원시 행성의 환경을 시뮬레이션이야.
서문
지구에 생명의 기원의 본질은 가장 불가사의 한 과학적인 질문 중 하나 남아있다. 1920 년대 러시아 생물 학자 알렉산더 오파 린과 영국의 진화 생물 학자와 유전 학자 존 홀 데인은 화학 진화를 촉진 수도 유기 화합물을 포함하는 원시 지구의 바다를 설명, "원시 수프"1,2의 개념을 제안했다. 화학자 초기 지구에서 간단한 출발 물질로부터 합성 될 수 있었다 어떻게 유기 분자 승낙 겨냥한 고의적 실험 연구를 수행하기 시작하면 그러나 1950 년대까지 없었다. 이를 위해 제 보고서 중 하나는 1951 소재 수성 CO 2 해법의 조사에서 포름산 합성했다.
1952 년 시카고 대학에서 다음 대학원생 스탠리 밀러 (Stanley Miller)는 가능성을 평가하는 실험을 수행에 대한 해롤드 유리의 접근이 유기 화합물생명의 기원에 대한 중요한 초기 지구에 abiologically 형성되었을 수 있습니다. 실험은 원시 지구를 시뮬레이션하기 위해 설계된 맞춤형 유리 장치 (그림 1A)를 사용하여 실시 하였다. 밀러의 실험은 초기 대양을 나타내는 액체 저수조의 존재, 초기 분위기를 나타내는 가스의 혼합물에 전기 방전의 작용에 의해 번개 했었. 또한, 상기 장치는 각각 가열 맨틀의 사용 및 응축기를 통해 증발과 침전을 시뮬레이션. 밀러는 사용되는 장치에 대한 자세한 정보는 다른 곳에서 4 찾을 수 있습니다. 스파크의 주 후, 플라스크 내의 내용물을 시각적으로 변환 하였다. 물은 탁한 붉은 색 (5)와 전극 (4)에 축적 된 노란색 - 갈색 물질을 돌렸다. 이 획기적인 연구는 시뮬레이션 원시 지구 조건 하에서 생체 분자의 첫 번째 신중하고 효율적으로 합성으로 간주됩니다.
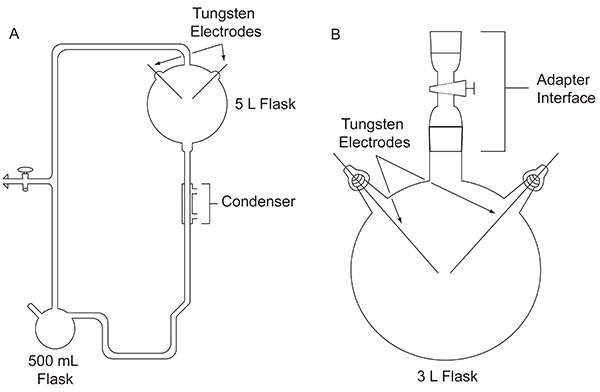
그림 1. 이 논문에서 논의 된 장치의 두 가지 유형의 비교. 원래 밀러 - 유리의 실험 (A)와 여기 (B)에 설명 된 프로토콜에서 사용되는 간단한 장치에 사용되는 고전적인 장치. 더 큰 이미지를 보려면 여기를 클릭하십시오 .
밀러의 고전적인 실험, 스파크 방전 실험의 수많은 변형, 다른 가스 혼합물을 사용하여 예를 들면, 수 초 어스 다양한 조건들은 중요 유기 화합물의 제조 타당성을 탐구 수행 된 결과의 1953 발행 후. 예를 들어, CH 4 / H 2 O / NH 이러한 6가 검출되지 않았다하더라도 두 S 가스 혼합물을, 부호화 황 함유 α-아미노산을 생산하는 능력에 대해 시험 하였다 3 / H. 방전을 실시 CH 4 / NH 3 혼합물의 기체 크로마토 그래피 - 질량 분석법 (GC-MS) 분석은 산 전구체 (7) 아미노되는 α-아미노 니트릴의 합성을 보였다. 1972 년, 첫 번째 오로 8 (그림 1B)에 의해 도입 된 간단한 장치를 사용하여, 밀러와 동료, 날짜 머치 슨 운석에서 발견되었던 코드 α-아미노산 9 및 비 단백질 아미노산 10 모두의 합성을 증명 방전에 CH 4, N 2 및 NH 3 소량 실시함으로써. 그 후, 동일한 실험 설계를 단순화하여, H 2 O를 함유하는 가스 혼합물은 N 2 및 CH 4, CO 2, CO는 STU으로 촉발되었다대기 탄소 종 (11)의 산화 상태의 함수로서 시안화 수소, 포름 알데히드, 및 아미노산의 수율 DY.
지난 몇 년 동안 다른 실험적인 디자인의 탐구뿐만 아니라, 중요한 분석의 발전은 최근 밀러에 의해 보관 방전 실험 샘플의 더 프로빙 조사를 주었 밀러의 고전적인 실험 이후에 발생한, 기술에 의해 촉진 된 것보다 밀러에 대한 액세스를했다 1950 년대에. 밀러의 화산 1955 년 4에보고 된 실험 (12), 그리고 1958 H 2 S 함유 실험 (13)이 많은 그 어느 포함하여 고전적인 실험보다 많은 아미노산과 아민의 더 다양한, 더 큰 존재비를 형성 한 것으로 나타났다 이전에 불꽃 방전 실험에서 확인되지 않았다.
이 문서에서 설명하는 실험을 사용하여 수행 할 수있다가스 혼합물의 다양한. 통상적으로, 적어도, 그러한 실험은 C 함유 가스, N 함유 가스 및 물을 포함 할 것이다. 일부 계획으로, 가스의 거의 모든 혼합물 그러나, 시스템의 몇몇 화학적 측면을 고려하는 것이 중요하다, 탐구 할 수있다. 예를 들어, 수성상의 pH가 14이 발생 화학에 상당한 영향을 미칠 수있다.
여기서 설명한 방법은 밀러 1,972 9,10 출판물에 설명 된 단순화 된 3 L 반응기를 이용한 밀러 - 유리의 실험과 유사 스파크 방전 실험을 수행하는 연구자 방법 지시에 맞게되었다. 이 실험은 가연성 기체에 작용하는 고전압 전기 아크를 포함하기 때문에, 그러한 메탄 또는 일산화탄소와 같은 환원 탄소 - 함유 가스의 연소시에 발생할 수있는 폭발의 위험을 제거하기 위해 반응 플라스크에서 O 2를 제거하는 데있어 매우 중요 또는 반응 오산소와 F의 H 2.
여기서 설명하는 실험을 수행하기 위해 준비 할 때 염두에 보관해야합니다 자세한 내용이 있습니다. 유리 진공 라인 및 가압 가스로 작업 할 때마다 첫째,이 파열 모두 고유의 위험이 존재하고 오버 압력. 따라서, 안전 안경을 항상 착용해야한다. 둘째, 실험은 일반적으로 대기압 이하에서 수행된다. 이 매니 폴드와 반응 플라스크를 가압 과잉의 위험을 최소화한다. 유리하지만, 1 기압 이상의 압력이 권장되지 않습니다, 대기압 이상 평가 될 수있다. 불용성 H 2 (예 : CH 4, NH 3 등) 감소 가스에서 해방 된 상태로 압력이 실험에서 증가 할 수 있습니다. 과잉 압력은 대기 O 2는 가능한 폭발의 결과로, 연소를 유도하고, 반응 플라스크를 입력 할 수 있습니다 씰 누출로 이어질 수 있습니다. 셋째,그것은 실험의 변형을 수행하는이 프로토콜의 변경이 안전하지 않은 조건이 생성되지 않도록 세심한 계획이 필요합니다 것을 염두에 두어야한다. 넷째, 그것은 매우 전향 적 실험주의 깊게 여러 번 이전에 그 또는 그녀가 잠재적 인 함정에 익숙하고 필요한 모든 하드웨어를 사용할 수 있고 장소에 있는지 확인하기 위해이 실험을 시도하여 전체 프로토콜을 통해 읽어 보는 것이 좋습니다. 마지막으로, 가연성 가스를 포함하는 전도성 실험은 실험자의 호스트 기관의 환경, 보건 및 안전 부서의 지침을 준수해야합니다. 어떤 실험을 진행하기 전에 이러한 권장 사항을 준수하십시오. 여기에 프로토콜에 설명 된 모든 단계는 저자의 호스트 기관 환경 보건 및 안전 지침을 준수합니다.
프로토콜
1. 매니 폴드 / 진공 시스템 설정
- 반응 플라스크에 가스를 도입하는 유리 매니 폴드를 사용합니다. 이 매니 폴드는 구입하거나 구성된 유리 제조 설비에 의해, 그러나 진공 장치, 가스 실린더, 진공 게이지, 및 반응 용기에 연결될 수있다 타이트한 진공 포트를 포함해야 할 수있다.
- 매니 폴드 밸브 간 유리 접합 유리 플러그를 사용합니다. 플러그의 모든 O-링이 필요한 실을 만드는 능력이 있는지 확인합니다. 글라스 조인트를 사용하는 경우에 필요한 경우 진공 그리스의 충분한 양은, 시일을 활용할 수 있도록 적용 할 수있다. 실리콘 진공 그리스 잠재적 유기 오염을 방지하는데 사용될 수있다.
- 매니 폴드에 유리 조절판을 사용합니다. 도장을 할 필요가 진공 그리스의 최소 금액을 적용합니다.
- 매니 폴드 볼륨을 측정합니다. 이 볼륨은 3 L 반응 플라스크에서의 최종 기체 압력에 관련된 계산을 위해 사용되며, 가능한 한 정확하게 알려 져야한다.
- 매니 폴드 모두 동시에 가스 실린더를 수용 할 수있을만큼의 연결이 없으면, 상기 매니 폴드에 한번에 하나의 실린더를 연결한다. 이와 관련, 매니 폴드 주변 대기로부터 격리 할 수 있도록 탭에 포함.
- 적절한 청소, 불활성, 그리고 화학 물질을 사용하고 매니 폴드 가스 실린더를 연결하는 저항 튜브와 ultratorr 진공 피팅을 누출. Ultratorr 피팅이 사용하는 경우, 손가락 강화되어야한다.
- 매니 폴드, <1 mmHg로의 진공을 확립 할 수있는 진공 펌프에 연결한다. 진공 펌프의 배기 흄 후드 내에 위치, 또는 제대로 다른 수단에 의해 배출되어야한다.
- 진공의 급속한 달성을 보장하고 펌프를 보호하기 위해, 매니 폴드와 진공 펌프 사이에 트랩을 삽입한다. 이 펌프에 들어가는 등 NH 3, CO 2 및 H 2 O와 같은 휘발성 물질을 차단하므로 액체 질소 손가락 트랩을 권장합니다. 관리는 워싱턴에 갇혀 휘발성 물질로,주의해야한다rming, 매니 폴드를 과압 유리 파열 될 수 있습니다.
- 매니 폴드, 압력계 또는 1 mmHg로 해상도 이상 할 수있는 다른 진공 게이지에 연결합니다. 다양한 장치가 사용될 수 있지만 수은은 매우 반응성이므로, 수은 압력계 또는 매 클라우드 게이지가 바람직하다.
- 측정하고 적당한 온도계를 사용하여 주위 온도를 기록한다.
2. 반응 플라스크의 준비
- 유기 오염 물질을 제거 할 수있는, 사용하기 전에 공중에서 적어도 3 시간 동안 500 ° C에서 모든 유리를 가열한다.
- 부드럽게 깨끗한 실험실 와이프와 메탄올로 세척하고, 공기 건조에 의해 텅스텐 전극을 청소합니다.
- 3 L의 반응 플라스크에 초순수 (18.2 MΩ cm, <5 PPB의 TOC) 200 ㎖를 붓는다.
- 전 중 빠른 용해 가스의 용해 및 반응물의 혼합을 보장합니다 미리 세정 및 살균 자기 교반 막대를 소개periment.
- 플라스크 내부의 약 1cm로 분리 팁, 진공 그리스의 최소량을 사용하여 3 L 반응 플라스크에 텅스텐 전극을 부착. 클립으로 고정합니다.
- 3 L의 반응 플라스크의 목에 내장 된 마개를 가진 어댑터를 삽입하고 클립으로 고정합니다.
- 어댑터를 통해 가스 매니 폴드에 3 L의 반응 플라스크를 연결합니다. 클립을 사용하거나 플라스크를 보호하기 위해 클램프.
- 가볍게 좋은 진공 밀봉을 보장하기 위해 모든 연결을 기름칠.
- 밸브 (6)와 조절판 1 (그림 4)를 제외하고, 매니 폴드의 모든 밸브 및 콕 마개를 열고 매니 폴드를 대피 진공 펌프의 전원을 켭니다. <1 mmHg로의 안정적인 진공 읽기, 개폐 밸브 1을 달성하고, 매니 폴드 진공 누출을 확인하기 위해 15 분 ~ 동안 앉아 수 있습니다되면. 아무 것도 발견되지 않으면 2.8 단계로 진행합니다. 누수를 식별하고 해결 될 때까지 그렇지 않으면 여러 가지 연결 문제를 해결.
- 반응 용기에 자석 교반을 pply. 개방 밸브 1 조절판 1의 압력이 <1 mmHg로 도달 할 때까지 3 L의 반응 플라스크의 빈 공간을 대피 (그림 4).
- (그림 4) 밸브 1을 닫고 3 L의 반응 플라스크 내부의 압력을 모니터링 할 수 있습니다. 측정 된 압력은 물의 증기압이 증가한다. 누출이 없는지 확인하기 위해,이 단계에서 ~ 5 분을 기다립니다. 밸브 1이이 단계에서 닫힌 상태에서 압력 (차압에 읽는)이 증가하면, 조절판 1의 누출 및 다양한 반응 플라스크의 연결을 확인합니다. 의 누출이 발견되지 않으면 다음 단계를 진행합니다.
3. 기체 NH 3의 소개
- NH 3의 200 mmHg로는 반응 플라스크에 도입 될 것이다되도록 매니 폴드에 도입하는 기체 NH 3의 필요한 압력을 계산한다. 이 작업을 수행하는 방법에 대한 자세한 내용은 토론 섹션에서 제공된다.
- 닫기 밸브1, 6, 및 조절판 1 매니 폴드에있는 가스를 도입하기 전에 (그림 4). 다른 밸브와 콕을 열어 둡니다.
- 작은 압력 (약 10 mmHg로)가 도달 한 다음 (그림 4) 밸브 1을 열고 1 mmHg로 <의 압력에 매니 폴드를 철수 할 때까지 매니 폴드에 NH 3를 소개합니다. 3 회 반복합니다.
- 단계 3.1에서 결정된 압력에 도달하는 다기관으로 NH 3를 소개한다.
- 3 L의 반응 플라스크에 NH 3의 200 mmHg로를 소개하는 오픈 조절판 1 (그림 4). NH 3는 반응 플라스크에서 물에 용해되며, 압력이 천천히 떨어질 것이다.
- 압력, 근접 조절판 1 (그림 4)를 삭제하고 압력계 읽을 압력을 기록 중지하면. 이 값은 플라스크 내부 압력을 나타내는 이상 매니 폴드 내로 도입 될 다른 가스에 대한 압력을 계산하는 데 사용될 것이다.
- 1 mmHg로 <의 압력에 매니 폴드를 대피 개방 밸브 1 (그림 4).
- (그림 4) 밸브 2를 닫고 매니 폴드에서 NH 3 가스 실린더를 분리합니다.
4. CH 4의 소개
- CH 4의 200 mmHg로는 3 L의 반응 플라스크에 도입 될 것이라는 등의 매니 폴드에 도입되는 CH 4의 필요한 압력을 계산합니다. 예 계산은 토론 섹션에 나타낸다.
- 매니 폴드에 CH 4 가스 실린더를 연결합니다.
- 밸브 (6)와 조절판 1 (그림 4)를 제외한 모든 밸브 및 콕 마개를 열고 1 mmHg로 <의 압력에 매니 폴드를 제거하고,.
- 닫기 밸브 1 매니 폴드 (그림 4) 철수 된 후에.
- 작은 압력 (약 10 mmHg로)을 얻을 때까지 매니 폴드에 CH 4를 소개합니다. 이것은 어떤 오염 가스 FR의 라인으로 제거톰 단계를 앞. <1 mmHg로 매니 폴드를 철수 밸브 1 (그림 4)를 엽니 다. 2 배 더 반복합니다.
- 단계 4.1에서 계산 된 압력이 도달 될 때까지 다기관으로 CH 4를 소개한다.
- 3 L의 반응 플라스크에 CH 4의 200 mmHg로를 소개하는 오픈 조절판 1 (그림 4).
- 닫기 조절판 CH 1 (4)의 의도 된 압력이 3 L 반응 플라스크 (도 4)에 도입하고, 압력계에 의해 측정 압력을 기록 되었으면.
- <1 mmHg로 매니 폴드를 철수 밸브 1 (그림 4)를 엽니 다.
- (그림 4) 밸브 2를 닫고 매니 폴드에서 CH 4 실린더를 분리합니다.
5. 또한 가스의 도입 (예를 들어, N 2)
- 이 시점에서 추가적인 가스를 도입 할 필요가 없다. 원하는 경우, 그것은 N이 100 mmHg로를 추가하는 것이 좋습니다. 이 경우, N이 100 mmHg로는 3 L 반응 플라스크에 도입 될 것이다되도록 매니 폴드 내로 도입되는 N 2의 필요한 압력을 계산한다. 예 계산은 토론 섹션에 나타낸다.
- 매니 폴드에 N 2 가스 실린더를 연결합니다.
- 밸브 (6)와 조절판 1 (그림 4)를 제외한 모든 밸브 및 콕 마개를 열고 1 mmHg로 <의 압력에 매니 폴드를 제거하고,.
- 닫기 밸브 1 매니 폴드 (그림 4) 철수 된 후에.
- 작은 압력 (약 10 mmHg로)을 얻을 때까지 매니 폴드에 N 2를 소개합니다. <1 mmHg로 매니 폴드를 철수 밸브 1 (그림 4)를 엽니 다. 2 배 더 반복합니다.
- 단계 5.1에서 계산 된 압력에 도달 할 때까지 다기관으로 N이 도입.
- 반응 플라스크에 N이 100 mmHg로를 소개하는 오픈 조절판 1 (그림 4).
- 닫기 조절판 한 N 2의 의도 압력 반응 플라스크 (도 4)에 도입하고 압력계를 사용하여 압력을 기록 되었으면.
- <1 mmHg로 매니 폴드를 철수 밸브 1 (그림 4)를 엽니 다.
- (그림 4) 밸브 2를 닫고 매니 폴드에서 N 2 실린더를 분리합니다.
6. 실험 시작
- 주위 공기는 매니 폴드를 입력하여 대기압까지 매니 폴드를 가져올 수 있도록, 일단 모든 가스가 반응 플라스크에 도입 된 조절판 (1)와 밸브 1 (도 4)를 폐쇄함으로써 매니 폴드에서 반응 플라스크를 분리.
- 주의 매니 폴드에서 반응 플라스크를 분리 한 후, 플라스크 어딘가에 (예 : 빈 흄 후드 내부) 방해되지 않습니다을 설정합니다.
- 진공 펌프를 분리하고 조심스럽게 냉각 트랩을 제거하고 완전히 내에서 배출 허용운영 흄 후드.
- 고주파 스파크 발생기에 연결된 테슬라 코일을 고정.
- 두 전극 사이의 갭에 걸쳐 전류의 효율적인 통로를 가능하게하는 전기 접지에 대향 텅스텐 전극을 연결한다.
- 제조 업체에서 제공되는 문서에 설명 된대로, 약 30,000 V에 스파크 발전기의 출력 전압을 설정합니다.
- 이전에 불꽃을 시작으로, 장치 및 실험 사이의 안전 방패 역할을, 흄 후드 창틀을 닫습니다. 실험을 시작하기에 테슬라 코일을 켜고 불꽃이 온 / 오프 사이클에 1 시간에 이주 (또는 다른 원하는 기간) 동안 계속 할 수 있습니다.
7. 실험 종료
- 테슬라 코일을 해제하여 실험을 중지합니다.
- 오픈 조절판 한 천천히 반응 플라스크에 외기를 도입하고 어댑터의 제거 및 텅스텐 전극을 용이하게하기 위해 (도 4) SA 그래서mples를 수집 할 수 있습니다. 원하는 경우, 진공 유해 반응 가스의 반응 플라스크를 대피 할 수있다.
8. 액체 샘플을 수집
- 열분해 유리 피펫을 사용하여, 예를 들면 진공 그리스 또는 다른 비 멸균 표면에 피펫을 터치하여 도입 할 수있는 것과 같은 오염 물질에 대한 노출을 최소화하기 위해주의하고, 반응 플라스크에서 액체 샘플을 제거합니다.
- 멸균 플라스틱이나 유리 용기에 샘플을 전송합니다. 플라스틱 용기는 유리 용기에 비해, 균열 또는 동결에 침입 적은 경향이 있습니다.
- 불용성 제품으로 -20 ° C 이하의 온도에 도달, 할 수있는 냉장고에 밀봉 샘플 용기 및 저장은 0 ℃에서 동결 시료 용액을 방지 할 수 있습니다
9. 장치를 청소
- 깨끗한 실험실을 사용하여 조심스럽게 장치의 목에 진공 그리스를 제거하는 물티슈, 적응ER 및 스톱 콕 및 텅스텐 전극을 둘러싸 유리.
- 철저하게 완전히 유리에서 유기 진공 그리스를 제거하는 톨루엔 단계 9.1에서 설명 된 것과 동일한 표면을 청소합니다. 실리콘 그리스를 사용하는 경우, 높은 진공 그리스는 토론 섹션에 설명 된대로, 미래의 문제를 생성, 열분해 후 유리에 남아있을 수 있습니다.
- 철저히 위해 브러시 다음과 같은 용매에 반응 플라스크를 청소 : 5 % 클리닝 세제로 초순수 (18.2 MΩ cm, <5 PPB의 TOC), 초순수 (18.2 MΩ cm, <5 PPB의 TOC), 메탄올, 톨루엔, 메탄올, 5 % 청소 세제로 초순수 (18.2 MΩ cm, <5 PPB의 TOC), 그리고 마지막으로 초순수 (18.2 MΩ cm, <5 PPB의 TOC).
- 알루미늄 호일로 반응 플라스크의 열려있는 모든 구멍을 커버 알루미늄 호일에있는 어댑터와 해당 구성 요소를 래핑합니다.
- 모든 유리 제품은 알루미늄 호일에 싸서되면, 적어도 3 시간 동안 열분해500 ℃에서 공기
- 부드럽게 깨끗한 메탄올 전극과 공기 건조를 할 수 있습니다.
10. 샘플 분석
참고 : 분석을 위해 샘플을 준비 할 때, 다음과 같은 산 가수 분해 프로토콜의 사용이 밖에도 15 상세히 설명 하였지만, 이상의 아미노산을 얻는 데 유용하다. 회수 된 샘플의 부분 가수 분해 자유로운 아미노산뿐만 아니라 비 생물 성 조건에서 합성된다 그들의 산 - 불안정성 전구체 양을 분석 할 수있는 기회를 제공한다.
- 아미노산 분석을 위해, (예컨대, 액체 크로마토 그래피 및 질량 분석 방법을 기반으로, 또는 다른 적합한 방법)의 적합한 기술을 사용한다. 이러한 분석 기술은 형광 검출 (HPLC-FD) (14) 및 비행 시간 형 양성 전기 분무 이온화 질량 분석법 (UHPL와 병렬 형광 검출과 초고속 성능 액체 크로마토 그래피로 고성능 액체 크로마토 그래피를 포함C-FD/ToF-MS) 12, 13. 이 원고는 HPLC-FD와 함께 삼중 사중 극 질량 분석기 (QQQ-MS)을 통해 분석 질량 분석을 사용하여 분석을 설명합니다.
결과
방전 실험에서 합성 된 제품은 매우 복잡 할 수 있으며,이를 연구하는 데 사용할 수있는 다양한 분석 방법이있다. 아미노산 분석을위한 문헌에서 일반적으로 사용되는 기술 중 일부는 여기에 설명되어 있습니다. 크로마토 그래피 및 질량 분석 방법은 밀러 - 유리의 분류 스파크 방전 실험에 의해 생성 된 복잡한 화학 혼합물을 분석하는데 매우 유용한 기술이다. 아미노산은 오 -phthaldialdehyde...
토론
여기에 설명 된 프로토콜에있는 많은 단계를 안전하고 올바르게 밀러 - 유리의 형식 실험을 수행하기위한 중요합니다. 먼저, 반응 플라스크 또는 시료와 접촉 할 모든 유리 및 시료 처리 툴은 살균 될 필요가있다. 소독 철저 초순수 (18.2 MΩ cm, <5 PPB의 TOC)에 문제가있는 항목을 세척 한 후 이전에 적어도 3 시간 동안 공기 중에서 500 ℃에서 열분해에 알루미늄 호일에 그들을 배치함으로써 달성된다...
공개
저자는 더 경쟁 재정적 이익을 선언하지 않습니다.
감사의 말
이 작품은 공동으로 화학 진화, CHE-1004570 및 우주 생물학의 고다드 센터의 NSF 센터에서, NSF 및 NASA 우주 생물학 프로그램에 의해 지원되었다. ETP는 NASA 행성 생물학 인턴쉽 프로그램을 제공하는 추가 자금 조달을 인정하고 싶습니다. 저자는 또한 초기 실험실 시설을 설치하는데 많은 도움을 박사 Asiri Galhena 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| Glass Plugs for Manifold | Chemglass | CG-983-01 | |
| High Vacuum Grease | Apiezon | N/A | Type M/N |
| Silicon High Vacuum Grease | Dow Corning | 1597418 | |
| Teflon PFA Tubing | McMaster-Carr | 51805K54 | |
| Ultra-Torr Vacuum Fittings | Swagelok | SS-4-UT-6 | |
| Dry Scroll Vacuum Pump | Edwards | A72401905 | |
| U-Tube Manometer | Alta-Robbins | 100SS | |
| Tungsten Electrodes | Diamond Ground Products | TH2-1/16 | 2% thoriated |
| Methanol | Alfa Aesar | N/A | Ultrapure HPLC Grade |
| Teflon-Coated Magnetic Stir Bar | McMaster-Carr | 5678K127 | |
| Gaseous NH3 | Airgas | AMAHLB | 99.99% purity |
| Gaseous CH4 | Airgas | ME UHP300 | 99.99% purity |
| Gaseous N2 | Airgas | NI UHP300 | 99.999% purity |
| Tesla Coil | Electro-Technic Products | 15001 | Model BD-50E |
| 24 hr Plug-in Basic Timer | General Electric Company | 15119 | |
| Cleaning Detergent | Alconox | 1104 | |
| Toluene | Thermo Fisher Scientific | N/A | Optima Grade |
| Luna Phenyl-Hexyl HPLC Column | Phenomenex | 00G-4257-E0 | Brand: Luna |
| Formic Acid | Sigma-Alrich | F0507 | Used to make 50 mM ammonium formate |
참고문헌
- Oparin, A. I. . The Origin of Life. , (1924).
- Haldane, J. B. The origin of life. Rationalist Annu. 148, 3-10 (1929).
- Garrison, W. M., Morrison, D. C., Hamilton, J. G., Benson, A. A., Calvin, M. Reduction of Carbon Dioxide in Aqueous Solutions by Ionizing Radiation. Science. 114, 416-418 (1951).
- Miller, S. L. Production of Some Organic Compounds under Possible Primitive Earth Conditions. J. Am. Chem. Soc. 77, 2351-2361 (1955).
- Miller, S. L. A Production of Amino Acids Under Possible Primitive Earth Conditions. Science. 117, 528-529 (1953).
- Heyns, H. K., Walter, W., Meyer, E. Model experiments on the formation of organic compounds in the atmosphere of simple gases by electrical discharges (Translated from German). Die Naturwissenschaften. 44, 385-389 (1957).
- Ponnamperuma, C., Woeller, F. α-Aminonitriles formed by an electric discharge through a mixture of anhydrous methane and ammonia. Biosystems. 1, 156-158 (1967).
- Oró, J. Synthesis of Organic Compounds by Electric Discharges. Nature. 197, 862-867 (1963).
- Ring, D., Wolman, Y., Friedmann, N., Miller, S. L. Prebiotic Synthesis of Hydrophobic and Protein Amino Acids. Proc. Natl. Acad. Sci. U.S.A. 69, 765-768 (1972).
- Wolman, Y., Haverland, W. J., Miller, S. L. Nonprotein Amino Acids from Spark Discharges and Their Comparison with the Murchison Meteorite Amino Acids. Proc. Natl. Acad. Sci. U.S.A. 69, 809-811 (1972).
- Roscoe, S., Miller, S. L. Energy Yields for Hydrogen Cyanide and Formaldehyde Syntheses: The HCN and Amino Acid Concentrations in the Primitive Ocean. Orig. Life. 17, 261-273 (1987).
- Johnson, A. P., et al. The Miller Volcanic Spark Discharge Experiment. Science. 322, 404 (2008).
- Parker, E. T., et al. Primordial synthesis of amines and amino acids in a 1958 Miller H2S-rich spark discharge experiment. Proc. Natl. Acad. Sci. U.S.A. 108, 5526-5531 (2011).
- Cleaves, H. J., Chalmers, J. H., Lazcano, A., Miller, S. L., Bada, J. L. A reassessment of prebiotic organic synthesis in neutral planetary atmospheres. Orig. Life Evol. Biosph. 38, 105-115 (2008).
- Glavin, D. P., et al. Amino acid analyses of Antarctic CM2 meteorites using liquid chromatography-time of flight-mass spectrometry. Meteorit. Planet. Sci. 41, 889-902 (2006).
- Zhao, M., Bada, J. L. Determination of α-dialkylamino acids and their enantiomers in geologic samples by high-performance liquid chromatography after a derivatization with a chiral adduct of o-phthaldialdehyde. J. Chromatogr. A. 690, 55-63 (1995).
- Strecker, A. About the artificial formation of lactic acid and a new Glycocoll the homologous body Justus Liebigs Annalen der Chemie. 75, 27-45 (1850).
- Miyakawa, S., Yamanashi, H., Kobayashi, K., Cleaves, H. J., Miller, S. L. Prebiotic synthesis from CO atmospheres: implications for the origins of life. Proc. Natl. Acad. Sci. U.S.A. 99, 14628-14631 (2002).
- Kobayashi, K., Kaneko, T., Saito, T., Oshima, T. Amino Acid Formation in Gas Mixtures by Particle Irradiation. Orig. Life Evol. Biosph. 28, 155-165 (1998).
- Sagan, C., Khare, B. N. Long-Wavelength Ultraviolet Photoproduction of Amino Acids on the Primitive Earth. Science. 173, 417-420 (1971).
- Harada, K., Fox, S. W. Thermal Synthesis of Natural Amino-Acids from a Postulated Primitive Terrestrial Atmosphere. Nature. 201, 335-336 (1964).
- Ponnamperuma, C., Lemmon, R. M., Mariner, R., Calvin, M. Formation of Adenine by Electron Irradiation of Methane Ammonia, and Water. Proc. Natl. Acad. Sci. USA. 49, 737-740 (1963).
- Bar-Nun, A., Bar-Nun, N., Bauer, S. H., Sagan, C. Shock Synthesis of Amino Acids in Simulated Primitive Environments. Science. 168, 470-473 (1970).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유