JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
단일 분자 수준에서 순환 고분자의 합성 및 용융 상태에서 그들의 확산 운동의 특성
요약
합성 및 단일 분자 수준에서 순환 고분자의 확산 움직임의 특성에 대한 프로토콜이 제공됩니다.
초록
We demonstrate a method for the synthesis of cyclic polymers and a protocol for characterizing their diffusive motion in a melt state at the single molecule level. An electrostatic self-assembly and covalent fixation (ESA-CF) process is used for the synthesis of the cyclic poly(tetrahydrofuran) (poly(THF)). The diffusive motion of individual cyclic polymer chains in a melt state is visualized using single molecule fluorescence imaging by incorporating a fluorophore unit in the cyclic chains. The diffusive motion of the chains is quantitatively characterized by means of a combination of mean-squared displacement (MSD) analysis and a cumulative distribution function (CDF) analysis. The cyclic polymer exhibits multiple-mode diffusion which is distinct from its linear counterpart. The results demonstrate that the diffusional heterogeneity of polymers that is often hidden behind ensemble averaging can be revealed by the efficient synthesis of the cyclic polymers using the ESA-CF process and the quantitative analysis of the diffusive motion at the single molecule level using the MSD and CDF analyses.
서문
Cyclic polymers are unique in that they do not have chain ends. They often exhibit unusual behaviors which is distinct from their linear counterpart, including increased thermal stability of polymer micelles by a linear-to-cyclic conversion,1,2 and spatial organization of DNA in bacterial cells by a loop formation.3 Topological interactions between the cyclic chains are believed to be the critical factor for such unusual behaviors.4,5 Therefore, characterizing the motion and relaxation of cyclic polymers under entangled conditions has been an important research topic in polymer science for decades.6
Cyclic polymer dynamics has been investigated using both synthetic and naturally occurring molecules by means of ensemble averaged experimental methods such as nuclear magnetic resonance (NMR), light scattering, and viscosity measurements.7-9 However, these studies often suffer from impurity molecules in the samples.10 Furthermore, spatiotemporal heterogeneities of the motion of individual molecules caused by inherent structural heterogeneity of entangled polymers are often hidden behind the ensemble averaging in these studies. In order to characterize molecular level dynamics of cyclic polymers, a synthesis method that provides high purity cyclic polymers and an experimental and analysis methods that allow for quantitative characterization of molecular motion at the single molecule level have to be developed. Here, we will show a method to synthesize high-purity cyclic and dicyclic poly(THF)s that incorporate a fluorophore unit using an electrostatic self-assembly and covalent fixation (ESA-CF) process11-13 and a method to analyze the motion of the individual fluorophore-incorporated polymer chains using a combination of mean-squared displacement (MSD) and cumulative distribution function (CDF) analyses.
A proper data processing has been shown to be essential for the accurate characterization of the diffusive motion. With an adequate MSD and CDF analyses, a multiple-mode diffusion of the cyclic and dicyclic polymers in the melt and semi-dilute solution of the linear polymer chains has been revealed,14-16 suggesting the significant effects of the topological states of the polymers on the diffusive motion of the chains under entangled conditions.17 While the experimental and analytical approaches to characterize the motion of the cyclic polymers are described in this protocol, the same method can be used to quantitatively characterize the diffusive motion in many other heterogeneous systems. The approach would be especially suitable when multiple diffusion components existing in the samples are to be analyzed.
프로토콜
단관 능성 및 이작 용성 폴리 1. 합성 (THF)
- 관능 폴리 (THF)
- 불꽃 2 구 100 ㎖의 둥근 바닥 플라스크를 건조. 진공 및 질소 (3 회)와 플라스크를 입력합니다.
- 플라스크에 증류수 테트라 하이드로 퓨란 (THF) (50 ㎖)를 추가합니다. 20 ℃에서 물을 용기에 플라스크를 놓고, 온도를 평형화.
- 주사기로 플라스크에 메틸 트리 플레이트 (0.5 밀리몰)를 추가합니다. 20 ° C에서 5 ~ 10 분 동안 혼합물을 교반한다.
- 주사기로 플라스크에 N의 페닐 피 롤리 딘 (4-6 당량.)를 추가합니다. 30 ~ 60 분 동안 혼합물을 교반한다.
- 완전히 감압 (약 100 토르)에서 용매를 제거한다. 아세톤 3-5 ml의 잔류 물을 용해. n 개의 헥산 300 ~ 500 ml의에 아세톤 용액을 추가합니다. 침전물을 여과하고, 감압하에 건조.
- 관능 성 폴리 (THF)
- 불꽃 2 구 100 ㎖의 둥근 바닥 플라스크를 건조. 버지니아cuum 질소 (3 회)와 플라스크를 입력합니다.
- 플라스크에 증류수 THF (50 ㎖)를 추가합니다. 20 ℃에서 물을 용기에 플라스크를 놓고, 온도를 평형화.
- 주사기로 플라스크에 트리플 무수물 (0.3 밀리몰)를 추가합니다. 20 ° C에서 5 ~ 10 분 동안 혼합물을 교반한다.
- 주사기로 플라스크에 N의 페닐 피 롤리 딘 (4-6 당량.)를 추가합니다. 30 ~ 60 분 동안 혼합물을 교반한다.
- 완전히 감압 (약 100 토르)에서 용매를 제거한다. 아세톤 3-5 ml의 잔류 물을 용해. n 개의 헥산 300 ~ 500 ml의 아세톤 용액을 추가합니다. 침전물을 여과하고, 감압하에 건조.
2. 페 릴렌의 합성 디이 미드 통합 4 무장 스타 8 모양의 Dicyclic 폴리 (THF)
- 무장 스타 폴리 (THF)
- 이온 교환
- 물, 페 릴렌 테트라 카르 복실 디이 미드의 나트륨 염 (10 ㎎ / ㎖, 150 ㎖)에 녹인다. 디졸브아세톤 관능 폴리 (THF) (160 ㎎ / ㎖, 4 ㎖). 격렬하게 교반 수용액에 아세톤 용액에 적가를 추가합니다. 여과에 의해 형성된 침전물을 수집합니다.
- 회수 된 침전물 (2.1.1.1) 네 배와 위의 절차를 반복합니다.
- 공유 고정
- 톨루엔 얻어진 침전물 (5 ㎎ / ㎖)에 녹인다. 4 시간 동안 용액을 환류시켰다.
- 완전히 감압 (약 100 토르)에서 용매를 제거한다. n은 헥산 / 아세톤 (2/1 부피 / 부피) 실리카 겔 플러그를 통해 잔류 물 필터. 생성물을 침전 빙수 (300-500 mL)에 상기 용액을 추가한다. 여과에 의해 침전물을 수집합니다.
- 이온 교환
- Dicyclic 8 모양의 폴리 (THF)
- 이온 교환
- 물, 페 릴렌 테트라 카르 복실 디이 미드의 나트륨 염 (6 ㎎ / ㎖, 50 ㎖)에 녹인다. (0.5 g을 관능 성 폴리 (THF)을 녹여) 아세톤의 30 ~ 50 ml를한다. 0 ° C에서 격렬하게 교반 수용액에 아세톤 용액에 적가를 추가합니다. 여과에 의해 형성된 침전물을 수집합니다.
- 회수 된 침전물 (2.2.1.1)으로 위의 절차를 반복합니다.
- 공유 고정
- 톨루엔 얻어진 침전물 (0.05 g / L)을 녹인다. 4 시간 동안 용액을 환류시켰다.
- 완전히 감압 (약 100 토르)에서 용매를 제거한다. 부분적으로 잔류 물을 용해 톨루엔을 추가합니다. 다시 침전 N 헥산 300 ~ 500 ml의에.
- n은 헥산 / 아세톤 (2/1 부피 / 부피) 실리카 겔 플러그를 통해 형성된 침전물을 필터링. 다시 침전 물 300 ~ 500 ml의에.
- 폴리스티렌 겔을 사용하는 컬럼 크로마토 그래피 (18)에 의해 형성된 침전물을 정제. 또한, REM에 클로로포름의 용리액 19 분취 겔 투과 크로마토 그래피 (GPC)에 의해 조질 생성물을 정제굴절율 (RI) 및 UV 검출기를 모니터링하여 비켜 부산물.
- 이온 교환
3. 단일 분자 형광 이미징 실험
- 샘플 준비
- 현미경 커버 전표의 청소
- 장소 번호 1.5 24 X 24mm 현미경 커버 염색 항아리에 미끄러 져.
- 15 분의 항아리와 초음파 처리로 1 M 포타슘 하이드 라이드 용액 (100 ㎖)를 추가합니다. 경사 분리하여 수산화 칼륨 용액을 붓고 수회 초순수 커버 슬립을 헹군다. 15 분의 항아리와 초음파 처리로 분광 등급 에탄올 (100 ㎖)를 추가합니다.
- 경사 분리하여 에탄올을 붓고 수회 초순수 커버 슬립을 헹군다. 경사 분리하여 초순수를 주입 한 후, 단계 3.1.1.2를 반복한다.
- 15 분의 항아리와 초음파 처리에 초순수를 추가합니다. 여러 번 초순수 커버 슬립 린스. 플라스틱 핀셋으로 항아리에서 커버 슬립을 꺼내 건조 공기 또는 건조 질소 중 하나에 의해 그들을 건조.
- 중합체 용융물의 샘플을 14, 15의 제조
- 유리 병에 표지되지 않은 선형 폴리 (THF) 100 ㎕를 추가하고는 헤어 드라이어를 이용하여 융점 (약 25 ℃) 이상의 온도로 가열한다.
- 형광 물질이 함유 중합체 (선형, 4- 무장 스타, 환상 또는 8 자형 dicyclic 2.1 2.2 합성)의 클로로포름 (1 ㎖, 10-6 M)을 녹인다. 비 표지 된 선형 폴리 (THF)의 용융물의 100 μL 용액을 1 μL를 추가한다.
- 철저하게 피펫 팁과 샘플을 혼합 한 후, 건조기를 사용하여 샘플을 가열하여 클로로포름을 증발시켰다.
주 :이 형광 혼입 폴리머 10-8 M을 함유하는 표지되지 않은 선형 폴리 (THF)의 용융물을 제공한다. - 샘플의 10 μL 마이크로 피펫 및 D를 사용하여보세요세정 커버 슬립에 그것을 ROP. 샘플의 다른 청소 커버 슬립을 넣고 두 커버 전표 사이의 샘플을 샌드위치.
- 부드럽게 플라스틱 핀셋을 사용하여 샘플을 누릅니다.
- 현미경 커버 전표의 청소
- 와이드 필드 형광 촬상 설정 15
- 반전 현미경의 뒷면 포트에 여기 레이저 (488 nm의) 소개
- 빔 경로에 여기 대역 필터 및 편광자를 삽입한다.
- 빔 확장기에 의해 직경 약 1cm에 빔을 확장합니다.
- 빔 경로에 1/4 파장 판을 삽입한다. 편광자의에 대하여 45도에서 파장 판의 광축을 설정한다. 또는, Berek 보상기를 삽입 및 / 4 λ하는 광학 지연을 설정합니다.
- 빔의 크기를 조정할 여기 빔 경로에 다이어프램을 삽입한다.
- 반전 광 microsco의 후면 포트에 레이저 광을 도입하기 전PE, 집광 렌즈 삽입 (평면 - 볼록 렌즈의 초점 거리를 ≈ 300mm)의 대물 렌즈 중 레이저 빔이 시준 된 위치.
- 필터 큐브에 장착 된 이색 미러를 사용하여 레이저 빔을 반사 한 후, 고 개구 수 (NA)의 대물 렌즈를 통해 샘플에 레이저 광을 도입 (예를 들면, NA 1.3, 100X 배율 오일 침지).
- 대물 렌즈에 목적 히터를 부착하고 30 ° C까지 온도를 설정합니다.
- 거꾸로 현미경의 무대에 샘플을 장착
- 대물 렌즈에 침지 기름 한 방울을 떨어 뜨리고 현미경 상태에서 샘플을 탑재합니다.
- 약 10 ㎛, 시료의 두께가 시료의 바닥 및 상부면의 축 방향 위치를 확인하여 수득되는 것을 보장한다.
- 샘플의 하부 표면 위의 몇 마이크로 미터 현미경의 초점을 조정한다.
- 대물 렌즈에서 원형 편광 여기 광을 얻습니다
- 대물 렌즈의 밖으로 평행 레이저 빔에 편광판을 삽입합니다.
- 편광자 후 파워 미터를 삽입하여 편광판을 투과 한 레이저의 강도를 기록한다. 편광자를 회전시킴으로써 서로 다른 편광 각도로 투과 레이저 파워를 기록한다.
- 전송 레이저 파워 모든 편광 각도에서 일정하지 않으면, 약간의 여기 빔 경로에 삽입 된 1/4 파장 판 또는 Berek 보상기를 회전한다.
- 상수 전송 레이저 출력 될 때까지 단계를 반복 3.2.5.2 및 3.2.5.3은 모든 편광 각도에서 얻을 수있다. 원 편광이 샘플을 얻을 수 있는지 확인합니다.
- 설치 전각 (전자 승산이) 장치 연결 - 전하 (CCD) 카메라
- 현미경의 측면 포트 EM-CCD 카메라를 부착와 T에 연결화상 획득 소프트웨어를 그가.
- 필요한 경우, 장치에 EM-CCD 카메라에 의해 생성 된 트랜지스터 - 트랜지스터 논리 (TTL) 신호를 전송하여 기계적 셔터 또는 여기 빔 경로에 삽입 음향 광 여과기 카메라 노출을 동기화. 대안 적으로, 레이저에 EM-CCD 카메라에 의해 생성 된 TTL 신호를 보내어 레이저 출력으로 상기 카메라 노출을 동기화.
주 : 출력이 입력 전력 트랜지스터 - 트랜지스터 논리에 의해 변조 될 수있는 고체 레이저 (TTL) 신호가 실험에 사용되는 경우에만 후자의 옵션이 적용될 수있다. - 단일 형광 물질의 고품질의 형광 이미지를 얻기 위해 카메라를 제어하는 소프트웨어를 사용하여 CCD 카메라에 EM 이득 (일반적으로 약 300)을 적용한다.
- ROI (region of interest)를 카메라를 제어하는 소프트웨어를 사용하여 (시야의 중심에 통상적으로 128 X 128 픽셀)로 설정한다.
주 :이 imagi 허용용융 샘플 내의 형광 물질이 함유 된 고분자 사슬의 움직임을 시각화에 필요한 프레임 전송 모드, 200 Hz에서 - (100)의 프레임 속도 (NG) 실험.
- 반전 현미경의 뒷면 포트에 여기 레이저 (488 nm의) 소개
- 실험을 실행
- 실험 조건 최적화
- 상기 여기 광의 경로에 삽입 된 진동판을 사용하여 직경 약 20 ㎛, 시료의 조명 영역을 조정한다.
- 수동 여기 빔 경로에 삽입 된 적절한 감광 (ND) 필터를 선택하여 8 mW의 - (4) 시료에 여기 레이저 파워를 설정한다.
참고 : - 2 kW 급 cm -2 샘플에서이 일의 평균 레이저 파워를 제공한다. - 200 Hz에서 - (100)의 프레임 속도로 샘플의 형광 기록 화상. 각 형광 물질이 함유 중합체로부터 얻어지는 형광 강도가 너무 낮 으면, 서서히 제를 사용하여 여기 전력을 증가샘플에서 약 100 mW에 도달 할 때까지 전자 ND 필터.
- 단일 분자 형광 화상의 품질이 여전히 만족스럽지 않으면, 표지되지 않은 폴리 (THF)의 순수 용융물의 형광 화상을 기록하여 샘플에서 형광 불순물을 확인한다. 높은 형광 배경이 관찰되는 경우, 다른 비 표지 폴리 (THF)을 사용합니다.
- 용융물에 형광 물질이 함유 중합체로부터 얻어지는 형광 스폿의 밀도가 공간을 (이 확산 동작의 분석에 오류를 발생) 분리가 너무 높으면 시료까지의 형광 물질이 함유 중합체의 농도를 감소 공간적으로 격리 된 반점이 관찰된다.
- 용융물에 형광 물질이 함유 중합체로부터 얻어지는 형광 스폿의 밀도 (이 이미징 실험의 낮은 처리량을 초래)가 너무 낮은 경우, appropr까지 시료에 형광 물질이 함유 중합체의 농도를 증가형광 현장의 늦었 밀도에 도달한다.
- 용융물의 형광 물질이 함유 중합체로부터 얻어지는 형광 이미지를 흐리게하는 경우, 화상 취득의 프레임 속도를 증가시킨다.
참고 :이 종종 일반적으로, 64 X 64 픽셀의 작은 투자 수익 (ROI)을 필요로한다.
- 실험 조건 최적화
- 이미지 획득
- 실험 조건이 최적화되면 시료가 평형 상태에 도달 할 수 있도록, 한 시간 동안 현미경 무대에 장착 된 샘플을 둡니다.
- 200Hz의 프레임 속도 - 100에 용융 상태의 형광 물질이 함유 된 고분자 1000 형광 이미지 시퀀스 - (500)를 기록한다. 기본 파일 형식은 TIFF 없으면, TIFF 형식으로 모든 이미지 시퀀스를 변환한다.
확산 모션 4. 분석
- 평균 제곱 변위 (MSD) 분석
- 같은 방법으로 형광 이미지 시퀀스 자르기각 이미지 시퀀스는 ImageJ에 같은 단일 잘 집중 확산 형광 물질이 함유 된 고분자 이용한 화상 처리 소프트웨어를 포함하고있다.
- 절단 된 이미지 시퀀스는 10 개 이상의 프레임들을 포함하면, 각각의 시퀀스가 10 프레임으로 구성되도록 복수의 시퀀스로 이미지 시퀀스를 분할.
- 정확하게 화상의 2 차원 가우시안 끼움 각 이미지 시퀀스에서의 분자의 위치를 결정한다.
- 수학 식 20을 이용하여 확산 계수 (D) 각각의 분자 확산 궤적 (분자, 즉, 시간에 따른 위치)의 평균 제곱 변위 (MSD) 분석에 의해 결정을
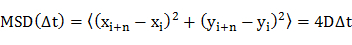
× 1 및 y i는 이미지 프레임 I의 분자의 위치이고, n은 프레임 전으로부터의 Δt 시간 경과와 프레임 번호를 나타낸다. - 의 확산 계수 플롯주파수 히스토그램.
참고 : 일반적으로, 히스토그램은 100 개 이상의 분자로 구성되어있다.
- 누적 분포 함수 (CDF) 분석
주 : CDF, P (R (2)는 I Δ t) 내가 t δ 일정 시간 지연 후 원점으로부터 반경 (R) 내에 확산 분자를 찾는 누적 확률에 대응한다.- 시간이 4.1.3에서 얻은 모든 확산 궤적에 대한 1Δt, 2Δt, ····, iΔt의 지연 동안 발생 제곱 변위를 계산합니다.
주 : 시간이 iΔt의 지연에 대한 이러한 계산은 총 내가 제곱 - 변위 m를 제공합니다. - 다른 R 2 값에서 R 2보다 작은 총 m의 전 데이터 세트 내에서 제곱 - 변위 (리터 I)의 수를 계산 (0 2 대 정규화 리터의 난 플롯은 CDF, P (R 2, iΔt)에 해당합니다.
- 시간이 4.1.3에서 얻은 모든 확산 궤적에 대한 1Δt, 2Δt, ····, iΔt의 지연 동안 발생 제곱 변위를 계산합니다.
- 별개의 확산 모델 CDFS 분석
참고 : 얻어진 CDFS는 별개의 확산 모델이 장착되어 있습니다; 균일 확산 모델은 D 분포가 가우시안 (단일 가우시안 모델)에 의해 설명되는 여러 확산 모드, 다중 확산 모드가되는 D 분포 다중 가우시안 (다중 가우시안 모델)에 의해 설명된다.- 균일 확산 모델에서는, 수학 식 21을 사용하여 CDF를 끼워 맞춤으로써, 평균 D를 결정
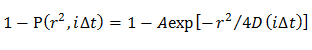
주 : 방정식에서 벗어나 분자의 이종 확산을 제안한다. - 단일 가우스 모델에서는 15을 사용하여 CDF 피팅하여 가우시안 (F (D))에 의해 기술 D의 확률 분포를 결정
켜기 3 "SRC ="/ 파일 / ftp_upload / 54503 / 54503equation3.jpg "/>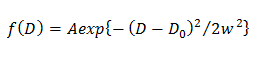
A, W 및 D는 0 가우스의 크기, 폭 및 중심 어디에. - 더블 가우시안 모델 (14)을 사용하여 CDF를 끼워 맞춤으로써 가우시안 (F (D))에 의해 기술 D 성분 J 번째의 확률 분포를 결정
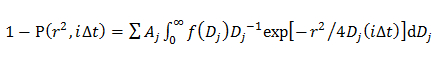

J는 각각의 확산 성분의 분획, α 및 J와 J w 및 D 0 J이고 가우스 성분 j 번째의 크기, 폭 및 중심이다.
- 균일 확산 모델에서는, 수학 식 21을 사용하여 CDF를 끼워 맞춤으로써, 평균 D를 결정
- 이론적 확률 DISTRI의 계산확산 계수의 bution
참고 : 인해 다른 확산 모델에 대해 계산 된 통계 오류 (P (D) D의 D)에 발생하는 D의 확률 분포; 균일 확산 모델은 D 분포가 가우시안 (단일 가우시안 모델)에 의해 설명되는 여러 확산 모드, 다중 확산 모드가되는 D 분포 다중 가우시안 (다중 가우시안 모델)에 의해 설명된다.- 균일 확산 모델에서는, 수학 식 22를 이용하여 D의 통계적 확률 분포를 계산
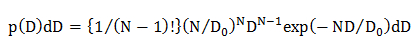
N이 확산 궤도 데이터 포인트의 수 (N = 10, 4.1.2 참조)이고, D 0 평균 확산 계수 (CDF를 분석에 의해 측정이 4.2.3.1 참조)이고, D는 실험적으로 얻어진 개별 궤도 용 확산 계수. - 에서단일 가우시안 확산 모델은 수학 식 15를 이용하여 D의 통계적 확률 분포를 계산

F (D)은 CDF 분석에 의해 결정된 D의 확률 분포 (4.2.3.2 참조)이고, D는 0 평균 확산 계수이다합니다 (CDF 분석에 의해 결정 4.2.3.2 참조). - 더블 가우시안 확산 모델에서는, 수학 식 14를 이용하여 D의 통계적 확률 분포를 계산

F (D의 J)은 CDF 분석에 의해 결정된 D (D의 j) 성분 j 번째의 확률 분포를 나타내고 (4.2.3.3 참조), 그리고 D의 0j은 CDF 결정 요소 j 번째 (평균 확산 계수 분석) 4.2.3.3를 참조하십시오.
- 균일 확산 모델에서는, 수학 식 22를 이용하여 D의 통계적 확률 분포를 계산
결과
페 릴렌 4 무장 스타를 디이는-통합 8 모양의 dicyclic 폴리 (THF) s는 정전 자기 조립 및 공유 고정 (ESA-CF) 프로세스 (그림 1, 그림 2)를 사용하여 합성 하였다. 시간 경과 단일 분자 형광 이미지는 4 무장 (그림 3a)를 측정하고 (그림 3b) 중합체를 8 자형 하였다. 시간 경과 형광 이미지 (그림 3)은 공간적으로 인해 체인?...
토론
4 무장과 8 모양의 중합체. 합성을위한 중요한 단계 인 ESA-CF 프로토콜 (그림 1)을 통해 제조 12, 24 단관 능성과 관능 성 선형 폴리 (THF)의 N -phenylpiperidinium 말 단기와이었다 하였다 위의 절차에 따라 합성. 11 이온 교환 복실 과잉 량을 함유하는 수용액에 트리 플레이트 카운터 음이온을 가진 폴리머 전구체의 아세톤 용액으로 재침을 실시 하였다.
공개
The authors have nothing to disclose.
감사의 말
This work was supported by a Grant-in-Aid for Scientific Research No. 22750122 (S.H.), No. 26288099 (T.Y.), and No. 23350050 (Y.T.) of the Japan Society for the Promotion of Science. S.H. is grateful for The Kurata Memorial Hitachi Science and Technology Foundation. The research reported in this publication was supported by the King Abdullah University of Science and Technology (S.H.).
자료
| Name | Company | Catalog Number | Comments |
| Materials | |||
| THF | Godo | ||
| Wakosil C-300 | Wako Pure Chemical Industries | ||
| Acetone | Godo | ||
| Toluene | Godo | ||
| n-Hexane | Godo | ||
| CHCl3 | Kanto Chemical | ||
| Bio-Beads S-X1 | Bio-Rad | ||
| Methyl triflate | Nacalai Tesque | ||
| Triflic anhydride | Nacalai Tesque | ||
| Potassium Hydroxide | Wako Pure Chemical Industries | ||
| Ethanol | Wako Pure Chemical Industries | ||
| Poly(tetrahydrofuran) | Aldrich | ||
| Chloroform | Wako Pure Chemical Industries | ||
| Immersion oil | Cargille | Type 37 / Type A | |
| Equipment | |||
| 2-Neck 100-ml round-bottom flask | |||
| Flask | |||
| Beaker | |||
| Funnel | |||
| Filter paper | Whatman | ||
| Reflux condenser | |||
| Syringe | |||
| Water bath | |||
| Magnetic stirrer | |||
| Rotary evaporator | |||
| Microscope cover slips (24 x 24 mm, No. 1) | Matsunami Glass | CO22241 | |
| Staining jar | AS ONE Corporation | 1-7934-01 | |
| Ultrasonic cleaner | VWR International | 142-0047 | |
| Inverted microscope | Olympus | IX71 | |
| Ar-Kr ion laser | Coherent | Innova 70C | |
| Berek compensator | Newport | 5540 | |
| Excitation filter | Semrock | LL01-488-12.5 | |
| Dichloric mirror | Omega optical | 500DRLP | |
| Emission filter | Semrock | BLP01-488R-25 | |
| Lens and mirror | Thorlabs | ||
| EM-CCD camera | Andor Technology | iXon | |
| Objective lens (100X, N.A. = 1.3) | Olympus | UPLFLN 100XOP | |
| Objective heater | Bioptechs | ||
| Preparative GPC | Japan Analytical Industry | LC-908 |
참고문헌
- Honda, S., Yamamoto, T., Tezuka, Y. Topology-Directed Control on Thermal Stability: Micelles Formed from Linear and Cyclized Amphiphilic Block Copolymers. J. Am. Chem. Soc. 132 (30), 10251-10253 (2010).
- Honda, S., Yamamoto, T., Tezuka, Y. Tuneable enhancement of the salt and thermal stability of polymeric micelles by cyclized amphiphiles. Nat. Commun. 4, (2013).
- Jun, S., Mulder, B. Entropy-driven spatial organization of highly confined polymers: Lessons for the bacterial chromosome. Proc. Natl. Acad. Sci. U. S. A. 103 (33), 12388-12393 (2006).
- McLeish, T. Polymers without beginning or end. Science. 297 (5589), 2005-2006 (2002).
- McLeish, T. Polymer dynamics: Floored by the rings. Nat. Mater. 7 (12), 933-935 (2008).
- Roovers, J., Tezuka, Y. . Topological Polymer Chemistry: Progress of Cyclic Polymers in Syntheses, Properties and Functions. , 137-156 (2013).
- Klein, J. Evidence for reptation in an entangled polymer melt. Nature. 271 (5641), 143-145 (1978).
- Leger, L., Hervet, H., Rondelez, F. Reptation in entangled polymer-solutions by forced rayleigh light-scattering. Macromolecules. 14 (6), 1732-1738 (1981).
- von Meerwall, E. D., Amis, E. J., Ferry, J. D. Self-diffusion in solutions of polystyrene in tetrahydrofuran - comparison of concentration dependences of the diffusion-coefficients of polymers, and a ternary probe component. Macromolecules. 18 (2), 260-266 (1985).
- Kapnistos, M., et al. Unexpected power-law stress relaxation of entangled ring polymers. Nat. Mater. 7 (12), 997-1002 (2008).
- Adachi, K., Takasugi, H., Tezuka, Y. Telechelics having unstrained cyclic ammonium salt groups for electrostatic polymer self-assembly and ring-emitting covalent fixation. Macromolecules. 39 (17), 5585-5588 (2006).
- Oike, H., Imaizumi, H., Mouri, T., Yoshioka, Y., Uchibori, A., Tezuka, Y. Designing unusual polymer topologies by electrostatic self-assembly and covalent fixation. J. Am. Chem. Soc. 122 (40), 9592-9599 (2000).
- Yamamoto, T., Tezuka, Y. Topological polymer chemistry: a cyclic approach toward novel polymer properties and functions. Polym. Chem. 2 (9), 1930-1941 (2011).
- Habuchi, S., Fujiwara, S., Yamamoto, T., Tezuka, Y. Single-molecule imaging reveals topological isomer-dependent diffusion by 4-armed star and dicyclic 8-shaped polymers. Polym. Chem. 6 (22), 4109-4115 (2015).
- Habuchi, S., Fujiwara, S., Yamamoto, T., Vacha, M., Tezuka, Y. Single-Molecule Study on Polymer Diffusion in a Melt State: Effect of Chain Topology. Anal. Chem. 85 (15), 7369-7376 (2013).
- Habuchi, S., Satoh, N., Yamamoto, T., Tezuka, Y., Vacha, M. Multimode Diffusion of Ring Polymer Molecules Revealed by a Single-Molecule Study. Angew. Chem. Int. Ed. 49 (8), 1418-1421 (2010).
- Habuchi, S., Tezuka, Y. . Topological Polymer Chemistry: Progress of Cyclic Polymers in Syntheses, Properties and Functions. , 265-290 (2013).
- Fernandez, P., Bayona, J. M. Use of off-line gel-remeation chromatography normal-phase liquid-chromatography fro the determination of polycyclic aromatic-compounds in environmental-samples and standard reference materials (air particulate matter and marine sediment). J. Chromatogr. 625 (2), 141-149 (1992).
- Biesenberger, J. A., Tan, M., Duvdevan, I., Maurer, T. Recycle gel permeation chromatography. 1. recycle principle and design. J. Polym. Sci. Pol. Lett. 9 (5), 353 (1971).
- Kusumi, A., Sako, Y., Yamamoto, M. Confined lateral diffusion of membrane-receptors as studied by single-particle tracking (nanovid microscopy) - effects of calcium-induced differentiation in cultured epithelial-cells. Biophys. J. 65 (5), 2021-2040 (1993).
- Schutz, G. J., Schindler, H., Schmidt, T. Single-molecule microscopy on model membranes reveals anomalous diffusion. Biophys. J. 73 (2), 1073-1080 (1997).
- Vrljic, M., Nishimura, S. Y., Brasselet, S., Moerner, W. E., McConnell, H. M. Translational diffusion of individual class II MHC membrane proteins in cells. Biophys. J. 83 (5), 2681-2692 (2002).
- Margineanu, A., et al. Photophysics of a water-soluble rylene dye: Comparison with other fluorescent molecules for biological applications. J. Phys. Chem. B. 108 (32), 12242-12251 (2004).
- Tezuka, Y., Oike, H. Self-assembly and covalent fixation for topological polymer chemistry. Macromol. Rapid Commun. 22 (13), 1017-1029 (2001).
- Deres, A., et al. The Origin of Heterogeneity of Polymer Dynamics near the Glass Temperature As Probed by Defocused Imaging. Macromolecules. 44 (24), 9703-9709 (2011).
- Flier, B. M. I., et al. Heterogeneous Diffusion in Thin Polymer Films As Observed by High-Temperature Single-Molecule Fluorescence Microscopy. J. Am. Chem. Soc. 134 (1), 480-488 (2012).
- Habuchi, S., Oba, T., Vacha, M. Multi-beam single-molecule defocused fluorescence imaging reveals local anisotropic nature of polymer thin films. Phys. Chem. Chem. Phys. 13 (15), 6970-6976 (2011).
- Zettl, U., et al. Self-Diffusion and Cooperative Diffusion in Semidilute Polymer Solutions As Measured by Fluorescence Correlation Spectroscopy. Macromolecules. 42 (24), 9537-9547 (2009).
- Kirstein, J., Platschek, B., Jung, C., Brown, R., Bein, T., Brauchle, C. Exploration of nanostructured channel systems with single-molecule probes. Nat. Mater. 6 (4), 303-310 (2007).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유