JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
디페닐 에테르의 수산화를 위한 Pt/CNTs 촉매의 산도 튜닝
요약
HNbWO6,HNbMoO 6,HTaWO6 고체 산 나노 시트 변형 Pt /CNTs의 합성을위한 프로토콜이 제시된다.
초록
본명은 HNbWO6,HNbMoO 6,HTaWO6 고체 산 나노시트 변형 Pt/CNTs의 합성방법을 제시한다. 다양한 고체 산 나노 시트의 무게를 변화시킴으로써, 다른고체 산 조성물을 가진 일련의 Pt/xHMNO 6/CNTs(x= 5, 20 wt%; M = Nb, 타; N =Mo, W)는 탄소 나노튜브 전처리, 프로토닉 교환, 고체 산 박리, 응집 및 최종 Pt 입자 함침에 의해 제조되었다. Pt/xHMNO6/CNT는 X선 회절, 주사 전자 현미경, 투과 전자 현미경 및 NH3-온도 프로그래밍 탈착이 특징입니다. 연구 결과는 HNbWO6 나노 시트가 CNTs에 부착되었다는 것을 밝혔습니다, 나노 시트의 일부 가장자리는 모양에 구부러지고. 지원되는 Pt 촉매의 산 강도는 다음과 같은 순서로 증가합니다: Pt/CNTs& Pt/5HNbWO 6/CNTs & Pt/20HNbMoO 6/CNTs & Pt/20HNbWO6/LT&PT/20HTaWO6/CNTs. 또한, 리그닌 유래 모델 화합물의 촉매 수소 변환: 합성된 Pt/20HNbWO6 촉매를 이용한 디페닐 에테르가 조사되었다.
서문
화학 물질의 제조를위한 많은 산업 공정은 수성 무기 산의 사용을 포함한다. 한 가지 대표적인 예는 사이클로헥산올을 생산하는 사이클로헥산의 수화를 위한 종래의H2SO4 공정이다. 이 과정은 유기 상에 있는 사이클로헥산과 산성 수성 상에 있는 사이클로헥산 생성물로, 따라서 간단한 증류에 의하여 분리 과정을 어렵게 하는 양면 시스템을 관련시킵니다. 분리 및 회수의 어려움 외에도 무기산은 장비에 매우 독성이 높고 부식성이 있습니다. 때로는 무기산의 사용은 제품 수율을 낮추고 피해야 하는 부산물을 생성합니다. 예를 들어,H2SO4를 사용하여 1,3-사이클로헥사디엔을 생산하는 2-사이클로헥센-1-올의 탈수는 중합 부산물1로이어질 것이다. 따라서 많은 산업 공정이 고체 산 촉매를 사용하는 쪽으로 이동합니다. 다양한 수분 내성 고체산은 상기 문제를 해결하고 HZSM-5 및 앰버리스트-15의 사용과 같은 제품 수율을 최대화하기 위해 사용된다. 고실리카 HZSM-5 제올라이트의 사용은 벤젠 2로부터의 사이클로헥산올 생산에서 H2 SO4를 대체하는 것으로 나타났다. 제올라이트는 중성 수성 상에 존재하기 때문에, 제품은 독점적으로 유기상으로 이동하여 분리 공정을 단순화한다. 그러나, 루이스 산-염기 adduct 로 인해 루이스 산 사이트에 물 분자의 형성, 제올리스틱 물질은여전히 비활성 사이트의 존재로 인해 낮은 선택성을 입증 3. 이러한 모든 고체 산 중, Nb2O5 루이스와 BrØnsted 산 사이트를 모두 포함 하는 최고의 후보 중 하나입니다. Nb2O5∙nH2O의 산도는 70% H2 SO4 용액에 해당하며, 이는 비질 양성자의 존재로 인한 것이다. 프로토닉 제올라이트 소재에 필적하는 BrØnsted 산도는 매우 높습니다. 이 산도는 물 제거 후 루이스 산도로 바뀝니다. 물의 존재, Nb2 O 5는 루이스 산도에서 감소 할 수있는 사위 NbO4-H2O adducts를 형성한다. 그러나, 루이스 산 사이트는 NbO 이후 여전히 효과적4 사탄 여전히 효과적인 양전하4. 이러한 현상은 포도당을 5-(하이드록시메틸) 퍼푸랄(HMF)으로 변환하고 물 속에서 테트라랄 주석으로 벤잘데히드의알릴화에 성공적으로 입증되었다 5. 수분 내성 촉매는 특히 물과 같은 환경 양성 용매에서 변환이 수행될 때 재생 에너지 응용 분야에서 바이오매스 변환에 매우 중요합니다.
많은 환경 양성 고산 촉매 중에서도 그래핀을 이용한 기능화된 탄소 나노물질, 탄소나노튜브, 탄소나노섬유, 메소공성 탄소물질은 바이오매스의 용맹화에 중요한 역할을 하고 있다. 조정 가능한 다공성, 매우 높은 비표면적 및우수한 소수성 6,7. 황산 유도체는 특히 안정적이고 활성이 높은 프로토닉 촉매 물질입니다. 그들은 황화 방향족 화합물 8의 불완전한 탄화 또는 불완전하게 탄화 된 설탕 의 황화에 의해 제조 될 수있다9. 그들은 액체H2SO 4의 사용에 필적하는 활성을 가진 매우 효율적인 촉매 (예를 들어, 더높은 지방산의 에스테르화)인 것으로 입증되었습니다. 그래핀 및 CNT는 표면적이 넓고 기계적 특성이 우수하고 내산성이 우수하며, 균일한 기공 크기 분포, 코크스 증착에 대한 내성을 가진 탄소 물질이다. 설포네이트 그래핀은 에틸 아세테이트10 및 이중 기능성 그래핀 촉매의 가수분해를 효율적으로 촉매하는 것으로 밝혀졌으며, 레불린산의 1-포트 변환을 γ-발레롤락톤(11)으로 용이하게 하는 것으로 밝혀졌다. CNT에 지원되는 이중 기능성 금속은 또한 VO 2-PANI/CNT에 걸쳐 HMF의 고도로 선택적 호기성 산화를 2,5-디포르밀푸란으로 변환하는 바이오매스 변환12,13에 적용하기 위한 매우 효율적인 촉매입니다. 촉매14.
Nb2O5 고체산, 기능화된 CNT 및 CNT에 지원되는 이중 기능성 금속의 고유한 특성을 활용하여, 우리는 높은 Nb(Ta) 기반 고체 산 나노시트 변형 Pt/CNTs의 일련의 합성을 위한 프로토콜을 보고합니다. 나노 시트 집계 방법에 의해 표면적. 또한, Pt/20HNbWO 6/CNTs는 HNbWO6나노시트에서 파생된 잘 분산된 Pt 입자와 강한 산성 부위의 시너지 효과의 결과로 최상의 활성 및 변환을 입증했습니다. 리그닌 유래 모델 화합물을 수소화에 의한 연료로 공급합니다.
프로토콜
주의: 본 백서에 설명된 화학물질의 적절한 취급 방법, 특성 및 독성은 관련 물질 안전 데이터 시트(MSDS)를 참조하십시오. 사용되는 화학 물질 중 일부는 독성 및 발암성이며 특별한주의를 기울여야합니다. 나노 물질은 잠재적으로 안전 위험 및 건강 영향을 야기할 수 있습니다. 흡입과 피부 접촉은 피해야 한다. 오토클레이브 반응기로 연기 후드에서 촉매 합성 및 촉매 성능 평가 수행과 같은 안전 예방 조치를 취해야 합니다. 개인 보호 장비는 반드시 착용해야 합니다.
1. CNT의 전처리13
- 100 mL 비커에 50 mL의 질산에 CNT1.0 g을 담급전시.
- 표면 불순물을 제거하고 촉매의 앵커링 효과를 향상시키기 위해 1.5 시간 동안 25 °C에서 용액을 초음파 처리합니다.
- 용액을 100 mL 둥근 바닥 플라스크로 옮김.
- 질산의 혼합물에 있는 해결책을 역류 (65%) 및 황산 (98 %) 60 °C에서 하룻밤 동안. 볼륨 비율을 3:1로 설정합니다. 이렇게 하면 CNT에 표면 결함이 발생합니다.
- 다중 벽 탄소 나노튜브 고체를 얻기 위해 용액을 필터링합니다. 탈이온수로 고체를 씻으시고.
- 고체를 80°C에서 14시간 동안 건조시다.
2. HNbWO6 고체 산 나노 시트의 제조15 프로토 균 교환 에 의해 각질 제거 다음
- 리2CO3(0.9236 g) 및 금속 산화물 Nb2 O5(3.3223 g) 및 WO3(5.7963 g)의 스투치량양을 1:1:2의 어금니 비율로 혼합한다.
- 800°C에서 고체 혼합물을 24시간 동안 1개의 중간 분쇄로 소성하였다.
- 50°C에서 2M HNO3 수성 용액의 200 mL에 LiNbWO6 분말 10.0 g을 놓고 60 h에서 산의 한 번의 교체와 함께 5 일 (120 시간)동안 용액 혼합물을 저어줍니다.
- 매일 산성 액을 교환하고 2.3 단계를 반복하십시오.
- 고체를 걸과 탈이온수로 3배 로 씻어 낸다.
- 고체를 80°C에서 하룻밤 동안 건조시다.
- pH가 9.5 – 10.0에 도달할 때까지 2.6단계에서 얻은 2.0 g의 프로톤화된 화합물로 150 mL의 탈이온화된 물 용액에 25wt.% TBAOH(테트라(n-butylammonium) 수산화액을 추가합니다.
- 위의 용액을 7일 동안 저어줍니다.
- 상기 용액을 원심분리하고 분산된 나노시트를 포함하는 상상용액을 수집한다.
3. HNbMO6 고체 산 나노 시트의 제조
참고: 절차는 첫 번째 및 세 번째 단계를 제외한 2단계의 절차와 유사합니다.
- Li2 CO3 및 금속산화물 Nb2O5 및 MoO3의 축척량양을 1:1:2의 몰 비율로 혼합합니다.
- 1개의 중간 분쇄와 함께 24시간 동안 공기 중800°C에서 상기 고체 혼합물을 소삭.
- LiNbMoO6 분말 10.0 g을 2M HNO3 수성 용액 의 200 mL에 50 °C에서 넣고 60 h에서 산의 한 번의 교체로 5 일 (120 시간)동안 용액 혼합물을 저어줍니다.
4. HTaWO6 고체 산 나노 시트의 제조
참고: 절차는 첫 번째 및 세 번째 단계를 제외한 2단계의 절차와 유사합니다.
- 리2 CO3 및 금속산화물 Ta2O5 및 WO3의 증식량양을 1:1:2의 몰 비율로 혼합합니다.
- 1개의 중간 분쇄와 함께 24시간 동안 공기 중900°C에서 상기 고체 혼합물을 소삭.
- 50°C에서 2M HNO3 수성 용액의 200 mL에 LiTaWO6 분말 10.0 g을 놓고 60 h에서 산의 한 번의 교체로 5 일 (120 시간)동안 용액 혼합물을 저어줍니다.
5. 나노 시트 응집 방법에 의한 HNbWO6/MWCNTs의 제조
- 1단계에서 얻어진 2.0 g의 멀티월 CNT를 250 mL 의 둥근 바닥 플라스크에 HNbWO6 나노시트의 100 mL 용액에 첨가한다.
- 1.0 M HNO3 수성 용액 100 mL을 둥근 바닥 플라스크에 드롭 와이즈로 추가하십시오. 이렇게 하면 나노시트 샘플이 집계됩니다.
- 용액을 50°C에서 6시간 동안 계속 저어줍니다.
- 고체를 걸과 탈이온수로 3배 로 씻어 낸다.
- 고체를 80°C에서 하룻밤 동안 건조시다.
- 건조된 고체를 계량하고 MWCNT에서 고체산의 % 로딩을 기록합니다.
6. 응침 방법에 의한 Pt/20HNbWO 6/CNT의 제조
- H2PtCl6∙H2O를 물에 녹입니다 (1.0 g / 100 mL).
- 제조된 나노시트를 수정된 CNTs 물질을 상기 Pt 수성 용액의 1.34 mL로 함침시킨다.
- 나노 시트 CNTs 물질을 80 °C에서 건조하고 3 시간 동안 400 °C에서 재료를 석회화합니다.
- Nb(Ta) 계 고체 산 나노시트 변형 Pt/CNTs 촉매를 구한다.
7. 리그닌 유래 방향족 에테르의 수산화
참고: 선택된 리그닌 유래 방향족 에테르는 본 실험에서 디페닐 에테르이다. 선택된 리그닌 유래 방향족 에테르는 본 실험에서 디페닐 에테르이다. Pt/20HTaWO 6/CNTs(이 백서에 나와 있지 않은 88.8%의 변환)의 활성은 Pt/20HNbWO6/CNTs(99.6%)보다낮기 때문에 사이클로헥산의 수율은 감소한다. 따라서, 비록, 시클로헥산의 높은 선택성은 Pt/20HTaWO6/CNTs를 통해 얻어졌지만, 디페닐 에테르의 낮은 변환은 그 이용을 제한한다. 발암 성 시약을 사용하여 반응을 수행하기 위해 적절한 보호 장비 및 연기 후드를 사용한다.
- 석영 모래 5 밀리리터에 0.05 그램의 촉매를 희석하십시오. 석영 울의 두 베개 사이에 고정 침대 반응기의 중간에 용액을로드합니다.
- 2 시간 동안 300 °C에서 H2 (40 mL / min)에서 촉매를 줄입니다.
- 디페닐 에테르 공급 원료(n-decane의 5.0 wt.% 반응물 및 가스 크로마토그래피 분석을 위한 내부 표준으로 2.0 wt.% n-dodecane 포함)를 다른 유량(0.05-0.06 mL/min)의 고정 베드 반응기로 펌핑합니다.
- 촉매 W(g)의 질량과 기판 F(g/min)의 유량 사이의 비율로 정의된 상이한 공간 시간에서 제품을 수집합니다.
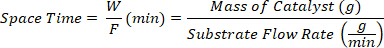
- 5977A MSD로 GC(HP-5, 30m x 0.32mm x 0.25 μm)로 액체 제품을 식별하고 가스 크로마토그래피(GC 450, FID, FFAP 모세관 열 30m x 0.32mm x 0.25μm)로 오프라인을 분석합니다.
- 반응물 의 변환을 결정(conv.%), 제품 I (Si %), 및 제품 i (Y i %)의 수율을 향한 선택성 다음 방정식을 사용하여 다음 을 사용하십시오.
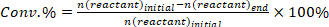 (1)
(1)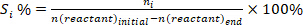 (2)
(2)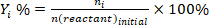 (3)
(3)
결과
X선 회절 패턴(XRD)은 LiNbWO6 및 상응하는 양성자 교환 촉매 샘플 HNbWO6에 대해 연구되어 위상을 결정하였다(도1 및 도2). NH3-온도 프로그래밍 탈착(NH3-TPD)을사용하여 촉매 샘플의 표면 산도를 조사하였다(그림3). X선 미세분석 및 투과 전자현미경(TEM)을 이은 주사전자현미경(SEM)을 기록하...
토론
질산을 가진 CNT의 전처리는 비표면적 (S BET)를 현저하게 증가시다. 원시 CNT는 처리 후 103m2/g의 비표면적을 가지며, 표면적은 134 m2/g로 증가하였다. 따라서, 이러한 전처리는 CNT 표면에 결함을 생성하여 고체산 변형 및 백금 입자 함침 후 촉매의 비표면적에 긍정적인 영향을 미칠 것이다. 나노 시트의 혼입 후 표면적이 감소하기 때문에,이 단계는 최종 촉매의 표면적을 최대?...
공개
우리는 공개 할 것이 없습니다.
감사의 말
이 논문에 설명된 이 작품은 중국 홍콩 특별행정구 연구보조금위원회(UGC/FDS25/E09/17)의 보조금으로 전액 지원되었습니다. 또한 촉매 특성화 및 촉매 성능 평가를 위한 고정 침대 반응기를 위한 분석 장비를 제공한 중국 국립 자연과학 재단(21373038 및 21403026)을 감사하게 생각합니다. Hongxu Qi 박사는 홍콩 연구 보조금 위원회 (UGC / FDS25 / E09 /17)에서 부여 한 연구 조교에 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| Carbon nanotubes (multi-walled) | Sigma Aldrich | 724769 | |
| Nitric acid (65%) | Sigma Aldrich | V000191 | |
| sulphuric acid (98%) | MERCK | 100748 | |
| Lithium carbonate (>99%) | Aladdin | L196236 | |
| Niobium pentaoxide (99.95%) | Aladdin | N108413 | |
| Tungsten trioxide (99.8%) | Aladdin | T103857 | |
| Molybdenum trioxide (99.5%) | Aladdin | M104355 | |
| Tantalum oxide (99.5%) | Aladdin | T104746 | |
| Chloroplatinic acid hexahydrate, ≥37.50% Pt basis | Sigma Aldrich | 206083 | |
| tetra (n-butylammonium) hydroxide 30-hydrate | Aladdin | D117227 | |
| Diphenyl ether, 98% | Aladdin | D110644 | |
| 2-Bromoacetophenone,98% | Aladdin | B103328 | |
| Diethyl ether,99.5% | Sinopharm | 10009318 | |
| n-Decane,98% | Aladdin | D105231 | |
| n-Dodecane,99% | Aladdin | D119697 | |
| Autoclave Reactor | CJF-0.05—0.1L (Dalian Tongda Equipment Technology Development Co., Ltd) | ||
| Tube furnace | SK2-1-10/12 (Luoyang Huaxulier Electric Stove Co., Ltd) |
참고문헌
- Jensen, J. L., Uaprasert, V., Fujii, C. R. Acid-Catalyzed Hydration of Dienes. 2. Changes in Activity Coefficient Ratios, Enthalpy, and Entropy as a Function of Sulfuric Acid Concentration. Journal of Organic Chemistry. 41 (10), 1675-1680 (1976).
- Ishida, H., Ono, M., Kaji, S., Watanabe, A. Synthesis of 1,3-Cyclohexadiene through Liquid Phase Dehydration of 2-Cyclohexen-1-ol in Aqueous Solution using Zeolite Catalyst. Nippon Kagaku Kaishi. 4, 267-275 (1997).
- Ishida, H. Liquid-phase hydration process of cyclohexene with zeolites. Catalysis Surveys from Japan. , 241-246 (1997).
- Ushikubo, T., Iizuka, T., Hattori, H., Tanabe, K. Preparation of highly acidic hydrated niobium oxide. Catalysis Today. 16, 291-295 (1993).
- Nakajima, K., et al. Nb2O5.nH2O as a heterogeneous catalyst with water-tolerant Lewis acid sites. Journal of the American Chemical Society. 133 (12), 4224-4227 (2011).
- Lam, E., Luong, J. H. T. Carbon Materials as Catalyst Supports and Catalysts in the Transformation of Biomass to Fuels and Chemicals. ACS Catalysis. 4 (10), 3393-3410 (2014).
- Sudarsanam, P., et al. Functionalised heterogeneous catalysts for sustainable biomass valorisation. Chemical Soceity Review. 47 (22), 8349-8402 (2018).
- Hara, M., et al. A carbon material as a strong protonic acid. Angewandte Chemie International Edition English. 43 (22), 2955-2958 (2004).
- Toda, M., et al. Biodiesel made with sugar catalyst. Nature. 438 (7065), (2005).
- Ji, J., et al. Sulfonated graphene as water-tolerant solid acid catalyst. Chemical Science. 2 (3), 484-487 (2011).
- Wang, Y., et al. Graphene-Based Metal/Acid Bifunctional Catalyst for the Conversion of Levulinic Acid to γ-Valerolactone. ACS Sustainable Chemistry & Engineering. 5 (2), 1538-1548 (2016).
- Ma, Q., et al. Catalytic depolymerization of lignin for liquefied fuel at mild condition by rare earth metals loading on CNT. Fuel Processing Technology. , 220-225 (2017).
- Rahzani, B., Saidi, M., Rahimpour, H. R., Gates, B. C., Rahimpour, M. R. Experimental investigation of upgrading of lignin-derived bio-oil component anisole catalyzed by carbon nanotube-supported molybdenum. RSC Advances. 7 (17), 10545-10556 (2017).
- Guo, Y., Chen, J. Bicomponent Assembly of VO2and Polyaniline-Functionalized Carbon Nanotubes for the Selective Oxidation of Biomass-Based 5-Hydroxymethylfurfural to 2,5-Diformylfuran. ChemPlusChem. 80 (12), 1760-1768 (2015).
- He, J., et al. Characterization of HNbMoO6, HNbWO6 and HTiNbO5 as solid acids and their catalytic properties for esterification reaction. Applied Catalysis A: General. , 145-152 (2012).
- Tagusagawa, C., Takagaki, A., Hayashi, S., Domen, K. Characterization of HNbWO6 and HTaWO6 Metal Oxide Nanosheet Aggregates As Solid Acid Catalysts. Journal of Physical Chemistry C. 113, 7831-7837 (2009).
- Niwa, M., Katada, N., Sawa, M., Murakami, Y. Temperature-Programmed Desorption of Ammonia with Readsorption Based on the Derived Theoretical Equation. Journal of Physical Chemistry. 99, 8812-8816 (1995).
- Leiva, K., et al. Conversion of guaiacol over supported ReOx catalysts: Support and metal loading effect. Catalysis Today. , 228-238 (2017).
- Deng, W., Liu, M., Tan, X., Zhang, Q., Wang, Y. Conversion of cellobiose into sorbitol in neutral water medium over carbon nanotube-supported ruthenium catalysts. Journal of Catalysis. 271 (1), 22-32 (2010).
- Huang, B., Huang, R., Jin, D., Ye, D. Low temperature SCR of NO with NH3 over carbon nanotubes supported vanadium oxides. Catalysis Today. 126 (3-4), 279-283 (2007).
- Takagaki, A., Tagusagawa, C., Hayashi, S., Hara, M., Domen, K. Nanosheets as highly active solid acid catalysts for green chemical syntheses. Energy & Environmental Science. 3 (1), 82-93 (2010).
- Hu, L. -. F., et al. Structure and photocatalytic performance of layered HNbWO6nanosheet aggregation. Journal of Nanophotonics. 9 (1), (2015).
- Geim, A. K. Graphene: Status and Prospects. Science. 324, 1530-1534 (2009).
- Golberg, D., et al. Boron Nitride Nanotubes and Nanosheets. ACS Nano. 4 (6), 2979-2993 (2010).
- Wilson, J. A., Yoffe, A. D. The transition metal dichalcogenides discussion and interpretation of the observed optical, electrical and structural properties. Advances in Physics. 18 (73), 193-335 (1969).
- Ma, R., Sasaki, T. Nanosheets of oxides and hydroxides: Ultimate 2D charge-bearing functional crystallites. Advanced Materials. 22 (45), 5082-5104 (2010).
- Pope, T. R., Lassig, M. N., Neher, G., Weimar Iii, R. D., Salguero, T. T. Chromism of Bi2WO6 in single crystal and nanosheet forms. Journal of Materials Chemistry C. 2 (17), 3223-3230 (2014).
- Yu, Y., et al. Controlled scalable synthesis of uniform, high-quality monolayer and few-layer MoS2 films. Scientific Reports. 3, 1866 (2013).
- Prasomsri, T., Shetty, M., Murugappan, K., Román-Leshkov, Y. Insights into the catalytic activity and surface modification of MoO3 during the hydrodeoxygenation of lignin-derived model compounds into aromatic hydrocarbons under low hydrogen pressures. Energy & Environmental Science. 7 (8), 2660-2669 (2014).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유