Method Article
중환자실에서 전기 임피던스 단층 촬영을 통한 폐 기능 모니터링
* 이 저자들은 동등하게 기여했습니다
요약
전기 임피던스 단층 촬영은 비침습적이고 방사선이 없는 실시간 폐 환기 모니터링 도구입니다. 흉부의 임피던스 변화를 측정하여 호흡별로 공기의 분포를 시각화할 수 있습니다. 처음에는 인공호흡 모니터링을 위해 고안된 전기 임피던스 단층 촬영은 식염수 정맥 주사를 통해 관류를 측정할 수도 있습니다.
초록
전기 임피던스 단층 촬영(EIT)은 지속적인 실시간 인공호흡 모니터링을 위한 획기적이고 비침습적이며 방사선이 없는 이미징 기술입니다. 또한 폐 관류 모니터링에도 적용됩니다. EIT는 흉부의 임피던스 변화를 측정하고 처리하여 폐 전체의 환기 및 관류 패턴을 정량화합니다. 임상의가 폐 기능의 호흡별 호흡 변화를 시각화할 수 있는 강력한 도구입니다.
EIT의 혁신적인 응용 분야는 숨을 참는 동안 고긴장 용액 주입의 운동 분석을 사용하여 폐 관류를 평가하는 능력입니다. 이 용액은 폐 혈관을 순환할 때 흉부에 임피던스 변화를 일으킵니다. 이 간접 방법을 사용하면 관류 패턴을 추정할 수 있어 병상에서의 폐 혈류 역학을 이해하는 데 크게 기여합니다.
EIT는 모니터링을 위한 도구일 뿐만 아니라 기흉 및 기관지 삽관과 같은 호흡기 병리의 진단에도 중요할 수 있습니다. 침습적 기계 환기를 받는 환자에서 다른 진단 도구로는 불가능한 환기/관류(V/Q) 불일치의 원인을 식별하는 데 도움이 될 수 있습니다. 또한 EIT는 PEEP(Positive End-Expiratory Pressure) 적정 및 일회 호흡량과 같은 인공호흡기 설정의 개별 최적화를 지원하여 중환자 치료에서 산소 공급과 폐 건강을 개선할 수 있습니다.
요약하자면, EIT는 병상 옆 폐 모니터링 및 진단의 패러다임 변화를 나타냅니다. EIT는 비침습적 특성과 데이터의 즉각성으로 인해 현대 호흡기 의학에서 없어서는 안 될 도구입니다. 응용 분야가 증가함에 따라 EIT는 특히 집중 치료 환경에서 호흡기 치료에 대한 이해와 접근 방식을 발전시키는 데 중추적인 역할을 할 것입니다.
서문
전기 임피던스 단층 촬영(EIT)은 시간 경과에 따른 임피던스의 변화를 지형 이미지로 변환하는 폐 모니터링 기술입니다. 이는 몸통을 가로질러 원주방향으로 위치한 전극에서 낮은 전기 교류(5-10mA)를 주입하여 달성됩니다(그림 1A). 임피던스는 이 전류의 흐름에 대한 조직의 반대를 반영합니다. 영감 중에는 임피던스가 증가하는 반면 만료 중에는 감소합니다. 임피던스의 유사한 변화는 정맥 주사액이 있을 때 발생합니다. 예를 들어, 혈액에 비해 전기 전도도가 높은 유체가 중앙 카테터를 통해 주입되면 전기 임피던스 1,2,3,4가 감소합니다.
실용성을 위해 EIT의 전극(16개 또는 32개)을 벨트에 배치한 다음 환자의 흉부 주위, 특히 4번째와 5 번째늑간 공간 사이에 위치합니다. 이 배치는 폐를 최적으로 볼 수 있도록 하고 횡격막 간섭을 줄입니다. 측정 과정에서 두 개의 서로 다른 전극은 사전 설정된 전류를 순차적으로 주입하고 나머지 전극은 해당 전압 판독값을 위한 수신기 역할을 합니다. 이 과정은 모든 전극 쌍에 대해 빠르게 반복되어 20-50Hz의 주파수로 흉부 주위를 회전합니다. 이러한 빠른 회전으로 인해 EIT는 시간 해상도가 높습니다. 흉부 EIT 장치는 각 측정 주기에서 흉부 단면의 전기 임피던스 분포를 계산하고 이 값을 2차원 이미지로 변환합니다. 이 이미지는 전용 모니터에 실시간으로 표시됩니다.
EIT에는 몇 가지 임상 응용 분야가 있습니다. 임피던스 기술을 기반으로 흉부 내부의 공기 분포와 관류 분포를 모니터링할 수 있으며, 특히 폐 임피던스의 변화를 일으키기 위해 조영제를 투여할 때 가능합니다. 기계 환기 환자를 위한 PEEP 설정을 결정하는 것은 폐 손상을 최소화하기 위해 까다롭고도 필수적입니다. 또한 시간 경과에 따른 환기 및 관류 변화를 추적할 수 있는 기능은 종단 환자 모니터링에 매우 귀중한 데이터를 제공합니다. 이러한 측면은 환자 상태가 급속히 발전할 수 있는 역동적인 임상 환경에서 매우 중요하다5.
EIT는 유량 센서를 통해 얻은 전체 역학 또는 EIT 장치가 인공호흡기와 연결된 경우 인공호흡기의 데이터를 쉽게 시각화할 수 있을 뿐만 아니라 과팽창 및 국소 붕괴에 대한 중요한 정보를 제공합니다 6,7,8,9. 생성된 이미지는 폐에 대한 기능적 정보를 제공하지만 해부학적 진단을 위한 것이 아니며 방사선을 방출하지 않습니다. 미국에서 EIT 장치 ENLIGHT 2100은 현재 미국 식품의약국(FDA)에서 승인한 유일한 장치입니다. 다른 회사들은 현재 성인, 어린이 및 신생아 인구에 대한 EIT 사용에 대한 FDA 승인을 획득하는 과정에 있습니다. 이 논문에서는 ENLIGHT 2100 장치의 하드웨어(예: 벨트 및 스크린), 환기 및 관류 맵을 사용했습니다.
EIT 세트 설정에는 모니터 자체 외에도 전극 벨트, 유량 센서 및 기준 케이블인 세 가지 필수 장비가 포함됩니다. 전극 벨트 는 단층 촬영 2차원 이미지를 얻는 데 사용됩니다. EIT 폐 이미지는 흉부 둘레 크기와 제조업체의 사양에 따라 32 x 32, 24 x 24 또는 16 x 16 픽셀과 같은 다양한 해상도의 2차원 표현으로 구성됩니다. 이미지는 재구성 알고리즘을 사용하여 전압 측정에서 생성됩니다. 유량 센서 는 단일 환자용으로 설계되었으며 성인 및 소아 환자용과 신생아용의 두 가지 크기로 제공됩니다. 성인-소아 유량 센서는 40mL 미만의 일회 호흡량을 측정할 수 없는 반면, 신생아 센서는 0에서 100mL까지의 일회 호흡량을 기록할 수 있습니다. 유량 센서가 없으면 EIT는 임피던스 데이터만 표시합니다. 유량 센서가 환자에게 연결되면 임피던스 파형의 데이터를 압력, 유량 및 부피 매개변수와 동기화할 수 있습니다. 기준 케이블 은 재사용이 가능하며 전류 주입 값에 대한 기준점 역할을 합니다.
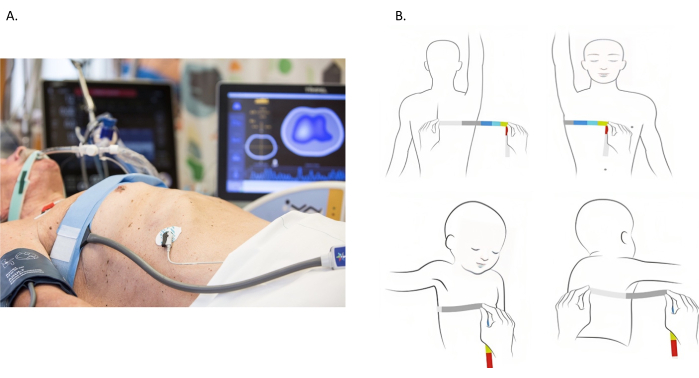
그림 1: 전기 임피던스 단층 촬영 전극 벨트의 배치. (A) 전기 임피던스 단층 촬영 전극 벨트는늑간 공간 4및 5 번째에서 가슴 주위에 배치됩니다. (B) 흉부 측정. 흉부는 흉부 전체에 측정 테이프를 감아 측정합니다. 그러나 대부분의 환자는 침대에 누워 있으며 흉부 전체를 측정하는 것은 불가능합니다. 다른 접근 방식이 이미지에 설명되어 있습니다. 흉부 둘레는 가시돌기에서 흉골까지 평가됩니다. 그런 다음 가슴의 반대쪽 부분을 설명하기 위해 측정을 두 배로 늘립니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
이 비디오 백서의 주요 초점은 독자에게 EIT 이미지를 기록하고 해석하는 데 능숙해지는 데 필요한 지식과 기술을 제공하는 것입니다. 이 목표를 추구하기 위해 EIT 원칙에 대한 개요를 제공하고, 폐의 공기 분포를 위한 실시간 시각화 기능을 선보이며, 관류 평가의 확장된 응용 분야를 살펴봅니다. 이러한 목표를 달성함으로써 우리는 청중이 폐 평가를 위해 EIT 기술을 자신 있게 활용할 수 있도록 하는 것을 목표로 합니다.
프로토콜
이 논문에 제공된 이미지는 익명으로 처리되었으며 ClinicalTrials.gov 에서 NCT04497454라는 번호로 등록되고 지역 윤리 위원회(브라질 상파울루 인코르 대학교/HC-FMUSP 4001231)의 승인을 받은 진행 중인 프로토콜의 일부였습니다.
1. EIT 장치 사용을 시작하는 방법
- EIT 벨트 및 배치
- 정확한 벨트 사이즈 선택을 위해 흉벽을 측정합니다.
- 측정 테이프를 사용하여 4번째 와 5번째 늑간 공간 사이의 흉부 둘레를 측정합니다(그림 1B). 가슴이 큰 환자의 경우 벨트를 더 높은 늑간 공간으로 이동하십시오.
- 전도성 젤이 있는 일회용 재료로 전극 벨트를 덮습니다.
알림: 이렇게 하면 머리카락이 많은 환자에서도 환자의 피부에 밀착되어 임피던스 신호를 쉽게 캡처할 수 있습니다. - 환자 흉벽의 4번째 및 5 번째늑간 공간 (측정된 둘레와 동일)에 벨트를 배치하고 벨트를 배치할 때 전극이 겹치지 않도록 합니다.
- 이미지 재구성 알고리즘이 벨트 크기에 비례하는 전방 간격을 허용하기 때문에 뒤쪽에 틈이 없이 연속성을 유지합니다.
- 벨트를 착용하는 동안 환자를 돌려 등에 접근하십시오. 기도, 모든 유입 정맥 또는 동맥 라인 및 배액관을 고정하고 의료 전문가가 제공하는 특정 지침을 따르십시오.
- 유량 센서를 Y-피스에 가까운 환기 회로에 연결하고 센서와 함께 위쪽으로 배치하여 유체 축적 및 신호 간섭을 방지합니다(그림 2A).
- 기준 전극을 심전도(ECG) 전극에 연결합니다.
참고: 기준 케이블 없이는 환자를 모니터링할 수 없습니다(그림 2B).- 성인 및 소아 환자의 경우 전극을 복부나 어깨에 위치시킵니다.
- 신생아 환자의 경우 전극을 다리에 위치시킵니다.
- EIT를 켜고 환자 인구 통계 데이터를 입력합니다(그림 3).
- 모니터링을 시작하고 환자의 움직임을 피하십시오. 모니터링을 시작한 후 참조 이미지가 생성되고 환기 스크린이 표시됩니다(그림 4). 두 개의 이미지, 즉 동적 이미지 와 환기 맵이 생성됩니다.
알림: 녹음하는 동안 벨트를 방해하는 환자의 움직임을 피하는 것이 중요합니다. - EIT 장치의 PEEP 적정 도구에 대한 단계별 안내
- 메인 화면 아이콘에서 PEEP 적정 도구를 선택합니다.
- Tool Options 아이콘을 클릭하여 Tool Options에 액세스합니다.
- Time Intervals(시간 간격)를 설정하여 각 조건에서 환기를 안정화하기 위해 적정 중 PEEP 변경에 대한 시간 간격을 조정합니다.
알림: 시간 간격은 환자의 상태(예: 혈역학적 불안정성)와 장치의 지시에 따라 다릅니다. - 자동 PEEP 변경 감지에 대한 임계값 을 조정합니다.
- PEEP 적정 화면에서 시작을 눌러 적정을 시작하여 PEEP 변경에 대해 조정된 시간을 기준으로 카운트다운을 시작합니다.
- 메시지가 표시되면 프로토콜에 따라 인공호흡기의 PEEP 값을 조정합니다. 장치는 자동으로 이 변경 사항을 감지하고 새 카운트다운을 시작합니다.
- PEEP 변경 사항 모니터링 - 각 PEEP 변경에 따라 화면이 업데이트됩니다. 자동 검색에 실패하면 수동으로 중지하고 절차에 주석을 추가합니다. 선택적으로, 주석을 제공하거나 적정의 이름을 지정합니다. 그러면 PEEP 적정 그래프가 표시됩니다.
- EIT 장치의 Perfusion 도구 에 대한 단계별 지침
- 환자 준비
- 충분한 진정제를 투여하고 필요한 경우 신경근 봉쇄를 보장하며, 호흡 노력이 절차를 방해할 수 있습니다.
알림: 환자는 기계적 환기 모니터링에도 불구하고 감지할 수 없는 호흡 노력을 보일 수 있습니다.
- 충분한 진정제를 투여하고 필요한 경우 신경근 봉쇄를 보장하며, 호흡 노력이 절차를 방해할 수 있습니다.
- 절차를 시작합니다. EIT 소프트웨어 내에서 시작 아이콘을 클릭하여 절차를 시작합니다.
- 환기 주기 인식
- 소프트웨어가 몇 가지 환기 주기를 인식하여 기준 데이터를 설정할 수 있도록 합니다.
- 무호흡증과 주사
- 0cmH2O의 압력 지원이 있는 CPAP(Continuous Positive Airway Pressure) 또는 PSV(Pressure Support Ventilation) 모드로 전환합니다. 이 상태를 20초 이상 유지합니다. 이 기간 동안 7.5% 고긴장성 식염수 또는 8.4% 중탄산염 10mL를 내부 경정맥 또는 쇄골하 정맥의 중심 정맥 접근 카테터를 통해 빠르고 일관되게 주입합니다.
- 환기를 복원하십시오. 주입이 완료되면 일반 환기 설정으로 돌아갑니다.
- 이미지 재구성
- EIT 알고리즘이 심장과 폐를 통해 흐르는 콘트라스트의 1차 통과 역학을 기반으로 관류 이미지를 재구성하도록 합니다.
- 환자 준비
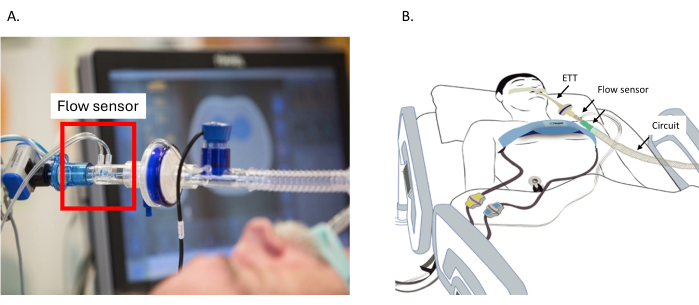
그림 2: 유량 센서의 배치. (A) 회로와 ETT 사이의 유량 센서 배치. (B) 흉부 주위의 벨트는 EIT 장치에 연결됩니다. 유량 센서는 ETT와 회로 사이에 연결됩니다. 배의 전극에 연결된 기준 케이블. 약어: ETT = 기관내관. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
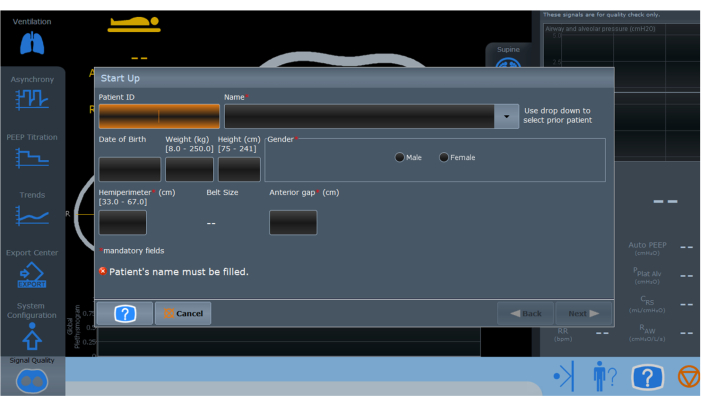
그림 3: 전기 임피던스 단층 촬영 모니터링 장치의 초기화 화면. 빨간색 별표로 표시된 필드는 적절한 설정 및 작동을 위해 완료해야 하는 필수 정보를 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
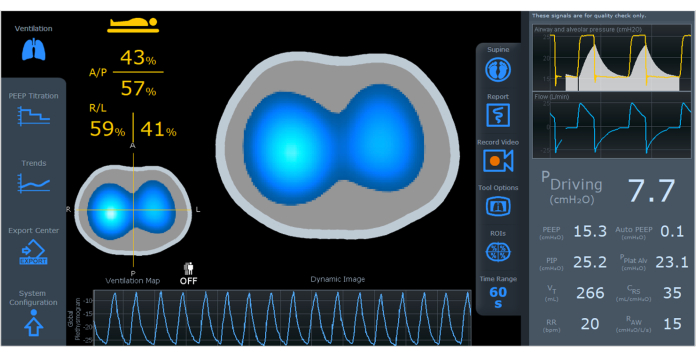
그림 4: 동적 이미지, 환기 맵 및 혈량계를 표시하는 EIT 화면. 화면 왼쪽에는 지역별로 나뉜 환기 분포((A/P, R/L)가 있습니다. 화면 오른쪽에는 구동 압력, PEEP, 자동 PEEP, PIP, PPlat Alv, VT, CRS, RR 및 RAW를 포함한 환기 매개변수가 있습니다. 약어: EIT = 전기 임피던스 단층 촬영; A/P=전방/후방, R/L=오른쪽/왼쪽; PEEP = 양말호기압; PIP = 최대 흡기 압력; PPlat Alv = 폐포 고원 압력; VT = 일회 호흡량; CRS = 호흡기 시스템 순응도; RR = 호흡수; RAW = 기도 저항. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
결과
환기 모니터링
동적 이미지(그림 4)는 지역적 변화를 나타내기 위해 진한 파란색(환기가 가장 적음)에서 흰색(가장 환기가 많음)에 이르는 색상을 사용하여 환기 중 공기 분포의 실시간 변화를 표시합니다. 회색 영역은 환기에 변화가 없음을 나타냅니다. 동적 이미지를 통해 폐내 시간 상수의 차이와 역설적 패턴의 존재를 빠르게 식별할 수 있습니다. 호흡 주기 동안 공기 변화가 제한된 영역은 과도한 팽창 또는 붕괴된 영역으로 인해 발생할 수 있다는 점에 유의하는 것이 중요합니다.
"환기 맵"(그림 4)은 호흡 주기 동안 정의된 단면에 걸쳐 공기량이 어떻게 분포되는지 보여줍니다. 밝은 파란색은 일회 호흡량의 대부분을 받는 폐 영역을 나타내며, 이는 흡기와 호기 사이의 임피던스 신호 변화에 비례합니다. 반대로, 진한 파란색은 볼륨 변화가 적은 영역을 나타냅니다. 환기 지도를 통해 폐 내 국소 환기 분포를 평가할 수 있습니다. 폐는 전방/후방, 우/좌측으로 나뉘어 있어 상세한 평가가 가능하며 화면의 특정 부위에 대한 혈량계를 표시할 수 있다4.
혈류도 흉부 임피던스 변동 곡선(그림 4)은 일회 호흡량에 해당하는 파동 진폭을 나타내며, 기준선은 폐 폭기 또는 FRC(Functional Residual Capacity) 또는 EELV(End-Expiratory Lung Volume)와 동일합니다. 폭기 정보는 총 흉곽 내 공기량의 상대적 변화를 추정할 수 있습니다.
화면 오른쪽의 기도 매개변수(그림 4)는 유량 센서에 의해 캡처되어 파형 그래프와 숫자로 표시됩니다. 구동 압력, 자동 PEEP, 폐포 고원 압력, 규정 준수 및 저항(오른쪽 숫자 열에 있음)과 같은 매개변수는 제어된 사이클 동안 계산됩니다. PEEP, 최대 압력, 일회 호흡량 및 호흡수 매개변수가 모든 주기에 표시됩니다. 근접 유량 센서를 사용하면 기계식 인공호흡기 브랜드 또는 모델에 관계없이 인공호흡기 및 임피던스 데이터를 동일한 화면에 통합할 수 있습니다.
PEEP 적정 도구(그림 5)
환자는 PEEP 적정에 영향을 줄 수 있는 자발적인 호흡 노력과 움직임을 피하고 인공호흡기와 동기화되어야 합니다. 이것은 적절한 진정제와 필요한 경우 마비제로 도달할 수 있습니다. 유량 센서와 인공호흡기 튜브는 정확한 모니터링을 유지하기 위해 액체 및 분비물과 같은 장애물이 없어야 합니다.
EIT는 지역 환기의 변화를 감지하고 유량계와 통합되면 기도 압력, 일회 호흡량 및 유량을 포함한 지역 호흡 역학을 추정할 수 있습니다. 지역별 규정 준수 변경 사항을 계산하여 다양한 PEEP 수준에서 축소된 영역과 과도하게 팽창된 영역의 백분율로 결과를 표시합니다. 일부 저자들은 PEEP를 과팽창 비율(그림 5의 흰색 곡선, 그림 6의 흰색 영역)과 붕괴 비율(그림 5의 파란색 곡선, 그림 6의 파란색 영역) 사이의 교차점으로 적정할 것을 제안했습니다. 이 PEEP 수준에서는 과도하게 팽창된 영역과 축소된 영역(그림 5의 주황색 곡선)과 폐 기능의 발생이 최소화됩니다. 현재 진행 중인 연구는 고혈압과 허탈의 교차점에서 설정된 PEEP가 임상적으로 유리한지 여부를 조사하고 있습니다.
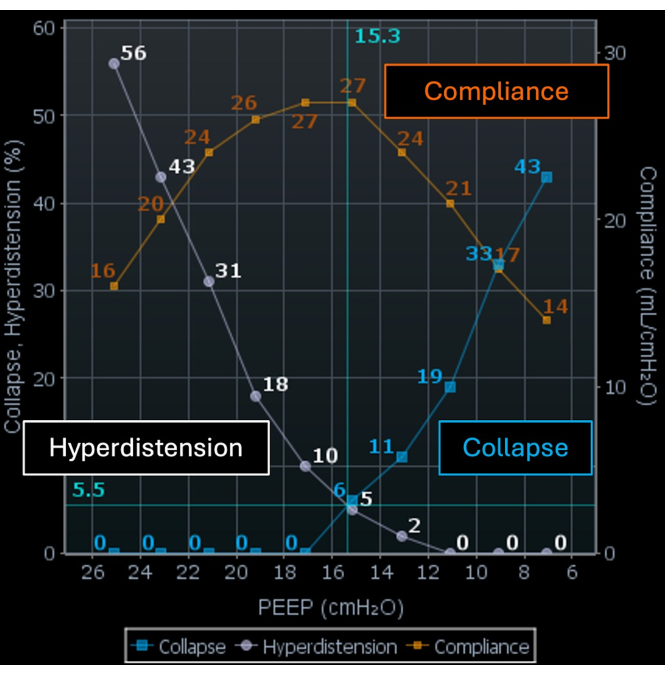
그림 5: EIT 화면의 PEEP 적정 도구. 주황색 곡선은 순응도를 나타내고, 흰색 곡선은 과팽창을 나타내고, 파란색 곡선은 붕괴를 나타냅니다. 약어: EIT = 전기 임피던스 단층 촬영; PEEP = 호기압의 양압. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
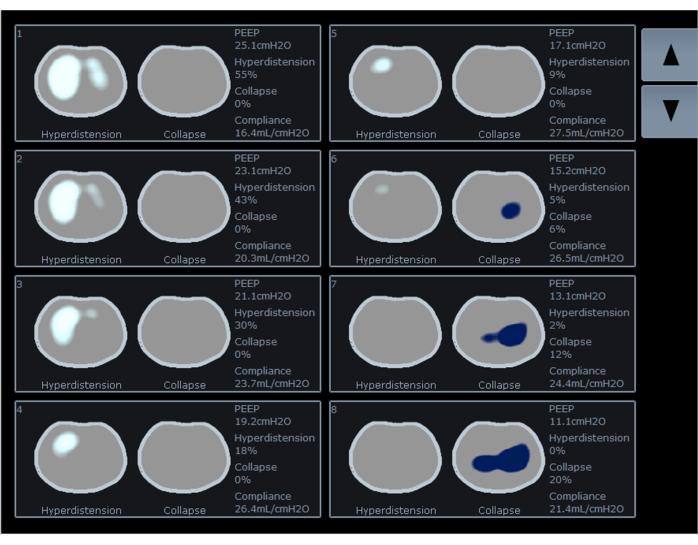
그림 6: 과팽창(흰색) 및 붕괴(파란색)의 백분율 표시와 EIT 화면에 다양한 PEEP 값에 대한 준수 . 약어: EIT = 전기 임피던스 단층 촬영; PEEP = 호기압의 양압. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
EIT를 통한 폐 관류 평가: 의료 제공자를 위한 가이드
전기 임피던스 단층 촬영(EIT)은 최근 전기 전도도의 변화를 측정하여 폐 환기를 위한 유용한 모니터링 도구로 인식되고 있습니다. EIT는 주로 폐 내 공기 분포를 평가하는 데 중점을 두지만 혁신적인 기술을 통해 폐 관류에 대한 귀중한 통찰력을 제공할 수도 있습니다.
흉부에서 혈액의 이동으로 인한 임피력의 변화는 환기와 관련된 것보다 훨씬 작은 진폭을 갖습니다. 따라서 EIT는 전통적으로 관류를 측정하는 데 사용되지 않았습니다. 그러나 고긴장성 식염수 정맥 주사와 호흡 참기 동작과 함께 포함하는 특정 방법은 혈류와 관련된 임피던스 변화를 분리하고 증폭할 수 있습니다. 이 용액이 혈관을 통과하면서 EIT가 감지할 수 있는 혈액의 전기적 특성을 변경합니다. EIT는 이 용액이 폐 혈관을 순환할 때 발생하는 임피던스 변화를 관찰하여 관류 패턴을 간접적으로 추론할 수 있습니다. 이 접근법을 통해 폐 내 환기와 관류에 대해 동시에 더 깊이 이해할 수 있습니다10. 이 도구는 미국 및/또는 현지 병원의 규정 및/또는 기타 국가의 법률 기관 규제 기관의 승인에 따라 연구 목적으로만 사용됩니다.
폐 관류 시각화
고긴장성 식염수 또는 중탄산나트륨과 같은 전기 전도성이 높은 용액의 정맥 주사는 폐혈관 내의 혈류를 시각화하는 데 도움이 됩니다(11,12,13). 더 높은 관류를 가진 영역은 덜 관류된 영역에 비해 다른 임피던스 패턴을 나타냅니다. 이러한 혁신적인 EIT의 적용은 환기 영상과 함께 관류에 대한 상대적 평가를 가능하게 하여 폐 기능에 대한 포괄적인 관점을 제공하여 일반적으로 폐 관류를 조절하는 요법으로 치료되는 관류 결함으로 인한 저산소혈증과 종종 환기 전략 또는 위치 변경으로 해결되는 환기 장애로 인한 저산소혈증을 구별하는 데 도움이 됩니다. 이 응용 프로그램은 또한 확립된 치료법(예: 흡입 산화질소, 항응고제 및 혈전 용해제)에 대한 반응으로 국소 폐 관류의 변화를 모니터링할 수 있습니다.
관류 도구
EIT의 관류 도구는 제어된 기계적 환기 중 폐혈류를 시각화하도록 특별히 설계되었습니다. 그것은 짧은 무호흡 기간 동안 고긴장성 식염수를 정맥에 주입하는 것을 포함합니다. 결과 이미지는 흉부 단면에서 노란색(높은 관류를 나타냄)에서 진한 빨간색(낮은 관류를 나타냄)에 이르는 색상으로 폐 관류의 분포를 표시합니다( 그림 7 참조).
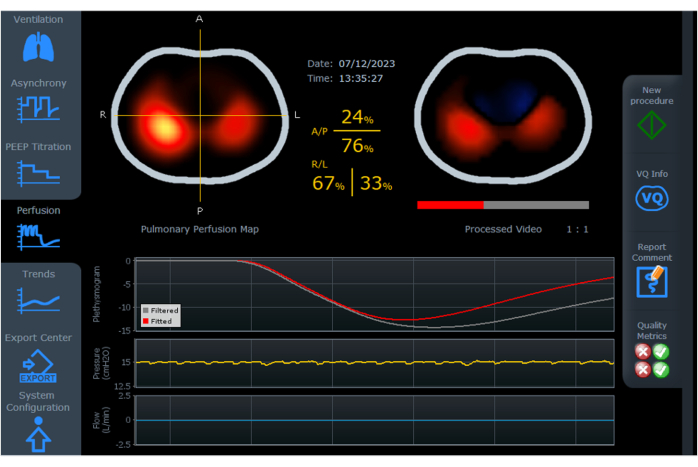
그림 7: 흉부의 다른 부위에 대한 관류 분포 비율의 변화. 가슴의 단면에서 노란색(높은 관류)에서 짙은 빨간색(낮은 관류)까지 다양한 색상으로 전방, 후방, 오른쪽 및 왼쪽에 대한 관류의 변화가 표시됩니다. 또한 처리된 비디오를 온라인으로 실행하여 심장을 통해 흐르는 대비를 파란색으로 표시한 다음 폐를 빨간색으로 표시하는 것도 가능합니다. 약어: A = anterior; P = 후방; R = 오른쪽; L = 왼쪽. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
온라인 및 오프라인 분석
EIT는 혈량검사와 폐 전체의 공기 분포를 지속적으로 측정합니다. 임피던스 변화는 일회 호흡량 변화를 반영하여 폐의 국소적 평가를 가능하게 합니다. 혈류측정은 흡기와 호기 중 폐 용적 변화를 그래픽으로 나타냅니다(그림 8). 공기의 변화는 폐의 다른 부분에서 측정할 수 있습니다. 이것은 EIT에서 가장 유리한 측정 방법 중 하나이며, 지역 환기를 평가합니다.
EIT 장치는 32 x 32 매트릭스를 생성하여 전체 폐 영역을 매핑합니다. 이 매트릭스는 폐 전체를 덮는 격자로 전달됩니다. 픽셀이라고 하는 그리드 내의 각 작은 사각형에는 저항률 또는 임피던스 값이 할당됩니다. 임피던스 값의 변화는 폐의 특정 부분에서 폐 용적의 변화에 해당합니다.
EIT는 전용 소프트웨어를 사용하여 이러한 임피던스 값의 변화를 취하고 이미지를 생성합니다. 이 이미지는 색상 척도로 표시되는 부피 변화의 크기를 이해하는 데 도움이 됩니다. 밝은 파란색은 높은 볼륨을 의미하고 진한 파란색은 낮은 볼륨을 나타냅니다. 임피던스의 변화나 일회 호흡량의 변화가 회색으로 표시되지 않습니다(그림 8). 본질적으로, 그것은 이러한 변화가 폐 내에서 발생한 위치를 정확하게 찾아내는 지도와 같은 기능을 합니다.
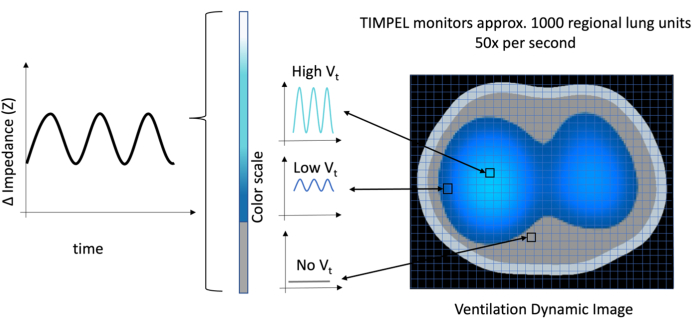
그림 8: 매트릭스 32 x 32의 각 픽셀(총 1,024픽셀)을 보여주는 Ventilation Dynamic Image. 환기의 진폭은 파동의 진폭과 색상의 강도로 표시되며, 회색은 볼륨이 없음을 나타내고 밝은 파란색에서 진한 파란색으로 전환되는 것은 각각 높은 볼륨에서 낮은 볼륨을 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
EIT가 도움이 될 수 있는 수많은 임상 상황이 있습니다. 예를 들어, 무기폐, 과팽창 및 기흉과 같은 폐 손상으로 이어질 수 있는 합병증 및 상태를 조기에 식별합니다. 무기폐는 입원 환자에게 가장 흔한 병리 중 하나입니다. 이는 폐 조직의 부분적 또는 완전한 붕괴를 수반하며, 폐 용적을 감소시키고 가스 교환을 방해합니다. 무기폐는 그림 9A와 같이 EIT에 의해 감지될 수 있습니다. 그림 9A와 그림 9B는 13분 미만의 간격을 두고 동일한 환자의 인공호흡 맵 이미지입니다. 그림 9A에서 임피던스 변화의 23%만이 후방 영역에서 발생하며, 이는 이 영역에서 관찰되는 밝은 파란색 및 진한 파란색 영역의 감소로도 볼 수 있습니다. PEEP가 4에서 10cmH2O로 증가한 후 그림 9B는 폐 후방의 환기가 23%에서 43%로 증가했음을 보여줍니다. 그림 9A와 비교했을 때, 환자는 18.8에서 27.6mL/cmH2O로 순응도가 증가했으며, 특히 이러한 증가는 양측 후방 영역에서 발생하며, 이는 후방부의 밝은 파란색과 진한 파란색 영역이 증가한 것에서 분명합니다(그림 9B). 또한, 구동 압력이 감소하는데, 이는 일회 호흡량과 PEEP의 추가 증가가 폐에 추가적인 스트레스를 가하지 않음을 나타냅니다14,15.
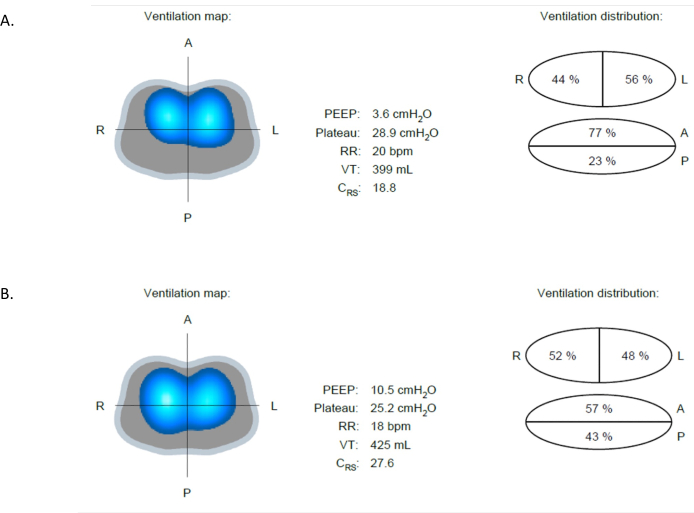
그림 9: 다양한 PEEP 값에서의 환기 차이. (A) PEEP 4cmH2O에서 이미지는 전방(통풍이 더 잘되는 영역)과 후(통풍이 덜 되는 영역) 사이의 환기 차이를 보여줍니다. (B) PEEP가 4에서 10cmH2O로 증가하면 후방 영역의 환기가 개선되는 것이 분명합니다. 약어: PEEP = positive-end expiratory pressure. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
과팽창은 폐 조직이 생리적 능력을 넘어 과도하게 팽창하거나 늘어나는 것을 말하며, 이로 인해 폐포와 주변 구조에 잠재적인 손상이 발생할 수 있습니다. 과팽창은 폐를 팽창시키기 위해 기계식 인공호흡기에서 가해지는 압력이 너무 높을 때 발생할 수 있습니다. 인공호흡기 시술 중 국소 폐 임피던스를 모니터링하면 과팽창과 폐 손상을 방지할 수 있다16. 도 10A에서, 환자는 22cmH2O의 PEEP에 있는 반면, 도 10B에서, PEEP는 12cmH2O로 감소된다. 그림 10B에서 EIT의 Ventilation Dynamic Image는 전방 폐의 밝은 파란색과 진한 파란색 영역의 증가를 표시하여 환기가 증가했음을 나타냅니다. 동시에 후폐의 밝은 파란색과 진한 파란색 영역이 감소하여(67%에서 43%로) 그림 10A에서 22cmH2O의 더 높은 PEEP와 관련된 과팽창의 완화를 시사합니다. 이 예는 EIT가 과팽창을 식별하고 폐 전체에 걸쳐 폐 보호 환기를 촉진하는 능력을 보여준다9.
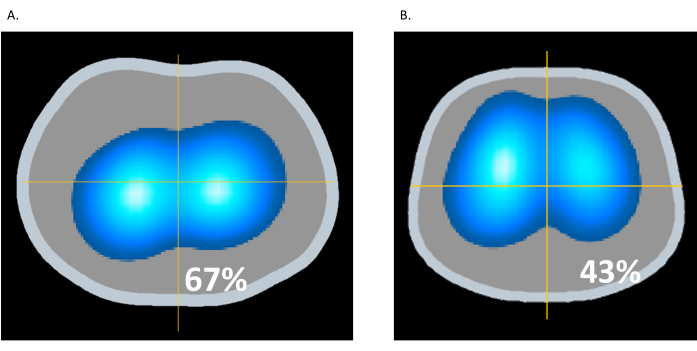
그림 10: PEEP의 변경 사항. (A) 22cmH2O의 PEEP; (B) 12cmH2O의 PEEP. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
기흉은 폐와 흉벽 사이의 공간인 흉막강에 공기가 존재하는 것을 특징으로 하는 질환입니다. 이러한 공기의 축적은 폐 허탈, 종격동 이동 및 혈역학적 붕괴로 이어질 수 있습니다. EIT를 사용하면 Ventilation Dynamic Image 17,18,19에 표시된 것처럼 흉부 임피던스의 변화를 실시간으로 관찰할 수 있습니다. Ventilation Dynamic Image에는 기흉이 의심되는 징후가 하나 있는데, 이를 "위상차가 뻣뻣한" 징후라고 합니다. "위상차" 표시는 폐의 임피던스 변화가 호흡 주기와 올바르게 정렬되지 않는 시각적 표시를 나타냅니다. 정상적인 호흡 주기에서 폐의 임피던스 변화는 흡입 및 호기 단계와 동기화되어야 합니다. 기흉이 발생하면 Ventilation Dynamic Image는 임피던스 변화가 정상적인 흡입 및 호기 단계와 동기화되지 않기 때문에 예상 패턴에서 벗어난 것을 보여줍니다. 또한 PEEP 감소에도 불구하고 호기말 폐 임피던스(EELI)의 증가를 의미하는 혈적계 기준선의 상승은 기흉의 존재를 추가로 나타낼 수 있습니다(그림 11).
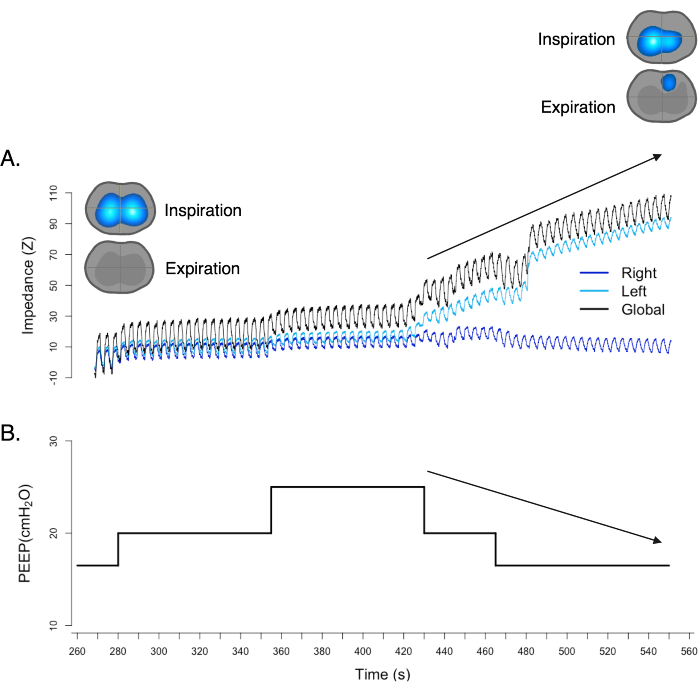
그림 11: 환기 맵의 "위상이 벗어남" 표시. 동시에, 혈량계는 PEEP의 감소에도 불구하고 기준선의 상승을 나타냅니다. 두 연구 결과 모두 기흉의 존재를 강력하게 지지하고 확인시켜줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
호흡 장애와 침습적 기계 환기를 포함한 지지적 개입의 필요성은 입원 환자에서 일반적입니다. 따라서 인공호흡 및 폐 관류를 모니터링하는 것은 신속하고 개인화된 진단 및 치료에 매우 중요합니다. X선 및 컴퓨터 단층 촬영 스캔(CT-scan)과 같은 표준 이미징 기술과 달리 EIT는 폐와 폐의 지역적 특성에 대한 비침습적이고 방사선이 없는 이미징을 실시간으로제공합니다 1,2,3,4,20. EIT는 이러한 기능으로 인해 중환자실과 수술실 모두의 병상에서 유용합니다. EIT는 인공호흡 모니터링을 제공할 뿐만 아니라 현재 일상적인 임상 실습에서는 실현 가능하지 않은 폐 관류를 분석할 수 있는 기능을 제공합니다 6,7,8.
기계 환기 중에는 폐를 보호하는 것이 주요 치료 목표입니다. 목표 중 하나는 폐포 손상으로 이어질 수 있는 폐의 무기폐와 과팽창을 피하는 것입니다. 일반적으로 PEEP는 무기폐를 예방하고 폐 용적을 유지하기 위해 투여됩니다. "PEEP 적정"으로 알려진 개별 환자에 대한 최적의 PEEP를 식별하는 것은 특히 급성 호흡곤란 증후군(ARDS), 비만 및 복부 고혈압과 같은 조건에서 중요한 방법입니다21,22.
PEEP 적정을 위한 기존 방법은 산소화 및 폐 역학에 의존합니다. 그러나 이 접근법은 국소적 폐 변화와 폐 영역이 과도하게 팽창되거나 축소되었는지 여부를 고려하지 않습니다. EIT와 같은 고급 기술은 흡기 및 호기 중 폐의 침상 옆에서 상세한 실시간 이미징을 제공합니다. EIT를 사용한 PEEP 적정은 실질 과팽창 및 붕괴를 최소화하면서 산소 공급 및 폐 역학을 최적화할 수 있습니다 23,24,25,26,27,28.
보다 최근에는 EIT의 관류 도구가 개발되어 국소 폐혈류에 대한 자세한 평가를 제공하여 의사와 의료진이 환기-관류 관계를 추정할 수 있습니다. EIT에 의해 평가된 폐 관류는 폐 혈관 확장제 요법에 대한 반응뿐만 아니라 환기 조정 및 산소 공급에 대한 반응을 결정하는 데에도 사용되었습니다 9,23,25,29,30,31. 또한, EIT는 또한 큰 폐 관류 결손을 감지할 수 있으며, 이는 혈전 색전증의 존재를 시사합니다32,33.
EIT에는 몇 가지 금기 사항이 있습니다. 첫째, EIT는 현재 심박 조율기 또는 이식형 제세동기를 사용하는 환자에게 권장되지 않습니다. 현재로서는 EIT 신호와 심박 조율기 기능의 전기적 간섭을 평가한 연구는 없습니다. 둘째, 임피던스 신호는 상당한 폐종격동 또는 피하 폐기종과 같은 조건에 의해 변경될 수 있으며, 이로 인해 환기 및 관류 맵의 올바른 해석이 손상될 수 있습니다. 마지막으로, 벨트가 피부에 밀착되어야 한다는 요구사항은 흉부 붕대를 감고 있는 환자에게 EIT를 사용하는 데 어려움을 준다34.
주의를 기울이고 특정 시나리오에서 관류 도구를 사용하지 않는 것이 중요합니다: 환자는 점점 더 많은 양의 승압제를 받고 있습니다. 고나트륨혈증 환자; 활동성 기흉 및/또는 기관지 흉막 누공이 있는 환자; 신생아 및 소아 환자. 기존 인공호흡 영상과 함께 관류 평가에 EIT를 활용하면 의료 서비스 제공자가 폐 기능에 대한 더 깊은 이해를 갖게 되어 다양한 임상 환경에서 환자의 진단 및 치료를 지원할 수 있습니다.
특정 모집단에 대한 고려 사항
EIT 기술의 원칙은 흉부 둘레와 벨트 크기에 따라 신생아, 소아 및 성인 환자에게 적용됩니다. 신생아용 벨트는 일회용이며 성인의 경우 48시간 대신 24시간 동안 착용하는 것이 좋습니다. 이 개체군과 관련된 작은 일회 호흡량(3mL에서 100mL까지)을 측정할 수 있고 1mL의 해당 데드 스페이스를 가질 수 있는 특정 유량 센서가 만들어졌습니다.
예를 들어, 온라인 모니터링은 폐를 사전 정의된 관심 영역(ROI)으로 분류합니다. 4개의 절반(왼쪽, 오른쪽, 전방 및 후방) 또는 4개의 수평 레이어. 그러나 오프라인 분석은 픽셀 단위와 같은 심층 분석을 위한 더 많은 기회를 제공할 수 있습니다. EIT의 모든 데이터는 제품 정보 관리(PIM)라는 독점 형식으로 저장됩니다. PIM 파일은 단층 촬영 재구성 전에 측정된 전압, 필터링되지 않은 신호 및 환기 매개변수를 포함하여 전처리된 정보를 캡슐화합니다. 오프라인 분석을 위해 PIM 파일을 추출하려면 USB 드라이브를 EIT 장치의 슬롯에 연결합니다. 그런 다음 인덱스 환자를 선택합니다. 오프라인 분석은 폐 생리학을 이해하는 데 필요한 모든 세부 데이터를 제공하기 때문에 유용합니다.
침상 진단 도구로서 EIT는 무기폐, 과팽창 및 기흉과 같은 상태를 진단하는 데 도움이 될 수 있습니다. 임상 증상 및 신체 검사 외에도 EIT는 이러한 진단에 대한 자세한 정보를 제공합니다. EIT는 기존 조사에 비해 더 빠른 정보 검색을 가능하게 합니다. 이 기능은 의사 및 기타 의료 인력이 환자를 진단하고 신속하게 치료할 수 있도록 권한을 부여합니다 24,35,36,37.
EIT를 사용하고 해석하는 방법을 배우는 것은 임상 실습에서 유익한 것으로 입증되었기 때문에 필수적입니다. EIT는 비침습적 특성과 실시간 모니터링 기능을 통해 다양한 의료 환경에서 의료 임상의에게 유용한 도구입니다.
공개
Glasiele Alcala, Caio C. A. Morais, Marcus Victor는 컨설팅 비용을 받았고, Carolyn La Vita는 이 연구에 사용된 장치를 제조하는 Timpel로부터 평가 비용을 받았습니다. Marcelo B. P. Amato는 Timpel의 소수 주주입니다. 다른 저자 중 누구도 이해 상충이 없습니다.
감사의 말
우리는 이 논문에 기여한 모든 공동 저자에게 진심으로 감사를 표하며 이 원고를 장비와 지원으로 아낌없이 지원해 준 TIMPEL Medical에 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| EIT equipment (ENLIGHT2100) | Timpel Medical | ||
| Belts | Timpel Medical | ||
| Belt coverage | Timpel Medical | ||
| Flow sensor | Philips | ||
| Reference Cable | Timpel Medical | ||
| Solution with high electrical conductivity (eg. hypertonic saline, sodium bicarbonate) | Not applicable |
참고문헌
- Costa, E. L., Lima, R. G., Amato, M. B. Electrical impedance tomography. Curr Opin Crit Care. 15 (1), 18-24 (2009).
- Frerichs, I., et al. Chest electrical impedance tomography examination, data analysis, terminology, clinical use and recommendations: consensus statement of the TRanslational EIT developmeNt stuDy group. Thorax. 72 (1), 83-93 (2017).
- Borges, J. B., et al. Regional lung perfusion estimated by electrical impedance tomography in a piglet model of lung collapse. J Appl Physiol (1985). 112 (1985), 225-236 (2012).
- Victorino, J. A., et al. et al. Imbalances in regional lung ventilation: a validation study on electrical impedance tomography. Am J Respir Crit Care Med. 169 (7), 791-800 (2004).
- Heines, S. J. H., et al. Pulmonary pathophysiology development of COVID-19 assessed by serial Electrical Impedance Tomography in the MaastrICCht cohort. Sci Rep. 12 (1), 14517 (2022).
- Nascimento, M. S., et al. Effect of general anesthesia and controlled mechanical ventilation on pulmonary ventilation distribution assessed by electrical impedance tomography in healthy children. PLoS One. 18 (3), e0283039 (2023).
- Zhao, Z., Fu, F., Frerichs, I. Thoracic electrical impedance tomography in Chinese hospitals: a review of clinical research and daily applications. Physiol Meas. 41 (4), 01 (2020).
- Kobylianskii, J., Murray, A., Brace, D., Goligher, E., Fan, E. Electrical impedance tomography in adult patients undergoing mechanical ventilation: A systematic review. J Crit Care. 35, 33-50 (2016).
- Costa, E. L., et al. Bedside estimation of recruitable alveolar collapse and hyperdistension by electrical impedance tomography. Intensive Care Med. 35 (6), 1132-1137 (2009).
- Mendes, P. V., et al. Lung perfusion during veno-venous extracorporeal membrane oxygenation in a model of hypoxemic respiratory failure. Intensive Care Med Exp. 10 (1), 15 (2022).
- Gaulton, T. G., et al. Regional lung perfusion using different indicators in electrical impedance tomography. J Appl Physiol (1985). 135 (3), 500-507 (2023).
- Martin, K. T., et al. Electrical impedance tomography identifies evolution of regional perfusion in a porcine model of acute respiratory dstress syndrome. Anesthesiology. 139 (6), 815-826 (2023).
- Xin, Y., et al. Improving pulmonary perfusion assessment by dynamic contrast-enhanced computed tomography in an experimental lung injury model. J Appl Physiol (1985). 134 (6), 1496-1507 (2023).
- vander Burg, P. S., Miedema, M., de Jongh, F. H., van Kaam, A. H. Unilateral atelectasis in a preterm infant monitored with electrical impedance tomography: a case report. Eur J Pediatr. 173 (12), 1715-1717 (2014).
- Riva, T., et al. Evaluation of atelectasis using electrical impedance tomography during procedural deep sedation for MRI in small children: A prospective observational trial. J Clin Anesth. 77, 110626 (2022).
- He, H., et al. Influence of overdistension/recruitment induced by high positive end-expiratory pressure on ventilation-perfusion matching assessed by electrical impedance tomography with saline bolus. Crit Care. 24 (1), 586 (2020).
- Girrbach, F., et al. Detection of posttraumatic pneumothorax using electrical impedance tomography-An observer-blinded study in pigs with blunt chest trauma. PLoS One. 15 (1), e0227518 (2020).
- Yang, Y., et al. Bedside electrical impedance tomography in early diagnosis of pneumothorax in mechanically ventilated ICU patients - a single-center retrospective cohort study. J Clin Monit Comput. 37 (2), 629-637 (2023).
- Kallio, M., et al. Electrical impedance tomography reveals pathophysiology of neonatal pneumothorax during NAVA. Clin Case Rep. 8 (8), 1574-1578 (2020).
- Pereira, S. M., et al. Individual positive end-expiratory pressure settings optimize intraoperative mechanical ventilation and reduce postoperative atelectasis. Anesthesiology. 129 (6), 1070-1081 (2018).
- Jimenez, J. V., Weirauch, A. J., Culter, C. A., Choi, P. J., Hyzy, R. C. Electrical impedance tomography in acute respiratory distress syndrome management. Crit Care Med. 50 (8), 1210-1223 (2022).
- Becher, T., et al. Individualization of PEEP and tidal volume in ARDS patients with electrical impedance tomography: a pilot feasibility study. Ann Intensive Care. 11 (1), 89 (2021).
- Barbas, C. S. V., Amato, M. B. P. Electrical impedance tomography to titrate PEEP at bedside in ARDS. Respir Care. 67 (8), 1061-1063 (2022).
- Maciejewski, D., Putowski, Z., Czok, M., Krzych, L. J. Electrical impedance tomography as a tool for monitoring mechanical ventilation. An introduction to the technique. Adv Med Sci. 66 (2), 388-395 (2021).
- Jonkman, A. H., et al. Lung recruitment assessed by electrical impedance tomography (RECRUIT): A multicenter study of COVID-19 acute respiratory distress syndrome. Am J Respir Crit Care Med. 208 (1), 25-38 (2023).
- Jimenez, J. V., et al. Electric impedance tomography-guided PEEP titration reduces mechanical power in ARDS: a randomized crossover pilot trial. Crit Care. 27 (1), 21 (2023).
- Sella, N., et al. Electrical impedance tomography: A compass for the safe route to optimal PEEP. Respir Med. 187, 106555 (2021).
- Slobod, D., et al. Integrating electrical impedance tomography and transpulmonary pressure monitoring to personalize PEEP in hypoxemic patients undergoing pressure support ventilation. Crit Care. 26 (1), 314 (2022).
- Spina, S., et al. Modulation of pulmonary blood flow in patients with acute respiratory failure. Nitric Oxide. 136-137, 1-7 (2023).
- Cenci, S., Santiago, R. S., Bittner, E. A., Berra, L. Assessing regional lung perfusion changes to inhaled pulmonary vasodilators by electrical impedance tomography. Am J Respir Crit Care Med. 208 (9), e39-e40 (2023).
- Ekkapat, G., Ribeiro De Santis Santiago, R., Victor, M., Berra, L. Electrical impedance tomography for assessing the impact of inhaled nitric oxide on pulmonary artery pressure. Anesthesiology. , (2024).
- He, H., et al. Bedside evaluation of pulmonary embolism by saline contrast electrical impedance tomography method: A prospective observational study. Am J Respir Crit Care Med. 202 (10), 1464-1468 (2020).
- He, H., et al. Three broad classifications of acute respiratory failure etiologies based on regional ventilation and perfusion by electrical impedance tomography: a hypothesis-generating study. Ann Intensive Care. 11 (1), 134 (2021).
- Ribeiro De Santis Santiago, R., et al. Lung imaging acquisition with electrical impedance tomography: Tackling common pitfalls. Anesthesiology. 139 (3), 329-341 (2023).
- Zhou, R., et al. Electrical impedance tomography to aid in the identification of hypoxemia etiology: Massive atelectasis or pneumothorax? A case report. Front Med (Lausanne). 9, 970087 (2022).
- Rubin, J., Berra, L. Electrical impedance tomography in the adult intensive care unit: clinical applications and future directions. Curr Opin Crit Care. 28 (3), 292-301 (2022).
- Tomicic, V., Cornejo, R. Lung monitoring with electrical impedance tomography: technical considerations and clinical applications. J Thorac Dis. 11 (7), 3122-3135 (2019).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유