Method Article
浸透圧を使用して皮下アンジオテンシンII注入は、マウスで誘導大動脈瘤パンプス
要約
浸透圧ポンプの皮下移植は、化合物の長期化と一貫性の配信のための便利なアプローチを提供します。このアプローチは、マウスの腹部および胸部大動脈瘤の両方を研究するために広く使用されています。
要約
Osmotic pumps continuously deliver compounds at a constant rate into small animals. This article introduces a standard protocol used to induce aortic aneurysms via subcutaneous infusion of angiotensin II (AngII) from implanted osmotic pumps. This protocol includes calculation of AngII amount and dissolution, osmotic pump filling, implantation of osmotic pumps subcutaneously, observation after pump implantation, and harvest of aortas to visualize aortic aneurysms in mice. Subcutaneous infusion of AngII through osmotic pumps following this protocol is a reliable and reproducible technique to induce both abdominal and thoracic aortic aneurysms in mice. Infusion durations range from a few days to several months based on the purpose of the study. AngII 1,000 ng/kg/min is sufficient to provide maximal effects on abdominal aortic aneurysmal formation in male hypercholesterolemic mouse models such as apolipoprotein E deficient or low-density lipoprotein receptor deficient mice. Incidence of abdominal aortic aneurysms induced by AngII infusion via osmotic pumps is 5 - 10 times lower in female hypercholesterolemic mice and also lower in both genders of normocholesterolemic mice. In contrast, AngII-induced thoracic aortic aneurysms in mice are not hypercholesterolemia or gender-dependent. Importantly, multiple features of this mouse model recapitulate those of human aortic aneurysms.
概要
大動脈瘤は破裂を予告し、通常の死につながる大動脈の恒久的な管腔の拡張を示します。この病気は、それぞれ、腹部大動脈瘤(AAAS)および胸部大動脈瘤(TAAに)と呼ばれている腹部や胸部大動脈領域の両方で発生します。分子機構と病態生理学的プロセスの不完全な理解に、大動脈瘤のいずれかのタイプの膨張や破裂を防ぐことができます何の実績のある薬物療法はありません。それは患者のサンプルを取得して、直接ヒトでの実験を行うことは困難であるので、AAASの定義のメカニズムに焦点を当てた研究はしばしば、動物モデルから推定されました。一般的に使用される動物モデルは、マウスへのアンジオテンシンII(AngIIの)の皮下注入です。このような大動脈内エラスターゼ灌流または開腹1,2を必要と塩化カルシウムの周囲大動脈アプリケーション、このメトとしてマウスでAAASを誘導するための他の外科的アプローチと比較すると、dは、体腔内への進入を必要とし、最小限の外科的専門知識3,4を必要としません。
AAASを誘導する浸透圧ポンプを介してのAngIIの皮下注入が最初に低密度リポタンパク質(LDL)受容体で報告された- / -マウスは、飽和脂肪に富む食事3を供給し、その後、アポEで- / -マウスは、通常の実験食4を供給しました。多くの最近の研究ではまたのAngIIは血中脂質が正常マウス5-7に AAASを誘導することを実証しました。注入のAngIIのアプローチは、AAASを誘導し、このモデルが人間AAASで観察された多くの機能を再現するため、分子機構と同様に(例えば、5-15)潜在的な治療戦略の開発を模索するために適用されています。例えば、喫煙、加齢、および男性の性別としてのヒトAAASのリスク要因もマウス16,17でのAngII誘発性AAASを増大させます。ヒトでのAAASと高コレステロール血症の関連は明確にする必要があります。しかし、ある有し高コレステロール血症がマウス18でのAngII誘発性AAASを増大することを一貫アン。マウスでのAngII誘発性AAASの病状は非常に不均一であり、深遠なマクロファージ浸潤、コラーゲン分解、血栓形成と解像度、および血管新生19-21によって特徴付けられます。ヒトでのAAASの最も一般的な腎臓下の大動脈の場所とは対照的に、マウスでのAngII誘発性AAASは副腎大動脈地域で発生します。 AngII誘発性AAASのもう一つの特徴は、ユビキタス貫血栓症につながる、貫中間休憩です。これは、ヒトでのAAASの病理学的開発はもっぱら起因する初期段階から動脈瘤組織の不足のために研究されていないため、経エラスチンの破壊はヒトで発生するかどうかは不明です。
マウスへのAngII注入はまた、主にヒトでのTAAのための最も一般的な領域である上行大動脈に制限されている胸部大動脈領域の深遠な拡大につながります 19,22-26アップ。 AngIIの輸液中に誘導さのAngII誘発性AAAS、TAAのと同様に、ヒトのTAA 25の多くの機能を再現。しかし、のAngII誘発性AAASとは対照的に、のAngII誘発性TAAは高コレステロール血症に関連付けられていないと性差を持っていません。
マウスに皮下のAngII注入の全体的な目標は、病理学的特徴とAAASとTAAの分子メカニズムを研究することです。
プロトコル
倫理の声明:マウスの研究では、ケンタッキー州制度動物実験委員会(:2006-0009 IACUCプロトコル番号)の大学の承認を得て行われています。マウスは、ケタミン(〜210ミリグラム/ kg)およびキシラジンの過剰摂取カクテル(〜30ミリグラム/キログラム)を使用して、終了時に安楽死させます。
AngII量の1計算
注:このプロトコルは、4男性のLDL受容体に4週間のAngII(千NG / kg /分)の注入の例を使用しています - / - マウスは、飽和脂肪に富んだ食餌を与え。
- 注入のために必要なのAngIIの量を計算する前にマウスを研究秤量します。
- 実験に必要なのAngIIの質量を計算するためのテンプレート( 表1)を使用します。テンプレートのステップ4の「ポンプ速度」としてポンプの指示に示されている「平均ポンプ速度」を使用してください。手動で5、およびステップ6 - - テンプレートでは、レコードが1〜ステップ10は自動的に計算されます。
- テンプレートでは、と仮定マウスは、4週間のAngII千NG / kg /分の注入時の体重1gを得ることができます。
注:各マウスは、マウス株および食事のような多くの変数に依存する非常に異なる体重増加を有していてもよいです。私たちは日常的にこれまでの研究から、私たち自身の経験に基づいて、「0」か「1グラム」を使用します。 - 各ポンプは、約250マイクロリットルを必要とするため、各マウスのためのAngII液300μlの総容量を計算します。
- テンプレートでは、と仮定マウスは、4週間のAngII千NG / kg /分の注入時の体重1gを得ることができます。
AngIIの2.解散
- ストアは、-20℃でのAngIIバイアルを凍結乾燥しました。開口部の前にRTへのAngIIバイアルを平衡化。
- 滅菌プラスチックチューブに計算された質量のAngII( 表1に示すように7.3 mg)を秤量します。
注:のAngIIの水溶液をガラスに結合するための強い親和性を有するため、メルクインデックスごとに、溶解用のガラス管を使用しないでください。 - 滅菌生理食塩水の計算量を追加します(1200μ凍結乾燥のAngII、キャップを含むプラスチックチューブにL)、溶液が透明になるまで反転により完全に混合。
- ラベルマウス番号#1、#2、#3、およびキャップを有する個々の滅菌プラスチックチューブの#4(0.5〜1.5ミリリットル)。ステップ1.2および表1で計算される体重に基づいて各マウスについて層状フード下のAngIIの溶液を調製します。
- 例えば、チューブ#1に、ピペット3.6μlの滅菌生理食塩水、その後、296.4μLのAngII液、ゆっくり上下にピペッティングすることによって十分に混合します。
- (;滅菌4ミリリットル)キャップ付きプラスチックチューブのラベルにマウス番号。これらは、ステップ3.13に記載されるようにポンプをインキュベートするために使用されます。
3.浸透圧ポンプの充填
- ポンプの本体と流量調節( 図1):2つの部分にポンプを取得します。各ボックスは、個別包装されている10ポンプ本体とフローモデレーターを持っています。ロット番号を記録します。
注:常に着用手袋は、ポンプの外部ケーシングに手から転送された油は、悪の機能をポンプに影響しますので。インプラントからの感染の危険性を回避するために、滅菌手袋、ガーゼ、チューブ、充填針を使用し、ポンプを準備するためにボートを量ります。 - これらは一度開け格納することができないように、研究のために必要なポンプ本体とフローモデレーターの数のみを開きます。 10以上のポンプが必要な場合は、別のロット番号からのポンプは異なる平均充填量とポンプ速度を持っているので、ポンプのロット番号は、一つの研究のために同じであることを確認してください。
- (本体とモデレータをフローの両方を含む)の各ポンプを計量し、小数点以下4桁に重みを注意してください(例えば、マウス#の1.1443グラム1)。テンプレート( 表1)に「ポンプの重量は空」と呼ばれるこの量は、充填率を算出するために使用されます。
- 1 ccの滅菌注射器にポンプ充填針を取り付け、慎重に適切からのAngII溶液で注射器を埋めます番号のプラスチックチューブ。これは、シリンジ内に空気を吸引しないようにすることが重要です。
- 針が下方に位置している注射器から慎重にすべての気泡を除去します。ポンプ内の気泡の導入を防止するために、この位置に針/注射器を保管してください。
- 静かにポンプ本体内に充填針を挿入します。ポンプ内に針の先端を進めます。ポンプの底にしっかりと針の先端を休まないでください。
- AngIIの溶液を用いてポンプを埋めるために、ゆっくりとシリンジプランジャーを押してください。ポンプ内部の暗い影が充填レベルを示しています。充填量は指示に従って、約246μlです。
- ポンプを充填停止し、流体のビーズがポンプの外に上昇すると、慎重にとすぐに針を取り除きます。
- 隙間が流量調節のヘッドとポンプ本体の上面( 図1)の間に見られなくなるまで、ポンプ本体の上部の穴を介してポンプへの流量調節を挿入します。
- moderatの挿入またはポンプ本体に流量調節の開口部から一部の流体漏れにつながります。慎重にモデレータの配置中に漏洩した可能性があるすべての余分な油を吸い取ります。
- 満たされたポンプを計量。テンプレートに「充填ポンプ重量」の重量を記録します。
- 充填率(%)=( "満たされた「ポンプ重量 - 「空」)を計算すると、千/ボリューム×100を埋める意味xは。
- 充填率が等しいか100%より大きくあるべきで、理想的には、表1に示すように充填率算出します。補充ポンプ充填率が<95%(気泡がポンプ内に存在してもよいことが暗示される)場合。
- モデレータヘッドを上に向けてラベル4ミリリットルチューブ(ステップ2.5)に充填ポンプを配置します。ポンプをカバーするために滅菌生理食塩水の十分な量を追加します。移植までの生理食塩水管にポンプを保管してください。
- 37ºCインキュベーター内チューブを置きます。インキュベートは、部分的なプライミングを可能にした後、マウスに移植するために、O / N(少なくとも12時間)ポンプ。パンプAngIIのINGは、マウスが手術からの事前のAngII注入の間に生じるいかなる潜在的なストレスに回復することができ、移植後約24時間を、開始します。
ポンプ注入の4準備
- オートクレーブ(重力モード、ドライサイクル、15分)ガーゼ、綿棒やハサミ、止血剤、鉗子、ステープルを含む外科用ツール、およびステープラー少なくとも1日手術前に。
- 処置室では、イソフルランを使用して麻酔用気化器を準備します。層流フード内で無菌ドレープを開き、およびイソフルラン麻酔のためのノーズコーンを配置します。層流フード内でベタジン、70%エタノール、滅菌水、ビーズ殺菌、防腐手でこする、綿棒、ガーゼ、充填ポンプを配置します。
- ドン・マスクとガウンは、その後、清潔な手で層流フード内で外側ドレープを開きます。滅菌手袋の上に置き、滅菌内部パックを開きます。
ポンプ注入の5の外科的処置
- 誘導チャムにマウスを置きます2% - 1.5の流速でイソフルランの流入とBER。横臥した後、3分 - 追加の2のためのマウスを監視します。左または右の肩の上に、四半期ほどの大きさの領域を剃ります。
- イソフルラン流出( 図2A)に接続されたコーンと同一平面の鼻で、層状フード内でマウスを置きます。外科医の利き手に向かってマウスの頭を置きます。麻酔下ながら乾燥を防止するために、マウスの目に獣医軟膏を使用してください。マウスは手術前の痛みの刺激に対する応答を持っていないことを確認してください。例えば、ペダル応答は痛みのための良好な指標です。
- スワブ、70%エタノールで3ワイプ続いベタジンで剃毛面積を拭きます。ドンまたは滅菌手袋を変更します。
- 前脚の肩甲骨の上に耳の後ろ〜1cmの切開を作るために、外科用メスを使用してください。この切開は、尾に垂直でなければなりません。皮膚のみではなく、下にある組織を切るように注意してください。
- ホールドFORC片手でのEPSは切開を開き、止血剤( 図2B)を使用して、皮膚の下に皮下トンネルを作るためにもう一方の手を使用しています。
- テールに向かって止血先端を進める、とポンプ用のポケットを作成します。これは慎重に袋を開くために、皮膚の下に止血剤の顎を開くことによって達成されます。切開から止血剤を撤回。
- マウス( 図2C)の後方に配置さモデレータヘッドを切開部にポンプを挿入します。そっとポケットに完全にポンプを押してください。無緊張や皮膚の伸縮に傷を閉鎖するのに十分な空き領域が必要です。
- ポンプが挿入された後、しっかりので、エッジが会う矯正、切開部の両側を挟まれ、( 図2D)を閉じるように1または2創傷クリップを配置します。傷の完全な閉鎖があることを確認するために切開部位を点検し、ポンプは、サイト上で直接押しされていないこと。
- 局所リドカインクリームを適用しますノーズコーンからきれいな綿のswab.Removeマウス(4重量/重量%)であり、それが意識を取り戻すまで加熱パッドの上に置きます。回収した後、マウスをそのケージに戻しています。
- マウスとの間に10秒間ビーズ滅菌器に手術器具を配置します。楽器が使用する前に冷却してください。マウスの間消毒手でこするときれいな手袋。完全な回復が達成されるまで、すべてのマウスを監視します。
- 密接に手術後のマウスを監視します。マウスが苦痛、脱水または見かけの体重減少の兆候を示している場合 - (0.3ミリリットル0.2)を皮下滅菌生理食塩水のボーラスを注入します。最初の10日の間に少なくとも一日二回、マウスを観察し、その後少なくとも一度毎日。任意のマウスは、AngIIの輸液中に死亡場合は、直ちに剖検を実行します。手術後14日 - 7との間に創傷クリップを削除します。
6.収穫、定着、クリーニング、および大動脈のイメージング
- OPEをカットし、腹側マウスの胸部と腹部の空洞を切り開いnは右心房、大動脈に血液を除去した後、大動脈27を収穫するために心臓の左心室を介して生理食塩水で灌流。
- 48時間27から24のために4%パラホルムアルデヒドまたは10%中性緩衝ホルマリン少なくとも3 mlを含有するプラスチックチューブで採取した大動脈を配置します。
- 慎重に外膜組織を削除します。ピンと黒のワックスのピン大動脈。同じ倍率で大動脈の画像を取得します。 図3に示すように、キャリブレーション用の各画像内の定規を含めます。
大動脈の7.エン面イメージング
- 大動脈弓の外側と内側の曲率を通って長手方向に開いて大動脈を切断し、腕頭、左頸動脈、左鎖骨下動脈などのオープン主要な枝を切りました。外側の外膜は、黒のワックスに隣接して敷設とフラットピン大動脈。
- 同じ倍率で大動脈の内膜表面の顔写真エン取得。ショーのように、キャリブレーション用の各画像内の支配者を含めます図4中のn。
結果
4男性のLDL受容体 - / - プロトコルの項で説明したマウスは、AngIIの注入の4週間後に安楽死させました。大動脈は、収穫、洗浄、および大動脈の拡張部分を可視化するために画像化しました。 図3に示すように 、大動脈は、副腎領域(AAAS; 図3A)の拡張を含むいくつかの異なる特性を有する、上昇領域(のTAA; 図3B)の拡大、または両方の領域の拡大(AAASとのTAAの両方の存在;図3C)、形態に対し、1マウスで) 図3D(肉眼的に正常でした。 図3Aの赤線で示すように、腹部大動脈の拡張は、副腎領域のex vivoでの最大幅を測定することによって定量化されます。 図4に示すように、大動脈の拡張を昇順測定するために、大動脈を切開し、固定した。内膜表面積は番目に囲ま上昇大動脈領域(面積で測定しましたTAAを定量する。図4(a)の E赤線)。定規は、両方の図3及び図4に示すように、測定値を標準化するために、各画像に含まれました。

。本体と流量調節: 満たされた浸透圧ポンプの図1.代表画像は 、各ポンプは、2つの別々の部分が含まれています。 AngIIでポンプ本体を充填した後、流量調節器は、ポンプをシールするために挿入されます。
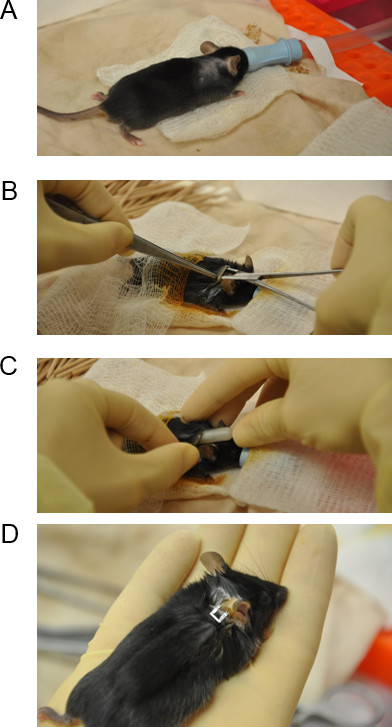
ポンプの移植手術の図2のプロセス(A)マウスをイソフルランと酸素を連続的に放出され、ノーズコーンを有する層流フード内に配置されます。 (B)ストレート止血剤は皮下トンネルを作るために皮膚切開に挿入されています。 (C)ポンプが挿通されています皮膚切開優しく; (D)皮膚切開は、ポンプ挿入後ステープルされています。
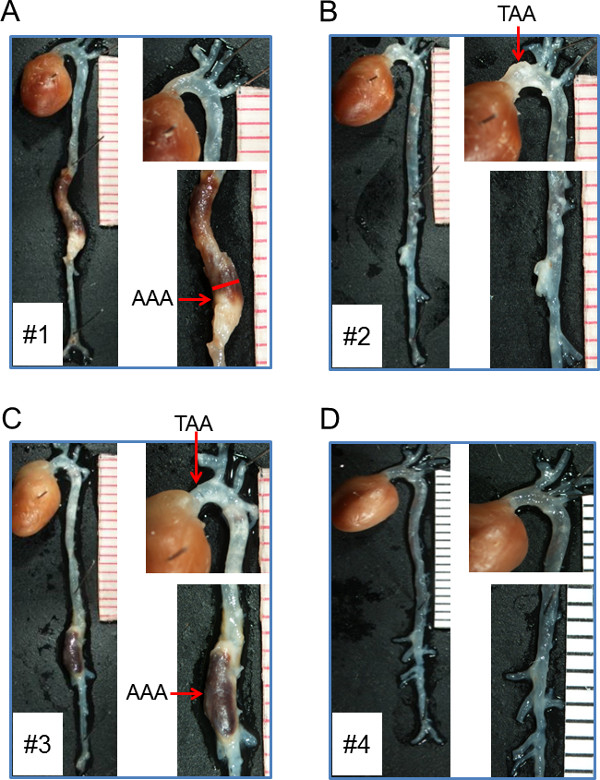
注入したマウスからの図3.大動脈画像(ex vivoで )のAngIIのAngII千NG / kg /分が男性のLDL受容体に注入した- 。/ - 28日間のマウス。 (A)AAASは、血栓症を伴います。レッドライン(2.05ミリメートル)は、副腎地域で最大の大動脈幅の測定を示しています。肉眼的に正常な腹部大動脈と大動脈拡張(TAA)を昇順(B); (C)昇順と副腎大動脈領域(のTAAおよびAAAS)の両方で深遠な拡張部分。 (D)昇順または副腎大動脈領域のいずれかの明白な拡張で極めて正常大動脈。
4.jpg "/>
AngIIを注入したマウス由来の胸部大動脈の領域図4.エン顔画像のAngII千NG / kg /分雄LDL受容体に注入した- 。/ - 28日間マウスを。赤い線で概説表面積は、大動脈弓の一部を含む昇順大動脈領域を示します。
| 1 | 線量必要 | 千 | NG / kg /分 | ||||
| 2 | 体重(最大マウス)を起動します | 24.8 | グラム | ||||
| 3 | 合計推定体重増加 | 1 | グラム | ||||
| 4 | ポンプ流量 | 0.25 | μL/時 | ||||
| 5 | νマウスのmber | 4 | |||||
| 6 | 動物のための時間当たりの線量 | 1518 | NG | ||||
| 7 | コンク必要 | 6072 | NG /μL | ||||
| 8 | 300 ulの解決のために | 1.82 | MG /300μlの | ||||
| ソリューションNEEDED | |||||||
| 9 | 合計のAngII(MG) | 7.3 | ミリグラム | ||||
| 10 | 食塩水に溶解&#160; | 1200 | μL | ||||
| マウス | 体重 | 希釈係数 | 容量(μL) | ポンプ重量(g) | 充填率 | ||
| # | (G) | AngII | 生理食塩水 | 空 | FILLED | (%) | |
| 1 | 24.5 | 1.0 | 296.4 | 3.6 | 1.1443 | 1.3877 | 99 |
| 2 | 23.0 | 0.9 | 278.2 | 21.8 | 1.1677 | 1.4145 | 100 |
| 3 | 24.8 | 1.0 | 300.0 | 0.0 | 1.1438 | 1.3904 | 100 |
| 4 | 21.8 | 0.9 | 263.7 | 36.3 | 1.1438 | 1.3904 | 100 |
| 希釈係数=最大のマウスのマウス/体重の体重 | |||||||
| マウス | 体重 | 希釈係数 | 容量(μL) | ポンプ重量(g) | 充填率 | ||
| # | (G) | AngII | 生理食塩水 | 空 | FILLED | (%) | |
| 1 | 24.5 | 1.0 | 296.4 | 3.6 | 1.1443 | 1.3877 | 99 |
| 2 | 23.0 | 0.9 | 278.2 | 21.8 | 1.1677 | 1.4145 | 100 |
| 3 | 24.8 | 1.0 | 300.0 | 0.0 | 1.1438 | 1.3904 | 100 |
| 4 | 21.8 | 0.9 | 263.7 | 36.3 | 1.1438 | 1.3904 | 100 |
表1:浸透圧ポンプを経由して28日間の注入のための計算。
ディスカッション
AngIIの皮下に提供する浸透圧ポンプは、マウスにおける大動脈瘤を誘発するルーチン的なアプローチです。多くの研究室からのデータに基づいて、これはマウスでAAAS 3,4とのTAA 22〜26の両方を研究するための信頼性が高く、再現性のある方法であることを一貫発見がありました。したがって、このマウスモデルは、ヒト大動脈瘤のいくつかの機能を再現すると、これらの壊滅的な疾患に機械的な洞察を提供したモデルであると考えられます。
老化は、ヒトでのAAASの危険因子であるが、これは、マウスにおける体系のAngII誘導性のAAASために研究されていません。 48週間4,5,7 -しかし、それはのAngII誘発性AAASの発生率および重症度は8歳の時にマウスで類似しているが表示されます。 TAAの形成に見かけ年齢に関連した差を示さなかった24週22-26、 -現在、8歳の時、マウスでのAngII誘発性のTAAを報告する唯一のいくつかの研究があります。
雌マウスのAngII 4,28を注入した雄マウスよりAAASのはるかに低い発生率を持っています。それのAngII誘導性のAAASの発生率はそれぞれ30%未満、対50%以上である、normo - コレステロール血症マウスよりハイパーではるかに高いことも注目に値します。 AngIIの注入中正常なおよび高コレステロール血症のマウスの両方で - (30%、およそ10)さらに、大動脈破裂は頻繁にあります。このようなLDL受容体などの高コレステロール血症のマウスに千NG / kg /分の速度でのAngIIの輸液、 - / - マウスは、西洋食またはアポリポタンパク質(アポE)を供給 - / - マウスは、正常または西洋食を与え、AAAの最大効果を持っています開発3,4,29。この注入速度は、高コレステロール血症マウスで目的の遺伝子を操作することがAAASを低減することが期待されている研究のために最適です。高コレステロール血症のマウスでの操作がAAASを強化することが期待されている場合は、500 ngの/ kg /分または30以下の割合でのAngIIを注入することをお勧めします。 AAASとは対照的に、何のデモはありません男性の性別や高コレステロール血症とのAngII誘発性のTAA 25の間nstrated関連。目的の遺伝子の操作はのTAAを強化することが期待されている場合は、同様にAAASに、我々はAngIIの輸液1,000 NG / kg /分より低い注入速度をお勧めします。
これはAngIIの誘発性大動脈瘤の発生率および重症度は、個々のマウス間および研究の間で変動していることを知ることも重要です。マウスは、大動脈瘤を発症しない場合は、1の潜在的な可能性は、AngIIのが正常マウスに配信されていないかもしれないということです。 AngIIの高い注入速度の検証については、のような千NG / kg /分、血圧の測定は、非侵襲的なテール-カフ法31を使用する前に、とのAngII注入、中に推奨されます。千NG / kgの割合でのAngII注入/分、マウスにおける収縮期血圧を上昇させます。また、血漿レニン濃度のAngIIをrに負のフィードバックを有するためのAngII注入中または終了時に測定することができますENIN分泌。したがって、AngIIの輸液は、血漿レニン濃度の減少につながります。 AngIIを注入したマウスは明白な大動脈の病変、血圧の増加なし、および血漿レニン濃度の減少を全く持っていない場合には、移植された浸透圧のAngIIはミニポンプを介して効率的に配信されていないことを示します。我々は、研究から、このマウスを取り外すことをお勧めします。これは、いくつかのマウスは、増加した収縮期血圧にもかかわらず、大動脈瘤を発症し、血漿レニン濃度を減少させないことに注意することも重要です。これらのマウスは、研究に残っている必要があります。
要約すると、のAngII注入は、マウスにおいて、大動脈瘤を誘導するために浸透圧ポンプを用いて皮下移植することによって達成されます。この方法は、AAASとのTAAの両方を研究するために使用されている指定された持続時間のために定義されたレートで一定のAngIIを提供します。
開示事項
この記事の出版は、アルゼットが主催しています。
謝辞
The research work presented in this manuscript was supported by a grant (HL107319 to Alan Daugherty and HL107326 to Lisa A. Cassis) from the National Institutes of Health of the United States of America. The content in this manuscript is solely the responsibility of the authors and does not necessarily represent the official views of the National Institutes of Health. The publication of this manuscript was sponsored by DURECT Corporation.
資料
| Name | Company | Catalog Number | Comments |
| Angiotensin II | Bachem | H-1705 | compound used to induce aortic aneurysms |
| Alzet Osmotic Pumps | DURECT Corporation | Alzet Model 2004 | feasible for 28-day infusion in mice weighed > 20 g |
| Saturated fat-enriched diet | Harlan Teklad | TD.88137 | 42% calories/calories to stimulate hypercholesterolemia in LDL receptor -/- mice |
参考文献
- Pyo, R., et al. Targeted gene disruption of matrix metalloproteinase-9 (gelatinase B) suppresses development of experimental abdominal aortic aneurysms. J Clin Invest. 105 (11), 1641-1649 (2000).
- Chiou, A. C., Chiu, B., Pearce, W. H. Murine aortic aneurysm produced by periarterial application of calcium chloride. J Surg Res. 99 (2), 371-376 (2001).
- Daugherty, A., Cassis, L. Chronic angiotensin II infusion promotes atherogenesis in low density lipoprotein receptor -/- mice. Ann NY Acad Sci. 892 (1), 108-118 (1999).
- Daugherty, A., Manning, M. W., Cassis, L. A. Angiotensin II promotes atherosclerotic lesions and aneurysms in apolipoprotein E-deficient mice. J Clin Invest. 105 (11), 1605-1612 (2000).
- Deng, G. G., et al. Urokinase-type plasminogen activator plays a critical role in angiotensin II-induced abdominal aortic aneurysm. Circ Res. 92 (5), 510-517 (2003).
- King, V. L., Trivedi, D., Gitlin, J. M., Loftin, C. D. Selective cyclooxygenase-2 inhibition with celecoxib decreases angiotensin II-induced abdominal aortic aneurysm formation in mice. Arterioscler Thromb Vasc Biol. 26 (5), 1137-1143 (2006).
- Uchida, H. A., Poduri, A., Subramanian, V., Cassis, L. A., Daugherty, A. Urokinase-type plasminogen activator deficiency in bone marrow-derived cells augments rupture of angiotensin II-induced abdominal aortic aneurysms. Arterioscler Thromb Vasc Biol. 31 (12), 2845-2852 (2011).
- Wang, Y. X., et al. Angiotensin II increases urokinase-type plasminogen activator expression and induces aneurysm in the abdominal aorta of apolipoprotein E-deficient mice. Am J Pathol. 159 (4), 1455-1464 (2001).
- Bruemmer, D., et al. Angiotensin II-accelerated atherosclerosis and aneurysm formation is attenuated in osteopontin-deficient mice. J Clin Invest. 112 (9), 1318-1331 (2003).
- Gavrila, D., et al. Vitamin E inhibits abdominal aortic aneurysm formation in angiotensin II-infused apolipoprotein E-deficient mice. Arterioscler Thromb Vasc Biol. 25 (8), 1671-1677 (2005).
- Wang, J., et al. IgE actions on CD4+ T cells, mast cells, and macrophages participate in the pathogenesis of experimental abdominal aortic aneurysms. EMBO Mol Med. 6 (7), 952-969 (2014).
- Yoshimura, K., et al. Regression of abdominal aortic aneurysm by inhibition of c-Jun N-terminal kinase. Nat Med. 11 (12), 1330-1338 (2005).
- Usui, F., et al. Inflammasome activation by mitochondrial oxidative stress in macrophages leads to the development of angiotensin II-induced aortic aneurysm. Arterioscler Thromb Vasc Biol. 35 (1), 127-136 (2015).
- Mellak, S., et al. Angiotensin II mobilizes spleen monocytes to promote the development of abdominal aortic aneurysm in apoe-/- mice. Arterioscler Thromb Vasc Biol. 35 (2), 378-388 (2015).
- Krishna, S. M., et al. Peptide antagonist of thrombospondin-1 promotes abdominal aortic aneurysm progression in the angiotensin II-infused apolipoprotein-E-deficient mouse. Arterioscler Thromb Vasc Biol. 35 (2), 389-398 (2015).
- Norman, P. E., Curci, J. A. Understanding the effects of tobacco smoke on the pathogenesis of aortic aneurysm. Arterioscler Thromb Vasc Biol. 33 (7), 1473-1477 (2013).
- Daugherty, A., Powell, J. T. Recent highlights of ATVB: aneurysms. Arterioscler Thromb Vasc Biol. 34 (4), 691-694 (2014).
- Liu, J., Daugherty, A., Lu, H. Angiotensin II and abdominal aortic aneurysms: an update. Curr Pharm Design. , (2015).
- Rateri, D. L., Howatt, D. A., Moorleghen, J. J., Charnigo, R., Cassis, L. A., Daugherty, A. Prolonged infusion of angiotensin II in apoE(-/-) mice promotes macrophage recruitment with continued expansion of abdominal aortic aneurysm. Am J Pathol. 179 (3), 1542-1548 (2011).
- Saraff, K., Babamusta, F., Cassis, L. A., Daugherty, A. Aortic dissection precedes formation of aneurysms and atherosclerosis in angiotensin II-infused, apolipoprotein E-deficient mice. Arterioscler Thromb Vasc Biol. 23 (9), 1621-1626 (2003).
- Daugherty, A., Cassis, L. A., Lu, H. Complex pathologies of angiotensin II-induced abdominal aortic aneurysms. J Zhejiang Univ Sci B. 12 (8), 624-628 (2011).
- Daugherty, A., Rateri, D. L., Charo, I. F., Owens, A. P., Howatt, D. A., Cassis, L. A. Angiotensin II infusion promotes ascending aortic aneurysms: attenuation by CCR2 deficiency in apoE-/- mice. Clin Sci (Lond). 118 (11), 681-689 (2010).
- Rateri, D. L., et al. Endothelial cell-specific deficiency of Ang II type 1a receptors attenuates Ang II-induced ascending aortic aneurysms in LDL receptor-/- mice). Circ Res. 108 (5), 574-581 (2011).
- Rateri, D. L., et al. Depletion of endothelial or smooth muscle cell-specific angiotensin II type 1a receptors does not influence aortic aneurysms or atherosclerosis in LDL receptor deficient mice. PLoS One. 7 (12), 10-1371 (2012).
- Rateri, D. L., et al. Angiotensin II induces region-specific medial disruption during evolution of ascending aortic aneurysms. Am J Pathol. 184 (9), 2586-2595 (2014).
- Davis, F. M., et al. Smooth muscle cell deletion of low-density lipoprotein receptor-related protein 1 augments angiotensin II-induced superior mesenteric arterial and ascending aortic aneurysms. Arterioscler Thromb Vasc Biol. 35 (1), 155-162 (2015).
- Daugherty, A., Rateri, D. Development of experimental designs for atherosclerosis studies in mice. Methods. 36 (2), 129-138 (2005).
- Henriques, T. A., Huang, J., D'Souza, S. S., Daugherty, A., Cassis, L. A. Orchidectomy, but not ovariectomy, regulates angiotensin II-induced vascular diseases in apolipoprotein E-deficient mice. Endocrinology. 145 (8), 3866-3872 (2004).
- Daugherty, A., Manning, M. W., Cassis, L. A. Antagonism of AT2 receptors augments angiotensin II-induced abdominal aortic aneurysms and atherosclerosis. Br J Pharmacol. 134 (4), 865-870 (2001).
- Wang, S., et al. Deficiency of receptor-associated protein attenuates angiotensin II-induced atherosclerosis in hypercholesterolemic mice without influencing abdominal aortic aneurysms. Atherosclerosis. 220 (2), 375-380 (2011).
- Daugherty, A., Rateri, D., Lu, H., Balakrishnan, A. Measuring blood pressure in mice using volume pressure recording, a tail-cuff method. J Vis Exp. (27), e1291 (2009).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved