Method Article
Subkutane Angiotensin-II-Infusion mit osmotischen Pumpen induziert Aortenaneurysmen bei Mäusen
In diesem Artikel
Zusammenfassung
Subkutane Implantation von osmotischen Pumpen bietet eine praktische Vorgehensweise für eine längere und konsistente Bereitstellung von Verbindungen. Dieser Ansatz wurde ausgiebig verwendet, um sowohl in Bauch- und Brust Aortenaneurysmen in Mäusen untersucht werden.
Zusammenfassung
Osmotic pumps continuously deliver compounds at a constant rate into small animals. This article introduces a standard protocol used to induce aortic aneurysms via subcutaneous infusion of angiotensin II (AngII) from implanted osmotic pumps. This protocol includes calculation of AngII amount and dissolution, osmotic pump filling, implantation of osmotic pumps subcutaneously, observation after pump implantation, and harvest of aortas to visualize aortic aneurysms in mice. Subcutaneous infusion of AngII through osmotic pumps following this protocol is a reliable and reproducible technique to induce both abdominal and thoracic aortic aneurysms in mice. Infusion durations range from a few days to several months based on the purpose of the study. AngII 1,000 ng/kg/min is sufficient to provide maximal effects on abdominal aortic aneurysmal formation in male hypercholesterolemic mouse models such as apolipoprotein E deficient or low-density lipoprotein receptor deficient mice. Incidence of abdominal aortic aneurysms induced by AngII infusion via osmotic pumps is 5 - 10 times lower in female hypercholesterolemic mice and also lower in both genders of normocholesterolemic mice. In contrast, AngII-induced thoracic aortic aneurysms in mice are not hypercholesterolemia or gender-dependent. Importantly, multiple features of this mouse model recapitulate those of human aortic aneurysms.
Einleitung
Aortenaneurysmen weisen Permanentlumen Erweiterung der Aorta, der Bruch deutet und in der Regel zum Tode führt. Diese Krankheit tritt sowohl in Bauch- und Brustaorta Regionen, die als abdominalen Aortenaneurysmen (AAA) und Brust Aortenaneurysmen (TAA), jeweils bezeichnet werden. Aufgrund einer unvollständigen Verständnis der molekularen Mechanismen und pathophysiologischen Prozessen, gibt es keine bewährten medizinischen Therapie, die Ausdehnung oder Bruch der beiden Typen von Aortenaneurysmen verhindern kann. Da es schwierig ist, die Patientenproben zu erwerben und führen Experimente am Menschen direkt, Forschung mit Schwerpunkt auf der Festlegung der Mechanismen der AAAS wurde häufig von Tiermodellen extrapoliert. Eine häufig verwendete Tiermodell ist die subkutane Infusion von Angiotensin II (AngII) in Mäuse. Im Vergleich zu anderen chirurgischen Ansätze zur Induktion AAAs bei Mäusen, wie intraaortalen Elastase Perfusion oder peri-Aorten-Anwendung von Calciumchlorid, die Laparotomie 1,2 erfordern, dieser method nicht den Eintritt in die Körperhöhle erforderlich und erfordert nur minimale chirurgische Kompetenz 3,4.
Subkutane Infusion AngII durch osmotische Pumpen AAAs induzieren, wurde zunächst in geringer Dichte-Lipoprotein (LDL) -Rezeptor berichtet - / - Mäusen gefüttert eine gesättigte Fettsäuren angereicherte Diät 3 und anschließend in apoE - / - Mäuse ein normales Labordiät 4 zugeführt. Viele neuere Studien haben auch gezeigt, dass AngII induziert AAAs in normolipidämischen Mäusen 5-7. Der Ansatz der Infusion AngII wurde angewendet, um AAAs induzieren und entdecken molekularen Mechanismen sowie die Entwicklung von potenziellen therapeutischen Strategien (zB 5-15), da dieses Modell rekapituliert viele Funktionen im menschlichen AAAs beobachtet. Zum Beispiel Risikofaktoren der menschlichen AAAs wie Rauchen, Alter und männliches Geschlecht vermehren auch AngII induzierten AAAs bei Mäusen 16,17. Der Verband der Hypercholesterinämie mit AAAs beim Menschen bedarf der Klärung. Allerdings hat es seinen konsequent, dass Hypercholesterinämie ergänzt AngII induzierten AAAs bei Mäusen 18. Pathologien der AngII induzierten AAAs bei Mäusen sind sehr heterogen und durch tiefe Makrophageninfiltration, Kollagenabbau, Thrombosebildung und Auflösung und Neovaskularisation 19-21 gekennzeichnet. Im Gegensatz zu den häufigsten infrarenalen Lage von AAAs in Menschen AngII induzierten AAAs in Mäusen in der Nebennierenaortaregion auftreten. Ein weiteres Merkmal der allgegenwärtigen AngII induzierten AAAS ist die transmurale medialen Bruch, was zu transmuralen Thrombose. Unklar ist, ob transmurale Elastin Bruch beim Menschen auftritt, da pathologischen Entwicklung AAAs beim Menschen nicht ausschließlich wegen des Mangels an aneurysma Geweben von früheren Stadien untersucht.
AngII Infusion in Mäuse führt zu tiefgreifenden Expansion des Brustaortaregion, die überwiegend auf die aufsteigende Aorta, die die häufigste Region ist für TAAs in Menschen beschränkt ist 19,22-26. Ähnlich wie AngII induzierten AAAs, TAAs beim AngII Infusion induzierte auch rekapitulieren viele Funktionen des menschlichen TAAs 25. Doch im Gegensatz zu AngII induzierten AAAs, AngII induzierten TAAs sind nicht mit Hypercholesterinämie assoziiert und keine Geschlechtsunterschiede haben.
Das übergeordnete Ziel des subkutanen AngII Infusion in Mäusen ist es, pathologische Merkmale und molekularen Mechanismen der AAAS und TAA zu studieren.
Protokoll
Ethics Statement: Maus Studien sind mit Genehmigung der University of Kentucky Institutional Animal Care und Verwenden Committee (: 2006-0009 IACUC Protokollnummer) durchgeführt. Mäuse werden nach Auflegen durch eine Überdosis von Ketamin Cocktail (~ 210 mg / kg) und Xylazin (~ 30 mg / kg) getötet.
1. Berechnung der AngII Betrag
Hinweis: Dieses Protokoll wird am Beispiel Infusion AngII (1,000 ng / kg / min) während 4 Wochen in 4 männliche LDL-Rezeptor - / - Mäuse einen gesättigten Fettsäuren angereicherte Diät gefüttert.
- Wiegen Sie studieren Mäusen vor der Berechnung der Höhe der AngII zur Infusion benötigt wird.
- Verwenden Sie die Vorlage (Tabelle 1), um die AngII Masse für das Experiment benötigte zu berechnen. Verwenden Sie die "Mean Pumprate" in der Gebrauchsanweisung der Pumpen als "Pumprate" in Schritt 4 der Vorlage angezeigt. In der Vorlage Rekord Schritte 1-5 manuell, und die Schritte 6-10 werden automatisch berechnet.
- In der Vorlage an, dassMäuse werden 1 g Körpergewicht während der Infusion von 1000 ng AngII / kg / min für 4 Wochen erhalten.
HINWEIS: Jede Maus sehr unterschiedliche Körpergewichtszunahme, die von vielen Variablen, wie zB Mausstamm und Ernährung hängen müssen. Wir verwenden routinemäßig "0" oder "1 g" auf der Grundlage unserer eigenen Erfahrungen aus früheren Studien. - Berechnen Sie eine 300 ul Gesamtvolumen von AngII Lösung für jede Maus, da jede Pumpe benötigt ca. 250 ul.
- In der Vorlage an, dassMäuse werden 1 g Körpergewicht während der Infusion von 1000 ng AngII / kg / min für 4 Wochen erhalten.
2. Die Auflösung des AngII
- Shop lyophilisiert AngII Fläschchen bei -20 ° C. Äquilibrieren AngII Fläschchen auf Raumtemperatur vor dem Öffnen.
- Wiegen des berechneten AngII Masse (7,3 mg, wie in Tabelle 1 gezeigt) in einen sterilen Kunststoffrohr.
HINWEIS: Pro Merck Index, keine Glasröhren zur Auflösung verwenden, da eine wässrige Lösung aus AngII hat eine starke Affinität für die Bindung an Glas. - Fügen Sie das berechnete Volumen steriler Kochsalzlösung (1.200 μl) in das Kunststoffrohr, das die lyophilisierte AngII, Kappe, und mischen durch Umdrehen, bis die Lösung klar ist.
- Etikett Maus Nummern # 1, # 2, # 3 und # 4 auf einzelne sterile Plastikröhrchen mit Kappen (0,5 - 1,5 ml). Vorbereitung AngII Lösung unter einer laminaren Abzugshaube für jede Maus basierend auf dem Körpergewicht, wie in Schritt 1.2 und Tabelle 1 berechnet.
- Zum Beispiel Pipette 3,6 ul steriler Kochsalzlösung in das Rohr # 1, dann 296,4 ul AngII Lösung und mischen durch Auf-und Abpipettieren sanft.
- Label Maus Zahlen auf Kunststoffröhrchen mit Kappen (4 ml, steril). Diese werden zur Inkubation von Pumpen, wie in Schritt 3.13 beschrieben, verwendet werden.
3. osmotische Pumpe Füllung
- Erhalten Pumpen in zwei getrennten Teilen: dem Hauptkörper der Pumpe und dem Strömungsmoderator (Abbildung 1). Jede Box verfügt über 10 Pumpenkörper und Strömungs Moderatoren, die einzeln verpackt sind. Notieren Sie die Chargennummer.
HINWEIS: Tragen Sie immerHandschuhen, da Öle von den Händen auf die Außenhülle von Pumpen übertragen wird sich negativ auf Pumpfunktion. Verwenden Sie sterile Handschuhe, Gaze, Rohre, Füllnadel und wiegen Boote, um die Pumpen vorbereitet, um das Risiko einer Infektion aus dem Implantat zu vermeiden. - Öffnen Sie nur die Anzahl der Pumpenkörper und Strömungs Moderatoren für das Studium benötigt, da diese nicht gespeichert einmal geöffnet werden. Wenn mehr als 10 Pumpen benötigt werden, sicherzustellen, dass die Chargennummern der Pumpen sind für eine Studie, da Pumpen verschiedener Chargen unterschiedliche mittlere Füllvolumen und Pumprate.
- Wiegen Sie jede Pumpe (einschließlich sowohl des Hauptkörpers und der Strömungsmoderator), und notieren Sie das Gewicht auf 4 Nachkommastellen (zB 1,1443 g Maus # 1). Dieses Gewicht, bezeichnet als "Pumpenleergewicht" in der Vorlage (Tabelle 1), wird verwendet, um den gefüllten Verhältnis zu berechnen.
- Befestigen Sie die Pumpe Füllnadel auf eine 1 cc sterile Spritze und sorgfältig füllen Sie die Spritze mit AngII Lösung aus dem geeignetnummerierten Kunststoffrohr. Es ist wichtig zu vermeiden, Luft in der Spritze.
- Entferne alle Luftblasen sorgfältig aus der Spritze, während die Nadel nach unten gerichtet ist. Halten der Nadel / Spritze in dieser Position, um die Einführung von Blasen in die Pumpe zu verhindern.
- Setzen Sie vorsichtig die Füllnadel in den Pumpenkörper. Vorab die Spitze der Nadel in die Pumpe. Ruhen darf die Spitze der Nadel fest an der Unterseite der Pumpe.
- Drücken Sie den Spritzenkolben langsam auf die Pumpe mit AngII Lösung zu füllen. Ein dunkler Schatten in der Pumpe zeigt den Füllstand. Das Füllvolumen beträgt ca. 246 & mgr; l pro Anleitung.
- Stopp Befüllen der Pumpe und entfernen Sie vorsichtig die Nadel so schnell wie eine Perle von Flüssigkeit steigt aus der Pumpe.
- Legen Strömungsmoderator in die Pumpe durch das Loch auf der Oberseite des Pumpenkörpers, bis kein Spalt zwischen dem Kopf des Strömungsmoderator und der Oberseite des Pumpenkörpers (Abbildung 1) zu sehen.
- Einfügen von moderatoder in den Pumpenkörper führt zu einer gewissen Flüssigkeit von der Öffnung des Strömungsmoderator. Alle zusätzliche Flüssigkeit, die während der Platzierung von Moderatoren zugespielt haben könnte vorsichtig tupfen.
- Wiegen gefüllt Pumpe. Das Gewicht unter "Pump Gewicht Gefüllt" in der Vorlage.
- Berechnen Füllungsgrad (%) = (Gewicht Pump "gefüllt" - "leer") x 1.000 / mittlere Füllvolumen x 100.
- Berechnen Füllungsgrad wie in Tabelle 1 angegeben Idealer, Füllungsgrad sollte gleich oder größer als 100% sein. Refill Pumpe, wenn der Füllungsgrad von <95% (Verwicklung dass Luftblasen können in der Pumpe vorhanden).
- Zeigen gefüllt Pumpe in den markierten 4-ml-Röhrchen (Schritt 2.5) mit der Moderator den Kopf nach oben zeigt. In ausreichendes Volumen an steriler Kochsalzlösung, um die Pumpe zu decken. Halten Pumpe in Rohr von Kochsalzlösung bis zur Implantation.
- Die Röhrchen in einem 37 ° C Inkubator. Inkubiere Pumpen O / N (mindestens 12 hr) zu Teil Priming zu ermöglichen, und dann in Mäuse implantiert. Pumpeing von AngII beginnt ungefähr 24 h nach der Implantation, die Mäuse, um sich von der Operation vor einer potenziellen Belastung während AngII Infusions sich zu erholen.
4. Vorbereitung für Pump Implantation
- Autoklaven (Schwerkraft-Modus, Trocken-Zyklus, 15 min) Gaze, Wattestäbchen und chirurgische Instrumente einschließlich Schere, Gefäßklemme, Pinzetten, Heftklammern und Hefter mindestens 1 Tag vor der Operation.
- In einem Verfahren Raum, vorzubereiten Vaporizer für Narkose mit Isofluran. Öffnen Sie sterilen Tüchern in einer Sterilbank und legen Bugnase für Isofluran-Narkose. Zeigen betadine, 70% Ethanol, steriles Wasser, Perle Sterilisator, antiseptisch Händedesinfektion, Tupfer, Gaze, und füllte Pumpen in einer laminaren Haube.
- Don eine Maske und Gewand, dann öffnen Sie eine äußere Tuch in einer laminaren Haube mit sauberen Händen. Setzen Sie auf sterile Handschuhe und öffnen Sie die sterile Innenpackung.
5. Chirurgisches Vorgehen der Pump Implantation
- Bewegen Sie die Maus in einem Induktions ChamBER mit Zufluss von Isofluran mit einer Flussrate von 1,5 - 2%. Überwachen Sie die Maus für eine zusätzliche 2-3 Minuten nach Festliegen. Rasieren Sie sich über eine Fläche etwa so groß wie ein Viertel, über den linken oder rechten Schulter.
- Platzieren der Maus in einer laminaren Abzugshaube, mit der Nase fluchtend mit einem Kegel Isofluran Abfluss (2A) verbunden ist. Legen Sie den Kopf der Maus die Richtung dominanten Hand des Chirurgen. Verwenden vet Salbe auf die Augen Maus bis zur Trockenheit während der Narkose zu verhindern. Sicherzustellen, dass die Maus keine Reaktion auf die Stimulation der Schmerz vor der Operation. So ist beispielsweise Pedalantwort ein guter Indikator für die Schmerzen.
- Tupfer und wischen rasierte Fläche mit Betadin, gefolgt von drei Tücher mit 70% Ethanol. Don oder ändern Sie sterile Handschuhe.
- Verwenden ein chirurgisches Skalpell, ein ~ 1 cm Einschnitt hinter dem Ohr über das Schulterblatt des vorderen Schenkels vorzunehmen. Dieser Einschnitt sollte senkrecht zum Schwanz. Seien Sie vorsichtig, um nur die Haut und nicht die darunter liegende Gewebe zu schneiden.
- Halten forceps in der einen Hand den Schnitt öffnen, und mit der anderen Hand, um einen subkutanen Tunnel unter der Haut mit einer Gefäßklemme (2B) zu machen.
- Voran hemostat Spitze in Richtung der Schwanz, und erstellen Sie eine Tasche für Pumpe. Dies geschieht durch vorsichtiges Öffnen der Backen der Gefäßklemme unter der Haut zu öffnen, ein Beutel durchgeführt. Ziehen Sie die Gefäßklemme aus Einschnitt.
- Legen Pumpe in den Einschnitt mit dem Moderator Kopf an der Rückseite der Maus (Abbildung 2c) positioniert. Schieben Sie die Pumpe vollständig in die Tasche. Es sollte genügend Freiraum, um die Wunde ohne Spannung oder Dehnung der Haut schließen.
- Sobald eine Pumpe eingesetzt wurde, fest klemmen beide Seiten des Einschnitts, Richten, damit die Kanten treffen, und setzen Sie 1 oder 2 Wundklammern zu schließen (2D). Überprüfen Sie die Einschnittstelle, um sicherzustellen, dass es die vollständige Schließung der Wunde, und dass die Pumpe nicht direkt auf der Website drücken.
- Bewerben topische Lidocain-Creme(4% w / w) mit einem sauberen Baumwoll swab.Remove Maus aus dem Nasenkegel, und legen Sie sie auf einem Heizkissen, bis er das Bewusstsein wiedererlangt. Nach der Wiederherstellung wird die Maus in seinen Käfig zurück.
- Legen Sie chirurgische Instrumente in ein Sicke Sterilisator für 10 Sekunden zwischen den Mäusen. Erlauben Instrumente vor Gebrauch zu kühlen. Saubere Handschuhe mit antiseptischen Händedesinfektion zwischen Mäusen. Überwachen Sie alle Mäuse, bis vollständige Genesung erreicht ist.
- Überwachen Sie Mäusen eng nach der Operation. Speisen Sie einen Bolus von steriler Kochsalzlösung (0,2 bis 0,3 ml) subkutan, wenn eine Maus zeigt Anzeichen von Leiden, Dehydrierung oder scheinbare Gewichtsverlust. Zumindest zweimal täglich zu beobachten Mäusen während der ersten 10 Tage, und mindestens einmal täglich danach. Führen Sie eine Obduktion sofort, wenn Mäusen während AngII Infusions sterben. Entfernen Wundklammern zwischen 7 - 14 Tage nach der Operation.
6. Ernten, Befestigung, Reinigung, und Imaging von Aorten
- Schneiden Sie die Maus, Brust- und Bauchhöhle ventral, schneiden open rechten Vorhof Perfusion mit Salzlösung durch die linke Herzkammer des Herzens, um Blut in die Aorta zu entfernen, und Ernte der Aorta 27.
- Platzieren geerntet Aorten in Kunststoffröhrchen, die mindestens 3 ml 4% Paraformaldehyd oder 10% neutral gepuffertem Formalin für 24 - 48 Std. 27
- Entfernen adventitiellen Gewebe sorgfältig. Pin Aorta auf schwarzem Wachs mit Stiften. Erwerben Aorten-Bilder mit gleicher Vergrößerung. Fügen Sie ein Lineal in jedem Bild zur Kalibrierung, wie in Abbildung 3 dargestellt.
7. En face-Imaging von Aorten
- Schnitten Aorta Längsrichtung durch den äußeren und inneren Krümmungs Aortenbogen und aufgeschnitten Hauptzweige einschließlich innominate, linken Halsschlagader und linken Schlüsselbeinarterie. Pin Aorta Wohnung mit Außen adventitiellen Verlegung neben dem schwarzen Wachs.
- Erwerben en face Bild der Intima-Oberfläche Aorta bei gleicher Vergrößerung. Fügen Sie ein Lineal in jedem Bild zur Kalibrierung, als Erscheinenn in der 4.
Ergebnisse
Die 4 männlichen LDL-Rezeptor - / - im Protokoll beschrieben Mäuse wurden nach 4 Wochen AngII Infusions euthanasiert. Aorten wurden geerntet, gereinigt und abgebildet, um Aorta Streckungen visualisieren. Wie in Figur 3 gezeigt, haben die Aorten verschiedene Eigenschaften einschließlich Erweiterung der Nebennierenregion (AAAs; 3A), die Erweiterung der Steigbereich (TAAs; 3B) oder die Expansion beider Bereiche (Anwesenheit beider AAAs und TAAs, Fig 3C), während die Morphologie in eine Maus war grob normal (3D). Dilatation der Aorta abdominalis wird durch Messung der ex vivo maximale Breite der Nebennierenregion quantifiziert, wie von der roten Linie in 3A dargestellt. Zur Messung der aufsteigenden Aorta Dilatation wurden Aorten aufgeschnitten und gemerkt, wie in Abbildung 4 dargestellt. Intima-Oberfläche wurde in der aufsteigenden Aorta Bereich (Bereich von th umgeben gemessene rote Linien in 4A), um TAAs zu quantifizieren. Ein Lineal wurde in jedem Bild enthalten ist, um Messungen zu standardisieren, da in beiden Figuren 3 und 4 gezeigt.

. Abbildung 1. Repräsentative Bild gefüllt osmotischen Pumpe Jede Pumpe enthält zwei Teile: einen Hauptkörper und einen Strömungsmoderator. Nach dem Füllen der Pumpenkörper mit AngII wird die Strömungsmoderator eingeführt wird, um die Pumpe abzudichten.
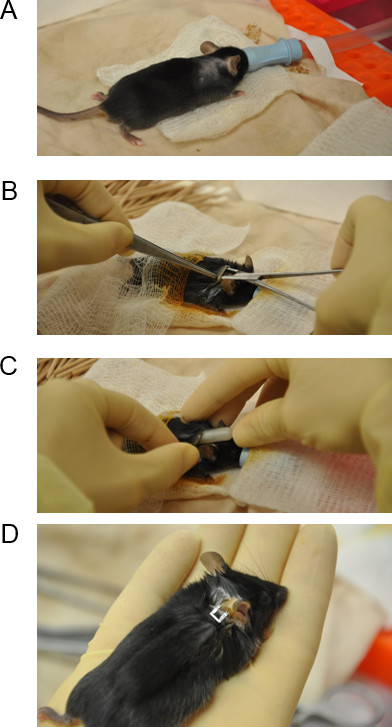
Figur 2. Prozess von Pumpenimplantationschirurgie (A) Maus wird in einen laminaren Haube mit einem Nasenkegel, der kontinuierlich ist Loslassen Isofluran und Sauerstoff zusammengebracht. (B) Ein gerader Hämostatikum in die Inzision einen subkutanen Tunnel bilden eingesetzt sind; (C) Die Pumpe wird durch das eingefügte Hautschnitt sanft; (D) Der Hautschnitt wird nach Pumpe Einschub geheftet.
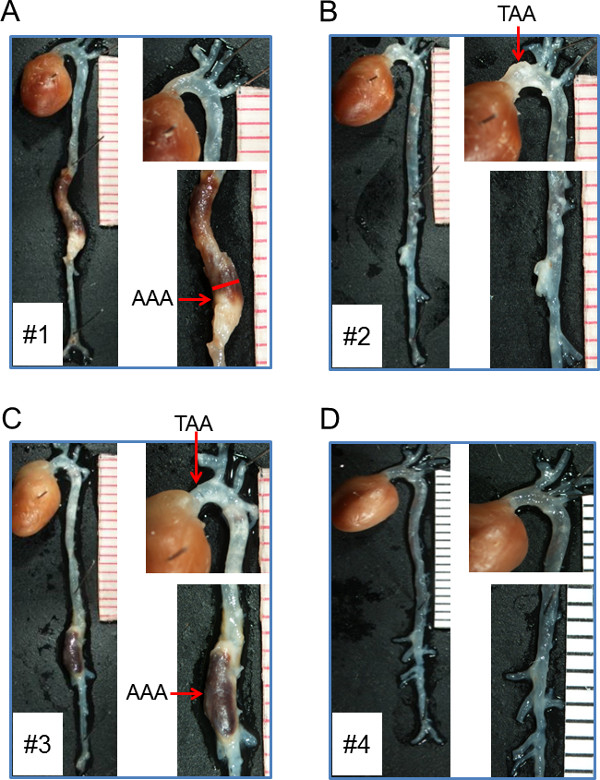
Abbildung 3 Aortic Bilder (ex vivo) von Mäusen, infundiert AngII AngII 1,000 ng / kg / min wurde bei männlichen LDL-Rezeptor infundierten -. / - Mäusen 28 Tage. (A) AAAs begleitet von Thrombose; Rote Linie (2,05 mm) zeigt die Messung der maximalen Aorta-Breite in der Nebennierenregion. (B) aufsteigenden Aorta Dilatation (TAA) mit grob normalen Bauchaorta; (C) Profunde Streckungen sowohl in der aufsteigenden und Nebennieren Aorten-Regionen (TAAs und AAA); (D) grob normalen Aorta ohne offensichtliche Erweiterung der aufsteigender oder Nebennieren Aorten-Region.
4.jpg "/>
Abbildung 4. En face Bilder der thorakalen Aorta Regionen aus Mäusen, die mit AngII AngII 1.000 ng / kg / min wurde bei männlichen LDL-Rezeptor-infundiert infundiert. - / - Mäuse für 28 Tage. Fläche durch eine rote Linie umrissen stellt die aufsteigenden Aorta Region einschließlich eines Teils der Aortenbogen.
| 1 | Dosis erforderlich | 1000 | ng / kg / min | ||||
| 2 | Starten Sie das Körpergewicht (größte Maus) | 24,8 | g | ||||
| 3 | Geschätzte Gesamtkörpergewichtszunahme | 1 | g | ||||
| 4 | Pumprate | 0,25 | ul / hr | ||||
| 5 | Number von Mäusen | 4 | |||||
| 6 | Dosis pro Stunde für die Tier | 1518 | ng | ||||
| 7 | Conc erforderlich | 6072 | ng / ul | ||||
| 8 | Für 300 ul Lösung | 1.82 | mg / 300 & mgr; | ||||
| LÖSUNG NOTWENDIG | |||||||
| 9 | Gesamt AngII (mg) | 7.3 | mg | ||||
| 10 | In Kochsalzlösung gelöst und# 160; | 1.200 | ul | ||||
| Maus | Körpergewicht | Verdünnungsfaktor | Volumen (ul) | Pump Gewicht (g) | Gefüllt Verhältnis | ||
| # | (g) | AngII | Salzig | Leer | Gefüllt | (%) | |
| 1 | 24,5 | 1.0 | 296,4 | 3.6 | 1,1443 | 1,3877 | 99 |
| 2 | 23,0 | 0.9 | 278,2 | 21,8 | 1,1677 | 1,4145 | 100 |
| 3 | 24,8 | 1.0 | 300,0 | 0.0 | 1,1438 | 1,3904 | 100 |
| 4 | 21,8 | 0.9 | 263,7 | 36,3 | 1,1438 | 1,3904 | 100 |
| Verdünnungsfaktor = Körpergewicht der Maus / Körpergewicht des größten Maus | |||||||
| Maus | Körpergewicht | Verdünnungsfaktor | Volumen (ul) | Pump Gewicht (g) | Gefüllt Verhältnis | ||
| # | (g) | AngII | Salzig | Leer | Gefüllt | (%) | |
| 1 | 24,5 | 1.0 | 296,4 | 3.6 | 1,1443 | 1,3877 | 99 |
| 2 | 23,0 | 0.9 | 278,2 | 21,8 | 1,1677 | 1,4145 | 100 |
| 3 | 24,8 | 1.0 | 300,0 | 0.0 | 1,1438 | 1,3904 | 100 |
| 4 | 21,8 | 0.9 | 263,7 | 36,3 | 1,1438 | 1,3904 | 100 |
Tabelle 1: Berechnung für die 28-Tage-Infusion über osmotische Pumpen.
Diskussion
Osmotische Pumpen liefern AngII subkutan ist eine Routine Ansatz zur Induktion von Aortenaneurysmen bei Mäusen. Basierend auf Daten von vielen Laboratorien haben kontinuierlich Ergebnisse, dass dies ein zuverlässiges und reproduzierbares Verfahren, um sowohl AAAs 3,4 und TAAs 22-26 in Mäusen untersucht. Daher wird dieses Mausmodell als ein Modell, das mehrere Funktionen des menschlichen Aortenaneurysmen rekapituliert und liefert mechanistische Einblicke in diese verheerenden Krankheiten.
Während Altern ist ein Risikofaktor für AAA in den Menschen, es wurde nicht systematisch für AngII induzierten AAAs bei Mäusen untersucht. Es scheint jedoch, Häufigkeit und Schwere von AngII induzierten AAAs ähnlich bei Mäusen im Alter von 8 - 48 Wochen 4,5,7. Derzeit gibt es nur wenige Studien, die über AngII induzierten TAAs in Mäusen im Alter von 8 bis 24 Wochen 22 bis 26, die nicht offensichtlich altersbedingten Unterschiede auf TAA Bildung zeigte.
Weibliche Mäuse haben eine viel geringere Inzidenz von AAAS als männliche Mäuse mit AngII 4,28 infundiert. Es ist auch erwähnenswert, dass das Auftreten von AngII induzierten AAAs in hyper- als normo-Cholesterolämie-Mäuse, die mehr als 50% gegenüber weniger als 30% ist, jeweils deutlich höher. Zusätzlich ist Aortenruptur häufige (ca. 10-30%) in beiden normo- und Hypercholesterinämie Mäusen während AngII Infusion. Die Infusion von AngII mit einer Rate von 1.000 ng / kg / min in Hypercholesterinämie Mäusen, wie LDL-Rezeptor - / - Mäusen gefüttert eine westliche Ernährung oder Apolipoprotein (ApoE) - / - Mäuse eine normale oder Western Diät gefüttert, hat eine maximale Wirkung auf AAA Entwicklung 3,4,29. Diese Infusionsrate optimal ist für eine Untersuchung, bei der Manipulation eines Gens von Interesse in hypercholesterolämischen Mäusen erwartet AAAs reduzieren. Wenn eine Manipulation in hypercholesterolämischen Mäusen erwartet AAAs vergrößern, empfiehlt es sich, AngII mit einer Rate von 500 ng / kg / min oder niedriger 30 zu infundieren. Im Gegensatz zu AAAs besteht keine Demonstrated Assoziation zwischen männlichen Geschlechts oder Hypercholesterinämie und AngII induzierten TAAs 25. Ähnlich wie AAA, wenn Manipulation eines Gens von Interesse wird erwartet, dass TAA zu erweitern, empfehlen wir Ihnen jedoch eine niedrigere Infusionsrate als 1000 ng / kg / min für AngII Infusion.
Es ist auch wichtig zu wissen, dass Häufigkeit und Schwere von AngII induzierten Aortenaneurysmen variieren zwischen den einzelnen Mäusen und zwischen den Studien. Wenn Mäuse nicht Aortenaneurysmen zu entwickeln, ist eine potentielle Möglichkeit, dass AngII möglicherweise nicht erfolgreich in Mäusen geliefert haben. Zur Validierung einer hohen Infusionsrate von AngII wie 1,000 ng / kg / min, die Messung der Blutdruck wird vor und während der Infusion AngII empfohlen unter Verwendung einer nicht-invasiven Schwanzmanschettenverfahren 31. AngII Infusion mit einer Geschwindigkeit von 1000 ng / kg / min erhöht den systolischen Blutdruck bei Mäusen. Auch kann der Plasma-Renin-Konzentrationen während AngII Infusion oder bei Beendigung seit AngII hat eine negative Feedback zu r gemessen werdenenin Sekretion. Daher führt AngII Infusion zu einer Reduzierung der Plasma-Renin-Konzentration. Wenn eine Maus mit AngII infundiert keine offensichtliche Aortaerkrankungen, keine Erhöhung des Blutdrucks, und keine Abnahme der Plasma-Renin-Konzentration würde dies anzeigen, dass AngII wurde nicht effizient durch die implantierte osmotische Minipumpe geliefert. Wir würden empfehlen, das Entfernen dieser Maus aus der Studie. Es ist auch wichtig zu beachten, dass einige Mäuse nicht entwickeln, trotz erhöhter systolischer Blutdruck Aortenaneurysmen und verminderte Plasma-Renin-Konzentration. Diese Mäuse sollten in der Studie bleiben.
Zusammengefasst ist AngII Infusion durch subkutane Implantation mit osmotischen Pumpen Aortenaneurysmen in Mäusen zu induzieren erreicht. Diese Methode liefert AngII ständig mit einer definierten Rate für bestimmte Zeitspannen, die verwendet werden, um beide AAAs und TAAs studieren.
Offenlegungen
Veröffentlichung dieses Artikels wird durch Alzet gesponsert.
Danksagungen
The research work presented in this manuscript was supported by a grant (HL107319 to Alan Daugherty and HL107326 to Lisa A. Cassis) from the National Institutes of Health of the United States of America. The content in this manuscript is solely the responsibility of the authors and does not necessarily represent the official views of the National Institutes of Health. The publication of this manuscript was sponsored by DURECT Corporation.
Materialien
| Name | Company | Catalog Number | Comments |
| Angiotensin II | Bachem | H-1705 | compound used to induce aortic aneurysms |
| Alzet Osmotic Pumps | DURECT Corporation | Alzet Model 2004 | feasible for 28-day infusion in mice weighed > 20 g |
| Saturated fat-enriched diet | Harlan Teklad | TD.88137 | 42% calories/calories to stimulate hypercholesterolemia in LDL receptor -/- mice |
Referenzen
- Pyo, R., et al. Targeted gene disruption of matrix metalloproteinase-9 (gelatinase B) suppresses development of experimental abdominal aortic aneurysms. J Clin Invest. 105 (11), 1641-1649 (2000).
- Chiou, A. C., Chiu, B., Pearce, W. H. Murine aortic aneurysm produced by periarterial application of calcium chloride. J Surg Res. 99 (2), 371-376 (2001).
- Daugherty, A., Cassis, L. Chronic angiotensin II infusion promotes atherogenesis in low density lipoprotein receptor -/- mice. Ann NY Acad Sci. 892 (1), 108-118 (1999).
- Daugherty, A., Manning, M. W., Cassis, L. A. Angiotensin II promotes atherosclerotic lesions and aneurysms in apolipoprotein E-deficient mice. J Clin Invest. 105 (11), 1605-1612 (2000).
- Deng, G. G., et al. Urokinase-type plasminogen activator plays a critical role in angiotensin II-induced abdominal aortic aneurysm. Circ Res. 92 (5), 510-517 (2003).
- King, V. L., Trivedi, D., Gitlin, J. M., Loftin, C. D. Selective cyclooxygenase-2 inhibition with celecoxib decreases angiotensin II-induced abdominal aortic aneurysm formation in mice. Arterioscler Thromb Vasc Biol. 26 (5), 1137-1143 (2006).
- Uchida, H. A., Poduri, A., Subramanian, V., Cassis, L. A., Daugherty, A. Urokinase-type plasminogen activator deficiency in bone marrow-derived cells augments rupture of angiotensin II-induced abdominal aortic aneurysms. Arterioscler Thromb Vasc Biol. 31 (12), 2845-2852 (2011).
- Wang, Y. X., et al. Angiotensin II increases urokinase-type plasminogen activator expression and induces aneurysm in the abdominal aorta of apolipoprotein E-deficient mice. Am J Pathol. 159 (4), 1455-1464 (2001).
- Bruemmer, D., et al. Angiotensin II-accelerated atherosclerosis and aneurysm formation is attenuated in osteopontin-deficient mice. J Clin Invest. 112 (9), 1318-1331 (2003).
- Gavrila, D., et al. Vitamin E inhibits abdominal aortic aneurysm formation in angiotensin II-infused apolipoprotein E-deficient mice. Arterioscler Thromb Vasc Biol. 25 (8), 1671-1677 (2005).
- Wang, J., et al. IgE actions on CD4+ T cells, mast cells, and macrophages participate in the pathogenesis of experimental abdominal aortic aneurysms. EMBO Mol Med. 6 (7), 952-969 (2014).
- Yoshimura, K., et al. Regression of abdominal aortic aneurysm by inhibition of c-Jun N-terminal kinase. Nat Med. 11 (12), 1330-1338 (2005).
- Usui, F., et al. Inflammasome activation by mitochondrial oxidative stress in macrophages leads to the development of angiotensin II-induced aortic aneurysm. Arterioscler Thromb Vasc Biol. 35 (1), 127-136 (2015).
- Mellak, S., et al. Angiotensin II mobilizes spleen monocytes to promote the development of abdominal aortic aneurysm in apoe-/- mice. Arterioscler Thromb Vasc Biol. 35 (2), 378-388 (2015).
- Krishna, S. M., et al. Peptide antagonist of thrombospondin-1 promotes abdominal aortic aneurysm progression in the angiotensin II-infused apolipoprotein-E-deficient mouse. Arterioscler Thromb Vasc Biol. 35 (2), 389-398 (2015).
- Norman, P. E., Curci, J. A. Understanding the effects of tobacco smoke on the pathogenesis of aortic aneurysm. Arterioscler Thromb Vasc Biol. 33 (7), 1473-1477 (2013).
- Daugherty, A., Powell, J. T. Recent highlights of ATVB: aneurysms. Arterioscler Thromb Vasc Biol. 34 (4), 691-694 (2014).
- Liu, J., Daugherty, A., Lu, H. Angiotensin II and abdominal aortic aneurysms: an update. Curr Pharm Design. , (2015).
- Rateri, D. L., Howatt, D. A., Moorleghen, J. J., Charnigo, R., Cassis, L. A., Daugherty, A. Prolonged infusion of angiotensin II in apoE(-/-) mice promotes macrophage recruitment with continued expansion of abdominal aortic aneurysm. Am J Pathol. 179 (3), 1542-1548 (2011).
- Saraff, K., Babamusta, F., Cassis, L. A., Daugherty, A. Aortic dissection precedes formation of aneurysms and atherosclerosis in angiotensin II-infused, apolipoprotein E-deficient mice. Arterioscler Thromb Vasc Biol. 23 (9), 1621-1626 (2003).
- Daugherty, A., Cassis, L. A., Lu, H. Complex pathologies of angiotensin II-induced abdominal aortic aneurysms. J Zhejiang Univ Sci B. 12 (8), 624-628 (2011).
- Daugherty, A., Rateri, D. L., Charo, I. F., Owens, A. P., Howatt, D. A., Cassis, L. A. Angiotensin II infusion promotes ascending aortic aneurysms: attenuation by CCR2 deficiency in apoE-/- mice. Clin Sci (Lond). 118 (11), 681-689 (2010).
- Rateri, D. L., et al. Endothelial cell-specific deficiency of Ang II type 1a receptors attenuates Ang II-induced ascending aortic aneurysms in LDL receptor-/- mice). Circ Res. 108 (5), 574-581 (2011).
- Rateri, D. L., et al. Depletion of endothelial or smooth muscle cell-specific angiotensin II type 1a receptors does not influence aortic aneurysms or atherosclerosis in LDL receptor deficient mice. PLoS One. 7 (12), 10-1371 (2012).
- Rateri, D. L., et al. Angiotensin II induces region-specific medial disruption during evolution of ascending aortic aneurysms. Am J Pathol. 184 (9), 2586-2595 (2014).
- Davis, F. M., et al. Smooth muscle cell deletion of low-density lipoprotein receptor-related protein 1 augments angiotensin II-induced superior mesenteric arterial and ascending aortic aneurysms. Arterioscler Thromb Vasc Biol. 35 (1), 155-162 (2015).
- Daugherty, A., Rateri, D. Development of experimental designs for atherosclerosis studies in mice. Methods. 36 (2), 129-138 (2005).
- Henriques, T. A., Huang, J., D'Souza, S. S., Daugherty, A., Cassis, L. A. Orchidectomy, but not ovariectomy, regulates angiotensin II-induced vascular diseases in apolipoprotein E-deficient mice. Endocrinology. 145 (8), 3866-3872 (2004).
- Daugherty, A., Manning, M. W., Cassis, L. A. Antagonism of AT2 receptors augments angiotensin II-induced abdominal aortic aneurysms and atherosclerosis. Br J Pharmacol. 134 (4), 865-870 (2001).
- Wang, S., et al. Deficiency of receptor-associated protein attenuates angiotensin II-induced atherosclerosis in hypercholesterolemic mice without influencing abdominal aortic aneurysms. Atherosclerosis. 220 (2), 375-380 (2011).
- Daugherty, A., Rateri, D., Lu, H., Balakrishnan, A. Measuring blood pressure in mice using volume pressure recording, a tail-cuff method. J Vis Exp. (27), e1291(2009).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten