Method Article
Caracterização de subconjuntos de monócitos humanos por sangue total Flow Cytometry Analysis
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Aqui nós apresentamos um protocolo para caracterizar subconjuntos de monócitos por citometria de fluxo de sangue total. Isso inclui como portão os subconjuntos e avaliar sua expressão de marcadores de superfície de estrutura de tópicos e dando um exemplo da avaliação da expressão de marcadores M2 (anti-inflamatório) e M1 (inflamatória).
Resumo
Os monócitos são colaboradores-chave em várias doenças inflamatórias e alterações a estas células, incluindo suas proporções de subconjunto e funções, podem ter significado patológico. Um método ideal para examinar alterações de monócitos é citometria de fluxo de sangue total, como a manipulação mínima de amostras por este método limita a ativação de célula diferente. No entanto, muitas abordagens diferentes são levadas para portão os subconjuntos de monócitos levando a identificação inconsistente de subconjuntos entre estudos. Aqui vamos demonstrar um método usando citometria de fluxo de sangue para identificar e caracterizar os subconjuntos de monócitos humanos (clássicos, intermediários e não-clássica). Descrevem como preparar as amostras de sangue por citometria de fluxo, portão os subconjuntos (certifique-se de células contaminantes foram removidas) e determinar a expressão de subconjunto monócito de marcadores de superfície — neste exemplo M1 e M2 marcadores. Este protocolo pode ser estendido para outros estudos que requerem um método padrão associado para avaliar as proporções do subconjunto de monócitos e expressão de subconjunto monócito de outros marcadores funcionais.
Introdução
Os monócitos são um tipo de glóbulos brancos que desempenham um papel importante na promoção e na resolução de inflamação. Existem três principais subconjuntos de monócitos reconhecidos, clássicos (~ 85%), intermediário (~ 5%) e os monócitos (~ 10%) não-clássica, que se caracterizam pelo seu grau de cluster de diferenciação (CD) 14 e CD16 expressão1. As proporções de subconjuntos de monócito podem ser diferente com a presença da doença, tais como uma maior percentagem de intermediários em vários Estados inflamatórios2,3 incluindo doenças cardiovasculares, onde o nível de intermediários é associados a eventos clínicos4,5. Além disso, em condições de doença, monócitos podem também sofrer alterações funcionais, com muitas mudanças detectáveis por uma diferença no marcador de superfície expressão6,7. Um exemplo é monócito M1-inclinação, um aumento de marcadores associados a macrófagos M1, que tem sido observado em doenças cardiovasculares, diabetes, obesidade e síndrome metabólica7,8,9 , 10.
Apesar da popularidade de citometria de fluxo, para avaliar a função e a proporção de subconjunto de monócitos, há uma variabilidade considerável na preparação da amostra e retenção de subconjunto entre os estudos, o que torna difícil comparar resultados entre tais estudos. Importante, não há consenso na delimitação de subconjuntos de monócitos, ainda uma abordagem padronizada é essencial dada a significância clínica das alterações nas proporções de subconjunto em várias doenças. Parte da dificuldade em gating surge do fato de que os monócitos diferenciarem o clássico através do intermediário para o subconjunto não-clássica11 e como tal, os monócitos existirem como um espectro contínuo em vez de populações distintas12 . Curiosamente, Zawada et al mostrou que usando qualquer um Retangular ou trapezoidal gating do subconjunto intermediário, resultou em um subconjunto de intermediário superior que previu um ponto de extremidade cardiovascular13. Isto ressalta que, pelo menos para o cálculo de proporções, a questão-chave está aplicando uma estratégia associada consistente entre amostras diferentes (e estudos), em vez de tentar definitivamente discriminar entre subconjuntos. Enquanto gating definitivo pode ser mais importante ao avaliar a função, a mudança na expressão de marcador entre subconjuntos é incremental12,14, e assim novamente, consistência em gating é talvez chave. Como tal, um objectivo gating método que reproducibly rateia os subconjuntos de monócitos entre diferentes amostras é necessária. O objetivo do método aqui apresentado é portão subconjuntos de monócitos com uma explicação clara e justificação para a técnica associada empregadas e avaliar os subconjuntos para expressão do marcador de superfície, proporcionando assim um método que permite aos investigadores têm confiança na utilização desta técnica ao avaliar amostras diferentes.
Protocolo
Este estudo foi aprovado pelo Comitê de ética em pesquisa humana WSLHD (HREC) (aprovação AU RED HREC/15/WMEAD/289).
1. amostra preparação para citometria de fluxo de sangue total
Nota: Como o sangue humano é potencialmente infeccioso, a afinação de amostra deve ser realizada em uma capa de risco biológico.
- Colete as amostras de sangue dos participantes dentro dos tubos de 3ml etileno diamina tetra acético (EDTA).
- Determine a contagem de glóbulos brancos (WBC) usando um analisador de Hematologia ou hemocytometer.
- Diluído com solução salina tamponada fosfato (PBS) (pH ~ 7,4) para ajustar a concentração de ~ 5 x 106 WBC/mL.
- Preparar a mistura de mestre suficiente para o número de tubos (por exemplo, para tubos de 14, prepare-se 16 x mestre mistura) através da combinação de volumes de 50 sangue µ l, 0,75 µ l anti CD14-V450, 0,5 µ l de anti CD16-APC e 0,625 µ l de 16x anti-HLA-DR-PerCP. Vórtice e pipeta 51.9 µ l da mistura em cada tubo (tabela 1).
Nota: Anticorpos devem ser titulados para determinar concentrações de coloração ideais para os anticorpos fluorescentes usados. - Adicionar marcador de superfície (M1 e M2 ou do isotipo controle, ficoeritrina (PE) rotulada) anticorpos (exemplo conforme tabela 2) e PE rotulagem de marcadores de células T (CD3), células B (CD19), neutrófilos (CD66b), e assassinas naturais (NK) cells (CD56) (tabela 3). Vórtice e incube por 30 min, 4 ° C, no escuro.
Nota: Marcadores de células NK, neutrófilos e linfócitos são incluídos apenas para a validação do método associada. - Adicionar 250 µ l de solução de fixação combinada glóbulo vermelho lise/WBC, vórtice suavemente imediatamente e incubar durante 10 min no escuro a 4 ° C.
- Adicione 250 µ l de PBS e girar as células para baixo em 260 x g durante 10 minutos à temperatura ambiente.
- Remover o sobrenadante, re-suspender as células em 300 µ l de 1% de formaldeído.
Nota: O formol é tóxico. Use luvas de nitrilo e na coifa. - Armazenar a 4 ° C, protegido da luz, até que a análise é executada.
Nota: Análise de fluxo é recomendada para ser feito no prazo de 48 h de preparação da amostra.
2. fluxo Cytometry
- Verifique log de citômetro de fluxo para assegurar pessoal facilidade realizaram verificações de controle de qualidade.
Nota: Para assegurar a coerência entre as análises, instrumento de controle de qualidade e manutenção consistente as intensidades de fluorescência de destino usando contas de controle são recomendadas. - Para definir a experiência de citometria de fluxo, clique em "novo experimento então"novo modelo"e"novo tubo"para adicionar os tubos. Selecione bivariadas parcelas clicando no ícone e use os menus suspensos para selecionar os parâmetros de eixo. Assegurar a inclusão de uma trama CD16/CD14 e um enredo exibindo um detector juntamente com tempo para monitorar a aquisição.
- Insira o tubo e clique em "Adquirir". Verifique as configurações de tensão do instrumento assegurando que o detector de sinais não estão fora de escala.
- Observe células caindo no portão da trama CD14/CD16 monócito. Definir limite de gravação de 5.000 eventos para o portão de monócitos clássica e clique em "Record".
- Continue a gravar dados para os tubos restantes. Depois gravou dados para todos os tubos, exporte dados de fluxo como arquivos de .fcs para análise.
Nota: Para assegurar a precisão, controles de compensação de cor única devem ser registadas. Uma matriz de compensação pode ser calculado e aplicado aos dados antes da análise para contabilizar espectral derramamento sobre15,16.
3. monócito Gating
- Abrir arquivos do software de análise. Duplo clique o nome de tubo e parâmetros selecionados os menus suspensos para visualizar as células em uma área de dispersão frente FSC (A) / encaminhar altura FSC(H) de dispersão. Crie um portal de exclusão dubleto clicando no ícone de ferramenta polígono portão e encerram as células como em (figura 1A).
- Selecione as células gated (clicando duas vezes sobre a região fechada) e no display novo caixa ajustar dropdown menu parâmetros para exibir as células em um FSC (A) / plotagem de dispersão lateral SSC(A). Clique no ícone do portão retangular e selecione generosamente a população de monócitos com base nas propriedades de dispersão para a frente e lateral para excluir a maioria dos linfócitos, células NK e granulócitos (figura 1B).
- Selecione as células fechadas e exibir em um terreno de CD14/CD16, selecionando os parâmetros usando os menus dropdown. Clique sobre o portão de polígono para selecionar os monócitos com base na sua forma característica "┐" (Figura 1).
- Selecione as células fechadas e exibir os monócitos em um terreno de CD16/HLA-DR, usando os menus suspensos para selecionar os parâmetros. Clique sobre o portão de polígono para selecionar as células positivas de HLA-DR e excluir qualquer restantes NK células e neutrófilos17 (Figura 1).
- Selecione as células fechadas e exibir as células positivas de HLA-DR em um terreno de CD14/HLA-DR usando menus suspensos para selecionar os parâmetros. Clique sobre o portão de polígono e desenhe um portão para excluir as células de baixa alta/CD14 em HLA-DR (B células expressam altos níveis de HLA-DR, mas não CD14) (Figura 1E).
Nota: célula B contaminação pode ocorrer e, portanto, deve ser investigada. Se a população não-clássica em Figura 1 não seja distinta as células à sua esquerda, em seguida, contaminação é provável. Passo 3.5 pode ser ignorado se células B não se sobrepõem com os monócitos não-clássica. - Selecione as células fechadas e usar os menus suspensos para exibi-las em um terreno de CD16/CD14. Selecione opções de enredo "Trama de Zebra", que permitirá portões de subconjunto de monócitos ser desenhada para determinar proporções de subconjunto (Figura 1F).
Nota: se trama zebra está disponível sobre o software de análise, pseudo cor (suave) ou trama do contorno pode ser adequada. - Clique no ícone do portão retangular e selecione os monócitos clássicos desenhando um portão retangular aproximado em torno da população de alta/CD16 baixo, clássico monócitos CD14. Em "Exibir", selecione "Mostrar medianas" para exibir a intensidade de fluorescência mediana para monócitos clássicas. Ajuste o portão, tal que a população tem uma distribuição igual de mediana à esquerda e à direita englobando todas as células para a esquerda.
- Selecione a população intermediária desenhando um portão retangular que engloba as células à direita do portão clássica. Ajustar a parte inferior da porta para excluir as células não-clássica, alinhando o portão com a parte inferior dos círculos concêntricos que estão completamente dentro do portão de monócitos clássica, que garante que o subconjunto intermediário tem uma expressão CD14 comparável do principal clássica população consistente com a nomenclatura atual.
- Portão do subconjunto não-clássica desenhando uma caixa retangular da borda inferior do subconjunto intermediário, selecionar todas as células para o fundo da população (Figura 1F).
- Em "Exibir", selecione "Mostrar as frequências do portão" para determinar a porcentagem de cada subconjunto de monócitos.
4. validação de método de Gating
- Para determinar se os tipos de células potencialmente contaminante são efetivamente fechado-para fora, primeiro identificar populações de diferentes células com anticorpos contra células T (CD3), células B (CD19), neutrófilos (CD66b) e células NK (CD56) (Figura 2).
Nota: Aqui T células e neutrófilos não se sentam perto a forma de "┐" de monócitos e estão fechados fora na Figura 1. - Confirme que as células NK são removidas na etapa 3.4 (Figura 1), e as células B são removidas na etapa 3.5 (Figura 1E) conforme mostrado na Figura 3. Se as células NK, ou células B não condomínio fechado-para fora, re-ajuste os portões.
5. fenotípica monócito marcador expressão
- Selecione as células de cada subconjunto de monócitos. Altere parâmetros de dropdown para criar um histograma para cada subconjunto de monócitos (Figura 1F) exibindo cada marcador e seu isotipo correspondente (Figura 4).
- Calcule o grau de expressão de cada marcador (mediana ou média geométrica) em comparação com o respectivos isotipo controle.
Resultados
A estratégia associada de monócitos e análise cytometry fluxo usado aqui (Figura 1) com êxito gated os subconjuntos de monócitos e revelaram suas proporções relativas. As proporções (para este exemplo) foram calculadas como 88,1% Então, 4.33% intermediários e não-7.49% então. Estes portões de subconjunto não estavam contaminados com as células B, células T, os neutrófilos ou células NK, que foi confirmado com marcadores CD19, CD3, CD56 e CD66b, respectivamente. Avaliando a posição relativa de outras populações, é evidente que as células T e neutrófilos cair fora da forma de monócitos "┐" em um terreno de CD16/CD14 (Figura 2A e 2D). No entanto, tanto a populações de células B e células NK em compromisso com a população de monócitos não-clássica (Figura 2B e 2C). As etapas da estratégia associada (Figura 1 e 1E) foram confirmadas para excluir as células NK (Figura 3A) e células B (Figura 3B). Embora a população de células B incluia uma pequena porção de monócitos não-clássica, a quantidade era insignificante.
Tendo fechado os subconjuntos, o grau a que expressaram diferentes marcadores de superfície, M1 (CD64, CD86 e CD120b) e M2 (CD163, CD11b e CD93) foi avaliada. Os marcadores mostraram expressão positiva em comparação com seus controles de isotipo correspondentes, como visto pela mudança de histogramas (Figura 4). A mediana dos marcadores foi maior do que os controles do isotipo.
A aplicação desta estratégia associada a uma amostra de sangue, que foi dividida em quatro tubos, manchado e analisados separadamente, produz resultados comparáveis entre os tubos (tabela 4).
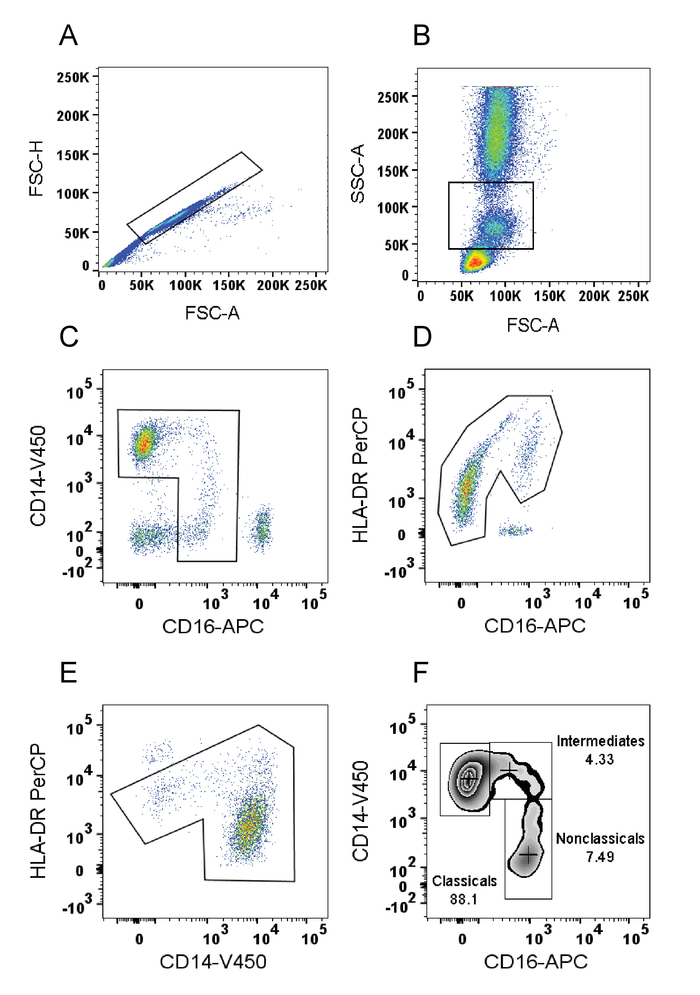
Figura 1: representante monócito gating estratégia em sangue humano total. (A) FSC(A) vs. FSC(H) Sinopse: Gating as células que têm uma área igual e altura, eliminando assim os aglomerados (FSC(A) maior em relação ao FSC(H)) e detritos (FSC muito baixa) K = 1000. (B) FSC(A) vs. SSC(A) Sinopse: ampla seleção de monócitos com base nas suas propriedades SSC/FSC. (C) CD16 vs CD14 Sinopse: Gating para selecionar os monócitos com base na sua forma característica "┐". (D) CD16 vs HLA-DR Sinopse: associada ao selecionar células positivas de HLA-DR e remover as células NK. (E) CD14 vs HLA-DR: associada para excluir as células B (HLA-DR CD14 de alta/baixa) os monócitos. (F) selecionado monócitos reexibidos na CD16 vs CD14 trama para portão os subconjuntos de monócitos. Para A F cor representa a densidade celular com azul e verde, indicando baixa densidade, vermelho e laranja indicando high-density e laranja indicando a densidade do mid-range. Clique aqui para ver uma versão maior desta figura.
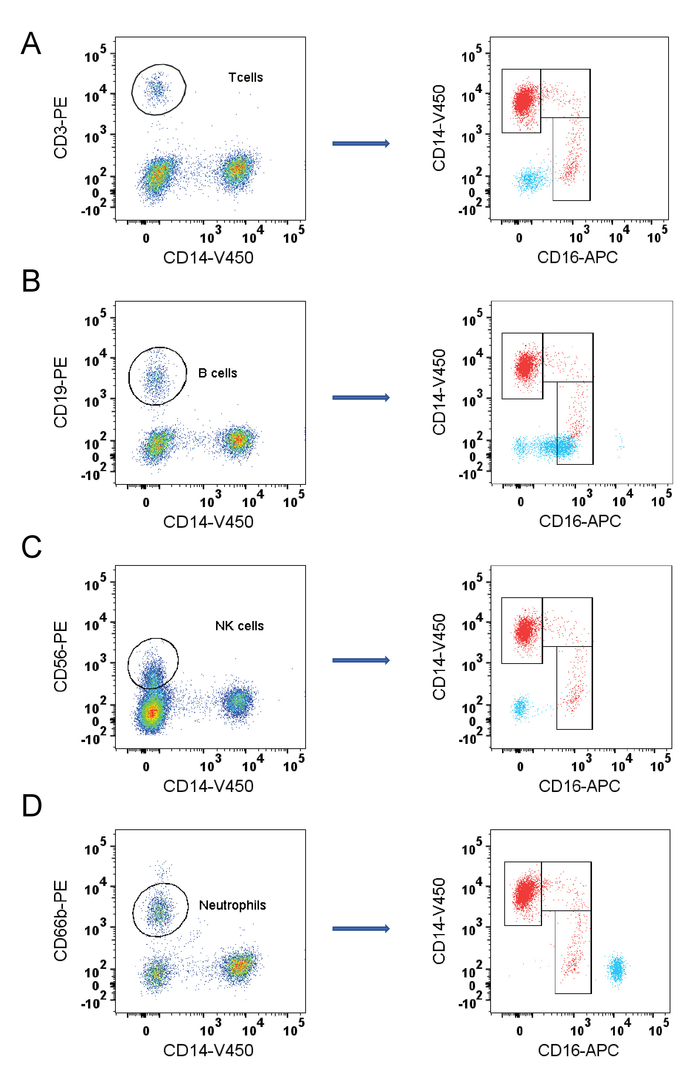
Figura 2: validação de gating estratégia por identificação de potencialmente contaminar células. Células potencialmente contaminantes são identificadas por marcadores células (A) T (CD3), células (B), B (CD19), células (C) NK (CD56) e (D) neutrófilos (CD66b). Os painéis do lado esquerdo mostram a identificação de cada população após gating conforme figura 1A e 1B, com a cor que representa a densidade celular de alta (vermelho) para baixo (azul). Os painéis do lado direito mostram cada população celular (azul) sobreposta sobre a trama de CD16/CD14 monócito final para revelar a proximidade dessas populações de monócitos (vermelhos). Clique aqui para ver uma versão maior desta figura.
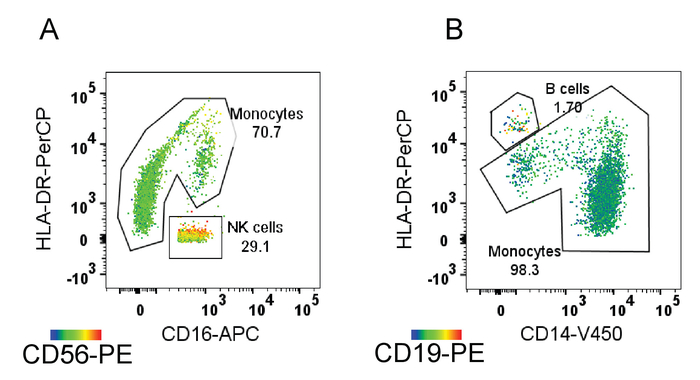
Figura 3: confirmação que passos associados remover células contaminantes. Calor mapas mostrando o grau de expressão de alta (vermelho) para baixo (azul) de CD56 (A) e (B) CD19. Etapas associadas com êxito excluem células com alta CD56 (células NK) e alta CD19 (células B). Clique aqui para ver uma versão maior desta figura.
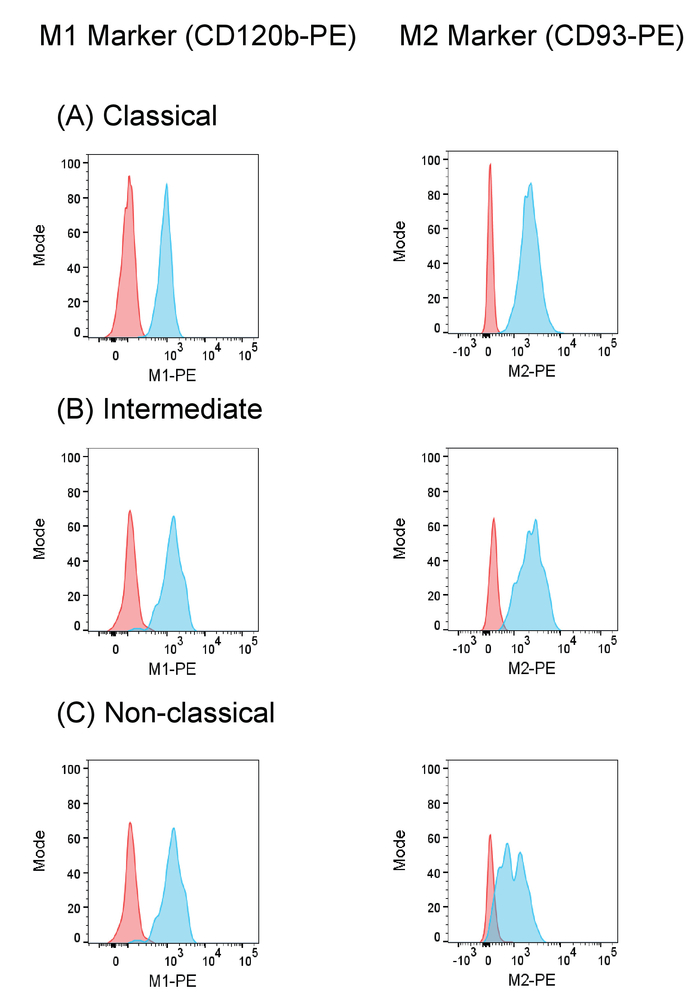
Figura 4: expressão de monócitos da M1 (CD120b) e M2 (CD93) marcadores. Alisado histogramas de monócitos M1 e M2 marcador expressão (azul), mostrando a clara mudança do isotipo (vermelho) para (A) Então, intermediários (B) e (C) não-então. Clique aqui para ver uma versão maior desta figura.
| Anticorpo | Volume (sangue de 50 µ l) | Sangue de 800 µ l de volume (16x) |
| CD14 - V450 | 0,75 Μ l | 12 Μ l |
| CD16 - APC | 0,5 Μ l | 8 Μ l |
| HLA-DR-PerCP | 0,625 Μ l | 10 Μ l |
Tabela 1: Anticorpos para o fluxo de sangue total e mistura de mestre.
| Tubo | Anticorpos de PE | Código | Isotipo do jogo | Concentração das ações | Volume de trabalho |
| 1 | IgG1 | BD (555749) | AT | 1,0 µ l µ g/20 | 0,625 Μ l |
| 2 | CD163 | BD (556018) | IgG1 BD | 0.125 µ l µ g/20 | 5 Μ l |
| 3 | CD64 | BD (558592) | IgG1 BD | 0,06 µ g/20µL | 10 Μ l |
| 4 | IgG1 | BD (555749) | AT | 1,0 µ l µ g/20 | 1,25 Μ l |
| 5 | CD86 | BD (555658) | IgG1 BD | 1,0 µ l µ g/20 | 1,25 Μ l |
| 6 | CD11b | BD (561001) | IgG1 BD | 1,0 µ l µ g/20 | 1,25 Μ l |
| 7 | IgG2a | P & D (IC003P) | AT | 25 µ g/mL | 5 Μ l |
| 8 | CD120b (TNFRII) | P & D (FAB226P) | R & D IgG2a | 25 µ g/mL | 5 Μ l |
| 9 | IgG1 | BL (400112) | AT | 0,2 mg/mL | 2,5 Μ l |
| 10 | CD93 | BL (336108) | IgG1 BL | 50 µ g/mL | 1,25 Μ l |
Tabela 2: M1/M2-PE fluorocromo rotulado de anticorpos monoclonais para o fluxo de sangue total.
| Tubo | Anticorpo | Volume de trabalho |
| 11 | CD3 | 5 Μ l |
| 12 | CD19 | 5 Μ l |
| 13 | CD66b | 1,25 Μ l |
| 14 | CD56 | 5 Μ l |
Tabela 3: PE fluorocromo rotulado de anticorpos monoclonais para células NK, neutrófilos e linfócitos (células T, células B).
| Tubo | % De música clássica | % Intermediário | % Não-clássico |
| 1 | 84,3 | 5.11 | 10.1 |
| 2 | 84,2 | 5.05 | 10.5 |
| 3 | 84,3 | 5,03 | 10.7 |
| 4 | 81,6 | 5,03 | 12.1 |
Tabela 4: Proporções de subconjunto de monócitos da amostra de sangue de um manchado e analisados separadamente.
Discussão
Citometria de fluxo de sangue total é uma abordagem ideal para estudar os monócitos, como as células são examinadas em condições perto seu microambiente fisiológica, proporcionando uma visão sobre seu papel na infecção e condições inflamatórias. Além disso, o uso de fresco (ou seja, não transformados) amostras de sangue minimiza as alterações ou transformações de celular que podem ocorrer devido a armazenamento ou manipulação de18,19, tais como aqueles conhecidos que ocorrem com os monócitos congelamento-descongelamento 20. preparação da amostra de prompt é recomendada como alguns marcadores são upregulated se amostras mantidas à temperatura ambiente antes de processamento19. As concentrações ideais de marcadores M1 e M2 foram determinadas por titulação, e isso deve ser feito para qualquer novo anticorpo limitar inespecificas, assegurando que o grau de mudança é devido a expressão do antígeno e não restringido pela falta de anticorpo. A remoção das células vermelhas do sangue e a fixação das células brancas do sangue com a solução de Lise são uma etapa importante no presente protocolo, como a presença de glóbulos vermelhos pode interferir com o fluxo cytometry21,22. Observe que, enquanto algumas soluções de Lise são compatíveis com coloração não-lavagem, populações mais claras são evidentes em nossas mãos quando é usada uma etapa de lavagem.
Configuração correta do citômetro de fluxo também é fundamental quando se compara a expressão de marcadores de monócitos. Recomendamos que os investigadores mantêm intensidades de fluorescência alvo consistente dos grânulos de controle e realizar o controle de qualidade do instrumento deve ser usado para fornecer resultados consistentes através de amostras diferentes executados em dias diferentes. Além disso, o isotipo controles são usados para auxiliar na interpretação de qualquer sinal de fundo específico gerado pela ligação de anticorpo específico. Os monócitos têm altos níveis de receptores de Fc11 e, portanto, são propensos a ligação não-específica. Digno de nota, o nível de ligação não-específica é diferente para os subconjuntos diferentes, e, portanto, o uso de um isotipo controle torna-se importante quando se compara o grau de expressão do marcador entre subconjuntos.
Outro critério importante a ser considerado é as associada etapas empregadas. Alguns estudos sugerem que é crucial para desenhar um portão apertado em torno do monócito população em FSC(A)/SSC(A) trama para se livrar da maioria dos não-monocítica CD16 células positivas23,24,25, mas isso pode levar a perda de alguns os monócitos como células não-monócitos podem sobrepor com monócitos no FSC/SSC parcelas26. Pelo contrário, para excluir outras células do sangue que podem contaminar os monócitos, a inclusão de um terceiro marcador de monócitos além CD14 e CD16, é essencial26,,27. Por esta razão, HLA-DR é usado frequentemente e é ideal como ela não é expressa por NK células ou neutrófilos17,28. Apesar de linfócitos (células B e células T) podem exprimir o HLA-DR, eles diferem de monócitos em relação à expressão de CD14. Enquanto HLA-DR é um marcador de terceiro ideal, CD86 também tem sido recomendada de27,5,29 , mas não foi usada aqui como também é um marcador de M1 e, portanto, o seu grau de expressão nos subconjuntos de monócitos foi avaliada.
Validação da estratégia associada usada é de importância crucial. Enquanto as células NK são conhecidas por se sobrepor com não-Então, se eles não são bloqueados por28, notamos que as células B podem também sobreposição com o não-então (Figura 2B); Se for esse o caso em outros estudos pode depender a escolha de fluorocromo, configuração do instrumento, sensibilidade do detector ou mesmo a condição da doença a ser examinado. Aqui, a sobreposição B células mostrou alta expressão de HLA-DR e não foram bloqueadas fora pela seleção de células positivas de HLA-DR em Figura 1. Pelo contrário, para remover as células B, usamos uma parcela adicional de CD14 / HLA-DR, onde as células B separam a partir de então-não devido à sua maior HLA-DR e baixa expressão de CD14.
Também existem muitas maneiras diferentes em que os portões para os monócitos se foram estabelecidos na literatura; Estes incluem quadrantes (os subconjuntos são separados por marcadores de quadrante) e caixas retangular ou trapezoidal13 (com caixas separadas para cada subconjunto) que além disso diferem em sua colocação delineando onde um subconjunto termina e outra começa. Essas diferenças provavelmente refletem o fato de que os monócitos existem como um continuum de células, diferenciando-se do clássico para não-clássica, em vez de populações claramente distintas. No entanto, porque as variações de técnicas para identificar os subconjuntos próprios podem levar a diferenças nas proporções calculadas monócito subconjunto, torna-se importante que o método associado é razoavelmente objetiva, ao invés de subjetivo, como isso será tornar o método mais robusto e reprodutível. Alguns estudos usam um isotipo controle para CD16 para determinar a fronteira entre o clássico e intermediário subconjuntos30. Por outro lado, para definir a separação entre intermediários e não-Então, foi proposto que a linha de corte pode ser vertical ou oblíqua, com a escolha para os investigadores, a condição de ser deve ser reprodutível, mas um portão retangular tem sido recomendado para facilitar comparações entre estudos13,30,31. Aqui, maior objectividade foi obtida plotando os dados em um terreno de zebra e aplicando regras visuais objetivas, porque parcelas zebra fornecem uma sugestão de visualização adicional através da mistura de gradiente de cor para cada bin igual probabilidade sobre uma parcela de contorno tradicional. A borda direita do subconjunto clássica foi desenhada tal que a população foi distribuída uniformente em torno da mediana da população. A divisão entre os intermediários e não-então também foram padronizada por ter a base de intermediários alinhe com a parte inferior dos círculos concêntricos no seio da população clássica (ou seja, a população intermediária claramente expressa níveis elevados de CD14, conforme a nomenclatura padrão1).
Enquanto alguns estudos têm sugerido o uso de marcadores adicionais, tais como C-C chemokine receptor tipo 2 (CCR2) ou 6-sulfo LacNAc (Slam) para a obtenção de sucesso enumeração de monócitos e revelar sua significância clínica32,33 , em nossas mãos o nível de expressão dos muitos marcadores funcionais de monócitos varia amplamente entre os indivíduos de14. Tal variação pode limitar a utilidade destes marcadores para definir subgrupos com base em sua expressão. Abordagens computacionais automatizadas também têm sido usadas para visualizar e cluster subconjuntos de monócitos, incluindo visual interativo estocástico vizinho incorporação (viSNE), t-distribuído estocástico vizinho incorporação (tSNE) ou progressão de Spanning-tree Análise da densidade-normalizado eventos (SPADE)34,35, que pode fornecer uma representação visual das células baseado no conjunto de vários marcadores usados. Enquanto isto foi mostrado para aumentar a precisão da estratégia associada na classificação de subconjunto de monócitos, é reconhecido que um inconveniente é o número de anticorpos (e canais correspondentes fluoróforo) necessários. Sua utilidade dependerá de perguntas que serão feitas; a complexidade extra não pode ser utilizada, por exemplo, em estudos de enumeração.
Condomínio fechados com nossa técnica de monócitos mostram proporções em consonância com a literatura e a expressão de marcadores de superfície por três subconjuntos pode ser facilmente determinada. Em geral, a técnica e a metodologia explicado aqui fornece um método simples e padronizado de enumerar as proporções de subconjunto de monócitos e avaliar a expressão do marcador de superfície, que pode ser estendida para incluir outros marcadores também, assim validar seus papéis funcionais em várias outras condições.
Divulgações
Os autores não têm nada para divulgar.
Agradecimentos
Citometria de fluxo foi realizada na instalação de núcleo de citometria de fluxo que é suportado pelo Instituto de pesquisa, Westmead Hub, câncer Instituto de pesquisa médica de New South Wales e nacional de saúde e Conselho de pesquisa médica de Westmead. Este estudo foi suportado pelo fundo de educação e pesquisa de química clínica.
Materiais
| Name | Company | Catalog Number | Comments |
| BD vacutainer blood collection set | Becton Dickinson | 367286 | |
| BD vacuitainer K2E 5.5 mg plus blood collection tubes -3.0 ml | Becton Dickinson | 7128959 | |
| Phospahate Buffered Saline (PBS) | Lonza | 17-516F | |
| 5ml polystyrene round bottom FACS tube (12 x 75 mm style) | Invitro technologies | 352054 | |
| V450 Mouse Anti-Human CD14 Antibody [MφP9] | BD Biosciences | 560349 | |
| APC Mouse monoclonal Anti-CD16 Antibody [3G8] | Abcam Australia | ab140477 | |
| Per CP Anti-Human HLA-DR Antibody [L243] | BioLegend | 307628 | |
| PE Mouse IgG1 κ Isotype Control [MOPC-21] | BD Biosciences | 555749 | Lot # 4283901 |
| PE Mouse Anti-Human CD163 Antibody [GHI/61] | BD Biosciences | 556018 | Lot # 2335626 |
| PE Mouse Anti-Human CD64 Antibody [10.1] | BD Biosciences | 558592 | Lot # 36768 |
| PE Mouse Anti-Human CD86 Antibody [2331 (FUN-1)] | BD Biosciences | 555658 | Lot # 3109766 |
| PE Mouse Anti-Human CD11b/Mac-1 Antibody [ ICRF44] | BD Biosciences | 561001 | Lot # 3228959 |
| PE Mouse IgG2A Isotype control [20102] | R&D Systems | IC003P | Lot # 1212031 |
| PE Human TNF RII/TNFRSF1B Antibody [22235] | R&D Systems | FAB226P | Lot # 612051 |
| PE Mouse IgG1, κ Isotype Control [MOPC-21] | BioLegend | 400112 | Lot # B220359 |
| PE Anti-human CD93 Antibody [VIMD2] | BioLegend | 336107 | Lot # B143544 |
| PE Mouse Anti-Human CD3 Antibody [SK7] | BD Biosciences | 347347 | Lot # 3010929 |
| PE Mouse Anti-Human CD19 Antibody [HIB19] | BD Biosciences | 561741 | Lot # 2307721 |
| PE Mouse Anti-Human CD56 Antibody [B159] | BD Biosciences | 561903 | Lot # 3011796 |
| PE Anti-human CD66b Antibody [G10F5] | BioLegend | 305105 | Lot # B154037 |
| OptiLyse C | Beckman Coulter | A11895 | |
| Formaldehyde solution 37% | Sigma | F1635 | |
| BD FACSCanto II Flow Cytometer | BD Biosciences | ||
| Automatic haematology analyser, XT-1800i | Sysmex | ||
| Centrifuge GS-6R | Beckman | ||
| Flowjo software v10.0.7 | Tree Star Inc |
Referências
- Ziegler-Heitbrock, L., et al. Nomenclature of monocytes and dendritic cells in blood. Blood. 116 (16), e74-e80 (2010).
- Rossol, M., Kraus, S., Pierer, M., Baerwald, C., Wagner, U. The CD14(bright) CD16+ monocyte subset is expanded in rheumatoid arthritis and promotes expansion of the Th17 cell population. Arthritis & Rheumatism. 64 (3), 671-677 (2012).
- Wildgruber, M., et al. The "Intermediate" CD14++CD16+ monocyte subset increases in severe peripheral artery disease in humans. Scientific Reports. 6, 39483 (2016).
- Heine, G. H., et al. Monocyte subpopulations and cardiovascular risk in chronic kidney disease. Nature Review Nephrology. 8 (6), 362-369 (2012).
- Rogacev, K. S., et al. CD14++CD16+ monocytes independently predict cardiovascular events: a cohort study of 951 patients referred for elective coronary angiography. Journal of the American College of Cardiology. 60 (16), 1512-1520 (2012).
- Bories, G., et al. Impaired alternative macrophage differentiation of peripheral blood mononuclear cells from obese subjects. Diabetes and Vascular Disease Research. 9 (3), 189-195 (2012).
- Fadini, G. P., et al. An unbalanced monocyte polarisation in peripheral blood and bone marrow of patients with type 2 diabetes has an impact on microangiopathy. Diabetologia. 56 (8), 1856-1866 (2013).
- Satoh, N., et al. Unbalanced M1/M2 phenotype of peripheral blood monocytes in obese diabetic patients: effect of pioglitazone. Diabetes Care. 33 (1), 7 (2010).
- Chen, X., Devaraj, S. Monocytes from metabolic syndrome subjects exhibit a proinflammatory M1 phenotype. Metabolic Syndrome and Related Disorders. 12 (7), 362-366 (2014).
- Williams, H., et al. Human classical monocytes display unbalanced M1/M2 phenotype with increased atherosclerotic risk and presence of disease. International Angiology. 36 (2), 145-155 (2017).
- Wong, K. L., et al. Gene expression profiling reveals the defining features of the classical, intermediate, and nonclassical human monocyte subsets. Blood. 118 (5), e16-e31 (2011).
- Hijdra, D., Vorselaars, A. D., Grutters, J. C., Claessen, A. M., Rijkers, G. T. Phenotypic characterization of human intermediate monocytes. Frontiers in Immunology. 4, 339 (2013).
- Zawada, A. M., et al. Comparison of two different strategies for human monocyte subsets gating within the large-scale prospective CARE FOR HOMe Study. Cytometry Part A. 87 (8), 750-758 (2015).
- Patel, V. K., Williams, H., Li, S. C. H., Fletcher, J. P., Medbury, H. J. Monocyte inflammatory profile is specific for individuals and associated with altered blood lipid levels. Atherosclerosis. 263, 15-23 (2017).
- Bayer, J., Grunwald, D., Lambert, C., Mayol, J. F., Maynadie, M. Thematic workshop on fluorescence compensation settings in multicolor flow cytometry. Cytometry Part B: Clinical Cytometry. 72 (1), 8-13 (2007).
- Szaloki, G., Goda, K. Compensation in multicolor flow cytometry. Cytometry Part A. 87 (11), 982-985 (2015).
- Abeles, R. D., et al. CD14, CD16 and HLA-DR reliably identifies human monocytes and their subsets in the context of pathologically reduced HLA-DR expression by CD14(hi) /CD16(neg) monocytes: Expansion of CD14(hi) /CD16(pos) and contraction of CD14(lo) /CD16(pos) monocytes in acute liver failure. Cytometry Part A. 81 (10), 823-834 (2012).
- Mukherjee, R., et al. Non-Classical monocytes display inflammatory features: Validation in Sepsis and Systemic Lupus Erythematous. Scientific Reports. 5, 13886 (2015).
- Lundahl, J., Halldén, G., Hallgren, M., Sköld, C. M., Hed, J. Altered expression of CD11b/CD18 and CD62L on human monocytes after cell preparation procedures. Journal of Immunological Methods. 180 (1), 93-100 (1995).
- Appleby, L. J., et al. Sources of heterogeneity in human monocyte subsets. Immunology Letters. 152 (1), 32-41 (2013).
- Dagur, P. K., McCoy, J. P., Robinson, J. P., et al. Collection, Storage, and Preparation of Human Blood Cells. Current protocols in cytometry. 73, (2015).
- Einwallner, E., et al. Lysis matters: Red cell lysis with FACS Lyse affects the flow cytometric enumeration of circulating leukemic blasts. Journal of Immunological Methods. 390 (1), 127-132 (2013).
- Tsujioka, H., et al. Impact of Heterogeneity of Human Peripheral Blood Monocyte Subsets on Myocardial Salvage in Patients With Primary Acute Myocardial Infarction. Journal of the American College of Cardiology. 54 (2), 130-138 (2009).
- Autissier, P., Soulas, C., Burdo, T. H., Williams, K. C. Immunophenotyping of lymphocyte, monocyte and dendritic cell subsets in normal rhesus macaques by 12-color flow cytometry: Clarification on DC heterogeneity. Journal of Immunological Methods. 360 (1), 119-128 (2010).
- Hristov, M., Schmitz, S., Nauwelaers, F., Weber, C. A flow cytometric protocol for enumeration of endothelial progenitor cells and monocyte subsets in human blood. Journal of Immunological Methods. 381 (1-2), 9-13 (2012).
- Zawada, A. M., et al. Monocyte heterogeneity in human cardiovascular disease. Immunobiology. 217 (12), 1273-1284 (2012).
- Zawada, A. M., et al. SuperSAGE evidence for CD14++CD16+ monocytes as a third monocyte subset. Blood. 118 (12), e50-e61 (2011).
- Heimbeck, I., et al. Standardized single-platform assay for human monocyte subpopulations: Lower CD14+CD16++ monocytes in females. Cytometry Part A. 77 (9), 823-830 (2010).
- Rogacev, K. S., et al. Monocyte heterogeneity in obesity and subclinical atherosclerosis. European Heart Journal. 31 (3), 369-376 (2010).
- Ziegler-Heitbrock, L., Hofer, T. P. J. Toward a Refined Definition of Monocyte Subsets. Frontiers in Immunology. 4, 23 (2013).
- Weber, C., et al. Role and analysis of monocyte subsets in cardiovascular disease. Joint consensus document of the European Society of Cardiology (ESC) Working Groups "Atherosclerosis & Vascular Biology" and "Thrombosis". Thromb Haemost. 116 (4), 626-637 (2016).
- Shantsila, E., et al. Immunophenotypic characterization of human monocyte subsets: possible implications for cardiovascular disease pathophysiology. Journal of Thrombosis and Haemostasis. 9 (5), 1056-1066 (2011).
- Hofer, T. P., et al. slan-defined subsets of CD16-positive monocytes: impact of granulomatous inflammation and M-CSF receptor mutation. Blood. 126 (24), 2601-2610 (2015).
- Qiu, P., et al. Extracting a cellular hierarchy from high-dimensional cytometry data with SPADE. Nature Biotechnology. 29, 886 (2011).
- Thomas, G. D., et al. Human Blood Monocyte Subsets: A New Gating Strategy Defined Using Cell Surface Markers Identified by Mass Cytometry. Arteriosclerosis, Thrombosis, and Vascular Biology. 37 (8), 1548-1558 (2017).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados