Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Поколение и количественная характеристика функциональных и поляризованных желчных эпителиальных кист
В этой статье
Резюме
Трехмерные (3D) клеточные системы являются актуальными моделями для изучения органогенеза. Предлагается метод на основе гидрогеля для производства желчных кист и их характеристики. Этот протокол распутывает барьеры 3D-характеристики, с помощью простого и надежного метода оценки эффективности образования кисты, размеров и проверки их функциональности.
Аннотация
Холангиоциты, эпителиальные клетки, которые выстраиваются желчных протоков в печени, контролировать образование желчи и модификации. В последние двадцать лет, в контексте заболеваний печени, 3-мерные (3D) модели на основе холангиоцитов появились такие как кисты, сфероиды, или трубчатые структуры для имитации топологии тканей для органогенеза, моделирования заболеваний, и исследования скрининга наркотиков. Эти структуры были в основном получены путем встраивания холангиоцитов в гидрогель. Основная цель состояла в изучении самоорганизации путем устранения эпителиальной полярности, функциональных и морфологических свойств. Тем не менее, очень немногие исследования сосредоточены на эффективности формирования кисты. В этом случае эффективность часто измеряется на основе изображений одной плоскости. Функциональные анализы и структурный анализ проводятся без представления потенциальной неоднородности распределения кисты, возникающей в результате гидрогелевой полимеризации неоднородности и побочных эффектов. Поэтому количественный анализ, когда он проводится, не может использоваться для сравнения с одной статьей на другую. Кроме того, эта методология не позволяет сравнивать 3D потенциал роста различных матриц и типов клеток. Кроме того, нет никакого упоминания об экспериментальном устранении неполадок для иммуностимуляторных кист. В этой статье мы предоставляем надежный и универсальный метод, чтобы показать, что первоначальное распределение клеток связано с неоднородным вертикальным распределением образования кисты. Клетки холангиоцитов, встроенные в гидрогель, следуют с анализом стеков вдоль глубины гидрогеля в течение 10 дней. С помощью этого метода, надежная кинета эффективность образования кисты и роста получается. Мы также представляем методы оценки полярности кисты и секретоорийной функции. Наконец, дополнительные советы по оптимизации иммуностимуляторов предоставляются для того, чтобы ограничить кист коллапс для визуализации. Этот подход может быть применен к другим исследованиям культуры 3D клеток, открывая тем самым возможности для сравнения одной системы с другой.
Введение
За последние три десятилетия область исследований in vitro продвинулась к системам 3D-культуры. Ряд протоколов появились для культивирования клеток в 3D как сфероиды или агрегаты в присутствии или отсутствии эшафота / матрицы, в капле, в агитации, в микрофлюидных устройств, илиплавающей 1. Использование методов 3D культуры доказало свои преимущества перед 2-мерными (2D) культурами, особенно для эпителиальных клеток, которые были показаны для самоостроения в 3D структурах, называемых кистами или acini. В этом случае клетки образуют монослой, окружающий люмен, где клетки приобретают свой полный эпителиальный фенотип с улучшенными физиологическими специфическимифункциями 2.
Многочисленные исследования способствовали разработке методов формирования этих эпителиальных органоидов в естественных матрицах. Это позволило резюмировать взаимодействия виво-клеток и клеточной микроэнвиронности, получить установление и стабильность эпителиального фенотипа3,4,5,6,7. В последнее время, и в частности, с целью разработки трансплантируемых органоидов и расшифровки потребности микроокноронии для организации эпителиальной программы, синтетические гидрогели были разработаны для повышения образования эпителиальных acini8,9,10. К сожалению, эти исследования сообщают о качественных данных, или представить методы расчета с использованием внутренних ссылок, таких как соотношение кист над не-кисты в 2Dплоскости 8,9,10. Это исключает любое сравнение между различными исследованиями с точки зрения эффективности, стабильности или морфологической и физиологической характеристики эпителиальных органоидов.
Микронапсуляция эпителиальных клеток в бисере с использованием микрофлюидных устройств позволила более реалистичные количественные и сравнительные результаты. Используя эту технологию, органоиды из различных типов клеток были сформированы и дифференцированы на основе морфологии между различными 3Dклеточными структурами 11,12. Тем не менее, эта технология не проста в работе и требует использования чистых помещений для производства микрофлюидных устройств. Эта технология была создана для нескольких типов гидрогеля, но требует технической адаптации, которая будет применяться к другим гидрогелям, ограничивая ее универсальность. Таким образом, большинство исследований, направленных на разработку эпителиальных органоидов полагаться на встраивание эпителиальных клеток в гидрогель навалом. В этих методах часто пренебрегают высокой неоднородностью структурирования геля и распределения клеток внутри всей 3D-культуры. Таким образом, большинство анализов относятся к одним 2D-изображениям, которые представляют собой лишь очень грубое распределение различных клеточных объектов во всем 3D томе.
Заболевания, которые влияют на желчные протоки, такие как холангиокарцинома, желчные атрезии, первичный склерозирующий холангит, среди прочего, являются основной причиной смертности и заболеваемости. За исключением трансплантации печени, Нет эффективных методов лечения этих условий13. Усилия по расследованию образования желчных протоков, причин заболеваний и прогрессирования позволят разработать новые методылечения 14.
Билиарные органотипические модели кист, сфероидов или трубчатых структур с использованием нормальных или полученных пациентом, дифференцированных или прародителя полученных холангиоцитовклеточных линий были разработаны 15,16,17,18,19,20. Различные исследования повторили полярность холангиоцитов, экспрессию маркеров холангиоцитов, наличие ресничок, секретореторию холангиоцитов и реабсорбтивную способность, а также образование и обструкцию люмена; все из которых представляют собой важные характеристики фенотипа холангиоцитов,морфологии, и функции 15,17,19. Другие сообщили о поддержании пациентов полученных желчных органоидов в течение длительных периодоввремени 20. Недавно мы исследовали роль биохимических и биофизических сигналов на желчных кист органогенеза21. Важно отметить, что патогенез желчных атрезия была изучена в желчных сфероидов и труб7,22. Кроме того, были успешно изучены ключевые особенности первичного склерозирующий холангит, такие как холангиоциты, секреция провоспалительных цитокинов, а также набор макрофагов с использованием желчныхсфероидов 15,20. Тем не менее, воспроизводимые в пробирке 3D количественные модели, которые физиологически модулировать фенотип холангиоцитов, физиологии и микроокниронии, где эти вопросы могут быть решены по-прежнему необходимы. Кроме того, лишь немногие публикации сообщили эффективность формированиякисты 21,23. Это важный момент, чтобы установить, особенно при исследовании органогенеза, причины заболеваний, и корреляция реакции препарата с функцией холангиоцитов и поляризации. Кроме того, с различиями в эшафот / матрица используется от протокола к протоколу, трудно сравнить между системами. Для решения этих вопросов мы предлагаем количественный, надежный и универсальный метод генерации желчных кист, имитирующих образование люменов, поляризацию холангиоцитов и секреторный функцию холангиоцитов. Важно отметить, что мы представляем систематический анализ, проведенный по оси З по 3D-гелю при оценке с течением времени, эффективности образования кисты, размера, жизнеспособности, поляризации и функциональности. Кроме того, мы использовали естественный гидрогель и нормальные крысиные холангиоциты (NRC) в качестве примера для протокола, но другие природные или синтетические гидрогели, а также эпителиальные клетки могут быть использованы для формирования 3D кистозных структур.
протокол
1. Поколение кист
ПРИМЕЧАНИЕ: Этот протокол может быть выполнен с любым типом гидрогеля, если гелеобразование позволяет встраивание клеток.
- Гидрогель покрытие
ПРИМЕЧАНИЕ: Правильное гидрогельное покрытие камерного слайда является критическим шагом, чтобы избежать образования 2D-клеточных слоев на дне хорошо, что может помешать последующей визуализации кисты и ухудшить расчет эффективности образования кисты.- Чтобы обеспечить однородность раствора геля, оттаивать гидрогель при 4 градусов по Цельсию в одночасье (O/N).
- Предустановка пипетки советы на льду или O / N при -20 градусов по Цельсию и 8-хорошо камеры слайд на -20 градусов по Цельсию O / N.
- Поместите гидрогель и 8-хорошо камерную горку на ведро со льдом, наполненное льдом.
- В конической трубке 15 мл приготовьте раствор, содержащий 40% гидрогеля (V/V) в холодной полной среде NRC (см. таблицу материалов)и поместите трубку на лед.
- Чтобы покрыть камерный слайд, используя холодные кончики пипетки, добавьте 50 МКЛ раствора гидрогеля по центру каждой хорошо, и распространилась по всей поверхности с помощью наконечника пипетки, удерживая камеру слайд на льду (Рисунок 1A).
ПРИМЕЧАНИЕ: Распространение гидрогеля раствор как можно более равномерно, избегая пузырьков. - Для полимеризации гидрогеля, инкубировать камеру слайд, по крайней мере 15 мин при 37 градусов по Цельсию, 5% CO2.
- Подготовка клеток
- Разогреть NRC полной среды, фосфат буфера солевого раствора (PBS), и трипсин-этилендиамин тетраацевой кислоты (трипсин-ЭДТА) в водяной бане предварительно нагревается до 37 градусов по Цельсию.
- В то время как гидрогель полимеризуется, убедитесь, что NRCs выращиваются до 70% слияния в Т-25см 2 коллагена покрытиемколбы 21. Вымойте клетки один раз с предварительно нагретым 1x PBS.
- Инкубировать NPC с 5 мл предварительно нагретого 1x PBS (для Т-25см 2 колбы) в течение 20 мин при 37 градусов по Цельсию, 5% CO2.
ПРИМЕЧАНИЕ: Этот шаг, который сокращает время инкубации с трипсином-ЭДТА, играет важную роль в сохранении самоорганизовывания свойств клеток. - Откажитесь от PBS, добавьте 1 мл трипсина-ЭДТА и инкубировать в течение 5-10 мин при 37 градусов по Цельсию, 5% CO2.
- Нейтрализовать с помощью 4 мл предварительно нагретой полной среды NRC. Соберите и перенесите подвеску клетки в коническую трубку 15 мл и вращайся при 150 x g в течение 4 мин.
- Откажитесь от среды и повторно посовелайте клеточные гранулы в 5 мл предварительно нагретой среды.
- Используя 40 мкм ситечко клеток, фильтровать клеточный раствор в 50 мл конической трубки и рассчитывать клетки.
ПРИМЕЧАНИЕ: Прохождение клеток через ситечко является критическим шагом для количественных результатов, которые будут воспроизводиться т.е., чтобы получить почти аналогичный размер ячейки агрегатов, которые будут внедрены.
- Встраивание клеточной подвески в гидрогельный раствор
- Подготовка раствора 1600 МКЛ 80% гидрогеля (V/V) в холодной полной среде NRC (трубка 1); держать во льду. Разбавить 5 х10 5 ячеек/мл в 1600 мкл холодной полной среды NRC (трубка 2) и держать во льду.
ПРИМЕЧАНИЕ: Этот шаг должен быть выполнен быстро, чтобы избежать полимеризации гидрогеля при смешивании его с клеточной подвеской и для поддержания жизнеспособности клеток. - Для приготовления раствора посева клеток 2,5 х 105 клеток/мл в 40% гидрогеля (V/V), смешать трубку 1 и трубку 2. Добавьте 400 МКЛ клеточного раствора в каждую колодец слайда камеры с гидрогелем, избегая пузырьков(рисунок 1B).
- Держите слайд камеры в инкубаторе при 37 градусов по Цельсию с 5% CO 2 до техпор, пока средства массовой информации не изменятся.
- После 2 дней в культуре, удалить 250 мкл среды из угла каждого хорошо, будьте осторожны, чтобы не пипетки из гидрогеля. Затем медленно добавьте 250 МКЛ среды культуры. Изменение среды каждые 2 дня.
ПРИМЕЧАНИЕ: Свести к минимуму движение камеры слайд, особенно во время инициации кисты.
- Подготовка раствора 1600 МКЛ 80% гидрогеля (V/V) в холодной полной среде NRC (трубка 1); держать во льду. Разбавить 5 х10 5 ячеек/мл в 1600 мкл холодной полной среды NRC (трубка 2) и держать во льду.
2. Квантификация кисты
- Киста изображения
ПРИМЕЧАНИЕ: Этот раздел должен быть выполнен быстро, чтобы не скомпрометировать жизнеспособность клетки, если микроскоп не оснащен нагревательной камерой для управления CO2 и температурой. Для обеспечения последовательной количественной оценки, репрезентативной распределения кисты в полном объеме гидрогеля, кисты изображения с помощью фазово-контрастной микроскопии и серийной визуализации (З-стеки), с заранее определенными параметрами в разных точках времени.- Возьмите стек вдоль глубины гидрогеля для каждой точки времени(рисунок 1C, D). В этом примере, стеки принимаются в дни 1, 2, 4, 7 и 10.
ПРИМЕЧАНИЕ: Проверьте, что начальное распределение клеток является однородным в гидрогеле, чтобы обеспечить применимость этого метода.- С фазо-контрастным микроскопом, оснащенным программным обеспечением для получения изображений, выберите 10-е объективное увеличение в окне ручной носовойпанели (рисунок 2B(1)).
- Включите белую лампу и выберите опцию изображения яркого поля.
- Включите камеру, выбрав кнопку"Играть"в подмене бара. Сосредоточьтесь на поле кист и установите время экспозиции(рисунок 2B(2)). Откройте окно Auto Capture Folder для автоматической экономии изображений(рисунок 2B(3)).
- Откройте окно захвата серии и определите с помощью винта верхние и нижние плоскости стека (те же координаты XY, но разные экранированные). Отрегулируйте шаг в зависимости от цели, уровня разрешения и нажмите кнопку«Бегите сейчас»,чтобы запустить приобретение(рисунок 2B(4)).
ПРИМЕЧАНИЕ: В этом примере кисты распространяются по толщине гидрогеля 520 мкм. 26 изображений приобретаются вдоль глубины гидрогеля с интервалом в 20 мкм. В зависимости от цели, к-шаг должен быть скорректирован, чтобы не пропустить ни одной кисты и обеспечить обнаружение одиночных клеток и агрегатов. - Возьмите по крайней мере 3 не пересекающихся стеки на колодец.
ПРИМЕЧАНИЕ: Эта выборка необходима, когда, как и в этом примере, кисты более многочисленны в глубине геля, чем по краям из-за неоднородности в гидрогелевой полимеризации. - Для того, чтобы репрезентативный набор данных повторил шаг 2.1.1.5. для 3 скважин в общей сложности.
ПРИМЕЧАНИЕ: Неоднородное распределение кист зависит от типа гидрогеля, его полимеризации и клеточной линии. Учитывая три «стеки на скважину» и три скважины за эксперимент, минимум 200 кист изображены в течение девяти стеков, чтобы охарактеризовать образование кисты и рост кисты в каждый момент времени.
- Возьмите стек вдоль глубины гидрогеля для каждой точки времени(рисунок 1C, D). В этом примере, стеки принимаются в дни 1, 2, 4, 7 и 10.
- Обработка изображений
ПРИМЕЧАНИЕ: В гидрогеле, NRCs можно найти как одиночные клетки, кисты или агрегаты. Кисты идентифицируются наличием круглой и тонкой контрастной клеточной оболочки, прилагая люмен, в то время как клеточные агрегаты представляют нерегулярную форму и не имеют люмена. Агрегаты и одиночные клетки имеют плотный и контрастный вид(рисунок 3B(4)).- Откройте программное обеспечение Фиджи, откройте стек и перейдите в меню Фиджи и нажмите Файл и открыть (Дополнительныйрисунок 1). Выберите стек для анализа. При необходимости выберитеопцию «Виртуальныйстек» инажмите кнопку «Да»дляоткрытия (рисунок 3A(1)).
- Дублировать стек через изображение Дубликат. Нажмите на поле "Дублировать стек" и нажмите "OK" (Дополнительный рисунок 2).
ПРИМЕЧАНИЕ: В этом примере, стеки находятся в формате файла .nd2, закодированном в 16 битах. - Создайте проекцию минимальной интенсивности из дублируемого стека. Перейти к меню Изображения Стеки Проект . Выберите тип проекции" Мин Интенсивность" инажмите" OK " (Рисунок 3A(2)) (Дополнительный рисунок 3).
- Вычесть фон из проекции. Перейти в меню Процесс (ru) Вычесть фон. Тип 500.0 пикселей радиуса подвижного шара и нажмите "световой фон", чтобы сделать кисты более контрастными, чем фон (Рисунок 3A(3)) (Дополнительный рисунок 4).
ПРИМЕЧАНИЕ: Радиус подвижного шара определяет размер области, на которой осуществляется вычитание фона. Этот параметр должен быть установлен размером с самый большой объект для идентификации. - Если требуется повышение контрастности, перейдите в меню Изображения Отрегулируйте Яркость/контрастность Авто Применить. Фиджи автоматически оптимизирует яркость и контрастность. В(рисунок 3A(3)), нижние и верхние серые значения были установлены на 49702 и 65452, соответственно (Дополнительный рисунок 5).
ПРИМЕЧАНИЕ: Если проекция не откалибрована, перейдите в меню Анализ Установите шкалу и ввести соответствующее соотношение калибровки мкм/пиксель(Дополнительная цифра 6).
- Измерение подсчета кисты и размера кисты
- Чтобы измерить приблизительный диаметр кисты, выберите инструмент прямой линии в меню Фиджи и нарисуйте линию по диаметру каждой кисты на окончательнойпроекции (рисунок 3B(4)). Добавьте новую область интереса (ROI), созданную для каждой кисты, менеджеру roi: нажмите наярлык «t»на клавиатуре для более быстрого подсчета и открытия менеджера рентабельности инвестиций. Нажмите" Показать все", чтобы увидеть подсчитанные кисты (Дополнительный рисунок 7)
- Убедитесь, что ни одна киста не осталась без учета, накладав набор ROIs из проекции на стеке. Для этого щелкните окно «К-стек», чтобы выбрать его. В roi Manager нажмите кнопку«Показать все»и переместите курсор вдоль стека, чтобы проверить это изображение на изображение, все кисты были подсчитаны(Дополнительный рисунок 8).
- После того, как новые кисты были подсчитаны и ROIs добавлены на шаг 2.3.1., выберите набор рентабельности инвестиций и сохранить его через окно roi Manager, нажав Подробнее Сохранить (Дополнительный рисунок 9).
- Выберите все ROIs в менеджере рентабельности инвестиций и нажмите" Мера" в ROI Manager, чтобы получить размер каждой кисты. Это откроет новое окно измерений под названием «Результаты»,пронумеровавкаждую кисту и ее предполагаемый размер. Затем сохраните .csv формате, нажав наокно «Результаты»и через меню: Файл Сохранить как (Дополнительный рисунок 10).
ПРИМЕЧАНИЕ: Макрос может быть создан для полуавтоматического процесса стеки, оценка кисты число / размеры из прогнозов, и хранить данные для более быстрой процедуры подсчета. Для этого выберите инструмент«Запись» вменю бара, нажав на плагины Макрос Запись.
- Количественная оценка эффективности образования кисты
- Подсчитайте количество кист в день Y,
 по проекции (Y-1, 2, 4, 7 или 10).
по проекции (Y-1, 2, 4, 7 или 10). - Чтобы рассчитать эффективность образования кисты для 1000 клеток в день Y, разделите количество кист, подсчитанных в тот момент времени, на количество клеток, посеянных в день 0, выведенных из объема гидрогеля, и умножьте на 1000(рисунок 3C, Рисунок 4).
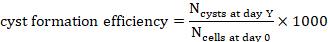
- Подсчитайте количество кист в день Y,
3. Жизнеспособность клеток
- Подготовка запасного раствора флуоресцеина диацетата (FDA) при 5 мг/мл путем растворения 5 мг FDA в 1 мл ацетона и хранить при -20 градусов по Цельсию.
- Приготовьте стоковое раствор йодида пропидия (PI) при концентрации 2 мг/мл в деионизированной воде (dH2O) и храните при 4 градусах Цельсия.
- Подготовка среды NRC без сыворотки теленка плода (FCS).
- Чтобы подготовить решение FDA/PI окрашивания, добавьте 4 МКЛ раствора запасов FDA (8 мкг/мл конечной концентрации) и 25 МКЛ раствора запаса PI (20 мкг/мл конечной концентрации) в 2,5 мл среды NRC без FCS.
- Удалите среду из камерного слайда, добавьте 250 МКЛ раствора окрашивания в каждую колодец и инкубировать 4-5 мин в темноте при 37 градусов по Цельсию, 5% CO2. Pipette из окрашивания раствор тщательно и мыть один раз с 250 йл 1x PBS.
- Аккуратно добавьте 250 МКЛ полной среды NRC к каждой хорошо и сфотографировать с помощью перевернутого флуоресцентного микроскопа с Техас красный и флуоресхейн изотиоцианат (FITC) фильтры. Живые клетки будут зелеными, а мертвые - красными(рисунок 5A).
ПРИМЕЧАНИЕ: Для количественной оценки живых/мертвых клеток, возьмите стеки по всему объему гидрогеля следующим шагом 2 и адаптируйте метод обработки изображений для флуоресценции.
4. Секреция деятельности
ПРИМЕЧАНИЕ: Активность секреции через апикаль мембраны холангиоцитов оценивается секреции флуоресхейна в люмене. Его специфичность может быть оценена путем выполнения того же теста с Verapamil, мульти-лекарственной устойчивостью (MDR) транспортер ингибитор24.
- Чтобы подготовить окрашивающий раствор Hoechst 33258 при 5 мкг/мл, добавьте 0,83 л раствора запаса Hoechst (15 мг/мл концентрации запасов в dH2O) в 2,5 мл среды NRC без FCS.
- Добавьте 250 мкл раствора Hoechst в каждую колодец и инкубировать при 37 градусов по Цельсию, 5% CO2 в течение 15 мин.
- Удалите раствор Hoechst и добавьте 250 мкл раствора FDA (8 мкг/мл окончательной концентрации) в каждой хорошо. Инкубационный 4-5 мин при 37 градусов по Цельсию, 5% CO2.
ПРИМЕЧАНИЕ: Как только клетки подвергаются FDA окрашивания решение, последующей деятельности флуорессейн секреции кинетики может быть полезно для калибровки времени, необходимого для кисты для секретирования. Для этого фотографи сфотографируете каждую минуту в течение 1 ч с помощью изображений замедленного действия. В этом примере время, необходимое для наблюдения NRC секретирования кисты в гидрогеле составляет около 15-20 мин. - Сделайте снимки с помощью перевернутого флуоресцентного микроскопа через 5 минут после полоскания со средой без FCS. Используйте фильтры 4',6-diamidino-2-фенилиндол (DAPI) и FITC, чтобы выявить маркировку ядер и накопление флуоресцеина в люмене(рисунок 6A). Чтобы количественно определить количество секрементных кист, возьмите стеки, как в шаге 2, и адаптируйте шаги обработки изображения к флуоресцентным изображениям.
ПРИМЕЧАНИЕ: Для теста Verapamil, предшествуют предыдущему процессу (шаги 4,3. до 4,4.) инкубации с Verapamil, в соответствии со следующими условиями: - Приготовьте складной раствор 10 мМ Верапамил в диметиловом сульфоксиде (ДМСО). Чтобы подготовить рабочий раствор 10 МКМ, смешайте 2,5 МКЛ раствора акций Verapamil с 2,5 мл среды культуры без FCS.
- Чтобы оценить, что флуоресценция в люмене является результатом секреции MDR, возьмите еще один слайд и добавьте 250 мкл рабочего раствора Verapamil в каждой из колодец и инкубировать 20 мин при 37 градусов по Цельсию, 5% CO2
- Удалите раствор и добавьте в каждую колодец 250 МКЛ раствора FDA (8 мкг/мл конечной концентрации). Инкубировать 4-5 мин в темноте при 37 градусов по Цельсию, 5% CO2. Затем вымойте 250 МКЛ 1x PBS, перед визуализацией(рисунок 6B, C).
5. Эпителиальная оценка полярности по иммунофлюоресценции
- Чтобы подготовить фиксирующий раствор, смешайте 4% формальдегид с 5% сахарозой, в 1x PBS, рН 7.4 и инкубировать в водяной бане, предварительно нагретой при 37 градусах Цельсия.
- Чтобы исправить клетки, аккуратно пипетка из среды культуры из хорошо, не повреждая матрицу. Медленно добавьте 400 мкл фиксируя раствора к стороне скважин. Инкубация в течение 20 минут при комнатной температуре (RT).
ПРИМЕЧАНИЕ: Всегда оставляйте 25 МКЛ жидкости над матрицей, чтобы предотвратить ее повреждение. - Аккуратно удалите фиксировавающий раствор и вымойте 3x с 400 МКЛ 1x PBS на (RT).
- Pipette из PBS, добавить 400 йл раствора пермялизации (0,5% Тритон X-100 в 1x PBS) и инкубировать 10 мин на RT.
- Аккуратно удалите раствор протеабилизации, а затем 3 быстрых моет с 400 йл 1x PBS и длинная шаг стирки 30 мин на RT.
ПРИМЕЧАНИЕ: На этом этапе слайд может храниться при 4 градусах Цельсия в течение 2 дней. В этом случае запечатать слайд парафиновой пленкой, чтобы предотвратить испарение и матричную сушку. - Удалите PBS, добавьте 400 МКЛ блокирующего раствора, содержащего 0,1% бивейного альбумин сыворотки (BSA) и 10% козьей сыворотки в 1x PBS и инкубировать в течение 60 мин на RT.
ВНИМАНИЕ: Концентрации BSA выше 0,1% приведет к опровержению люмена и дальнейшему коллапсу кисты (см. раздел Представитель результаты)(рисунок 7A). - Pipette из блокирующего решения и мыть один раз с 400 йл PBS/0,05% Tween 20 и отказаться.
- Добавьте 150 МКЛ раствора антител, например, E-кадерин антитела разбавленные 1:400 и фаллоидин 568 (16,2 нМ окончательной концентрации) в 1x PBS и инкубировать в течение 90 мин на RT.
ПРИМЕЧАНИЕ: Это разбавление E-кадерин так же используется, как и в стандартном 2D иммунофторесценции протокола. - Вымойте образец с 400 МКЛ PBS/0.05% Tween 20, 3x; каждый раз инкубации образца в течение 10 минут на RT.
- Добавьте 150 мл вторичного антитела (коза анти-кролик IgG Alexa Fluor Plus 647), разбавленный 1:500 в 1x PBS и инкубировать 60 мин на RT.
- Вымойте 3x с 400 йл PBS/0.05% Tween 20, каждый раз инкубации образца в течение 10 мин на RT.
- Вымойте 3x с 400 йл 1x PBS, каждый раз инкубации образца в течение 10 минут на RT.
- Отбросьте PBS последней стирки и подготовить слайд камеры для визуализации с помощью конфокальные микроскопии после одного из двух вариантов ниже.
- Добавьте 400 мкл 1x PBS и 50 МКЛ DAPI на колодец. Образцы могут быть исследованы через дно колодец без необходимости монтажа с крышкой(рисунок 7B).
- Добавьте 100 мкл на колодец антифадного реагента, содержащего DAPI, и дайте слайду высохнуть O/N на RT.
Результаты
Формирование и характеристика кист
Системы культуры 3D клеток являются важным инструментом для изучения органогенеза и моделированиязаболеваний 25. К сожалению, большинство из этих методов являются качественными или использовать внутреннюю количественную оце?...
Обсуждение
Для изучения органогенеза и поддержания 3D клеточных структур, различные ткани были смоделированы, используя различные клеточные происхождение, но и различные типы внеклеточных матриц, включая синтетические гидрогели8,9,10,
Раскрытие информации
Авторов нечего раскрывать.
Благодарности
Мы благодарим д-ра Николаса ЛаРуссо (Клиника Майо, Рочестер, Миннесота, Соединенные Штаты), который любезно предоставил линию сотовой линии СРН.
Эта работа получила финансовую поддержку как программы iLite RHU (грант ANR-16-RHUS-0005), так и ДГУ Гепатинова.
Мы благодарим Изабель Гарсин и Резо д'Образера Челлилера Пэрис Саклай за их поддержку в визуализации.
Материалы
| Name | Company | Catalog Number | Comments |
| 10 µl- Pipette Eppendorf Research Plus | Thermo Fisher Scientific | 3120000020 | |
| 100 µl - Pipette Eppendorf Research Plus | Thermo Fisher Scientific | 3120000046 | |
| 1000 µl - Pipette Eppendorf Research Plus | Thermo Fisher Scientific | 3120000062 | |
| 1X PBS | Thermo Fisher Scientific | 14190-094 | |
| 200 µl - Pipette Eppendorf Research Plus | Thermo Fisher Scientific | 3120000054 | |
| 3,3′,5-Triiodo-L-thyronine sodium salt | Sigma-Aldrich | T5516 | NRC complete medium final concentration = 3.4 µg/mL |
| Acetic acid | VWR | 20104-298 | 0.02N final |
| Aerosol barrier pipettes tips 10 µl (Fisherbrand) | Thermo Fisher Scientific | 2707439 | |
| Aerosol barrier pipettes tips 1000 µl (Fisherbrand) | Thermo Fisher Scientific | 2707404 | |
| Aerosol barrier pipettes tips 200 µl (Fisherbrand) | Thermo Fisher Scientific | 2707430 | |
| Antibiotic Antimicotic Solution (100X) | Sigma-Aldrich | A5955 | NRC complete medium final concentration = 1:100 dilution |
| Bovine pituitary extract | Thermo Fisher Scientific | 13028-014 | NRC complete medium final concentration = 30 µg/mL |
| Bovine serum albumin | Sigma-Aldrich | A2153 | 1:1000 dilution |
| Chemically Defined Lipid Concentrate (100X) | Thermo Fisher Scientific | 11905-031 | NRC complete medium final concentration = 1:100 dilution |
| Collagen high concentration, rat tail | Thermo Fisher Scientific | 354249 | 50 µg/mL final concentration |
| Dexamethasone | Sigma-Aldrich | D4902 | NRC complete medium final concentration = 0.393 µg/mL |
| DMEM F12 | Thermo Fisher Scientific | 21331-020 | NRC complete medium final concentration = 1X |
| E-cadherin Rabbit anti-Human, Rat, Polyclonal | Thermo Fisher Scientific | PA5-32178 | 1:400 dilution |
| Eclipse TE300 inverted microscope | Nikon | imaging | |
| Ethanolamine | Sigma-Aldrich | E9508 | NRC complete medium final concentration = 0.32 mM |
| Fetal calf serum | Thermo Fisher Scientific | 10270-106 | NRC complete medium final concentration = 5:100 dilution |
| Fluoroshield with DAPI (Mounting medium) | Sigma-Aldrich | F6057 | |
| Formaldehyde 16% (W/V) | Thermo Fisher Scientific | 28906 | 4% (W/V) |
| Goat serum | Thermo Fisher Scientific | 16210-064 | 1:10 dilution |
| Hamamatsu camera (Digital camera C11440 ORCA - flash 4.OLT) | Hamamatsu | imaging | |
| Hoechst 33258 | Sigma-Aldrich | B1155 | 5 µg/mL final concentration |
| IgG (H+L) Highly Cross-Adsorbed Goat anti-Rabbit, Alexa Fluor Plus 647 | Thermo Fisher Scientific | A32733 | 1:500 dilution |
| ImageJ version 2.0.0-rc-69/1.52n | Open source image processing software | ||
| Insulin-Transferrin-Selenium (100X) | Thermo Fisher Scientific | 51300-044 | NRC complete medium final concentration = 1:100 dilution |
| L-Glutamine (100X) | Thermo Fisher Scientific | 25030-024 | NRC complete medium final concentration = 1:100 dilution |
| Matrigel GFR (stock concentration 9.7 mg/mL) | Thermo Fisher Scientific | 356231 | 4:10 dilution |
| NIS Elements software version 4.50.00 | Nikon | image acquisition and display | |
| Non-Essential-Amino-Acids-Solution (100X) | Thermo Fisher Scientific | 11140-035 | NRC complete medium final concentration = 1:100 dilution |
| Objective Plan Fluor 10X/0.30 Ph1 DL (∞/1.2 WD 15.2) | Nikon | ||
| Prolong Gold Antifade Reagent | Thermo Fisher Scientific | P36931 | |
| Propidium Iodide (PI) | Sigma-Aldrich | P4170 | 20 µg/mL final concentration |
| Rhodamine Phalloidin | Thermo Fisher Scientific | R415 | 16.2 nM final concentration |
| Sir-Actin / Verapamil kit | Spirochrome | SC001 | 10 µM final concentration |
| Soybean trypsin inhibitor | Thermo Fisher Scientific | 17075-029 | NRC complete medium final concentration = 50 µg/mL |
| Sterile cell strainer 40 µm (Fisherbrand) | Thermo Fisher Scientific | 22363547 | |
| Sterile pipettes 10 mL (Fisherbrand) | Thermo Fisher Scientific | 1367811E | |
| Sterile pipettes 5 mL (Fisherbrand) | Thermo Fisher Scientific | 1367811D | |
| Sterile tubes 1.5 mL (Fisherbrand) | Thermo Fisher Scientific | 11926955 | |
| Sterile tubes 15 mL (Fisherbrand) | Thermo Fisher Scientific | 7200886 | |
| Sterile tubes 50 mL (Fisherbrand) | Thermo Fisher Scientific | 553913 | |
| Sucrose | Sigma-Aldrich | S0389 | 5:100 dilution |
| Tissue culture treated flask 25cm2 (Falcon) | Thermo Fisher Scientific | 353108 | |
| Triton X-100 | Sigma-Aldrich | T8787 | 5:1000 dilution |
| Trypsin-EDTA (0.05%) phenol red | Thermo Fisher Scientific | 25300-054 | 1X |
| Tween-20 | Sigma-Aldrich | P1379 | 5:10000 dilution |
| Vitamin (100X) | Thermo Fisher Scientific | 11120-037 | NRC complete medium final concentration = 1:100 dilution |
| μ-Slide 8 Well ibiTreat, Ibidi | Clinisciences | 80826 |
Ссылки
- Edmondson, R., Broglie, J. J., Adcock, F., Yang, L. Three-Dimensional Cell Culture Systems and Their Applications in Drug Discovery and Cell-Based Biosensors. ASSAY and Drug Development Technologies. 12 (4), 207-218 (2014).
- Martín-Belmonte, F., et al. Cell-polarity dynamics controls the mechanism of lumen formation in epithelial morphogenesis. Current Biology. 18, 507-513 (2008).
- Debnath, J., Muthuswamy, S. K., Brugge, J. Morphogenesis and oncogenesis of MCF-10A mammary epithelial acini grown in three-dimensional basement membrane cultures. Methods. 30 (3), 256-268 (2003).
- Artym, V. V., Matsumoto, K. Imaging Cells in Three-Dimensional Collagen Matrix. Current Procotols in Cell Biology. , (2010).
- Petersen, O. W., Ronnov-Jessen, L., Howlett, A. R., Bisell, M. J. Interaction with basement membrane serves to rapidly distinguish growth and differentiation pattern of normal and malignant human breast epithelial cells. Proceedings of the National Academy of Sciences of the United States of America. 89, 9064-9068 (1992).
- Kim, S. P., Lee, D. H., Park, J. K. Development of hepatocyte spheroids immobilization technique using alternative encapsulation method. Biotechnology and Bioprocess Engineering. 3, 96-102 (1998).
- Lorent, K., et al. Identification of a plant isoflavonoid that causes biliary atresia. Science Translational Medicine. 7 (286), 67 (2015).
- Nowak, M., Freudenberga, U., Tsurkana, M. V., Wernera, C., Levental, K. R. Modular GAG-matrices to promote mammary epithelial morphogenesis in vitro. Biomaterials. 112, 20-30 (2017).
- Miroshnikova, Y. A., et al. Engineering Strategies to Recapitulate Epithelial Morphogenesis Within Synthetic Three-Dimensional Extracellular Matrix With Tunable Mechanical Properties. Physical Biology. 8 (2), 026013 (2011).
- Ozdemir, T., et al. Tuning Hydrogel Properties to Promote the Assembly of Salivary Gland Spheroids in 3D. ACS Biomaterials Science & Engineering. 2 (12), 2217-2230 (2016).
- Dolega, M. E., Abeille, F., Picollet-D'hahan, N., Gidrol, X. Controlled 3D culture in Matrigel microbeads to analyze clonal acinar development. Biomaterials. 52, 347-357 (2015).
- Laperrousaz, B., et al. Direct transfection of clonal organoids in Matrigel microbeads: a promising approach toward organoid-based genetic screens. Nucleic Acids Research. 46 (12), 70 (2018).
- Lazaridis, K. N., LaRusso, N. F. The Cholangiopathies. Mayo Clinic Proceedings. 90 (6), 791-800 (2015).
- Tam, P. K., Yiua, R. S., Lendahl, U., Andersson, E. R. Cholangiopathies - Towards a molecular understanding. EBioMedicine. 35, 381-393 (2018).
- Loarca, L., et al. Development and characterization of cholangioids from normal and diseased human cholangiocytes as an in vitro model to study primary sclerosing cholangitis. Laboratory Investigation. 97, 1385-1396 (2017).
- De Assuncao, T. M., Jalan-Sakrikar, N., Huebert, R. C. Regenerative medicine and the biliary tree. Seminars in Liver Disease. 37, 17-27 (2017).
- Dianat, N. H., et al. Generation of functional cholangiocyte-like cells from human pluripotent stem cells and HepaRG cells. Hepatology. 60, 700-714 (2014).
- Masyuk, A. I., et al. Cholangiocyte autophagy contributes to hepatic cystogenesis in polycystic liver disease and represents a potential therapeutic target. Hepatology. 67 (3), 1088-1108 (2018).
- Sampaziotis, F., Cardoso, M., Madrigal, P., Bertero, A., Saeb-Parsy, K., et al. Cholangiocytes derived from human induced pluripotent stem cells for disease modeling and drug validation. Nature Biotechnology. 33 (8), 845-852 (2015).
- Soroka, J. C., et al. Bile-Derived Organoids From Patients With Primary Sclerosing Cholangitis Recapitulate Their Inflammatory Immune Profile. Hepatology. 70 (3), 871-882 (2019).
- Funfak, F., et al. Biophysical Control of Bile Duct Epithelial Morphogenesis in Natural and Synthetic Scaffolds. Frontiers in Bioengineering and Biotechnology. 7 (417), 417 (2019).
- Du, Y., et al. Bile Duct-on-a-Chip With Organ-Level Functions. Hepatology. , (2019).
- Shiota, J. M., Mohamad Zaki, N. H., Merchant, J. L., Samuelson, L. C., Razumilava, N. Generation of Organoids from Mouse Extrahepatic Bile Ducts. Journal of Visualized Experiments. (146), e59544 (2019).
- Bircsak, K. M., Richardson, J. R., Aleksunes, L. M. Inhibition of Human MDR1 and BCRP Transporter ATPase Activity by Organochlorine and Pyrethroid Insecticides. Journal of Biochemical and Molecular Toxicology. 27 (2), 157-164 (2013).
- Fennema, E., Rivron, N., Rouwkema, J., Blitterswijk, C., Boer, J. Spheroid culture as a tool for creating 3D complex tissues. Trends in Biotechnology. 31 (2), 108-115 (2013).
- Kanade, S., Nataraj, G., Ubale, M., Mehta, P. Fluorescein Diacetate Vital Staining for Detecting Viability of Acid-Fast Bacilli in Patients on Antituberculosis Treatment. International Journal of Mycobacteriology. 5 (3), 294-298 (2016).
- Rieger, A. M., Nelson, K. L., Konowalchuk, J. D., Barreda, D. R. Modified Annexin V/Propidium Iodide Apoptosis Assay For Accurate Assessment of Cell Death. Journal of Visualized Experiments. (50), e2597 (2011).
- Tabibian, J. H., Masyuk, A., Masyuk, T. V., O'Hara, S. P., LaRusso, N. F. Physiology of Cholangiocytes. Comprehensive Physiology. 3 (1), (2013).
- Spirlì, C., et al. Functional polarity of Na+/H+ and Cl-/HCO3- exchangers in a rat cholangiocyte cell line. American Journal Physiology. 275, 1236-1245 (1998).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены