Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Bioengineering
Manipulation af enkelt neurale stamceller og neuroner i hjernen skiver ved hjælp af Robotic Microinjection
Denne protokol viser brugen af en robot platform for mikroinjektion i enkelt neurale stamceller og neuroner i hjernen skiver. Denne teknik er alsidig og tilbyder en metode til sporing af celler i væv med høj rumlig opløsning.
Et centralt spørgsmål i udviklingsmæssige neurobiologi er, hvordan neurale stamceller og progenitor celler danner hjernen. For at besvare dette spørgsmål, man har brug for at mærke, manipulere, og følge enkelte celler i hjernevævet med høj opløsning over tid. Denne opgave er yderst udfordrende på grund af kompleksiteten af væv i hjernen. Vi har for nylig udviklet en robot, der guider en mikroinjektionsnål ind i hjernevæv, når billeder erhvervet fra et mikroskop til at levere femtoliter mængder opløsning til enkelte celler. Robotdriften øger det samlede udbytte, der er en størrelsesorden større end manuel mikroinjektion og giver mulighed for præcis mærkning og fleksibel manipulation af enkelte celler i levende væv. Med dette kan man mikroinject hundredvis af celler inden for en enkelt organotypic skive. Denne artikel viser brugen af mikroinjektion robot til automatiseret mikroinjektion af neurale progenitor celler og neuroner i hjernen væv skiver. Mere generelt kan det bruges på ethvert epitelvæv med en overflade, der kan nås af pipetten. Når den er sat op, kan mikroinjektionsrobotten udføre 15 eller flere mikroinjektioner pr. minut. Mikroinjektionsrobotten på grund af dens gennemløb og versalitet vil gøre mikroinjektion til en stort set ligetil højtydende cellemanipulationsteknik, der skal anvendes i bioengineering, bioteknologi og biofysik til udførelse af enkeltcelleanalyser i organotypiske hjerneskiver.
Denne protokol beskriver brugen af en robot til at målrette og manipulere enkelte celler i hjernevæv skiver, med fokus især på enkelt neurale stamceller og neuroner. Robotten blev udviklet til at løse et centralt spørgsmål i udviklingsmæssige neurobiologi, det er, hvordan neurale stamceller og progenitor celler bidrager til hjernen morfoogenese1,2,3,4,5. For at besvare dette spørgsmål, man har brug for at mærke og spore enkelt neurale stamceller og følge deres afstamning progression over tid at korrelere enkelt celle adfærd med væv morfosse. Dette kan opnås på forskellige måder, fx ved at elektroporere hjernevæv i livmoderen eller ved at mærke enkelt celle ved hjælp af lipofile matricer. Selv om magtfulde, disse metoder mangler præcis enkelt celle opløsning (elektroporation) og / eller muligheden for at manipulere det intracellulære rum (lipofile farvestof). Mikroinjektion i enkelte celler blev udviklet for at overvinde denneudfordring 6,7,8. Under mikroinjektion indsættes en pipette kortvarigt i en enkelt celle i intakt væv under tryk på mikroinject femtoliter mængder reagenser9. Vi har tidligere beskrevet en manuel procedure for mikroinjekting enkelt neurale stamceller i organotypisk væv (Figur 1A)10,11. Mikroinjektion i neurale stamceller er afhængig af brugen af en mikropipette, der indsættes i enkelte neurale stamceller til at injicere en opløsning, der indeholder en fluorescerende farvestof, sammen med andre molekyler af interesse. Den selektive målretning af neurale stamceller opnås ved at nærme sig den udviklende telencephalon via ventrikulær overflade (eller ventrikel, se tegneserie i figur 1A), der dannes af den apikale plasmamembran af aptiske forfædre (tegneserie i figur 1A). Denne proces skal gentages for hver celle, som eksperimentatoren ønsker at injicere. Endvidere er mikroinfektionens succes afhængig af den præcise kontrol af dybden og varigheden af mikropipetteinjektion i vævet. Således, på trods af de unikke fordele, manuel mikroinjektion er yderst kedelig og kræver betydelig praksis til at udføre på rimelig gennemløb og udbytte, hvilket gør denne teknik vanskeligt at bruge på en skalerbar måde. For at overvinde denne begrænsning har vi for nylig udviklet en billedguidet robot, Autoinjector12 (eller microinjection robot), der automatisk kan udføre mikroinjektioner i enkelte celler.
Mikroinjektionsrobotten gør brug af mikroskopiske billedbehandlings- og computersynsalgoritmer til præcist at målrette specifikke steder i 3D-rummet i væv til mikroinjektion (Figur 1B). Mikroinjektionsrobotten kan konstrueres ved at foretage relativt enkle ændringer af et eksisterende mikroinjektionsopsætning. Mikroinjektionsrobottens overordnede skema er vist i figur 1C. En pipette er monteret i en pipetteholder fastgjort til en treakset manipulator. Et mikroskop kamera bruges til at erhverve billeder af vævet og mikroinjektion nålen. Et brugerdefineret trykreguleringssystem bruges til at styre trykket inde i pipetten, og en programmerbar mikromanipulator bruges til at styre placeringen af mikroinjektorpipetten. Kamerabillederne af vævs- og mikroinjektionspipetten bruges til at bestemme den rumlige placering af mikroinjektionspipettespidsen og de steder, hvor mikroinjektioner skal udføres. Softwaren beregner derefter baner, der er nødvendige for at flytte pipetten i vævet. Al hardware styres af den software, vi tidligere har udviklet. Al software er skrevet i kodningssprog (f.eks https://github.com/bsbrl/Autoinjector. Den grafiske brugergrænseflade (GUI) giver brugeren mulighed for at billedet væv og mikropipette, og at tilpasse bane af mikroinjektion. Vores system kan etableres ved hjælp af relativt enkle ændringer til et omvendt mikroskop udstyret med brightfield og epi-fluorescens filtre.
Først giver vi instruktioner om forberedelse hjernen organotypiske væv skiver til mikroinjektion. Derefter illustrerer protokollen start af mikroinjektionsrobotten efterfulgt af forberedende trin, såsom pipettebevægelseskalibrering, der skal gøres før mikroinjektion. Dette efterfølges af at definere injektionsparametrene. Efter dette, brugeren kan definere bane, der anvendes af mikroinjektion robot og starte injektion procedure. Det mikroindsjævlede væv (i dette tilfælde hjerneorganotypiske vævsskiver) kan holdes i kultur i forskellige tidsperioder afhængigt af det eksperimentelle design10,11. Vævet kan behandles til at følge og studere identiteten og skæbnen for de injicerede celler og deres afkom. Alternativt kan de mikroopterede celler følges ved hjælp af levende billeddannelse. Inden for rammerne af denne protokol, viser vi brugen af robotten til automatisk mikroinjstion neurale progenitor celler i organotypic skiver af musen E14.5 dorsale telencephalon. Robotten er yderligere i stand til mikroinjektion i nyfødte neuroner i musen telencephalon, samt i den menneskelige føtale telencephalon12.
Sammenfattende beskriver vi en robotplatform, der kan bruges til at følge og manipulere enkelte celler i væv. Platformen gør brug af tryk, og det er derfor yderst alsidigt med hensyn til den kemiske karakter af forbindelsen til at injicere. Desuden kan det tilpasses til målceller andre end stamceller. Vi forventer, at vores system også let kan tilpasses andre modelsystemer.
Alle dyreforsøg blev gennemført i overensstemmelse med den tyske dyrevelfærdslovgivning, og de nødvendige licenser blev indhentet fra den regionale etiske kommission for dyreforsøg i Dresden, Tyskland (Tierversuchskommission, Landesdirektion Dresden). Organotypic skiver blev fremstillet af E14.5 eller E16.5 C57BL/6 mus embryonale telencephalon (Janvier Labs).
1. Installation af software
- Følg vejledningen for at installere softwaren fra https://github.com/bsbrl/Autoinjector.
2. Fremstilling af reagenser og pipetter
- Agarose: Forbered 3% agarose ved separat opløsning af 3 g bred vifte agarose og 3 g lavt smeltepunkt agarose i 100 ml cellekultur-grade PBS i to separate 200 ml glasflasker, henholdsvis. Opbevares ved stuetemperatur i op til 3 måneder.
- Tyrodopløsning: 1 g natriumbikarbonat og tyrods salt (brug hele flaskens indhold) og 13 ml 1 M HEPES i 1 L destilleret vand. PH-3 til 7,4. Opløsningen filtreres gennem et 0,2 μm flasketopfilter.
- Skive kultur medium (SCM): Tilføj 10 ml rotte serum, 1 ml N-2 supplement (100x), 2 ml B27 supplement (50x) og 1 ml HEPES (pH 7.3) buffer i 84 ml Neurobasal medium. Aliquot 5 ml SCM i 15 ml rør. Opbevares ved -20 °C.
- CO2-IndependentMicroinjection Medium (CIMM): Forbered 5x DMEM modificeret lavgloseopløsning (uden fenolrød) ved at opløse pulveret i 200 ml destilleret vand. Filter opløsning gennem en 0,2 μm flaske-top filter (for DMEM pulver, bruge indholdet af hele flasken). For at forberede 100 ml CIMM 20 ml 5x DMEM modificeret opløsning, 1 ml HEPES-buffer, 1 ml N2-tillæg (100x), 2 ml B27 supplement (50x), 1 ml penicillin-streptomycin (100x), 1 ml 2 ml glutamin og 74 ml destilleret vand. Opløsningen opbevares ved 4 °C.
- Rekonstitutionsbuffer: Forbered rekonstitutionsbufferen ved at opløse 262 mM NaHCO3, 0,05 N NaOH, 200 mM HEPES i destilleret vand. Opløsningen steriliseres ved filtrering gennem et 0,22 μm-filtersystem i en steril glasflaske. Aliquot 500 μL rekonstitutionsbuffer i lufttætte mikrocentrifugerør. Opbevares ved 4 °C.
- Mikroinjektionsfarvelager: Dextran opløses med et fluorescerende mærke i RNase-frit destilleret vand (slutkoncentration 10 μg/μL). Der tilberedes 5 μL-aliquots, og opbevares ved -20 °C, indtil de anvendes.
- Træk mikroinjektionpipetterne ud af borosilikatglaskapillærer (1,2 mm ydre diameter, 0,94 mm indvendig diameter) ved hjælp af mikropipettetrækkeren. Beskyt pipetterne mod støv. Opbevar ikke pipetter i mere end 2 – 3 dage. Til dette eksperiment var trækparametrene HEAT: rampetemperatur +1 – 5; TRÆK: 100; VEL: 110; DEL: 100. HEAT og VEL er de parametre, der påvirker den mest form og størrelse af pipetten.
BEMÆRK: Den optimale mikroinjektionspipette har en lang og fleksibel spids for at undgå celleskader under mikroinjektion.
3. Fremstilling af vævssnit
- Smelt de 3% brede rækkevidde agarose ved hjælp af en mikrobølgeovn før hjernevæv dissektion. Agarosestørkne ikke ved at holde vandbadet ved 37 °C før indlejring. Sørg for, at pipetterne er beskyttet mod støv. Opbevar ikke pipetter i mere end 2 – 3 dage.
- Optø en aliquot af SCM og varm 10 – 12 ml CIMM og 20 ml tyroders opløsning til 37 °C ved hjælp af et vandbad.
- Fluorescerende sporstof (Dextran-3000 eller Dextran-10000-Alexa konjugeret; slutkoncentration 5 – 10 μg/μL) med de andre kemiske stoffer, der skal injiceres. Mikroinfektionsopløsningen centrifugeres ved 16,000 x g i 30 minutter ved 4 °C. Saml supernatant og overføre i et nyt rør. Hold mikroinfektionsopløsningen på is, indtil den er i brug.
- Brug hovederne fra E13.5 – E16.5 museembryoner til at forberede organotypiske vævskiver af telencephalon. Fjern huden og åbne kraniet ved hjælp af scelinnerne, bevæger sig langs midterlinjen. Dissekere den embryonale hjerne ud af det åbne kranium og fjern de meninges, der dækker hjernevævet, startende fra hjernesiden. Lad den dissekerede hele hjerne i Tyrods opløsning være på en 37 °C varmeblok.
BEMÆRK: Alle dissektionstrin, der er beskrevet i 3.4, skal udføres i forvarmt Tyrids opløsning. - Hæld den brede vifte smeltet agarose i en engangs indlejring skimmel. Når agarose er afkølet til 38 – 39 °C, omhyggeligt overføre hjerner (højst 4) i det ved hjælp af en Pasteur pipette. Brug altid skæretips til dette trin.
- Rør agarose omkring vævet enten ved hjælp af en spatel eller et par Dumont #1 stænt uden at røre vævet. Lad agarose størkne ved stuetemperatur. Når agarose har størknet, trim overskydende agarose omkring vævet.
- Fyld bufferbakken med PBS. Orient hjernen med rostro-caudal akse af vævet vinkelret på bakken (brug som vartegn olfaktoriske pærer, der repræsenterer rostral-meste af hjernen). Skær 250 μm skiver ved hjælp af en vibratome.
- Fyld en 3,5 cm petriskål med 2 ml forvarmede medier. Ved hjælp af en plastik Pasteur pipette, overføre skiver (10 - 15) til denne parabol. Når det er gjort, flytte petriskålen med skiverne i skiven kultur inkubator. Skærne fastholdes ved 37 °C i en befugtet atmosfære, der indeholder 40% O2 / 5% CO2 / 55% N2 indtil brug.
4. Mikroinjektion
- Tænd computeren, mikroskopet, mikroskopkameraet, manipulatorer, trykplatformen og tryksensoren. Indlæs programmet ved at klikke på filen "launchapp.py" i hovedmappen, der er hentet fra GitHub, og angiv enhedsindstillingerne på pop op-skærmen (se trin 1.1 for at få installationsinstruktioner).
- Opret et ydre tryk for at forhindre uønsket tilstopning, før pipetten nedsænkes i opløsningen. Hvis du vil lægge pres på pipetten, skal du skubbe kompensationstrykbjælken til 24 - 45 % og klikke på Angiv værdier. Dernæst indstilles trykket til et tilstrækkeligt tryk ved at dreje den mekaniske trykventilknap til 1 – 2 PSI (69 – 138 mbar) som angivet af trykføleren.
- Overfør skiverne til en 3,5 cm petriskål indeholdende 2 ml forvardt CIMM. Placer skiver, der skal microinjected i midten af petriskålen. Petriskålen overføres til det forvarmede (37 °C) mikroinjektionsstadiet.
- Mikroinfektionpipetten indlæses med 1,4 -1,6 μL mikroopoptret opløsning (fra trin 3.3) med en langspidss plastpipette. Sæt mikroinjektionspipetten på pipetten.
- Brug den laveste forstørrelse på mikroskopet, bringe skiven i fokus og guide mikropipetten til dette synsfelt (FOV), så det er fokuseret på det samme plan som skivemålet. Skift mikroskopets udgang til kameraet for at se FOV'en i applikationen.
- Klik på forstørrelsesknappen øverst til venstre i grænsefladen for at starte enhedskalibrering. Et vindue vil bede om at vælge forstørrelsen. Vælg 10x forstørrelse, eller hvad forstørrelse linsen er indstillet til (f.eks 4x, 10x, 20x, 40x) og tryk på Ok. Softwaren antager den interne objektive linse er 10x (den mest almindelige objektive linse forstørrelse).
- Refokuser pipettespidsen ved hjælp af mikroskopets mikrometriske hjul, og klik på pipettespidsen med markøren. Tryk derefter på trin 1.1-knappen, og tryk på OK i pop op-vinduet. Pipetten bevæger sig i Y-retningen. Klik på spidsen af pipetten, og tryk på trin 1.2-knappen. Sætvinkelboksen skal ind i endelysfeltet og trykke på setvinklen.
- Indtast de ønskede parametre i kontrolpanelet Automatiseret mikroinjektion. For mikroinjektion i aptiske stamfader indstille injektionsafstanden til 20 – 40 μm og dybde til 10 – 15 μm. For mikroinjektion i neuroner indstille injektion afstand 30 – 40 μm fra den basale side, og dybde til 10 – 30 μm afhængigt af hvad der bliver målrettet. Indstil altid hastigheden til 100 %. Klik på Angiv værdier.
BEMÆRK: Indflyvningsafstanden er den afstand, pipetten trækker ud af vævet, før du går til den næste injektionsafstand, dybden er dybden i vævet, som mikroinjektionen går, afstanden langs strækningen mellem sekventielle injektioner, hastighed er pipettens hastighed i μm/s. - Klik på knappen Tegn kant, og træk markøren langs den ønskede bane i pop op-vinduet for at definere injektionsbane. For mikroinjecterende stamceller fra progenitoren er telencephalonoverfladens ventrale side målrettet som vist i figur 2A. Bring pipetten til starten af linjen og klik på spidsen af pipetten. Klik på Kør bane for at starte mikroinjecting. Gentag dette trin for hvert fly af injektion målrettet (normalt gjort for 3 – 4 fly med 40 – 75 injektioner per fly).
5. Vævskultur og vævsskiverbehandling for immunfluorescens
- Kollagenblandingen (1,5 mg/ml): Til et rør tilsættes 1,25 ml af matrixopløsningen, 0,5 ml destilleret vand, 0,5 ml 5x DMEM-F12-opløsning og 0,25 ml rekonstitutionsbuffer. Hold det på is, indtil brug.
- Hent petriskålen, der indeholder de mikrooptrigtede skiver fra skivens kulturinkubationskammer, og nedsænk skiverne i kollagenblandingen.
- Overfør skiverne sammen med 200 – 300 μL kollagenblanding i en 14 mm brønd af en 35 mm glasbundet skål. Sørg for, at skiverne er dækket af meget mindre kollagen. Dette sæt op giver mulighed for de optimale betingelser for næringsstoffer og iltoptagelse.
- Orient skiverne og samtidig sikre, at der er tilstrækkelig plads mellem skiverne ved hjælp af to par vicesser. Petriskålen inkuberes i 5 min ved 37 °C ved hjælp af en varmeblok for at gøre det muligt for kollagen at størkne. Overvej denne gang som t = 0 af skive kultur.
- Flyt petriskålen tilbage til skivens kulturkubvøse i yderligere 40 min. Derefter tilsættes 2 ml af den forvarmede SCM. Skiver holdes i kultur indtil det ønskede tidspunkt.
- Tag skiverne ud af skiven kultur inkubator og aspirere SCM. Vask kollagen-indlejrede skiver med 1x PBS. Der tilsættes 4% (wt/vol) paraformaldehyd (i 120 mM fosfatbuffer, pH 7.4) og lad vævet blive ved RT i 30 min. Flyt den derefter til 4 °C for at give mulighed for natfiksering.
- Aspirere paraformaldehydopløsningen næste dag og udfør 1x PBS vasker. For at fjerne skiverne fra kollagen skal du bruge to par vicesser til forsigtigt at udtrække skiverne under et stereomikroskop.
- Brug en mikrobølgeovn til at smelte de 3% (wt / vol) lavt smeltepunkt agarose til behandling af mikroindjøjvet skiver. Hæld den smeltede agarose i en engangs indlejring skimmel og lad det køle af til omkring 38 – 39 °C.
- Overfør vævsskiverne fra trin 5.7 til denne form, der indeholder lavt smeltende agarose ved hjælp af en plastik Pasteur pipette. Sørg for, at pialsiden af skiven er op, og at ventrikeloverfladen vender nedad. Hvis det er nødvendigt orientere i overensstemmelse hermed. Lad agarose køle ned til RT for at størkne.
- Trim den ekstra agarose omkring skiverne. Vend agaroseblokken for at sikre, at snitfladen er parallel med vibratomens skæreblad. Skær 50 μm tykke sektioner med vibratom.
- Fyld en 24 brøndskål med 1x PBS. Overfør sektionerne i denne ret ved hjælp af en fin-tip pensel. Udfør immunfluorescens i henhold til standardprotokollerne.
Microinjection tjener det formål at spore og manipulere enkelte neurale stamceller og deres afkom i levende væv og til at følge deres afstamning progression i et fysiologisk miljø. I denne artikel har vi demonstreret brugen af mikroinjektionsrobotten til målretning og automatisk mikroinjecting organotypic skiver af musetelcephalonen. Figur 2 illustrerer repræsentative billeder af vellykkede indsprøjtede progenitorceller, og figur 3 illustrerer injicerede nyfødte neuroner. Når injiceres med Dextran Alexa-488 (eller Alexa-A555) farvestof, celler synes fuldt fyldt med farvestoffet. Med hensyn til apikale stamfader (Figur 2) konfokale billeddannelse tillader rekonstruere med høj rumlig opløsning cellemorfologi, tilstedeværelsen - eller fraværet- af den apikale og basale vedhæftet fil, og at kombinere den morfologiske undersøgelse med markør udtryk. Ved at kombinere disse kriterier, kan brugeren tildele en bestemt celle skæbne til mikroindsjænges celler og deres afkom. Med hensyn til neuron injektion, brugeren kan rekonstruere neuronal morfologi, herunder struktur og funktioner i apical dendrite og axon. Automatiseret mikroinjektion kan give betydeligt højere gennemløb i forhold til manuel mikroinjektion (Figur 2B). Endvidere bekræfter EdU-mærkningen, at cellernes levedygtighed ikke påvirkes af automatisering (figur 2C). Holde organotypiske skive i kultur giver mulighed for følgende afstamning progression af de mikroopjectede celler (vi viste 4 - 24h i figur 2D). Hvis mikroinjektionsopløsningen indeholder genetisk materiale (DNA, mRNA, CRISPR-Cas9 guider) eller rekombinant proteiner, giver dette mulighed for at undersøge, om og hvordan afstamningsprogression påvirkes af manipulationen.
Mikroinjektion i enkelte neurale stamceller i væv giver fremragende enkelt celle opløsning og af den grund har det været brugt til at dissekere cellebiologi af neurale stamceller progression og skæbne overgang (Figur 3A). Microinjection tillader levering af komplekse blanding af kemikalier. Vi har tidligere gjort brug af denne funktion til at studere junctional kobling i neurale progenitor celler ved at blande gap-junctional gennemtrængelig med hul junctional uigennemtrængelig fluorescerendefarvestoffer 12. Vi udvidede tidligere arbejde ved at studere junctional kobling i nyfødte neuroner, ved at injicere Lucifer Gul sammen med Dextran-A555 (Figur 3B). Som vist i figur 3Bkobles en del af nyfødte pyramide neuroner via mellemrumskryds til tilstødende neuroner. Denne observation er i overensstemmelse med tanken om, at umodne neuroner kommunikere via gap-junction13,14. Endvidere, målretning neuroner viser, at brugen af mikroinjektion robot kan generaliseres til flere celletyper i udviklingslandene pattedyr hjernen. Denne eksperimentelle opsætning vil være nyttig til at dissekere cellebiologi af neuroner i væv, for eksempel ved at levere specifikke oligopeptider til at forstyrre protein-protein interaktioner.
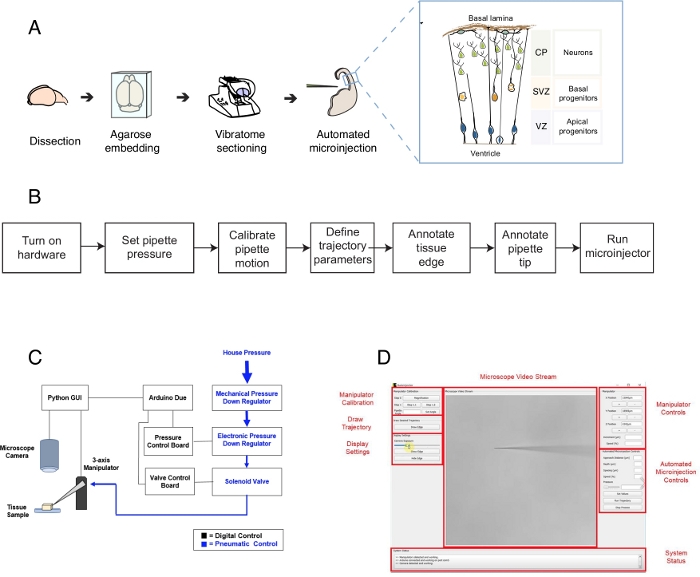
Figur 1: Automatiseret opsætning og protokol for mikroinjektion. a)Samlet protokol for vævspræparat og automatiserede mikroinjektioner ved hjælp af mikroinjektionsrobotten. Højre indsat: Cartoon skematisk af mus Telencephalon målrettet til mikroinjektion i denne protokol. (B)Rutediagram over de automatiserede mikroinjektionstrin. C) Skematisk af mikroinjektion robot hardware. d) Grafisk brugergrænseflade (GUI) af den software, der bruges til at styre og betjene mikroinjektionsrobotten. Dette tal er tilpasset fra ref.12. Klik her for at se en større version af dette tal.
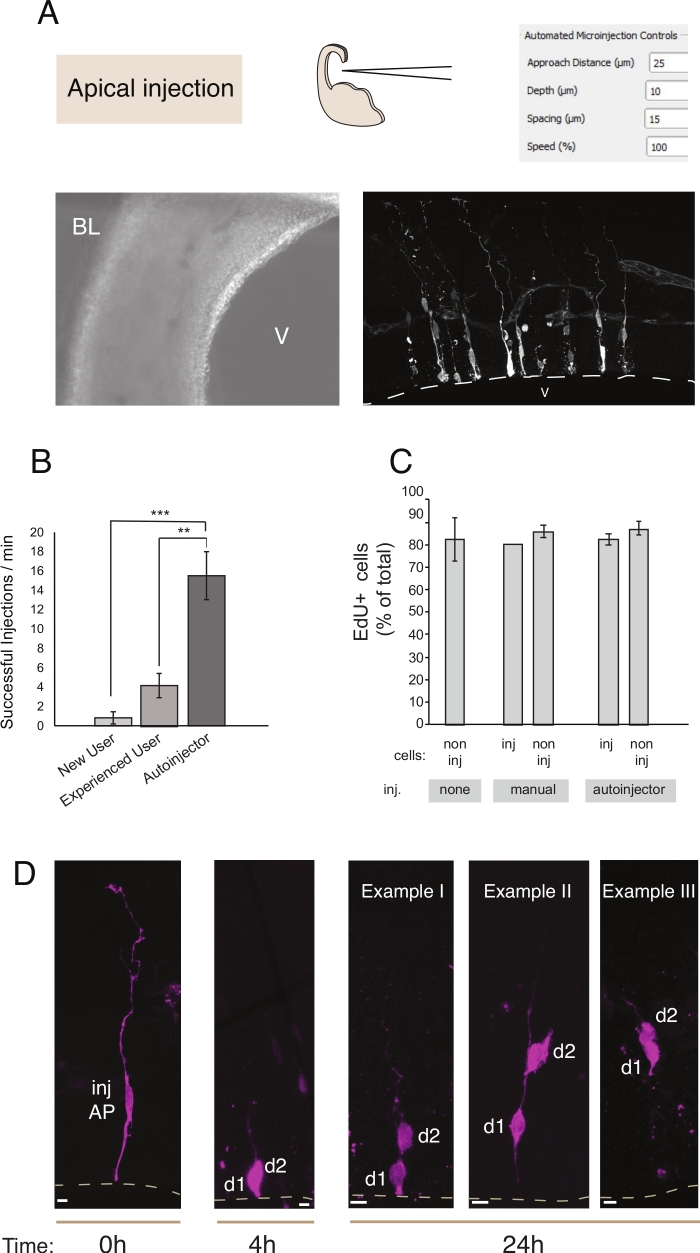
Figur 2: Mikroinjektion af robotinjekt i apikale forfædre. Skematiske og forventede resultater ved brug af mikroinjektionsrobotten til at målrette apikale progenitorer (AP'er) via den apikale overflade (apikale injektion). (A) Øverste række. Til venstre: skematisk af processen. Til højre: GUI med relevante parametre for apical injektion. Nederste række. Til venstre: fase kontrast billede taget under injektion procedure (V: hjertekammer; BL: basal lamina). Til højre: repræsentative resultater, der viser mikroindsjævede APs. Stiplede linje repræsenterer ventrikel (V). Skalabar: 10 μm. (B) Vellykkede injektioner i minuttet for en nybegynder bruger på det manuelle mikroinjektionssystem, en erfaren bruger på det manuelle mikroinjektionssystem og mikroinjektionsrobotten. c) EdU-inkorporering i mikroindsøgte celler og i celler, der ikke injiceres, i det injicerede område. Organotypic skiver af musen E14.5 dorsal telencephalon var enten i) ikke injiceres eller (ii) udsat for manuel eller automatiseret mikroinjektion (injiceret skive) ved hjælp af Dextran-A488 (for manuel og autoinjector). Skiver blev holdt i kultur i overværelse af EdU i 24 timer, så blev de faste og farves for DAPI og EdU. Indsprøjtede og ikke-injicerede celler i det injicerede område blev scoret for EdU positivitet. (D) Brug af mikroinjektionsrobotten Lineage-sporing. Et fluorescerende farvestof (Dx3-A555, magenta) injiceres i en enkelt neuralstamcelle (t = 0 h). Fluorescerende farvestof er opdelt i datterceller (d1, d2) under mitose. Dette gør det muligt at følge afkommet af den injicerede celle (t = 4 timer og 24 timer) og afsløre afstamning progression over tid. For t = 24 h, viser vi flere eksempler på afkomet man forventer at finde. Skalastænger: 10 μm. Grafer i B og C er taget fra ref.12Klik her for at se en større version af dette tal.
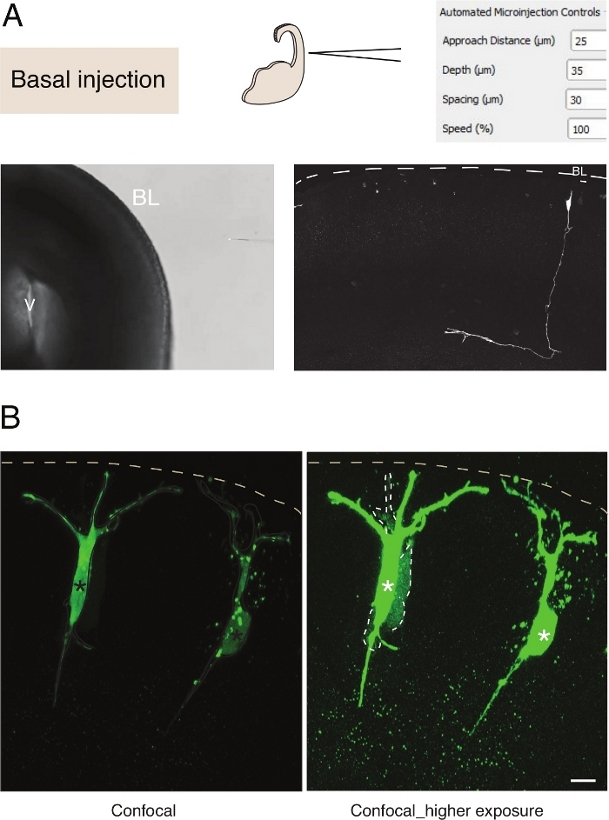
Figur 3: Mikroinjektion af robotinjektion i neuroner. Skematiske og forventede resultater ved brug af mikroinjektionsrobotten til at målrette pyramide neuroner (N) via den basale overflade (basal injektion). (A) Øverste række. Til venstre: skematisk af processen. Til højre: GUI med relevante parametre for basal injektion. Nederste række. Til venstre: fase kontrast billede taget under injektion procedure (V: hjertekammer; BL: basal lamina). Til højre: repræsentative resultater, der viser en microinjected N. Stiplet linje repræsenterer basal lamina (BL). Skalabar: 10 μm.(B)Brug af autoinjektoren til at studere mellemrumskommunikation i væv. Pyramideale neuroner blev injiceret med en opløsning, der indeholder to farvestoffer: hullet junctional-uigennemtrængelig Dx-A555 (ikke vist) og gap-junctional gennemtrængelige Lucifer Yellow (grøn). Dx-A555 er begrænset til den målrettede celle (stjerner), mens LY spreder til celler, der er forbundet via mellemrum krydset til den målrettede celle (stiplede linjer). Venstre panel: Lav eksponering, kun de mikroopjæoperede celler er synlige. Højre panel: Høj eksponering giver mulighed for visualisering af de injicerede celler samt de koblede celler (stiplede linjer). Skalabar: 10 μm. Klik her for at se en større version af dette tal.
Supplerende fil: Fejlfinding af flere almindelige fejl, der opstår under mikroinjektion. Klik her for at downloade denne fil.
Mikroinjektion i enkelte neurale stamceller i væv giver fremragende enkelt celle opløsning og af den grund har det været brugt til at dissekere cellebiologi af neurale stamceller progression og skæbne overgang (Figur 2; seogså 10,11,12). Den automatiserede mikroinjektionsprocedure kan udføres på andre typer celler i både embryonale mus og humant hjernevæv. Repræsentative resultater af mikroinjektion af nyfødte neuroner ved at målrette telencephalonens basale overflade er vist i figur 3.
Det princip, der er etableret her, kan anvendes til at målrette mod flere forskellige celletyper i embryonale musehjerner og menneskelige hjerner. Vi har tidligere vist, at mikroinjektion robot også kan bruges til at målrette enkelt progenitor celler i musen hindhjernen og telencephalon og nyfødte neuroner i musen og menneskelige udvikle neocortex12. For at opnå de bedste resultater af injektionsproceduren bør man optimere alle trinnene, før du starter injektionen. Det er vigtigt nøje at overveje og optimere forberedelsen af levedygtige og velbevarede organotypiske vævsskiver fra hjernevæv (Figur 1). Det er afgørende at være hurtig i dissektions- og udskæringsproceduren i figur 1. For apical injektion rettet mod AP'er, bør man vælge skiver, der viser den ideelle orientering af den apikale overflade. For AP injektion, den ideelle orientering er den apikale overflade vinkelret på bunden af petriskålen. Enhver anden orientering vil være eftergivende samt, men den apikale overflade vinkelret på Petriskålen giver et bredere overfladeareal til injektion, hvilket øger succes injektion. Til injektion i neuroner, orienteringen af skiven spiller lidt at ingen effekt.
Når skiverne til injektion er valgt, injektion procedure per skive tager cirka 5 minutter. I betragtning af at man arbejder med levende væv, anbefales det stærkt at fremskynde injektionsproceduren. Til dette formål anbefaler vi at indstille alle parametre for injektion via GUI(Figur 1D),før vævet er klar, for at reducere unødvendig ventetid. Se den supplerende fil for at få foretaget fejlfinding.
I tilfælde af langsigtet skivekultur kan trin efter den automatiserede mikroinjektionsprocedure påvirke cellernes sundhed og dermed eksperimentet. Derfor anbefales det stærkt at køre en kvalitetskontroltest og optimere snitkulturforholdene. For at evaluere cellernes levedygtighed efter udskærings- og injektionsproceduren udførte vi EdU-mærkning under kulturen, og vi kvantificerede antallet af pyknotiske kerner (en proxy for apoptotiske celler) i kulturerne og injiceret væv12. Disse kvantificeringer afslørede ingen væsentlig indvirkning af mikroinfektion på vævs levedygtighed (figur 2C). Vi anbefaler at køre lignende kvalitetskontrol, samtidig med at der etableres organotypiske vævsskærings- og mikroinjektionsrørledning i laboratoriet.
Sammenlignet med manuel mikroinjektion giver mikroinjektionsrobotten flere fordele. For det første er indlæringskurven for brugeren mindre stejl i forhold til manuel injektion: en ny bruger vil nå et højt færdighedsforløb efter et begrænset antal sessioner, typisk 1 eller 2. For det andet kræver en tilsvarende færdighed i tilfælde af manuel mikroinjektion måneders træning. Injektionsproceduren er hurtigere og mere effektiv (Figur 2B). Vi kvantificerede disse parametre og fandt ud af, at mikroinjektionsrobotten overgik en dygtig manuel bruger med hensyn til injektionssucces (% af vellykket injektion/samlet antal injektioner) og i det samlede antal injektioner pr.tidsenhed 12. Dette resulterer i en samlet 300% stigning i injektionseffektiviteten (% af vellykket injektion/min.) for mikroinjektionsrobotten sammenlignet med en dygtig bruger. Stigningen i effektivitet var endnu mere udtalt, når man sammenligner mikroinjektion robot med en nybegynder bruger og nåede 700%. Sidst men ikke mindst kan mikroinfektionsrobotten nemt programmeres til systematisk at udforske alle rumlige parametre. Dette er især fordelagtigt, når mikroinjektionsrobotten tilpasses nye celler eller væv, eller når mikroinjektionsrobotten bruges til formål, der kræver forskellig rumlig opløsning.
Opbygning af mikroinjektionsrobotten kræver minimale ændringer af et eksisterende epi-fluorescensmikroskop12. Vi har tidligere givet instruktioner til denne tilpasning på https://github.com/bsbrl/Autoinjector. Når hardwaren er konfigureret, giver denne protokol vigtige metodologiske detaljer for at foretage automatiserede mikroinjektioner. Samlet set mikroinjektion robot har en vellykket injektion sats på 15,52 + 2,48 injektioner / min, hvilket er 15x større end en uerfaren bruger (1,09 ± 0,67 injektioner / min), og 3x større end en ekspert bruger (4,95 ± 1,05 injektioner / min)12. Denne forbedring i vellykket injektion sats giver både nybegyndere og ekspert brugere til at injicere flere celler i en kortere tid, som er afgørende for at bevare væv levedygtighed. Derudover kan mikroinjektionsrobotten tilpasses, og bøjningsdybden, injektionstallet, antallet af injektioner, afstanden mellem injektionerne kan alle indstilles ved hjælp af GUI'en. Disse funktioner gør det muligt at bruge mikroinjektionsrobotten som et værktøj til at optimere tidligere besværlige eksperimenter og til at udforske grundlæggende nye eksperimenter, der kræver højere udbytte end tidligere muligt.
De vigtigste begrænsninger i mikroinjektionsproceduren, vi beskrev her, er relateret til fremstilling af vævsskiver, et afgørende skridt, der kræver omfattende optimering. Desuden er mikroinjektion afhængig af tilstedeværelsen af en overflade, der kan gribes an af glaspipetten. Denne funktion begrænser den type væv og væv steder, der kan målrettes via mikroinjektion ved hjælp af den nuværende opsætning.
Mikroinjektionsrobotten bruger i øjeblikket brightfield imaging og har været anvendt i in vitro hjerne skive præparater. I fremtiden kunne mikroinjektionsrobotten kombineres med 2-fotonbilleddannelse for at øge specificiteten af enkeltcellemålretning in vivo til molekylær- eller farvestofmærkning. Der er allerede gjort en sådan indsats for encellet elektrofysiologi15,16. Den nuværende enhed kræver manuel observation af mikroinjektionsproceduren. Fremtidige versioner kan omfatte strategier for rengøring tilstoppede mikroinjection pipetter17 eller integration af væskehåndtering robotter18 for multiplexed, fuldt autonome microinjections. Disse enheder kan øge omfanget af mikroinjektion af størrelsesordener. Tilpasning af algoritmer til parallel kontrol af flere mikroinjektionspipetter19 kunne muliggøre multiplexed levering af snesevis af farvestoffer og molekylære reagenser til de samme celler i de samme eksperimenter. Dette har potentiale til at åbne nye muligheder for molekylær screening i væv.
Mikroinjektionsrobotten kan bruges til at mærke funktionelt identificerede celler ved hjælp af DNA- eller RNA-stregkoder. Dette kan igen kombineres med andre enkeltcelleanalyseteknikker, såsom enkeltcelle-RNA-sekvensering (scRNAseq) og elektronmikroskopi. Vores foreløbige resultater viser, at mikroinjected celler og deres afkom kan inddrives og isoleres ved hjælp af væv dissociation efterfulgt af FACS sortering (Taverna, ikke-offentliggjorte resultater). FACS-sorterede celler kan derefter bruges til scRNAseq. Desuden viser de foreløbige resultater, at mikroinktionrobottens enkeltcelleopløsningskapacitet kan anvendes i kombination med elektronmikroskopisk analyse til at udforske cellebiologien på neurale stamceller i væv ved høj rumlig opløsning (Taverna og Wilsch-Bräuninger, ikke-offentliggjorte resultater). Disse data tyder på, at mikroinjektionsrobotten kan bruges som et redskab til korrelativt lys og elektronmikroskopi i væv og i bredere forstand til multimodal analyse af celleidentitet og adfærd i væv.
Microinjection er afhængig af brugen af tryk, og man har råd til at injicere løsninger med høj molekylær kompleksitet (f.eks. en hel transskription). Denne funktion af mikroinjektion er blevet udnyttet i fortiden til isolering og kloning ligand-gated receptorer20. Langs denne linje kan mikroinjektionsrobotten bruges til modellering og studier af multi-genic træk på celleniveau. Kombineret med en sub-pooling strategi, mikroinjection robot kan også bruges som en platform til at identificere det mindste sæt af gener, der driver en bestemt egenskab / cellulære adfærd. Hidtil har mikroinjektionsrobotten været brugt til at manipulere cellens biokemi via levering af mRNA, DNA eller rekombinant proteiner10,21,22. Vi forudser en anvendelse af mikroinjektionsrobotten ved sondering af biofysik i det intracellulære rum, for eksempel ved at levere nanomaterialer eller nanomaskiner, der tillader sensing og/eller manipulation af de biofysiske egenskaber i det intracellulære rum.
Forfatterne har intet at afsløre.
Forfatterne vil gerne anerkende Nomis Foundation (ET). SBK anerkender midler fra maskinindustrien, College of Science and Engineering, MnDRIVE RSAM initiativ fra University of Minnesota, Minnesota institut for videregående uddannelse, National Institutes of Health (NIH) 1R21NS103098-01, 1R01NS111028, 1R34NS11654, 1R21NS112886 og 1R21 NS111196. GS blev støttet af National Science Foundation Graduate Research Fellowship og NSF IGERT uddannelse tilskud.
| Name | Company | Catalog Number | Comments |
| Chemicals | |||
| Agarose, Low Melt | Carl Roth | Cat# 6351.2 | |
| Agarose, Wild Range | Sigma-Aldrich | Cat# A2790 | |
| Best-CA 221 Glue | Best Klebstoffe GmbH & Co.KG | Cat# CA221-10ml | |
| B-27 Supplement | Thermo Fisher Scientific | Cat# 17504044 | |
| Cellmatrix Type-IA (Collagen, Type !) | FUJIFILM Wako Chemicals | Cat# 637-00653 | |
| Distilled Water | |||
| DMEM-F12, CO2 independent (w/o Phenol red) | Sigma-Aldrich | Cat# D2906 | |
| DMEM-F12, CO2 independent (with Phenol red) | Sigma-Aldrich | Cat# D8900 | |
| HEPES-NAOH, pH 7.2, 1M (HEPES buffer) | Carl Roth | Cat# 9105.3 | |
| L-Glutamine, 200 mM | Thermo Fisher Sientific | Cat# 25030024 | |
| Mowiol 4-88 | Sigma-Aldrich | Cat# 81381 | |
| N-2 Supplement | Thermo Fisher Scientific | Cat# 17502048 | |
| Neurobasal Medium | Thermo Fisher Scientific | Cat# 21103049 | |
| Nuclease-free water | Thermo Fisher Scientific | Cat# AM9937 | |
| O2 (40%), CO2 (5%), N2 (55%) Mix, 50 liters | |||
| Paraformaldehyde | Merck | Cat# 818715 | |
| PBS | |||
| Penicillin-Streptomycin (10,000 U/mL) | Thermo Fisher Scientific | Cat# 15140122 | |
| Rat serum | Charles River Laboratories | ||
| Japan | |||
| Sodium bicarbonate (NaHCO3) | Merck | Cat# 106323 | |
| Sodium hydroxide (NaOH) | Merck | Cat# 106482 | |
| Tyrode’s salt | Sigma | Cat# T2145-10x1L) | |
| Equipment | |||
| Borosilicate glass capillaries, 1.2 mm outer diameter x 0.94 mm inner diameter | Sutter Instruments | Cat# BF-120-94-10 | |
| Bottle-top filter system, 500 mL | Corning | Cat# 430769 | |
| Computer PC | |||
| Custom pressure rig | Custom pressure rig | ||
| Electronic pressure regulator | Parker Hannifin | Cat# 990-005101-002 | |
| Falcon tubes, 15 mL | Corning | Cat# 430791 | |
| Falcon tubes, 50 mL | Corning | Cat# 430829 | |
| Fine-tip paintbrush | |||
| Flaming/ Brown micropipette puller | Sutter Instruments | Cat# P-97 | |
| Forceps, Dumont no. 3 | Fine Science Tools | Cat# 11231-30 | |
| Forceps, Dumont no. 5 | Fine Science Tools | Cat# 11255-20 | |
| Forceps, Dumont no. 55 | Fine Science Tools | Cat# 11252-20 | |
| Heating block | Labtech International | Cat # Dri block Digi2 | |
| Inverted fluorescence microscope | Zeiss | Cat# Axiovert 200 | |
| Light source | Olympus | Cat# Highlight 3100 | |
| Manual pressure regulator | McMaster Carr | Cat# 0-60 PSI 41795K3 | |
| Microloader Tips | Eppendorf | Cat# 5242956.003 | |
| Microcontroller | Arduino | Cat# Arduino Due | |
| Microscope camera Hamamatsu Orca Flash 4.0 V3 | |||
| Motorized stage XY for microscope | |||
| Multiwell plate, 24 wells | Nunc | Cat# 142475 | |
| Pasteur pipettes, plastic | |||
| Petri dish, 60 x 15 mm | Greiner | Cat# 628102 | |
| Petri dish, 35 x 10 mm | Nunc | Cat# 153066 | |
| Petri dish, 34 x 14 mm, including Microwell no. 1.5 cover glass | MatTek | Cat# P35G-1.5-14-C | |
| Pipette holder | Warner Instruments | Cat# 64-2354 MP-s12u | |
| Pipette and tips | |||
| Puller filament, 3.0-mm square box filament | Sutter Instrument | Cat# FB330B | |
| Slice culture incubation box | MPI-CBG | Cat# custom made | |
| Solenoid valve | Cat# LHDA053321H-A | ||
| Stereomicroscope | Olympus | Cat# SZX12 | |
| Tabletop centrifuge | Heraeus | Cat# 5431622 | |
| Thermometer | |||
| Three-axis Manipulator | Sensapex Inc | Cat# tree-axis uMP | |
| Vibratome | Leica | Cat# VT1000s | |
| Whole-embryo-culture-system incubator | Ikemoto Company | Cat# RKI-10-0310 | |
| Waterbath | |||
| Software and Algorithms | |||
| Arduino | Arduino | ||
| Fiji | RRID: SCR_002285 | ||
| Python | Python Software foundation | Python 2.7.12 | |
| ZEN | RRID: SCR_013672 |
- Taverna, E., Götz, M., Huttner, W. B. The Cell Biology of Neurogenesis: Toward an Understanding of the Development and Evolution of the Neocortex. Annual Review of Cell and Developmental Biology. 30 (1), 465-502 (2014).
- Götz, M., Huttner, W. B. The cell biology of neurogenesis. Nature Reviews Molecular Cell Biology. 6 (10), 777-788 (2005).
- Di Lullo, E., Kriegstein, A. R. The use of brain organoids to investigate neural development and disease. Nature Reviews Neuroscience. 18 (10), 573-584 (2017).
- Lancaster, M. A., Knoblich, J. A. Organogenesisin a dish: Modeling development and disease using organoid technologies. Science. 345 (6194), 1247125 (2014).
- Kretzschmar, K., Clevers, H. Organoids: Modeling Development and the Stem Cell Niche in a Dish. Developmental Cell. 38 (6), 590-600 (2016).
- Pepperkok, R. et al. Automatic microinjection system facilitates detection of growth inhibitory mRNA. Proceedings of the National Academy of Sciences of the United States of America. 85 (18), 6748-6752 (1988).
- Pepperkok, R., Lowe, M., Burke, B., Kreis, T. E. Three distinct steps in transport of vesicular stomatitis virus glycoprotein from the ER to the cell surface in vivo with differential sensitivities to GTPγS. Journal of Cell Science. 111 (13), 1877-1888 (1998).
- Pepperkok, R. et al. β-COP is essential for biosynthetic membrane transport from the endoplasmic reticulum to the Golgi complex in vivo. Cell. 74 (1), 71-82 (1993).
- Ansorge, W., Pepperkok, R. Performance of an automated system for capillary microinjection into living cells. Journal of Biochemical and Biophysical Methods. 16 (4), 283-292 (1988).
- Taverna, E., Haffner, C., Pepperkok, R., Huttner, W. B. A new approach to manipulate the fate of single neural stem cells in tissue. Nature Neuroscience. 15 (2), 329-337 (2012).
- Wong, F. K., Haffner, C., Huttner, W. B., Taverna, E. Microinjection of membrane-impermeable molecules into single neural stem cells in brain tissue. Nature Protocols. 9 (5), 1170-1182 (2014).
- Shull, G., Haffner, C., Huttner, W. B., Kodandaramaiah, S. B., Taverna, E. Robotic platform for microinjection into single cells in brain tissue. EMBO Reports. 20 (10), e47880 (2019).
- Jabeen, S., Thirumalai, V. The interplay between electrical and chemical synaptogenesis. Journal of Neurophysiology. 120 (4), 1914-1922 (2018).
- Nagy, J. I., Pereda, A. E., Rash, J. E. Electrical synapses in mammalian CNS: Past eras, present focus and future directions. Biochimica et Biophysica Acta - Biomembranes. 1860 (1), 102-123 (2018).
- Suk, H.J. et al. Closed-loop real-time imaging enables fully automated cell-targeted patch-clamp neural recording in vivo. Neuron. 95 (5), 1037-1047 (2017).
- Annecchino, L. A. et al. Robotic automation of in vivo two-photon targeted whole-cell patch-clamp electrophysiology. Neuron. 95 (5), 1048-1055 (2017).
- Kolb, I. et al. Cleaning patch-clamp pipettes for immediate reuse. Scientific Reports. 6, 35001 (2016).
- Holst, G. L. et al. Autonomous patch-clamp robot for functional characterization of neurons in vivo: development and application to mouse visual cortex. Journal of Neurophysiology. 121 (6), 2341-2357 (2019).
- Kodandaramaiah, S. B. et al. Multi-neuron intracellular recording 1 in vivo via interacting autopatching 2 robots. ELife. 7, 24656 (2018).
- Lubbert, H. et al. cDNA cloning of a serotonin 5-HT1c receptor by electrophysiological assays of mRNA-injected Xenopus oocytes (RNA fractionation/hybrid depletion/hybrid selection/choroid plexus/voltage clamp). Neurobiology. 84 (2) 4332-4336 (1987).
- Florio, M. et al. Human-specific gene ARHGAP11B promotes basal progenitor amplification and neocortex expansion. Science. 347 (6229), 1465-1470 (2015).
- Kalebic, N. et al. CRISPR/Cas9-induced disruption of gene expression in mouse embryonic brain and single neural stem cells in vivo. EMBO Reports. 17 (3), 338-348 (2016).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved