Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Bioengineering
Manipulation av single neurala stamceller och nervceller i hjärnan skivor med hjälp av Robotic Microinjection
Detta protokoll visar användningen av en robotplattform för microinjection i enstaka neurala stamceller och nervceller i hjärnan skivor. Denna teknik är mångsidig och erbjuder en metod för att spåra celler i vävnad med hög rumslig upplösning.
En central fråga i utvecklingsneurobiologi är hur neurala stam- och progenitorceller bildar hjärnan. För att besvara denna fråga, måste man märka, manipulera, och följa enstaka celler i hjärnvävnaden med hög upplösning över tiden. Denna uppgift är extremt utmanande på grund av komplexiteten i vävnader i hjärnan. Vi har nyligen utvecklat en robot, som guidar en mikroinjektionsnål till hjärnvävnad när vi använder bilder som förvärvats från ett mikroskop för att leverera femtolitervolymer av lösning till enstaka celler. Robotdriften ökar resulterande en övergripande avkastning som är en storleksordning större än manuell mikroinjektion och möjliggör exakt märkning och flexibel manipulering av enstaka celler i levande vävnad. Med detta kan man mikroinjekta hundratals celler i en enda organotypisk skiva. Denna artikel visar användningen av microinjection roboten för automatiserade microinjection av neurala stamceller och nervceller i hjärnan vävnad skivor. Mer allmänt, Det kan användas på någon epitelial vävnad med en yta som kan nås av pipetten. När den har ställts in kan mikroinjektionsroboten utföra 15 eller fler mikroinjektioner per minut. Microinjection roboten på grund av dess genomströmning och mångsidighet kommer att göra mikroinjektion en i stort sett okomplicerad högpresterande cell manipulation teknik som ska användas i bioteknik, bioteknik och biofysik för att utföra encelliga analyser i organotypiska hjärnan skivor.
Detta protokoll beskriver användningen av en robot för att rikta och manipulera enstaka celler i hjärnvävnad skivor, med fokus i synnerhet på enstaka neurala stamceller och nervceller. Roboten utvecklades för att ta itu med en central fråga i utvecklingsneurobiologi, det är hur neural stam och stamceller bidrar till hjärnans morfogenes1,2,3,4,5. För att besvara denna fråga, måste man märka och spåra enda neurala stamceller och följa deras härstamning progression över tiden att korrelera enda cell beteende med vävnad morfogenes. Detta kan uppnås på olika sätt, t.ex., genom att elektroporera hjärnvävnad in utero eller genom att märka encelliga med hjälp av lipofila dör. Även kraftfull, dessa metoder saknar exakt enda cell upplösning (electroporation) och/eller möjligheten att manipulera det intracellulära utrymmet (lipofilt färgämne). Microinjection i enstaka celler utvecklades för att övervinna denna utmaning6,7,8. Under mikroinjektion sätts en pipett kort i en enda cell inom intakt vävnad under tryck till mikroinject femtolitervolymer av reagenser9. Vi har tidigare beskrivit ett manuellt förfarande för mikroinjecting enda neurala stamceller i organotypisk vävnad (Figur 1A)10,11. Mikroinjektion i neurala stamceller bygger på användning av en mikropipette som sätts in i enstaka neurala stamceller för att injicera en lösning som innehåller ett fluorescerande färgämne, tillsammans med andra molekyler av intresse. Den selektiva inriktningen av neurala stamceller uppnås genom att närma sig den utvecklande telencephalon via ventrikulära ytan (eller ventrikeln, se tecknad serie i figur 1A), som bildas av den apikala plasmamembran av apikala progenitorer (tecknad i figur 1A). Denna process måste upprepas för varje cell som försökssprutaren önskar att injicera. Vidare är framgången för mikroinjektion beroende av den exakta kontrollen av djupet och varaktigheten av mikropipetteinjektion i vävnaden. Således, trots de unika fördelarna, är manuell mikroinjektion extremt tråkigt och kräver betydande praxis för att utföra på rimliga genomströmning och avkastning, vilket gör denna teknik svår att använda på ett skalbart sätt. För att övervinna denna begränsning har vi nyligen utvecklat en bildstyrd robot, Autoinjector12 (eller microinjection robot) som automatiskt kan utföra mikroinjektioner i enstaka celler.
Mikroinjektionsroboten använder sig av mikroskopiska bild- och datorseendealgoritmer för att exakt rikta in sig på specifika platser i 3D-rymd inom vävnad för mikroinjektion (Figur 1B). Mikroinjektionsroboten kan konstrueras genom att göra relativt enkla modifieringar av en befintlig mikroinjektionsuppställning. Mikroinjektionsrobotens övergripande schematiska schema visas i figur 1C. En pipetter är monterad i en pipetthållare som är fäst vid en treaxlad manipulator. En mikroskopkamera används för att skaffa bilder av vävnaden och mikroinjektionsnålen. Ett anpassat tryckregleringssystem används för att kontrollera trycket inuti pipetten och en programmerbar mikromanipulator används för att kontrollera positionen för mikroinjektorpipetten. Kamerabilderna av vävnaden och mikroinjektionspipetten används för att bestämma den rumsliga placeringen av mikroinjektionspipetsspetsen och de platser där mikroinjektioner behöver utföras. Programvaran beräknar sedan banor som behövs för att flytta pipetten i vävnaden. All hårdvara styrs av den programvara som vi tidigare utvecklat. All programvara är skriven på kodningsspråk (t.ex. Python och Arduino) och kan laddas ner från https://github.com/bsbrl/Autoinjector med instruktioner. Det grafiska användargränssnittet (GUI) gör det möjligt för användaren att avbilda vävnaden och mikropipettet, och att anpassa banan för mikroinjektion. Vårt system kan upprättas med hjälp av relativt enkla modifieringar av ett inverterat mikroskop utrustat med ljusfält och epi-fluorescensfilter.
Först ger vi instruktioner om att förbereda hjärnan organotypiska vävnad skivor för microinjection. Sedan protokollet illustrerar starta microinjection robot följt av förberedande steg, såsom pipett rörelsekalibrering, som måste göras före mikroinjektion. Detta följs genom att man definierar injektionsparametrarna. Efter detta kan användaren definiera banan som används av mikroinjektionsroboten och starta injektionsproceduren. Den mikroinjekerade vävnaden (i detta fall hjärnan organotypiska vävnad skivor) kan hållas i kultur för olika tidsperioder beroende på den experimentelladesignen 10,11. Vävnaden kan bearbetas för att följa och studera identitet och ödet för de injicerade cellerna och deras avkomma. Alternativt kan de mikroinjekerade cellerna följas med hjälp av live-avbildning. Inom ramen för detta protokoll, visar vi användningen av roboten för att automatiskt microinjection neurala stamceller i organotypiska skivor av musen E14.5 dorsala telencephalon. Roboten är ytterligare kan mikroinjection i nyfödda nervceller i musen telencephalon, liksom i den mänskliga fetala telencephalon12.
Sammanfattningsvis beskriver vi en robotplattform som kan användas för att följa och manipulera enstaka celler i vävnad. Plattformen använder sig av tryck och det är därför extremt mångsidig när det gäller den kemiska karaktären hos föreningen att injicera. Dessutom kan den anpassas till andra målceller än stamceller. Vi förväntar oss att vårt system enkelt anpassas till andra modellsystem också.
Alla djurstudier genomfördes i enlighet med tysk djurskyddslagstiftning, och de nödvändiga licenserna erhölls från den regionala Etiska kommissionen för djurförsök i Dresden, Tyskland (Tierversuchs, Landesdirektion Dresden). Organotypiska skivor framställdes från E14.5 eller E16.5 C57BL/6 mus embryonala telencephalon (Janvier Labs).
1. Installation av programvara
- Följ instruktioner för att installera programvaran från https://github.com/bsbrl/Autoinjector.
2. Beredning av reagenser och pipetter
- Agarose: Bered 3% agaros genom att separat lösa upp 3 g brett spektrum agaros och 3 g lågsmältpunkt agaros i 100 mL cellkultur-grade PBS i två separata 200 mL glasflaskor, respektive. Förvaras i rumstemperatur i upp till 3 månader.
- Tyrodelösning: Lös 1 g natriumbikarbonat och Tyrodes salt (använd innehållet i hela flaskan) och 13 mL på 1 M HEPES i 1 L destillerat vatten. Justera pH-värdet till 7,4. Filtrera lösningen genom ett 0,2 μm flask-top-filter.
- Skiva odlingsmedium (SCM): Tillsätt 10 mL råttserum, 1 mL av 2 mM glutamin, 1 mL penicillin-streptomycin (100x), 1 mL av N-2 tillägg (100x), 2 mL av B27 tillägg (50x) och 1 mL hepes (pH 7.3) buffert till 84 mL av Neurobasal medium. Alikvot 5 mL av SCM i 15 mL rör. Förvaras vid -20 °C.
- CO2-Independent Microinjection Medium (CIMM): Förbered 5x DMEM modifierad lågglukoslösning (utan fenolrött) genom att lösa upp pulvret i 200 mL destillerat vatten. Filtrera lösning genom ett 0,2 μm flask-top filter (för DMEM-pulvret, använd innehållet i hela flaskan). För att förbereda 100 mL CIMM, blanda 20 mL 5x DMEM modifierad lösning, 1 mL HEPES buffert, 1 mL av N2-tillägg (100x), 2 mL B27-tillägg (50x), 1 mL penicillin-streptomycin (100x), 1 mL på 2 mM glutamin och 74 mL destillerat vatten. Förvara lösningen vid 4 °C.
- Rekonstitutionsbuffert: Förbered rekonstitutionsbufferten genom att lösa upp 262 mM NaHCO3, 0,05 N NaOH, 200 mM HEPES i destillerat vatten. Sterilisera lösningen genom filtrering genom ett flasktopp 0,22 μm-filtersystem till en steril glasflaska. Alikvot 500 μL rekonstitutionsbuffert till lufttäta mikrocentrifugrör. Förvaras vid 4 °C.
- Mikroinjektionsfärgämneslager: Lös upp den fluorescerande märkta Dextran i RNase fritt destillerat vatten (slutkoncentration 10 μg/μL). Förbered 5 μL alikvoter och förvara vid -20 °C tills användning.
- Dra mikroinjektionspipetterna från kapillärer av borosilikatglas (1,2 mm ytterdiameter, 0,94 mm innerdiameter) med hjälp av mikropipettedragaren. Skydda pipetterna mot damm. Förvara inte pipetter i mer än 2 – 3 dagar. För detta experiment var de dragparametrar VÄRME: ramp temperatur +1 – 5; DRAG: 100; VEL: 110; DEL: 100. HEAT och VEL är de parametrar som påverkar pipettens mest form och storlek.
OBS: Den optimala mikroinjektionspipetten har en lång och flexibel spets, för att undvika cellskador vid mikroinjektion.
3. Beredning av vävnadsskiva
- Smält den 3% brett spektrum agaros med hjälp av en mikrovågsugn före hjärnvävnaden dissekering. Låt inte agaros stelna genom att hålla i ett vattenbad vid 37 °C före ingjutning. Se till att pipetterna skyddas mot damm. Förvara inte pipetter i mer än 2 – 3 dagar.
- Tina en alikvot av SCM och varm 10 – 12 mL CIMM och 20 mL av Tyrodes lösning till 37 °C med hjälp av ett vattenbad.
- Blanda den fluorescerande spårämne (Dextran-3000 eller Dextran-10000-Alexa konjugerad; slutkoncentration 5 – 10 μg/μL) med de övriga kemiska(n) som skall injiceras. Centrifugera mikroinjektionslösningen vid 16, 000 x g i 30 min vid 4 °C. Samla in supernatanten och överför till ett nytt rör. Håll mikroinjektionslösningen på is tills användning.
- Använd huvudena från E13.5 – E16.5-musembryon för att förbereda organotypiska vävnadsskivor av telencefalon. Ta bort huden och öppna skallen med hjälp av tång, rör sig längs mittlinjen. Dissekera ut den embryonala hjärnan från den öppna skallen och ta bort hjärnhinnorna som täcker hjärnvävnaden från den ventrala sidan av hjärnan. Lämna den dissekerade hela hjärnan i Tyrodes lösning på ett 37 °C-värmeblock.
OBS: Alla dissektionssteg som beskrivs i 3.4 måste utföras i prewarmed Tyrodes lösning. - Häll det breda sortiment smält agaros i en disponibel inbäddning mögel. När agaros kyls till 38 – 39 °C, för försiktigt över hjärnorna (högst 4) till den med hjälp av en Pasteurpipett. Använd alltid skärspetsar för detta steg.
- Rör om i agarose runt vävnaden antingen med hjälp av en spatel eller ett par Dumont #1 tövappar utan att röra vävnaden. Låt agaros stelna i rumstemperatur. När agaros har stelnat, trimma överskottet uppstod som omger vävnaden.
- Fyll buffertfacket med PBS. Orient hjärnan med rostro-caudal axeln av vävnaden vinkelrätt mot facket (använd som landmärke luktglödlampor, som representerar rostral-mest delen av hjärnan). Skär 250 μm skivor med hjälp av en vibratom.
- Fyll en 3,5 cm Petriskål med 2 mL förvärmda media. Med hjälp av en pasteurpipett av plast överför du skivor (10 - 15) till denna maträtt. När du är klar, flytta Petri skålen med skivor i skiva kultur inkubator. Underhåll skivor vid 37 °C i en befuktad atmosfär som innehåller 40% O2 / 5% CO2 / 55% N2 tills användning.
4. Mikroinjektion
- Slå på datorn, mikroskop, mikroskopkamera, manipulatorer, tryckrigg och trycksensor. Ladda programmet genom att klicka på filen "launchapp.py" i huvudmappen som hämtats från GitHub och ange enhetsinställningarna i popup-skärmen (se anvisningar för installation av steg 1.1).
- Skapa ett utåttryck för att förhindra oönskad igensättning innan du dränker ner pipetten i lösningen. För att utöva tryck på pipetten, skjuter du kompensationstryckfältet till 24 – 45 % och klickar på Ange värden. Därefter ställer du in trycket på ett tillräckligt tryck genom att vrida den mekaniska tryckventilsratten till 1 – 2 PSI (69 – 138 mbar) som indikeras av tryckgivaren.
- Överför skivorna till en 3,5 cm Petriskål som innehåller 2 mL förvärkad CIMM. Placera skivorna som ska mikroinjected i mitten av petriskålen. Överför petriskålen till det förvärmda (37 °C) mikroinjektionsstadiet.
- Ladda mikroinjektionspipettet med 1,4 –1,6 μL mikroinjekterad lösning (från steg 3.3) med hjälp av en långspets plastpipett. Sätt in mikroinjektionspipetten på pipetthållaren.
- Med hjälp av den lägsta förstoringen på mikroskopet, föra segmentet i fokus och styra mikropipettet till detta synfält (FOV) så att den är inriktad på samma plan som skiva målet. Växla utdata från mikroskopet till kameran för att se FOV i ansökan.
- Klicka på förstoringsknappen uppe till vänster i gränssnittet för att initiera kalibrering av enheten. Ett fönster kommer att uppmana att välja förstoringen. Välj 10x förstoring, eller vad förstoring linsen är inställd på (t.ex. 4x, 10x, 20x, 40x) och tryck ok. Programvaran förutsätter den interna objektiva linsen är 10x (den vanligaste objektiva objektivet förstoring).
- Fokusera om pipettspetsen med hjälp av mikroskopets mikrometriska hjul och klicka på pipettspetsen med markören. Därefter trycker du på knappen steg 1.1 och trycker på OK i popup-fönstret. Pipetten kommer att röra sig i Y riktning. Klicka på pipettens spets och tryck på knappen steg 1.2. Slutligen, ange 45 i Pipette vinkel rutan och tryck på Set vinkel.
- Ange önskade parametrar i panelen Automatiserade mikroinjektionskontroller. För mikroinjektion i apikala progenitorer ställa in injektionsavståndet till 20 – 40 μm och djup till 10 – 15 μm. För mikroinjektion i nervceller som injektionen avståndet 30 – 40 μm från basalsidan, och djup till 10 – 30 μm beroende på vad som är riktade. Ställ alltid in hastigheten till 100%. Klicka på Ange värden.
OBS: Inflygningsavståndet är avståndet pipetten drar ut ur vävnaden innan du flyttar till nästa injektionsavstånd, djup är djupet in i vävnad mikroinjektionen går, avstånd är avståndet längs linjen mellan sekventiella injektioner, hastighet är pipettens hastighet i μm/s. - Klicka på knappen Rita kant och dra markören längs önskad bana i popup-fönstret för att definiera banan för injektion. För stamceller från mikroinjecting progenitor är telencefalonytans ventrala sida riktad enligt figur 2A. För pipetten till linjens start och klicka på spetsen på pipetten. Klicka på Kör bana för att starta mikroinjecting. Upprepa detta steg för varje plan av injektion riktade (vanligtvis gjort för 3 – 4 plan med 40 – 75 injektioner per plan).
5. Vävnadskultur och bearbetning av vävnadsskivor för immunofluorescens
- Förbered kollagenblandningen (1,5 mg/mL): Till ett rör tillsätt 1,25 mL av matrislösningen, 0,5 mL destillerat vatten, 0,5 mL 5x DMEM-F12-lösning och 0,25 mL rekonstitutionsbuffert. Håll den på is tills den används.
- Erhåll petriskålen som innehåller de mikroinjekterade skivorna från snittodlingsinkubationskammaren och sänk ned skivorna i kollagenblandningen.
- Överför skivorna tillsammans med 200 – 300 μL kollagenblandning till en 14 mm brunn av en 35 mm glas-bottenskål. Se till att skivorna är täckta av mycket mindre kollagen. Denna uppsättning möjliggör de optimala förutsättningarna för näringsämnen och syreupptagning.
- Orientera skivorna samtidigt som du ser till att det finns tillräckligt med utrymme mellan skivorna med hjälp av två par typpor. Inkubera Petri-skålen i 5 min vid 37 °C med hjälp av ett värmeblock för att ge kollagenet möjlighet att stelna. Betrakta den här gången som t = 0 av segmentkultur.
- Flytta petriskålen tillbaka till skiva kultur inkubatorn för ytterligare 40 min. Tillsätt sedan 2 mL av den förvärmda SCM. Skivor hålls i kultur tills önskad tidpunkt.
- Ta skivorna ur skiva kultur inkubator och aspirera SCM. Tvätta de kollageninbäddade skivorna med 1x PBS. Tillsätt 4% (wt/vol) paraformaldehyd (i 120 mM fosfatbuffert, pH 7,4) och lämna vävnaden vid RT i 30 min. Flytta den sedan till 4 °C för att möjliggöra fixering över natten.
- Aspirera paraformaldehydlösningen nästa dag och utför 1x PBS tvättar. För att ta bort skivorna från kollagenet, använd två par tlyktor för att försiktigt extrahera skivorna under ett stereomikroskop.
- Använd en mikrovågsugn för att smälta den låga smältpunkten på 3 % (wt/vol) för bearbetning av mikroinjected slices. Häll den smälta agaros i en disponibel ingjutning mögel och låt den svalna till runt 38 – 39 °C .
- Överför vävnadsskivorna från steg 5.7 till denna form som innehåller låg smältnings uppstod med hjälp av en pasteurpipett av plast. Se till att pialsidan av skivan är uppåt och ventrikulära ytan är vänd nedåt. Om det behövs orientera därefter. Låt agaros svalna till RT för att stelna.
- Trimma den extra agarose som omger skivorna. Orientera agarosblocket för att säkerställa att snittytan är parallell med vibratomens skärblad. Använd vibratom, skär 50 μm tjocka sektioner.
- Fyll en 24 brunnsfat med 1x PBS. Överför sektionerna i denna maträtt med hjälp av en fin-tip pensel. Utför immunofluorescens enligt standardprotokollen.
Microinjection tjänar syftet att spåra och manipulera enstaka neurala stamceller och deras avkomma i levande vävnad och att följa deras härstamning progression i en fysiologisk miljö. I den här artikeln har vi visat användningen av microinjection roboten för inriktning och automatiskt microinjecting organotypic skivor av musen telecephalon. Bild 2 illustrerar representativa bilder av framgångsrikt injicerade stamceller och figur 3 illustrerar injicerade nyfödda nervceller. När det injiceras med Dextran Alexa-488 (eller Alexa-A555) färgämne, celler visas helt fylld med färgämnet. När det gäller apikala progenitorer (Figur 2) möjliggör konfokal avbildning rekonstruera med hög rumslig upplösning cellen morfologi, närvaro -eller frånvaro- av den apikala och basala fästning, och att kombinera den morfologiska förfrågan med markör uttryck. Genom att kombinera dessa kriterier kan användaren tilldela en specifik cell öde till microinjected cellerna och deras avkomma. När det gäller neuron injektion, användaren kan rekonstruera neuronal morfologi, inklusive struktur och funktioner i apikala dendrite och axon. Automatiserad mikroinjektion kan ge betydligt högre genomströmning jämfört med manuell mikroinjektion (Bild 2B). Vidare bekräftar EdU-märkning att cellens bärkraft inte påverkas av automatisering (Bild 2C). Att hålla organotypiska skiva i kultur gör följande härstamning progression av de mikroinjected cellerna (vi visade 4 - 24h i figur 2D). Om mikroinjektionslösningen innehåller genetiskt material (DNA, mRNA, CRISPR-Cas9-guider) eller rekombinanta proteiner, så gör detta det möjligt att studera om och hur härstamningsprogression påverkas av manipuleringen.
Mikroinjektion i enstaka neurala stamceller i vävnad ger utmärkt enda cellupplösning och av den anledningen har den använts för att dissekera cellbiologin för neural stamcellsprogression och ödesövergång (Figur 3A). Microinjektion möjliggör leverans av komplex blandning av kemikalier. Vi har tidigare använt oss av denna funktion för att studera junctional koppling i neurala stamceller genom att blanda gap-junctional permeabla med gap junctional ogenomträngliga fluorescerande färgämnen12. Vi utökade tidigare arbete genom att studera junctional koppling i nyfödda nervceller, genom att injicera Lucifer Yellow tillsammans med Dextran-A555 (Figur 3B). Som visas i figur 3B, en andel av nyfödda pyramidala nervceller kopplas via gap korsningar till angränsande nervceller. Denna iakttagelse är förenlig med tanken att omogna nervceller kommunicera via gap-junction13,14. Dessutom visar inriktning nervceller att användningen av microinjection roboten kan generaliseras till flera celltyper i den utvecklande däggdjur hjärnan. Denna experimentella setup kommer att vara användbart för att dissekera cellbiologi av nervceller i vävnad, till exempel genom att leverera specifika oligopeptider att störa protein-protein interaktioner.
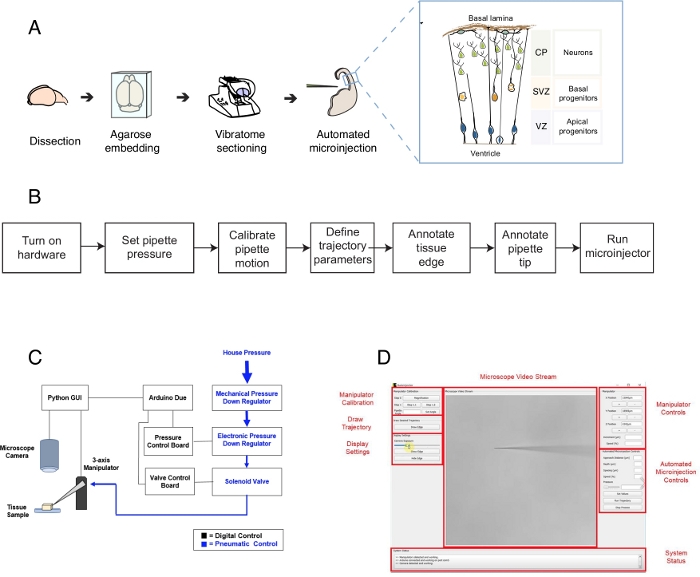
Bild 1: Automatiserad mikroinjektionsinställning och protokoll. (A) Övergripande protokoll för vävnadsberedning och automatiserade mikroinjektioner med hjälp av mikroinjektionsroboten. Rätt infälld: Tecknad schematisk av mus Telencephalon riktade för microinjection i detta protokoll. (B) Flödesschema av de automatiserade mikroinjektionsstegen. (C) Schematiska av microinjection robot hårdvara. (D) Grafiskt användargränssnitt (GUI) av den programvara som används för att styra och driva mikroinjektionsroboten. Denna siffra är anpassad från ref.12. Vänligen klicka här för att visa en större version av denna figur.
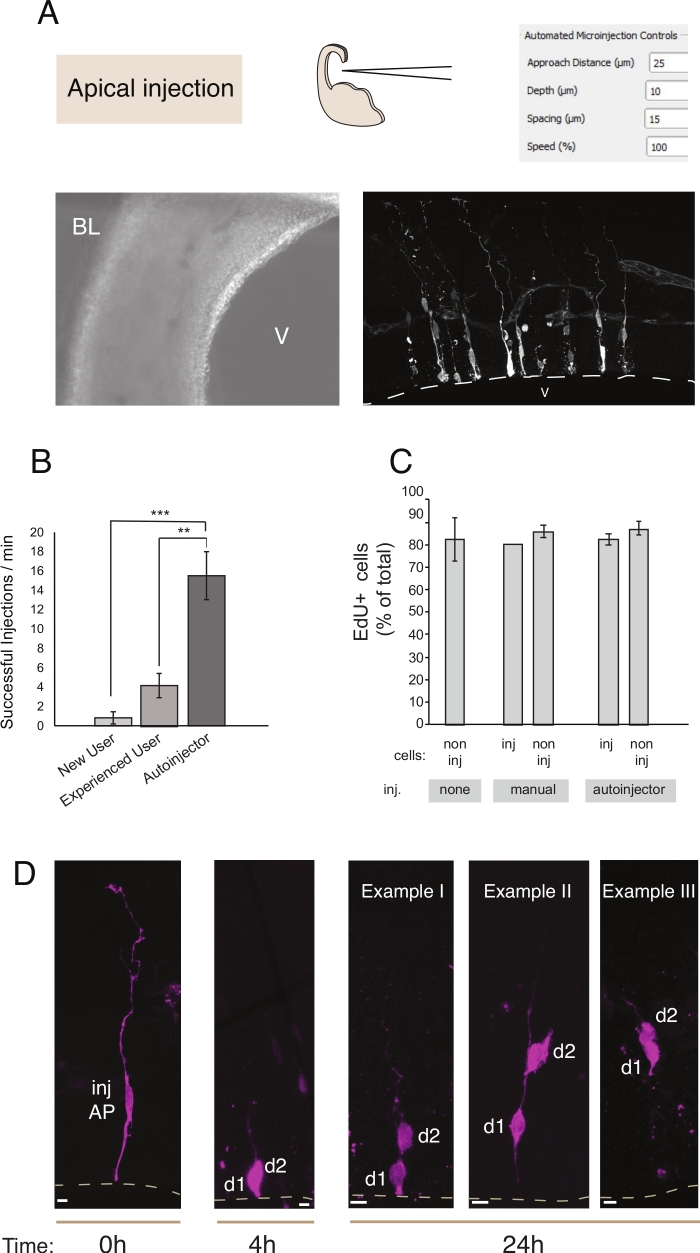
Figur 2: Robotmikroinjektion till apikala progenitorer. Schematiska och förväntade resultat när du använder microinjection-roboten för att rikta apkala progenitorer (APs) via den apikala ytan (apikal injektion). (A) Översta raden. Till vänster: schematisk för processen. Till höger: GUI med relevanta parametrar för apikala injektion. Nedre raden. Till vänster: faskontrastbild som tagits under injektionsproceduren (V: ventrikel; BL: basal lamina). Till höger: representativa resultat som visar microinjected APs. Streckad linje representerar ventrikeln (V). Skala bar: 10 μm. (B) Framgångsrika injektioner per minut för en novis användare på det manuella mikroinjektionssystemet, en erfaren användare på det manuella mikroinjektionssystemet, och mikroinjektionsroboten. (C) EdU-inkorporering i mikroinjekerade celler och i icke injicerade celler i det injicerade området. Organotypiska skivor av mus E14.5 dorsala telencephalon var antingen (i) icke injiceras eller (ii) utsätts för manuell eller automatiserad mikroinjektion (injiceras skiva) med hjälp av Dextran-A488 (för manuell och autoinjector). Skivor hölls i kultur i närvaro av EdU för 24 h, då de var fasta och färgade för DAPI och EdU. Injicerade och icke-injicerade celler i det injicerade området fick poäng för EdU positivitet. (D) Användning av mikroinjection roboten Härstamning spårning. Ett fluorescerande färgämne (Dx3-A555, magenta) injiceras i enstaka neurala stamceller (t = 0 h). Det fluorescerande färgämnet skiljs till dottercellerna (d1, d2) under mitos. Detta möjliggör följande avkomman av den injicerade cellen (t = 4 h och 24 h) och avslöjar härstamningsförloppet över tiden. För t = 24 h, visar vi flera exempel på avkomman man förväntar sig att hitta. Skala barer: 10 μm. Grafer i B och C är hämtade från ref.12 Vänligenklicka här för att visa en större version av denna figur.
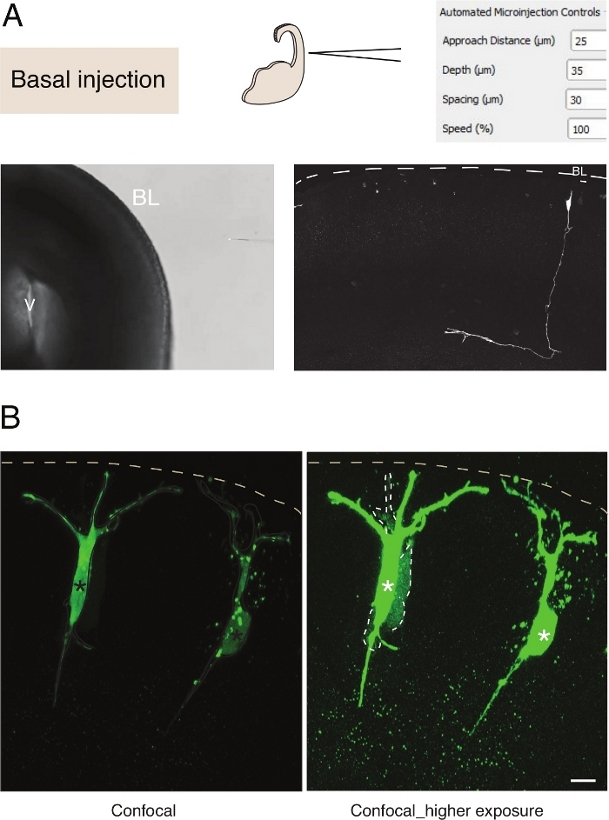
Figur 3: Robotmikroinjektion i nervceller. Schematiska och förväntade resultat när man använder mikroinjektionsroboten för att rikta in sig på pyramidala nervceller (N) via den basala ytan (basal injektion). (A) Översta raden. Till vänster: schematisk för processen. Till höger: GUI med relevanta parametrar för basal injektion. Nedre raden. Till vänster: faskontrastbild som tagits under injektionsproceduren (V: ventrikel; BL: basal lamina). Till höger: representativa resultat som visar en microinjected N. Streckad linje representerar den basala lamina (BL). Skala bar: 10 μm. (B) Användning av autoinjektorn för att studera gap junctional kommunikation i vävnad. Pyramidal nervceller injicerades med en lösning som innehåller två färgämnen: gapet junctional-ogenomtränglig Dx-A555 (visas inte) och gap-junctional permeabla Lucifer Yellow (grön). Dx-A555 är begränsad till den riktade cellen (asterisker), medan LY-spridning till celler som är anslutna via gap junction till den riktade cellen (streckade linjer). Vänster panel: Låg exponering, endast de mikroinjekerade cellerna är synliga. Höger panel: Hög exponering möjliggör visualisering av de injicerade cellerna samt de kopplade cellerna (streckade linjer). Skala bar: 10 μm. Vänligen klicka här för att visa en större version av denna figur.
Kompletterande Fil: Felsökning av flera vanliga fel som uppstår under mikroinjection. Vänligen klicka här för att ladda ner denna fil.
Mikroinjektion i enstaka neurala stamceller i vävnad ger utmärkt encellsupplösning och av den anledningen har den använts för att dissekera cellbiologin för neural stamcellsprogression och ödesövergång (Figur 2; seäven 10,11,12). Den automatiserade mikroinjektionsproceduren kan utföras på andra typer av celler i både embryonala möss och mänsklig hjärnvävnad. Representativa resultat av mikroinjektion av nyfödda nervceller genom att rikta basal ytan av telencephalon visas i figur 3.
Den princip som upprättas här kan tillämpas för att rikta flera olika celltyper i embryonala mus hjärnor och mänskliga hjärnor. Vi har tidigare visat att mikroinjektionsroboten även kan användas för att rikta in sig på enstaka progenitorceller i musens hindbrain och telencefalon och nyfödda nervceller i musen och humana utvecklande neocortex12. För att få bästa resultat av injektionsproceduren bör man optimera alla steg innan injektionen påbörjas. Det är viktigt att noga överväga och optimera beredningen av livskraftiga och välbevarade organotypiska vävnadsskivor från hjärnvävnaden (Figur 1). Det är avgörande att vara snabb i dissektion och skivning förfarande illustreras i figur 1. För apikala injektion inriktning på APs, bör man plocka skivor som visar den idealiska orienteringen av den apikala ytan. För APs injektion är den idealiska orienteringen den apikala ytan vinkelrätt mot botten av petriskålen. Alla andra orientering kommer att vara tillåtande samt, men den apikala ytan vinkelrätt mot Petri-skålen ger en bredare yta för injektion, vilket ökar framgången för injektion. För injektion i nervceller spelar orienteringen av skivan lite eller ingen effekt.
När de skivor som ska injiceras har valts tar injektionsproceduren per skiva cirka 5 minuter. Med tanke på att man arbetar med levande vävnad, det rekommenderas starkt att påskynda injektionsproceduren. För detta ändamål rekommenderar vi att du ställer in alla parametrar för injektion via GUI (Bild 1D) innan vävnaden är klar, för att minska eventuell onödig väntetid. För felsökning hänvisas till tilläggsfilen.
Vid lång sikt skiva kultur, steg efter den automatiserade mikroinjektionsproceduren kan påverka hälsan hos cellerna och därigenom experimentet. Därför rekommenderas det starkt att köra ett kvalitetskontrolltest och att optimera segmentkulturförhållandena. För att utvärdera cellens livskraft efter skivnings- och injektionsproceduren utförde vi EdU-märkning under kulturen och vi kvantifierade antalet pyknotiska kärnor (en proxy för apoptotiska celler) i kulturerna och injicerad vävnad12. Dessa kvantifieringar avslöjade inte någon signifikant påverkan av mikroinjektion på vävnadsens livskraft (Figur 2C). Vi rekommenderar att du kör liknande kvalitetskontroller samtidigt som organotypic vävnad skivning och microinjection pipeline i labbet.
Jämfört med manuell mikroinjektion ger mikroinjektionsroboten flera fördelar. För det första är inlärningskurvan för användaren mindre brant jämfört med manuell injektion: en ny användare kommer att nå en hög kompetens efter ett begränsat antal sessioner, vanligtvis 1 eller 2. För det andra, när det gäller manuell mikroinjektion, kräver en jämförbar färdighet månader av utbildning. Injektionsproceduren är snabbare och effektivare (Figur 2B). Vi kvantifierade dessa parametrar och fann att mikroinjektionsroboten överträffade en skicklig manuell användare med avseende på injektionsframgången (% av framgångsrik injektion/totalt antal injektioner) och i det totala antalet injektioner per enhetstid12. Detta resulterar i en övergripande 300% ökning av injektionseffektivitet (% av framgångsrik injektion/min) för microinjection roboten jämfört med en skicklig användare. Effektivitetsökningen var ännu mer uttalad när man jämförde mikroinjektionsroboten med en nybörjaranvändare och nådde 700%. Sist men inte minst kan mikroinjektionsroboten enkelt programmeras för att systematiskt utforska alla rumsliga parametrar. Detta är särskilt fördelaktigt när man anpassar mikroinjektionsroboten för att rikta in sig på nya celler eller vävnader, eller när man använder mikroinjektionsroboten för ändamål som kräver olika rumslig upplösning.
Att bygga mikroinjektionsroboten kräver minimala ändringar i ett befintligt epi-fluorescensmikroskop12. Vi har tidigare lämnat instruktioner för denna anpassning https://github.com/bsbrl/Autoinjector. När maskinvaran är setup, detta protokoll ger viktiga metodologiska detaljer för framgångsrikt företag automatiserade mikroinjektioner. Sammantaget har microinjection roboten en framgångsrik injektionshastighet på 15,52 + 2,48 injektioner / min, vilket är 15x större än en oerfaren användare (1,09 ± 0,67 injektioner / min), och 3x större än en expertanvändare (4,95 ± 1,05 injektioner / min)12. Denna förbättring i framgångsrik injektionshastighet ger både nybörjare och expertanvändare att injicera fler celler på kortare tid vilket är viktigt att bevara vävnadsens livskraft. Dessutom är microinjection roboten anpassningsbar och banan, injektionens djup, antal injektioner, avstånd mellan injektioner kan alla vara avstämda med hjälp av GUI. Dessa funktioner gör att microinjejektionsroboten kan användas som ett verktyg för att optimera tidigare mödosamma experiment, och för att utforska fundamentalt nya experiment som kräver högre avkastning än tidigare möjligt.
De viktigaste begränsningarna i mikroinjektionsförfarandet vi beskrev här är relaterade till beredning av vävnadsskivor, ett avgörande steg som behöver omfattande optimering. Dessutom microinjection bygger på förekomsten av en yta som kan närma sig glaset pipetten. Den här funktionen begränsar den typ av vävnader och vävnadsplatser som kan riktas via mikroinjektion med hjälp av den nuvarande inställningen.
Microinjection robot använder för närvarande brightfield imaging och har använts i in vitro hjärnan skiva preparat. I framtiden kan mikroinjektionsroboten kombineras med 2-fotonavbildning för att öka specificiteten hos encellsinriktning in vivo för molekylär eller färgfärgsmärkning. Sådana ansträngningar har redan gjorts för encellig elektrofysiologi15,16. Den aktuella enheten kräver manuell observation av mikroinjektionsproceduren. Framtida versioner kan innehålla strategier för rengöring av igensatta mikroinjektionspipetter17 eller integrering av vätskehanteringsrobotar18 för multiplexerade, helt autonoma mikroinjektioner. Dessa enheter kan öka omfattningen av mikroinjektion med storleksordningar. Anpassning av algoritmer för parallell kontroll av flera microinjection pipetter19 skulle kunna möjliggöra multiplexed leverans av dussintals färgämnen och molekylära reagenser i samma celler inom samma experiment. Detta har potential att öppna nya vägar för molekylär screening i vävnad.
Mikroinjektionsroboten kan användas för att tagga funktionellt identifierade celler med DNA- eller RNA-streckkoder. Detta skulle i sin tur kunna kombineras med andra encelliga analystekniker, såsom single cell RNA-sekvensering (scRNAseq) och elektronmikroskopi. Våra preliminära resultat visar att microinjected celler och deras avkomma kan återvinnas och isoleras med hjälp av vävnad dissociation följt av FACS sortering (Taverna, opublicerade resultat). Facs sorterade celler kan sedan användas för scRNAseq. Vidare visar preliminära resultat att mikroinjerobotens encellsupplösningsförmåga kan användas i kombination med elektronmikroskopisk analys för att utforska cellbiologin på neurala stamceller i vävnad vid hög spatial upplösning (Taverna och Wilsch-Bräuninger, opublicerade resultat). Dessa data tyder på att microinjection roboten kan användas som ett verktyg för korrelativt ljus och elektronmikroskopi i vävnad och i vidare bemärkelse, för den multimodala analysen av cellens identitet och beteende i vävnad.
Microinjejektion bygger på användning av tryck och man har råd med att injicera lösningar med högmolekylär komplexitet (t.ex. en hel transkriptom). Denna funktion av mikroinjektion har utnyttjats tidigare för att isolera och kloning ligand-gated receptorer20. Längs denna linje, microinjection robot kan användas för modellering och studera multi-genic egenskaper på cellnivå. Kombinerat med en sub-pooling strategi, microinjection roboten kan också användas som en plattform för att identifiera den minsta uppsättningen gener som driver en viss egenskap / cellulära beteende. Hittills har mikroinjektionsroboten använts för att manipulera cellens biokemi via leverans av mRNA, DNA eller rekombinanta proteiner10,21,22. Vi förutser en tillämpning av microinjection roboten i sondering biofysiken i intracellulära utrymmet, till exempel genom att leverera nanomaterial eller nanomaskiner som tillåter avkänning och/eller manipulation av de biofysiska egenskaperna hos intracellulära utrymmet.
Författarna har inget att avslöja.
Författarna vill erkänna Nomis Foundation (ET). SBK erkänner medel från avdelningen För maskinteknik, Högskola av vetenskap och iscensätta, MnDRIVE RSAM-insats av universitetar av Minnesota, Minnesota avdelning av högre utbildning, Medborgareinstitut av vård-(NIH) 1R21NS103098-01, 1R01NS111028, 1R34NS111654, 1R21NS112886 och 1R21 NS1111196. GS stöddes av National Science Foundation Graduate Research Fellowship och NSF IGERT utbildningsbidrag.
| Name | Company | Catalog Number | Comments |
| Chemicals | |||
| Agarose, Low Melt | Carl Roth | Cat# 6351.2 | |
| Agarose, Wild Range | Sigma-Aldrich | Cat# A2790 | |
| Best-CA 221 Glue | Best Klebstoffe GmbH & Co.KG | Cat# CA221-10ml | |
| B-27 Supplement | Thermo Fisher Scientific | Cat# 17504044 | |
| Cellmatrix Type-IA (Collagen, Type !) | FUJIFILM Wako Chemicals | Cat# 637-00653 | |
| Distilled Water | |||
| DMEM-F12, CO2 independent (w/o Phenol red) | Sigma-Aldrich | Cat# D2906 | |
| DMEM-F12, CO2 independent (with Phenol red) | Sigma-Aldrich | Cat# D8900 | |
| HEPES-NAOH, pH 7.2, 1M (HEPES buffer) | Carl Roth | Cat# 9105.3 | |
| L-Glutamine, 200 mM | Thermo Fisher Sientific | Cat# 25030024 | |
| Mowiol 4-88 | Sigma-Aldrich | Cat# 81381 | |
| N-2 Supplement | Thermo Fisher Scientific | Cat# 17502048 | |
| Neurobasal Medium | Thermo Fisher Scientific | Cat# 21103049 | |
| Nuclease-free water | Thermo Fisher Scientific | Cat# AM9937 | |
| O2 (40%), CO2 (5%), N2 (55%) Mix, 50 liters | |||
| Paraformaldehyde | Merck | Cat# 818715 | |
| PBS | |||
| Penicillin-Streptomycin (10,000 U/mL) | Thermo Fisher Scientific | Cat# 15140122 | |
| Rat serum | Charles River Laboratories | ||
| Japan | |||
| Sodium bicarbonate (NaHCO3) | Merck | Cat# 106323 | |
| Sodium hydroxide (NaOH) | Merck | Cat# 106482 | |
| Tyrode’s salt | Sigma | Cat# T2145-10x1L) | |
| Equipment | |||
| Borosilicate glass capillaries, 1.2 mm outer diameter x 0.94 mm inner diameter | Sutter Instruments | Cat# BF-120-94-10 | |
| Bottle-top filter system, 500 mL | Corning | Cat# 430769 | |
| Computer PC | |||
| Custom pressure rig | Custom pressure rig | ||
| Electronic pressure regulator | Parker Hannifin | Cat# 990-005101-002 | |
| Falcon tubes, 15 mL | Corning | Cat# 430791 | |
| Falcon tubes, 50 mL | Corning | Cat# 430829 | |
| Fine-tip paintbrush | |||
| Flaming/ Brown micropipette puller | Sutter Instruments | Cat# P-97 | |
| Forceps, Dumont no. 3 | Fine Science Tools | Cat# 11231-30 | |
| Forceps, Dumont no. 5 | Fine Science Tools | Cat# 11255-20 | |
| Forceps, Dumont no. 55 | Fine Science Tools | Cat# 11252-20 | |
| Heating block | Labtech International | Cat # Dri block Digi2 | |
| Inverted fluorescence microscope | Zeiss | Cat# Axiovert 200 | |
| Light source | Olympus | Cat# Highlight 3100 | |
| Manual pressure regulator | McMaster Carr | Cat# 0-60 PSI 41795K3 | |
| Microloader Tips | Eppendorf | Cat# 5242956.003 | |
| Microcontroller | Arduino | Cat# Arduino Due | |
| Microscope camera Hamamatsu Orca Flash 4.0 V3 | |||
| Motorized stage XY for microscope | |||
| Multiwell plate, 24 wells | Nunc | Cat# 142475 | |
| Pasteur pipettes, plastic | |||
| Petri dish, 60 x 15 mm | Greiner | Cat# 628102 | |
| Petri dish, 35 x 10 mm | Nunc | Cat# 153066 | |
| Petri dish, 34 x 14 mm, including Microwell no. 1.5 cover glass | MatTek | Cat# P35G-1.5-14-C | |
| Pipette holder | Warner Instruments | Cat# 64-2354 MP-s12u | |
| Pipette and tips | |||
| Puller filament, 3.0-mm square box filament | Sutter Instrument | Cat# FB330B | |
| Slice culture incubation box | MPI-CBG | Cat# custom made | |
| Solenoid valve | Cat# LHDA053321H-A | ||
| Stereomicroscope | Olympus | Cat# SZX12 | |
| Tabletop centrifuge | Heraeus | Cat# 5431622 | |
| Thermometer | |||
| Three-axis Manipulator | Sensapex Inc | Cat# tree-axis uMP | |
| Vibratome | Leica | Cat# VT1000s | |
| Whole-embryo-culture-system incubator | Ikemoto Company | Cat# RKI-10-0310 | |
| Waterbath | |||
| Software and Algorithms | |||
| Arduino | Arduino | ||
| Fiji | RRID: SCR_002285 | ||
| Python | Python Software foundation | Python 2.7.12 | |
| ZEN | RRID: SCR_013672 |
- Taverna, E., Götz, M., Huttner, W. B. The Cell Biology of Neurogenesis: Toward an Understanding of the Development and Evolution of the Neocortex. Annual Review of Cell and Developmental Biology. 30 (1), 465-502 (2014).
- Götz, M., Huttner, W. B. The cell biology of neurogenesis. Nature Reviews Molecular Cell Biology. 6 (10), 777-788 (2005).
- Di Lullo, E., Kriegstein, A. R. The use of brain organoids to investigate neural development and disease. Nature Reviews Neuroscience. 18 (10), 573-584 (2017).
- Lancaster, M. A., Knoblich, J. A. Organogenesisin a dish: Modeling development and disease using organoid technologies. Science. 345 (6194), 1247125 (2014).
- Kretzschmar, K., Clevers, H. Organoids: Modeling Development and the Stem Cell Niche in a Dish. Developmental Cell. 38 (6), 590-600 (2016).
- Pepperkok, R. et al. Automatic microinjection system facilitates detection of growth inhibitory mRNA. Proceedings of the National Academy of Sciences of the United States of America. 85 (18), 6748-6752 (1988).
- Pepperkok, R., Lowe, M., Burke, B., Kreis, T. E. Three distinct steps in transport of vesicular stomatitis virus glycoprotein from the ER to the cell surface in vivo with differential sensitivities to GTPγS. Journal of Cell Science. 111 (13), 1877-1888 (1998).
- Pepperkok, R. et al. β-COP is essential for biosynthetic membrane transport from the endoplasmic reticulum to the Golgi complex in vivo. Cell. 74 (1), 71-82 (1993).
- Ansorge, W., Pepperkok, R. Performance of an automated system for capillary microinjection into living cells. Journal of Biochemical and Biophysical Methods. 16 (4), 283-292 (1988).
- Taverna, E., Haffner, C., Pepperkok, R., Huttner, W. B. A new approach to manipulate the fate of single neural stem cells in tissue. Nature Neuroscience. 15 (2), 329-337 (2012).
- Wong, F. K., Haffner, C., Huttner, W. B., Taverna, E. Microinjection of membrane-impermeable molecules into single neural stem cells in brain tissue. Nature Protocols. 9 (5), 1170-1182 (2014).
- Shull, G., Haffner, C., Huttner, W. B., Kodandaramaiah, S. B., Taverna, E. Robotic platform for microinjection into single cells in brain tissue. EMBO Reports. 20 (10), e47880 (2019).
- Jabeen, S., Thirumalai, V. The interplay between electrical and chemical synaptogenesis. Journal of Neurophysiology. 120 (4), 1914-1922 (2018).
- Nagy, J. I., Pereda, A. E., Rash, J. E. Electrical synapses in mammalian CNS: Past eras, present focus and future directions. Biochimica et Biophysica Acta - Biomembranes. 1860 (1), 102-123 (2018).
- Suk, H.J. et al. Closed-loop real-time imaging enables fully automated cell-targeted patch-clamp neural recording in vivo. Neuron. 95 (5), 1037-1047 (2017).
- Annecchino, L. A. et al. Robotic automation of in vivo two-photon targeted whole-cell patch-clamp electrophysiology. Neuron. 95 (5), 1048-1055 (2017).
- Kolb, I. et al. Cleaning patch-clamp pipettes for immediate reuse. Scientific Reports. 6, 35001 (2016).
- Holst, G. L. et al. Autonomous patch-clamp robot for functional characterization of neurons in vivo: development and application to mouse visual cortex. Journal of Neurophysiology. 121 (6), 2341-2357 (2019).
- Kodandaramaiah, S. B. et al. Multi-neuron intracellular recording 1 in vivo via interacting autopatching 2 robots. ELife. 7, 24656 (2018).
- Lubbert, H. et al. cDNA cloning of a serotonin 5-HT1c receptor by electrophysiological assays of mRNA-injected Xenopus oocytes (RNA fractionation/hybrid depletion/hybrid selection/choroid plexus/voltage clamp). Neurobiology. 84 (2) 4332-4336 (1987).
- Florio, M. et al. Human-specific gene ARHGAP11B promotes basal progenitor amplification and neocortex expansion. Science. 347 (6229), 1465-1470 (2015).
- Kalebic, N. et al. CRISPR/Cas9-induced disruption of gene expression in mouse embryonic brain and single neural stem cells in vivo. EMBO Reports. 17 (3), 338-348 (2016).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved