Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Bioengineering
Enkel, rimelig og modulær mønster av celler ved hjelp av DNA
Her presenterer vi en protokoll for mikropatternceller ved encellet oppløsning ved hjelp av DNA-programmert vedheft. Denne protokollen bruker en stasjonær fotolitografiplattform for å lage mønstre av DNA-oligonukleotider på en glasssklie og merker deretter cellemembraner med kommersielt tilgjengelige komplementære oligonukleotider. Hybridisering av oligos resulterer i programmert celleadhesjon.
Den relative plasseringen av celler er et sentralt trekk ved mikromiljøet som organiserer cellecelleinteraksjoner. For å studere interaksjonene mellom celler av samme eller annen type, har mikropatterningsteknikker vist seg nyttige. DNA-programmert montering av celler (DPAC) er en mikropatteringsteknikk som retter seg mot vedheft av celler til et substrat eller andre celler ved hjelp av DNA-hybridisering. De mest grunnleggende operasjonene i DPAC begynner med å dekorere cellemembraner med lipidmodifiserte oligonukleotider, og deretter strømme dem over et substrat som har blitt mønstret med komplementære DNA-sekvenser. Celler holder seg selektivt til substratet bare der de finner en komplementær DNA-sekvens. Ikke-tilhengerceller vaskes bort, og avslører et mønster av tilhengerceller. Ytterligere operasjoner inkluderer ytterligere runder med celle-substrat eller cellecelleadhesjon, samt overføring av mønstrene dannet av DPAC til en innebygd hydrogel for langsiktig kultur. Tidligere krevde metoder for mønster av oligonukleotider på overflater og dekorasjon av celler med DNA-sekvenser spesialisert utstyr og tilpasset DNA-syntese. Vi rapporterer en oppdatert versjon av protokollen, ved hjelp av en billig stasjonær fotolitografi oppsett og kommersielt tilgjengelig kolesterol modifisert oligonukleotider (CMOer) distribuert ved hjelp av et modulært format. CMO-merkede celler holder seg til høy effektivitet til DNA-mønstrede substrater. Denne tilnærmingen kan brukes til å mønstre flere celletyper samtidig med høy presisjon og til å lage matriser med mikrobrikker innebygd i en ekstracellulær matrise. Fordelene med denne metoden inkluderer dens høye oppløsning, evne til å bygge inn celler i et tredimensjonalt mikromiljø uten å forstyrre mikropatternet, og fleksibilitet i å mønstre en hvilken som helst celletype.
Plasseringen av celler med hensyn til hverandre i et vev er et viktig trekk ved mikromiljøet1,2,3,4. Teknikker som brukes til å mønstre levende celler i romlig kontrollerte ordninger er verdifulle eksperimentelle verktøy for å studere differensiering4,5,6,7,8, cellemotilitet9, morfogenese10,11,12, metabolisme13og cellecelleinteraksjoner7,14 . Det finnes en rekke metoder for mønsterceller, hver med sine egne fordeler og ulemper3,4. Metoder som skaper klebende øyer med ekstracellulære matriseproteiner (ECM), for eksempel mikrokontakttrykk og laserkuttede sjablonger, er enkle og skalerbare. Det er imidlertid vanskelig å mønstre mer enn en eller to celletyper om gangen fordi limegenskapene til forskjellige celletyper til forskjellige ECM-molekyler ofte er like15,16,17. Mer komplekse mikropatterner kan opprettes med lysindusert molekylær adsorpsjon (LIMAP), en teknikk som bruker UV-lys til å fyre opp PEG-belagte regioner og tillate påfølgende protein adsorpsjon18,19. Denne prosessen kan gjentas for å opprette mikropatterner med høy oppløsning med flere celletyper. Kryssbinding av celler til de forskjellige proteinplaster kan imidlertid forekomme, noe som resulterer i dårlig mønster spesifisitet19. Fysiske metoder som såddceller på mikromekaniske rekonfigurerbare kulturenheter kan skape strukturerte samkulturer med dynamisk kontroll, men uten fleksibiliteten i mønsterdesign av mikrokontakttrykk eller LIMAP14,8. I motsetning til de andre teknikkene kan bioprinting skape tredimensjonale ordninger av celler i hydrogeler20,21. Bioprinted konstruksjoner har imidlertid mye lavere oppløsning enn andre mikropatterningsteknikker, med en gjennomsnittlig funksjonsstørrelse på størrelse med hundrevis av mikron22. En ideell cellemønstermetode vil ha høy oppløsning, mønster flere celletyper, bruke utstyr og reagenser som er lett tilgjengelige, og ha muligheten til å legge inn vellykkede mønstre i en hydrogel for tredimensjonal (3D) cellekultur. I denne artikkelen presenterer vi CMO-DPAC, en cellemikropatteringsteknikk som bruker fleksibiliteten og hastigheten til DNA-hybridisering for å målrette celleadhesjon mot et substrat. Denne metoden er tilpasset fra våre tidligere protokoller23,24 for å gjøre den rimeligere, modulær og tilgjengelig. Ved hjelp av den nåværende protokollen skal ethvert laboratorium kunne sette opp et fullt funksjonelt system uten spesialisert utstyr eller ekspertise.
DNA-programmert montering av celler (DPAC) er en kraftig vevsteknikkteknikk som mønstrer celler ved encellet oppløsning med presis kontroll over cellecelleavstand og vevsgeometri. I DPAC er cellemembraner dekorert med DNA-oligonukleotider (oligos) ved hjelp av to lipidmodifiserte oligoer designet for å hybridisere på cellemembranen. Fordi oligoene er konjugert til hydrofobe lipider, partisjonerer de raskt til cellemembranen25 der de hybridiserer, øker netto hydrofobiskheten til de ikke-kovalent bundne molekylene, og dermed forbedrer levetiden på celleoverflaten26. Oligoene presenteres på celleoverflaten på en måte der de kan hybridisere med komplementære oligoer på andre celler eller DNA-funksjonaliserte glasssklier for å lage definerte 2D- eller 3D-cellemønstre med foreskrevet sammensetning, cellecelleavstand og geometri23,24. De mønstrede mikrotissuene kan spaltes av overflaten enzymatisk og legges inn i en hydrogel for langvarig 3D-kultur. Når de brukes i kombinasjon med primære celler eller stamceller, kan de resulterende samlingene av celler gjennomgå morfogenese og dannes i organoider23,27,28. DPAC har blitt brukt til å undersøke dynamikken i voksen nevral stamcelle skjebne som svar på konkurrerende signaler6,29, for å studere selvorganisering av pattedyr epitelceller23,28, og for å generere "vev origami" gjennom mesenchymal kondensasjon27.
DPAC muliggjør nøyaktig plassering av flere cellepopulasjoner og har vesentlig bedre oppløsning enn ekstruderingsbaserte bioprintere (i størrelsesorden mikron)22,23. I tillegg, i motsetning til ECM-baserte mønstermetoder som mikrokontaktutskrift, krever ikke DPAC differensialadhesjon av de forskjellige celletypene til en ECM-belagt overflate15,23. Det er ideelt for å svare på spørsmål om hvordan sammensetningen av et vev påvirker atferden, hvordan celler integrerer flere cellulære og mikroenvironmentale signaler når de tar beslutninger6,29, og hvordan par celler samhandler med hverandre. En fordel med denne metoden i forhold til andre mikropatterningsmetoder er at den kan brukes til 3D-cellekultur i et enkelt bildeplan, noe som letter tidsforløpstudier av vev selvorganisering og organoid morfogenese23,27,30.
Til tross for disse fordelene har vellykket implementering av DPAC krevd syntese av tilpassede oligonukleotidreagenser og tilgang til spesialisert utstyr for DNA-mønster23,24, noe som begrenser utbredt adopsjon. For eksempel må de optimale lipidmodifiserte oligoene (LMOene) som brukes i den opprinnelige protokollen, tilpasses syntetisert, modifisert med lignocerinsyre eller palmesyre og renset26. Denne prosessen krever bruk av en DNA-synthesizer og et høytytende flytende kromatografiinstrument, samt kjøp av tilhørende reagenser som metylamin, et kontrollert stoff som er underlagt både institusjonelle og føderale forskrifter. Som et alternativ kan LMOer tilpasses kjøpt i bulk, men dette krever en betydelig forhåndsinvestering i teknologien.
For å overvinne disse begrensningene har vi utviklet en revidert versjon av DPAC som bruker kommersielt tilgjengelige kolesterolmodifiserte oligos (CMOer) i stedet for de tilpassede syntetiserte LMOene. For ytterligere å redusere kostnadene og øke fleksibiliteten til plattformen, har vi endret oss til et modulært, tre-oligo-system. I stedet for å bestille en ny kolesterolmodifisert oligo for hver unike cellepopulasjon, kan en bruker av denne protokollen i stedet bruke de samme kolesterolmodifiserte oligoene ("Universal Anchor" og "Universal Co-Anchor") for hver cellepopulasjon og deretter bruke en billig, umodifisert oligo ("Adapter Strand") som hybridiserer med både Universal Anchor og enten det aminfunksjonaliserte DNA på overflaten eller Adapter Strand av en annen celletype.
En annen begrensning i den opprinnelige DPAC-protokollen var at den opprettet dna-mønstrede lysbilder ved hjelp av en høyoppløselig væskeskriver (f.eks. Nano eNabler, BioForce Nanosciences)23,24. Selv om dette instrumentet har ekstraordinær oppløsning og lave reagenskrav, er det ikke tilgjengelig for de fleste institusjoner og har en relativt lav utskriftshastighet (omtrent 1 funksjon mønstret per sekund). Nylig har to fotolittografiske metoder blitt utviklet for å mønstre DNA-funksjoner på overflater. Viola og kolleger brukte et polyakrylamid- og benzofenonbelegg som kovalent bundet enkeltstrenget DNA-oligos ved eksponering for UV-lys30. Ved hjelp av denne metoden var de i stand til å lage vevstillaser som gjennomgikk store, programmerte formendringer som følge av cellekontraktilitet og selvorganisering. Scheideler et al. utviklet en metode som bruker UV-eksponering av en positiv fotoresist for selektivt å eksponere aminmodifiserte DNA-oligos til et aldehydfunksjonalisert lysbilde29. Etter baking og reduktiv aminering er det aminmodifiserte DNA-et kovalent bundet til overflaten. Denne metoden ble brukt til å undersøke responsen til voksne nevrale stamceller for å presentere selvfornyelse og differensieringssignaler. Denne artikkelen tilpasser Scheideler et al.s protokoll for å lage DNA-mønstrene som vil fange CMO-merkede celler. Denne fotopatterningsprotokollen kan utføres uten å bruke et rent rom. Den bruker billig og kommersielt tilgjengelig utstyr som enkelt kan distribueres på en benkeplate eller avtrekkshette. Bruken av billig eller DIY (gjør-det-selv) fotolittografiutstyr øker tilgjengeligheten til forskere uten tilgang til rene romfasiliteter og lar forskere prøve teknikken uten en stor investering av tid eller ressurser31,32. Imidlertid kan bedre oppløsning og justering av flere DNA-funksjoner oppnås ved å bruke den kommersielle spinnfrakkeren og maskejusteringen som vanligvis finnes i renromsanlegg.
Her beskriver vi en metode for å mønster celler ved encellet oppløsning ved hjelp av DNA-basert vedheft. For det første brukes fotopatterning med en positiv fotoresist til å lage høyoppløselige mønstre av aminmodifisert DNA på et aldehydmodifisert glasssubstrat. Deretter behandles lysbildet for å redusere ikke-spesifikt cellevedlegg, og PDMS-flytceller opprettes for å begrense celler over mønstrede områder. Celler merkes deretter med korte DNA-oligonukleotider som er funksjonalisert med kolesterol og som et resultat settes inn i cellemembranen. Cellene blir deretter strømmet over DNA-mikropatternene. Hybridisering mellom celleoverflate-DNA og DNA på glassoverflaten resulterer i spesifikk vedheft av cellene til DNA-mønsteret. Ikke-tilhengerceller vaskes bort, og avslører det tilhengercellemønsteret. Denne prosessen kan gjentas for å mønstre flere celletyper eller opprette flerlagsstrukturer. Om ønskelig kan cellene bygges helt inn i en ECM for 3D-cellekultur.
1. Design eksperiment
- Planlegg ønsket eksperiment, med tanke på funksjonsstørrelse, funksjonsavstand, antall involverte celletyper og arrangementet av celler med hensyn til hverandre. Se Tilleggsfil 1, en veiledning for eksperimentell utforming og Tilleggsfil 2, som inneholder eksempel-oligo-sekvenser.
- Design fotomaske ved hjelp av dataassistert designprogramvare. Et eksempel på en fotomaske finnes i Tilleggsfil 3.
- Tegn et rektangel av dimensjonene til en standard mikroskopsklie (25 mm x 75 mm).
- Tegn fire rektangulære områder som er 10 mm brede og 10 mm lange, fordelt jevnt over lysbildet.
- I hvert område tegner du funksjoner som har ønsket størrelse, form og avstand for eksperimentet. Celler vil bare følge disse funksjonene i eksperimentet.
- Hvis du vil opprette justerte fotomasker for flere celletyper, oppretter du en hovedtegning med alle sett med funksjoner, og deretter lagrer du versjoner som tilsvarer hver celletype.
- Bestill en høyoppløselig (minst 20 000 prikker per tomme) gjennomsiktighetsfotomaske fra denne CAD-tegningen med funksjonene tegnet i 1,2,3 gjennomsiktige og større områder svarte.
2. Photopattern DNA på aldehyd-funksjonaliserte lysbilder (protokoll tilpasset fra Scheideler et al.29 )
- Hvis du mønstrer flere celletyper, fremstiller du fiducial markører på det aldehydfunksjonaliserte lysbildet før DNA-mønstre for å lette justeringen av funksjoner. Alternative metoder for å lage fiducial markører foreslås i Supplemental File 1.
- For å lage metallfidusialmarkører, bruk S1813 positiv fotoresist som beskrevet i trinn 2.3 - 2.11. Bruk en fotomaske som inneholder store funksjoner som vil være enkle å justere senere. Inkorporer disse funksjonene i utformingen av fotomaskene som skal brukes til DNA-mønster.
- Deponer en tynn film (100 Angstroms) titan på lysbildet ved hjelp av elektronpistolfordampning29. Fjern overflødig metall og fotoresist ved hjelp av aceton, og fortsett deretter til DNA-fotopatterning.
- Forbered en 20 μM løsning av en 5'-amin-modifisert oligo i DNA-buffer (50 mM natriumfosfat i vann, pH = 8,5). Se Tilleggsfil 2 for foreslåtte oligosekvenser.
MERK: Det er mulig å bruke så lite som 5 μM aminmodifisert oligo for noen mønstre og bruksområder, så overflate-DNA-konsentrasjonen må kanskje optimaliseres. - Forvarm en varm plate til 100 °C.
- Bruk dobbeltsidig tape eller et vakuum for å feste en aldehydfunksjonalisert glasssklie til rotoren til en spinnfrakker.
FORSIKTIG: Skyv løsrivelse under spin-coating er en sikkerhetsrisiko. Bruk alltid spincoateren i en lukket beholder med et lokk, for eksempel en akrylboks.
MERK: Merk et hjørne av lysbildet ved hjelp av en diamantspiss eller lignende for å skrape glasset. Dette hjelper med lysbildeidentifikasjon og orientering etter at fotoresisten er vasket bort. - Bruk en engangspipette for å slippe den positive fotoresisten på aldehydskuffen. For jevne belegg, legg til små dråper fotoresist over lysbildet, i stedet for en stor dråpe i midten (Supplerende figur 1A).
- Bruk spin coater, spinn lysbildet på 3000 rpm i 30 s.
- Plasser gliden på 100 °C kokeplate i 1,5 min (myk bake) for å krysskoble fotoresisten.
- Fjern lysbildet fra kokeplaten. Plasser en fotomaske med funksjonene som er ønsket for dette eksperimentet på toppen av lysbildet, og vei fotomasken ned med et glassstykke (Supplerende figur 1B,C). Dekk hele oppsettet i en ugjennomsiktig boks (Tilleggsfigur 1D). Eksponere med en UV-lampe (365 nm bølgelengde, 360 mW, 5 tommer fra lysbilde, total strålende energitetthet 100 mJ/cm2) i 2 minutter.
MERK: UV-lys vil bryte polymerbindingene i fotoresisten under gjennomsiktige områder av fotomasken, og skape regioner der DNA senere vil kunne feste seg. - Utvikle lysbildet ved å fordype deg i utviklerløsningen i 3-5 min (Supplerende figur 1E).
- Skyll bort overflødig utviklerløsning med vann. Tørk under en strøm av luft eller nitrogen. (Supplerende figur 1F).
- Bekreft at fotolitografien var vellykket ved å se på lysbildet under mikroskopet. Fordi fotoresisten er UV-lysfølsom, gjør du dette trinnet raskt og lagrer deretter lysbildet i mørket mens du forbereder andre lysbilder (hvis aktuelt).
MERK: Et mønstret lysbilde skal ha skarpt definerte kanter for hver funksjon, ingen sprekker og ingen funksjonsforvrengning ved kantene. Eksempler på korrekt og feil fotolittografi finnes i Supplerende figur 2A. Se tabell 1 for feilsøking av forslag hvis fotolitografi ikke gir ønsket funksjonskvalitet. - Legg til en dråpe med den 20 μM aminmodifiserte oligoløsningen (trinn 2.1) på hver fotopatternerte region i lysbildet. Bruk en pipettespiss til å spre dråpen forsiktig over hele regionen, og pass på at du ikke riper på lysbildet. (Supplerende figur 1G).
- Stek skredet i en ovn på 65-70 °C til DNA-oppløsningen er helt tørket på glideflaten (ca. 1 time).
- Utfør reduktiv reduksjon ved å plassere de mønstrede, bakte lysbildene i en 15 cm cellekulturrett og legg i en avtrekkshette på toppen av en shaker. Vei ut 100 mg natriumborohydrid. I en avtrekkshette tilsettes 40 ml fosfatbufret saltvann (PBS), bland forsiktig og legg til parabolen som inneholder de mønstrede lysbildene. La reaksjonen fortsette i 15 min med mild risting.
MERK: Aminet på oligo danner først en Schiff-base med aldehydene på glideflaten. Dette er en reversibel kovalente binding som må konverteres til en irreversibel obligasjon før bruk i DPAC. Tilsetning av et reduksjonsmiddel (natriumborohydrid) konverterer Schiff-basen til en sekundær amin ved reduktiv aminering.
FORSIKTIG: Reaksjonen av natriumborohydrid med vann skaper hydrogengass og vil fortsette å gjøre det i flere timer eller dager etter at reaksjonen begynner. Utfør det reduktive avmineringstrinnet i en avtrekkshette og oppbevar alt natriumhydridoppløsningsavfall i en åpen eller løst avkortet beholder i avtrekkshetten i minst 24 timer. - Fjern ikke-acted DNA ved å vaske to ganger med 0,1% natriumddecylsulfat (SDS) i vann, deretter tre ganger med destillert vann. Tørk gliden under en strøm av nitrogen eller luft.
- Skyll lysbildet med aceton for å fjerne den gjenværende fotoresisten.
MERK: På dette tidspunktet har DNA-et vært irreversibelt og kovalent festet til lysbildet, og alle uberørte aldehydfunksjonelle grupper har blitt konvertert til alkoholer. Fotoresisten er ikke lenger nødvendig. - Hvis flere oligoer skal mønstres, går du tilbake til trinn 2.4, justerer fotomasken med fiducial merker og gjentar.
MERK: Eksperimentet kan settes på pause her. Oppbevar sklier i en vakuumdesiccator. Under tørre forhold kan lysbildene lagres i opptil 3 måneder uten tap av kvalitet.
3. Gjør lysbilde hydrofob (valgfritt) (protokoll tilpasset fra Todhunter et al.24 )
MERK: Det er fordelaktig, men ikke nødvendig, å endre lysbildets overflatekjemi for å gjøre den mer inert og hydrofob. Ikke-spesifikt cellevedlegg reduseres på disse flatene33, og dermed lindres ikke-spesifikk binding av celler til ikke-mønstrede områder i lysbildet. I tillegg, hvis de mønstrede cellene til slutt vil bli innebygd i en hydrogel og overført av lysbildet, er overflatebehandlingen avgjørende for pålitelig bevegelse av den cellebelastede hydrogelen over lysbildet uten forvrengning eller riving. Silanisering med (tridecafluoro-1,1,2,2-tetrahydrooctyl) dimetylklorosilane resulterer i tilstedeværelse av hydrofobe fluoroalkylgrupper på glideoverflaten.
FORSIKTIG: Utfør alle trinn fra 3.1 og utover i en kjemisk avtrekkshette for å forhindre eksponering for eddiksyre og metylenkloriddamp.
- Skyll lysbildet med 10% eddiksyre og tørk deretter under en luftstrøm.
- I en glass Coplin krukke, lag en løsning på 60 ml metylenklorid (dichloromethane), 0,6 ml trietylamin og 0,6 ml (tridekafluoro-1,1,2,2-tetrahydrooctyl) dimetylchlorosilane. Rør med en metallspatel for å blande.
MERK: Disse reagensene er følsomme for vann. De skal lagres under tørre forhold og brukes så frisk som mulig. - Legg lysbildet til Coplin-krukken som inneholder silanoppløsningen. Plasser Coplin krukke på en orbital shaker (satt til 60-80 rpm) og la reaksjonen av silan og lysbildet gå videre i 15 min.
- Bruk metall tang for å fjerne lysbildet fra silanoppløsningen. Dypp lysbildet i en Coplin-krukke som inneholder metylenklorid i 1 minutt for å fjerne overflødig silan fra lysbildet.
- Senk sklien ned i et konisk rør på 50 ml som inneholder etanol. Skake. Senk sklien ned i et 50 ml konisk rør som inneholder destillert vann. Skake.
MERK: Metylenklorid og vann er ikke blandbart, så en etanolskylling er nødvendig for å fjerne overflødig metylenklorid før sluttvannskylling. - Fjern gliden fra vannet og inspiser den. Skredet skal være ganske tørt, med eventuelle vanndråper som har en kontaktvinkel på over 90°. La lysbildene tørke helt og oppbevares i vakuumdesiccator til bruk.
MERK: Eksperimentet kan settes på pause her. Oppbevar sklien under tørre forhold.
4. Forbered PDMS-strømningsceller og skyv for eksperiment
MERK: Rektangulære PDMS-strømningsceller brukes til å konsentrere cellene over de mønstrede områdene i lysbildet. For eksperimenter dyrket i 3D danner strømningscellene en mugg for hydrogelen.
- Gjør SU-8 master til bruk som mugg for PDMS-strømningsceller.
- Forvarm kokeplaten til 95 °C.
- Tilsett 5 ml SU-8 2075 i en silisiumskive.
- Spin frakk SU-8 på waferen ved 500 rpm i 10s, etterfulgt av 1000 rpm i 30s. Dette bør opprette funksjoner på opptil 240 μm i høyde34.
- Stek skiven på varmeplaten i minst 45 minutter.
- Fjern skiven fra varmeplaten. Sett fotomasken (se Tilleggsfil 4) (emulsjonssiden ned) på toppen av skiven og vei den ned med en glassplate for å sikre kontakt mellom fotomasken og lysbildet.
- Utsett med UV-lys (365 nm) for en stråleenergitetthet på 350 mJ/cm2.
- Stek skive på kokeplaten i 12-15 min.
- Plasser skiven i en bred glassbeholder. Dekk wafer med SU-8 utviklerløsning. Plasser på en shaker og utvikle mens agitating i minst 15 min.
- Bruk tang for å fjerne skiven fra utviklerløsningen. Skyll i 5 s ved å sprøyte mer utviklerløsning fra en spruteflaske. Spray med isopropylalkohol for å skylle. Hvis det oppstår et hvitt bunnfall, returner waferen til utviklerløsningen og utvikle deg lenger.
- Tørrskive under en strøm av luft eller nitrogen.
- Stek lysbildet i 5 min.
MERK: Når hovedskiven er opprettet, kan den brukes på nytt på ubestemt tid så lenge funksjonene forblir intakte.
- Klargjør PDMS.
- I en veiebåt legger du til polydimetylsiloksanelastomer og crosslinker i forholdet 10:1 (med masse). Rør kraftig for å sikre jevn blanding.
- Gass PDMS i en vakuumdesiccator i 15-30 min til ingen flere bobler er synlige.
- Legg masterskiven i en 15 cm vevskulturrett. Hell PDMS over skiven. Hvis det oppstår bobler, de-gass i en vakuumdesiccator i noen minutter.
- Stek i 60 °C ovn i 3 timer.
MERK: Etter steking kan PDMS-strømningsceller lagres på benken på ubestemt tid.
- Klargjør PDMS-flytceller for eksperimentet.
- Kort tid før du starter et CMO-DPAC-eksperiment, kutt ut det nødvendige antallet PDMS-strømningsceller fra hovedskiven. Plasma oksiderer med 10 cc/min romluft i 90 s for å gjøre overflaten hydrofil.
- Klipp ut hver enkelt strømningscelle slik at det er 1-2 mm PDMS igjen på hver side, og klipp deretter opp toppen og bunnen av strømningscellen for å lage et innløp og utløp.
- Hent mønstret lysbilde som er opprettet i trinn 2 og 3. Juster over fotomasken.
- Bruk fotomasken som referanse til å plassere PDMS-flytcellene på lysbildet der hvert mønstrede område befinner seg.
- Tilsett 50 μL fosfatbufret saltvann (PBS) + 1 % bovint serumalbumin (BSA) i innløpet til hver strømningscelle, som vist i Supplerende figur 1H. Bekreft at strømningscellen er fullstendig fylt av PBS + 1% BSA og at det ikke er store bobler. Fortsett umiddelbart til trinn 5 og 6.
MERK: Blokkering med BSA minimerer ikke-spesifikk celleadhesjon til glideflaten.
5. Løft og merk celler med kolesterolmodifisert DNA
- Forbered kolesterolmodifiserte DNA-løsninger.
- For hvert sett med celler i eksperimentet blander du sammen 3 μL av en 100 μM lagerløsning av den kolesterolmodifiserte Universal Anchor Strand med 3 μL av en 100 μM lagerløsning av en Adapter Strand. Inkuber i 1 minutt. Dette vil pre-hybridisere oligos. Tilsett 69 μL fosfatbufret saltvann (PBS) for å lage en 4 μM universalanker + adapterløsning.
- For hvert sett med celler i eksperimentet, legg til 3 μL av en 100 μM Universal kolesterolmodifisert Co-Anchor Strand lagerløsning til 12 μL PBS, og lag en 20 μM løsning.
- Forbered encellede suspensjon(er).
- For tilhengerceller, bruk trypsin eller annet dissosiasjonsmiddel for å fjerne cellene fra kulturflasken. Legg til kulturmedier for å nøytralisere trypsin og sentrifuge for å pellet cellene. For ikke-tilhengerceller, samle celle suspensjon og sentrifuge å pellet cellene.
- Resuspend cellepellet i 1 ml iskalde PBS eller serumfrie medier. Overfør 1-3 millioner celler til et 1,5 ml mikrosenterrør. Sentrifuge ved 160 x g i 4 min.
MERK: Hvis celletypen som brukes er utsatt for klumping/aggregering, bruker du PBS uten kalsium- og magnesiumioner for alle vasketrinn for å redusere uønsket celleaggregering. Hvis levedyktighet er en spesiell bekymring for celletypen som brukes, bruk serumfrie medier i stedet for PBS. Medier som inneholder foster bovint serum anbefales ikke for cellemerking, da det kan hindre inkorporering av lipidmodifiserte oligos. 35
- Merk cellene med kolesterolmodifiserte oligos.
- Resuspend cellepellet i 75 μL iskalde PBS eller serumfrie medier. Hold cellene i en isbøtte gjennom hele merkings- og vaskeprosessen for å maksimere celle levedyktigheten og minimere tap av kolesterolmodifiserte oligos fra celleoverflaten.
MERK: Resuspending av cellene før du legger til DNA sikrer at fordelingen av DNA er jevn over cellepopulasjonen. - Legg til 75 μL av 4 μM Universal Anchor + Adapter-løsningen som ble opprettet i trinn 5.1.1 i mikrocentrifugerøret som inneholder celleopphenget. Bland grundig ved pipettering. Inkuber i 5 min på is.
- Tilsett 15 μL av universal co-anchor-løsningen i mikrocentrifugerøret. Bland grundig ved pipettering. Inkuber i 5 min på is.
- Fjern overflødig oligos fra celleopphenget. Tilsett 1 ml iskald PBS eller serumfrie medier i mikrosenterrøret. Bland med en P1000 pipette. Sentrifuge ved 160 x g i 4 min ved 4 °C. Kast supernatanten. Gjenta to ganger til.
MERK: Hvis cellene er tilbøyelige til å klumpe seg, må du sende cellesuspensjonen gjennom et filter på 40 μm før sluttvasken. Hvis celler er utsatt for adsorpsjon på siden av mikrocentrifugerøret, bør du vurdere å forhåndsblokkere røret med kasein.
- Resuspend cellepellet i 75 μL iskalde PBS eller serumfrie medier. Hold cellene i en isbøtte gjennom hele merkings- og vaskeprosessen for å maksimere celle levedyktigheten og minimere tap av kolesterolmodifiserte oligos fra celleoverflaten.
6. Mønster de DNA-merkede cellene
- Resuspend cellene i iskalde PBS eller serumfrie medier for å skape en celletett løsning på minst 25 millioner celler / ml.
MERK: For ett lysbilde som bruker fire av strømningscellene på 10 mm x 15 mm x 200 μm PDMS som er beskrevet i trinn 4, er det nødvendig med ca. 100 μL av denne tette celleopphengen. Selv om de fleste av disse cellene ikke vil følge mønsteret og til slutt vil bli kassert, forbedrer det å ha en ekstremt konsentrert løsning av celler over mønsteret dramatisk effektiviteten av cellemønster. - Plukk opp lysbildet og vipp det litt. Legg til 25 μL celleoppheng i innløpet til hver strømningscelle på det mønstrede lysbildet. Fjern PBS + 1% BSA-løsningen fra stikkontakten, slik at celleopphenget kan fylle PDMS-strømningscellen. Inkuber på is eller ved romtemperatur i 30 s.
MERK: På dette tidspunktet bør det å se på strømningscellen under et mikroskop vise tettpakkede celler med lite eller ingen hull synlige mellom cellene. Se Supplerende figur 2B. - Aspirer 5 μL celleoppheng fra utløpet av lysbildet og legg det tilbake i innløpet. Gjenta 10 ganger per flytcelle.
MERK: Vedheften av CMO-merkede celler til det DNA-mønstrede lysbildet er nesten øyeblikkelig. Å flyte cellene over mønsteret flere ganger øker sannsynligheten for at en celle vil strømme over et gitt DNA-sted og bli fanget. - Rør forsiktig PBS eller serumfrie medier inn i innløpet til hver strømningscelle for å vaske ut overflødige celler. Samle cellefjæringen fra utløpet. Gjenta 2-4 ganger eller til en visuell inspeksjon av lysbildet under mikroskopet bekrefter at det ikke er overflødige celler igjen.
MERK: Det kan være en fordel å lagre overflødige celler fra den første vasken. Hvis mønstereffektiviteten er utilfredsstillende, kan overflødige celler sentrifugeres og brukes på nytt i et lavere volum av PBS for å skape en mer celletett løsning, og deretter kan prosessen gjentas fra trinn 6.2. - Gjenta trinn 6.1-6.4 for hvert sett med celler i mønsteret. For mønstre der flere celletyper er direkte mønstret av overflatemalen, starter du med den minst tallrike celletypen for mønsteret og slutter med den mest tallrike celletypen.
MERK: Det anbefales å gjøre hver runde med cellulær montering sekvensielt i stedet for å samle cellene, selv under forhold der cellene alle er merket med ortogonale DNA-sekvenser. Sammenslåing av cellene fortynner effektivt hver cellepopulasjon og reduserer mønstereffektiviteten. - Når den siste runden med cellesamling er fullført, vil de neste trinnene variere basert på det spesifikke eksperimentet. Hvis cellene er ment å forbli på glasset, legger du til medier i en Petri-tallerken som inneholder lysbildet, og deretter bruker du tang til å skyve PDMS-strømningscellene ut av lysbildet. Hvis cellene skal bygges inn i en hydrogel og dyrkes i 3D, går du videre til trinn 7.
7. Overfør til hydrogel for 3D-kultur (valgfritt)
- Forbered en hydrogelforløperløsning som inneholder 2 % DNase.
MERK: Sammensetningen av løsningen vil variere basert på eksperimentelt oppsett. Matrigel og blandinger av Matrigel og kollagen Jeg jobber godt i denne protokollen, men andre hydrogeler er også mulig. - Tilsett 50 μL hydrogeloppløsning som inneholder 2 % DNase, i innløpet til hver strømningscelle. Aspirer overflødig væske fra utløpet, og driv hydrogelløsningen inn i strømningscellen. For viskøse hydrogelforløpere kan det være nødvendig å vippe gliden litt for å hjelpe hydrogelstrømmen inn i strømningscellen.
- Inkuber skredet ved 37 °C i 30-45 min (avhengig av hydrogelgelasjonskinetikk) slik at hydrogelen kan sette og spalte den DNA-baserte vedheften mellom cellene og overflaten.
- Fjern hver strømningscelle fra lysbildet og plasser på toppen av hydrogelforløperløsningen.
- Tilsett 50 μL hydrogelforløper i en brønn med en 2-brønns kammersklie eller en 6-brønns plate.
- Pipette 10 μL PBS på hver side av hver strømningscelle.
- Bruk et barberblad eller fine pinsett til å fordele PBS langs hele lengden av strømningscellen, og løft deretter forsiktig sidene av strømningscellen slik at PBS rushes under hydrogelen.
MERK: Dette vil "flyte" hydrogelen over lysbildet, slik at den kan overføres uten forvrengning eller riving. - Bruk et barberblad til å flytte strømningscellen forsiktig til kanten av glasssklie.
- Snu lysbildet. Med barberbladet skyver du strømningscellen av lysbildet slik at den lander på toppen av barberbladet.
- Plukk strømningscellen av barberbladet ved hjelp av buede tang. Inverter strømningscellen slik at cellene er på bunnen, og plasser deretter på toppen av dråpen av hydrogelforløperløsning.
- Gjenta trinn 7.4.1 - 7.4.6 for hver strømningscelle.
- Inkuber i minst 30 minutter slik at hydrogelen som inneholder de mønstrede cellene, kan binde seg til hydrogelunderlaget, noe som resulterer i full innebygging av de mønstrede cellene.
- Fjern PDMS-flytcellen.
- Legg til nok medier til å fordype PDMS-flytcellen.
MERK: Tilstrømningen av medier vil løsne vedheftet mellom hydrogelen og PDMS-strømningscellen. - Bruk buede tang, orientert langs den lange aksen i flytcellen, til å skyve flytcellen forsiktig til den spretter av og flyter inn i mediet. Samle strømningscellen med tang og kast.
MERK: For optimale resultater, spre de buede tangene og påfør forsiktig trykk på veggene i PDMS-strømningscellen. Bruk kraft i retning av den lange aksen til strømningscellen.
- Legg til nok medier til å fordype PDMS-flytcellen.
8. Bekreft vellykket merking av celler med CMO (valgfritt, for feilsøking)
- Bestill et fluorescerende modifisert (FAM eller AF647) oligonukleotid som er komplementært til overflateadhesjonssekvensen til Adapter Strand som brukes i eksperimentet.
- Merk celler med CMO DNA og vask ut overflødig DNA som beskrevet i trinn 5. Resuspend i 200 μL iskald PBS.
- Utgjør en 4 μM løsning av fluorescerende merket komplementært oligonukleotid i PBS. Tilsett 200 μL av denne løsningen til cellesuspensjonen. Inkuber på is i 5 min.
- Tilsett 1 ml iskald PBS. Bland. Sentrifuger cellene for å pellet dem. Fjern supernatant. Gjenta denne prosessen to ganger til for å vaske ut dna som ikke har hybridisert.
- Utfør analytisk strømningscytometri for å kvantifisere tilstedeværelsen av DNA på celleoverflaten.
- På et strømningscytometer analyserer du kontrollceller som ikke er merket med DNA. Sett opp porter basert på denne populasjonen.
- Analyser CMO-merkede celler som har blitt behandlet med et fluorescerende merket komplementært oligonukleotid.
- Beregn gjennomsnittlig fluorescensintensitet.
Denne protokollen gjør det mulig å mønstre celler i 2D og 3D med høy presisjon og uten bruk av tilpassede reagenser eller dyrt renromsutstyr. Figur 1 viser en oversikt over protokollen. For det første opprettes DNA-funksjonaliserte lysbilder gjennom fotolittografi. Deretter er celler merket med CMOer. Cellene flyter deretter over lysbildet, der de bare festes til de DNA-funksjonaliserte områdene i lysbildet. Etter at overflødige celler er vasket bort, avsløres ønsket mønster av celler. Disse cellene kan dyrkes på lysbildet eller bygges inn i en hydrogel som inneholder DNase og overføres fra lysbildet for 3D-cellekultur.
Merking av celler med CMOer gjør det mulig å feste seg til det DNA-mønstrede lysbildet (figur 2). For det første er den kolesterolmodifiserte Universal Anchor Strand forhåndshybridisert med Adapter Strand. Deretter blandes Universal Anchor + Adapter-løsningen 1:1 med celleopphenget. Kolesterolet på Universal Anchor + Adapter-komplekset settes inn i cellemembranen. Tillegg av kolesterolmodifisert Universal Co-Anchor Strand, som hybridiserer med Universal Anchor Strand, forbedrer stabiliteten til CMO-komplekset i cellemembranen ved å øke netto hydrofobiskheten til komplekset26. Etter å ha vasket ut overflødig DNA fra celleopphenget, blir cellene strømmet over lysbildet. Hybridisering mellom Adapter Strand og Surface DNA Strand resulterer i tilknytning av celler til de DNA-mønstrede områdene i lysbildet.
Mønsteret av cellene er opprettet ved hjelp av fotolitografi for å begrense vedlegget av aminmodifisert DNA oligos til bestemte områder av en aldehydmodifisert glass lysbilde29 (Figur 3A). Positiv fotoresist er spin-belagt på en aldehyd-funksjonalisert lysbilde. En gjennomsiktighetsfotomaske plasseres deretter oppå lysbildet, og lysbildet utsettes for UV-lys. Etter utvikling er områdene i lysbildet som ble utsatt for UV-lys ikke lenger belagt i fotoresist og har dermed utsatt aldehydgrupper. En 20 μM løsning av aminmodifisert DNA-oligos slippes deretter på lysbildet og spres for å dekke de mønstrede områdene. Baking etterfulgt av reduktiv aminering resulterer i et kovalent bånd mellom det aminmodifiserte DNA-et og skredet. Bemerkelsesverdig kan denne prosessen gjentas for å mønstre flere oligos uten tap av funksjonalitet i de tidligere mønstrede oligos (Figur 3B). Det bør imidlertid utvises forsiktighet for å unngå overlappende mønstre, noe som resulterer i tilstedeværelse av begge oligoene ved redusert konsentrasjon (Supplerende figur 3). Flere cellepopulasjoner kan mønstres sekvensielt ved å bruke adapterstrenger som er forskjellige i det modulære domenet (de 20 basene nærmest 3'-enden).
Selv om denne fotopatterningsprotokollen ble utviklet av Scheideler et al. i sammenheng med et rent rom, har vi vist at det er mulig å oppnå lignende resultater med et billig, "hjemmebrygget" fotolitografioppsett som passer lett i en kjemisk avtrekkshette. Oppsettet inkluderer en spin coater på $ 400 laget av en DC-motor, digital kontroller og CD-kakeboks, samt en UV-lampe som ble montert fra individuelle komponenter og plassert i en gjenbrukt sharps-beholder (Tilleggsfigur 1). Den største fordelen med hjemmebrygget fotoliografioppsett er at det er veldig rimelig (< $ 1000 for alt utstyret) samtidig som du kan lage funksjoner i enkeltcellestørrelse. Bruken av billig utstyr har imidlertid sine begrensninger - for eksempel er det mer utfordrende å nøyaktig justere fiducial markører for å mønstre flere DNA-oligoer uten bruk av maskejustering. Vi anbefaler dette rimelige fotolitografioppsettet for laboratorier som ikke har praktisk tilgang til et rent rom eller som vil prøve denne metoden uten en stor investering.
For å identifisere optimale forhold for DNA-programmert celleadhesjon varierte vi systematisk konsentrasjonene av DNA-tråder på celleoverflater og målte effektiviteten av celleadhesjon til DNA-modifiserte glassoverflater. Konsentrasjonen av Universal Anchor + Adapter Strand og Universal Co-Anchor i merkingsløsninger ble variert over flere størrelsesordener (Figur 4A,B), noe som resulterte i 104 - 106 DNA-komplekser per celle (Supplerende figur 4). Celleadhesjon var doseavhengig, med minimal celleadhesjon til DNA-mønsteret når cellene ble merket med CMOer i en konsentrasjon på 0,05 μM eller mindre, og høyt belegg ved en konsentrasjon på 2,5 μM og høyere. Vi brukte derfor en 2 μM-løsning av Universal Anchor + Adapter Strand og 2 μM løsning av Universal Co-Anchor i de fleste eksperimenter. Celleadhesjon forventes også å avta dersom mengden DNA som brukes på glassoverflaten gikk ned29, eller hvis uoverensstemmelsene mellom adapterstrengen og overflatestrengen økte. Du finner mer informasjon om adapterstrengsekvensutforming i Tilleggsfil 2. CMO-merking ved hjelp av adapterstrenger uten CpG-repetisjoner stimulerte ikke TLR9 i HEK-celler som uttrykker musen TLR9 (Supplerende figur 5).
Vi tilbyr flere demonstrasjoner som den reviderte protokollen gir reproduserbar og effektiv DNA-programmert celleadhesjon. For eksempel, humane navlestrengsbentelceller (HUVECs) merket med CMOer festet til DNA-mønstre med høy effektivitet. CMO-merkede HUVECer fulgte i tillegg til LMO-merkede HUVECer (figur 5A). Celler mønstret ved hjelp av CMO-DPAC beholdt sin levedyktighet og funksjonalitet. Celler merket med CMOer ble farget av calcein AM og ethidium homodimer for å vurdere levedyktighet (Supplerende figur 6). Forskjeller i levedyktighet sammenlignet med umerkede kontrollceller var små (94 % vs. 97 %). Enkle MDCK-er mønstret via CMO-DPAC og overført til Matrigel var i stand til å spre seg og polarisere riktig etter 5 dager med kultur (Figur 5B). DPAC gir også en måte å utdype mønstre av celler i den tredje dimensjonen (Figur 5C). Flerlags, flercellulære aggregater kan for eksempel opprettes ved å veksle mellom lag med celler merket med komplementære CMOer (figur 5C). Disse eksperimentene viser at protokollen er reproduserbar, ikke påvirker cellens levedyktighet eller funksjonalitet negativt, og gir cellulære mønstre som kan dyrkes innenfor et enkelt bildeplan i en 3D ECM.
Ved å gi ortogonale DNA-sekvenser for å lede celleadhesjon, gir DPAC et middel til å mønstre flere celletyper på en enkelt overflate. For å implementere denne funksjonen i DPAC må DNA-mønstre generert av fotolitografi være på linje med hverandre. Metallfiduciary markører avsatt på lysbildet tillatt for justering av flere fotomasker og derfor mønster av flere celletyper samtidig. MCF10Som farget med forskjellige unike fargestoffer ble merket med ortogonale CMOer og mønstret for å skape en visualisering av UC Berkeley- og UCSF-logoene (Figur 6). Dette eksperimentet viser at flere unike cellepopulasjoner kan mønstres sammen med høy presisjon og uten krysskontaminering.
Vellykket mønster av celler ved hjelp av CMO-DPAC krever fotolitografi av høy kvalitet, tilstrekkelig konsentrasjon av oligo på celleoverflaten, høy tetthet av celler over mønsteret og tilstrekkelig vasking. Hvis du ikke gjør noe av dette, påvirkes det endelige resultatet. Supplerende figur 2 inneholder eksempelbilder av korrekt og feil fotolittografi (Tilleggsfigur 2A), ønsket celletetthet over mønsteret for å lage fullt okkuperte mønstre (Tilleggsfigur 2B), tap av mønstrede celler på grunn av altfor kraftig pipettering under påfølgende trinn i DPAC (Tilleggs figur 2C) og uønsket klumping av celler (Supplerende figur 2D). Tabell 1 inneholder en liste over vanlige feilpunkter og den foreslåtte feilsøkingen. Bruk av fluorescerende komplementære oligos anbefales som et verktøy for feilsøking for å bekrefte tilstedeværelsen av mønstret DNA på lysbildet og tilstedeværelsen av CMOer på celleoverflaten ved strømningscytometri (se trinn 8 i protokollen).
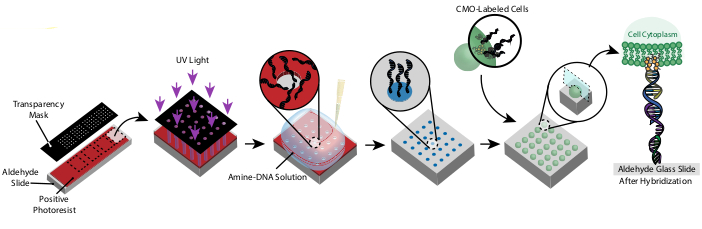
Figur 1: Oversikt over CMO-DPAC-protokollen. For det første er et DNA-mønstret lysbilde opprettet ved å belegge en aldehydfunksjonalisert glasssklie med en positiv fotoresist, dekke den med en gjennomsiktig maske i ønsket mønster og utsette den for UV-lys. Den UV-eksponerte fotoresisten vaskes bort med utvikleren, og etterlater eksponerte områder av aldehydsklie og tillater binding av aminfunksjonalisert DNA til overflaten. Celler merkes deretter med CMOer og strømmes over overflaten. DNA-et på cellemembranen hybridiserer til DNA på overflaten, noe som resulterer i vedheft. Klikk her for å se en større versjon av denne figuren.
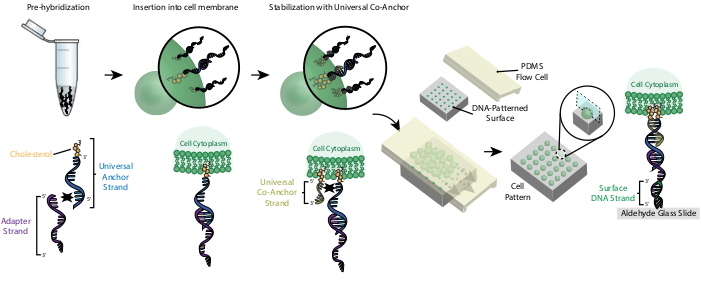
Figur 2: Celler er merket med CMOer i en trinnvis prosess. For det første er den kolesterolmodifiserte Universal Anchor Strand forhåndshybridisert med Adapter Strand. Deretter blandes Universal Anchor + Adapter-løsningen med celleopphenget. Kolesterolet på Universal Anchor + Adapter-komplekset settes inn i cellemembranen. Etter inkubasjon legges den kolesterolmodifiserte Universal Co-Anchor Strand til cellefjæringen, hvor den hybridiserer med Universal Anchor Strand og setter inn i cellemembranen. Tilsetningen av det andre kolesterolmolekylet øker netto hydrofobiskheten til DNA-komplekset og stabiliserer det i membranen26. Etter å ha vasket ut overflødig DNA, blir cellene konsentrert og lagt til en PDMS-strømningscelle på toppen av den mønstrede overflaten. 3' enden av Adapter Strand hybridiserer med Surface DNA Strand på glasssklie, noe som resulterer i vedheft til lysbildet spesielt i regioner funksjonalisert med komplementært DNA. Klikk her for å se en større versjon av denne figuren.
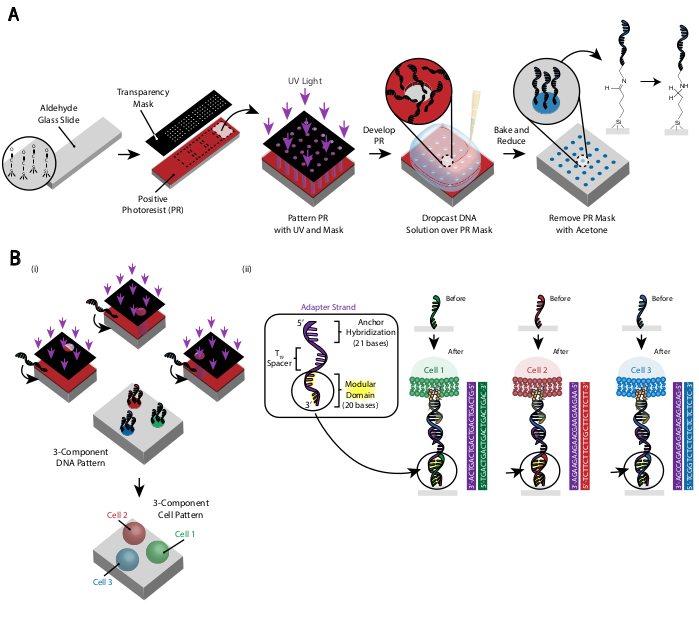
Figur 3: Fotolitografi brukes til å lage DNA-mønstrede lysbilder som til slutt dikterer plasseringen av celler. (A) Oversikt over fotolitografiprosess. Et aldehydfunksjonalisert lysbilde er spin-belagt med en positiv fotoresist. UV-lys skinner på lysbildet gjennom en gjennomsiktig bildemaske som er gjennomsiktig der celleadhesjon er ønsket. Etter at skredet er utviklet, har regionene som tidligere var utsatt for UV-lys nå eksponert aldehydgrupper. En 20 μM løsning av en amin-funksjonalisert DNA-oligo blir deretter sluppet på lysbildet og spredt over de mønstrede områdene. Lysbildet blir deretter bakt for å indusere dannelsen av Schiff-bindinger (C =N) mellom amin- og aldehydgruppene, en reversibel kovalente binding29. Etterfølgende reduktiv aminering med 0,25% natriumborohydrid i PBS konverterer Schiff-basen til en sekundær amin ved reduktiv aminering, noe som resulterer i en irreversibel binding mellom DNA og lysbildet. Den gjenværende fotoresisten kan deretter fjernes ved å skylle med aceton. (B) Denne prosessen kan gjentas for å lage DNA-mønstre med flere komponenter og derfor utføre eksperimenter med flere cellepopulasjoner. (i) Etter at den første oligo er mønstret, er lysbildet igjen belagt med fotoresist og protokollen fortsetter som før. Justering av fotomaskene ved hjelp av fiduciary markører er nødvendig for å mønstre flere DNA-tråder. (ii) Hver celletype som mønstres, er forskjellig i det 20-baserte modulære domenet til Adapter Strand. Ved å bruke ortogonale sett med komplementære oligos, kan flere celletyper mønstres uten kryssadhesjon. Klikk her for å se en større versjon av denne figuren.
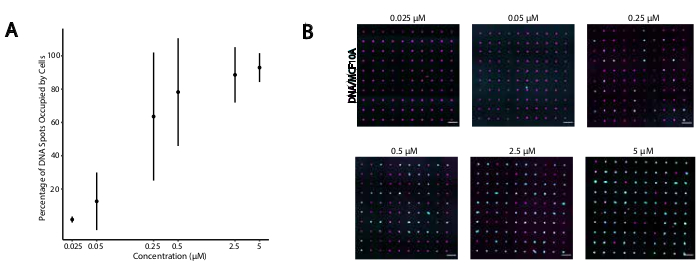
Figur 4: Vedheft av CMO-merkede celler til DNA-mønstre øker som en funksjon av CMO-konsentrasjon under merking. I dette eksperimentet ble Universal Anchor + Adapter Strand (pre-hybridisert) og Universal Co-Anchor brukt ved like konsentrasjoner. Konsentrasjon refererer til konsentrasjonen av CMO i cellefjæringen under CMO-merking av celler. (A) Kvantifisering av prosentandelen av DNA-flekker med 15 μm diameter som ble okkupert av CMO-merkede MCF10A-celler som en funksjon av CMO-konsentrasjon under cellemerking. Data representert som gjennomsnittet ± standardavvik fra tre eksperimenter. (B) Representative bilder av DNA-mønstrene (magenta) og festet MCF10As (cyan) ved forskjellige konsentrasjoner av CMO. Skalalinje = 100 μm. Klikk her for å se en større versjon av denne figuren.
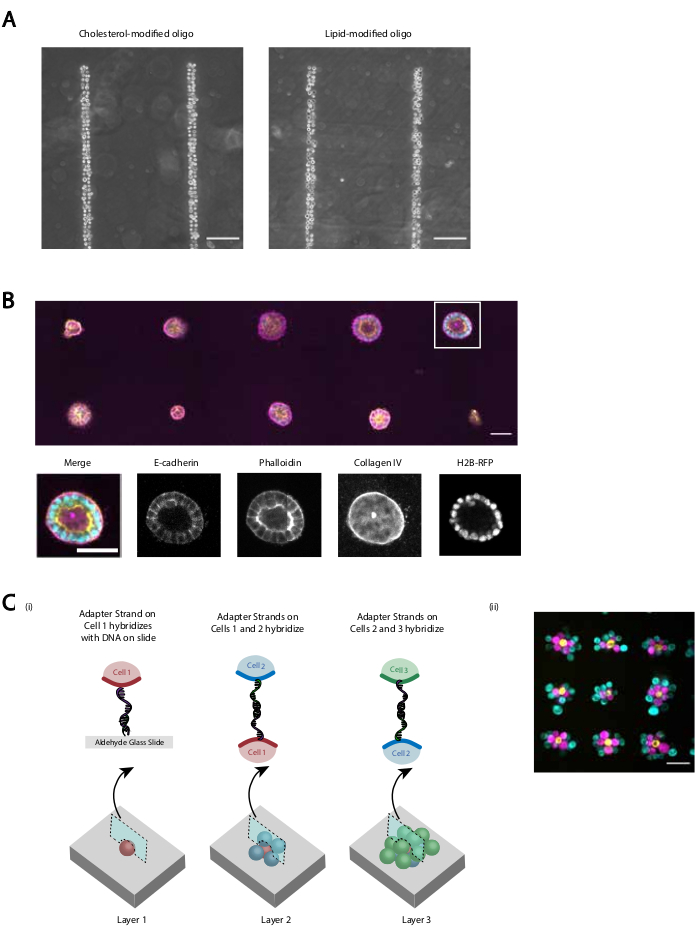
Figur 5: CMO-DPAC kan brukes til å lage todimensjonale cellemønstre som senere kan bygges inn i en tredimensjonal hydrogel for kultur og/eller lagdelt for å skape flerlagsstrukturer. (A) Direkte sammenligning mellom CMO-merkede humane navlestrengsvene endotelceller (HUVEC) og LMO-merkede HUVECer festet til et lineært DNA-mønster. Begge metodene for cellemerking resulterer i nesten 100% belegg av DNA-mønsteret. (B) Single Madin-Darby Canine Kidney cells (MDCKs) som uttrykker H2B-RFP ble mønstret på 15 μm diameter flekker fordelt 200 μm fra hverandre og deretter innebygd i Matrigel. Etter 120 h kultur ble de resulterende epitelcystene festet og farget for E-kadherin, aktin og kollagen IV. Sfæroid i hvit boks vises i detalj. Skalalinje = 50 μm. (C) Flerlags cellulære strukturer kan opprettes ved å merke separate cellepopulasjoner med komplementære adapterstrenger og mønster sekvensielt slik at hvert nytt tillegg av celler holder seg til cellelaget før det. (i) Et skjema av sekvensiell mønster av cellepopulasjoner for å opprette flerlagsstrukturer. (ii) Trelags cellemengder av MCF10Aer (visualisert ved hjelp av fargestoffer) ble opprettet ved hjelp av denne prosessen. Skalalinje = 50 μm. Klikk her for å se en større versjon av denne figuren.

Figur 6: Flere celletyper kan mønstres uten krysskontaminering eller tap av vedheft. Flere aminmodifiserte DNA-oligoer ble mønstret sekvensielt på en aldehydsklie og justert ved bruk av metallfiduciary markører. Tre populasjoner av MCF10As (cyan, magenta, gul) ble farget med unike fargestoffer merket med komplementære CMOer, og mønstret på lysbildet, noe som resulterte i et bilde av UC Berkeley- og UCSF-logoene. Skalastang 1 mm. Klikk her for å se en større versjon av denne figuren.
Supplerende figur 1: Eksempelbilder av fotolitografioppsettet på benken. (A) Skyv på spin coater, dekket med positiv fotoresist, før spinnbelegg. (B) Bilde av gjennomsiktighetsfotomaske. (C) Under eksponeringen er fotomasken smurt mellom den fotoresistbelagte sklien og en glassskive. (D) Huset til UV-lampen ble laget av en re-purposed sharps container. (E) Skyv nedsenket i utviklerløsningen. (F) Utviklet lysbilde. (G) Aminmodifisert DNA-løsning spredt på mønstrede områder av skredet. (H) PDMS-flytceller plassert over mønstrede områder i lysbildet. Klikk her for å laste ned denne filen.
Supplerende figur 2: Noen eksempler på vanlige feil i denne protokollen. (A) (i) Underbaking før UV-eksponering eller overutviklende funksjoner etter eksponering kan resultere i funksjoner som har ujevne kanter og kan være uregelmessige i størrelse. (ii) Et eksempel på et riktig fotopatnert lysbilde som har rene kanter rundt funksjoner, ensartet funksjonsstørrelse og ingen åpenbare sprekker i mønsteret. Skalastang = 50 μm. (B) Celletetthet er avgjørende for mønstereffektivitet. Når du observerer cellene på toppen av mønsteret under et mikroskop, bør det være få hull mellom cellene, som det fremgår av eksempelbildet til venstre. Skalastang = 50 μm. (C) Mønstrede celler kan være følsomme for væskekrefter som oppstår fra altfor kraftig pipettering, noe som kan skade og løsne de mønstrede cellene. Cellemengder med flere lag er spesielt sårbare, ettersom én celle nederst støtter en struktur med flere celler. (i) En matrise med cellemengder som er innebygd i Matrigel. (ii) Et rutenett av celleaggregater som løsnet som følge av pipettering viskøs Matrigel for kraftig. (D) Klumping av celler kan forekomme, spesielt med epitelceller. Disse klumpene er vanligvis homotypiske, men kan være heterotypiske (celler som holder seg til allerede mønstrede celler av en annen type) hvis cellene er spesielt klissete. Bildet viser tre forskjellige populasjoner av MCF10As ble mønstret på en matrise sammensatt av tre forskjellige encellede DNA-flekker (15 μm). De fleste DNA-flekker har 2-4 celler festet. Klumping kan løses ved EDTA-behandling eller ved å filtrere ut klumpene før mønster. Skalastang = 100 μm. Klikk her for å laste ned denne filen.
Supplerende figur 3: Overlappende fotopatterner resulterer i tilstedeværelse av begge oligoene ved redusert konsentrasjon. To ortogonale aminmodifiserte oligoer ble fotopatternert sekvensielt, først en vertikal linje (Strand 1), etterfulgt av en horisontal linje som overlappet den (Strand 2). Oligoene ble deretter visualisert ved hybridisering med fluorescerende komplementære oligos. (A) Fluorescens bilde av Strand 1. (B) Kvantifisering av fluorescensprofilen til Strand 1 over en 100 μm vertikal linje som spenner over overlappingen. (C) Fluorescens bilde av Strand 2. (D) Kvantifisering av fluorescensprofilen til Strand 2 over en 100 μm horisontal linje som spenner over overlappingen. Skalastang = 50 μm. Klikk her for å laste ned denne filen.
Supplerende figur 4: Kvantifisering av DNA-komplekser på celleoverflaten som en funksjon av CMO-merkingskonsentrasjon. HUVEC ble merket med forskjellige konsentrasjoner av CMO-oppløsning, vasket og deretter inkubert med en fluorescerende komplementær tråd. Et MESF (Molecules of Equivalent Soluble Fluorochrome) mikrosfæresett ble brukt til å gjøre kvantitativ strømningscytometri og estimere antall DNA-komplekser på celleoverflaten som en funksjon av CMO-konsentrasjon under merking. Klikk her for å laste ned denne filen.
Supplerende figur 5: CMO-merking stimulerer ikke TLR9-responsen. Det ble utført et eksperiment for å se om CMO-merking ville utløse DNA-deteksjonsmekanismen til TLR9 og om dette ville bli påvirket av CPG-er i Adapter Strand-sekvensen. HEK-celler som uttrykker musen TLR9 ble inkubert over natten med 0,2 μM av enten ODN 1826 (en CpG-inneholdende TLR9-agonist), CMO Universal Anchor + Universal Co-Anchor + AdapterStreng som inneholder samme sekvens som ODN 1826 (CMO-CpG), eller CMO Universal Anchor + Universal Co-Anchor + Adapter Strand som inneholder en lignende sekvens, men med utskifting av CPG-ene med GPCer (CMO-GpC). TLR9 stimulering ville resultere i produksjon av SEAP (utskilt embryonal alkalisk fosfatase). SEAP-sekresjon ble kvantifisert av en kolorimetrisk analyse (absorbans). Behandlingstilstanden ble sammenlignet med hvileceller som bare ble behandlet med PBS. Inkubasjon med CMO-GPC stimulerte ikke TLR9-uttrykket. Inkubasjon med CMO-CpG var litt høyere enn hvileceller, men mye lavere enn ODN-1826. Klikk her for å laste ned denne filen.
Supplerende figur 6: Levedyktigheten til celler etter CMO-merkingsprosessen. For å vurdere hvordan protokollen påvirker levedyktigheten, ble HUVEC-er delt inn i fire populasjoner: en forble på is i 1 time, en ble spottet med PBS, men ellers tatt gjennom alle sentrifugerings- og vasketrinn, en ble merket med CMOer, og en ble merket med CMOer og filtrert gjennom et 40 μm filter for å fjerne klumper. Cellene ble deretter farget med calcein AM og ethidium homodimer for å vurdere antall levende og døde celler. Alle behandlinger resulterte i betydelig redusert levedyktighet enn iskontrollen (enveis ANOVA med Tukey post-hoc-analyse), men median levedyktighet for CMO-merking (med eller uten filtrering) var ca. 94%. Data samlet inn fra tre uavhengige eksperimenter. * = p < 0,05. = p < 0.0001 Klikk her for å laste ned denne filen.
| Resultat | Mulige årsaker | Foreslåtte rettelser |
| Fotolitografi – funksjoner er sprukket | Inkonsekvent eller utilstrekkelig mykbaking | Øk tiden for mykbaking opptil 3 minutter; verifisere faktisk temperatur på kokeplaten og øke temperaturen etter behov |
| Fotolitografi - funksjoner er ikke skarpe eller har fotoresist igjen i dem | Underutvikling | Øk tiden lysbildet bruker på utviklerløsning. innlemme mild agitasjon |
| Fotolittografi – funksjoner inkonsekvent på tvers av lysbilde | UV-lys er kanskje ikke sentrert eller ikke fokusert på riktig måte | Juster UV-lysoppsettet for å sikre kollatert lys med jevn intensitet |
| Celler holder seg ikke til mønstrede flekker med høy effektivitet | Ikke nok DNA på overflaten | Bekreft at DNA er til stede på overflaten ved å hybridisere lysbildet med fluorescerende komplementære oligos og deretter bildebehandling under mikroskop |
| Celler er utilstrekkelig merket med CMO | Tilsett fluorescerende komplementære oligos til celleoppheng og bekreft fluorescens via strømningscytometri | |
| Ikke nok celler over mønster | Samle celler ved å vaske ut fra PDMS strømningscelle, sentrifuge og suspendere på nytt i lavere volum for å konsentrere cellene | |
| For mye gjenværende CMO i cellefjæring, hybridisering med DNA på lysbilde | Legg til et nytt vasketrinn. Pass på å fjerne så mye supernatant som mulig med hver vask. | |
| For mye internalisering av CMO på grunn av tid og temperatur | Arbeid raskt etter merking av cellene med CMO; holde celler og gli på is og bruke iskalde reagenser | |
| Celler klumpete | Celler ble ikke tilstrekkelig separert under trypsinisering | Bruk PBS + 0,04% EDTA under cellevask; passere cellefjæring gjennom 35 μm filter før den endelige vasken |
| Celler følger ikke spesifikt | Hvis i ett bestemt område - kan skyldes riper på lysbilde, feiljustering av PDMS strømningsceller, eller søl av DNA utenfor mønsterområdet | Unngå riper, vær forsiktig med å justere PDMS-strømningscellene etter mønsterområdet |
| Hvis cellene holder seg overalt – utilstrekkelig blokkering eller vasking | Legg til flere vasker etter mønster av cellene; pipet mer kraftig under vasker; blokk med 1% BSA lenger før du starter cellemønster; silaniser lysbilde (valgfritt trinn 3) eller bekreft at silaniseringen var vellykket ved å måle kontaktvinkelen til vanndråpen | |
| Bobler dannes i flytcellen | Pipetteringsfeil, ujevn hydrofil overflate skapt under plasmaoksidasjon | Hvis boblene er små, legger du til PBS i innløpet til strømningscellen, og de kan vaskes ut. Hvis boblene er større, bruker du skånsomt trykk på PDMS-strømningscellen og dytter boblene mot innløpet eller uttaket. |
| Celler holder seg i utgangspunktet til mønster, men fjernes under vask, mønster av andre celletyper, eller legger til hydrogelforløperen | Skjærkreftene fra pipettering for kraftig kan føre til at cellene løsner fra overflaten | Pipet mer forsiktig under etterfølgende vasker, runder med cellemønster eller tilsetning av hydrogelforløpere. Fordi hydrogelforløperne er viskøse, er det mer sannsynlig at de får mønsteret til å løsne, så vær ekstra forsiktig. Flerlagsstrukturer har en tendens til å være topptunge og er mer utsatt for å bli løsnet. |
| Vev deformeres under 3D-overføring | Hydrogel stikker for å gli | Bekreft hydrofobiskheten til lysbildet ved hjelp av måling av kontaktvinkel |
| Bruk barberbladet til å løfte PDMS helt på begge kanter, slik at PBS kan flyte under vevet | ||
| Dette kan skje med rene kollagenhydrgeler – vurder å justere proteinkonsentrasjonen eller sammensetningen av hydrogel | ||
| Celler overføres ikke med hydrogelen og forblir på lysbildet | Øk Turbo DNAse konsentrasjonen eller øke inkubasjonstiden | |
| Hydrogel er ikke solid nok | Øk inkubasjonstiden og/eller gelasjonsmekanismen for den aktuelle hydrogelen (f.eks. for kollagen, sørg for at pH er riktig) | |
| Hydrogel tårer ved fjerning av PDMS | Gjør PDMS-strømningsceller hydrofile ved hjelp av plasmaoksidasjon før du begynner å eksperimentere, slik at de lett løsner ved tilsetning av medier. Bruk tang veldig forsiktig for å løsne PDMS. |
Tabell 1: En feilsøkingsveiledning for å identifisere og løse potensielle feil som kan oppstå fra denne protokollen. Spesielt kan dårlig vedheft av celler til mønsteret ha mange grunnårsaker, og denne guiden skal hjelpe med identifisering og løsning av disse problemene.
Tilleggsfil 1. Klikk her for å laste ned denne filen.
Tilleggsfil 2. Klikk her for å laste ned denne filen.
Tilleggsfil 3. Klikk her for å laste ned denne filen.
Tilleggsfil 4. Klikk her for å laste ned denne filen.
I denne artikkelen presenterer vi en detaljert protokoll for høyoppløselig mønster av celler i 2D og 3D for in vitro cellekultureksperimenter. I motsetning til tidligere publiserte versjoner av denne metoden, fokuserer protokollen som presenteres her på brukervennlighet: den krever ikke høyt spesialisert utstyr, og alle reagenser kan kjøpes fra leverandører i stedet for å kreve tilpasset syntese. I motsetning til andre cellemikropatterningsmetoder er denne metoden rask og celletype agnostisk: det krever ikke spesifikk vedheft til ekstracellulære matriseproteiner15. Celler mønstret av CMO-DPAC kan bygges inn i en ekstracellulær matrise som Matrigel eller kollagen, noe som resulterer i 3D-kulturer med mye høyere romlig oppløsning enn det som for tiden er mulig med ekstruderingsutskriftsbaserte metoder22. CMO-DPAC kan brukes til å lage hundrevis til tusenvis av mikroskopiske funksjoner per lysbilde, slik at mange replikeringer kan utføres samtidig.
En av de viktigste parametrene for å lykkes med denne protokollen er tettheten av celler som legges til flytcellene på toppen av det mønstrede lysbildet. Ideelt sett bør tettheten være minst 25 millioner celler / ml. Når den lastes inn i strømningscellene, resulterer denne tettheten av celler i en nesten tettpakket monolayer av celler over mønsteret (Supplerende figur 2B). Disse høye celletetthetene maksimerer sannsynligheten for at en celle vil bosette seg direkte på toppen av et DNA-sted og følge. Hvis du reduserer celletettheten, reduseres den totale mønstereffektiviteten. Et annet kritisk trinn i denne protokollen er å suspendere cellene grundig i PBS eller serumfrie medier før du legger til CMO-løsningen. CMO-ene partisjonerer veldig raskt i cellemembraner og legger cmo-løsningen direkte til en cellepellet vil resultere i heterogen merking av celler. Etter å ha lagt CMO-løsningen til cellefjæringen, er det viktig å blande grundig ved pipettering slik at cellene er jevnt merket med CMOene. Etter inkubasjonene er det nødvendig å vaske ut overflødige CMOer grundig gjennom flere sentrifugerings- og vasketrinn. Overflødig gratis CMO tilstede i cellefjæringen vil binde seg til det mønstrede aminmodifiserte DNA-et på glasssklie, blokkere hybridisering og vedheft av CMO-modifiserte celler i suspensjon. Tid er også en viktig faktor for denne protokollen. Det er viktig å jobbe så raskt som mulig når du bruker CMOer og for å holde cellene på is for å minimere internalisering av CMOene og maksimere celle levedyktigheten. Flowcytometriforsøk har vist at CMOer ikke vedvarer så lenge på celleoverflaten som LMOer, med 25% tap av CMO-komplekser over to timer inkubasjon på is36. Videre vil levedyktigheten til celler reduseres etter hvert som cellehåndteringstiden øker. Levedyktighet kan maksimeres ved å jobbe raskt, holde celler på is, bruke iskalde reagenser og bruke serumfrie medier for å gi noen næringsstoffer.
Selv om CMO-DPAC kan være en kraftig måte å studere cellebiologi ved å mønstre celler med høy presisjon, har den sine begrensninger. CMO-DPAC-eksperimenter kan være utfordrende, spesielt ettersom den eksperimentelle kompleksiteten legges til med flere celletyper, lag eller 3D-cellekultur (Tilleggsfil 1). Eksperimentelle feil kan være vanlige når du starter denne protokollen, som beskrevet i tabell 1. Derfor anbefaler vi at brukere innfører kvalitetskontrollkontroller (bekrefter at DNA er til stede på lysbildet, bekrefter at cellene er tilstrekkelig merket med DNA (trinn 8), som bekrefter at overflødige celler er grundig vasket bort, etc.) for å sikre at eksperimentet lykkes og for å identifisere trinn som kan kreve ytterligere optimalisering. Vi håper at informasjonen i dette manuskriptet og dets tilleggsfiler vil bidra til å lette enhver nødvendig feilsøking.
Kolesterol er et bioaktivt molekyl hvis internalisering kan påvirke cellemetabolisme, genuttrykk og membranfluiditet37,38. En tidligere studie sammenlignet effektene på genuttrykk av CMO- og LMO-merkede celler ved hjelp av enkeltcellet RNA-sekvensering. CMO-merkede HEK-celler hadde endret genuttrykk sammenlignet med umerkede og LMO-merkede celler36. Merking av celler med CMOer resulterte i differensialuttrykket (> 1,5 ganger) av åtte gener i forhold til umerkede kontroller, inkludert AP2B1, som har vært knyttet til kolesterol og sphingolipid transport (GeneCards) og MALAT1, en lang ikke-koding RNA som regulerer kolesterolakkumulering39. Selv om de er små, kan disse transkripsjonelle responsene likevel være av bekymring hvis det aktuelle eksperimentet studerer metabolisme, membrandynamikk eller andre kolesterolrelaterte veier i celler.
Denne protokollen er fleksibel og kan justeres for å møte behovene til hvert eksperiment. Fordi CMO setter seg inn i lipidmembranen i stedet for å bruke en bestemt reseptor, er metoden celletypeagnostisk (HUVECer, MCF10As, HEKs og MDCK er demonstrert her). Selv om kolesterol er et annet hydrofobt anker enn våre tidligere publiserte LMOer, har vi så langt funnet at de oppfører seg på samme måte. Dermed forventer vi at CMOene fungerer med noen av de mange forskjellige celletypene som vi tidligere har publisert med LMOer, inkludert, men ikke begrenset til nevrale stamceller, fibroblaster, perifere mononukleære celler i blodet, tumorceller og primære pattedyrepiterieceller6,23,27,29,36 . CMO-merking stimulerer ikke TLR9, noe som tyder på at protokollen er kompatibel med immunceller. Membran inkorporering av CMO er en funksjon av total cellestørrelse og graden av negativ ladning i cellen glykokalyx35. Dermed har vi inkludert en protokoll (trinn 8) for å teste omfanget av membraninnretning som er egnet til rask optimalisering. De spesifikke egenskapene til hvert cellemønster vil uunngåelig variere basert på eksperimentell design (se Tilleggsfil 1 for mer veiledning). Selv om fotopatterningsprotokollen beskrevet ovenfor for mønster av DNA anbefales, bør enhver metode for romlig begrensende dråper med amin-DNA-løsning fungere, for eksempel bruk av høyoppløselige dråpeskrivere. Mønsteroppløsningen og minimumsavstanden for funksjoner varierer avhengig av metoden som brukes. Det er også teoretisk mulig å kombinere DNA-fotopatterning-delene av denne protokollen med andre metoder som har blitt brukt til å merke celler med DNA, for eksempel med DNA hybridisert til membran-uttrykte sinkfingre40, ved hjelp av NHS-konjugert DNA41, og reagerer azido sialsyrerester på celleoverflaten med fosfinkonjugert DNA42 . CMO-DPAC kan brukes på en rekke eksperimenter som krever tett kontroll over cellecelleavstand, inkludert studier av interaksjoner mellom cellepar, samkultureksperimenter som ser på overføring av signaler fra "avsender" celler til "mottaker" celler, og undersøkelser av effekten av nærliggende ekstracellulære signaler på stamcelledifferensiering6,29 . Metoden kan også brukes til å lage mikrobrikker som kan brukes til å studere cellemigrering i tre dimensjoner, selvorganisering av celler i vev23,27og det dynamiske samspillet mellom celler og ECM27. Vi håper at denne protokollen vil gi forskere en tilgjengelig plattform for å utforske nye anvendelser av DNA-basert cellemønster med høy oppløsning i sine egne laboratorier.
Z.J.G. er rådgiver og aksjeeier i Provenance Biosciences.
Forfatterne vil takke Jeremy Garcia for å ha testet denne protokollen og Bhushan Kharbikar for å ha gitt opplæring i utstyret ved UCSF Biomedical Micro and Nanotechnology Core. Denne forskningen ble delvis støttet av tilskudd fra Department of Defense Breast Cancer Research Program (W81XWH-10-1-1023 og W81XWH-13-1-0221), NIH (U01CA199315, DP2 HD080351-01, 1R01CA190843-01, 1R21EB019181-01A og 1R21CA182375-01A1), NSF (MCB1330864) og UCSF Center for Cellular Construction (DBI-1548297), et NSF Science and Technology Center. O.J.S ble finansiert av et NSF Graduate Research Fellowship, et Siebel-stipend og et P.E.O. Scholarship. Z.J.G og A.R.A. er Chan-Zuckerberg BioHub-etterforskere.
| Name | Company | Catalog Number | Comments |
| 2-well Chambered Coverglass w/ non-removable wells | Thermo Fisher Scientific | 155379 | |
| Acetic Acid | Sigma-Aldrich | A6283 | |
| Adapter with External SM1 Threads and Internal SM3 Thread | ThorLabs | SM3A1 | |
| Aldehyde Functionalized Slides | Schott | Nexterion Slide AL | Store under dry conditions after opening. |
| All Plastic Syringes, 1 mL | Fisher Scientific | 14-817-25 | |
| Amine-Modified DNA Oligo | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| Aspheric Condenser Lens | ThorLabs | ACL7560 | |
| Borosilicate Disc, 6in Diameter X 1/2in Thick | Chemglass | CG-1906-23 | |
| Cell Culture Dishes 60x15 mm style | Corning | 353002 | |
| Cholesterol-Modified Oligo | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| Diamond Scribe | Excelta | 475B | |
| DNA Oligonucleotide | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| DPBS, no calcium, no magnesium | Thermo Fisher Scientific | 14190250 | |
| Isopropyl Alcohol | Sigma-Aldrich | 278475 | |
| Matrigel Matrix, Growth Factor Reduced | Corning | 354230 | |
| Methylene Chloride (Stabilized/Certified ACS) | Fisher Scientific | D37-4 | |
| MF-321 Developer | Kayaku Advanced Materials | n/a | |
| Microposit S1813 Positive Photoresist | Kayaku Advanced Materials | n/a | |
| Ø3" Adjustable Lens Tube, 0.81" Travel | ThorLabs | SM3V10 | |
| Oven | Thermo Scientific | 51-028-112H | |
| PE-50 Compact Benchtop Plasma Cleaning System | Plasma Etch | PE-50 | |
| Photomask (custom) | CAD/Art Services | n/a | Minimum feature size guaranteed by CAD/Art Services is 10 microns. |
| Razor Blades | Fisher Scientific | 12-640 | |
| RCT Basic Hot Plate | IKA | 3810001 | |
| Silicon Wafer (100 mm) | University Wafer | 590 | |
| Sodium Borohydride, 98%, granules | Acros Organics | 419471000 | |
| Spin Coater Kit | Instras | SCK-200 | This is a low cost option, but any spin coater that can maintain a speed of 3000 rpm will suffice. |
| SU-8 2075 | Microchem | Y111074 0500L1GL | |
| SU-8 Developer | Microchem | Y020100 4000L1PE | |
| Sylgard 184 Silicone Elastomer Kit | Dow | 2646340 | |
| Syringe Needles | Sigma-Aldrich | Z192341 | |
| T-Cube LED Driver, 1200 mA Max Drive Current | ThorLabs | LEDD1B | |
| Tridecafluoro-1,1,2,2-tetrahydrooctyl dimethylchlorosilane | Gelest | SIT8170.0 | |
| Triethylamine | Sigma-Aldrich | 90335 | |
| Turbo DNase | Thermo Fisher Scientific | AM2238 | |
| Tweezers Style N7 | VWR | 100488-324 | The curved shape of these tweezers is essential for delicately picking up the PDMS flow cells containing patterned tissues. |
| UV LED (365 nm, 190 mW (Min) Mounted LED, 700 mA) | ThorLabs | M365L2 | |
| Wafer Tweezers | Agar Scientific | T5063 | |
| WHEATON Dry-Seal vacuum desiccator | Millipore Sigma | W365885 |
- Kreeger, P. K., Strong, L. E., Masters, K. S. Engineering approaches to study cellular decision-making. Annual Review of Biomedical Engineering. , 49-72 (2018).
- Goubko, C. a., Cao, X. Patterning multiple cell types in co-cultures: A review. Materials Science and Engineering C. 29 (6), 1855 (2009).
- Sun, W., et al. The bioprinting roadmap. Biofabrication. 12 (2), 022002 (2020).
- Liu, W. F., Chen, C. S. Cellular and multicellular form and function. Advanced Drug Delivery Reviews. 59 (13), 1319-1328 (2007).
- Duffy, R. M., Sun, Y., Feinberg, A. W. Understanding the role of ECM protein composition and geometric micropatterning for engineering human skeletal muscle. Annals of Biomedical Engineering. 44 (6), 2076-2089 (2016).
- Chen, S., et al. Interrogating cellular fate decisions with high-throughput arrays of multiplexed cellular communities. Nature Communications. 7, 10309 (2016).
- Shaya, O., et al. Cell-cell contact area affects notch signaling and notch-dependent patterning. Developmental Cell. 40 (5), 505-511 (2017).
- Rao, N., et al. A co-culture device with a tunable stiffness to understand combinatorial cell-cell and cell-matrix interactions. Integrative Biology. 5 (11), 1344 (2013).
- Sriraghavan, V., Desai, R. A., Kwon, Y., Mrksich, M., Chen, C. S. Micropatterned dynamically adhesive substrates for cell migration. Langmuir. 26 (22), 17733-17738 (2010).
- Wong, L., Pegan, J. D., Gabela-Zuniga, B., Khine, M., McCloskey, K. E. Leaf-inspired microcontact printing vascular patterns. Biofabrication. 9 (2), 021001 (2017).
- Chen, T. H., et al. Directing tissue morphogenesis via self-assembly of vascular mesenchymal cells. Biomaterials. 33 (35), 9019-9026 (2012).
- Laurent, J., et al. Convergence of microengineering and cellular self-organization towards functional tissue manufacturing. Nature Biomedical Engineering. 1 (12), 939-956 (2017).
- Lin, C., Khetani, S. R. Micropatterned co-cultures of human hepatocytes and stromal cells for the assessment of drug clearance and drug-drug interactions. Current Protocols in Toxicology. 2017, 1-23 (2017).
- Hui, E. E., Bhatia, S. N. Micromechanical control of cell-cell interactions. Proceedings of the National Academy of Sciences of the United States of America. 104 (14), 5722-5726 (2007).
- D'Arcangelo, E., McGuigan, A. P. Micropatterning strategies to engineer controlled cell and tissue architecture in vitro. BioTechniques. 58 (1), 13-23 (2015).
- Martinez-Rivas, A., González-Quijano, G. K., Proa-Coronado, S., Séverac, C., Dague, E. Methods of micropatterning and manipulation of cells for biomedical applications. Micromachines. 8 (12), (2017).
- Lee, S., et al. Simple lithography-free single cell micropatterning using laser-cut stencils. Journal of Visualized Experiments. (158), e60888 (2020).
- Strale, P. O., et al. Multiprotein printing by light-induced molecular adsorption. Advanced Materials. 28 (10), 2024-2029 (2016).
- Melero, C., et al. Light-induced molecular adsorption of proteins using the primo system for micro-patterning to study cell responses to extracellular matrix proteins. Journal of Visualized Experiments. (152), e60092 (2019).
- Reid, J. A., Mollica, P. M., Bruno, R. D., Sachs, P. C. Consistent and reproducible cultures of large-scale 3D mammary epithelial structures using an accessible bioprinting platform. Breast Cancer Research. , 1-13 (2018).
- Wang, Z., Lee, S. J., Cheng, H. -. J., Yoo, J. J., Atala, A. 3D bioprinted functional and contractile cardiac tissue constructs. Acta Biomaterialia. 70, 48-56 (2018).
- Miri, A. K., et al. Effective bioprinting resolution in tissue model fabrication. Lab on a Chip. 19 (11), 2019-2037 (2019).
- Todhunter, M. E., et al. Programmed synthesis of three-dimensional tissues. Nature Methods. 12 (10), 975-981 (2015).
- Todhunter, M. E., Weber, R. J., Farlow, J., Jee, N. Y., Gartner, Z. J. Fabrication of 3D microtissue arrays by DNA programmed assembly of cells. Current Protocols in Chemical Biology. 8 (3), 147-178 (2016).
- Csizmar, C. M., Petersburg, J. R., Wagner, C. R. Programming cell-cell interactions through non-genetic membrane engineering. Cell Chemical Biology. 25 (8), 931-940 (2018).
- Weber, R. J., Liang, S. I., Selden, N. S., Desai, T. A., Gartner, Z. J. Efficient targeting of fatty-acid modified oligonucleotides to live cell membranes through stepwise assembly. Biomacromolecules. 15 (12), 4621-4626 (2014).
- Hughes, A. J., et al. Engineered tissue folding by mechanical compaction of the mesenchyme. Developmental Cell. 44 (2), 165-178 (2018).
- Weber, R. J., et al. Rapid organoid reconstitution by chemical micromolding. ACS Biomaterials Science & Engineering. 2 (11), 1851-1855 (2016).
- Scheideler, O. J., et al. Recapitulating complex biological signaling environments using a multiplexed, DNA-patterning approach. Science Advances. 6 (12), (2020).
- Viola, J. M., et al. Guiding cell network assembly using shape-morphing hydrogels. Advanced materials (Deerfield Beach, Fla.). , 2002195 (2020).
- Mohammad, A., Davis, M., Aprelev, A., Ferrone, F. A. Note: Professional grade microfluidics fabricated simply. Review of Scientific Instruments. 87 (10), 1-4 (2016).
- Lee, O. J., Chuah, H. S., Umar, R., Chen, S. K., Yusra, A. F. I. Construction of cost effective homebuilt spin coater for coating amylose-amylopectin thin films. Journal of Fundamental and Applied Sciences. 9 (2), 279 (2018).
- Webb, K., Hlady, V., Tresco, P. A. Relative importance of surface wettability and charged functional groups on NIH 3T3 fibroblast attachment, spreading, and cytoskeletal organization. Journal of Biomedical Materials Research. 41 (3), 422-430 (1998).
- Processing Guidelines for: SU-8 2025, SU-8 2035, SU-8 2050, SU-8 2075. Microchem SU-8 2000 Permanent Expoxy Negative Photoresist Available from: https://kayakuam.com/wp-content/uploads/2019/09/SU-82000DataSheet2025thru2075Ver4.pdf (2019)
- Palte, M. J., Raines, R. T. Interaction of nucleic acids with the glycocalyx. Journal of the American Chemical Society. 134 (14), 6218-6223 (2012).
- McGinnis, C. S., et al. MULTI-seq: sample multiplexing for single-cell RNA sequencing using lipid-tagged indices. Nature Methods. 16 (7), 619-626 (2019).
- Maxfield, F. R., van Meer, G. Cholesterol, the central lipid of mammalian cells. Current Opinion in Cell Biology. 22 (4), 422-429 (2010).
- Luo, J., Yang, H., Song, B. L. Mechanisms and regulation of cholesterol homeostasis. Nature Reviews Molecular Cell Biology. 21 (4), 225-245 (2020).
- Liu, L., Tan, L., Yao, J., Yang, L. Long non-coding RNA MALAT1 regulates cholesterol accumulation in ox-LDL-induced macrophages via the microRNA-17-5p/ABCA1 axis. Molecular Medicine Reports. 21 (4), 1761-1770 (2020).
- Mali, P., Aach, J., Lee, J. H., Levner, D., Nip, L., Church, G. M. Barcoding cells using cell-surface programmable DNA-binding domains. Nature Methods. 10 (5), 403-406 (2013).
- Hsiao, S. C., et al. Direct cell surface modification with DNA for the capture of primary cells and the investigation of myotube formation on defined patterns. Langmuir. 25 (12), 6985-6991 (2009).
- Gartner, Z. J., Bertozzi, C. R. Programmed assembly of 3-dimensional microtissues with defined cellular conductivity. Proceedings of the National Academy of Sciences. (17), 1-5 (2009).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved