Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Bioengineering
Enkel, prisvärd och modulär mönstra av celler med HJÄLP AV DNA
Här presenterar vi ett protokoll till mikromönsterceller vid encellsupplösning med hjälp av DNA-programmerad vidhäftning. Detta protokoll använder en bänkfotografiplattform för att skapa mönster av DNA-oligonukleotider på en glasrutschbana och märker sedan cellmembran med kommersiellt tillgängliga kompletterande oligonukleotider. Hybridisering av oligos resulterar i programmerad cell vidhäftning.
Den relativa placeringen av celler är en viktig egenskap hos mikromiljön som organiserar cell-cellinteraktioner. För att studera interaktionerna mellan celler av samma eller annan typ har mikropapperstekniker visat sig vara användbara. DNA-programmerad cellsammansättning (DPAC) är en mikropatterningsteknik som riktar in sig på vidhäftning av celler till ett substrat eller andra celler som använder DNA-hybridisering. De mest grundläggande operationerna i DPAC börjar med att dekorera cellmembran med lipidmodifierade oligonukleotider och sedan flöda dem över ett substrat som har mönstrats med kompletterande DNA-sekvenser. Celler fäster selektivt vid substratet endast där de hittar en kompletterande DNA-sekvens. Icke-vidhäftande celler tvättas bort, vilket avslöjar ett mönster av vidhäftande celler. Ytterligare operationer inkluderar ytterligare omgångar av cellsubstrat eller cellcells vidhäftning, samt överföring av de mönster som DPAC bildat till en inbäddad hydrogel för långsiktig kultur. Tidigare krävde metoder för att mönstra oligonukleotider på ytor och dekorera celler med DNA-sekvenser specialiserad utrustning respektive anpassad DNA-syntes. Vi rapporterar en uppdaterad version av protokollet, med hjälp av en billig benchtop fotolitografi setup och kommersiellt tillgängliga kolesterol modifierade oligonukleotider (CMOs) distribueras med ett modulärt format. CMO-märkta celler håller fast vid DNA-mönstrade substrat med hög effektivitet. Den här metoden kan användas för att mönstra flera celltyper samtidigt med hög precision och för att skapa matriser med mikrotissuer inbäddade i en extracellulär matris. Fördelarna med denna metod inkluderar dess höga upplösning, förmåga att bädda in celler i en tredimensionell mikromiljö utan att störa mikropattern och flexibilitet i att mönstra någon celltyp.
Placeringen av celler med avseende på varandra i en vävnad är en viktig egenskap hos mikromiljön1,2,3,4. Tekniker som används för att mönstra levande celler till rumsligt kontrollerade arrangemang är värdefulla experimentella verktyg för att studera differentiering4,5,6,7,8, cellmotilitet9,morfogenes10,11,12, metabolism13och cellcellsinteraktioner7,14 . Det finns en mängd olika metoder för mönstra celler, var och en med sina egna fördelar och nackdelar3,4. Metoder som skapar självhäftande öar av excellulära matrisproteiner (ECM), såsom mikrokontakttryck och laserskurna stenciler, är enkla och skalbara. Det är dock svårt att mönstra mer än en eller två celltyper åt gången eftersom de självhäftande egenskaperna hos olika celltyper till olika ECM-molekyler ofta är liknande15,16,17. Mer komplexa mikromönster kan skapas med ljusinducerad molekylär adsorption (LIMAP), en teknik som använder UV-ljus för att ablatera PEG-belagda regioner och möjliggöra efterföljande proteinadsorption18,19. Den här processen kan upprepas för att skapa högupplösta mikromönster med flera celltyper. Korsbindning av celler till de olika proteinplåstren kan dock uppstå, vilket resulterar i dålig mönster specificitet19. Fysiska metoder som sådd av celler på mikromekaniska omkonfigurerbara odlingsenheter kan skapa strukturerade samkulturer med dynamisk kontroll, men utan flexibilitet i mönsterdesignen av mikrokontakttryck eller LIMAP14,8. Till skillnad från de andra teknikerna kan bioprinting skapa tredimensionella arrangemang av celler inom hydrogeler20,21. Bioprintade konstruktioner har dock mycket lägre upplösning än andra mikropapperstekniker, med en genomsnittlig funktionsstorlek i storlek på hundratals mikron22. En idealisk cellmönstermetod skulle ha hög upplösning, mönster flera celltyper, använda utrustning och reagenser som är lättillgängliga och har förmågan att bädda in framgångsrika mönster i en hydrogel för tredimensionell (3D) cellkultur. I den här artikeln presenterar vi CMO-DPAC, en cell micropatterning teknik som använder flexibiliteten och hastigheten av DNA hybridisering för att rikta cell vidhäftning till ett substrat. Denna metod har anpassats från våra tidigare protokoll23,24 för att göra den mer prisvärd, modulär och tillgänglig. Med hjälp av det aktuella protokollet bör alla labb kunna installera ett fullt fungerande system utan någon specialiserad utrustning eller expertis.
DNA-programmerad cellsammansättning (DPAC) är en kraftfull vävnadsteknik som mönster celler vid encellsupplösning med exakt kontroll över cellcellsavstånd och vävnadsgeometri. I DPAC är cellmembran dekorerade med DNA-oligonukleotider (oligos) med hjälp av två lipidmodifierade oligos utformade för att hybridisera på cellmembranet. Eftersom oligos är konjugerade till hydrofoba lipider, delar de snabbt till cellmembranet25 där de hybridiserar, vilket ökar nettohydrofobin hos de icke-kovalent bundna molekylerna och därmed förbättrar deras livslängd vid cellytan26. Oligos presenteras på cellytan på ett sätt där de kan hybridisera med kompletterande oligos på andra celler eller DNA-funktionaliserade glasglasbilder för att skapa definierade 2D- eller 3D-cellmönster med föreskriven sammansättning, cellcellsavstånd och geometri23,24. De mönstrade mikrotissuerna kan klyvas av ytan enzymatiskt och bäddas in i en hydrogel för långvarig 3D-kultur. När de används i kombination med primärceller eller stamceller kan de resulterande samlingarna av celler genomgå morfogenes och bildas till organoider23,27,28. DPAC har tillämpats för att undersöka dynamiken i vuxna neurala stamcells öde som svar på konkurrerande signaler6,29, för att studera självorganisering av bröst epitelceller23,28, och för att generera "vävnad origami" genom mesenkymal kondensation27.
DPAC möjliggör exakt placering av flera cellpopulationer och har betydligt bättre upplösning än extruderingsbaserade bioprinters (i storleksordningen mikron)22,23. Till skillnad från ECM-baserade mönskningsmetoder som mikrokontaktutskrift kräver DPAC dessutom inte differentiell vidhäftning av de olika celltyperna till en ECM-belagd yta15,23. Det är idealiskt för att svara på frågor om hur sammansättningen av en vävnad påverkar dess beteende, hur celler integrerar flera cellulära och mikromiljösignaler när man fattar beslut6,29, och hur par av celler interagerar med varandra. En fördel med denna metod jämfört med andra mikropappersmetoder är att den kan användas för 3D-cellkultur i ett enda bildplan, vilket underlättar tidsfördröjningsstudier av vävnadens självorganisering och organoidmorfogenes23,27,30.
Trots dessa fördelar har framgångsrik implementering av DPAC krävt syntes av anpassade oligonukleotidreagenser och tillgång till specialiserad utrustning för DNA-mönstraring23,24, vilket begränsar utbredd användning. Till exempel måste de optimala lipidmodifierade oligos (LMOs) som används i det ursprungliga protokollet anpassas, modifieras med lignocersyra eller palmitsyra och renas26. Denna process kräver användning av en DNA-synthesizer och ett högpresterande vätskekromatografiinstrument, liksom inköp av tillhörande reagenser som metylamin, ett kontrollerat ämne som omfattas av både institutionella och federala bestämmelser. Som ett alternativ kan LMOs skräddarsys i bulk, men detta kräver en betydande investering i tekniken.
För att övervinna dessa begränsningar har vi utvecklat en reviderad version av DPAC som använder kommersiellt tillgängliga kolesterolmodifierade oligos (CMOs) i stället för de anpassade syntetiserade LMOs. För att ytterligare minska kostnaderna och öka flexibiliteten i plattformen har vi bytt till ett modulärt tre-oligosystem. Istället för att beställa en ny kolesterolmodifierad oligo för varje unik cellpopulation kan en användare av detta protokoll istället använda samma kolesterolmodifierade oligos ("Universal Anchor" och "Universal Co-Anchor") för varje cellpopulation och sedan använda en billig, oförändrad oligo ("Adapter Strand") som hybridiseras med både universalankaret och antingen det aminfunktionaliserade DNA:t på ytan eller adaptersträngen av en annan celltyp.
En annan begränsning av det ursprungliga DPAC-protokollet var att det skapade de DNA-mönstrade bilderna med hjälp av en högupplöst vätskeskrivare (t.ex. Nano eNabler, BioForce Nanosciences)23,24. Även om detta instrument har extraordinär upplösning och låga reagenskrav, är det inte tillgängligt för de flesta institutioner och har en relativt låg utskriftsfrekvens (ungefär 1 funktion mönstrad per sekund). Nyligen har två fotolitografiska metoder utvecklats för att mönster DNA-funktioner på ytor. Viola och kollegor använde en polyakrylamid- och bensofenonbeläggning som kovalent bundna enkelsträngade DNA-oligos vid exponering för UV-ljus30. Med denna metod kunde de skapa vävnadsställningar som genomgick storskaliga, programmerade formförändringar som ett resultat av cellkontraktilitet och självorganisering. utvecklade en metod som använder UV-exponering av en positiv fotoresist för att selektivt exponera aminmodifierade DNA-oligos för en aldehydfunktionaliserad bild29. Efter bakning och reduktiv amination binds det aminmodifierade DNA:t kovalent till ytan. Denna metod användes för att undersöka svaret från vuxna neurala stamceller på rumsligt presenterade självförnyelse och differentiering ledtrådar. Denna artikel anpassar Scheideler et al.s protokoll för att skapa DNA-mönster som kommer att fånga CMO-märkta celler. Detta fotopappersprotokoll kan utföras utan att använda ett rent rum. Den använder billig och kommersiellt tillgänglig utrustning som enkelt kan placeras på en bänkskiva eller rökhuv. Användningen av billig eller DIY (gör-det-själv) fotolitografiutrustning ökar tillgängligheten till forskare utan tillgång till rena rumsanläggningar och gör det möjligt för forskare att prova tekniken utan en stor investering av tid eller resurser31,32. Bättre upplösning och justering av flera DNA-funktioner kan dock uppnås genom att använda den kommersiella spinnbelagten och maskjusteraren som vanligtvis finns i renrumsanläggningar.
Här beskriver vi en metod för att mönstra celler vid encellsupplösning med hjälp av DNA-baserad vidhäftning. För det första används fotopatterning med en positiv fotoresist för att skapa högupplösta mönster av aminmodifierat DNA på ett aldehydmodifierat glassubstrat. Därefter behandlas bilden för att minska icke-specifika cellbilaga och PDMS-flödesceller skapas för att begränsa celler över mönstrade områden. Cellerna märks sedan med korta DNA-oligonukleotider som funktionaliseras med kolesterol och därmed sätts in i cellmembranet. Cellerna flödas sedan över DNA-mikromönster. Hybridisering mellan cell-ytan DNA och DNA på glasytan resulterar i specifik vidhäftning av cellerna till DNA-mönstret. Icke-vidhäftande celler tvättas bort, vilket avslöjar det vidhäftande cellmönstret. Den här processen kan upprepas för att mönster flera celltyper eller för att skapa strukturer med flera lager. Om så önskas kan cellerna bäddas in helt i en ECM för 3D-cellkultur.
1. Designexperiment
- Planera önskat experiment med hänsyn till funktions storlek, funktions avstånd, antal celltyper som är inblandade och arrangemang av celler med avseende på varandra. Se Kompletterande fil 1, en guide för experimentell design, och Kompletterande fil 2, som innehåller exempel oligosekvenser.
- Designa fotomask med hjälp av datorstödd designprogramvara. Ett exempel fotomask finns i Kompletterande fil 3.
- Rita en rektangel av måtten på en standardmikroskopbild (25 mm x 75 mm).
- Rita fyra rektangulära områden som är 10 mm breda och 10 mm långa, jämnt fördelade över rutschkanan.
- I varje region ritar du funktioner som är önskad storlek, form och avstånd för experimentet. Cellerna följer bara dessa funktioner i experimentet.
- Om du vill skapa justerade fotomasker för flera celltyper skapar du en huvudritning med alla uppsättningar funktioner och sparar sedan versioner som motsvarar varje celltyp.
- Beställ en högupplöst (minst 20 000 prickar per tum) genomskinlighetsfotomask från denna CAD-ritning med funktionerna ritade i 1.2.3 transparent och de större regionerna svarta.
2. Fotopattern-DNA på aldehydfunktionaliserade diabilder (protokoll anpassat från Scheideler et al.29 )
- Om du mönstrar flera celltyper, tillverka fiducial markörer på den aldehydfunktionaliserade bilden före någon DNA-mönstra för att underlätta justering av funktioner. Alternativa metoder för att skapa fiducial markörer föreslås i kompletterande fil 1.
- För att skapa metallfiducial markörer, applicera S1813 positiv fotoresist enligt beskrivningen i steg 2.3 - 2.11. Använd en fotomask som innehåller stora funktioner som är lätta att justera senare. Införliva dessa funktioner i utformningen av fotomaskerna som kommer att användas för DNA-mönstraring.
- Sätt in en tunn film (100 Angstroms) titan på rutschkanan med hjälp av elektronkanonavdunstning29. Ta bort överflödig metall och fotoresist med aceton och fortsätt sedan till DNA-fotopapperningen.
- Förbered en 20 μM-lösning av en 5'-aminmodifierad oligo i DNA-buffert (50 mM natriumfosfat i vatten, pH = 8,5). Se Kompletterande fil 2 för föreslagna oligosekvenser.
OBS: Det är möjligt att använda så lite som 5 μM aminmodifierad oligo för vissa mönster och tillämpningar, så ytans DNA-koncentration kan behöva optimeras. - Förvärm en värmeplatta till 100 °C.
- Använd dubbelsidig tejp eller ett vakuum för att fästa en aldehydfunktionaliserad glasrutschbana på rotorn på en spinnbelagt.
VARNING: Glidavlossning under spinnbeläggning är en säkerhetsrisk. Använd alltid spinnkatainern i en sluten behållare med lock, t.ex. en akryllåda.
OBS: Märk ett hörn av bilden med hjälp av en diamantskrivare eller liknande redskap för att repa glaset. Detta hjälper till med bildidentifiering och orientering efter att fotoresisten har tvättats bort. - Använd en engångspipeett för att släppa den positiva fotoresisten på aldehydrutschbanan. För jämna beläggningar, tillsätt små droppar av fotoresisten över bilden, istället för en stor droppe i mitten (Kompletterande figur 1A).
- Snurra glidet vid 3000 varv/min med hjälp av spinnbelagten i 30 s.
- Placera bilden på 100 °C kokplatta i 1,5 min (mjukbakning) för att korsa länkfotoresisten.
- Ta bort bilden från värmeplattan. Placera en fotomask med de funktioner som önskas för detta experiment ovanpå bilden och väg fotomasken ner med en glasbit(Kompletterande figur 1B, C). Täck hela installationen i en ogenomskinlig ruta(kompletterande figur 1D). Exponera med en UV-lampa (365 nm våglängd, 360 mW, 5 tum från rutschkanan, total strålande energitäthet 100 mJ/cm2) i 2 min.
OBS: UV-ljus kommer att bryta polymerbindningarna i fotoresisten under genomskinliga områden av fotomasken, vilket skapar regioner där DNA senare kommer att kunna klibba. - Utveckla bilden genom att fördjupa i utvecklarlösningen i 3-5 min (Kompletterande figur 1E).
- Skölj bort överflödig utvecklarlösning med vatten. Torka under en ström av luft eller kväve. (Kompletterande figur 1F).
- Bekräfta att fotolitografin lyckades genom att titta på bilden under mikroskopet. Eftersom fotoresisten är UV-ljuskänslig gör du det här steget snabbt och lagrar sedan bilden i mörker medan du förbereder andra bilder (om tillämpligt).
OBS: En väl mönstrad bild ska ha skarpt definierade kanter för varje funktion, ingen sprickbildning och ingen funktionsförvrängning i kanterna. Exempel på korrekt och felaktig fotolitografi finns i kompletterande figur 2A. Se tabell 1 för felsökningsförslag om fotolitografi inte ger önskad funktionskvalitet. - Tillsätt en droppe av den 20 μM amaminmodifierade oligolösningen (steg 2.1) på varje fotomönsterregion i bilden. Använd en pipettspets för att försiktigt sprida droppen över hela regionen, var försiktig så att du inte kliar på bilden. (Kompletterande figur 1G).
- Grädda rutschkanan i en ugn på 65-70 °C tills DNA-lösningen har torkat helt på glidytan (ca 1 h).
- Utför reduktiv amination genom att placera de mönstrade, bakade rutschbanorna i en 15 cm cellkulturrätt och placera i en rökhuva ovanpå en shaker. Väg 100 mg natriumborohydrid. Tillsätt 40 ml fosfatbuffrad saltlösning (PBS) i en rökhuv, blanda försiktigt och lägg till skålen som innehåller de mönstrade bilderna. Låt reaktionen fortsätta i 15 minuter med mild skakning.
OBS: Amin på oligo bildar först en Schiff-bas med aldehyderna på glidytan. Detta är en reversibel kovalent obligation som måste omvandlas till en oåterkallelig obligation innan den används i DPAC. Tillsats av ett reducerande medel (natriumborohydrid) omvandlar Schiffbasen till en sekundär amin genom reduktiv amination.
VARNING: Reaktionen av natriumborohydrid med vatten skapar vätgas och kommer att fortsätta att göra det i timmar eller dagar efter att reaktionen börjar. Utför det reduktiva aminationssteget i en rökhuv och förvara allt natriumborohydridlösningsavfall i en öppen eller löst täckt behållare i rökhuven i minst 24 timmar. - Ta bort oreagerat DNA genom att tvätta två gånger med 0,1% natriumdydecylsulfat (SDS) i vatten och sedan tre gånger med destillerat vatten. Torka rutschkanan under en ström av kväve eller luft.
- Skölj bilden med aceton för att ta bort den återstående fotoresisten.
OBS: Vid denna tidpunkt har DNA:t irreversibelt och kovalent fästs vid bilden och alla oreagerade aldehydfunktionella grupper har omvandlats till alkoholer. Fotoresisten behövs inte längre. - Om flera oligos kommer att mönstras återgår du till steg 2.4, justerar fotomasken med fiduciala märken och upprepar.
OBS: Experimentet kan pausas här. Förvara rutschkanorna i en vakuumdesiccator. Under torra förhållanden kan bilderna förvaras i upp till 3 månader utan kvalitetsförlust.
3. Gör glidhydrofobisk (tillval) (protokoll anpassat från Todhunter et al.24 )
OBS: Det är fördelaktigt, men inte nödvändigt, att ändra bildens ytkemi för att göra den mer inert och hydrofobisk. Icke-specifik celltillbehör reduceras på dessa ytor33, vilket minskar icke-specifik bindning av celler till omönstrade områden i bilden. Dessutom, om de mönstrade cellerna i slutändan kommer att bäddas in i en hydrogel och överföras från bilden, är ytbehandlingen avgörande för tillförlitlig rörelse av den cellbelastade hydrogelen över glidbanan utan förvrängning eller rivning. Silanisering med (tridecafluoro-1,1,2,2-tetrahydrooctyl) dimetylklorosilan resulterar i förekomst av hydrofoba fluoroalkylgrupper på glidytan.
VARNING: Utför alla steg från 3.1 och framåt i en kemisk rökhuv för att förhindra exponering för ättiksyra och metylenkloridångor.
- Skölj bilden med 10% ättiksyra och torka sedan under en luftström.
- I en coplinburk i glas bereder du en lösning på 60 ml metylenklorid (diklormetan), 0,6 ml trietylamin och 0,6 ml (tridekafluor-1,1,2,2-tetrahydroktyl) dimetylklosilan. Rör om med en metallspatel för att blanda.
OBS: Dessa reagenser är känsliga för vatten. De bör förvaras under torra förhållanden och användas så färska som möjligt. - Lägg i bilden i Coplin-burken som innehåller silanlösningen. Placera Coplin-burken på en orbital shaker (inställd på 60-80 rpm) och låt silanens och glidets reaktion utvecklas i 15 minuter.
- Använd metalltång för att ta bort glidningen från silanlösningen. Sänk ned glid i en Coplin-burk som innehåller metylenklorid i 1 minut för att avlägsna överflödig silan från diabilden.
- Sänk ned rutschkanan i ett koniskt rör på 50 ml som innehåller etanol. Agitera. Sänk ned rutschkanan i ett koniskt rör på 50 ml som innehåller destillerat vatten. Agitera.
OBS: Metylenklorid och vatten är inte lätt att ta bort, så en etanolsköljning behövs för att avlägsna överskott av metylenklorid före den slutliga vattensköljningen. - Ta bort glidbanan från vattnet och inspektera den. Rutschkanan ska vara ganska torr, med alla vattendroppar som har en kontaktvinkel på mer än 90°. Låt bilderna torka helt och förvaras i vakuumavsickare tills de används.
OBS: Experimentet kan pausas här. Förvara rutschkanan under torra förhållanden.
4. Förbered PDMS-flödesceller och skjut för experiment
OBS: Rektangulära PDMS-flödesceller används för att koncentrera cellerna över de mönstrade områdena i bilden. För experiment odlade i 3D bildar flödescellerna en form för hydrogelen.
- Gör SU-8-hanterare att använda som mögel för PDMS-flödesceller.
- Förvärm hotplate till 95 °C.
- Tillsätt 5 ml SU-8 2075 i en kiselskiva.
- Snurra täck SU-8 på skivan vid 500 varv/min i 10s, följt av 1 000 varv/min i 30-talet. Detta bör skapa funktioner upp till 240 μm i höjd34.
- Mjukbaka skivan på kokplattan i minst 45 minuter.
- Ta bort skivan från kokplattan. Lägg fotomasken (se Kompletterande fil 4) (emulsionssidan nedåt) ovanpå skivan och väg ner den med en glasskiva för att säkerställa kontakt mellan fotomasken och bilden.
- Exponera med UV-ljus (365 nm) för en strålande energitäthet på 350 mJ/cm2.
- Grädda wafer på kokplattan i 12-15 min.
- Placera wafer i bred glasbehållare. Täck wafer med SU-8 utvecklarlösning. Placera på en shaker och utvecklas medan du agiterar i minst 15 min.
- Använd tång för att ta bort wafer från utvecklarlösningen. Skölj i 5 s genom att spruta mer utvecklarlösning från en sprutflaska. Spraya med isopropylalkohol för att skölja. Om en vit fällning visas, returnera wafer till utvecklarlösningen och utveckla längre.
- Torka wafer under en ström av luft eller kväve.
- Grädda rutschkanan i 5 min.
OBS: När huvudskivan har skapats kan den återanvändas på obestämd tid så länge funktionerna förblir intakta.
- Förbered PDMS.
- I en vägbåt, tillsätt polydimethylsiloxanelastomer och tvärlänk i ett 10:1-förhållande (efter massa). Rör om kraftigt för att säkerställa jämn blandning.
- Avgasa PDMS i en vakuumavsickering i 15-30 minuter tills inga fler bubblor är synliga.
- Placera masterskivan i en 15 cm vävnadskulturrätt. Häll PDMS över skivan. Om bubblor uppträder, avgasa i en vakuumavsickering i några minuter.
- Grädda i 60 °C ugn i 3 h.
OBS: Efter bakning kan PDMS flödesceller förvaras på bänkskivan på obestämd tid.
- Förbered PDMS-flödesceller för experimentet.
- Strax innan du startar ett CMO-DPAC-experiment ska du klippa ut det önskade antalet PDMS-flödesceller från huvudskivan. Plasma oxiderar med 10 cc/min rumsluft i 90 s för att göra ytan hydrofil.
- Klipp ut varje enskild flödescell så att det finns 1-2 mm PDMS kvar på varje sida och skär sedan upp toppen och botten av flödescellen för att skapa ett inlopp och utlopp.
- Hämta mönstrad bild som skapats i steg 2 och 3. Justera ovanpå fotomasken.
- Använd fotomasken som referens och placera PDMS-flödescellerna på bilden på platsen för varje mönstrad region.
- Tillsätt 50 μL fosfatbuffrad saltlösning (PBS) + 1% bovint serumalbumin (BSA) till inloppet i varje flödescell, enligt kompletterande figur 1H. Bekräfta att flödescellen är helt fylld av PBS + 1% BSA och att det inte finns några stora bubblor. Fortsätt omedelbart till steg 5 och 6.
OBS: Blockering med BSA minimerar icke-specifik cell vidhäftning till glidytan.
5. Lyft och märka celler med kolesterolmodifierat DNA
- Förbered de kolesterolmodifierade DNA-lösningarna.
- För varje uppsättning celler i försöket, blanda ihop 3 μL av en 100 μM lagerlösning av den kolesterolmodifierade universalankarsträngen med 3 μL av en 100 μM lagerlösning av en adaptersträng. Inkubera i 1 minut. Detta kommer att förhybrifiera oligos. Tillsätt 69 μL fosfatbuffrad saltlösning (PBS) för att skapa en 4 μM Universal Anchor + Adapter-lösning.
- För varje uppsättning celler i experimentet tillsätt 3 μL av en 100 μM Universell kolesterolmodifierad Co-Anchor Strand-stamlösning till 12 μL PBS, vilket skapar en 20 μM-lösning.
- Förbered encellsupphängningen/encellsupphängarna.
- För vidhäftande celler, använd trypsin eller annat dissociationsmedel för att avlägsna cellerna från odlingskolven. Tillsätt odlingsmedier för att neutralisera trypsin och centrifug för att pelletera cellerna. För icke-vidhäftande celler, samla cellupphängningen och centrifugera för att pelletera cellerna.
- Återsuspend cellpelleten i 1 ml iskall PBS eller serumfritt medium. Överför 1-3 miljoner celler till ett 1,5 ml mikrocentrifugerör. Centrifug vid 160 x g i 4 min.
OBS: Om den celltyp som används är benägen att klumpa ihop sig/aggregeras, använd PBS utan kalcium- och magnesiumjoner för alla tvättsteg för att minska oönskad cellaggregering. Om lönsamheten är ett särskilt problem för den celltyp som används, använd serumfria medier i stället för PBS. Media som innehåller fetala nötkreatur serum rekommenderas inte för cellmärkning eftersom det kan hindra införlivande av lipidmodifierade oligos. 35 År
- Märk cellerna med kolesterolmodifierade oligos.
- Återsuspendera cellpelleten i 75 μL iskall PBS eller serumfria medier. Håll cellerna i en ishink under hela märknings- och tvättprocessen för att maximera cellens livskraft och minimera förlusten av de kolesterolmodifierade oligos från cellytan.
OBS: Återupplivning av cellerna innan du lägger till DNA säkerställer att fördelningen av DNA är enhetlig över cellpopulationen. - Tillsätt 75 μL av 4 μM Universal Anchor + Adapter-lösningen som skapades i steg 5.1.1 till mikrocentrifugeröret som innehåller cellupphängningen. Blanda noggrant genom pipettering. Inkubera i 5 min på is.
- Tillsätt 15 μL av universalankarlösningen till mikrocentrifugeröret. Blanda noggrant genom pipettering. Inkubera i 5 min på is.
- Ta bort överflödiga oligos från cellupphängningen. Tillsätt 1 ml iskall PBS eller serumfritt medium till mikrocentrifugeröret. Blanda med en P1000 pipett. Centrifug vid 160 x g i 4 min vid 4 °C. Kasta supernatanten. Upprepa två gånger till.
OBS: Om cellerna är benägna att klumpa ihop sig, passera cellupphängningen genom ett 40 μm-filter före den slutliga tvätten. Om cellerna är benägna att adsorption på sidan av mikrocentrifugeröret, överväg att förblockera röret med kasein.
- Återsuspendera cellpelleten i 75 μL iskall PBS eller serumfria medier. Håll cellerna i en ishink under hela märknings- och tvättprocessen för att maximera cellens livskraft och minimera förlusten av de kolesterolmodifierade oligos från cellytan.
6. Mönstra de DNA-märkta cellerna
- Återanvänd cellerna i iskalla PBS eller serumfria medier för att skapa en celltäta lösning på minst 25 miljoner celler/ml.
OBS: För en bild med fyra av de 10 mm x 15 mm x 200 μm PDMS-flödesceller som beskrivs i steg 4 krävs cirka 100 μL av denna täta cellfjädring. Även om de flesta av dessa celler inte kommer att hålla sig till mönstret och i slutändan kommer att kasseras, förbättrar en extremt koncentrerad lösning av celler över mönstret dramatiskt effektiviteten hos cellmönster. - Ta upp rutschkanan och luta den något. Tillsätt 25 μL cellfjädring till inloppet i varje flödescell på den mönstrade bilden. Ta bort PBS + 1% BSA-lösningen från uttaget, så att cellupphängningen kan fylla PDMS-flödescellen. Inkubera på is eller vid rumstemperatur i 30 s.
OBS: Vid denna tidpunkt bör titta på flödescellen under ett mikroskop visa tätt packade celler med små eller inga luckor synliga mellan celler. Se kompletterande figur 2B. - Aspirera 5 μL cellfjädring från utloppet på bilden och lägg tillbaka den i inloppet. Upprepa 10 gånger per flödescell.
OBS: Vidhäftningen av CMO-märkta celler till den DNA-mönstrade bilden är nästan omedelbar. Att flöda cellerna över mönstret flera gånger ökar sannolikheten för att en cell kommer att flöda över en given DNA-fläck och fångas. - Pipetten PBS eller serumfria medier försiktigt in i inloppet i varje flödescell för att tvätta ut överflödiga celler. Samla cellfjädringen från uttaget. Upprepa 2-4 gånger eller tills en visuell inspektion av bilden under mikroskopet bekräftar att det inte finns några överflödiga celler kvar.
OBS: Det kan vara fördelaktigt att spara överskottscellerna från den första tvätten. Om mönskningseffektiviteten är otillfredsställande kan överskottscellerna centrifugeras och återanvändas i en lägre volym PBS för att skapa en mer celltäta lösning, och sedan kan processen upprepas från steg 6.2. - Upprepa steg 6.1-6.4 för varje uppsättning celler i mönstret. För mönster där flera celltyper är direkt mönstrade av ytmallen börjar du med den minst rikliga celltypen av mönstret och avslutar med den mest rikliga celltypen.
OBS: Det är lämpligt att göra varje omgång cellulär montering sekventiellt istället för att slå samman cellerna, även under förhållanden där cellerna alla är märkta med ortogonala DNA-sekvenser. Poolning av cellerna späder effektivt varje cellpopulation och minskar mönstraringseffektiviteten. - När den sista cell sammansättnings omgången är klar varierar nästa steg beroende på det specifika experimentet. Om cellerna är avsedda att finnas kvar på glaset lägger du till media i en Petri-skål som innehåller bilden och använder sedan försiktigt tång för att knuffa bort PDMS-flödescellerna från bilden. Om cellerna kommer att bäddas in i en hydrogel och odlas i 3D, fortsätt till steg 7.
7. Överför till hydrogel för 3D-kultur (valfritt)
- Förbered en hydrogelprekursorlösning som innehåller 2% DNase.
OBS: Lösningens sammansättning varierar beroende på experimentell installation. Matrigel och blandningar av Matrigel och kollagen jag fungerar bra i detta protokoll, men andra hydrogeler är också möjliga. - Tillsätt 50 μL hydrogellösning som innehåller 2% DNase till inloppet i varje flödescell. Aspirera överskottsvätskan från utloppet och kör hydrogellösningen in i flödescellen. För trögflytande hydrogelprekursorer kan det krävas att bilden lutas något för att hjälpa hydrogelen att flöda in i flödescellen.
- Inkubera glidningen vid 37 °C i 30-45 min (beroende på hydrogelgelgelingkinetik) så att hydrogelen kan ställas in och klyva den DNA-baserade vidhäftningen mellan cellerna och ytan.
- Ta bort varje flödescell från bilden och placera ovanpå hydrogelprekursorlösningen.
- Tillsätt 50 μL hydrogelprekursor till en brunn i en 2-väl kammarrutschbana eller en 6-välplatta.
- Pipett 10 μL PBS på vardera sidan av varje flödescell.
- Använd ett rakblad eller finpunkts pincett för att fördela PBS längs hela flödescellens längd och lyft sedan försiktigt sidorna av flödescellen så att PBS rusar under hydrogelen.
OBS: Detta kommer att "flyta" hydrogelen över bilden, vilket möjliggör överföring utan förvrängning eller rivning. - Använd ett rakblad för att försiktigt flytta flödescellen till glasglasets kant.
- Invertera bilden. Med rakbladet knuffar du bort flödescellen från rutschkanan så att den landar ovanpå rakbladet.
- Plocka bort flödescellen från rakbladet med böjda tångar. Invertera flödescellen så att cellerna är på botten och placera sedan ovanpå droppen av hydrogelprekursorlösning.
- Upprepa steg 7.4.1 - 7.4.6 för varje flödescell.
- Inkubera i minst 30 minuter så att hydrogelen som innehåller de mönstrade cellerna kan binda till hydrogelunderlägget, vilket resulterar i fullständig inbäddning av de mönstrade cellerna.
- Ta bort PDMS-flödescellen.
- Lägg till tillräckligt med media för att fördjupa PDMS-flödescellen.
Obs: Tillströmningen av media kommer att lossa vidhäftningen mellan hydrogelen och PDMS-flödescellen. - Använd böjda tångar, orienterade längs flödescellens långa axel, för att försiktigt knuffa flödescellen tills den poppar av och flyter in i mediet. Samla flödescellen med tång och kassera.
OBS: För optimalt resultat, sprid de böjda tångarna och applicera försiktigt tryck på väggarna i PDMS-flödescellen. Applicera kraft i flödescellens långa axel.
- Lägg till tillräckligt med media för att fördjupa PDMS-flödescellen.
8. Bekräfta lyckad märkning av celler med CMO (valfritt, för felsökning)
- Beställ en fluorescerande modifierad (FAM eller AF647) oligonukleotid som kompletterar yt vidhäftningssekvensen hos adaptersträngen som används i experimentet.
- Märk celler med CMO DNA och tvätta bort överflödigt DNA enligt beskrivningen i steg 5. Resuspend i 200 μL iskall PBS.
- Gör en 4 μM-lösning av den fluorescerande märkta kompletterande oligonukleotid i PBS. Tillsätt 200 μL av denna lösning till cellfjädringen. Inkubera på is i 5 min.
- Tillsätt 1 ml iskall PBS. Centrifugera cellerna för att pelletera dem. Ta bort supernatant. Upprepa denna process ytterligare två gånger för att tvätta bort dna som inte har hybridiserats.
- Utför analytisk flödescytometri för att kvantifiera närvaron av DNA på cellytan.
- Analysera kontrollceller som inte har märkts med DNA på en flödescytometer. Sätt upp grindar baserat på denna befolkning.
- Analysera CMO-märkta celler som har behandlats med en fluorescerande märkt kompletterande oligonukleotid.
- Beräkna genomsnittlig fluorescensintensitet.
Detta protokoll gör det möjligt att mönstra celler i 2D och 3D med hög precision och utan användning av anpassade reagenser eller dyr renrumsutrustning. Bild 1 visar en översikt över protokollet. För det första skapas DNA-funktionaliserade bilder genom fotolitografi. Därefter är cellerna märkta med cmos. Cellerna flödas sedan över bilden, där de endast fäster vid de DNA-funktionaliserade områdena i bilden. Efter att överflödiga celler tvättats bort avslöjas önskat mönster av celler. Dessa celler kan odlas på bilden eller bäddas in i en hydrogel som innehåller DNase och överföras från bilden för 3D-cellkultur.
Märkning av celler med cmos gör det möjligt att fästa dem i den DNA-mönstrade bilden (figur 2). Först är den kolesterolmodifierade Universal Anchor Strand förhybridiserad med adaptersträngen. Därefter blandas universalankar- + adapterlösningen 1:1 med cellupphängningen. Kolesterolet på universalankar- + adapterkomplexet skärs in i cellmembranet. Tillägg av den kolesterolmodifierade Universal Co-Anchor Strand, som hybridiserar med Universal Anchor Strand, förbättrar stabiliteten hos CMO-komplexet i cellmembranet genom att öka nettohydrofobin hos komplexet26. Efter att ha tvättat ut överskottet av DNA från cellupphängningen flödas cellerna över bilden. Hybridisering mellan adaptersträngen och Surface DNA-strängen resulterar i att celler fästs i de DNA-mönstrade områdena i bilden.
Cellernas mönster skapas med hjälp av fotolitografi för att begränsa fastsättningen av aminmodifierade DNA-oligos till specifika regioner i en aldehydmodifierad glasbild29 (figur 3A). Positiv fotoresist är spin-coated på en aldehydfunktionaliserad bild. En genomskinlig fotomask placeras sedan ovanpå bilden och bilden utsätts för UV-ljus. Efter att ha utvecklats är de regioner i bilden som utsattes för UV-ljus inte längre belagda med fotoresist och har därmed exponerade aldehydgrupper. En 20 μM-lösning av aminmodifierade DNA-oligos släpps sedan på bilden och sprids för att täcka de mönstrade regionerna. Bakning följt av reduktiv amination resulterar i ett kovalent band mellan det aminmodifierade DNA och bilden. Anmärkningsvärt nog kan denna process upprepas för att mönster flera oligos utan någon förlust av funktionaliteten hos de tidigare mönstrade oligos (figur 3B). Man bör dock vara försiktig så att överlappande mönster undviks, vilket resulterar i att båda oligos finns i en minskad koncentration (kompletterande figur 3). Flera cellpopulationer kan mönstras sekventiellt med hjälp av adaptersträngar som skiljer sig åt i deras modulära domän (de 20 baserna närmast 3'-änden).
Även om detta fotopatterning protokoll utvecklades av Scheideler et al. i samband med ett rent rum, har vi visat att det är möjligt att uppnå liknande resultat med en billig, "hembryggd" fotolitografiinställning som passar lätt i en kemisk rökhuv. Installationen innehåller en spin coater för $ 400 tillverkad av en DC-motor, digital styrenhet och CD-tårtlåda, samt en UV-lampa som monterades från enskilda komponenter och inrymdes i en repurposed sharps behållare(Kompletterande figur 1). Den största fördelen med hembryggningsfotolitografiinställningen är att den är mycket prisvärd (< $ 1000 för all utrustning) samtidigt som den fortfarande kan skapa encellsstora funktioner. Användningen av billig utrustning har dock sina begränsningar - till exempel är det mer utmanande att exakt justera fiducial markörer för att mönster flera DNA-oligos utan användning av en maskjusterare. Vi rekommenderar denna billiga fotolitografiinställning för labb som inte har bekväm tillgång till ett rent rum eller som vill prova den här metoden utan en stor investering.
För att identifiera optimala förhållanden för DNA-programmerad cell vidhäftning varierade vi systematiskt koncentrationerna av DNA-strängar på cellytor och mätte effektiviteten hos cell vidhäftning till DNA-modifierade glasytor. Koncentrationen av Universal Anchor + Adapter Strand och Universal Co-Anchor i märkningslösningar varierade mellan flera storleksordningar (figur 4A, B), vilket resulterade i 104 - 106 DNA-komplex per cell(kompletterande figur 4). Cell vidhäftning var dosberoende, med minimal cell vidhäftning till DNA-mönstret när celler märktes med CMOs vid en koncentration av 0, 05 μM eller mindre, och hög beläggning vid en koncentration av 2,5 μM och högre. Vi använde därför en 2 μM-lösning av Universal Anchor + Adapter Strand och 2 μM-lösning av Universal Co-Anchor i de flesta experiment. Cell vidhäftningen förväntas också minska om mängden DNA som används på glasytan minskade med29 eller om obalansen mellan adaptersträngen och ytsträngen ökade. Mer information om Adapter Strand-sekvensdesign finns i Kompletterande fil 2. CMO-märkning med adaptersträngar utan cpg-upprepningar stimulerade inte TLR9 i HEK-celler som uttrycker mus TLR9(kompletterande figur 5).
Vi tillhandahåller flera demonstrationer som det reviderade protokollet ger reproducerbar och effektiv DNA-programmerad cell vidhäftning. Till exempel, mänskliga navelveniska endotel celler (HUVECs) märkt med CMOs följde DNA mönster med hög effektivitet. CMO-märkta HUVECs följde såväl som LMO-märkta HUVECs(figur 5A). Celler mönstrade med CMO-DPAC behöll sin livskraft och funktionalitet. Celler märkta med cmos färgades av kalcein AM och etidium homodimer för att bedöma livskraften(kompletterande figur 6). Skillnader i livskraft jämfört med omärkta kontrollceller var små (94% jämfört med 97%). Enstaka MDCKs mönstrade via CMO-DPAC och överfördes till Matrigel kunde föröka sig och polarisera korrekt efter 5 dagars kultur (figur 5B). DPAC ger också ett sätt att utveckla mönster av celler i den tredje dimensionen (figur 5C). Flerskiktsaggregat kan till exempel skapas genom alternerande lager av celler märkta med kompletterande cmos(figur 5C). Dessa experiment visar att protokollet är reproducerbart, påverkar inte cellens livskraft eller funktionalitet negativt och ger cellulära mönster som framgångsrikt kan odlas inom ett enda bildplan i en 3D ECM.
Genom att tillhandahålla ortogonala DNA-sekvenser för att rikta cell vidhäftning ger DPAC ett sätt att mönstra flera celltyper på en enda yta. För att implementera denna funktion i DPAC måste DNA-mönster som genereras av fotolitografi anpassas till varandra. Metallförvaltare som deponerats på bilden tillät justering av flera fotomasker och därmed mönstra av flera celltyper samtidigt. MCF10As färgade med olika unika färgämnen var märkta med ortogonala CMOs och mönstrade för att skapa en visualisering av UC Berkeley och UCSF logotyper (figur 6). Detta experiment visar att flera unika cellpopulationer kan mönstras tillsammans med hög precision och utan korskontaminering.
Framgångsrik mönstrad av celler med CMO-DPAC kräver högkvalitativ fotolitografi, tillräcklig koncentration av oligo på cellytan, en hög densitet av celler över mönstret och tillräcklig tvättning. Om något av dessa steg misslyckas påverkas slutresultatet. Kompletterande figur 2 innehåller exempelbilder av korrekt och felaktig fotolitografi (kompletterande figur 2A), önskad celltäthet över mönstret för att skapa fullt upptagna mönster (kompletterande figur 2B),förlust av mönstrade celler på grund av alltför kraftig pipettering under efterföljande steg av DPAC (Kompletterande figur 2C) och oönskad klump av celler(kompletterande figur 2D). Tabell 1 innehåller en lista över vanliga felpunkter och den föreslagna felsökningen. Användning av fluorescerande kompletterande oligos rekommenderas som ett verktyg för felsökning för att bekräfta förekomsten av mönstrat DNA på bilden och närvaron av CMOs på cellytan genom flödescytometri (se steg 8 i protokollet).
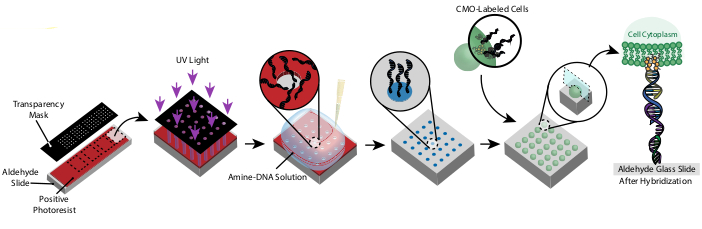
Bild 1: Översikt över CMO-DPAC-protokollet. Först skapas en DNA-mönstrad bild genom att belägga en aldehydfunktionaliserad glasrutschbana med en positiv fotoresist, täcka den med en genomskinlig mask i önskat mönster och utsätta den för UV-ljus. Den UV-exponerade fotoresisten tvättas bort med utvecklaren, vilket lämnar utsatta regioner i aldehydrutschbanan och möjliggör bindning av aminfunktionaliserat DNA till ytan. Celler märks sedan med cmos och flödas över ytan. DNA:t på cellmembranet hybridiseras till DNA på ytan, vilket resulterar i vidhäftning. Klicka här för att se en större version av den här figuren.
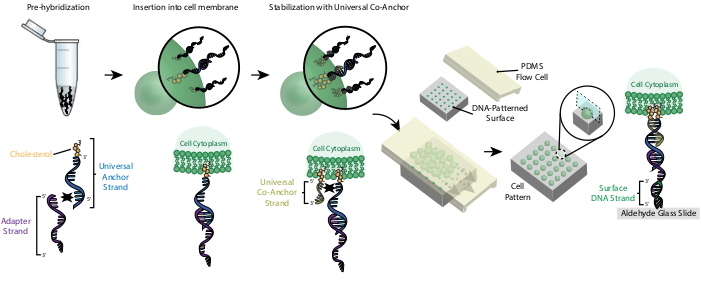
Bild 2: Celler är märkta med cmos i en stegvis process. Först är den kolesterolmodifierade Universal Anchor Strand förhybridiserad med adaptersträngen. Därefter blandas universalankar- + adapterlösningen med cellfjädringen. Kolesterolet på universalankar- + adapterkomplexet skärs in i cellmembranet. Efter inkubation tillsätts den kolesterolmodifierade Universal Co-Anchor Strand till cell suspensionen, där den hybridiseras med Universal Anchor Strand och skär in i cellmembranet. Tillsatsen av den andra kolesterolmolekylen ökar NETTOhydrofobin i DNA-komplexet och stabiliserar det i membranet26. Efter att ha tvättat ut överflödigt DNA koncentreras cellerna och läggs till en PDMS-flödescell ovanpå den mönstrade ytan. Adaptersträngens 3' ände hybridiseras med Surface DNA-strängen på glasrutschbanan, vilket resulterar i vidhäftning av bilden specifikt i regioner som funktionaliserats med kompletterande DNA. Klicka här för att se en större version av den här figuren.
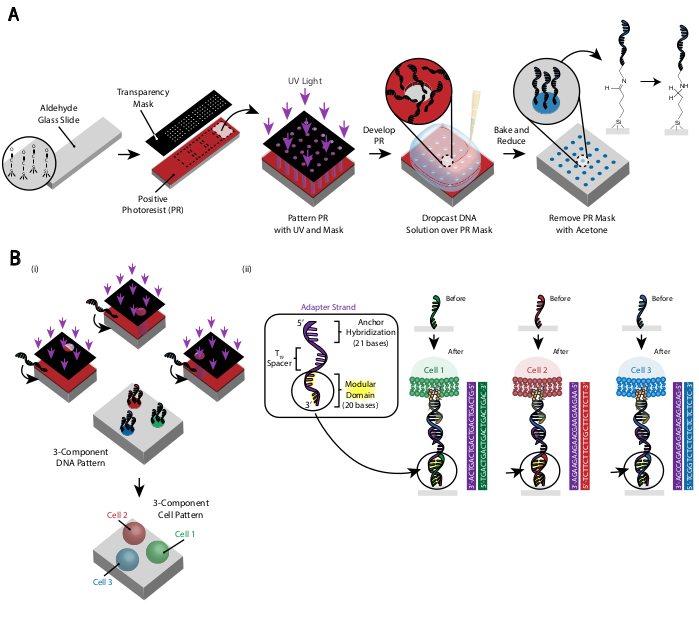
Bild 3: Fotolitografi används för att skapa DNA-mönstrade bilder som i slutändan kommer att diktera placeringen av celler. ( A) Översikt över fotolitografiprocessen. En aldehydfunktionaliserad rutschkana är spin-coated med en positiv fotoresist. UV-ljus lyser på bilden genom en genomskinlig fotomask som är transparent där cell vidhäftning önskas. Efter att rutschkanan har utvecklats har de regioner som tidigare utsatts för UV-ljus nu exponerat aldehydgrupper. En 20 μM-lösning av en aminfunktionaliserad DNA-oligo släpps sedan på rutschkanan och sprids över de mönstrade regionerna. Diabilden bakas sedan för att inducera bildandet av Schiffbindningar (C=N) mellan amin- och aldehydgrupperna, en reversibel kovalent bindning29. Efterföljande reduktiv amination med 0,25% natrium boryohydrid i PBS omvandlar Schiff-basen till en sekundär amin genom reduktiv amination, vilket resulterar i ett oåterkalleligt band mellan DNA och bilden. Den återstående fotoresisten kan sedan tas bort genom att skölja med aceton. (B) Denna process kan upprepas för att skapa DNA-mönster med flera komponenter och därmed utföra experiment med flera cellpopulationer. i) När den första oligo mönstras, är bilden igen belagd med photoresist och protokollet fortsätter som tidigare. Justering av fotomaskerna med hjälp av förvaltningsmarkörer är nödvändig för att mönstra flera DNA-strängar. ii) Varje celltyp som mönstras skiljer sig åt i adaptersträngens modulära 20-basdomän. Genom att använda ortogonala uppsättningar av kompletterande oligos kan flera celltyper mönstrades utan kors vidhäftning. Klicka här för att se en större version av den här figuren.
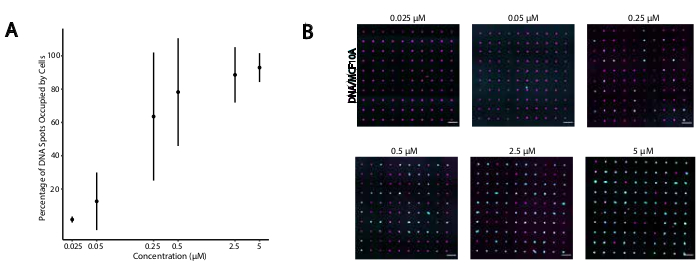
Figur 4: Vidhäftning av CMO-märkta celler till DNA-mönster ökar som en funktion av CMO-koncentrationen under märkning. I detta experiment användes Universal Anchor + Adapter Strand (förhybridiserad) och Universal Co-Anchor vid lika koncentrationer. Med koncentration avses koncentrationen av cmo i cellupphängningen under CMO-märkning av celler. a)Kvantifiering av den procentandel av DNA-fläckar med 15 μm diameter som upptogs av CMO-märkta MCF10A-celler som en funktion av CMO-koncentrationen under cellmärkning. Data representerade som medelvärde ± standardavvikelse från tre experiment. (B) Representativa bilder av DNA-mönstren (magenta) och vidhäftade MCF10As (cyan) vid olika koncentrationer av CMO. Skalningslist = 100 μm. Klicka här för att se en större version av denna siffra.
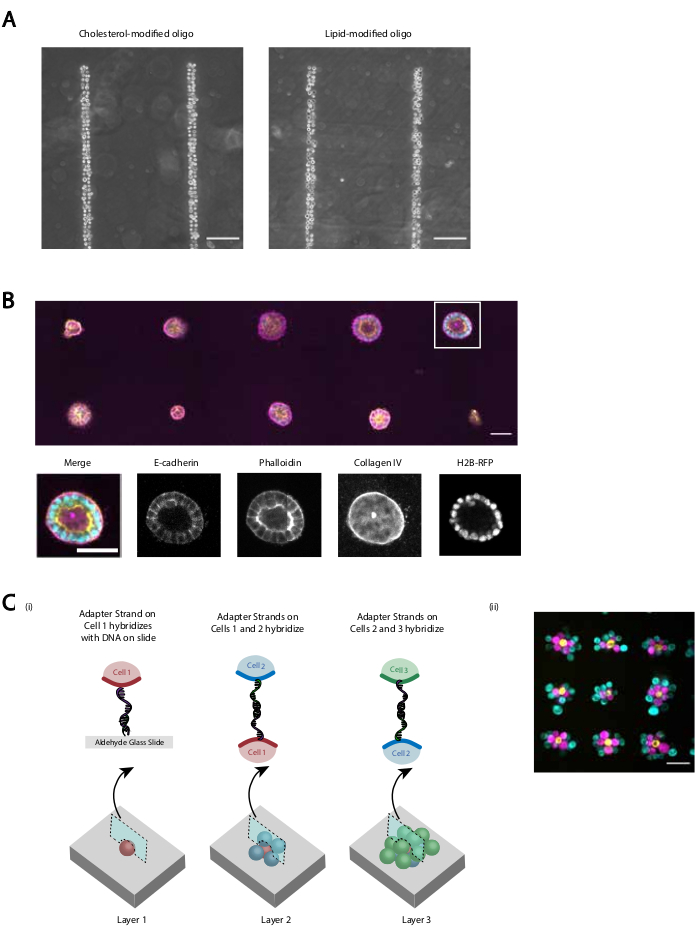
Bild 5: CMO-DPAC kan användas för att skapa tvådimensionella cellmönster som sedan kan bäddas in i en tredimensionell hydrogel för odling och/eller skiktad för att skapa flerskiktsstrukturer. ( A) Direkt jämförelse mellan CMO-märkta humana navelvens endotelceller (HUVECs) och LMO-märkta HUVECs som följs av ett linjärt DNA-mönster. Båda metoderna för cellmärkning resulterar i nästan 100% beläggning av DNA-mönstret. B)Single Madin-Darby Canine Kidney cells (MDCKs) som uttrycker H2B-RFP mönstrades på 15 μm diameter fläckar med 200 μm mellanrum och därefter inbäddat i Matrigel. Efter 120 h av kultur, de resulterande epitelial cystor fixades och färgades för E-cadherin, aktin och kollagen IV. Sfäroid i vit låda visas i detalj. Skalstreck = 50 μm. (C) Flerskiktade cellulära strukturer kan skapas genom att märka separata cellpopulationer med kompletterande adaptersträngar och mönstra sekventiellt så att varje ny tillsats av celler fäster vid cellskiktet före det. i) Ett schema över sekventiell mönstrad av cellpopulationer för att skapa flerskiktsstrukturer. ii) Treskiktade cellaggregat av MCF10As (visualiseras med hjälp av färgämnen) skapades med hjälp av denna process. Skalstreck = 50 μm. Klicka här för att se en större version av denna siffra.

Bild 6:Flera celltyper kan mönstras utan korskontaminering eller förlust av vidhäftning. Flera amine-modifierade DNA oligos mönstrades sekventiellt på en aldehyd slide och justeras genom användning av metall fiduciary markörer. Tre populationer av MCF10As (cyan, magenta, gul) färgades med unika färgämnen märkta med kompletterande CMOs, och mönstras på bilden, vilket resulterar i en bild av UC Berkeley och UCSF logotyper. Skalstreck 1 mm. Klicka här för att se en större version av denna siffra.
Kompletterande figur 1: Exempelbilder av bänkskivans fotolitografiinställning. (A) Glid på spinnrockaren, täckt med positiv fotoresist, före spinnbeläggning. (B) Bild av genomskinlighet fotomask. c)Under exponeringen är fotomasken inklämd mellan den fotoresistbelagdarutschkanan och en glasskiva. (E) Glid nedsänkt i utvecklarlösning. (F) Utvecklad bild. g)Amine-modifierad DNA-lösning sprids på mönstrade delar av bilden. (H)PDMS-flödesceller placerade ovanpå mönstrade områden i bilden. Klicka här för att ladda ner den här filen.
Kompletterande figur 2: Några exempel på vanliga fel i detta protokoll. ( a)i) Underbakning före UV-exponering eller överutvecklingsfunktioner efter exponering kan resultera i egenskaper som har ojämna kanter och kan vara oregelbundna i storlek. (ii) Ett exempel på en korrekt fotopatternerad bild som har rena kanter runt funktioner, enhetlig funktionsstorlek och inga uppenbara sprickor i mönstret. Skalstång = 50 μm. (B) Celltätheten är avgörande för mönskningseffektiviteten. När du observerar cellerna ovanpå mönstret under ett mikroskop bör det finnas få mellanrum mellan cellerna, vilket framgår av exempelbilden till vänster. Skalstång = 50 μm. (C) Mönstrade celler kan vara känsliga för vätskekrafter som uppstår vid alltför kraftig pipettering, vilket kan skada och rubba de mönstrade cellerna. Flerskiktscellaggregat är särskilt sårbara, eftersom en cell längst ned stöder en struktur med flera celler. i) En matris med cellaggregat som har bäddats in i Matrigel. ii) Ett rutnät av cellaggregat som lossnat till följd av att viskösen Matrigel för kraftigt ryckts ut. (D) Klumpning av celler kan förekomma, särskilt med epitelceller. Dessa klumpar är vanligtvis homotypiska men kan vara heterotypiska (celler som följer redan mönstrade celler av en annan typ) om cellerna är särskilt klibbiga. Bilden visar tre olika populationer av MCF10As mönstrades på en matris bestående av tre olika encelliga DNA-fläckar (15 μm). De flesta DNA-fläckar har 2-4 celler fästa. Klumpar kan lösas genom EDTA-behandling eller genom att filtrera bort klumpar före mönstraring. Skalstång = 100 μm. Klicka här för att ladda ner den här filen.
Kompletterande figur 3: Överlappande fotomönster resulterar i förekomst av båda oligos vid minskad koncentration. Två ortogonala amin-modifierade oligos var photopatterned sekventiellt, först en vertikal linje (Strand 1), följt av en horisontell linje som överlappade den (Del 2). Oligos visualiserades sedan genom hybridisering med fluorescerande kompletterande oligos. (A) Fluorescensbild av del 1. b)Kvantifiering av fluorescensprofilen för del 1 över en vertikal linje på 100 μm som sträcker sig över överlappningen. c)Fluorescensbild av del 2. d)Kvantifiering av fluorescensprofilen för del 2 över en horisontell linje på 100 μm som sträcker sig över överlappningen. Skalstång = 50 μm. Klicka här för att ladda ner den här filen.
Kompletterande figur 4: Kvantifiering av DNA-komplex på cellytan som en funktion av cmo-märkningskoncentrationen. HUVECs var märkt med olika koncentrationer av CMO lösning, tvättas och sedan inkuberas med en fluorescerande kompletterande sträng. Ett MESF-mikrosfärkit (Molecules of Equivalent Soluble Fluorochrome) användes för att göra kvantitativ flödescytometri och uppskatta antalet DNA-komplex på cellytan som en funktion av CMO-koncentrationen under märkning. Klicka här för att ladda ner den här filen.
Kompletterande figur 5: CMO-märkning stimulerar inte TLR9-svaret. Ett experiment utfördes för att se om CMO-märkning skulle utlösa DNA-detektionsmekanismen för TLR9 och om detta skulle påverkas av cpgs i Adapter Strand-sekvensen. HEK-celler som uttrycker mus TLR9 inkuberades över natten med 0,2 μM av antingen ODN 1826 (en CpG-innehållande TLR9-agonist), CMO Universal Anchor + Universal Co-Anchor + Adapter Strand som innehåller samma sekvens som ODN 1826 (CMO-CpG) eller CMO Universal Anchor + Universal Co-Anchor + Adapter Strand som innehåller en liknande sekvens men med ersättning av CpGs med GPCs (CMO-CpG). TLR9 stimulering skulle resultera i produktion av SEAP (utsöndrad embryonal alkalisk fosfatas). SEAP utsöndring kvantifierades av en koloretmetric analys (absorbans). Behandlingsförhållandena jämfördes med viloceller som endast behandlades med PBS. Inkubation med CMO-GPC stimulerade inte TLR9 uttryck. Inkubationen med CMO-CpG var något högre än viloceller men mycket lägre än ODN-1826. Klicka här för att ladda ner den här filen.
Kompletterande figur 6: Cellernas livskraft efter cmo-märkningsprocessen. För att bedöma hur protokollet påverkar livskraften delades HUVECs upp i fyra populationer: en förblev på is i 1 h, en var mock-märkt med PBS men annars togs genom alla centrifug- och tvättsteg, en var märkt med CMOs och en var märkt med CMOs och filtrerades genom ett 40 μm filter för att ta bort klumpar. Cellerna färgades sedan med kalcein AM och etidium homodimer för att bedöma antalet levande och döda celler. Alla behandlingar resulterade i signifikant minskad livskraft än iskontrollen (enkelriktad ANOVA med Tukey post-hoc-analys), men medianviabiliteten för CMO-märkning (med eller utan filtrering) var cirka 94%. Data som samlats in från tre oberoende experiment. * = p < 0,05. = p < 0.0001 Klicka här för att ladda ner den här filen.
| Resultat | Möjliga orsaker | Föreslagna korrigeringar |
| Fotolitografi – funktionerna är spruckna | Inkonsekvent eller otillräcklig mjukbakning | Öka tiden för mjukbakning upp till 3 minuter; kontrollera den faktiska temperaturen på värmeplattan och öka temperaturen vid behov |
| Fotolitografi – funktionerna är inte skarpa eller har photoresist kvar i dem | Underutveckling | Öka tiden som bilden spenderar i utvecklarlösningen; innehåller mild agitation |
| Fotolitografi – funktioner inkonsekventa över bilden | UV-ljus kanske inte är centrerat eller inte fokuserat korrekt | Justera UV-ljusinställningen för att säkerställa kollimerat ljus med jämn intensitet |
| Celler håller inte fast vid mönstrade fläckar med hög effektivitet | Inte tillräckligt med DNA på ytan | Bekräfta att DNA finns på ytan genom att hybridisera bilden med fluorescerande kompletterande oligos och sedan avbildning under mikroskop |
| Cellerna är otillräckligt märkta med CMO | Tillsätt fluorescerande kompletterande oligos till cellfjädring och bekräfta fluorescens via flödescytometri | |
| Inte tillräckligt med celler över mönstret | Samla celler genom att tvätta ut från PDMS flödescell, centrifug och suspendera i lägre volym för att koncentrera cellerna | |
| För mycket återstående cmo i cellupphängning, hybridisering med DNA på glid | Lägg till ytterligare ett tvättsteg. Var noga med att ta bort så mycket supernatant som möjligt med varje tvätt. | |
| För mycket internalisering av cmo på grund av tid och temperatur | Arbeta snabbt efter märkning av cellerna med CMO. hålla celler och glida på is och använda iskalla reagenser | |
| Celler klump | Cellerna separerades inte tillräckligt under trypsiniseringen | Använd PBS + 0,04% EDTA under celltvättar; passera cellfjädring genom 35 μm filter före den slutliga tvätten |
| Celler fäster icke-specifikt | Om i ett specifikt område – kan bero på repor på bilden, feljustering av PDMS-flödesceller eller spill av DNA utanför mönsterområdet | Undvik repor, var noga med att justera PDMS-flödescellerna till mönsterområdet |
| Om celler sitter överallt – otillräcklig blockering eller tvätt | Lägg till fler tvättar efter mönstra av cellerna; pipetten kraftigare under tvättar; block med 1% BSA längre innan cellmönster påbörjas; silanize slide (valfritt steg 3) eller bekräfta att silanisering lyckades genom att mäta kontaktvinkeln för vattendroppe | |
| Bubblor bildas i flödescellen | Pipetteringsfel, ojämn hydrofil yta skapad under plasmaoxidation | Om bubblor är små, tillsätt PBS till inloppet i flödescellen och de kan tvättas ut. Om bubblorna är större, tryck försiktigt på PDMS-flödescellen och knuffa bubblorna mot inloppet eller utloppet. |
| Celler håller initialt fast vid mönster men avlägsnas under tvättar, mönstra av andra celltyper eller lägger till hydrogelprekursoren | Skjuvningskrafterna från pipettering för kraftigt kan orsaka att cellerna lossnar från ytan | Pipettera mer försiktigt under efterföljande tvättar, rundor av cellmönster eller tillsats av hydrogelprekursorer. Eftersom hydrogelprekursorerna är trögflyttade är de mer benägna att orsaka att mönstret lossna, så var extra försiktig. Flerskiktsstrukturer tenderar att vara topptunga och är mer mottagliga för att rubbas. |
| Vävnad deformeras under 3D-överföring | Hydrogel fastnar på glid | Bekräfta hydrofobi för bild med hjälp av kontaktvinkelmätningar |
| Använd rakblad för att lyfta PDMS helt på båda kanterna, så att PBS kan flyta under vävnaden | ||
| Detta kan hända med rena kollagenhydrogeler – överväg att justera proteinkoncentrationen eller sammansättningen av hydrogel | ||
| Celler överförs inte med hydrogelen och förblir på bilden | Öka Turbo DNAse-koncentrationen eller öka inkubationstiden | |
| Hydrogel är inte tillräckligt solid | Öka inkubationstiden och/eller geleringsmekanismen för hydrogelen i fråga (t.ex. för kollagen, se till att pH-värdet är korrekt) | |
| Hydrogel tårar när du tar bort PDMS | Gör PDMS flödesceller hydrofila med plasmaoxidation innan experimentet påbörjas så att de lätt lossnar när de lägger till media. Använd tång mycket försiktigt för att lossa PDMS. |
Tabell 1: En felsökningsguide för att identifiera och lösa potentiella fel som kan uppstå från det här protokollet. I synnerhet kan dålig vidhäftning av celler till mönstret ha många grundorsaker och den här guiden bör hjälpa till att identifiera och lösa dessa problem.
Kompletterande fil 1. Klicka här för att ladda ner den här filen.
Kompletterande fil 2. Klicka här för att ladda ner den här filen.
Kompletterande fil 3. Klicka här för att ladda ner den här filen.
Kompletterande fil 4. Klicka här för att ladda ner den här filen.
I den här artikeln presenterar vi ett detaljerat protokoll för högupplöst mönstra av celler i 2D och 3D för in vitro cell kultur experiment. Till skillnad från tidigare publicerade versioner av denna metod fokuserar protokollet som presenteras här på användbarhet: det kräver inte högspecialiserad utrustning och alla reagenser kan köpas från leverantörer istället för att kräva anpassad syntes. Till skillnad från andra cellmikropatterningsmetoder är denna metod snabb och celltypoberoende: det kräver inte specifik vidhäftning till extracellulära matrisproteiner15. Celler mönstrade av CMO-DPAC kan bäddas in i en extracellulär matris som Matrigel eller kollagen, vilket resulterar i 3D-kulturer med mycket högre rumslig upplösning än vad som för närvarande är möjligt med extruderingstryckbaserade metoder22. CMO-DPAC kan användas för att skapa hundratals till tusentals mikroskopiska funktioner per bild, vilket gör att många replikat kan utföras samtidigt.
En av de viktigaste parametrarna för framgången för detta protokoll är densiteten hos celler som läggs till flödescellerna ovanpå den mönstrade bilden. Helst bör densiteten vara minst 25 miljoner celler/ml. När den laddas in i flödescellerna resulterar denna densitet av celler i ett nästan tätt packat monoskikt av celler ovanför mönstret (Kompletterande figur 2B). Dessa höga celltätheter maximerar sannolikheten för att en cell kommer att bosätta sig direkt ovanpå en DNA-punkt och hålla fast. Om celltätheten minskas den totala mönstraringseffektiviteten. Ett annat kritiskt steg i detta protokoll är att noggrant suspendera cellerna i PBS eller serumfria medier innan cmo-lösningen läggs till. CmOs-partitionen mycket snabbt i cellmembran och att lägga till CMO-lösningen direkt till en cellpellet resulterar i heterogen märkning av celler. Efter att ha lagt till CMO-lösningen till cellupphängningen är det viktigt att blanda noggrant genom pipettering så att cellerna är jämnt märkta med cmos. Efter inkubationerna är det nödvändigt att noggrant tvätta ut överskottet av cmos genom flera centrifugering och tvätta steg. Överflödig fri cmo som finns i cellupphängningen binder till det mönstrade aminmodifierade DNA på glasrutschbanan, vilket blockerar hybridisering och vidhäftning av de CMO-modifierade cellerna i suspension. Tiden är också en viktig faktor för detta protokoll. Det är viktigt att arbeta så snabbt som möjligt när du använder cmos och att hålla cellerna på is för att minimera internaliseringen av cmos och maximera cellens livskraft. Flödescytometriexperiment har visat att cmos inte kvarstår lika länge på cellytan som LMOs, med 25% förlust av CMO-komplex under två timmars inkubation på is36. Dessutom kommer cellernas livskraft att minska när cellhanteringstiden ökar. Livskraften kan maximeras genom att arbeta snabbt, hålla cellerna på is, använda iskalla reagenser och använda serumfria medier för att ge vissa näringsämnen.
Även om CMO-DPAC kan vara ett kraftfullt sätt att studera cellbiologi genom att mönstra celler med hög precision, har det sina begränsningar. CMO-DPAC-experiment kan vara utmanande, särskilt som den experimentella komplexiteten läggs till med flera celltyper, lager eller 3D-cellkultur (Kompletterande fil 1). Experimentella fel kan vara vanliga när det här protokollet startas, enligt beskrivningen i tabell 1. Därför rekommenderar vi att användare inför kvalitetskontrollkontroller (bekräftar att DNA finns på bilden, bekräftar att cellerna är tillräckligt märkta med DNA (steg 8), bekräftar att överflödiga celler har tvättats bort noggrant etc.) för att se till att experimentet lyckas och för att identifiera steg som kan kräva ytterligare optimering. Vi hoppas att informationen i detta manuskript och dess kompletterande filer kommer att underlätta eventuell nödvändig felsökning.
Kolesterol är en bioaktiv molekyl vars internalisering kan påverka cellmetabolism, genuttryck och membranvätska37,38. I en tidigare studie jämfördes effekterna på genuttryck av CMO- och LMO-märkta celler med hjälp av encellig RNA-sekvensering. CMO-märkta HEK-celler hade förändrat genuttrycket jämfört med omärkta och LMO-märkta celler36. Märkning av celler med cmos resulterade i differentialuttrycket (> 1,5-faldigt) av åtta gener i förhållande till omärkta kontroller, inklusive AP2B1, som har kopplats till kolesterol och sphingolipid transport (GeneCards) och MALAT1, ett långt icke-kodande RNA som reglerar kolesterolackumulering39. Medan mindre, dessa transkriptionella svar kan ändå vara oroande om experimentet i fråga studerar metabolism, membran dynamik, eller andra kolesterol-associerade vägar i celler.
Detta protokoll är flexibelt och kan justeras för att uppfylla behoven för varje experiment. Eftersom CMO sätter sig in i lipidmembranet istället för att använda någon specifik receptor, är metoden celltyp agnostisk (HUVECs, MCF10As, HEKs och MDCKs har visats här). Även om kolesterol är ett annat hydrofobiskt ankare än våra tidigare publicerade LMOs, har vi hittills funnit att de beter sig på samma sätt. Således förväntar vi oss att cmos fungerar med någon av de många olika celltyper som vi tidigare har publicerat med LMOs, inklusive men inte begränsat till neurala stamceller, fibroblaster, perifera blodmononkleära celler, tumörceller och primära bröst epitelceller6,23,27,29,36 . CMO-märkning stimulerar inte TLR9, vilket tyder på att protokollet är kompatibelt med immunceller. Membraninkorporering av cmo är en funktion av total cellstorlek och graden av negativ laddning i cellen glykocalyx35. Således har vi inkluderat ett protokoll (steg 8) för att testa omfattningen av membraninkorporering som är mottaglig för snabb optimering. De specifika egenskaperna hos varje cellmönster kommer oundvikligen att variera beroende på den experimentella designen (se Kompletterande fil 1 för mer vägledning). Även om fotopatterning protokollet som beskrivs ovan för mönstrar AV DNA rekommenderas, bör alla metoder för rumsligt begränsa droppar av amine-DNA-lösning fungera, såsom användning av högupplösta droppskrivare. Mönsterupplösningen och minimifunktionens avstånd varierar beroende på vilken metod som används. Det är också teoretiskt möjligt att kombinera DNA-fotopatteringavsnitten i detta protokoll med andra metoder som har använts för att märka celler med DNA, till exempel med DNA hybridiserat till membranut uttryckta zinkfingrar40, med hjälp av NHS-konjugerat DNA41, och reagera azido sialic acid rester på cellytan med fosfin-konjugerat DNA42 . CMO-DPAC kan tillämpas på en mängd olika experiment som kräver noggrann kontroll över cellcellsavstånd, inklusive studier av interaktioner mellan par av celler, samkulturexperiment som tittar på överföring av signaler från "avsändarceller" till "mottagarceller" och undersökningar av effekten av närliggande extracellulära signaler på stamcellsdifferentiering6,29 . Metoden kan också användas för att skapa mikrotissuer som kan användas för att studera cellmigration i tre dimensioner, cellernas självorganisering i vävnader23,27och det dynamiska samspelet mellan celler och ECM27. Vi hoppas att detta protokoll kommer att ge forskare en tillgänglig plattform för att utforska nya tillämpningar av högupplöst DNA-baserad cellmönster i sina egna laboratorier.
Z.J.G. är rådgivare och aktieägare i Provenance Biosciences.
Författarna vill tacka Jeremy Garcia för att ha testat detta protokoll och Bhushan Kharbikar för att ha tillhandahållit utbildning om utrustningen vid UCSF Biomedical Micro and Nanotechnology Core. Denna forskning stöddes delvis av bidrag från Institutionen för försvar bröstcancerforskningsprogram (W81XWH-10-1-1023 och W81XWH-13-1-0221), NIH (U01CA199315, DP2 HD080351-01, 1R01CA190843-01, 1R21EB019181-01A och 1R21CA182375-01A1), NSF (MCB1330864) och UCSF Center for Cellular Construction (DBI-1548297), ett NSF(MCB1330864) och UCSF Center for Cellular Construction (DBI-1548297), ett NSF(MCB1330864) och UCSF Center for Cellular Construction (DBI-1548297), ett NSF(MCB1330864) och UCSF Center for Cellular Construction (DBI-1548297), ett NSF(MCB1330864) och UCSF Center for Cellular Construction (DBI-1548297), ett NSF-center( O.J.S finansierades av ett NSF Graduate Research Fellowship, ett Siebel-stipendium och ett P.E.O. Stipendium. Z.J.G och A.R.A. är Chan-Zuckerberg BioHub-utredare.
| Name | Company | Catalog Number | Comments |
| 2-well Chambered Coverglass w/ non-removable wells | Thermo Fisher Scientific | 155379 | |
| Acetic Acid | Sigma-Aldrich | A6283 | |
| Adapter with External SM1 Threads and Internal SM3 Thread | ThorLabs | SM3A1 | |
| Aldehyde Functionalized Slides | Schott | Nexterion Slide AL | Store under dry conditions after opening. |
| All Plastic Syringes, 1 mL | Fisher Scientific | 14-817-25 | |
| Amine-Modified DNA Oligo | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| Aspheric Condenser Lens | ThorLabs | ACL7560 | |
| Borosilicate Disc, 6in Diameter X 1/2in Thick | Chemglass | CG-1906-23 | |
| Cell Culture Dishes 60x15 mm style | Corning | 353002 | |
| Cholesterol-Modified Oligo | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| Diamond Scribe | Excelta | 475B | |
| DNA Oligonucleotide | IDT | n/a | See Supplemental File 1 for suggested sequences. |
| DPBS, no calcium, no magnesium | Thermo Fisher Scientific | 14190250 | |
| Isopropyl Alcohol | Sigma-Aldrich | 278475 | |
| Matrigel Matrix, Growth Factor Reduced | Corning | 354230 | |
| Methylene Chloride (Stabilized/Certified ACS) | Fisher Scientific | D37-4 | |
| MF-321 Developer | Kayaku Advanced Materials | n/a | |
| Microposit S1813 Positive Photoresist | Kayaku Advanced Materials | n/a | |
| Ø3" Adjustable Lens Tube, 0.81" Travel | ThorLabs | SM3V10 | |
| Oven | Thermo Scientific | 51-028-112H | |
| PE-50 Compact Benchtop Plasma Cleaning System | Plasma Etch | PE-50 | |
| Photomask (custom) | CAD/Art Services | n/a | Minimum feature size guaranteed by CAD/Art Services is 10 microns. |
| Razor Blades | Fisher Scientific | 12-640 | |
| RCT Basic Hot Plate | IKA | 3810001 | |
| Silicon Wafer (100 mm) | University Wafer | 590 | |
| Sodium Borohydride, 98%, granules | Acros Organics | 419471000 | |
| Spin Coater Kit | Instras | SCK-200 | This is a low cost option, but any spin coater that can maintain a speed of 3000 rpm will suffice. |
| SU-8 2075 | Microchem | Y111074 0500L1GL | |
| SU-8 Developer | Microchem | Y020100 4000L1PE | |
| Sylgard 184 Silicone Elastomer Kit | Dow | 2646340 | |
| Syringe Needles | Sigma-Aldrich | Z192341 | |
| T-Cube LED Driver, 1200 mA Max Drive Current | ThorLabs | LEDD1B | |
| Tridecafluoro-1,1,2,2-tetrahydrooctyl dimethylchlorosilane | Gelest | SIT8170.0 | |
| Triethylamine | Sigma-Aldrich | 90335 | |
| Turbo DNase | Thermo Fisher Scientific | AM2238 | |
| Tweezers Style N7 | VWR | 100488-324 | The curved shape of these tweezers is essential for delicately picking up the PDMS flow cells containing patterned tissues. |
| UV LED (365 nm, 190 mW (Min) Mounted LED, 700 mA) | ThorLabs | M365L2 | |
| Wafer Tweezers | Agar Scientific | T5063 | |
| WHEATON Dry-Seal vacuum desiccator | Millipore Sigma | W365885 |
- Kreeger, P. K., Strong, L. E., Masters, K. S. Engineering approaches to study cellular decision-making. Annual Review of Biomedical Engineering. , 49-72 (2018).
- Goubko, C. a., Cao, X. Patterning multiple cell types in co-cultures: A review. Materials Science and Engineering C. 29 (6), 1855 (2009).
- Sun, W., et al. The bioprinting roadmap. Biofabrication. 12 (2), 022002 (2020).
- Liu, W. F., Chen, C. S. Cellular and multicellular form and function. Advanced Drug Delivery Reviews. 59 (13), 1319-1328 (2007).
- Duffy, R. M., Sun, Y., Feinberg, A. W. Understanding the role of ECM protein composition and geometric micropatterning for engineering human skeletal muscle. Annals of Biomedical Engineering. 44 (6), 2076-2089 (2016).
- Chen, S., et al. Interrogating cellular fate decisions with high-throughput arrays of multiplexed cellular communities. Nature Communications. 7, 10309 (2016).
- Shaya, O., et al. Cell-cell contact area affects notch signaling and notch-dependent patterning. Developmental Cell. 40 (5), 505-511 (2017).
- Rao, N., et al. A co-culture device with a tunable stiffness to understand combinatorial cell-cell and cell-matrix interactions. Integrative Biology. 5 (11), 1344 (2013).
- Sriraghavan, V., Desai, R. A., Kwon, Y., Mrksich, M., Chen, C. S. Micropatterned dynamically adhesive substrates for cell migration. Langmuir. 26 (22), 17733-17738 (2010).
- Wong, L., Pegan, J. D., Gabela-Zuniga, B., Khine, M., McCloskey, K. E. Leaf-inspired microcontact printing vascular patterns. Biofabrication. 9 (2), 021001 (2017).
- Chen, T. H., et al. Directing tissue morphogenesis via self-assembly of vascular mesenchymal cells. Biomaterials. 33 (35), 9019-9026 (2012).
- Laurent, J., et al. Convergence of microengineering and cellular self-organization towards functional tissue manufacturing. Nature Biomedical Engineering. 1 (12), 939-956 (2017).
- Lin, C., Khetani, S. R. Micropatterned co-cultures of human hepatocytes and stromal cells for the assessment of drug clearance and drug-drug interactions. Current Protocols in Toxicology. 2017, 1-23 (2017).
- Hui, E. E., Bhatia, S. N. Micromechanical control of cell-cell interactions. Proceedings of the National Academy of Sciences of the United States of America. 104 (14), 5722-5726 (2007).
- D'Arcangelo, E., McGuigan, A. P. Micropatterning strategies to engineer controlled cell and tissue architecture in vitro. BioTechniques. 58 (1), 13-23 (2015).
- Martinez-Rivas, A., González-Quijano, G. K., Proa-Coronado, S., Séverac, C., Dague, E. Methods of micropatterning and manipulation of cells for biomedical applications. Micromachines. 8 (12), (2017).
- Lee, S., et al. Simple lithography-free single cell micropatterning using laser-cut stencils. Journal of Visualized Experiments. (158), e60888 (2020).
- Strale, P. O., et al. Multiprotein printing by light-induced molecular adsorption. Advanced Materials. 28 (10), 2024-2029 (2016).
- Melero, C., et al. Light-induced molecular adsorption of proteins using the primo system for micro-patterning to study cell responses to extracellular matrix proteins. Journal of Visualized Experiments. (152), e60092 (2019).
- Reid, J. A., Mollica, P. M., Bruno, R. D., Sachs, P. C. Consistent and reproducible cultures of large-scale 3D mammary epithelial structures using an accessible bioprinting platform. Breast Cancer Research. , 1-13 (2018).
- Wang, Z., Lee, S. J., Cheng, H. -. J., Yoo, J. J., Atala, A. 3D bioprinted functional and contractile cardiac tissue constructs. Acta Biomaterialia. 70, 48-56 (2018).
- Miri, A. K., et al. Effective bioprinting resolution in tissue model fabrication. Lab on a Chip. 19 (11), 2019-2037 (2019).
- Todhunter, M. E., et al. Programmed synthesis of three-dimensional tissues. Nature Methods. 12 (10), 975-981 (2015).
- Todhunter, M. E., Weber, R. J., Farlow, J., Jee, N. Y., Gartner, Z. J. Fabrication of 3D microtissue arrays by DNA programmed assembly of cells. Current Protocols in Chemical Biology. 8 (3), 147-178 (2016).
- Csizmar, C. M., Petersburg, J. R., Wagner, C. R. Programming cell-cell interactions through non-genetic membrane engineering. Cell Chemical Biology. 25 (8), 931-940 (2018).
- Weber, R. J., Liang, S. I., Selden, N. S., Desai, T. A., Gartner, Z. J. Efficient targeting of fatty-acid modified oligonucleotides to live cell membranes through stepwise assembly. Biomacromolecules. 15 (12), 4621-4626 (2014).
- Hughes, A. J., et al. Engineered tissue folding by mechanical compaction of the mesenchyme. Developmental Cell. 44 (2), 165-178 (2018).
- Weber, R. J., et al. Rapid organoid reconstitution by chemical micromolding. ACS Biomaterials Science & Engineering. 2 (11), 1851-1855 (2016).
- Scheideler, O. J., et al. Recapitulating complex biological signaling environments using a multiplexed, DNA-patterning approach. Science Advances. 6 (12), (2020).
- Viola, J. M., et al. Guiding cell network assembly using shape-morphing hydrogels. Advanced materials (Deerfield Beach, Fla.). , 2002195 (2020).
- Mohammad, A., Davis, M., Aprelev, A., Ferrone, F. A. Note: Professional grade microfluidics fabricated simply. Review of Scientific Instruments. 87 (10), 1-4 (2016).
- Lee, O. J., Chuah, H. S., Umar, R., Chen, S. K., Yusra, A. F. I. Construction of cost effective homebuilt spin coater for coating amylose-amylopectin thin films. Journal of Fundamental and Applied Sciences. 9 (2), 279 (2018).
- Webb, K., Hlady, V., Tresco, P. A. Relative importance of surface wettability and charged functional groups on NIH 3T3 fibroblast attachment, spreading, and cytoskeletal organization. Journal of Biomedical Materials Research. 41 (3), 422-430 (1998).
- Processing Guidelines for: SU-8 2025, SU-8 2035, SU-8 2050, SU-8 2075. Microchem SU-8 2000 Permanent Expoxy Negative Photoresist Available from: https://kayakuam.com/wp-content/uploads/2019/09/SU-82000DataSheet2025thru2075Ver4.pdf (2019)
- Palte, M. J., Raines, R. T. Interaction of nucleic acids with the glycocalyx. Journal of the American Chemical Society. 134 (14), 6218-6223 (2012).
- McGinnis, C. S., et al. MULTI-seq: sample multiplexing for single-cell RNA sequencing using lipid-tagged indices. Nature Methods. 16 (7), 619-626 (2019).
- Maxfield, F. R., van Meer, G. Cholesterol, the central lipid of mammalian cells. Current Opinion in Cell Biology. 22 (4), 422-429 (2010).
- Luo, J., Yang, H., Song, B. L. Mechanisms and regulation of cholesterol homeostasis. Nature Reviews Molecular Cell Biology. 21 (4), 225-245 (2020).
- Liu, L., Tan, L., Yao, J., Yang, L. Long non-coding RNA MALAT1 regulates cholesterol accumulation in ox-LDL-induced macrophages via the microRNA-17-5p/ABCA1 axis. Molecular Medicine Reports. 21 (4), 1761-1770 (2020).
- Mali, P., Aach, J., Lee, J. H., Levner, D., Nip, L., Church, G. M. Barcoding cells using cell-surface programmable DNA-binding domains. Nature Methods. 10 (5), 403-406 (2013).
- Hsiao, S. C., et al. Direct cell surface modification with DNA for the capture of primary cells and the investigation of myotube formation on defined patterns. Langmuir. 25 (12), 6985-6991 (2009).
- Gartner, Z. J., Bertozzi, C. R. Programmed assembly of 3-dimensional microtissues with defined cellular conductivity. Proceedings of the National Academy of Sciences. (17), 1-5 (2009).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved