Um procedimento simplificado e padronizado para gerar vetores de vírus adeno-associados de alto título e alta qualidade utilizando uma plataforma de fábrica de células
In This Article
Summary
À medida que o campo da terapia gênica continua a evoluir, há uma necessidade crescente de métodos inovadores que possam enfrentar esses desafios. Aqui, é apresentado um método único, que agiliza o processo de geração de vetores AAV de alto rendimento e alta pureza usando uma plataforma de fábrica de células, atendendo aos padrões de qualidade para estudos in vivo .
Abstract
A pesquisa pré-clínica de terapia gênica, particularmente em modelos de roedores e animais de grande porte, requer a produção de vetores AAV com alto rendimento e pureza. As abordagens tradicionais em laboratórios de pesquisa geralmente envolvem o uso extensivo de placas de cultura de células para cultivar células HEK293T, um processo que pode ser trabalhoso e problemático. Aqui, é apresentado um método interno exclusivo, que simplifica esse processo com uma plataforma específica de fábrica de células (ou pilhas de células, CF10). Uma integração de partição bifásica de polietilenoglicol/aquosa com ultracentrifugação de gradiente de iodixanol melhora o rendimento e a pureza dos vetores AAV gerados. A pureza dos vetores AAV é verificada por meio de SDS-PAGE e coloração de prata, enquanto a proporção de partículas cheias e vazias é determinada por microscopia eletrônica de transmissão (TEM). Essa abordagem oferece uma plataforma de fábrica de células eficiente para a produção de vetores AAV em altos rendimentos, juntamente com um método de purificação aprimorado para atender às demandas de qualidade para estudos in vivo .
Introduction
Os vetores de vírus adeno-associados (AAV) tornaram-se uma ferramenta indispensável na pesquisa de terapia gênica, oferecendo uma combinação única de eficácia e segurança para a entrega de genes1. Os métodos tradicionais para gerar AAVs em ambientes de laboratório têm sido fundamentais para o avanço de nossa compreensão e aplicação da terapia gênica2. No entanto, esses métodos, embora fundamentais, exibem certas limitações e desafios, especialmente em termos de rendimento, eficiência de tempo e qualidade dos vetores produzidos, notadamente a proporção de partículas cheias e vazias3.
O procedimento convencional para a produção de AAV envolve principalmente a transfecção de células HEK2934. Esse processo, normalmente conduzido em placas de cultura de células, requer que as células sejam transfectadas com um plasmídeo contendo o gene de interesse junto com o plasmídeo auxiliar e o plasmídeo do capsídeo AAV 5,6. Após a transfecção, as células produzem partículas de AAV, que são então colhidas e purificadas 5,6. O processo de purificação geralmente envolve ultracentrifugação, uma etapa crítica na obtenção de vetores AAV de alta pureza7. A ultracentrifugação, particularmente usando cloreto de césio (CsCl) ou gradiente de iodixanol, é um método padrão para separar partículas de AAV de detritos celulares e outras impurezas8. Esta etapa é crucial para alcançar a pureza e concentração desejadas dos vetores AAV, o que afeta diretamente sua eficácia na entrega do gene8. Apesar de seu uso generalizado, a ultracentrifugação tradicional tem suas desvantagens. Por exemplo, o rendimento dos vetores AAV deste método pode ser variável e muitas vezes baixo, o que representa desafios significativos quando são necessárias grandes quantidades de vetores de alto título, particularmente para estudos in vivo ou modelos animais de grandeporte 9.
Outro aspecto crítico da qualidade do vetor AAV é a proporção de partículas cheias e vazias10. As preparações de AAV geralmente contêm uma mistura dessas partículas; no entanto, apenas as partículas completas contêm o material genético terapêutico. A presença de uma alta proporção de partículas vazias pode reduzir significativamente a eficiência da entrega de genes10. Avaliar e otimizar a proporção de partículas cheias e vazias é, portanto, um parâmetro chave na avaliação da eficácia dos vetores AAV. Os métodos tradicionais, embora capazes de produzir vetores AAV, muitas vezes lutam para controlar essa proporção de forma consistente, levando a variações na potência do vetor10.
Aqui, é apresentado um método único, que agiliza o processo de geração de vetores AAV de alto rendimento e alta pureza usando uma plataforma de fábrica de células livre do uso intensivo de mão-de-obra HEK293T culturas de células em placas de células, integrando partição bifásica de polietilenoglicol/aquosa com ultracentrifugação de gradiente de iodixanol. A pureza do vetor AAV é confirmada por SDS-PAGE e coloração com prata, e a proporção de partículas cheias e vazias é determinada por microscopia eletrônica de transmissão (MET), atendendo aos padrões de qualidade para estudos in vivo 11.
Protocol
Os detalhes dos reagentes, plasmídeos e equipamentos usados no estudo estão listados na Tabela de Materiais. A composição dos buffers usados é fornecida no Arquivo Suplementar 1.
1. Preparação do plasmídeo
- Plasmídeos de transformação (pAAV-GOI, pHelper, pAAV-Cap) em E. coli.
NOTA: Qualquer cepa de E.coli pode ser usada para amplificação de plasmídeo. Para alguns plasmídeos, células competentes especiais, como NEB estável, podem melhorar o rendimento do plasmídeo. Os três plasmídeos usados neste protocolo são pAAV-GOI: pAAV-CMV-GFP, pHelper: pAdDeltaF6 e pAAV-Cap: pAAV-RC6. - Cultivar bactérias em meio LB contendo os antibióticos seletivos apropriados em volume ideal a 37 °C por 16-18 h.
NOTA: Ao usar células estáveis NEB, cultive a 30 ° C por 18-20 h. - Colha DNA de plasmídeo centrifugando a E. coli. meio de cultura a 4000 x g, 4 °C, durante 15 min.
- Despeje cuidadosamente o líquido sobrenadante do frasco da centrífuga em um recipiente de resíduos e purifique o DNA do plasmídeo do pellet com um kit de purificação de plasmídeo livre de endotoxinas em grande escala.
NOTA: Certifique-se de despejá-lo lentamente e evitar respingos. - Meça a concentração e a pureza do DNA usando um espectrofotômetro.
NOTA: Verifique a pureza do DNA verificando a proporção OD260 / OD280 . A proporção para DNA puro é de cerca de 1,8. A concentração de DNA deve estar acima de 1 μg/μL para a etapa posterior de co-transfecção. Faça estoques de glicerol bacteriano adicionando 500 μL da cultura durante a noite a 500 μL de glicerol a 50% em um criovírus e armazene a -80 ° C.
2. Preparando células HEK293T
- Semeie células HEK293T com meio DMEM com alto teor de glicose contendo 10% de FBS em uma fábrica de células de 10 camadas (CF10) e deixe as células crescerem na incubadora durante a noite.
NOTA: As passagens das células 293T devem ser inferiores a 10 para ter a condição ideal para uma produção robusta de AAV. Se possível, não adicione antibióticos aos meios de cultura neste momento. O CF10 tem aproximadamente 42 vezes a área de superfície de crescimento de uma placa de cultura de células de 150 mm. Semear a mesma densidade celular numa placa de cultura de células de 150 mm para permitir a verificação do crescimento celular ao microscópio. Prepare a suspensão de células de 1075 mL, adicione a suspensão de células de 25 mL a um prato de 150 mm e adicione o restante ao CF10. - Verifique a confluência celular no dia seguinte antes da transfecção.
NOTA: As células devem atingir 80% -90% de confluência no momento da transfecção, observando ao microscópio.
3. Transfecção tripla de plasmídeos AAV
- Calcule a quantidade de cada plasmídeo necessária (pAAV-GOI, pHelper, pAAV-sorotype) para ter uma proporção molar de 1,2: 1: 1 com 2,5-5 mg de DNA total por CF10.
NOTA: A razão molar dos três plasmídeos pode ser variável para a eficácia ideal da transfecção. É melhor testá-lo em uma configuração de pequena escala antes de passar para essa configuração CF10. pAAV-CMV-GFP, pAdDeltaF6 e pAAV-RC6 são usados para fazer o vírus AAV6-CMV-GFP como exemplo. A fórmula da calculadora PEI está listada na Tabela 1. - Alíquota de 350 mL de OptiMEM em um frasco estéril de 500 mL.
- Adicione todos os três DNA de plasmídeo ao frasco que contém o Opti-MEM. Misture bem.
- Adicionar 15 ml de solução de polietilenimina (PEI) a 1 mg/ml (proporção de 1:3 μg de ADN para μg de PEI). Agite a mistura OptiMEM/DNA/PEI para cima e para baixo vigorosamente por 30 s.
NOTA: Não há problema em fazer bolhas. - Incube a mistura em temperatura ambiente por 10-15 min.
NOTA: Uma incubação mais longa pode reduzir a eficiência da transfecção. - Adicione a solução OptiMEM/DNA/PEI ao frasco de 1 L contendo 700 mL de DMEM de baixa glicose com 10 mM de HEPES e 2% de FBS. Misture bem.
NOTA: Neste estudo, a baixa glicose no DMEM mostrou melhor produção do vetor AAV após a co-transfecção. A adição de HEPES ajuda a manter as células em melhores condições. Misture girando a garrafa lentamente. Evite criar muitas bolhas. - Retire o CF10 da incubadora e aspire o meio para um recipiente de resíduos.
NOTA: Coloque o CF10 na superfície dentro do exaustor e levante gradualmente um lado para cima, aspire lentamente a mídia sem soltar as células. - Adicione cuidadosamente a mistura transfectante ao CF10. Certifique-se de que todas as dez camadas estejam cobertas com mídia.
NOTA: Adicione 25 mL de mistura transfectante no prato de 150 mm. Monitore as células diariamente até a colheita. Adicione a mistura transfectante restante ao CF10 despejando lentamente. Gire o CF10 com muito cuidado e garanta um volume igual para cada camada. - Devolva o CF10 à incubadora por 72-96 h.
NOTA: Verifique o prato do monitor de 150 mm para decidir quando colher os vetores AAV. Quando as células se desprendem facilmente com uma carga total de AAV, é hora de colher.
4. Colheita de vetores AAV
- Colha o vírus 3-4 dias após a transfecção, agitando o CF10 vigorosamente. Despeje o meio nos tubos cônicos de 250 mL e gire o vírus a 4000 x g por 20 min a 4 ° C.
NOTA: Para o sorotipo AAV6 usado neste protocolo, 80% do AAV permanecerá principalmente ligado ao material celular no pellet. E os 20% de AAV foram secretados na mídia. Essas proporções podem diferir para outros sorotipos de AAV. - Filtre o sobrenadante clarificado com unidade de filtro de 0,45 μm e guarde-o para precipitação.
- Enxágue o CF10 com 500 mL de tampão DPBS 1x e centrifugue a 4000 x g por 20 min a 4 °C.
- Rejeitar o sobrenadante utilizando um sistema de vácuo e uma pipeta de aspiração. Adicionar 20 ml de tampão de lise de AAV por CF10 a -80 °C até à purificação.
NOTA: Transfira o lisado de AAV para um tubo cônico de 50 mL para posterior extração de AAV. - Retire o sobrenadante filtrado, adicione 40% de solução de NaCl PEG-2,5 M para uma concentração final de 8% de PEG e incube em uma câmara fria em um rotador orbital por pelo menos 3 h ou durante a noite.
NOTA: Para 100 mL de sobrenadante, adicione 25 mL de solução de NaCl PEG-2,5 M a 40%. - Precipitar o vírus centrifugando a 4000 x g durante 30 min a 4 °C.
NOTA: Transfira a mistura para tubos cônicos de 250 mL para centrifugação. - Aspire para remover o sobrenadante e adicione 5-10 mL de tampão de ressuspensão AAV HEPES para suspender os pellets. Transfira para um tubo cônico de 50 mL para continuar a purificação a jusante ou armazene-o a -80 °C.
5. Extração de AAV
- Descongele o pellet de vírus em banho-maria a 37 °C por 10-15 min com um shaker.
NOTA: Vortex o lisado AAV para derreter completamente. - Congelar em banho de etanol 100% a -80 °C por 20-30 min.
NOTA: Alternativamente, o ciclo de congelamento pode ser feito com um béquer frio 100% etanol cercado por gelo seco. - Execute congelamento/descongelamento 3-4 vezes e vórtice no meio, se necessário.
NOTA: Este ciclo pode ser pausado na etapa de congelamento. Conservar o lisado de AAV a -80 °C até ao trabalho a jusante. - Descongelar o lisado de AAV (a partir do passo 5.3) e o AAV ressuspenso (do passo 4.7)" num banho-maria a 37 °C durante 10-15 min com um agitador e vórtice.
NOTA: Certifique-se de derreter completamente e misture. - Adicione a nuclease da benzonase (250 unidades / μL) ao lisado de AAV e o AAV ressuspenso para uma concentração final de 50 unidades / mL. Vortex a solução.
- Incubar em banho-maria a 37 °C com agitação durante 30 min.
NOTA: Retire as alíquotas de desoxicolato de sódio a 10% em banho-maria para dar tempo de dissolver, aquecer e misturar bem. - Adicione 10% de desoxicolato de sódio para uma concentração final de 0,5% e incube a 37 °C com um agitador ligado por 30 min.
NOTA: O desoxicolato de sódio foi usado para aumentar a liberação de AAV das células. - Distribua a solução bruta de AAV em tubos de centrífuga de 2 mL e centrifugue a 14.000 x g por 10 min a 4 ° C.
- Transfira o sobrenadante para um tubo cônico de 50 mL.
NOTA: Use uma pipeta de 1 mL para transferir o sobrenadante. Descarte os pellets. - Adicione uma quantidade igual de clorofórmio e extraia AAV por vórtice por 1-2 min.
NOTA: A solução deve tornar-se opaca, branca, semelhante ao leite. - Transfira a solução leitosa para tubos de centrífuga de 2 mL e distribua uniformemente. Centrifugue a 14.000 x g por 10 min a 4 °C.
- Pipetar cuidadosamente a camada rosa superior e transferi-la para um novo tubo cónico de 50 ml.
NOTA: Não perturbe as camadas de clorofórmio/proteína. - Meça o volume final usando uma pipeta. De acordo com a tabela de volume bruta de AAV-PEG-Sulfato (Tabela 2), misture volumes apropriados de 50% (NH4)2SO4 e solução de PEG a 40%. Vórtice por 2 min.
- Transfira a mistura para tubos de centrífuga de 2 mL para distribuir uniformemente. Centrifugue a 14.000 x g por 10 min a 4 °C
- Recolha a camada inferior utilizando uma agulha de 22 G e uma seringa de 3 ml. Colete o AAV em um tubo cônico de 50 mL e armazene-o a 4 ° C para posterior ultracentrifugação com gradientes de iodixanol.
6. Purificação de AAV por ultracentrifugação de gradiente de iodixanol
- Preparar os gradientes de iodixanol de novo antes de carregar o AAV de acordo com o número de tubos de ultracentrifugação utilizados (Quadro 3).
NOTA: O vermelho de fenol foi usado para observar as camadas. - Sobreponha cada solução em um tubo de vedação rápida de ultracentrífuga de polipropileno de topo redondo lentamente usando uma seringa de 10 mL conectada com uma agulha longa puntada de 16 G. Evite bolhas.
- Adicione cuidadosamente até 17 mL de solução de AAV no topo do gradiente com uma seringa de 22 G. Use tampão de diálise AAV para completar o tubo.
NOTA: Adicione a solução AAV carregando gotas contra a parede no tubo da ultracentrífuga. Não perturbe as camadas de gradiente. - Sele os tubos da ultracentrífuga com um selador elétrico.
NOTA: Equilibre os tubos antes de enviá-los para a ultracentrífuga com ±0,2 g de diferença. - Centrifugar a 350.000 x g durante 2 h num rotor Ti70 a 4 °C.
- Remova cuidadosamente os tubos do rotor e coloque-os no rack de tubos da ultracentrífuga.
NOTA: Certifique-se de que os gradientes não sejam perturbados. - Colete as frações AAV seguindo as etapas abaixo:
- Estabilize o tubo em um suporte.
- Perfure os tubos da ultracentrífuga ligeiramente abaixo da interface de 40% a 60% com uma agulha de 19 G conectada a uma seringa de 10 mL.
NOTA: A abertura da agulha deve estar voltada para cima, voltada para o gradiente de 40%. - Faça um furo na parte superior do tubo com uma agulha de 16 G.
- Colete até 5 mL por tubo. Evite coletar a contaminação da proteína na interface de 25% a 40%.
- Repita para cada tubo de ultracentrífuga.
NOTA: Transfira as frações AAV para um tubo cônico de 50 mL.
7. Ultracentrifugação de gradientes de iodixanol de segunda rodada
NOTA: Esta etapa é opcional. Esta etapa é para reduzir a proporção de AAV vazio para um capsídeo AAV completo de maior qualidade.
- Dilua o AAV >1:1 com tampão de diálise AAV.
NOTA: O AA Deve ser diluído em pelo menos 50% para poder ser carregado sobre a camada de 30% de iodixanol. - Cubra cada solução (Tabela 4) em um tubo de ultracentrifugação usando uma agulha puntada de 16 G e coloque lentamente uma seringa de 10 mL. Evite bolhas.
- Adicione cuidadosamente 20 mL de solução diluída de AAV no topo do gradiente com uma seringa de 22 G. Use tampão de diálise AAV para completar o tubo.
- Repita as etapas 6.4 a 6.7.
8. Diálise e concentração de AAV
- Transfira o vírus AAV para o de diálise usando uma nova agulha de 18 G e uma seringa de 10 mL. Injete lentamente o vírus no e remova o ar dele.
- Adicione uma barra de agitação ao copo contendo tampão de diálise AAV e coloque-a em uma placa de agitação.
- Coloque o de diálise no tampão de diálise com uma bóia flutuante. Agitar a 4 °C. Troque 2-3 vezes o tampão de diálise AAV.
NOTA: Use buffer suficiente para permitir que o flutue e execute a troca de buffer. Cubra o copo com papel alumínio. - Usando uma seringa de 10 mL acoplada a uma agulha de 18 G, colete o vírus do para uma unidade de filtro centrífugo.
- Centrifugue a 4.000 x g por 15-30 min a 4 °C.
NOTA: Limpe o AAV com tampão de diálise AAV 2-3 vezes. Concentre o AAV até que ~ 200 μL restantes estejam no topo do filtro. - Colete o AAV concentrado da unidade de filtro. Enxágue o filtro com mais 300 μL de tampão de diálise AAV e transfira-o para o AAV concentrado.
- Filtre o vírus através de um filtro de seringa de 0,22 μm usando uma seringa de tuberculina luer slip de 1 mL. Para garantir a menor quantidade de perda de volume, use a seringa de 10 mL para empurrar o ar através do filtro 2-3 vezes.
- Conservar temporariamente o vírus AAV purificado a 4 °C para titulação.
NOTA: Titular o vírus, alíquota e armazenar a -80 °C dentro de 1 semana.
9. Titulação do vírus AAV
NOTA: A reação em cadeia da polimerase quantitativa TaqMan (qPCR) foi usada para titular o AAV purificado.
- Trate os vetores AAV com DNase I e incube a 37 °C por 30 min, depois incube a 95 °C por 10 min.
NOTA: Como exemplo de reação de 10 μL, 2 μL de amostra de vírus AAV, 1 μL de DNase, 1 μL de tampão DNase e 6 μL H2O são usados. Pode ser realizado em termociclador com tubos de PCR. - Prepare os conjuntos de primers direcionados à região de inserção do AAV.
NOTA: Os alvos podem ser o promotor, o transgene e o repórter na construção AAV. Os primers estão listados na Tabela 5. - Preparar padrões de plasmídeos de ADN (10, 1, 0,1, 0,01, 0,001 e 0,0001 pg/μL) e um controlo negativo (H2O).
- Prepare a mistura principal de qPCR, incluindo primers, de acordo com as instruções do fabricante.
- Colocar os padrões e as amostras em triplicado numa placa PCR. Adicione a mistura de qPCR aos padrões e amostras. Sele a placa e execute a reação qPCR de acordo com as instruções do fabricante.
NOTA: As condições de reação dependem dos materiais/reagentes e do instrumento. Ciclos de PCR rápidos e convencionais são aplicáveis. - Calcule o título do vírus AAV.
NOTA: A concentração da amostra neste protocolo é de 1/10 de diluição das amostras originais. - Aliquotar o vírus AAV em tubos de 1,5 mL e armazenar a 4 °C por até um mês e armazenar a -80 °C a longo prazo.
NOTA: Evite ciclos de congelamento/descongelamento para o armazenamento. Quando usado para experimentos in vivo , não use descongelar duas alíquotas.
10. Controle de qualidade do AAV
NOTA: Os vírus AAV foram caracterizados quanto à pureza pela coloração de prata SDS-PAGE usando um gel SDS-PAGE e corados usando um kit de coloração disponível comercialmente.
- Desnature 3 x 109 vg da amostra de vírus AAV com tampão Laemmli.
NOTA: Use um vírus AAV de referência como controle. O capsídeo completo de referência AAV6-CMV-GFP é usado. - Carregue o AAV desnaturado em um gel SDS-PAGE com gradiente de 4% a 20% e opere a 180 V por 50 min.
- Remova o gel da placa de eletroforese. Pinte o gel com um kit de coloração de prata de acordo com as instruções do fabricante.
- Verifique as proteínas do capsídeo AAV VP1, VP2 e VP3.
NOTA: O vírus AAV puro contém apenas a proteína do capsídeo VP1, VP2 e VP3. Se não for puro, outras bandas de proteína seriam visíveis no gel.
NOTA: A microscopia eletrônica de transmissão (MET) de vírions AAV recombinantes corados negativamente foi realizada para avaliar a integridade morfológica e a relação cheio/vazio. - Pegue uma grade EM com uma pinça e coloque-se no banco com o lado brilhante da grade voltado para cima.
- Pipetar 5 μL de amostra de AAV na grelha e deixá-la secar por evaporação.
NOTA: Dilua o AAV, se necessário. 1012 vg/mL é um título médio. Pode levar de 30 a 60 minutos para secar a grade. - Lave a grelha pipetando, gota a gota, com cerca de 200 μL de H2O na grelha.
- Remova o excesso de água colocando lentamente um papel de cromatografia verticalmente ao lado da grade.
- Pipetar 5 μL de solução de acetato de uranilo a 2% na grade. Incube por 5 min e retire a umidade conforme mencionado acima. Deixe a grade secar.
- Visualize as partículas AAV sob um microscópio eletrônico de transmissão (com ampliação de 50.000 vezes). Os capsídeos virais com genoma viral aparecerão como hexágonos brancos homogêneos, enquanto os capsídeos vazios aparecerão como hexágonos com uma borda branca, mas um centro escuro.
- Conte aleatoriamente pelo menos 100 partículas para determinar a porcentagem aproximada de cheio vs. partículas AAV vazias.
Representative Results
Neste protocolo passo a passo detalhado, uma plataforma padronizada é demonstrada para produzir vírus AAV de alto título e alta qualidade com o CF10 em um ambiente de laboratório de pesquisa em larga escala. Comparado com placas de cultura de células convencionais, o CF10 fornece uma maneira conveniente de cultivar grandes quantidades de células e produzir o vírus AAV (Figura 1). Várias condições de cultura foram testadas para determinar se as células em um ambiente ideal podem promover a produção viral. Um DMEM com baixo teor de glicose suplementado com HEPES 10 mM e FBS 2% apresentou a melhor produção de AAV.
Vários protocolos foram testados para purificar AAVs. A maioria dos procedimentos tem baixo rendimento de vírus e impureza dos capsídeos do AAV. Aqui, um protocolo de purificação revisado foi desenvolvido, combinando o AAV de pellets celulares e meios de cultura (Figura 2). Descobrimos que 80% do AAV estava nas células e outros 20% do AAV estavam nos meios de cultura, que foram secretados pelas células. Ambas as partes do AAV foram tratadas com DNase para remover o DNA livre. O desoxicolato de sódio foi usado para liberar ainda mais o AAV das células. Os AAVs foram então extraídos com extração de clorofórmio seguida de uma partição aquosa bifásica. Essas etapas permitiram que a maioria dos contaminantes de proteínas fosse removida. O AAV permanece solúvel na fase de sulfato de amônio.
Os contaminantes restantes foram removidos com uma ultracentrifugação descontínua com gradiente de iodixanol (Figura 3A). O gradiente também foi útil na remoção dos capsídeos vazios do AAV, especialmente com a segunda rodada de ultracentrifugação com gradiente de iodixanol.
A pureza do vírus AAV foi determinada por coloração de prata. Quando três bandas principais correspondentes à proteína do capsídeo AAV, VP1, VP2 e VP3, com pureza superior a 90%, foram obtidas, o vírus AAV foi adequado para uso in vivo (Figura 3B). A proporção de capsídeo cheio para capsídeo vazio do AAV foi acessada pelo MET (Figura 3C). Apenas um capsídeo completo com uma inserção de transgene permitiria a expressão do transgene no tecido alvo. Uma grande porção do capsídeo vazio também pode induzir uma resposta imune ao capsídeo AAV. Essas verificações de qualidade são necessárias para cada vírus AAV produzido e purificado antes do uso.
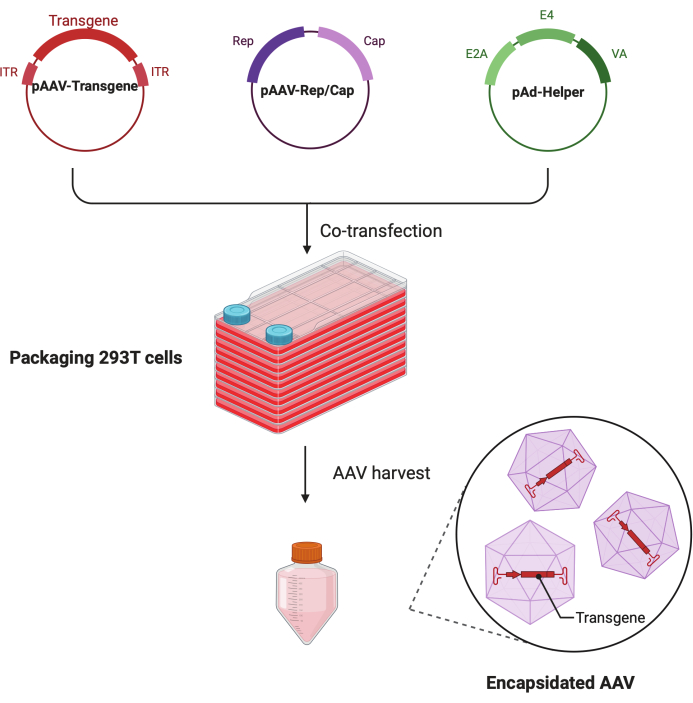
Figura 1: Ilustração esquemática da produção de AAV pelo método de transfecção tripla de células HEK293T. Clique aqui para ver uma versão maior desta figura.
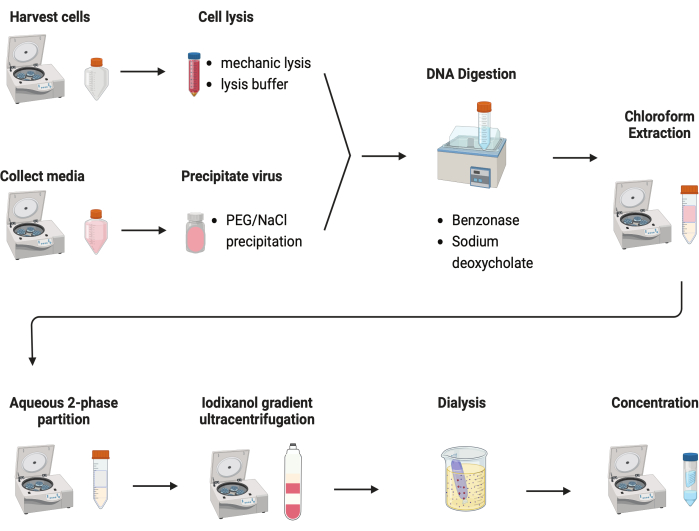
Figura 2: Ilustração esquemática da purificação do AAV. Clique aqui para ver uma versão maior desta figura.
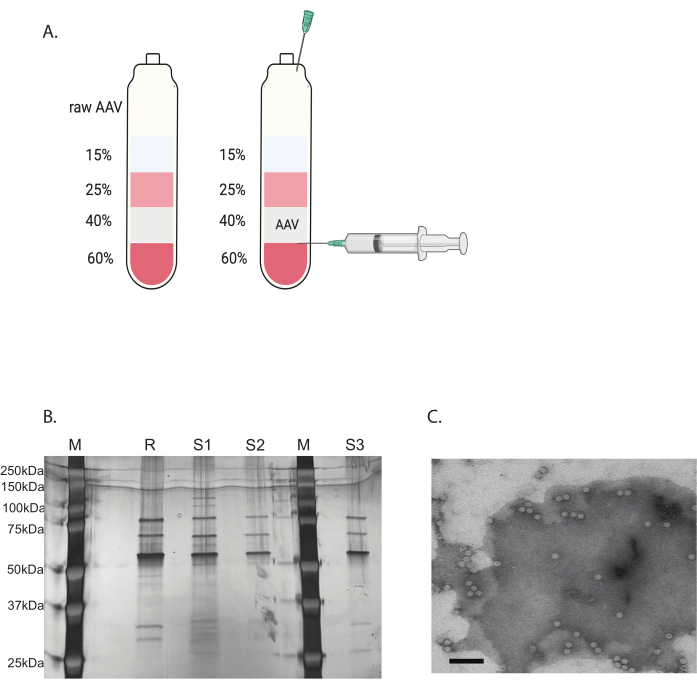
Figura 3: Purificação do AAV por ultracentrifugação com gradiente de iodixanol e verificação da pureza do vírus AAV. (A) Camadas de gradiente de iodixanol e a posição da agulha para a colheita. (B) Gel representativo avaliando o conteúdo e a pureza do capsídeo. M: marcador molecular; R: referência AAV6 capsídeo completo; S1: capsídeo AAVDJ fabricado internamente com uma rodada de ultracentrifugação; S2: capsídeo AAVDJ fabricado internamente com duas rodadas de ultracentrifugação; S3: capsídeo AAV6 fabricado internamente. (C) Imagem de microscopia eletrônica de AAV. Vírus coletado após a purificação. Os capsídeos virais contendo um genoma viral aparecem como hexágonos brancos homogêneos, enquanto os capsídeos vazios aparecem como hexágonos com uma borda branca, mas um centro escuro. Barra de escala: 100 nm. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Calculadora PEI para embalagens AAV. Clique aqui para baixar esta tabela.
Tabela 2: Tabela de volume bruto de AAV-PEG-Sulfato. Clique aqui para baixar esta tabela.
Tabela 3: Preparação do gradiente de iodixanol. Clique aqui para baixar esta tabela.
Tabela 4: Preparação da segunda rodada do gradiente de iodixanol. Clique aqui para baixar esta tabela.
Tabela 5: Primers de titulação AAV. Clique aqui para baixar esta tabela.
Arquivo Suplementar 1: Composições dos buffers usados para o estudo. Clique aqui para baixar este arquivo.
Discussion
Aqui, é introduzido um protocolo tecnicamente avançado para produção em larga escala de vetores AAV de alto título e alta qualidade usando uma plataforma de fábrica de células (CF10), representando uma melhoria significativa em relação aos métodos convencionais de placa de cultura de células. O uso de fábricas de células simplifica o processo de cultivo de grandes volumes de células, facilitando a produção de vírus AAV de forma mais eficiente1. Além disso, otimizando as condições de cultura, particularmente com DMEM de baixa glicose suplementado com HEPES 10 mM e FBS 2%, uma produção viral significativamente aumentada foi confirmada, indicando o papel crucial do ambiente celular no rendimento do vírus.
O protocolo de purificação revisado, que combina AAV de pellets celulares e meios de cultura, aborda o problema comum de baixos rendimentos de vírus e impurezas observados em muitos protocolos existentes. As etapas de extração de clorofórmio e partição aquosa de duas fases removem efetivamente a maioria dos contaminantes de proteínas, com o AAV permanecendo solúvel na fase de sulfato de amônio. A melhoria no rendimento e na pureza dos vetores AAV usando o PEG / partição bifásica aquosa combinada com ultracentrifugação de gradiente de iodixanol, em oposição aos métodos tradicionais de ultracentrifugação de gradiente, pode ser atribuída à separação inicial aprimorada com PEG / partição bifásica aquosa, pureza refinada com ultracentrifugação de gradiente de iodixanol e redução na copurificação de contaminantes12. Primeiro, a introdução de PEG/partição bifásica aquosa antes da ultracentrifugação melhora significativamente a separação inicial das partículas de AAV dos detritos celulares e outros contaminantes. O PEG, um polímero de alto peso molecular, quando misturado com uma solução aquosa, cria duas fases distintas13. Os vetores AAV têm uma propensão a particionar preferencialmente em uma dessas fases (comumente a fase rica em PEG), enquanto muitos contaminantes e impurezas são particionados na outra13. Essa partição seletiva concentra efetivamente as partículas de AAV e remove uma porção substancial de impurezas mesmo antes da ultracentrifugação, aumentando assim o rendimento e reduzindo a carga de contaminantes que entra na etapa de ultracentrifugação13. Em segundo lugar, a ultracentrifugação com gradiente de iodixanol refina ainda mais a pureza dos vetores AAV. O iodixanol, um meio gradiente iso-osmolar não iônico, permite uma separação mais suave e controlada em comparação com os gradientes tradicionais de CsCl14. Nesse gradiente, as partículas AAV migram para uma posição no gradiente que corresponde à sua densidade de empuxo14. É importante ressaltar que esse processo é eficaz na separação de capsídeos AAV completos (contendo a carga genética) de capsídeos vazios (sem material genético), que é um determinante crucial da qualidade do vetor. A natureza iso-osmolar do iodixanol também preserva a integridade dos capsídeos do AAV melhor do que agentes hiperosmolares como o CsCl, potencialmente levando a maiores rendimentos de vetores funcionais intactos14. Finalmente, os métodos tradicionais de ultracentrifugação, especialmente aqueles que usam gradientes de CsCl, às vezes podem co-purificar contaminantes que têm densidades flutuantes semelhantes aos vetores AAV15. Ao usar a partição PEG como etapa preliminar, a carga de tais contaminantes é bastante reduzida antes da ultracentrifugação13. Essa redução na carga de contaminantes significa que o gradiente de iodixanol pode funcionar de forma mais eficaz e seletiva na purificação de vetores AAV, levando a uma maior pureza15.
A pureza e a qualidade dos vetores AAV são rigorosamente avaliadas por meio de coloração com prata e TEM11. A observação de três bandas principais correspondentes às proteínas do capsídeo AAV VP1, VP2 e VP3, com pureza superior a 90%, indica a adequação desses vetores AAV para uso in vivo . A análise TEM para determinar a proporção de capsídeos cheios e vazios é particularmente crucial, pois uma alta proporção de capsídeos vazios pode levar à redução da eficiência de entrega de genes e potenciais respostas imunes11. Essa verificação de qualidade, embora essencial, aumenta a complexidade processual e pode exigir conhecimento técnico adicional.
Em conclusão, o protocolo oferece avanços técnicos significativos na produção de vetores AAV, particularmente em termos de escalabilidade e pureza. No entanto, as complexidades associadas ao processo de purificação e a necessidade de equipamentos e conhecimentos especializados ainda podem ser uma limitação menor para sua aplicação em determinados ambientes de pesquisa. Um maior refinamento e simplificação dessas técnicas poderia tornar essa abordagem mais acessível e amplamente aplicável no campo da pesquisa em terapia genética.
Disclosures
Os autores declaram que a pesquisa foi conduzida na ausência de quaisquer relações comerciais ou financeiras que pudessem ser interpretadas como um potencial conflito de interesses.
Acknowledgements
TZ projetou os experimentos. TZ, VD, SB e JP realizaram os experimentos. TZ e VD geraram dados e analisaram os dados. TZ e YX escreveram o manuscrito. TZ e GG revisaram o manuscrito. Este trabalho foi apoiado pelo Hospital Infantil UPMC de Pittsburgh.
Materials
| Name | Company | Catalog Number | Comments |
| 293T/17 cells | ATTC | CRL-11268 | |
| (NH4)2SO4 | Millipore Sigma | 1.01217.1000 | |
| 0.5 M EDTA | MilliporeSigma | 324506-100ml | |
| 1 mL Henke-Ject syringe | Fisher Scientific | 14-817-211 | |
| 10% pluronic F68 solution | Fisher Scientific | 24-040-032 | |
| 10x Tris/Glycine/SDS Buffer | Biorad | 1610732 | |
| 1M HEPES | Fisher Scientific | 15-630-080 | |
| 2% Uranyl Acetate Solution | Electron Microscopy Sciences | 22400-2 | |
| 4%–20% Precast Protein Gels | biorad | 4561094 | |
| 40% PEG solution | Sigma | P1458-50ML | |
| AAV6 reference full capsids | Charles River Laboratories | RS-AAV6-FL | |
| Accutase Cell Detachment Solution | Fisher Scientific | A6964-100ML | |
| Benzonase | Sigma | E1014-25KU | |
| BioLite Cell Culture Treated Dishes 150 mm | Fisher Scientific | 12-556-003 | |
| Centrifugal Filter Unit | MilliporeSigma | UFC905024 | |
| Corning PES Syringe Filters | Fisher Scientific | 09-754-29 | |
| Dialysis Cassettes, 10 K MWCO | Fisher Scientific | PI66810 | |
| Disposable PES Filter Units 1 L 0.2 µm | Fisher Scientific | FB12566506 | |
| Disposable PES Filter Units 1 L 0.45 µm | Fisher Scientific | FB12566507 | |
| Disposable PES Filter Units 500 mL 0.2 µm | Fisher Scientific | FB12566504 | |
| DMEM high glucose | Fisher Scientific | 10-569-044 | |
| DMEM low glucose | Fisher Scientific | 10567022 | |
| DNase | NEB | M0303S | |
| DPBS 1x | Fisher Scientific | 14-190-250 | |
| Fetal Bovin Serum (FBS) | Biowest | S1620 | |
| Formvar/Carbon 300 Mesh, Cu | Electron Microscopy Sciences | FCF300-Cu-50 | |
| glycerol | Sigma | G5516-1L | |
| KCl | Sigma | P9541-500G | |
| LB agar | Sigma | L2897-250G | |
| LB broth | Fisher Scientific | BP9732-500 | |
| MgCL2·6H2O | Sigma | M9272-100G | |
| NEB stable competent cells | NEB | C3040H | |
| Nest Biofactory 10 chamber | MidSci | 771302 | |
| NucleoBond Xtra Maxi EF | Macherey-Nagel | 740424 | |
| Opti-MEM | Fisher Scientific | 31-985-088 | |
| OptiPrep Density Gradient Medium | Millipore Sigma | D1556-250ml | |
| pAAV-CMV-GFP | Addgene | 105530 | |
| pAAV-DJ | Cell BioLab | VPK-420-DJ | |
| pAAV-RC6 | Cell BioLab | VPK-426 | |
| pAdDeltaF6 | Addgene | 112867 | |
| PEG 8000 | Promega | V3011 | |
| PEI Max | Polysciences, Inc | 49553-93-7 | |
| Pen-Strep | Fisher Scientific | 15-140-163 | |
| Phenol red | Millipore Sigma | 1.07242.0100 | |
| Pierce Silver Stain Kit | Thermo Fisher Scientific | 24612 | |
| QuickSeal tube | Fisher Scientific | NC9144589 | |
| Sodium Chloride | Sigma | 1162245000 | |
| sodium deoxycholate | Millipore Sigma | D6750-100G | |
| Taqman Fast Advanced Master Mix | Thermo Fisher Scientific | 4444557 | |
| Type 70 Ti Fixed-Angle Titanium Rotor | Beckman Coulter | 337922 | |
| Western Blotting Substrate | ThermoFisher | 32209 |
References
- Arjomandnejad, M., Dasgupta, I., Flotte, T. R., Keeler, A. M. Immunogenicity of recombinant adeno-associated virus (AAV) vectors for gene transfer. BioDrugs. 37 (3), 311-329 (2023).
- Liu, Y., Siriwon, N., A Rohrs, J., Wang, P. Generation of targeted adeno-associated virus (AAV) vectors for human gene therapy. Curr Pharm Des. 21 (22), 3248-3256 (2015).
- Bilal, A. S., et al. Optimization of large-scale Adeno-Associated Virus (AAV) production. Curr Protoc. 3 (5), e757 (2023).
- Rashnonejad, A., Chermahini, G. A., Li, S., Ozkinay, F., Gao, G. Large-scale production of adeno-associated viral vector serotype-9 carrying the human survival motor neuron gene. Mol Biotechnol. 58, 30-36 (2016).
- Challis, R. C., et al. Systemic AAV vectors for widespread and targeted gene delivery in rodents. Nat Protoc. 14 (2), 379-414 (2019).
- Challis, R. C., et al. Publisher Correction: Systemic AAV vectors for widespread and targeted gene delivery in rodents. Nat Protoc. 14 (8), 2597-2597 (2019).
- Mueller, C., Ratner, D., Zhong, L., Esteves-Sena, M., Gao, G. Production and discovery of novel recombinant adeno-associated viral vectors. Curr Protoc Microbiol. 26 (1), 14 (2012).
- Guo, P., Wiersch, J., Xiao, X., Gittes, G. Simplified purification of AAV and delivery to the pancreas by intraductal administration. Methods Mol Biol. 1950, 373-387 (2019).
- Berns, K. I., Srivastava, A. Next generation of adeno-associated virus vectors for gene therapy for human liver diseases. Gastroenterol Clin North Am. 48 (2), 319-330 (2019).
- Khasa, H., Kilby, G., Chen, X., Wang, C. Analytical band centrifugation for the separation and quantification of empty and full AAV particles. Mol Ther Methods Clin Dev. 21, 585-591 (2021).
- Chen, H. Comparative observation of the recombinant adeno-associated virus 2 using transmission electron microscopy and atomic force microscopy. Microsc Microanal. 13 (5), 384-389 (2007).
- Burnham, B., et al. Analytical ultracentrifugation as an approach to characterize recombinant adeno-associated viral vectors. Hum Gene Ther Methods. 26 (6), 228-242 (2015).
- Kato, M., et al. In situ-formable, dynamic crosslinked poly (ethylene glycol) carrier for localized adeno-associated virus infection and reduced off-target effects. Commun Biol. 6 (1), 508 (2023).
- Sena-Esteves, M., Gao, G. Enrichment of fully packaged virions in column-purified recombinant adeno-associated virus (rAAV) preparations by iodixanol gradient centrifugation followed by anion-exchange column chromatography. Cold Spring Harb Protoc. 2020 (2), 095638 (2020).
- Matsumoto, M., Wangelin, J. R., Murphy, M. L. Purification of avian encephalomyelitis virus by ultracentrifugation in a nonlinear cesium chloride gradient. Avian Dis. 22 (3), 496-502 (1978).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved