Method Article
نمذجة البنية الرباعية من خلال قياس الطيف الكتلي المتقاطع الكيميائي: توسيع تقارير TX-MS Jupyter
In This Article
Summary
ينشئ قياس الطيف الكتلي المستهدف المتقاطع نماذج بنية البروتين الرباعية باستخدام بيانات قياس الطيف الكتلي التي تم الحصول عليها باستخدام ما يصل إلى ثلاثة بروتوكولات اكتساب مختلفة. عند التنفيذ كسير عمل مبسط على خادم الويب Cheetah-MS ، يتم الإبلاغ عن النتائج في دفتر ملاحظات Jupyter. هنا ، نوضح الجوانب الفنية لكيفية توسيع Jupyter Notebook لإجراء تحليل أكثر تعمقا.
Abstract
يمكن أن تكون التفاعلات بين البروتين والبروتين صعبة الدراسة ولكنها توفر رؤى حول كيفية عمل الأنظمة البيولوجية. يعمل قياس الطيف الكتلي المستهدف المتقاطع (TX-MS) ، وهو طريقة تجمع بين نمذجة بنية البروتين الرباعية وقياس الطيف الكتلي الكيميائي المتقاطع ، على إنشاء نماذج بنية عالية الدقة باستخدام البيانات التي تم الحصول عليها من عينات معقدة وغير مجزأة. هذا يزيل واحدة من العقبات الرئيسية أمام تحليل بنية البروتين المعقدة لأن البروتينات ذات الأهمية لم تعد بحاجة إلى تنقيتها بكميات كبيرة. تم تطوير خادم الويب Cheetah-MS لجعل النسخة المبسطة من البروتوكول أكثر سهولة للمجتمع. بالنظر إلى بيانات MS / MS جنبا إلى جنب ، يقوم Cheetah-MS بإنشاء دفتر ملاحظات Jupyter ، وهو تقرير رسومي يلخص أهم نتائج التحليل. يمكن أن يؤدي توسيع Jupyter Notebook إلى الحصول على رؤى أكثر تعمقا وفهم أفضل للنموذج وبيانات قياس الطيف الكتلي التي تدعمه. يوضح البروتوكول التقني المعروض هنا بعض الامتدادات الأكثر شيوعا ويشرح المعلومات التي يمكن الحصول عليها. وهو يحتوي على كتل للمساعدة في تحليل بيانات اكتساب MS / MS جنبا إلى جنب والتأثير العام ل XLs المكتشفة على النماذج الرباعية المبلغ عنها. يمكن تطبيق نتيجة هذه التحليلات على النماذج الهيكلية المضمنة في دفتر الملاحظات باستخدام NGLView.
Introduction
تدعم التفاعلات بين البروتين والبروتين بنية ووظيفة الأنظمة البيولوجية. يمكن أن يوفر الوصول إلى الهياكل الرباعية للبروتينات رؤى حول كيفية تفاعل بروتينين أو أكثر لتشكيل هياكل عالية الترتيب. ومما يؤسف له أن الحصول على هياكل رباعية لا يزال يشكل تحديا؛ وينعكس هذا في العدد الصغير نسبيا من إدخالات بنك بيانات البروتين (PDB)1 التي تحتوي على أكثر من بولي ببتيد واحد. يمكن دراسة التفاعلات بين البروتين والبروتين باستخدام تقنيات مثل علم البلورات بالأشعة السينية والرنين المغناطيسي النووي و cryo-EM ، ولكن الحصول على كمية كافية من البروتين النقي في ظل الظروف التي يمكن فيها تطبيق الطرق يمكن أن يستغرق وقتا طويلا.
تم تطوير قياس الطيف الكتلي الكيميائي المتقاطع للحصول على بيانات تجريبية عن تفاعلات البروتين والبروتين مع قيود أقل على إعداد العينات حيث يمكن استخدام مطياف الكتلة للحصول على بيانات عن عينات معقدة بشكل تعسفي2،3،4،5،6،7،8،9 . ومع ذلك، فإن الطبيعة التوافقية لتحليل البيانات والعدد الصغير نسبيا من الببتيدات المترابطة تتطلب تجزئة العينات قبل التحليل. لمعالجة هذا القصور ، قمنا بتطوير TX-MS ، وهي طريقة تجمع بين النمذجة الحسابية وقياس الطيف الكتلي الكيميائي المتقاطع10. يمكن استخدام TX-MS على عينات معقدة بشكل تعسفي وهو أكثر حساسية بكثير مقارنة بالطرق السابقة10. وهو يحقق ذلك عن طريق تسجيل جميع البيانات المرتبطة بتفاعل معين بين البروتين والبروتين كمجموعة بدلا من تفسير كل طيف MS بشكل مستقل. يستخدم TX-MS أيضا ما يصل إلى ثلاثة بروتوكولات مختلفة لاكتساب MS: MS1 عالي الدقة (hrMS1) ، والاستحواذ المعتمد على البيانات (DDA) ، والاستحواذ المستقل عن البيانات (DIA) ، مما يوفر فرصا لتحديد الببتيد المتقاطع من خلال الجمع بين ملاحظات متعددة. سير العمل الحسابي TX-MS معقد لعدة أسباب. أولا ، يعتمد على برامج تحليل MS متعددة11،12،13 لإنشاء نماذج بنية البروتين14،15. ثانيا ، يمكن أن تكون كمية البيانات كبيرة. ثالثا ، يمكن أن تستهلك خطوة النمذجة كميات كبيرة من قوة معالجة الكمبيوتر.
وبالتالي ، من الأفضل استخدام TX-MS كسير عمل حسابي تلقائي ومبسط من خلال خادم الويب Cheetah-MS16 الذي يعمل على البنى التحتية الحسابية الكبيرة مثل سحب الكمبيوتر أو المجموعات. لتسهيل تفسير النتائج ، أنتجنا دفتر Jupyter Notebook17 التفاعلي. هنا ، نوضح كيف يمكن توسيع تقرير Jupyter Notebook لتقديم تحليل أكثر تعمقا لنتيجة معينة.
Protocol
1. إرسال سير العمل في https://txms.org.
- انتقل إلى https://txms.org وانقر فوق "استخدام الفهد-MS."
- لإرسال سير العمل، تحتاج إلى توفير ملفين PDB وملف MS/MS mzML أو MGF واحد. يمكنك أيضا النقر فوق "تحميل عينة البيانات" لرؤية الإصدار التجريبي من سير العمل.
ملاحظة: يرجى الاطلاع على الصفحة اليدوية لخادم الويب للحصول على معلومات مفصلة حول كيفية إرسال وظيفة. يدعم خادم الويب مختلف وكلاء الوصلات المتقاطعة غير القابلة للانقسام ، وما يصل إلى 12 تعديلا بعد الترجمة (PTMs) ، وخيارات تتعلق بالنمذجة الحسابية وتحليل بيانات MS. تم تصميم أزرار المساعدة الصغيرة أيضا على صفحة الإرسال لعرض مزيد من المعلومات حول كل خيار.
2. تشغيل الفهد-MS.
ملاحظة: تحويل التنسيقات الخاصة بالمورد إلى mzML أو MGF باستخدام برنامج ProteoWizard MSConvert19.
- قم بتحميل بيانات MS إلى https://txms.org. ثم انقر فوق "اختيار ملف" وحدد بيانات MS ، والتي يجب أن تكون في تنسيقات بيانات mzML / MGF18.
ملاحظة: تتوفر أمثلة على البيانات على https://txms.org. ويمكن أيضا الوصول إلى هذه البيانات مباشرة من خلال zenodo.org، DOI 10.5281/zenodo.3361621. - قم بتحميل ملفين PDB إلى https://txms.org. انقر فوق "اختيار ملف" وحدد ملفات PDB لتحميلها.
ملاحظة: في حالة عدم وجود هياكل تجريبية، قم بإنشاء نماذج باستخدام، على سبيل المثال، SWISS-MODEL 20 إذا كانت الهياكل المتجانسة متوفرة، أو trRosetta21,22 أو Robetta 23,24 خوادم الويب لتنبؤات بنية de novo. - إرسال سير عمل جديد. انقر فوق "إرسال" لتلقي علامة معرف الوظيفة. ثم اتبع النموذج إلى قسم النتائج باستخدام هذه العلامة.
ملاحظة: تستغرق حساب النتيجة وقتا، لذا يرجى الانتظار حتى ينتهي سير العمل، وتخزين علامة معرف المهمة للعودة إلى صفحة النتائج. يتم إجراء الحساب على البنية التحتية للحساب عن بعد. إذا كنت ترغب في تشغيل TX-MS محليا ، فيرجى الرجوع إلى Hauri et al.10. - افحص تقرير Jupyter Notebook باستخدام العارض عبر الإنترنت. بعد ذلك، مرر لأسفل إلى "إبلاغ" في قسم النتائج باستخدام علامة معرف الوظيفة.
3. تثبيت JupyterHub.
- قم بتثبيت عامل الرصيف وفقا للتعليمات في https://docs.docker.com/install/.
- قم بتنزيل حاوية رصيف JupyterHub باستخدام ملحق Jupyter openBIS25. الأمر العام هو "docker pull malmstroem / jove:latest" ، ولكن قد يختلف على منصات أخرى.
ملاحظة: للاطلاع على مناقشة عامة حول كيفية تنزيل الحاويات، يرجى الرجوع إلى https://www.docker.com/get-started. من الممكن أيضا تنزيل الحاوية من zenodo.org ، DOI 10.5281 / zenodo.3361621.
ملاحظة: يتوفر رمز مصدر ملحق Jupyter openBIS هنا: https://pypi.org/project/jupyter-openbis-extension/. - بدء تشغيل حاوية عامل الرصيف: تشغيل عامل الرصيف -p 8178:8000 malmstroem / jove:latest.
ملاحظة: المنفذ الذي يستخدمه JupyterHub افتراضيا هو 8000. هذا المنفذ قابل للتكوين ، ويجب ضبط الأوامر أعلاه وفقا لذلك إذا تم تغييرها. المنفذ 8178 هو خيار تعسفي ويمكن تغييره. يجب تعديل عناوين URL النموذجية الواردة أدناه وفقا لذلك. - انتقل إلى العنوان التالي: http://127.0.0.1:8178. قم بتسجيل الدخول باستخدام اسم المستخدم "المستخدم" وكلمة المرور "المستخدم".
ملاحظة: العنوان http://127.0.0.1 يعني أن حاوية عامل الرصيف قيد التشغيل على الكمبيوتر المحلي. إذا تم تشغيل حاوية عامل الرصيف على خادم، فاستخدم عنوان IP أو عنوان URL الخاص بالخادم (على سبيل المثال، https://example.com). تعتمد حاوية عامل الرصيف على Ubuntu Bionic 18.04 و JupyterHub 0.9.6 وامتداد Jupyter openBIS 0.2. من الممكن تثبيت هذا في أنظمة التشغيل الأخرى ، ولكن لم يتم اختبار ذلك.
4. قم بتنزيل التقرير.
- إنشاء دفتر ملاحظات جديد بالنقر فوق جديد| Python 3 باستخدام القائمة الموجودة بالقرب من الجزء العلوي الأيمن من الصفحة. سيؤدي ذلك إلى فتح علامة تبويب جديدة تحتوي على دفتر ملاحظات يسمى Untitled (أو شيء مشابه).
- انقر فوق "تكوين اتصالات openBIS" في قائمة أدوات Jupyter.
- املأ الاسم: txms. عنوان URL: https://txms.org; المستخدم: ضيف. كلمة المرور: guestpasswd.
- انقر فوق "اتصال".
- اختر الاتصال الجديد وانقر فوق "اختر اتصال."
- ابحث عن قالب التقرير (على سبيل المثال، /CHEETAH/WF70) وانقر فوق تنزيل.
ملاحظة: تحتاج إلى ضبط قالب التقرير استنادا إلى النتائج والتقرير الذي حصلت عليه من تشغيل وظيفتك على خادم الويب Cheetah-MS. - أعد تشغيل التقرير بالنقر فوق | الخلية تشغيل الكل.
5. تمديد التقرير.
- إضافة خلية جديدة في الأسفل: | الخلية تدرج أدناه.
- اكتب الرمز المطلوب. على سبيل المثال، يرجى الاطلاع على قسم النتائج التمثيلية أدناه.
- قم بتنفيذ الخلية عن طريق الضغط على "Shift-Enter".
النتائج
يوفر TX-MS مخرجات هيكلية مدعومة بقيود تجريبية مشتقة من MS. وهو يعمل من خلال الجمع بين أنواع مختلفة من الحصول على بيانات MS مع النمذجة الحسابية. لذلك ، من المفيد تحليل كل بيانات MS بشكل منفصل وتوفير تصور لبنية الإخراج. تحتوي البيانات التكميلية 1 على مثال دفتر ملاحظات يمكنه تحليل بيانات DDA و DIA المنتجة كمخرجات TX-MS. يمكن للمستخدمين اختيار XL للاهتمام. من خلال تشغيل دفتر الملاحظات ، سيتم عرض طيف MS2 من XL حيث تساعد الألوان المختلفة على التمييز بين الشظايا المتعلقة بالببتيد الأول والببتيد الثاني وأيونات الشظايا التوافقية. يمكن أيضا تعيين XL إلى الهيكل باستخدام أداة NGLView المضمنة في دفتر ملاحظات Jupyter.
يمكن أن تساعد خلية أخرى في دفتر الملاحظات هذا المستخدمين على تحليل بيانات DIA وتصورها. ومع ذلك ، فإن تصور بيانات DIA أكثر صعوبة لأن البيانات التي تم تحليلها تحتاج إلى إعدادها بالتنسيق الصحيح.
يوضح الشكل 1 مثالا على بنية M1 والألبومين مع تعيين أعلى XLs على الهيكل. حصلت TX-MS على جميع XLs بعد تحليل بيانات hrMS1 و DDA و DIA ، وقدم بروتوكول RosettaDock النماذج الحسابية.
نظرا لأن هذا التقرير عبارة عن دفتر ملاحظات Jupyter ، يمكن إضافة أي رمز Python صالح إلى خلايا دفتر الملاحظات الجديدة. على سبيل المثال، ستقوم التعليمة البرمجية أدناه بإنشاء رسم بياني فوق عدد MS2، مما يشير إلى مدى دعم كل ارتباط متقاطع بواسطة البيانات الأساسية.
استيراد seaborn كما sns
sns.distplot (ms2 ['count']) ؛
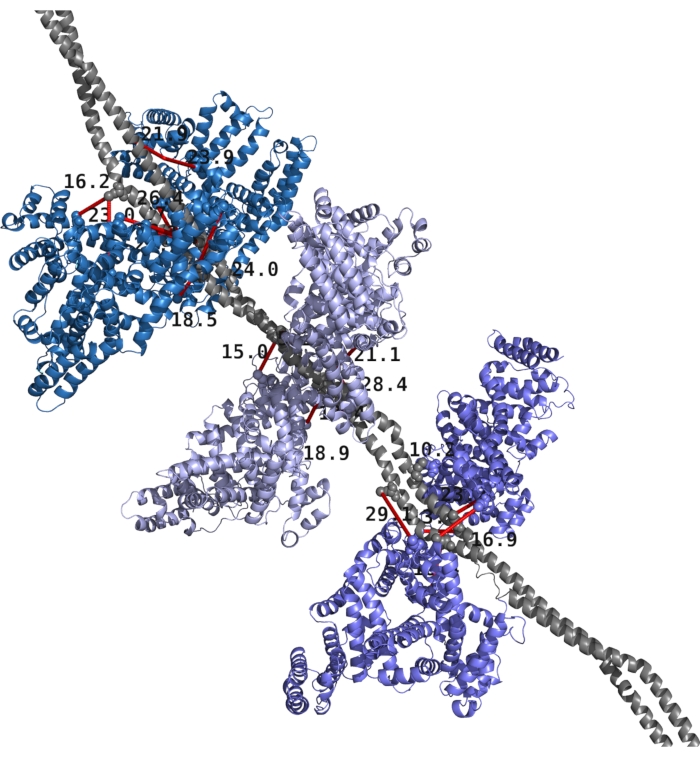
الشكل 1: النموذج الهيكلي لبروتين العقدية المقيحة M1 والألبومين البشري مع تعيين XLs على الهيكل. يظهر بروتين M1 باللون الرمادي ويشكل متجانسا. يتم تقديم جزيئات الألبومين الستة كأزواج في ظلال مختلفة من اللون الأزرق. يتم إعطاء الروابط المتقاطعة والمسافات باللون الأحمر مع نص أسود. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
ملف تكميلي. بيانات دفتر ملاحظات Jupyter. يرجى النقر هنا لتنزيل هذا الملف.
Discussion
غالبا ما تكون مهام سير العمل الحسابية الحديثة معقدة ، مع أدوات متعددة من العديد من البائعين المختلفين ، والاعتماد المتبادل المعقد ، وأحجام البيانات العالية ، والنتائج متعددة الأوجه. ونتيجة لذلك، أصبح من الصعب على نحو متزايد توثيق جميع الخطوات المطلوبة للحصول على نتيجة بدقة مما يجعل من الصعب استنساخ النتيجة المعطاة. هنا ، نعرض استراتيجية عامة تجمع بين أتمتة وسهولة سير العمل الآلي الذي ينتج تقريرا عاما ، مع المرونة في تخصيص التقرير بطريقة قابلة للتكرار.
ويلزم الوفاء بثلاثة متطلبات لكي يعمل البروتوكول: أولا، تحتاج البروتينات المختارة للتحليل إلى التفاعل بطريقة تمكن تجربة الربط المتبادل الكيميائي من إنتاج أنواع متقاطعة بتركيز عال بما فيه الكفاية ليتم اكتشافها بواسطة مطياف الكتلة؛ وثانيا، ينبغي أن تتفاعل البروتينات المختارة للتحليل بطريقة تمكن تجربة الربط المتبادل الكيميائي من إنتاج أنواع مترابطة بتركيز عال بما فيه الكفاية بحيث يمكن أن يكتشفها مطياف الكتلة؛ وثانيا، ينبغي أن تتفاعل البروتينات المختارة للتحليل بطريقة تمكن تجربة الربط المتبادل الكيميائية من إنتاج أنواع مترابطة بتركيز عال بما فيه الكفاية بحيث يمكن كشفها بواسطة مطياف الكتلة؛ وثانيا، ينبغي أن تتفاعل البروتينات المختارة للتحليل بطريقة تمكن تجربة الربط المتبادل الكيميائي من إنتاج أنواع مترابطة بتركيز عال بما فيه الكفاية بحيث يمكن كشف تحتوي أجهزة قياس الطيف الكتلي المختلفة على مستويات مختلفة من الكشف وتعتمد أيضا على بروتوكول الاكتساب بالإضافة إلى اختيار الكاشف المتبادل. يسمح الإصدار الحالي من بروتوكول TX-MS فقط ب DSS ، وهو كاشف ربط متجانس بين ليسين وليسين ومتعدد الوظائف. ومع ذلك ، فإن هذا القيد يرجع في المقام الأول إلى احتمال أن خطوة التعلم الآلي ستحتاج إلى تعديل للكواشف الأخرى. تم تحسين هذا القيد في خادم الويب Cheetah-MS حيث يمكن النظر في كاشفين آخرين متقاطعين ، ولكن الثلاثة كلها كواشف غير قابلة للانقسام. ثانيا ، يحتاج البروتينان إما إلى بنية محددة تجريبيا أو أن يتم نمذجتهما باستخدام تقنيات النمذجة المقارنة أو تقنيات de novo . لا يمكن نمذجة جميع البروتينات ، ولكن مزيجا من البرامج المحسنة والترسب المستمر للهياكل التجريبية في PDB يوسع عدد البروتينات التي يمكن نمذجتها. ثالثا ، يجب أن تظل البروتينات المتفاعلة متشابهة بما فيه الكفاية في حالاتها المرتبطة وغير المرتبطة بحيث يمكن لخوارزميات الالتحام المستخدمة من قبل TX-MS و Cheetah-MS إنشاء هياكل رباعية ذات جودة كافية لتمكين التسجيل. هذا الشرط غامض نسبيا ، حيث أن الجودة المقبولة تعتمد بشكل كبير على النظام ، حيث تكون البروتينات الأصغر ذات البنية المعروفة أسهل عموما في المقارنة من البروتينات الأكبر ذات البنية غير المعروفة.
في حالة وجود نتيجة سلبية ، تحقق أولا من أن TX-MS وجد روابط داخلية ، روابط متقاطعة بين المخلفات التي تشكل جزءا من نفس سلسلة polypeptide. إذا لم يتم اكتشاف أي منها ، فإن التفسير الأكثر ترجيحا هو أن هناك خطأ ما حدث في إعداد العينة أو الحصول على البيانات. إذا كانت قيود المسافة المتعددة لا تدعم النماذج، فقم بفحص النماذج بصريا للتأكد من أن التشكيل مدعوم ببقايا متقاطعة. لا توجد طريقة واضحة لمحور أحد الجهات الفاعلة دون تعطيل رابط متقاطع واحد على الأقل. إذا كانت هناك روابط متقاطعة أطول من المسافة المسموح بها للكاشف المتقاطع المحدد ، فحاول تحسين نمذجة الجهات الفاعلة البينية من خلال دمج بيانات الربط المتبادل.
من الممكن استخدام تطبيقات برمجية بديلة لتحقيق نتائج مكافئة بشرط أن تكون حساسية البرنامج المختار قابلة للمقارنة مع حساسية TX-MS. على سبيل المثال ، هناك إصدارات عبر الإنترنت من RosettaDock و HADDOCK وغيرها. من الممكن أيضا تحليل بيانات الربط الكيميائي من خلال xQuest / xProphet 5,6 و plink7 و SIM-XL26.
نحن نطبق باستمرار TX-MS و Cheetah-MS على المشاريع الجديدة27،28،29 ، وبالتالي تحسين التقارير التي تنتجها هذه الأساليب للسماح بتحليل أكثر تفصيلا للنتائج دون جعل التقارير أكبر.
Disclosures
ليس لدى المؤلفين ما يكشفون عنه.
Acknowledgements
تم دعم هذا العمل من قبل مؤسسة كنوت وأليس والنبرغ (رقم المنحة 2016.0023) والمؤسسة الوطنية السويسرية للعلوم (رقم المنحة. P2ZHP3_191289). بالإضافة إلى ذلك ، نشكر S3IT ، جامعة زيورخ ، على بنيتها التحتية الحاسوبية ودعمها الفني.
Materials
| Name | Company | Catalog Number | Comments |
| Two Protein DataBank files of the proteins of interest. | N/A | N/A | Example files available on txms.org and zenodo.org, DOI 10.5281/zenodo.3361621 |
| An mzML data file acquired on a sample where the proteins of interest were crosslinked. | N/A | N/A | Example files available on txms.org or zenodo.org, DOI 10.5281/zenodo.3361621 |
References
- Berman, H. M., et al. The Protein Data Bank. Acta Crystallographica Section D: Biological Crystallography. 58 (6), 899-907 (2002).
- Herzog, F., et al. Structural Probing of a Protein Phosphatase 2A Network by Chemical Cross-Linking and Mass Spectrometry. Science. 337 (6100), 1348-1352 (2012).
- Hoopmann, M. R., et al. Kojak: efficient analysis of chemically cross-linked protein complexes. Journal of Proteome Research. 14 (5), 2190-2198 (2015).
- Seebacher, J., et al. Protein cross-linking analysis using mass spectrometry, isotope-coded cross-linkers, and integrated computational data processing. Journal of Proteome Research. 5 (9), 2270-2282 (2006).
- Rinner, O., et al. Identification of cross-linked peptides from large sequence databases. Nature Methods. 5 (4), 315-318 (2008).
- Walzthoeni, T., et al. False discovery rate estimation for cross-linked peptides identified by mass spectrometry. Nature Methods. 9 (9), 901-903 (2012).
- Yang, B., et al. Identification of cross-linked peptides from complex samples. Nature Methods. 9 (9), 904-906 (2012).
- Chu, F., Baker, P. R., Burlingame, A. L., Chalkley, R. J. Finding Chimeras: a Bioinformatics Strategy for Identification of Cross-linked Peptides. Molecular & Cellular Proteomics. 9 (1), 25-31 (2010).
- Holding, A. N., Lamers, M. H., Stephens, E., Skehel, J. M. Hekate: Software Suite for the Mass Spectrometric Analysis and Three-Dimensional Visualization of Cross-Linked Protein Samples. Journal of Proteome Research. 12 (12), 5923-5933 (2013).
- Hauri, S., et al. Rapid determination of quaternary protein structures in complex biological samples. Nature Communications. 10 (1), 192 (2019).
- Röst, H. L., et al. OpenSWATH enables automated, targeted analysis of data-independent acquisition MS data. Nature Biotechnology. 32 (3), 219-223 (2014).
- Röst, H. L., et al. OpenMS: a flexible open-source software platform for mass spectrometry data analysis. Nature Methods. 13 (9), 741-748 (2016).
- Quandt, A., et al. Using synthetic peptides to benchmark peptide identification software and search parameters for MS/MS data analysis. EuPA Open Proteomics. 5, 21-31 (2014).
- Bradley, P., et al. Free modeling with Rosetta in CASP6. Proteins: Structure, Function, and Bioinformatics. 61 (S7), 128-134 (2005).
- Gray, J. J. High-resolution protein-protein docking. Current Opinion in Structural Biology. 16 (2), 183-193 (2006).
- Khakzad, H., et al. Cheetah-MS: a web server to model protein complexes using tandem cross-linking mass spectrometry data. Bioinformatics. , (2021).
- Malmström, L. Chapter 15: Computational Proteomics with Jupyter and Python. Methods in Molecular Biology. 15, 237-248 (1977).
- Martens, L., et al. mzML--a community standard for mass spectrometry data. Molecular & Cellular Proteomics. 10 (1), (2011).
- Chambers, M. C., et al. A cross-platform toolkit for mass spectrometry and proteomics. Nature Biotechnology. 30 (10), 918-920 (2012).
- Waterhouse, A., et al. SWISS-MODEL: homology modelling of protein structures and complexes. Nucleic Acids Research. 46 (W1), W296-W303 (2018).
- Yang, J., et al. Improved protein structure prediction using predicted interresidue orientations. Proceedings of the National Academy of Sciences. 117 (3), 1496-1503 (2020).
- Koehler Leman, J., et al. Macromolecular modeling and design in Rosetta: recent methods and frameworks. Nature Methods. 17 (7), 665-680 (2020).
- Chivian, D., et al. Prediction of CASP6 structures using automated Robetta protocols. Proteins: Structure, Function, and Bioinformatics. 61 (S7), 157-166 (2005).
- Chivian, D., et al. Automated prediction of CASP-5 structures using the Robetta server. Proteins: Structure, Function, and Bioinformatics. 53 (S6), 524-533 (2003).
- Bauch, A., et al. openBIS: a flexible framework for managing and analyzing complex data in biology research. BMC Bioinformatics. 12, 468 (2011).
- Lima, D. B., et al. SIM-XL: A powerful and user-friendly tool for peptide cross-linking analysis. Journal of Proteomics. 129, 51-55 (2015).
- Happonen, L., et al. A quantitative Streptococcus pyogenes-human protein-protein interaction map reveals localization of opsonizing antibodies. Nature Communications. 10, 2727 (2019).
- Khakzad, H., et al. Structural determination of Streptococcus pyogenes M1 protein interactions with human immunoglobulin G using integrative structural biology. PLOS Computational Biology. 17 (1), E1008169 (2021).
- Khakzad, H., et al. In vivo cross-linking MS of the complement system MAC assembled on live Gram-positive bacteria. Frontiers in Genetics. 11, (2020).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved