Method Article
نموذج إصابة الكلى الحادة الناجمة عن سيسبلاتين في حمار وحشي الكبار
* These authors contributed equally
In This Article
Summary
يصف هذا البروتوكول الإجراءات للحث على إصابة الكلى الحادة (AKI) في سمك الحمار الوحشي البالغ باستخدام سيسبلاتين كعامل كلي. قمنا بتفصيل الخطوات لتقييم قابلية إعادة إنتاج التقنية وتقنياتين لتحليل الالتهاب وموت الخلايا في الأنسجة الكلوية ، وقياس التدفق الخلوي و TUNEL ، على التوالي.
Abstract
يستخدم سيسبلاتين عادة ككيماوي. على الرغم من أن له آثار إيجابية في الأفراد الذين عولجوا من السرطان، سيسبلاتين يمكن أن تتراكم بسهولة في الكلى بسبب انخفاض وزنه الجزيئي. هذا التراكم يسبب موت الخلايا الأنبوبية ويمكن أن تحفز على تطوير إصابة الكلى الحادة (AKI) ، والتي تتميز بانخفاض سريع في وظائف الكلى ، وتلف الأنسجة ، وتسلل الخلايا المناعية. إذا تدار في جرعات محددة سيسبلاتين يمكن أن يكون أداة مفيدة كمحفز AKI في النماذج الحيوانية. وقد ظهرت حمار وحشي كنموذج مثير للاهتمام لدراسة وظائف الكلى, تجديد الكلى, والإصابة, كما هياكل الكلى الحفاظ على أوجه التشابه الوظيفي مع الثدييات. حمار وحشي الكبار حقن مع سيسبلاتين يظهر انخفاض البقاء على قيد الحياة, موت خلايا الكلى, وزيادة علامات الالتهاب بعد 24 ح بعد الحقن (hpi). في هذا النموذج، يمكن تقييم تسلل الخلايا المناعية وموت الخلية عن طريق قياس التدفق الخلوي وتقيس TUNEL. يصف هذا البروتوكول الإجراءات للحث على AKI في حمار وحشي الكبار عن طريق حقن سيسبلاتين داخل الصفاق ويوضح في وقت لاحق كيفية جمع الأنسجة الكلوية لمعالجة قياس التدفق الخلوي واختساب TUNEL موت الخلية. وستكون هذه التقنيات مفيدة لفهم آثار سيسبلاتين كعامل كلي البروتينات وستسهم في توسيع نماذج AKI في حمار وحشي الكبار. ويمكن أيضا أن يستخدم هذا النموذج لدراسة تجديد الكلى, في البحث عن المركبات التي تعالج أو منع تلف الكلى ودراسة التهاب في AKI. وعلاوة على ذلك، فإن الأساليب المستخدمة في هذا البروتوكول تحسين توصيف تلف الأنسجة والالتهاب، والتي هي أهداف علاجية في الأمراض المصاحبة للكلى.
Introduction
الكلى هي المسؤولة عن العديد من الوظائف الفسيولوجية الهامة التي تحافظ على التوازن، مثل ترشيح الدم، وإزالة المخلفات الزائدة، وتنظيم تركيزات الأيونات1. تلف الأنسجة الكلوية يمكن أن يؤدي إلى حالة غير متجانسة تسمى إصابة الكلى الحادة (AKI) ، والتي توصف سريريا بأنها انخفاض سريع في وظيفة الكلى الناجمة عن تدمير وموت الخلايا الظهارية الأنبوبية ، إصابة الخلايا البطانية ، وتسلل الكريات البيض 2،3. AKI هو شرط من المتوقع أن يحدث في 8-16٪ من دخول المستشفيات4،مع ارتفاع معدل الوفيات التي تتراوح بين 20 إلى 50٪ في وحدة العناية المركزة (ICU)5. ويرتبط هذا المرض مع زيادة الإقامة في المستشفى واستخدام كبير للموارد المالية5. وتشمل العوامل الايولوجية الجفاف، والصدمة، والالتهابات، والإنتان، وأمراض القلب والأوعية الدموية، والأدوية كلي البروتينات6. يعرف السمية الكلوية بأنها إصابة كلوية ناجمة عن المخدرات ، مما يسبب آثارا مثل AKI ، اعتلالات الأنابيب ، و اعتلالات الكبيبات7. تؤثر السمية الكلوية على ثلثي مرضى وحدة العناية المركزة ، حيث أن ما يقرب من 20٪ من الأدوية الموصوفة في وحدة العناية المركزة تعتبر8،9، وهذا يشمل الأدوية المضادة للالتهابات غير الستيرويدية (مضادات الالتهاب غير الستيروئيدية) والمضادات الحيوية مثل فانكومايسين وأمينوغليكوزيد ، وعوامل العلاج الكيميائي مثل الميثوتريكسات و سيسبلاتين7. سيسبلاتين هو واحد من أقوى الأدوية والعلاج الكيميائي شيوعا، وتستخدم في علاج الأورام الصلبة، مثل الرأس والرقبة، الخصية، المبيض، والمثانة10. في الكلى ، يتم استيعاب cisplatin في الأنبوب الملتوي القريب (PCT) من خلال الناقل القيصري العضوي 2 (OCT-2) وفي تركيزات عالية يرتبط بالحمض النووي الذي يؤدي إلى مسارات موت الخلية7،10،11،12. تراكم هذا الدواء في الكلى يساهم في السمية الكلوية مع الموت والالتهاب13. هذا الآثار الجانبية الضارة يؤثر بشكل كبير على حياة وتشخيص ثلث مرضى السرطان الذين يخضعون لعلاج سيسبلاتين ، لذلك لا بد من البحث عن علاجات جديدة يمكن أن تقلل من السمية الكلوية دون فقدان تأثير القتل على الخلايا السرطانية10.
وبسبب هذا التأثير الكلوي ، يستخدم سيسبلاتين عادة كمحث AKI في النماذج الحيوانية التجريبية ، كما هو موضح إلى الأمام. في القوارض، تم الإبلاغ عن أول نموذج AKI الناجمة عن سيسبلاتين في عام 197114 ولكن في الوقت الحاضر، ظهرت العديد من البروتوكولات المختلفة باستخدام الآثار التراكمية التي تعتمد على الجرعة من سيسبلاتين15. وبالتالي، اعتمادا على الجرعة وعدد من التطبيقات، يمكن أن تكون درجات مختلفة من شدة إصابة الكلىالناجمة 16،17،18،19،20،21. وتتكون الطريقة الأكثر شيوعا من حقن داخل الصفاق (أي p.) جرعة واحدة من سيسبلاتين تليها القتل الرحيم في الأيام التالية. في هذا البروتوكول الكلاسيكي، جرعة واحدة عالية من السيتبلاتين (10-13 ملغم/كغ في الفئران و/أو 3-8 ملغم/كغ في الفئران) تحفز تغييرات هيستولوجية حادة، مثل فقدان حدود الفرشاة وحطام الخلية داخل التجويف الأنبوبي، بعد أيام قليلة من حقن سيسبلاتين. شدة التغيرات النسيجية تعتمد على الجرعة ، ويلاحظ وجود علامات على التجديد بعد 7 أيام من حقن سيسبلاتين16،17.
على الرغم من أن نماذج القوارض راسخة ، قررنا الاستفادة من خصائص فقاريات أخرى ، مع تركيز دراساتنا على سمك الحمار الوحشي(دانيو ريو). وقد استخدمت هذه الأسماك على نطاق واسع لنمذجة الأمراض البشرية، وذلك بسبب صغر حجمها، والإخصاب الخارجي، وارتفاع معدلات الإنجاب، والتطور السريع، وشفافية الأجنة واليرقات، وانخفاض تكلفة الصيانة، وتشريح مماثلة للثدييات (مع بعض الاستثناءات)، وارتفاع قدرة تجديد الأنسجة، والسلوك الاجتماعي، 70٪ من التشابه الجيني مع البشر و 84٪ مع الجينات المرتبطة بالأمراض البشرية22. Streisinger وآخرون23،24،25 بدأت الدراسات مع حمار وحشي التي أكدت عمليا على استخدام هذا الكائن الحي نموذج للتحليل الجيني للتنمية الفقاريات. في أبحاث الكلى ، ظهرت سمكة الحمار الوحشي ليس فقط في الدراسات التنموية ولكن أيضا كأداة وراثية في البحث عن جينات جديدة مرتبطة بحالات الكلى26. وعلاوة على ذلك، فإن قدرة التجديد دون تشكيل ندبة والقدرة على توليد الكلية من خلال حياتهم، ودعا نيونيفروجينيسيس، وجعل حمار وحشي نموذجا حيوانيا رئيسيا للبحث التجديد27،28. وعلاوة على ذلك، فإن توافر نماذج تجريبية لأمراض الكلى المختلفة، بما في ذلك إصابات الكلى الحادة والمزمنة، يدل على براعة هذا الكائن التجريبي26،29. كما هو الحال في الثدييات ، يتم اشتقاق السلف الكلوي لسمك الحمار الوحشي من الوسيط المتوسط. تولد هذه السلف الكلوية المعرضة التي سوف تتطور في وقت لاحق إلى mesonephros، والتي سيتم الحفاظ عليها كجهاز ناضجة حتى سن البلوغ29،30.
وتقع الكلى حمار وحشي الكبار على الجدار الظهري للجسم، بين المثانة السباحة والعمود الفقري29. من وجهة نظر بطنية، يمكن تقسيم حمار وحشي إلى ثلاث مناطق(الشكل 1A):الرأس (H)، الجذع (Tr)، والذيل (تا)29. نفس الثدييات، حمار وحشي لديه الكلية كوحدات وظيفية من الكلى، والتي تنقسم إلى شرائح أنبوبية(الشكل 1A):الكلي (RC)، أنبوب ملتوية قريبة (PCT)، أنبوب مستقيم قريب (PST)، القاصد في وقت مبكر (DE)، في وقت متأخر من القاص (DL) وجمع القناة (CD)29. حمار وحشي تشترك في الحفظ الجيني وأوجه التشابه الهيكلي مع الكليرونات البشرية (الشكل 1B) ولكن يفتقر إلى بعض الجزيئات مثل أنبوبي وسيطة، والمعروف أيضا باسم حلقة هنل (LH)29،31. عادة ما تكون أسماك المياه العذبة مثل حمار وحشي محاطة بوسط منخفض جدا ، وبسبب هذا ، فإنها تميل إلى أن تكون مفرطة السمية وتعتمد على الخياشيم والجلد في المراحل المبكرة ، والكلى لتنظيم التناضح وإفراز الماء32. يبدأ ترشيح الدم من الشريان الأورطي الظهري بواسطة الفروس حوالي 48 ساعة بعد الإخصاب (hpf)33،34. الكلى من حمار وحشي ليس فقط جهاز إفراز النفايات الأيضية ولكن أيضا يعمل كعضو دموي من 4 أيام بعد الإخصاب (dpf) إلى مرحلة البلوغ وهو ما يعادل نخاع العظام في الثدييات35. أثناء التنمية، والخلايا الجذعية الدموية (HSCs) بذور الكلى، وتجديد الذات، وتوليد النخاعي، الغدة الدرقية، وأنساب الخلايا اللمفاوية، والحفاظ على عوامل النسخ، والجزيئات الإشارات، والبرامج الوراثية المحفوظة للغاية مع الثدييات36،37. وقد كشفت الدراسات أن معظم الغدة الدرقية، خثار، النخاع، والخلايا اللمفاوية في الجهاز المناعي البشري موجودة في حمار وحشي37،38. الخصائص الفريدة لهذا الحيوان والميزات المحفوظة مع الكلى البشرية جعلت هذا الكائن الحي النموذجي مفيدا في البحث عن وظائف الكلى والإصابات والتجديد.
على الرغم من أن الكلى من حمار وحشي درس جيدا وبعض نماذج من AKI متوفرة بالفعل في اليرقات وسمك الحمار الوحشي الكبار28، في وقت إنشاء هذا البروتوكول لم يكن هناك أي دليل على نموذج AKI غير المستحث كيميائيا غير المضاد الحيوي في حمار وحشي الكبار. وإلى جانب ذلك، يركز مختبرنا على اختبار البكتيريا بروبيوتيك والمركبات المشتقة من الكائنات الحية المجهرية لدراسة التجديد وتلف الكلى، وبالتالي ركزنا جهودنا في خلق نموذج جديد AKI الناجم عن سيسبلاتين في الأسماك الكبار. توضح مقالة الفيديو المعروضة في هذه المخطوطة إجراءات نموذج جديد لتحريض AKI باستخدام حقنة أي p. من 120 ميكروغرام سيسبلاتين لكل غرام من الحيوان (120 ميكروغرام /غرام) (الشكل 2A). واستندت هذه الجرعة في البداية على دراسات AKI الناجمة عن سيسبلاتين في نماذج مورين التي ذهبت حوالي 10 ملغ / كغ (أي ما يعادل 10 ميكروغرام / غرام)14,15,16,17, ومع ذلك, هذه الجرعة لم تكن كافية للحث على تلف الكلى المتعلقة بالسمية الكلوية (البيانات غير مبينة). وهكذا، قمنا بزيادة الجرعة لتلك المستخدمة في هذهالدراسة (الشكل 2B). كشف عملنا عن تأثير يعتمد على الجرعة من سيسبلاتين في معدل البقاء على قيد الحياة بعد الحقن مع تحريض تلف أنسجة الكلى 24 hpi كما هو مبين من خلال فقدان الهيكل الأنبوبي ، وزيادة التسلل الالتهابي ، وارتفاع معدل موت الخلايا. هنا، ونحن نصف اثنين من التقنيات لتحليل تطوير AKI الناجم عن سيسبلاتين: تدفق قياس الخلايا، لتحليل تسلل الخلايا، و TUNEL، لقياس موت الخلية. قياس التدفق الخلوي هو تقنية تقيس الخصائص الفيزيائية (الحجم والحبيبة) والكيميائية (المركبات الفلورية) للخلايا. داخل السيتومتر، يمر تعليق الخلية عبر سائل غمد ينظم الخلايا في خط واحد، مما يسمح لها بالمرور عبر شعاع ليزر خلية واحدة في كل مرة(الشكل 3A). سيقوم كاشف أمام شعاع الضوء بقياس مبعثر الأمام (FSC) ، الذي يرتبط بحجم الخلية ، وأجهزة الكشف إلى الجانب ستقيس مبعثر الجانب (SSC) الذي يرتبط بحبيبة الخلايا. وسوف أجهزة الكشف الأخرى قياس مضان من الجسيمات، والبروتينات الفلورية، أو الخلايا التي تحمل اسم الأجسام المضادة39،40. كما الأجسام المضادة التجارية لسمك الحمار الوحشي نادرة في الوقت الحاضر، واستخدام المراسلين الحيوان والمؤشرات الحيوية الفلورية يسمح لتحسين هذا التحليل وتحديد مجموعات الخلايا المتنوعة41،42،43. أداة أخرى مستخدمة في هذا البروتوكول كان نقل deoxynucleotidyl الطرفية (TdT) dUTP إنهاء وضع العلامات (TUNEL) المقايسة. إن اختبار TUNEL هو طريقة اكتشاف موت الخلايا المبرمج في مرحلة متأخرة تعتمد على قدرة TdT على تحديد الحمض النووي المجزأ وتسميته بإزالة الأكسجين الموسوم بعلامة فلورية يمكن تصورها وقياسها كميا بواسطة المجهر44 (الشكل 3B). وبالنظر إلى أن واحدة من أكثر السمات لفتا للاكي هو تحريض موت الخلايا المبرمج في خلايا الكلى أنبوبي3, هذه التقنية مفيد للغاية لأنه يمكن تحليلها عن طريق قياس التدفق الخلوي و / أو المجهر.
النهج المعروضة في هذه المقالة يسمح بمراقبة حالة AKI وتقديم نموذج حاد جديد لدراسة اضطرابات AKI التي يمكن أن تكون مفيدة للبحث عن أهداف علاجية جديدة في AKI المرتبطة سيسبلاتين.
Protocol
وقد وافقت لجنة أخلاقيات استخدام الحيوان التابعة لمعهد العلوم الطبية الحيوية في جامعة ساو باولو في السابق على الإجراءات الموصوفة في هذا البروتوكول لاستخدامها في نموذج سمك الحمار الوحشي.
1. AKI التعريفي عن طريق الحقن داخل الصفاق Cisplatin
- إعداد حل عمل سيسبلاتين عن طريق تخفيف محلول المخزون إلى 850 ميكروغرام / مل في 0.9٪ NaCl. حافظ على درجة حرارة الغرفة، محمية من الضوء.
تنبيه: يوصي النسيج بالتلاعب في سيسبلاتين بمعدات الحماية الشخصية (PPE) بما في ذلك النظارات الواقية والقفازات ومعطف المختبر. تخزين محلول المخزون في درجة حرارة الغرفة، محمية من الضوء. - إعداد 150 ملغم/لتر MS-222 (تريكين) مخدر في مياه النظام45. تخدير حمار وحشي الكبار (5-9 أشهر) عن طريق الغمر لمدة 1-2 دقيقة تقريبا.
ملاحظة: يجب أن تكون الأسماك المخدرة بشكل فعال غير راعية للمس. لاختبار التخدير الفعال، اضغط برفق على الزعنفة الكودية لمراقبة رد الفعل.
تنبيه: Tricaine هو مهيج للجلد والعينين، واستخدام معدات الوقاية الشخصية للتلاعب. - باستخدام ملعقة بلاستيكية نقل الأسماك إلى سطح ماصة، مثل المناشف الورقية، لإزالة المياه الزائدة في جميع أنحاء الجسم. ثم، مع ملعقة بلاستيكية نقل الأسماك إلى طبق بيتري على مقياس ووزن الأسماك. يحيط علما وزن السمك كما سيكون من الضروري لحسابات الجرعة.
ملاحظة: امتصاص المياه الزائدة من الأسماك يمنع المبالغة في وزن الحيوان، لا الإفراط في الجفاف منذ يضر بالأسماك. - لتحقيق الجرعة النهائية من 120 ميكروغرام / غرام من الوزن، وتقسيم ميكروغرام من الجرعة النهائية (120 ميكروغرام) لكل ميكروغرام من محلول عمل سيسبلاتين (850 ميكروغرام) وتحويل هذا العدد إلى ميكرولتر (ميكرولتر) عن طريق ضرب ل 1000، للحصول على حجم 120 ميكروغرام من سيسبلاتين (141.2 ميكرولتر). ثم ضرب هذا العدد (141.2 ميكرولتر) لوزن السمك (ز) للحصول على الحجم النهائي لحقنها.
- مع ملعقة بلاستيكية، نقل السمك على اسفنجة مبللة مع قطع قليلا لعقد ذلك، مع الجانب البطني حتى. يجب أن يكون الإسفنج مبللا بمخدر في مياه النظام.
- ملء 31 G 1.0 مل حقنة الأنسولين مع حجم محسوب من محلول عمل سيسبلاتين.
- أدخل الإبرة في الجزء داخل الصفاق للحيوان بالقرب من زعنفة الحوض ، بزاوية ضحلة لتجنب ثقب الأحشاء(الشكل 2A). ثم حقن ببطء الحل.
- بعد حقن وضع السمك في خزان للتعافي من التخدير. مشاهدة الأسماك لعلامات الانتعاش الطبيعي(على سبيل المثال، حركات السباحة، حركات opercular).
ملاحظة: يجب أن يتعافى الحيوان في 3-5 دقائق القادمة. إذا لزم الأمر، وتحفيز الأسماك عن طريق تحريكه مع ملعقة بلاستيكية، ماصة البلاستيك باستور، أو وضعه على مقربة من خرطوم مع فقاعات. - للسيطرة على الأسماك، وإجراء نفس الإجراء عن طريق حقن حل من 0.9٪ NaCl. استخدم نفس الحساب بعد نسبة وزن الجسم: سيكون الحجم الذي سيتم حقنه 141 ميكرولتر مضروبا في وزن السمك (ز).
- رصد بقاء الأسماك على الأقل مرتين في اليوم في الأيام التالية (الشكل 2B).
2. عزل الكلى ومعالجة الأنسجة لتدفق الخلايا المناعية
- لهذا الإجراء، استخدم الخلايا المناعية الفلورية الحيوانات المعدلة وراثيا ملحوظ (على سبيل المثال،TG (mpo:GFP)).
- بعد 24 hpi من 120 ميكروغرام / غرام سيسبلاتين ، والقتل الرحيم الحيوانات عن طريق صدمة تحت الحرارية (تقشعر لها الأبدان السريع).
ملاحظة: وقد ثبت أن الصدمة الحرارية لتكون أكثر فعالية كطريقة القتل الرحيم من جرعة زائدة MS-222. صدمة تحت الحرارية هو أقل إرهاقا وسريعة ومتسقة، وأكثر أمانا للموظفين من استخدام MS-222، وقد سبق وصف46،47. - في خزان عبور الخارجي إعداد المياه الجليدية في نسبة 5:1 من الجليد إلى مياه النظام، ووضع الخزان الداخلي مع شاشة فوق الجليد، والانتظار حتى تصل المياه 2-4 درجة مئوية.
ملاحظة: يجب ألا تكون الأسماك على اتصال مباشر مع الجليد، لأن هذا قد يسبب حروقا حرارية وألما. - نقل الحيوان إلى الماء المثلج، والانتظار على الأقل 10 دقيقة حتى يكون هناك فقدان التوجه وعدم وجود حركة opercular.
- مع ملعقة بلاستيكية، ضع السمك على مناشف ورقية لتجفيف الماء الزائد.
- نقل السمك إلى لوحة تشريح agarose 3٪ وأخذها تحت مجسمة مع الضوء العلوي. مع مقص، وقطع رأس الأسماك مما يجعل قطع سريع فقط وراء العينين، وإزالة الرأس.
- مع مقص غرامة جعل قطع من الجانب المفتوح إلى كلوكا وإزالة الأعضاء الداخلية مع ملقط غرامة.
- استخدام دبابيس الحشرات لقرصة الجانبين من جدران الجسم لفتح الذبيحة وفضح الكلى تعلق على العمود الفقري.
- فصل الكلى مع ملقط غرامة ووضع الجهاز في لوحة بئر 6 مع محلول بارد من 1x PBS/2٪ FBS. ابق على الجليد.
- التقاط الأنسجة مع ماصة بلاستيكية باستور وتمرير الأنسجة من خلال مصفاة الخلية 40 ميكرومتر على أنبوب 50 مل، يذبل بلطف مع المكبس حقنة.
- غسل مرتين مع 1 مل من 1x PBS/2٪ FBS وجمع الخلايا في أنبوب 50 مل.
- خلايا الطرد المركزي في 400 × غرام لمدة 5 دقائق في 4 درجة مئوية.
- التقط بعناية كل الناتنات مع ميكروبايت 1 مل وتجاهله. إضافة 500 ميكرولتر من البارد 1x برنامج تلفزيوني لإعادة إنفاق الخلايا ووضعها في أنابيب قياس الخلايا تدفق 5 مل. ابق على الجليد.
- عد الخلايا في غرفة نيوباور مما يجعل تخفيف 1:10 في تريبان الأزرق(على سبيل المثال،تأخذ 10 ميكرولتر من العينة وتخلط مع 90 ميكرولتر من تريبان الأزرق). إضافة 10 ميكرولتر من الخليط إلى غرفة نيوباور وعدد الخلايا تحت المجهر.
ملاحظة: من المتوقع تحقيق أفضل النتائج مع 1-5 × 106 خلايا / مل وقابلية البقاء >80٪.
تنبيه: تريبان الأزرق هو عامل مسرطن، استخدم معدات الوقاية الشخصية للتعامل معها. - خذ الخلايا لقراءتها بواسطة مقياس الخلايا. ثم تحليل النتائج التي تحدد السكان من الفائدة.
3. تجهيز الكبار زيبرافيش أنسجة الكلى ل TUNEL المقايسة
- لهذا الإجراء، استخدم الحيوانات البرية(على سبيل المثال،AB، توبنغن، الخ) أو معدل وراثيا بلون فلوري مختلف عن طقم TUNEL، حيث يمكن أن تتداخل الفلورسينس المماثلة مع تحليل TUNEL.
- بعد 24 hpi من 120 ميكروغرام / غرام سيسبلاتين ، والقتل الرحيم الحيوانات عن طريق صدمة تحت الحرارية (تقشعر لها الأبدان السريع). انظر 2.3-2.4.
- تشريح الأسماك كما هو موضح في 2.5-2.6؛ يجب أن تبقى الكلية متصلة العمود الفقري أثناء إجراء التثبيت (موضح أدناه).
- باستخدام دبابيس الحشرات ، قم بقرص جانبي جدران الجسم لفتح الذبيحة ودبوسها على سطح الفلين للحفاظ على تعرض الكلى.
ملاحظة: يضمن هذا الإجراء بقاء الكلية في الوضع الصحيح للتحليل اللاحق. - ثم ضع سطح الفلين مع الكلى التي تواجه أسفل في لوحة بئر 6 على محلول الطازجة من 4٪ paraformaldehyde (PFA). يبقيه بين عشية وضحاها في 4 °C.
تنبيه: PFA مسرطن ومهيج للبشرة والأسطح المخاطية. إعداد حلول PFA تحت غطاء محرك السيارة الكيميائي باستخدام معدات الوقاية الشخصية بما في ذلك معدات حماية العين. - في اليوم التالي، تشريح الكلى كما هو الحال في 2.8. وضع الكلى في طبق بيتري 60 ملم مع برنامج تلفزيوني 1x وشطف مرتين في برنامج تلفزيوني 1x.
- إعداد 2٪ agarose لتوليد مصفوفة دعم للأنسجة.
- تجاهل جميع المتبقية 1x برنامج تلفزيوني من طبق بيتري وصب 2٪ agarose ببطء لتغطية الجهاز كله. ثم وضع الكلى باستخدام ملقط ناعم تحت مجسم لمنع الكلى لأضعاف. دع الآغروز يترسخ في درجة حرارة الغرفة.
ملاحظة: هذا الإجراء سوف يحافظ على اتجاه وشكل الجهاز من خلال المعالجة النسيجية لأن الشكل الشبيه بأوراق الأعضاء يسبب ميلا إلى الطي إذا لم يكن داخل مصفوفة داعمة. - بعد التصلب agarose، استخدم مشرط لقطع agarose حول الأنسجة، وتشكيل مكعبات صغيرة، وإزالة فائض من الآغاروز حول الأنسجة.
- ضع مكعبات الآغاروز في كاسيت مناسب للمعالجة النسيجية.
ملاحظة: يمكن القيام بالخطوات التالية يدويا أو في معالج الأنسجة التلقائي. - أولا، معالجة الأنسجة في كاسيت باتباع الخطوات التالية لمدة 45 دقيقة لكل منهما في درجة حرارة الغرفة: حمام واحد من الإيثانول 50٪، حمام واحد من الإيثانول 70٪، حمامين متتاليين من الإيثانول 95٪، وثلاثة حمامات متتالية من الإيثانول 100٪. بعد ذلك ، قم بمعالجة الأنسجة في حمامين متتاليين من Xylene وثلاثة حمامات متتالية من البارافين. هذا الأخير يستمر 1 ساعة لكل منهما في 60 درجة مئوية.
تنبيه: إجراء تغييرات تحت غطاء محرك السيارة الكيميائي، والأبخرة من الإيثانول والزيلين هي مهيجة وسامة. - لإعداد كتل البارافين، تذوب العدس البارافين إلى 60 درجة مئوية.
- افتح الكاسيت البلاستيكي مع الأنسجة في الداخل وأبقه على طبق دافئ. قوالب معدنية الاحماء للبارافين.
- مع ملاقط وضع الأنسجة على قالب معدني بحيث طول الكلى موازية لقاعدة العفن. إضافة البارافين، وإعادة تخصيص الأنسجة إذا لزم الأمر.
- تغطية القالب مع قاعدة كاسيت وإضافة البارافين حتى يتم تغطية الشبكة. السماح ترسيخ في درجة حرارة الغرفة ومن ثم وضع في -20 درجة مئوية لعملية تماسك أسرع.
- الافراج عن كتلة البارافين من القالب المعدني حوالي 20-30 دقيقة في وقت لاحق.
- مع microtome، قسم الأنسجة جزءا لا يتجزأ من البارافين إلى سمك 5 ميكرومتر. استخدام الشرائح الزجاجية silanized أو مشحونة إيجابيا لجمع الأنسجة.
4. اختبار TUNEL
ملاحظة: يستخدم البروتوكول التالي مجموعة أدوات الكشف عن موت الخلايا في الموقع (جدول المواد).
- أنسجة Dewax الشرائح وضعها في اثنين من الحمامات المتتالية من الزيلين لمدة 5 دقائق. ثم ترطيب الأنسجة من خلال سلسلة متدرج من الإيثانول: 100٪-95٪-70٪-50٪، لمدة 5 دقائق لكل منهما.
- وضع الشرائح في تشغيل مياه الصنبور الباردة لشطف قبالة الإيثانول. الحفاظ على الشرائح في الماء المقطر.
- إعداد غرفة حاضنة مظلمة. إضافة مناشف ورقية مبللة في الجزء السفلي للحفاظ على الرطوبة أثناء خطوات الحضانة.
ملاحظة: في حالة عدم وجود غرفة حاضنة من الممكن استخدام طبق بيتري مع ورقة رطبة في الجزء السفلي واثنين من المسواك لوضع الشريحة. - إعداد بروتيناز K حل العملالطازجة : 10 ميكروغرام / مل في 10 mM تريس / HCl، درجة الحموضة 7.4-8.
ملاحظة: يستخدم البروتين K كعامل permeabilization، على النحو الموصى به من قبل النسيج. - ضع الشرائح في غرفة الحاضنة المظلمة وأضف حل عمل Proteinase K حتى تغطي العينات. حضانة لمدة 30 دقيقة في 37 درجة مئوية.
- بينما العينات هي احتضان، وإعداد خليط رد فعل TUNEL: إضافة 50 ميكرولتر من محلول إنزيم إلى 450 ميكرولتر تسمية الحل. حماية من الضوء.
ملاحظة: يمكن ضبط وحدة التخزين التي سيتم إعدادها بنفس نسبة 1:10. ويحسب حجم ليكون 50 ميكرولتر من الخليط لكل قسم؛ هذا يمكن أن يتغير اعتمادا على حجم العينات. - التقاط غرفة مظلمة وغسل الشرائح مرتين مع برنامج تلفزيوني 1x.
- بعد ذلك ، قم بتجفيف المنطقة المحيطة بالعينة باستخدام الورق الماصة وإضافة 50 ميكرولتر من خليط تفاعل TUNEL على كل شريحة نسيج ، ونشر المحلول بحيث يتم تغطية العينة بأكملها. حضانة عند 37 درجة مئوية لمدة 2 ساعة. حماية من الضوء.
- بعد الحضانة، شطف الشريحة ثلاث مرات مع برنامج تلفزيوني 1x وتجفيف المنطقة حول العينة باستخدام المناشف الورقية.
- إضافة 50 ميكرولتر من DAPI 1:1000 إلى العينات، لاحتواء النووية، واحتضان لمدة 5 دقائق في درجة حرارة الغرفة. حماية من الضوء.
- شطف مرة أخرى ثلاث مرات مع برنامج تلفزيوني 1x وتجفيف المنطقة المحيطة بالعينة.
- جبل الشريحة مع المتوسطة المائية المضادة للتلاشي، ووضع غطاء، وختم مع طلاء الأظافر. تخزين الشرائح أفقيا، محمية من الضوء عند 4 درجة مئوية.
ملاحظة: خصائص المضادة للتلاشي من المتوسطة المتصاعدة هي للحفاظ على مضان العينات ولكن من الممكن استخدام أي وسيلة هيدروفيلية المتاحة. خطوة الختم النهائي مع طلاء الأظافر أمر بالغ الأهمية لتجنب الجفاف. - تصور العينات تحت المجهر الفلوري. لهذا النوع من الصباغ الفلوري، استخدم الطول الموجي للإثارة في نطاق 520-560 نانومتر (أخضر) والكشف في نطاق 570-620 نانومتر (أحمر).
النتائج
كلية حمار وحشي هو جهاز مصطبغة مسطحة تقع على الجدار الظهري ووحدتها الوظيفية الأساسية، وكلية، يتم الحفاظ مع الثدييات (الشكل 1). خصوصية وجود كلية واحدة فقط مع قدرة عالية على التجديد يجعل هذا الكائن الحي نموذج خيار ممتاز لإصابة الكلى نموذج. تم تصميم البروتوكولات المقدمة في هذا العمل لحث AKI عن طريق الحقن داخل الصفاق (أي p.) من سيسبلاتين في حمار وحشي الكبار(الشكل 2)و ليتم تحليلها في وقت لاحق من قبل اثنين من التقنيات مفصلة قبل: تدفق قياس الخلايا (الشكل 3A) و TUNEL (الشكل 3B). يتم تصوير مخطط انسيابي للعملية بأكملها في الشكل 4. تم تطبيق جرعات سيسبلاتين في البداية على تلك الموصوفة في نماذج الماوس15،16،17، حيث المعيار المستخدم هو 10-13 ملغ من سيسبلاتين لكل كيلوغرام من الحيوان (ملغ / كجم). ومع ذلك ، أظهرت سمكة الحمار الوحشي أن تكون أكثر مقاومة للسيسبلاتين من الماوس (البيانات غير المعروضة) ، وزادت الجرعة النهائية. عندما قمنا بتقييم معدل بقاء الحيوانات على قيد الحياة، أظهرت التجارب تأثير تعتمد على الجرعة من سيسبلاتين(الشكل 5A). ولهذا السبب، نوصي باتباع التعليمات تماما كما هو موضح في هذا البروتوكول ومراقبة معدل بقاء الحيوانات باستمرار كمقياس للاستنساخ، قبل جمع أي مواد. بعد حقن i.p. من 120 ميكروغرام / غرام سيسبلاتين (الشكل 5A، الخط الأحمر) ، لوحظ انخفاض في بقاء حوالي 30٪ من الحيوانات في أول 24 ساعة وانخفض البقاء تدريجيا حتى وصل إلى حوالي 20٪ من الحيوانات الحية في اليوم 5 بعد الحقن ، ثم استقر(الشكل 5A). لم تتأثر سمية سيسبلاتين بجنس الحيوانات ، لأن الذكور والإناث لديهم منحنيات بقاء مماثلة(الشكل 5B).
أظهر تحليل حركية AKI الناجم عن سيسبلاتين زيادة الالتهاب وموت الخلايا في الكلى 24 hpi. واحدة من أسرع الطرق والكمية لتقييم الالتهاب هو تدفق قياس الخلايا ولكن نظرا لعدم وجود أجسام مضادة ضد مستضدات حمار وحشي المتاحة تجاريا لهذه التقنية، من الضروري استخدام خط المعدلة وراثيا مع علامة المناعة. في الوقت الحاضر، يمكن الوصول إلى العديد من خطوط حمار وحشي وضع العلامات على الخلايا المناعية (الجدول 1). يمكن استخدام هذه الخطوط بشكل طري أو في تركيبة ، نظرا لذخيرة كافية للتحليل48،49،50،51،52،53،54،55،56،57،58،59،60. هذا يبسط بشكل كبير تقنية منذ ليس من الضروري أي خطوة حضانة الأجسام المضادة، على العكس من ذلك، بعد عزل الخلايا عن طريق الفصل الميكانيكي، والقراءة المباشرة على السيتومتر ممكن.
كما ذكرنا من قبل ، فإن كلية حمار وحشي ليست فقط جهاز ترشيح الدم مع وظائف الهوستاتيكي ولكن أيضا الموقع التشريحي للهيماتوبيس في البالغين ، أي ما يعادل نخاع العظم في الثدييات33،34،35. بهذه الطريقة عندما نحللها عن طريق قياس التدفق الخلوي من الممكن التفريق بين مجموعات الخلايا المماثلة للدم البشري61،62 (الشكل 6A) ، وهذا يسمح لنا بتحديد مجموعات الخلايا في البداية من حيث الحجم والحبيبة واستبعاد الحطام. في هذه الحالة، استخدمنا خط المعدلة وراثيا يسمى Tg(mpo:GFP)52 الذي يعبر عن بروتين الفلورسنت الأخضر (GFP) جنبا إلى جنب مع إنزيم myeloperoxidase، الذي هو موجود في العدلات. مع العلم بذلك، كانت استراتيجيتنا البوابة على أساس الفصل الأولي للسكان الحبيبية(الشكل 6B). بعد ذلك ، تم استبعاد خلايا مزدوجة ، لأنها يمكن أن تغير بشكل كبير التحليل وتؤدي إلى استنتاجات غير دقيقة. ومزدوج هو حدث واحد يتكون من 2 جزيئات مستقلة ويمكن استبعادها عن طريق اختيار ارتفاع مبعثر إلى الأمام (FSC-H) مقابل منطقة مبعثر إلى الأمام (FSC-A) مؤامرة الكثافة (الشكل 6C). بعد هذه الخطوة، تم تحديد الخلايا التي عبرت عن علامة الفلورسنت واختيارها(الشكل 6D). وأخيرا، استخرجت الإحصاءات السكانية من التحليل ورسمت كنسبة مئوية من الخلايا(الشكل 6 ه).
واحدة من أبرز خصائص السمية الكلوية سيسبلاتين هو موت الخلايا الأنبوبية10، وتصور هذا بسهولة استخدمنا المقايسة TUNEL للكشف عن موت الخلايا المبرمج. توصي هذه الطريقة باستخدام الخلايا والأنسجة البرية التي تفتقر إلى علامات الفلورسنت ، لأن الفلورسينس الموازي سيتداخل مع التحليل ، في حالة سمك الحمار الوحشي ينصح باستخدام خطوط من النوع البري ، مثل AB أو Tübingen أو TAB أو خط معدل وراثيا مع بروتين فلوري لا يتعارض مع لون تفلور TUNEL. تقنية TUNEL يسمح التحليل عن طريق قياس التدفق الخلوي أو المجهر. الفحص المجهري لديه ميزة الحفاظ على بنية الأنسجة، مما يسمح لمعرفة الخلايا التي تموت. تحت المجهر الفلوري ، يمكن تمييز النواة الساطعة للخلايا المبرمج بسهولة عن الخلفية. الحيوانات حقن مع سيسبلاتين (الشكل 7B) لديها خلايا ميتة أكثر من السيطرة (الشكل 7A) في 24 hpi. تم إجراء القياس الكمي النهائي مع خيار عداد الخلية من برنامج فيجي وأظهرت إحصائيا أكثر الخلايا الميتة في الكلى التي تعالج سيسبلاتين مما كانت عليه في الضوابط (الشكل 7C)
أظهر البروتوكول الموصوف في هذه المخطوطة كيفية استخدام سيسبلاتين كمحفز ل AKI في سمك الحمار الوحشي البالغ ، وهو مستجيب للجرعة وسريع وموثوق به. استنادا إلى البيانات التي تم الحصول عليها من معدلات البقاء على قيد الحياة وقياس علامات السمية الكلوية للسيسبلاتين بما في ذلك الالتهاب (التي تم اكتشافها عن طريق قياس التدفق الخلوي) وموت الخلايا (التي تم اكتشافها بواسطة فحص TUNEL) ، نقترح هذا النموذج لدراسة السمية الكلوية سيسبلاتين وكذلك للعلاجات المستقبلية في الأمراض المرتبطة ب AKI.
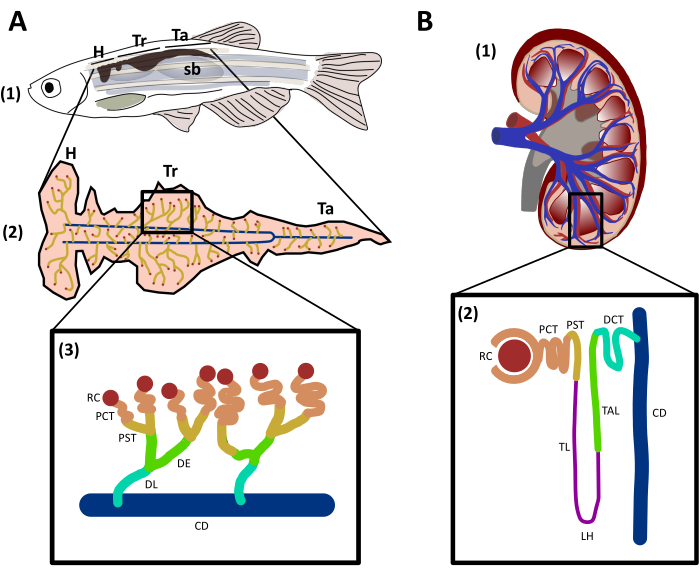
الشكل 1: هيكل ومقارنة الحمار الوحشي والكلى البشرية. أ. (1) منظر الجانبية حمار وحشي الكبار مع الكلى ممثلة في البني الداكن الموجود في الجدار الظهري للأسماك، بين المثانة السباحة (sb) والعمود الفقري. (2) عرض البطين للكلية تظهر الكلية (الأصفر) متصلة القناة جمع (الأزرق). يتم وضع علامة على مناطق مختلفة من الكلى: الرأس (H) والجذع (Tr) والذيل (Ta). (3) التخطيطي الذي يمثل نييفرونات سمك الحمار الوحشي وشرائحها المسماة والملونة لمطابقة المناطق المحفوظة وراثيا مع الكليفرون البشري. ب. (1) منظر برجي لكلية بشرية. (2) التخطيطي الذي يصور كليفرون الإنسان مع شرائح المسمى والملونة. RC: الكلية; معاهدة التعاون بشأن البراءات: أنبوب ملتوية قريبة; توقيت المحيط الهادي: أنبوب مستقيم قريب; TL: طرف رفيع; LH: حلقة من هنل; TAL: سميكة تصاعدي الطرف; DE: القاصي في وقت مبكر; DL: تأخر القاصد; DCT: أنبوبي ملتوية الثنية; CD: جمع القناة. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
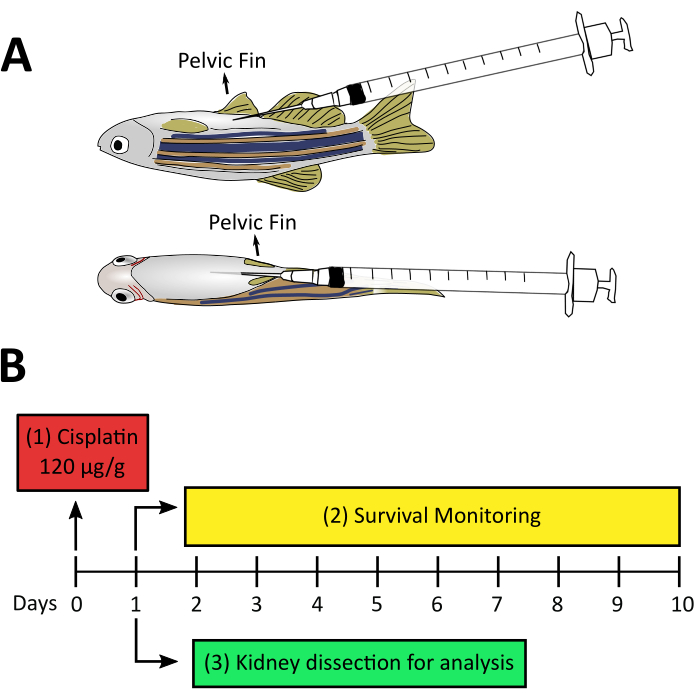
الشكل 2:التصميم التجريبي ل AKI الناجم عن سيسبلاتين. أ. عرض الجانبية والبطينية من حمار وحشي الكبار مشيرا إلى موقف الإبرة أثناء إجراء الحقن. تخترق الإبرة بزاوية 20-30 درجة من البطن ويتم إدخالها ببطء بالتوازي مع الجدار البطني وتجنب ثقب الأحشاء. باء - ال 20 في المائ التصميم التجريبي للكيمياء الكيمياء الناجمة عن سيسبلاتين: (1) حقن سيسبلاتين 120 ميكروغرام/غرام لكل في اليوم صفر. (2) قبل محاولة الخطوة 3، ينصح بمراقبة بقاء الأسماك بعد الحقن من اليوم الأول حتى اليوم العاشر. (3) تشريح الكلى بعد يوم واحد من حقن سيسبلاتين لمزيد من تقنيات المعالجة. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
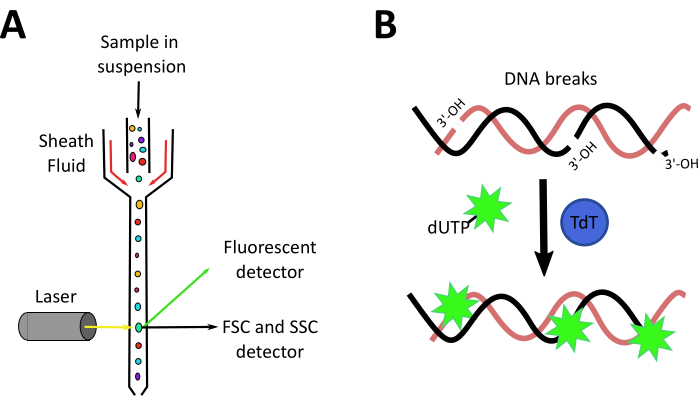
الشكل 3: آليات تدفق الخلايا وتقنيات TUNEL. أ. نظرة عامة على مقياس التدفق الخلوي: يركز تعليق الخلايا بشكل هيدروديناميكي على خط واحد بواسطة سائل غمد ، مما يؤدي إلى مرور الخلايا واحدا تلو الآخر أمام شعاع الليزر. تقيس أجهزة الكشف الأمامية والجانبية التشتت الأمامي (FSC) والتشتت الجانبي (SSC) وفلورة الخلايا. باء - ال 20 في المائ مبدأ المقايسة TUNEL. محطة deoxynucleotidyl transferase (TdT) يتوسط إضافة dUTP الفلورسنت ملحوظ إلى 3'-OH ينتهي من الحمض النووي مجزأة. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
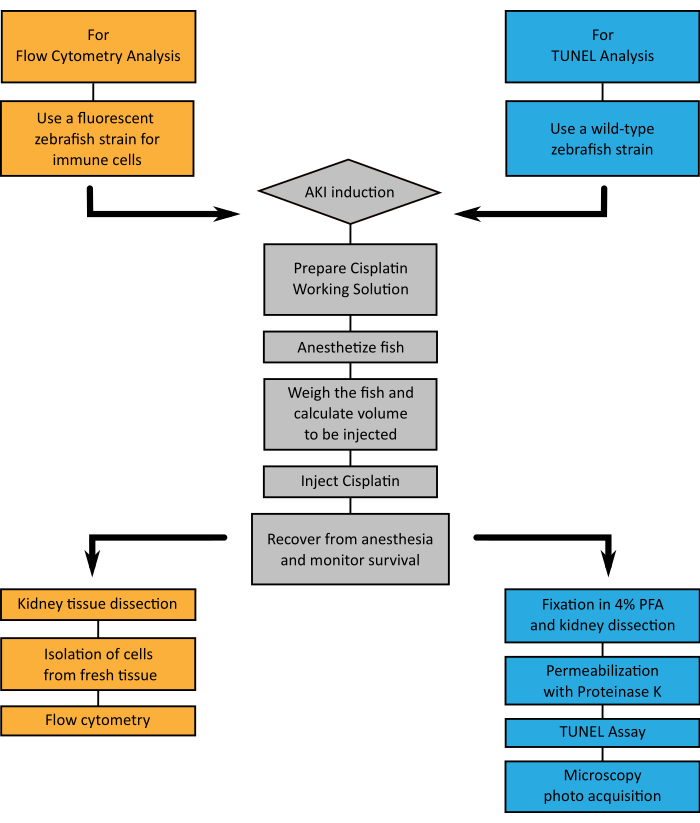
الشكل 4:مخطط انسيابي للتقنيات الممثلة. أ. مخطط انسيابي يوضح الخطوات الواجب اتباعها عند اختيار تحليل أنسجة الكلى من خلال قياس التدفق الخلوي (البرتقالي) أو TUNEL (الأزرق)، عند تحفيز AKI عن طريق حقن سيسبلاتين (رمادي). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
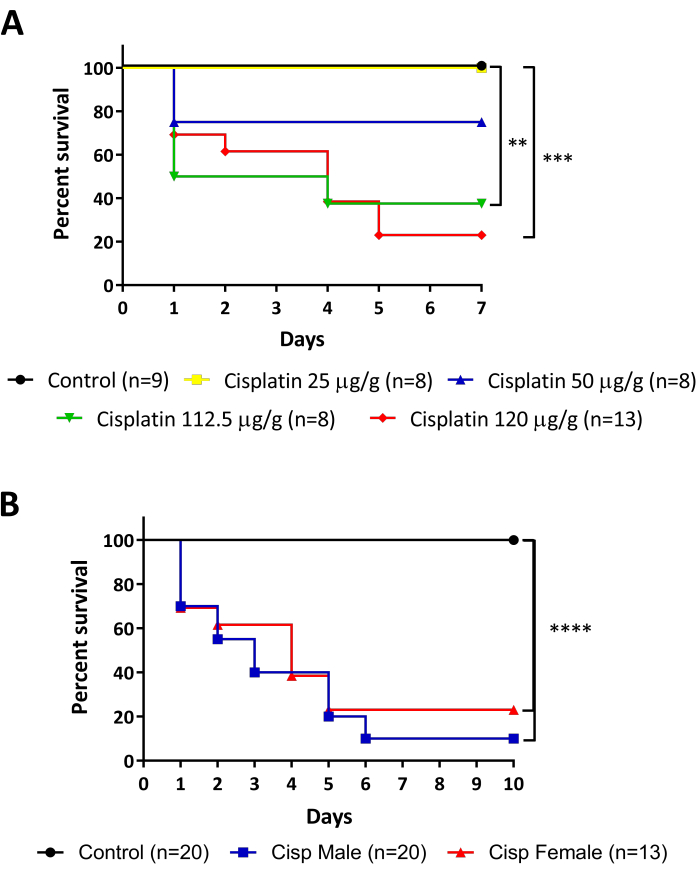
الشكل 5: رصد البقاء على قيد الحياة من الأسماك حقن سيسبلاتين. أ. معدل البقاء على قيد الحياة من جرعات مختلفة من حقن سيسبلاتين (25 - 50 - 112.5 - 120 ميكروغرام / غرام). سجل رتبة (مانتل كوكس) اختبار ، ** ع < 0.01. باء - ال 20 في المائ معدل البقاء على قيد الحياة من الذكور مقابل الإناث حقن مع 120 ميكروغرام / غرام سيسبلاتين. سجل رتبة (مانتل كوكس) اختبار ، *** ع < 0.001. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
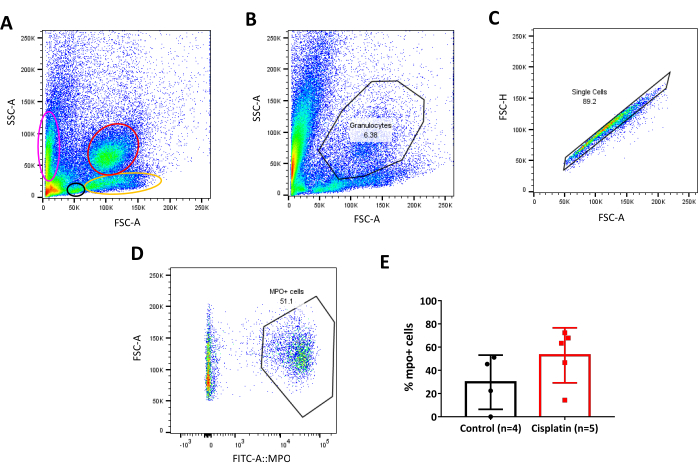
الشكل 6: بوابة استراتيجية لخط حمار وحشي المعدلة وراثيا. أ. كثافة قطعة من خلايا الكلى الكبار حمار وحشي، يتم فصل السكان حسب الحجم (FSC-A) والحبيبة (SSC-A). يتم اختيار مجموعات سكانية مختلفة من قبل البيضاوي الملونة / الدوائر. الوردي: إريثرويد; أسود: اللمفاوي; الأصفر: السلائف؛ الأحمر: الخلايا الحبيبية. باء - ال 20 في المائ مؤامرة كثافة منطقة مبعثر الجانب (SSC-A) ومنطقة مبعثر إلى الأمام (FSC-A) لاختيار السكان الحبيبية في الكلى. جيم - الدوائر التي لا يمكن أن مؤامرة كثافة من الأمام مبعثر عالية (FSC-H) وإلى الأمام منطقة مبعثر (FSC-A) لاختيار السكان singlets داخل بوابة الحبيبية. د- مؤامرة كثافة منطقة مبعثر إلى الأمام (FSC-A) و FITC-A:MPO لاختيار الخلايا الإيجابية mpo:GFP (العدلات) في الكلى. ويعتبر السكان إيجابية حوالي 103 على، من كثافة الفلورية. هاء - ال هاء الرسم البياني للنسبة المئوية للخلايا الإيجابية mpo:GFP (العدلات) في السيطرة مقابل سيسبلاتين، 24 hpi. غير مدفوعة ر-اختبار. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
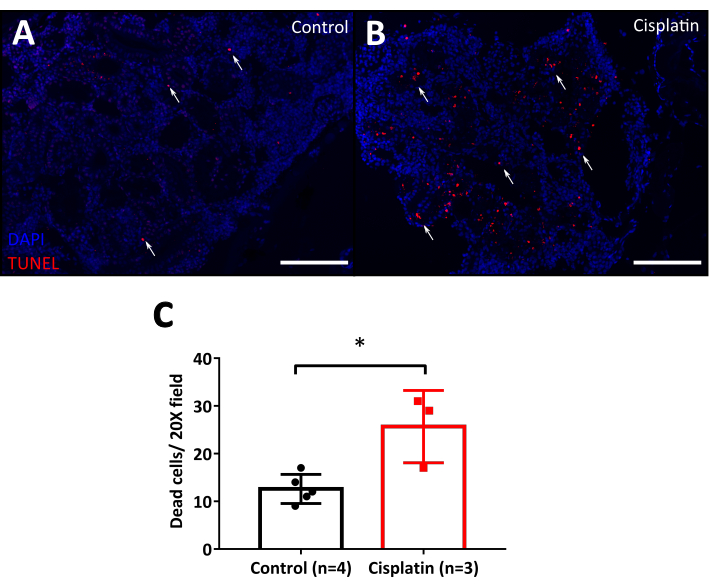
الشكل 7: اختبار TUNEL من الأسماك حقن سيسبلاتين. أ. صور دقيقة من الكلى الكبار ثابتة 24 ساعة بعد 120 ميكروغرام / غ حقن سيسبلاتين. يتم حقن الضوابط مع 0.9٪ NaCl. TUNEL الخلايا الموجبة (الخلايا المبرمج) ملطخة باللون الأحمر (الأسهم البيضاء). يستخدم DAPI (الأزرق) كطين مضاد نووي. شريط المقياس: 50 ميكرومتر. باء - ال 20 في المائ الرسم البياني الذي يبين القياس الكمي لعدد الخلايا الميتة في الكلى حسب الحقل 20x. غير مدفوع ر-اختبار، * ص < 0.05. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
| خط معدل وراثيا | نوع الخلية المسمى | مراجع |
| TG(spi1:EGFP)pA301 | خلايا النخاع | وارد وآخرون 200348 |
| TG(zpu1:GFP) | خلايا النخاع | هسو وآخرون 200449 |
| Tg(mhc2dab:GFP)sd6 | مونوسيت | ويتامر وآخرون 201150 |
| TG(lysC:DsRED2) | العدلات | قاعة وآخرون 200751 |
| TG(mpo:GFP) | العدلات | ماتياس وآخرون 200652 |
| Tg(mpeg1:mCherry) | الضامة | إليت وآخرون 201153 |
| Tg(mpeg1:Dendra2) | الضامة | هارفي وآخرون 201354 |
| TG(lck:GFP) | الخلايا التائية | لانغينو وآخرون 200455 |
| TgBAC (إيكاروس:EGFP) | الخلايا التائية | باجوغلي وآخرون 200956 |
| TG(rag1:GFP) | الخلايا التائية | جيسن وآخرون 199957 |
| TG(rag2:GFP) | الخلايا التائية | جيسن وآخرون 200158 |
| TG (CD79: GFP) | خلايا B | ليو وآخرون 201759 |
| Tg(CD45:DsRed) | الكريات البيض | برتراند وآخرون 200860 |
الجدول 1: خطوط زيبرافيش المعدلة وراثيا للخلايا المناعية. الجدول استئناف أسماء خطوط مراسل حمار وحشي مع نوع كل من الخلايا المناعية المسمى والمقالات المرجعية حيث تم بناؤها. مزيج من هذه الخطوط حمار وحشي يمكن أن توفر إمكانيات جديدة لاختيار الخلية عن طريق قياس التدفق الخلوي.
Discussion
استمر انتشار أمراض الكلى في الازدياد في جميع أنحاء العالم، ليصبح مشكلة صحية عامة عالمية تؤثر على الملايين من الناس63. إيجاد وسيلة لعلاج المصابين الكلى الأفراد ذات أهمية قصوى، فضلا عن فهم المزيد عن المسببات والتقدم. وقد تم استخدام العديد من الدراسات نماذج حيوانية لفهم الضرر الكلوي. وقد درس الكلى حمار وحشي (الشكل 1) لسنوات في علم الأحياء التنموية والبحوث الإصابة بسبب قدراتها الذاتية تجديد والتشابه الجيني29,64. هنا، نقدم نموذج AKI جديد في حمار وحشي الكبار باستخدام خصائص سيسبلاتين كعامل nephrotoxic، بالتفصيل خطوات لتحقيق رد فعل سريع وحاد مع الضرر مرئية في أقرب وقت 24 hpi (الشكل 2). وعلاوة على ذلك، هنا نشرح اثنين من التقنيات التي من شأنها أن تساعد على تقييم تلف الأنسجة بعد حقن سيسبلاتين، وتدفق قياس الخلايا و TUNEL (الشكل 3).
نماذج AKI الحالية في حمار وحشي الكبار تشمل حقن i.p. من جنتاميسين الذي يسبب أضرارا واسعة النطاق في تدمير الكلية والتبول، وأحداث تولد النيونفروجين تبدأ من اليوم 5، ويتم الانتهاء من التجديد من قبل 21 يوما بعد الحقن65. من ناحية أخرى ، تم إنشاء نموذج لإصابة الكلى الحادة المرتبطة بالإنتان (S-AKI) من خلال العدوى مع Edwardsiella tarda، نظرا لزيادة التعبير عن علامات AKI بشكل كبير ، مثل بروتين ربط عامل النمو الشبيه بالإنسولين -7 (IGFBP7) ، ومثبط الأنسجة من metalloproteinases 2 (TIMP-2) ، وجزيء إصابة الكلى -1 (KIM-1) ، في اليرقات وسمك الحمار الوحشي البالغ66. ومن المعروف أن حمار وحشي لكونه عالي الإنتاجية للبحث عن العوامل العلاجية وهذا يشمل استخدام البروبيوتيك والأيض المشتقة من الميكروبيوتا لدراسة وظائف الكلى وتجديد67. ومع ذلك، يمكن أن تؤثر النماذج المتاحة بشكل مباشر على نتيجة هذه العلاجات. وهكذا، أنشأنا طريقة مختلفة للحث على AKI في حمار وحشي الكبار (الشكل 4)،وذلك باستخدام سيسبلاتين كعامل معروف كلي البروتين التي لن يكون لها آثار معروفة مباشرة على ميكروبيوتا الأسماك، كما هو الحال مع نموذج جنتاميسين لكونه مضاد حيوي، أو العدوى مع E. tarda، لكونها نموذج الإنتان. ومع ذلك ، في نفس الوقت الذي كنا نطور بروتوكول سيسبلاتين لدينا ، استكشفت مجموعة أخرى أيضا الآثار الكلية للسيسبلاتين في سمك الحمار الوحشي البالغ ، وتبسيط الجرعة إلى 10-20-30 ميكروغرام لكل68. على الرغم من أنها أظهرت أيضا تأثير سيسبلاتين تعتمد على الجرعة في البقاء على قيد الحياة، ونحن نوصي الحذر في استخدام كمية واحدة من سيسبلاتين لجميع الأسماك، كما حمار وحشي من نفس العمر يمكن أن يكون لها أحجام مختلفة جدا والوزن وهذا يمكن أن تحفز الاختلافات في النتائج69،70. نعتقد أنه من المهم ضبط الجرعة على الوزن المقابل للحيوان ، كما هو الحال في الفئران وهذه الدراسة.
في تجاربنا مع حمار وحشي الكبار، أظهرت سيسبلاتين تأثير الجرعة والاستجابة. وقد تصور هذا من خلال رصد معدل بقاء الحيوانات بعد حقن سيسبلاتين (الشكل 5). استخدمنا البقاء على قيد الحياة كوسيلة لتقدير شدة جرعة سيسبلاتين وليس كمقياس للسمية الكلوية ، حيث لا توجد علامة مادية أخرى مرئية خلال وقت الرصد. هذا يمكن أن تكون قابلة للمقارنة مع القوارض، والتي يمكن تعديل شدة إصابة الكلى من قبل جرعة وتواتر حقن سيسبلاتين15،وتحقيق جرعات قاتلة مع تركيزات أعلى من سيسبلاتين71. وينظر أيضا الميت في الأيام التالية في نموذج اليرقات من سيسبلاتين72. منذ كان هدفنا للحث على إصابة حادة في غضون أيام قليلة، اخترنا جرعة 120 ميكروغرام /غرام من سيسبلاتين كما هو ممكن لمراقبة تلف الكلى 24 ساعة بعد الحقن، ومع ذلك، يمكن تعديل هذا اعتمادا على أهداف الدراسة.
في البشر، يتم تشخيص سريريا AKI عن طريق انخفاض معدل الترشيح الكبيبات (GFR)، وارتفاع الكرياتينين المصل، والنيتروجين اليوريا في الدم3. في حمار وحشي، ذخيرة نماذج AKI يتضمن بعض النماذج الجينيةالمشروطة 73،74 وبعض النماذج ذات الصلة بالمخدرات65،72، ولكن كما لا يمكن قياس بعض المعلمات الوظيفية AKI على حمار وحشي بسبب صعوبات تقنية(على سبيل المثال، جمع الدم)، تعتمد معظم الأبحاث تقنيات مورفولوجية وبصرية لمراقبة ملامح AKI1،75 مثل دراستنا.
في القوارض ، يدخل cisplatin الخلايا الظهارية في الأنابيب القريبة وال البعيدة ، داخل الخلية يخضع لتنشيط التمثيل الغذائي ويصبح تفاعليا للغاية يتصرف على العضيات الخلوية ويحفز على تغييرات في بنية الخلية. هذه التغييرات يمكن أن تحفز موت الخلايا المبرمج وautphagy وحتى نخر، بجرعات عالية جدا. ردا على هذا الضرر ، يتم إطلاق العديد من السيتوكينات ويتم تجنيد الكريات البيض مما يؤدي إلى التهاب ويؤثر على وظائف الجهاز15. وهذا يسلط الضوء على أهمية تقييم نوع الخلايا التي يمكن العثور عليها في الكلى المصابة، كمقيمين أو خلايا مناعية مخترقة. هنا أظهرنا كيفية تقييم هذا عن طريق قياس التدفق الخلوي ، وذلك باستخدام خطوط مراسل المناعة المعدلة وراثيا المتاحة في الوقت الحاضر(الجدول 1). سيسبلاتين زيادة النسبة المئوية للنوات(mpo:GFP الخلايا الإيجابية) في الكلى 24 ح بعد الحقن (الشكل 6). في حالة حمار وحشي، والكلى هي مكانة من HSCs التي تؤدي إلى أنواع خلايا الدم المختلفة. ومع ذلك ، فإن العديد من المحببات والكواعم عادة ما تنتشر في الدم. في مثالنا، استخدمنا خط mpo:GFP المعدل وراثيا الذي يعبر عن GFP تحت مروج myeloperoxidase من العدلات52. أظهرت الدراسات الأصلية للخط المعدل وراثيا mpo:GFP التعبير عن myeloperoxidase في حالات مختلفة من نضوج العدلات76 ولكن استراتيجيتنا البوابة ركزت على كسر المحببة التي تضم الخلايا الناضجة القادمة من الدم52، وبهذه الطريقة تحليلنا تشمل الخلايا المتسللة وليس الخلايا المقيمة. هذا مهم للنظر عند عزل السكان الخلية المطلوبة.
كما هو موضح أعلاه ، فإن موت الخلايا المبرمج هو العلامة الأكثر كلاسيكية ل AKI المرتبط ب cisplatin. هنا، أظهرنا بروتوكول بسيط لتوطين الخلايا الميتة من خلال اختبار TUNEL. حقن سيسبلاتين زيادة عدد الخلايا المبرمج 24 hpi (الشكل 7). ويمكن قياس ذلك بسهولة عن طريق عد الخلايا الميتة مباشرة من الأنسجة. ومع ذلك، لتحديد الموت الخلية محددة استخدام الأجسام المضادة ضد الخلية المطلوبة(على سبيل المثال، خلايا أنبوبية)، أو استخدام خط مراسل المعدلة وراثيا يمكن استخدامها جنبا إلى جنب مع هذه التقنية. بالمقارنة مع نموذج يسببه جنتاميسين من AKI, سيسبلاتين ويبدو أن نموذجا أكثر شدة, منذ كان أعلى جنتاميسين موت الخلايا المبرمج في اليوم الثالث بعد الحقن65.
على الرغم من وجود مجموعة متنوعة من الآثار الجانبية, سيسبلاتين لا يزال يستخدم على نطاق واسع في علاج السرطان, بسبب فعاليته ضد أنواع مختلفة من السرطان, بما في ذلك سرطان, أورام الخلايا الجرثومية, الأورام اللمفاوية, وsarcomas77. يحدث السمية الكلوية في ثلث المرضى في العلاج مع سيسبلاتين10، وبالتالي فإن البحث عن الاستراتيجيات التي يمكن أن تقلل من هذا التأثير وزيادة إعادة التشتيت أمر حتمي. نحن نعتقد أن الأساليب والتقنيات الواردة في هذه المخطوطة ستساعد على توضيح آليات إصابة الكلى وإيجاد أهداف علاجية يمكن أن تكون ضرورية لتحسين نوعية حياة الأفراد الذين يعانون من مضاعفات كلوية ، في الغالب تلك المتعلقة باستخدام سيسبلاتين.
Disclosures
وليس لدى صاحبي البلاغ ما يكشفان عنه.
Acknowledgements
وقد دعم هذا البحث صندوق أمبارو à Pesquisa do Estado de São Paulo - FAPESP (2015/21644-9؛ 2017/05264-7)؛ 2017/05687-5؛ 2018/20722-4)، كونسيلهو ناسيونال دي ديسينفولفيمنتو سينتيفيكو إي تينولوغيكو (CNPq) وكوارديناساو دي أبيرفيسوامنتو دي بيسال دي نيفل سوبيريور (CAPES)، الرمز المالي 001. نشكر المتعاونين لدينا في مختبر ماريا ريتا دوس سانتوس إي باسوس بوينو ومرفق زيبرافيش التابع لقسم علم الوراثة وعلم الأحياء التطوري، في معهد العلوم البيولوجية في جامعة ساو باولو. نشكر كريستيان نافا دي سوزا بريدا وتيريزا راكيل دي أوليفيرا رامالهو على التعليقات والاقتراحات المتعلقة بالمخطوطة. نحن نقدر ونشكر مارسيو فيلار مارتينز، من فريق الوسائط المتعددة في معهد العلوم الطبية الحيوية، على تسجيل هذا الفيديو وطبعته وإنتاجه.
Materials
| Name | Company | Catalog Number | Comments |
| 1x PBS | Made by diluting 10 X PBS (prepared in lab) in distilled water | ||
| 31 G 1.0 cc insulin syringe | BD Plastipak | 990256 | Needle: BD Precision Glide 300110 |
| 3.5 L Fish tank | Tecniplast | Part of the aquactic system | |
| 6 well plate | Corning | 351146 | |
| 10 mM Tris/HCl | Prepared from solid Tris Base (Promega, H5135), adjusted to pH 7.4-8 with HCl (Merck, 1003171000) | ||
| 50 ml Falcon tube | Corning | 352070 | |
| 2-3% Agarose | Invitrogen | 16500-500 | Dissolve 2 or 3% agarose (w/v) in 1x PBS, warm until dissolve. |
| 2% FBS | Gibco | 12657-09 | Dilute 2% (w/v) directly in 1x PBS |
| 4% Paraformaldehyde | Sigma-Aldrich | P6148-500G | Dissolve 4% PFA (w/v) in warm 1x PBS, mix until dissolve in a hot plate in a fume hood. Aliquot and store at -20 °C |
| 50% Ethanol | Made by diluting 100% ethanol in distilled water | ||
| 70% Ethanol | Made by diluting 100% ethanol in distilled water | ||
| 90% Ethanol | Made by diluting 100% ethanol in distilled water | ||
| 100% Ethanol | Synth | 00A1115.01.BJ | |
| 100% Xylene | Synth | 00X1001.11.BJ | |
| Cell strainer 40 µm | Corning | 431750 | |
| Cisplatin | Blau Farmacêutica | 16020227 | C-PLATIN 1 mg/mL. Store at room temperature. |
| Cork board sheet | Obtained from local stationary store | ||
| DAPI | Sigma-Aldrich | D9542 | Stock solution 20 mg/ml dissolved in water |
| Fine forceps | Fine Science Tools | 11254-20 | |
| Flow cytometry tubes | Corning | 352052 | |
| Glass slide | Thermo-Fisher | 4445 | |
| Histology cassette | Ciencor | 2921 | |
| Immuno stain chamber | Ciencor | EP-51-05022 | |
| Incubator | NAPCO | 5400 | Set to 37 °C |
| Insect pins | Papillon | Model micro15x20 | |
| In Situ Cell Death Detection Kit | Roche Diagnostics | 12156792910 | |
| Metal mold | Leica Biosystems | 3803081 | |
| Micropipette 200-1000 µL | Eppendorf | Use 1 mL tips | |
| MS-222 (Tricaine) | Fluka Analytical | A5040-25G | |
| NaCl 0.9% | Synth | C1060.01.AG | Dissolve 0.9% NaCl (w/v) in distilled water |
| Nail polish | Prefer transparent | ||
| Neubauer chamber | Precicolor HGB | ||
| Pasteur plastic pipet | United Scientific Supplies | P31201 | |
| Paraplast | Sigma-Aldrich | P3558 | |
| Petri dish | J.ProLab | 0307-1/6 | 60 and 100 mm |
| Plastic spoon | Obtained from local store | ||
| Proteinase K | New England BioLabs | P8102 | Diluite from stock 20 mg/ml |
| Scissors | Fine Science Tools | 14060-09 | |
| Scalpel blade | Solidor | ||
| Sponge | Obtained from local store | ||
| Trypan Blue | Cromoline | 10621/07 | |
| Vannas Spring Scissors | Fine Science Tools | 15000-00 | |
| Vectashield Antifade Mounting Medium | Vector Laboratories | H-1000-10 | |
| Centrifuge | Eppendorf | 5810R | |
| Cytometer | BD Biosciences | FACSCanto II | |
| Fluorescence Stereoscope | Zeiss | Axio Zoom.V16 | |
| Fluorescence Microscope | Zeiss | AxioVert.A1 | |
| Microtome | Leica | Jung Supercut | |
| Scale | Ohaus Corporation | AR2140 |
References
- McKee, R. A., Wingert, R. A. Zebrafish Renal Pathology: Emerging Models of Acute Kidney Injury. Current Pathobiology Reports. 3 (2), 171-181 (2015).
- Guo, C., Dong, G., Liang, X., Dong, Z. Epigenetic regulation in AKI and kidney repair: mechanisms and therapeutic implications. Nature Reviews Nephrology. 15 (4), 220-239 (2019).
- Makris, K., Spanou, L. Acute Kidney Injury: Definition, Pathophysiology and Clinical Phenotypes. Clinical Biochemist Reviews. 37 (2), 85-98 (2016).
- Sawhney, S., et al. Intermediate and Long-term Outcomes of Survivors of Acute Kidney Injury Episodes: A Large Population-Based Cohort Study. American Journal of Kidney Diseases. 69 (1), 18-28 (2017).
- Saxena, A., Meshram, S. V. Predictors of Mortality in Acute Kidney Injury Patients Admitted to Medicine Intensive Care Unit in a Rural Tertiary Care Hospital. Indian Journal of Critical Care Medicine. 22 (4), 231-237 (2018).
- Sawhney, S., Fraser, S. D. Epidemiology of AKI: Utilizing Large Databases to Determine the Burden of AKI. Advances in Chronic Kidney Disease. 24 (4), 194-204 (2017).
- Sales, G. T. M., Foresto, R. D. Drug-induced nephrotoxicity. Revista da Associação Médica Brasileira. 66, 82-90 (2020).
- Perazella, M. A. Drug use and nephrotoxicity in the intensive care unit. Kidney International. 81 (12), 1172-1178 (2012).
- Taber, S. S., Mueller, B. A. Drug-associated renal dysfunction. Critical Care Clinics. 22 (2), 357-374 (2006).
- Pabla, N., Dong, Z. Cisplatin nephrotoxicity: mechanisms and renoprotective strategies. Kidney International. 73 (9), 994-1007 (2008).
- Wang, D., Lippard, S. J. Cellular processing of platinum anticancer drugs. Nature Reviews Drug Discovery. 4 (4), 307-320 (2005).
- Shirmanova, M. V., et al. Chemotherapy with cisplatin: insights into intracellular pH and metabolic landscape of cancer cells in vitro and in vivo. Scientific Reports. 7 (1), 8911 (2017).
- Xu, Y., et al. A Role for Tubular Necroptosis in Cisplatin-Induced AKI. Journal of the American Society of Nephrology. 26 (11), 2647-2658 (2015).
- Kociba, R. J., Sleight, S. D. Acute toxicologic and pathologic effects of cis-diamminedichloroplatinum (NSC-119875) in the male rat. Cancer Chemotherapy Reports. 55 (1), 1-8 (1971).
- Perše, M., Večerić-Haler, &. #. 3. 8. 1. ;. Cisplatin-Induced Rodent Model of Kidney Injury: Characteristics and Challenges. BioMed Research International. 2018, 1462802 (2018).
- Dobyan, D. C., Levi, J., Jacobs, C., Kosek, J., Weiner, M. W. Mechanism of cis-platinum nephrotoxicity: II. Morphologic observations. Journal of Pharmacology and Experimental Therapeutics. 213 (3), 551-556 (1980).
- Singh, G. A possible cellular mechanism of cisplatin-induced nephrotoxicity. Toxicology. 58 (1), 71-80 (1989).
- Jodrell, D. I., et al. The renal effects of N10-propargyl-5,8-dideazafolic acid (CB3717) and a non-nephrotoxic analogue ICI D1694, in mice. British Journal of Cancer. 64 (5), 833-838 (1991).
- McKeage, M. J., et al. Lack of nephrotoxicity of oral ammine/amine platinum (IV) dicarboxylate complexes in rodents. British Journal of Cancer. 67 (5), 996-1000 (1993).
- Gautier, J. C., et al. Evaluation of novel biomarkers of nephrotoxicity in two strains of rat treated with Cisplatin. Toxicologic Pathology. 38 (6), 943-956 (2010).
- Vinken, P., et al. Tissue Kim-1 and urinary clusterin as early indicators of cisplatin-induced acute kidney injury in rats. Toxicologic Pathology. 40 (7), 1049-1062 (2012).
- Zorzetto, R., Guimarães, M. Um peixe modelo. Pesquisa FAPESP. 209, 16-21 (2013).
- Streisinger, G., Walker, C., Dower, N., Knauber, D., Singer, F. Production of clones of homozygous diploid zebra fish (Brachydanio rerio). Nature. 291 (5813), 293-296 (1981).
- Chakrabarti, S., Streisinger, G., Singer, F., Walker, C. Frequency of gamma-Ray Induced Specific Locus and Recessive Lethal Mutations in Mature Germ Cells of the Zebrafish, BRACHYDANIO RERIO. Genetics. 103 (1), 109-123 (1983).
- Walker, C., Streisinger, G. Induction of Mutations by gamma-Rays in Pregonial Germ Cells of Zebrafish Embryos. Genetics. 103 (1), 125-136 (1983).
- Morales, E. E., Wingert, R. A. Zebrafish as a Model of Kidney Disease. Results and Problems in Cell Differentiation. 60, 55-75 (2017).
- Poureetezadi, S. J., Wingert, R. A. Little fish, big catch: zebrafish as a model for kidney disease. Kidney International. 89 (6), 1204-1210 (2016).
- McCampbell, K. K., Wingert, R. A. New tides: using zebrafish to study renal regeneration. Translational Research. 163 (2), 109-122 (2014).
- Drummond, I. A., Davidson, A. J. Zebrafish kidney development. Methods in Cell Biology. 100, 233-260 (2010).
- Saxén, L., Sariola, H. Early organogenesis of the kidney. Pediatric Nephrology. 1 (3), 385-392 (1987).
- Diep, C. Q., et al. Identification of adult nephron progenitors capable of kidney regeneration in zebrafish. Nature. 470 (7332), 95-100 (2011).
- Hill, A. J., Bello, S. M., Prasch, A. L., Peterson, R. E., Heideman, W. Water permeability and TCDD-induced edema in zebrafish early-life stages. Toxicological Sciences. 78 (1), 78-87 (2004).
- Drummond, I. A., et al. Early development of the zebrafish pronephros and analysis of mutations affecting pronephric function. Development. 125 (23), 4655-4667 (1998).
- Majumdar, A., Drummond, I. A. Podocyte differentiation in the absence of endothelial cells as revealed in the zebrafish avascular mutant, cloche. Developmental Genetics. 24 (3-4), 220-229 (1999).
- Song, H. D., et al. Hematopoietic gene expression profile in zebrafish kidney marrow. Proceedings of the National Academy of Sciences of the United States of America. 101 (46), 16240-16245 (2004).
- Gore, A. V., Pillay, L. M., Venero Galanternik, M., Weinstein, B. M. The zebrafish: A fintastic model for hematopoietic development and disease. Wiley Interdisciplinary Reviews: Developmental Biology. 7 (3), 312 (2018).
- Paik, E. J., Zon, L. I. Hematopoietic development in the zebrafish. The International Journal of Developmental Biology. 54 (6-7), 1127-1137 (2010).
- Palis, J., Yoder, M. C. Yolk-sac hematopoiesis: the first blood cells of mouse and man. Experimental Hematology. 29 (8), 927-936 (2001).
- O'Donnell, E. A., Ernst, D. N., Hingorani, R. Multiparameter flow cytometry: advances in high resolution analysis. Immune Network. 13 (2), 43-54 (2013).
- Perfetto, S. P., Chattopadhyay, P. K., Roederer, M. Seventeen-colour flow cytometry: unravelling the immune system. Nature Reviews Immunology. 4 (8), 648-655 (2004).
- Ma, D., Zhang, J., Lin, H. F., Italiano, J., Handin, R. I. The identification and characterization of zebrafish hematopoietic stem cells. Blood. 118 (2), 289-297 (2011).
- Kulkeaw, K., et al. Purification of zebrafish erythrocytes as a means of identifying a novel regulator of haematopoiesis. British Journal of Haematology. 180 (3), 420-431 (2018).
- Ratnayake, D., Currie, P. D. Fluorescence-Activated Cell Sorting of Larval Zebrafish Muscle Stem/Progenitor Cells Following Skeletal Muscle Injury. Methods in Molecular Biology. 1889, 245-254 (2019).
- Kyrylkova, K., Kyryachenko, S., Leid, M., Kioussi, C. Detection of apoptosis by TUNEL assay. Methods in Molecular Biology. 887, 41-47 (2012).
- Collymore, C., Tolwani, A., Lieggi, C., Rasmussen, S. Efficacy and safety of 5 anesthetics in adult zebrafish (Danio rerio). Journal of the American Association for Laboratory Animal Science. 53 (2), 198-203 (2014).
- Wilson, J. M., Bunte, R. M., Carty, A. J. Evaluation of rapid cooling and tricaine methanesulfonate (MS222) as methods of euthanasia in zebrafish (Danio rerio). Journal of the American Association for Laboratory Animal Science. 48 (6), 785-789 (2009).
- Matthews, M., Varga, Z. M. Anesthesia and euthanasia in zebrafish. Institute for Laboratory Animal Research Journal. 53 (2), 192-204 (2012).
- Ward, A. C., et al. The zebrafish spi1 promoter drives myeloid-specific expression in stable transgenic fish. Blood. 102 (9), 3238-3240 (2003).
- Hsu, K., et al. The pu.1 promoter drives myeloid gene expression in zebrafish. Blood. 104 (5), 1291-1297 (2004).
- Wittamer, V., Bertrand, J. Y., Gutschow, P. W., Traver, D. Characterization of the mononuclear phagocyte system in zebrafish. Blood. 117 (26), 7126-7135 (2011).
- Hall, C., Flores, M. V., Storm, T., Crosier, K., Crosier, P. The zebrafish lysozyme C promoter drives myeloid-specific expression in transgenic fish. BMC Developmental Biology. 7, 42 (2007).
- Mathias, J. R., et al. Resolution of inflammation by retrograde chemotaxis of neutrophils in transgenic zebrafish. Journal of Leukocyte Biology. 80 (6), 1281-1288 (2006).
- Ellett, F., Pase, L., Hayman, J. W., Andrianopoulos, A., Lieschke, G. J. mpeg1 promoter transgenes direct macrophage-lineage expression in zebrafish. Blood. 117 (4), 49-56 (2011).
- Harvie, E. A., Green, J. M., Neely, M. N., Huttenlocher, A. Innate immune response to Streptococcus iniae infection in zebrafish larvae. Infection and Immunity. 81 (1), 110-121 (2013).
- Langenau, D. M., et al. In vivo tracking of T cell development, ablation, and engraftment in transgenic zebrafish. Proceedings of the National Academy of Sciences of the United States of America. 101 (19), 7369-7374 (2004).
- Bajoghli, B., et al. Evolution of genetic networks underlying the emergence of thymopoiesis in vertebrates. Cell. 138 (1), 186-197 (2009).
- Jessen, J. R., Willett, C. E., Lin, S. Artificial chromosome transgenesis reveals long-distance negative regulation of rag1 in zebrafish. Nature Genetics. 23 (1), 15-16 (1999).
- Jessen, J. R., Jessen, T. N., Vogel, S. S., Lin, S. Concurrent expression of recombination activating genes 1 and 2 in zebrafish olfactory sensory neurons. Genesis. 29 (4), 156-162 (2001).
- Liu, X., et al. Zebrafish B Cell Development without a Pre-B Cell Stage, Revealed by CD79 Fluorescence Reporter Transgenes. Journal of Immunology. 199 (5), 1706-1715 (2017).
- Bertrand, J. Y., Kim, A. D., Teng, S., Traver, D. CD41+ cmyb+ precursors colonize the zebrafish pronephros by a novel migration route to initiate adult hematopoiesis. Development. 135 (10), 1853-1862 (2008).
- de Jong, J. L., Zon, L. I. Histocompatibility and hematopoietic transplantation in the zebrafish. Advances in Hematology. 2012, 282318 (2012).
- Ossowski, P., et al. Differentiation of morphotic elements in human blood using optical coherence tomography and a microfluidic setup. Optics Express. 23 (21), 27724-27738 (2015).
- McCullough, K., et al. Measuring the population burden of chronic kidney disease: a systematic literature review of the estimated prevalence of impaired kidney function. Nephrology Dialysis Transplantation. 27 (5), 1812-1821 (2012).
- Drummond, B. E., Wingert, R. A. Insights into kidney stem cell development and regeneration using zebrafish. World Journal of Stem Cells. 8 (2), 22-31 (2016).
- McCampbell, K. K., Springer, K. N., Wingert, R. A. Atlas of Cellular Dynamics during Zebrafish Adult Kidney Regeneration. Stem Cells International. 2015, 547636 (2015).
- Wen, X., et al. A zebrafish model of infection-associated acute kidney injury. American Journal of Physiology-Renal Physiology. 315 (2), 291-299 (2018).
- Gong, J., Noel, S., Pluznick, J. L., Hamad, A. R. A., Rabb, H. Gut Microbiota-Kidney Cross-Talk in Acute Kidney Injury. Seminars in Nephrology. 39 (1), 107-116 (2019).
- Kim, M. J., Moon, D., Jung, S., Lee, J., Kim, J. Cisplatin nephrotoxicity is induced via poly(ADP-ribose) polymerase activation in adult zebrafish and mice. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 318 (5), 843-854 (2020).
- Parichy, D. M., Elizondo, M. R., Mills, M. G., Gordon, T. N., Engeszer, R. E. Normal table of postembryonic zebrafish development: staging by externally visible anatomy of the living fish. Developmental Dynamics. 238 (12), 2975-3015 (2009).
- Singleman, C., Holtzman, N. G. Growth and maturation in the zebrafish, Danio rerio: a staging tool for teaching and research. Zebrafish. 11 (4), 396-406 (2014).
- Wagner, T., Kreft, B., Bohlmann, G., Schwieder, G. Effects of fosfomycin, mesna, and sodium thiosulfate on the toxicity and antitumor activity of cisplatin. Journal of Cancer Research and Clinical Oncology. 114 (5), 497-501 (1988).
- Hentschel, D. M., et al. Acute renal failure in zebrafish: a novel system to study a complex disease. American Journal of Physiology-Renal Physiology. 288 (5), 923-929 (2005).
- Zhou, W., Hildebrandt, F. Inducible podocyte injury and proteinuria in transgenic zebrafish. Journal of the American Society of Nephrology. 23 (6), 1039-1047 (2012).
- Huang, J., et al. A zebrafish model of conditional targeted podocyte ablation and regeneration. Kidney International. 83 (6), 1193-1200 (2013).
- Christou-Savina, S., Beales, P. L., Osborn, D. P. Evaluation of zebrafish kidney function using a fluorescent clearance assay. Journal of Visualized Experiments. (96), e52540 (2015).
- Lieschke, G. J., Oates, A. C., Crowhurst, M. O., Ward, A. C., Layton, J. E. Morphologic and functional characterization of granulocytes and macrophages in embryonic and adult zebrafish. Blood. 98 (10), 3087-3096 (2001).
- Dasari, S., Tchounwou, P. B. Cisplatin in cancer therapy: molecular mechanisms of action. European Journal of Pharmacology. 740, 364-378 (2014).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved