Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Einzelne Liposomen Messungen für das Studium der Protonen-Pumpen Membran Enzyme mit Elektrochemie und Fluoreszenz-Mikroskopie
In diesem Artikel
Zusammenfassung
Hier präsentieren wir ein Protokoll, um den molekularen Mechanismus der Protonen-Translokation über Lipidmembranen der einzelnen Liposomen, studieren mit Cytochrom Bo3 als Beispiel. Kombination von Elektrochemie und Fluoreszenz-Mikroskopie, pH-Änderungen in das Lumen der einzelne Vesikel, mit einzelnen oder mehreren Enzym können individuell erkannt und analysiert werden.
Zusammenfassung
Protonen-Pumpen Enzyme des Elektrons übertragen Ketten paar Redoxreaktionen an Protonen-Translokation durch die Membran, erstellen eine Proton-treibende Kraft für die ATP-Produktion verwendet. Der amphiphilen Charakter der Membranproteine erfordert besonderes Augenmerk auf deren Handhabung und Rekonstitution in die natürliche Lipid-Umwelt ist unverzichtbar, wenn Transport Membranverfahren wie Protonen-Translokation zu studieren. Hier zeigen wir eine Methode, die für die Untersuchung des Protonen-Pumpen-Mechanismus der Membran Redox Enzyme verwendet worden ist, Cytochrom Bo3 aus Escherichia coli als Vorbild nehmen. Eine Kombination der Elektrochemie und Fluoreszenz-Mikroskopie dient zur Steuerung der Redox-Status des Quinone Pool und Monitor pH-Wert ändert sich in das Lumen. Durch die räumliche Auflösung der Fluoreszenz-Mikroskopie können Hunderte von Liposomen gleichzeitig gemessen werden, während die Enzym-Inhalt auf ein einziges Enzym oder Transporter pro Liposomen verkleinert werden kann. Die jeweiligen einziges Enzym Analyse kann Muster in der Enzym-funktionale Dynamik zeigen, die sonst durch das Verhalten der gesamten Bevölkerung verborgen sein könnte. Wir fügen Sie eine Beschreibung eines Skripts zur automatischen Bildanalyse.
Einleitung
Informationen über Enzym Mechanismen und Kinetik ist in der Regel auf das Ensemble oder makroskopischen Ebene mit Enzym Bevölkerung in die Tausende bis Millionen von Molekülen, erhalten wo Messungen einen statistischen Durchschnitt darstellen. Es ist jedoch bekannt, dass komplexe Makromoleküle wie Enzyme Heterogenität in ihrem Verhalten zeigen können und molekulare Mechanismen beobachtet auf der Ensemble-Ebene nicht unbedingt für jedes Molekül gelten. Solche Abweichungen der einzelnen Molekül-Skala wurden weitgehend durch Studien der einzelnen Enzyme mit einer Vielzahl von Methoden, die in den letzten zwei Jahrzehnten1bestätigt. Vor allem, wurde Fluoreszenz-Detektion von einzelnen Enzymaktivität zur Heterogenität der Enzyme Aktivität2,3 zu untersuchen oder entdecken den sogenannten Memory-Effekt (Perioden der hohen Enzyme Tätigkeit ist es gelungen, durch Zeiten der niedrigen Aktivität und umgekehrt)4,5.
Viele einzelne Enzymstudien erfordern, dass die Enzyme auf der Oberfläche oder räumlich feste auf andere Weise ausreichend lange in das Sichtfeld für kontinuierliche Beobachtung bleiben immobilisiert sind. Enzym-Kapselung in Liposomen nachweislich Enzym Immobilisierung und verhindern, dass mögliche negative Auswirkungen aufgrund der Oberfläche-Enzym oder Protein-Protein Interaktionen6,7zu aktivieren. Darüber hinaus bieten die Liposomen eine einzigartige Möglichkeit einzelne Membranproteine in ihrer natürlichen Lipid Bilayer Umwelt8,9,10zu studieren.
Eine Klasse von Membranproteinen, Transporter, übt eine direktionale Translokation von Stoffen über die Zellmembran, ein Verhalten, das nur untersucht werden kann, wenn Proteine in der Lipid Bilayer (z.B. Liposome)11wieder hergestellt werden, 12,13. Zum Beispiel spielt Protonen-Translokation, ausgestellt durch mehrere Enzyme von prokaryotischen und eukaryotischen Elektronentransport Ketten, eine wichtige Rolle in der Zellatmung durch die Schaffung einer Proton-treibende Kraft für die ATP-Synthese verwendet. In diesem Fall ist das Proton Pumpen Aktivität an den Elektronentransfer gekoppelt, obwohl der genaue Mechanismus dieses Prozesses oft schwer fassbar bleibt.
Vor kurzem haben wir die Möglichkeit, paar Fluoreszenz-Detektion mit Elektrochemie, Proton, die Aktivität der einzelnen Enzyme von der Klemme Ubiquinol-Oxidase von Escherichia coli (Cytochrom Bo3) Pumpen zu studieren die Liposomen14wieder hergestellt. Dies wurde erreicht durch Verkapselung von einer pH-Sensitive Membran undurchlässig Leuchtstofffärbung in das Lumen der Liposome aus E. vorbereitet coli polaren Lipide (Abbildung 1A). Die Protein-Menge wurde optimiert, so dass die meisten Liposomen entweder keinen oder nur einen rekonstituierte Enzym-Molekül (nach Poisson-Verteilung) enthalten. Die beiden Substrate von Cytochrom Bo3 wurden zur Verfügung gestellt, indem Sie die Lipid-Mischung, die die Liposomen und (ambient) Sauerstoff in Lösung gebildet Ubiquinon hinzufügen. Die Liposomen sind dann dünn auf einer halbtransparenten ultrasanfte gold Elektrode, bedeckt mit einer selbst-zusammengebauten monomolekularen Film des 6-Mercaptohexanol adsorbiert. Zu guter Letzt wird die Elektrode an der Unterseite einer einfachen Spectroelectrochemical Zelle (Abbildung 1 b) montiert. Elektrochemische Quinone Pool Redox staatlicher Kontrolle erlaubt es flexibel auslösen oder die enzymatische Reaktion jederzeit zu stoppen, während der pH-Sensitive Farbstoff zur pH-Wert-Änderungen in das Lumen der Liposomen durch Protonen-Translokation durch Überwachung dient der Enzyme. Durch die Verwendung der Fluoreszenzintensität von einem zweiten und Lipid gebundener Fluoreszenzfarbstoff, die Größe und das Volumen der einzelnen Liposomen kann ermittelt werden und somit die Quantifizierung des Enzyms Proton Pumpen Aktivität. Mit dieser Technik fanden wir vor allem, dass Cytochrom Bo3 Moleküle in der Lage sind, einen spontanen Leck Zustand zu schließen, die schnell verflüchtigt sich die Protonen treibende Kraft. Das Ziel dieses Artikels ist es, die Technik der einzelnen Liposomen Messungen im Detail vorstellen.
Protokoll
1. Vorbereitung der Lipid/UQ-10/FDLL Mischung
Hinweis: E. coli Lipide die Liposomen Vorbereitung soll regelmÄÑig und gründlich gemischt mit Ubichinon-10 (Enzym-Substrat) und langwellige fluoreszierenden Farbstoff-markierten Lipide (für Liposomen Größenbestimmung) vor der Rekonstitution.
- Mit einer Glasspritze, Transfer 200 µL Chloroform Bestand an Lipid polar extrahiert aus Escherichia coli (25 mg/mL) in Glasfläschchen, 5 mg Aliquote zu machen.
- Fügen Sie 50 µL von 1 mg/mL Ubichinon-10 (UQ-10; in Chloroform) zu den Lipiden zu endgültigen Verhältnis UQ-10: Lipide 1: 100 (1 % w/w).
- Die Lipide/UQ-10 Mischung 20 µL von 1 mg/mL (0,4 % w/w) eine langwellige fluoreszierenden Farbstoff-markierten Lipid (FDLL) hinzufügen.
- Homogenisieren Sie die Chloroform-Lösung von kurz aufschütteln zu und verdampfen Sie die meisten Chloroform durch eine sanfte Stickstoff oder Argon fließen. Entfernen Sie die Chloroform Spuren ganz durch weitere Verdampfung unter Vakuum für mindestens 1 h.
Hinweis: Lipid Aliquote können unter inerter Atmosphäre bei-20 ° C für mehrere Monate gespeichert werden.
2. Wiederherstellung der Cytochrom Bo3
Hinweis: Für die Reinigung von Cytochrom Bo3 aus E. Coli, führen Sie das Protokoll von Rumbley Et Al. Fügen Sie 15 um hohe Reinheit des nativ gefaltet Enzym Proben zu gewährleisten, Größe-Ausschluss Chromatographie nach der Affinität Reinigungsschritt von Rumbley Et Al. beschrieben 15
- Fügen Sie 312.5 µL 40 mm MOPS-KOH/60 mM K2SO4, pH 7,4, bis ein Aliquot der Lipide/UQ-10/FDLL trocken (5 mg, Schritt 1.4) mischen und mit Vortex mischen, bis die Lipid-Film vollständig Nukleinsäuretablette ist, gefolgt von 2 min Behandlung in ein Ultraschallbad.
- Fügen Sie 125 µL 25 mM 8-Hydroxypyren-1,3,6-Trisulphonic Säure (HPTS), einem pH-sensitiven Fluoreszenzfarbstoff, die in Liposomen verkapselt werden muss.
- 137,5 µL 250 mM n-Octyl β-D-Glucopyranoside (OGP) Tensid, mischen mit Wirbel und in ein Ultraschall-Wasserbad für 10 min um sicherzustellen, dass alle Lipide in Tensid Micellen solubilisiert werden beschallen. Übertragen Sie die Dispersion in einem 1,5 mL Plastikrohr.
Hinweis: Trübe Suspension von Lipiden sollte nach der Solubilisierung mit Tensid durchsichtig. - Fügen Sie die erforderliche Menge an Cytochrom Bo3 (siehe Hinweis unten) und Reinstwasser zu einem Gesamtvolumen von 50 µL (Cytochrom Bo3 Lösung plus Wasser) hinzufügen. Bei 4 ° C für 10 min auf einem Roller-Mixer inkubieren.
Hinweis: Typisch für einzelne Enzym Bedingungen beträgt 0,1-0,2 % (w/w Protein-Lipid, dh. 5 – 10 µg Protein), obwohl es bis zu 1 – 2 % (50 – 100 µg Protein) erhöht werden kann, wenn das Ziel ist es, nur die elektrochemische Aktivität (siehe unten) zu beobachten. Als Negativkontrolle können Liposomen ohne Cytochrom Bo3 vorbereitet werden. - 2 x 50 mg und 2 x 100 mg Polystyrol Microbeads in vier 1,5 mL-Tube Kappen wiegen und schließen mit Paraffin Film um Austrocknen zu verhindern.
Hinweis: Vor Gebrauch, Polystyrol Microbeads mit Methanol gewaschen werden, Wasser und im Wasser nach Anleitung des Herstellers gespeichert.
Hinweis: Wenn ein Wasser/Microbead-Gemisch verwendet wird, kann Polystyrol Microbeads bequem an der Kappe mit einer Mikropipette mit einer breiten Spitze übertragen. Wasser kann dann aus der Microbeads mit einer Mikropipette mit einer dünnen Spitze entfernt werden. - Fügen Sie 1St50 mg Polystyrol Microbeads in die Rekonstitution Mischung (Schritt 2.4), indem man die Kappe mit Polystyrol Microbeads auf 1,5 mL-Kunststoff-Tube mit Dispersion und eine kurze Spritztour für ein paar Sekunden durchführen. Bei 4 ° C auf einem Roller-Mixer für Polystyrol Microbeads zu adsorbieren, das Tensid für 30 mininkubieren.
- Wiederholen Sie die Ergänzungen von Polystyrol Microbeads und Inkubationen wie folgt: Fügen Sie 50 mg von Microbeads für 60 min Inkubation; Hinzufügen von 100 mg Microbeads für 60 min Inkubation; und 100 mg Microbeads für 120 min Inkubation hinzufügen.
Hinweis: Die Lösung über die abgerechneten Microbeads transluzente während Schritt 2.6 schaltet wie Proteoliposomes gebildet werden.
- Wiederholen Sie die Ergänzungen von Polystyrol Microbeads und Inkubationen wie folgt: Fügen Sie 50 mg von Microbeads für 60 min Inkubation; Hinzufügen von 100 mg Microbeads für 60 min Inkubation; und 100 mg Microbeads für 120 min Inkubation hinzufügen.
- Trennen Sie die Proteoliposome-Lösung von der Polystyrol Microbeads mit einer Mikropipette mit einer dünnen Spitze. Verdünnen Sie die Dispersion in 90 mL 20 mm MOPS-KOH/30 mM K2SO4, pH 7.4 (MOPS-Puffer) und Transfer in ein Ti45 Ultrazentrifuge Rohr.
- Ultrazentrifuge die Dispersion mit Typ 45 Ti Rotor bei 125.000 x g (bei rmax) für 1 h nach der Proteoliposomes pellet.
Hinweis: Kleinere Zentrifuge Röhren können verwendet werden, obwohl die Verdünnung in großen Puffervolumen hilft, um die Konzentration der gossene HPTS zur endgültigen Sperrung zu reduzieren. - Entsorgen Sie den Überstand, spülen Sie die Pellets mit 20 mM MOPS-KOH/30 mM K2SO4, pH-Wert 7,4 gepuffert (ohne resuspending das Pellet). Nach der Spülung Puffer verwerfen, wieder aussetzen Sie die Proteoliposomes in 500 µL MOPS-Puffer durch pipettieren sie hin und her mit dünnen Spitze Mikropipette. Anschliessend transfer zum 1,5 mL-Kunststoff-Rohr.
- Zentrifugieren Sie die Suspension für 5 min bei 12.000 x g, die Ablagerungen zu entfernen. Den überstand (rekonstituierten Proteoliposomes) in ein neues Fläschchen zu übertragen.
- Speichern Sie die wiederhergestellten Proteoliposomes Dispersion bei 4 ° C über Nacht und innerhalb von 2 Tagen aufbrauchen.
3. Herstellung von semi-transparenten Gold-Elektroden
Hinweis: Die glatte Oberfläche gold erhält man durch eine Template-stripping-Methode aus einer 30 nm dicke Schicht von 99,99 % Gold aus einem atomar glatte Silizium-Wafer. Die geringen Dicke der Goldschicht ist wichtig, da es halbtransparent, um Fluoreszenz Beobachtung erlaubt sein muss. Details zu gold Verdunstung (physische Aufdampfen, PVD) finden an anderer Stelle16 und einzige Vorlage-stripping wird hier behandelt. Alternativ können ultra-glatte gold Chips anderswo erworben werden (siehe Tabelle der Materialien).
- Kleben Sie bis zu 9 Glas Deckel rutscht (0,17 mm dick) auf die verdampfte Goldoberfläche mit Bi-Komponenten Low-Fluoreszenz Epoxy ein. Den Klebstoff bei 80 ° C für 4 h zu heilen.
- Kurz vor Modifikation mit einem selbst-zusammengebauten monomolekularen Film (Schritt 4) trennen Sie das Glas Deckel rutscht aus der Silizium-Wafer mit einer Klinge. Durch die dünne Abdeckung rutscht Vorsicht beim Abnehmen des Abdeckung rutscht um nicht knacken oder brechen die Glas-Folien.
4. Änderung der Goldoberfläche mit selbst-zusammengebauten Monolayer (SAM)
- 5 mL Wasser-Lösung von 1 mM 6-Mercaptohexanol (6MH) vorzubereiten.
- 6MH Lösung frisch freistehende Gold-beschichteter Deckel rutscht (Schritt 3.1) eintauchen und lassen Sie über Nacht bei 20 – 25 ° C (> 16 h), die SAM zu bilden.
Hinweis: Thiol-Lösungen haben einen unangenehmen Geruch, einem geschlossenen Gefäß sollte verwendet werden, wenn das Gold-beschichteter Deckglas zu bebrüten. - Am nächsten Tag entfernen Sie das Gold-beschichteter Deckglas aus der 6MH-Projektmappe, kurz waschen Sie, mit Wasser oder Methanol und Isopropanol. Unter einem sanften Gasstrom trocken.
5. elektrochemische Prüfung der Proteoliposomes-Aktivität
Hinweis: Die elektrochemische Aktivität des Enzyms wird zunächst auf einer dicht gepackten Liposomen-Schicht (Schritt 5) überprüft und unteren Vesikel Deckungen dienen in einzelne Vesikel Experiment zur Messung pH-Veränderungen in das Lumen der Liposome (Schritt 6).
- Montieren Sie das Gold-beschichteter Deckglas in einer Spectro-elektrochemische Zelle (siehe Abbildung 1). Stellen Kontakt zu Gold mit einem flachen Draht außerhalb einer Fläche definiert ein Gummi o-Ring.
- Fügen Sie 2 mL der Pufferlösung Elektrolyt hinzu und platzieren Sie der Referenz- und zusätzliche Elektroden in der Zelle.
Hinweis: Weitere im Diskussion Abschnitt diskutiert, werden Referenzen Elektroden ohne Chlorid bevorzugt verhindert Bildung von Au (I) Cl während der Elektrochemie. Hier, eine Hg/Hg2SO4 (SA. K2SO4) Bezugselektrode dient und Potenziale erhalten im Vergleich zu Standard-Wasserstoff-Elektrode (SHE) mit 0,658 V Vs SHE für Hg/Hg2SO4 (sat. K2SO4). - Laufen Sie elektrochemische Impedanz Spektroskopie (0,1 Hz – 100 kHz) bei open-Cell potenzielle (OCP) Potenzial zur Bewertung der Qualität von SAM. Eintritt Impedanzwerte umwandeln und teilen Sie durch 2πω zu einen Cole-Cole-Plot, Plotten, wo ω die Frequenz ist (siehe die folgenden Referenzen16,17,18 Einzelheiten zu konvertieren und Interpretation der Impedanz Spektren).
Hinweis: Sollte kompakt und dicht SAMs von 6MH Halbkreis Cole-Cole-Plot eine enge verleihen und geben Werte der Kapazität im Bereich von 2,5 bis 3,0 µF/cm2 (Abbildung 2A). Wenn signifikante Abweichung von Halbkreis Form oder Out-of-Range-Kapazität Werte erhalten werden, ändern Sie die Elektrode. - Führen Sie leere zyklische Voltammograms (CVs) mit Scan Rate 100 und 10 mV/s in der potenziellen Region -0,3-0,8 V. Ein typischer Lebenslauf zeigt (Abb. 2 b, gestrichelten Linie).
Hinweis: Dies sollte fast reine kapazitives Verhalten und das Fehlen von erheblichen faradaic Strom, auch unter ambient Sauerstoffbedingungen demonstrieren, wie hier verwendet. - Die elektrochemische Zelle Proteoliposomes (0,5 mg/mL letzte Lipide Konzentration, 1-2 % (w/w) Verhältnis von Cytochrom Bo3 , Lipid) hinzu und mischen Sie leicht mit einer Pipette. Warten Sie, bis die Adsorption von Proteoliposomes auf der Elektrodenoberfläche ist fertig (30-60 min bei Raumtemperatur).
Hinweis: Zyklische Voltammograms (CVs) bei 10 mV/s führen während der Proteoliposomes-Adsorption, den Prozess zu folgen. Die Adsorption ist beendet, wenn aufeinander folgende CVs nicht mehr ändern. Informationen über CV-Techniken finden Sie in den folgenden Lehrbüchern. 19 , 20 - Waschen Sie die Zelle durch eine Änderung der Pufferlösung mindestens 10 Mal aber zu vermeiden Sie, so dass der Elektrodenoberfläche komplett trocken.
- Führen Sie die elektrochemische Impedanz Spektroskopie am OCP (Abb. 2A, blaue Linie) zu bestätigen, dass SAM auf die Elektrode gold unverändert bleibt und CVs mit scan Preise 10 und 100 mV/s Ubiquinol katalytische Oxidation (und Sauerstoffreduktion) von Cytochrom beobachten Bo 3 Beginn Potenziale der elektrochemischen Quinone Reduktion über 0 V Vs SHE) (Abb. 2 b).
6. Nachweis von enzymatischen Proton Pumpen durch Fluoreszenz-Mikroskopie
- Ändern Sie die gold-Elektrode wie in Schritt 5, aber mit 100 x weniger Proteoliposomes im Vergleich zu Schritt 5.5 (d.h. 5 µg/mL). Für einzelne Enzymstudien, reduzieren die Cytochrom Bo3 Lipid-Verhältnis auf 0,1-0,2 % (w/w).
Hinweis: Liposomen werden dünn auf der Elektrodenoberfläche eine einzelne Vesikel Überwachung durch Fluoreszenzmikroskopie ermöglichen adsorbieren. Unter diesen Single-Enzym ist die Menge des Enzyms immobilisiert auf der Elektrodenoberfläche unzureichend für die Beobachtung eines katalytischen Stroms. - Legen Sie die elektrochemische Zelle auf das Öl Ziel (60 X) eine invertierte Fluoreszenzmikroskop mit einem Tropfen Immersionsöl. Mit entsprechenden Filtern für FDLL Fluoreszenz, konzentrieren Sie sich auf der Elektrodenoberfläche. Einzelne Liposomen sollte als helle Flecken an die Beugungsgrenze das Mikroskopobjektiv angezeigt werden. Nehmen Sie ein Bild der FDLL Fluoreszenz.
- Wechseln zu einem HPTS Fluoreszenz-Filter-Sets auf dem Mikroskop, ob HPTS Fluoreszenz sichtbar und deutlich vom Hintergrund zu unterscheiden ist (an die gewählte Belichtungszeit, siehe Punkt 6.4). Die Lichtintensität zu erhöhen, wenn es nicht der Fall ist.
- Programmieren die Mikroskop-Software eine zeitgesteuerte Bildaufnahme auszuführen, indem abwechselnd zwei HPTS Filtersätze (Menü Anwendungen | Define/Run ND Erwerb). Legen Sie die Verzögerung zwischen Bild Akquisitionen auf Minimum. Verwenden Sie in diesem Experiment ein 1 s-Exposition und 0,3 s Verzögerung (aufgrund der Revolver-Bewegung).
Hinweis: Das Verhältnis zwischen Fluoreszenz-Intensitäten auf diese beiden Kanäle wird später in pH-Wert innerhalb der Liposomen zu jedem Zeitpunkt konvertiert werden. Die Dauer des Erwerbs variieren entsprechend der erwarteten pH-Wert Änderungsrate; 5 min in diesem Artikel verwendet. - Passen Sie die Einstellungen von dem Potentiostaten um das Potential während der Bildaufnahme zu ändern. In diesem Experiment, z. B. die folgende Sequenz: 0 – 60 s: kein Potential angelegt (d.h. OCP); 60 – 180 s: -0,2 V (Vs SHE); 180 – 300 s: 0,4 V (Vs SHE). In diesem Fall nur das angewandte Potenzial in der zweiten Phase (-0,2 V Vs SHE) ist ausreichend, um effizient die Quinone Pool reduzieren.
- Führen Sie gleichzeitig den zeitgesteuerten Bilder Erwerb (Mikroskop) und die mögliche Abfolge (Potentiostaten) durch manuelles starten beide Messungen zur gleichen Zeit.
Hinweis: Das Experiment kann auf die gleichen Elektrode mehrmals wiederholt werden durch verschieben den Mikroskoptisch in einen anderen Bereich auf der Oberfläche. Die Verzögerung zwischen den Akquisitionen sollte mindestens 5-10 min, komplette pH Gleichgewichtherstellung von Liposomen auf der Oberfläche zu versichern. Unterschiedlicher Dauer und mögliche Muster können je nach Bedarf, angewendet werden, obwohl imaging Zeit während der Akquisition durch Immunofluoreszenz HPTS begrenzt ist.
7. Analyse der Fluoreszenzbilder
Hinweis: Ein typisches Experiment erzeugt eine Reihe von Bildern mit einem Zeitschritt (z. B. 2,6 s) für jeden der beiden Kanäle, d. h. (Dauer * 2 / 2,6) Bilder. Ein Beispiel für solche Stellen Sie während ein einziges Enzym-Experiment aufgezeichneten Bild kann über die Forschung Daten Leeds Repository21zugegriffen werden. Eine Bild-Behandlung besteht aus mehreren Schritten mithilfe von Fidschi (ImageJ) und allgemeine mathematische Analyse Programmier-Sprache Software (im folgenden zur Tabelle der Materialien als scripting Software, Näheres siehe bezeichnet).
- Verwenden Sie Fidschi Zeit verfallen Datei zu trennen, Bilder ausrichten und speichern als separate Kanäle und Zeitrahmen.
- Offene Zeit verfallen Datei mithilfe des Bioformats-Importeurs innerhalb von Fidschi (Makro-Befehl: laufen ("Bio-Formate Importeur")).
- Verwenden Sie das Plugin StackReg um jeden Frame mit dem ersten Stadium Bewegungen berücksichtigen auszurichten oder Temperaturdrift ist aufgetreten beim Erwerb (Makro-Befehl: laufen ("StackReg", "Transformation = Übersetzung")).
- Speichern Sie separate unkomprimiertes Image-Dateien für jeden Kanal und jedem Zeitschritt im TIFF-Format in einem Ordner.
- Extrahieren Sie die genauen Zeitstempel für jeden Frame aus der Zeit verfallen Dateimetadaten und speichern Sie sie als CSV-Datei in demselben Ordner wie die Bilder. Alternativ extrahieren Sie Zeitstempel mit der Datenerfassungs-Software zu und speichern Sie manuell in eine CSV-Datei mit einem Tabellenkalkulationsprogramm.
Hinweis: Der Ordner mit Bildern und Zeitstempel ist nun bereit, durch die scripting Software analysiert werden. 7.1.1 Schritte. – 7.1.4. mit einem Fidschi-Skript automatisiert werden kann (ein Skript in Python geschrieben, für Batch-Verarbeitung von Time Lapse Dateien vorgesehen ist, verwenden Sie "Strg-Shift-N" (in Windows), dann Datei | Offene , das Skript zu laden).
- Verwenden Sie scripting Software für die automatisierte Verarbeitung der Bilder. Laden Sie den bereitgestellten Code der Software und klicken Sie auf Run zu Ende. Wenn Sie aufgefordert werden, wählen Sie den Ordner mit den Bildern aus Schritt 7.1.
Hinweis: Ein Skript für die Analyse wird als Mlx-Format live Skript mit ausführlichen Anmerkungen zu identifizieren einzelne Liposomen, passen sie auf 2D-Gauß-Funktion, Filtern und quantifizieren die pH-Werte zu jedem Zeitpunkt bereitgestellt. Die folgenden Teilschritte werden durch das Skript automatisch ausgeführt.- Laden Sie alle Zeiträume Bilder für ein einzelnes Experiment in den Speicher.
- Im Durchschnitt alle Bilder für einen einzelnen Kanal (Wählen Sie den Kanal mit der höchsten Fluoreszenzintensität) und der gemittelte Bild verwenden, um alle Maxima zu identifizieren, die die einzelnen Liposomen entsprechen könnte.
- Passform der identifizierten Maxima auf das gemittelte Bild 2D-Gauß funktionieren und speichern das Ergebnis passt Parameter für jedes Liposomen (siehe Abbildung 4A z.B. ausgestattete Liposomen).
- Filtern Sie die Höchstwerte nach den erwarteten einzelne Liposomen Kriterien, wie Größe, Rundheit und Intensität. Ablehnen, Liposomen, die aufgrund der geringen Signal-Rausch schlecht ausgestattet sind, eng benachbarten Liposomen oder auch nahe an den Bildrand.
- Laden Sie Zeitstempel aus der externen Datei und passen Sie jedes gefilterte Liposomen der 2D-Gauß-Funktion auf jedem Zeitrahmen Bild separat.
Hinweis: Die Verwendung der Parallelprogrammierung und multicore CPU kann erheblich verbessern die Rechengeschwindigkeit zu diesem Zeitpunkt. - Filtern Sie die Liposomen wieder nach ähnlichen Kriterien wie in Schritt 7.2.4 aber angewendet auf jedem Zeitrahmen.
- Definieren Sie auf jedem Zeitschritt die Fluoreszenz Intensitätsverhältnis ein Liposom als das Verhältnis der Volumina ausgestattete 2D Gauß-Funktion in zwei Kanälen umgeben. Berechnen Sie die pH-Werte aus dem Verhältnis der Intensitäten ermittelt aus den beiden HPTS Kanälen und mit Hilfe einer Eichkurve (Schritt 8). Plot resultierende pH-Zeit-Verläufe für die Liposomen und beobachten Sie ihren pH-Wert ändern, wenn das Potential anliegt.
8. Durchführung einer Kalibrationskurve HPTS Fluoreszenz
Hinweis: HPTS Fluoreszenz-Verhältnis in einem intravesicular pH-Wert konvertieren möchten, muss eine Kalibrierungskurve zunächst festgestellt werden, dass die besondere Bedingungen der Experimente wie gold Transmission, Filter Qualität usw.berücksichtigen würde. Dieser Schritt muss nur einmal oder zweimal durchgeführt werden und die Kalibrierdaten können verwendet werden, solange die Parameter Setup und Messung in Schritt 6 unverändert.
- Bereiten Sie eine Elektrode mit dünn adsorbierten Liposomen (ohne Cytochrom Bo3 wie in den Schritten 5 und 6.1 beschrieben).
- 2 mL des Puffers erstelle ich die Konzentration 100 ng/mL fügen Sie 2 µL von 0,1 mg/mL Gramicidin Lösung in Ethanol hinzu.
- Zwei Fluoreszenzbilder für die beiden HPTS Kanäle zu erfassen.
- Ändern Sie den pH-Wert der Zelle durch Zugabe von kleinen Aliquote 1 M HCl oder 1 M H2SO4. Messen Sie den pH-Wert des Puffers mit einem standard-pH-Meter und erfassen Sie zwei Fluoreszenzbilder für die beiden HPTS Kanäle zu.
- Wiederholen Sie die Schritte 8,4 für den pH-Bereich 6 bis 9.
- Mit dem Algorithmus von 7,2, passen, zu filtern und die durchschnittliche HPTS Fluoreszenz Verhältnis zwischen einzelnen Liposomen bei jedem pH-Wert zu berechnen. Übernehmen Sie die HPTS Verhältnis durchschnittlich alle Liposomen.
- Passen Sie die resultierende pH-Verhältnis-Abhängigkeit, die folgende Gleichung:
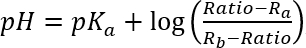 , wo pKein, Rein und Rbsind passende Parameter.
, wo pKein, Rein und Rbsind passende Parameter. - Verwenden Sie pKein, Rein und Rbdas HPTS Verhältnis der einzelnen Liposomen in Schritt 7.2.7 zu konvertieren. auf pH-Werte.
Ergebnisse
Die Qualität des Gold-modifizierte Deckglases (Elektrode) mit einem SAM 6MH wird vor jedem Experiment mit elektrochemische Impedanz Spektroskopie überprüft. Abbildung 2A zeigt repräsentative Cole-Cole-Grundstücke mit elektrochemische Impedanz Spektroskopie vor und nach der Liposomen adsorbiert werden gemessen. Wenn die Qualität der SAM ausreicht, sollte Impedanz Spektroskopie ein fast reines kapazitives Verhalten, was zu einem Halbkreis Cole-Cole-Grunds...
Diskussion
Die beschriebene Methode eignet sich studieren Proton Pumpen durch respiratorische Membranproteine, die in Liposomen wiederhergestellt werden können und sind in der Lage, Elektronen mit dem Quinone Pool austauschen. Protonen-Pumpen-Aktivität kann auf der Single-Enzym-Ebene mit pH-Sensitive (ratiometrischen) Farbstoffe in den Liposomen Lumen (Abbildung 1A) gekapselt überwacht werden.
Die Methode beruht auf der Fähigkeit von Ubichinon (oder andere Quinones), in ...
Offenlegungen
Die Autoren haben nichts preisgeben.
Danksagungen
Die Autoren erkennen die BBSRC (BB/P005454/1) für die finanzielle Unterstützung. NH wurde durch VILLUM Foundation Young Investigator Programm finanziert.
Materialien
| Name | Company | Catalog Number | Comments |
| 6-Mercapto-1-hexanol (6MH) | Sigma | 451088 | 97% |
| 8-hydroxypyrene-1,3,6-trisulphonic acid (HPTS) | BioChemika | 56360 | |
| Aluminium holder (Electrochemical cell) | Custom-made | 30x30x7 mm; inner diameter: 26 mm; hole diameter: 15 mm | |
| Auxiliary electrode | platinum wire | ||
| Chloroform | VWR Chemicals | 83627 | |
| E.coli polar lipids | Avanti | 100600C | 25 mg/mL in chloroform |
| Epoxy | EPO-TEK | 301-2FL | low fluorescence epoxy |
| Fiji (ImageJ 1.52d) | Required plugins: StackReg and TurboReg (http://bigwww.epfl.ch/thevenaz/stackreg/) | ||
| Filter cube ("ATTO633") | Chroma Technology Corporation | Ex: 620/60 nm; DM: 660 nm; Em: 700/75 nm | |
| Filter cube ("HPTS1") | Chroma Technology Corporation | Ex: 470/20 nm; DM: 500 nm; Em: 535/48 nm | |
| Filter cube ("HPTS2") | Chroma Technology Corporation | Ex: 410/300 nm; DM: 500 nm; Em: 535/48 nm | |
| Filter cube ("Texas Red") | Chroma Technology Corporation | Ex: 560/55 nm; DM: 595 nm; Em: 645/75 nm | |
| Fluorescent dye-labelled lipids (FDLL) | ThermoFisher Scientific | T1395MP | TexasRed-DHPC was used in this work (λexc 595 nm; λem 615 nm) |
| Fluorescent dye-labelled lipids (FDLL) (alternative) | ATTO-TEC | AD 633-161 | ATTO633-DOPE can be used as alternative (λexc 630 nm; λem 651 nm) |
| Gel filtration column | GE Healthcare | 28-9893-33 | HiLoad 16/600 Superdex 75 pg, for additional protein purification |
| Glass coverslips | VWR International | 631-0172 | No 1.5 |
| Glass syringe | Hamilton | 1725 RNR | 250 µL |
| Glass vials | Scientific Glass Laboratories Ltd | T101/V1 | 1.75 mL capacity |
| Gold | GoodFellow | 99.99% | |
| Gramacidin | Sigma | G5002 | |
| Mercury sulfate reference electrode | Radiometer (Hash) | E21M012 | |
| Microcentrifuge | Eppendorf | Minispin NL040 | |
| Microscope | Nikon | Eclipse Ti | |
| Microscope Camera | Andor | Zyla 5.5 sCMOS | |
| Microscope Lamp | Nikon | Intensilight C-HGFI | |
| NIS-Elements AR 5.0.2 | Nikon | Microscope acquisition software | |
| n-Octyl β-D-glucopyranoside | Melford Laboratories | B2007 | |
| Nova 1.10 | Metrohm | Potentiostat control software | |
| Objective | Nikon | Plan Apo λ 60x/1.4 oil | |
| OriginPro 2017 | OriginLab | Plotting software | |
| O-ring (Electrochemical cell) | Orinoko | Inner diameter: 16 mm; cross section: 1.5 mm | |
| Plastic tubes | Eppendorf | 3810X | 1.5 mL |
| Polystyrene microbeads | Bio-RAD | 152-3920 | Biobeads, 20-50 mesh |
| Potentiostat | Metrohm Autolab | PGSTAT 128N | |
| Potentiostat | CH Instruments | CHI604C | |
| Scripting software | Matlab | R2017a | Required toolboxes: 'Image Processing Toolbox', 'Parallel Computing Toolbox', 'Curve Fitting Toolbox', 'System Identification Toolbox', 'Optimization Toolbox' |
| Silicon wafers | IDB Technologies LTD | Si-C2 (N<100>P) | Ø 25 mm, 525 um thick |
| Teflon cell (Electrochemical cell) | Custom-made | Outer diameter: 26 mm; inner diameter: 13.5 mm | |
| Temple-Stripped Ultra-Flat Gold Surfaces | Platypus Technologies | AU.1000.SWTSG | Alternative ready-to-use ultra-flat gold surfaces (Thickness below 100 nm on demand) |
| Thin micropipette tips | Sarstedt | 70.1190.100 | or similar gelloader tips 200 µL |
| Ubiquinone-10 | Sigma | C-9538 | |
| Ultracentrifuge | Beckman-Coulter | L-80XP | with Ti 45 rotor |
| Ultrasonic bath | Fisher Scientific | FB15063 |
Referenzen
- Claessen, V. I., et al. Single-Biomolecule Kinetics: The Art of Studying a Single Enzyme. Annual Review of Analytical Chemistry. 3 (1), 319-340 (2010).
- Rojek, M. J., Walt, D. R. Observing Single Enzyme Molecules Interconvert between Activity States upon Heating. PLoS ONE. 9 (1), e86224 (2014).
- Velonia, K., et al. Single-Enzyme Kinetics of CALB-Catalyzed Hydrolysis. Angewandte Chemie International Edition. 44 (4), 560-564 (2005).
- Lu, H. P., Xun, L., Xie, X. S. . Single-molecule enzymatic dynamics. 282 (5395), 1877-1882 (1998).
- Engelkamp, H., Hatzakis, N. S., Hofkens, J., De Schryver, F. C., Nolte, R. J. M., Rowan, A. E. Do enzymes sleep and work?. Chemical Communications. 9 (9), 935-940 (2006).
- Boukobza, E., Sonnenfeld, A., Haran, G. Immobilization in Surface-Tethered Lipid Vesicles as a New Tool for Single Biomolecule Spectroscopy. The Journal of Physical Chemistry B. 105 (48), 12165-12170 (2001).
- Hsin, T. -. M., Yeung, E. S. Single-Molecule Reactions in Liposomes. Angewandte Chemie International Edition. 46 (42), 8032-8035 (2007).
- García-Sáez, A. J., Schwille, P. Single molecule techniques for the study of membrane proteins. Applied Microbiology and Biotechnology. 76 (2), 257-266 (2007).
- Onoue, Y., et al. A giant liposome for single-molecule observation of conformational changes in membrane proteins. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1788 (6), 1332-1340 (2009).
- Jefferson, R. E., Min, D., Corin, K., Wang, J. Y., Bowie, J. U. Applications of Single-Molecule Methods to Membrane Protein Folding Studies. Journal of Molecular Biology. 430 (4), 424-437 (2018).
- Rigaud, J. L., Pitard, B., Levy, D. Reconstitution of membrane proteins into liposomes: application to energy-transducing membrane proteins. BBA - Bioenergetics. 1231 (3), 223-246 (1995).
- Jesorka, A., Orwar, O. Liposomes: Technologies and Analytical Applications. Annual Review of Analytical Chemistry. 1 (1), 801-832 (2008).
- Seddon, A. M., Curnow, P., Booth, P. J. Membrane proteins, lipids and detergents: Not just a soap opera. Biochimica et Biophysica Acta - Biomembranes. 1666 (1-2), 105-117 (2004).
- Li, M., et al. Single Enzyme Experiments Reveal a Long-Lifetime Proton Leak State in a Heme-Copper Oxidase. Journal of the American Chemical Society. 137 (51), 16055-16063 (2015).
- Rumbley, J. N., Furlong Nickels, E., Gennis, R. B. One-step purification of histidine-tagged cytochrome bo3 from Escherichia coli and demonstration that associated quinone is not required for the structural integrity of the oxidase. Biochimica et Biophysica Acta (BBA) - Protein Structure and Molecular Enzymology. 1340 (1), 131-142 (1997).
- Jeuken, L. J. C., et al. Phase separation in mixed self-assembled monolayers and its effect on biomimetic membranes. Sensors and Actuators, B: Chemical. 124 (2), 501-509 (2007).
- Barsoukov, E., Macdonald, J. R. . Impedance Spectroscopy Theory, Experiment, and Applications. , (2005).
- Jeuken, L. J. C., Connell, S. D., Henderson, P. J. F., Gennis, R. B., Evans, S. D., Bushby, R. J. Redox Enzymes in Tethered Membranes. Journal of the American Chemical Society. 128 (5), 1711-1716 (2006).
- Compton, R. G., Banks, C. E. Chapter 4. Understanding voltammetry. , (2018).
- Girault, H. H. Chapter 10. Analytical and Physical Electrochemistry. , (2004).
- Mazurenko, I., Jeuken, L. J. C. . Timelapse (movie) of single vesicles fluorescence change upon potential application. , (2018).
- Li, M., Khan, S., Rong, H., Tuma, R., Hatzakis, N. S., Jeuken, L. J. C. Effects of membrane curvature and pH on proton pumping activity of single cytochrome bo3enzymes. Biochimica et Biophysica Acta - Bioenergetics. 1858 (9), 763-770 (2017).
- Li, M., Tuma, R., Jeuken, L. J. C. . MATLAB code for the analysis of proton transport activity in single liposomes. , (2017).
- Li, M., Tuma, R., Jeuken, L. J. C. . Time-resolved fluorescence microscopic data (traces) of individual lipid vesicles with proton transport activity. , (2017).
- Paula, S., Volkov, A. G., Van Hoek, A. N., Haines, T. H., Deamer, D. W. Permeation of protons, potassium ions, and small polar molecules through phospholipid bilayers as a function of membrane thickness. Biophysical Journal. 70 (1), 339-348 (1996).
- Brookes, P. S., Hulbert, A. J., Brand, M. D. The proton permeability of liposomes made from mitochondria) inner membrane phospholipids: No effect of fatty acid composition. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1330 (2), 157-164 (1997).
- Eriksson, E. K., Agmo Hernández, V., Edwards, K. Effect of ubiquinone-10 on the stability of biomimetic membranes of relevance for the inner mitochondrial membrane. Biochimica et Biophysica Acta - Biomembranes. 1860 (5), 1205-1215 (2018).
- Seneviratne, R., et al. A reconstitution method for integral membrane proteins in hybrid lipid-polymer vesicles for enhanced functional durability. Methods. , 1-8 (2018).
- Veshaguri, S., et al. Direct observation of proton pumping by a eukaryote P-type ATPase. Science. 351 (6280), 1-6 (2016).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten