Method Article
Entfernten Labor Management: Respiratorischen Virus-Diagnostik
In diesem Artikel
Zusammenfassung
Ein schnell einsetzbaren, off-Grid Labor wurde entworfen und für abgelegene, ressourcenbeschränkte globale Einstellungen gebaut. Die Eigenschaften und kritische Aspekte der logistisch verbessert, erweiterbar, multifunktionale Labormodule werden erforscht. Eine Checkliste für einen Labor-Workflow und ein Protokoll für die Atemwege virale diagnostischer Test entwickelt und vorgestellt.
Zusammenfassung
Einen Aufwärtstrend in den letzten Pandemien (Ebola, Zika, MERS, Grippe, etc.) betont die Notwendigkeit für eine weitere "flink" koordinierte Reaktion, die befasst sich mit eine Vielzahl von Themen von Transport, Zugang, Einrichtungen, Geräte und Kommunikation bis hin zu Anbieter Ausbildung. Zu diesem Zweck haben wir eine innovative, skalierbare, Logistik erweitert, mobile, Laboreinrichtung für Notfälle und Epidemien in den globalen Einstellungen ressourcenbeschränkte entwickelt. Nutzen einen Hintergrund im klinischen Betrieb als ein akademisches medizinisches Zentrum, wir eine schnell einsetzbaren, modulare BSL-2 und BSL-3 Anlage mit benutzerfreundlicher Software für Verfolgung und Verwaltung von Medikamenten und Verbrauchsmaterialien in abgelegenen Regionen während der Epidemien entworfen und Ausbrüche. Hier präsentieren wir Ihnen unsere intermodalen, mobil, erweiterbare Versandbehälter Laborgeräten. Das Design des Labors erleichtert Netznutzung durch Minimierung von Stromverbrauch und ermöglicht alternative Wasserquellen. Geräteinformationen Kommunikations-Technologie (IKT)-Plattform (i) benutzerfreundliches Tablet-basierte Dokumentation bietet (Ii) verstärkte Verfolgung von Patienten und Lieferungen und (Iii) Kommunikation vor Ort mit eingebauten Telehealth-Funktionen integriert. Um Qualität in remote-Umgebungen zu gewährleisten, haben wir eine Checkliste für einen Labor-Workflow und ein Protokoll für die Atemwege virale Diagnose mit Reverse Transkription Polymerase-Kettenreaktion (RT-PCR) entwickelt. Wie beschrieben, ermöglicht dieses innovativen und umfassenden Ansatz für die Bereitstellung von Labor-Fähigkeit in globalen Umgebungen beschränkten Ressourcen.
Einleitung
Schnelldiagnostik ist ein kritischer Instrument rechtzeitig virale Infektion Kontrolle, vor allem, wenn frühe Symptomatik eine Vielzahl von Infektionskrankheiten nicht zu unterscheiden ist. Die jüngsten Ebola-Ausbruch (2014-2015) in Westafrika1,2, Zika-Virus-Epidemien (2015-2016) in Asien und Lateinamerika3,4, die Entstehung des Nahen Osten respiratorische Syndrom (MERS) coronavirus Infektionen5,6, und die ungewöhnlich tödlichen Grippe (Influenza) Epidemien (2017-2018) in der US-7,8 deckte die Notwendigkeit schnell einsetzbaren, Laboreinrichtungen, die eine Vielzahl von Adresse Fragen von Transport, Zugang, Einrichtungen, Geräte und Kommunikation.
Off-Grid-Fähigkeit (autark mit Strom und Wasser-Versorgung, etc.) ist entscheidend in ländlichen, ressourcenbeschränkte globale Einstellungen9,10,11. Unsere Erfahrung im klinischen Betrieb und globale Programme am Baylor College of Medicine wurde entworfen und erstellt ein Container-basierte mobile Labor mit Funktionen für die einfache Bereitstellung, Einrichtung und multifunktionale Nutzung (BSL-2 und BSL-3) verwendet. Bilder von dieser vielseitigen, logistisch verbessert Laboreinrichtung ist in Abbildung 1dargestellt.
Diesem schnell einsetzbaren, Laboreinrichtung hat eine erweiterbare Design ähnlich wie die zuvor beschriebenen Container-Klinik (der "Emergency Smart Pod")12,13,14, entwickelt von Baylor College of Medicine und gesponsert von USAID. Eine verpackte Einheit (im Transportmodus) hat die Abmessungen von 9 9 Zoll x 8 Feet x 8 Fuß (Abb. 1A, B), und baut auf einer Fläche von 170 qm (15,75 m2) (Abbildung 1, D). Das Gerät kann von zwei bis vier Personen in weniger als zehn Minuten bereitgestellt werden.
Entfernte Labor ist für BSL-2 Lab Facility (Abbildung 2A) gebaut, mit einer separaten, modular, aufsteckbar, BSL-3-Einheit (Abb. 2 b) für die Arbeit mit Infektionserregern entworfen, die schweren oder lebensgefährlichen Krankheit durch Inhalation verursachen 15. die Verbindung der beiden Labormodule ermöglicht die Optimierung der Experimente Abläufe, gemeinsame Nutzung von Ressourcen und Kosten sparen (Abbildung 2 C-E).
Die Module sind luftdicht und wasserdicht, einen komfortablen, Energie effizienten mobilen Unterstand zu schaffen. Heizungs-, Lüftungs- und Klimaanlage (HVAC) dient zur zentralisierten und temperaturgeführte Einheiten. Im Allgemeinen wird das Design der Labor-Geräte Stromverbrauch durch die Verwendung von eigenen Alternativen Stromquellen wie Sonnenkollektoren und/oder einen unabhängigen elektrischen Generator minimiert. Jede Einheit beinhaltet ein Waschbecken und Augenwischerei-Station, Strom und Wasser Anschlüsse (Abb. 3A-C). Die IKT-Plattform bietet eine optionale Tablet-basierte (Android Handy/Tablet oder iPhone/iPad) Dokumentation app für Lieferung Tracking und Labor-Ergebnis-Dokumentation (Abbildung 3D) entwickelt in Partnerschaft mit Baylor Information Technology (IT) Forschungsgruppe, die erfahrene mit eingeschränkter Konnektivität in remote-Umgebungen arbeiten. Das System funktioniert mit dem Mobilfunk- oder WLAN-Signale und ermöglicht die Dokumentation ohne Konnektivität mit sofortige Sicherung oder Übertragung zu einem secure Cloud basierte Server wenn die Verbindung wieder hergestellt ist.
Das Labor hat mehrere wichtige Infektionskontrolle Eigenschaften einschließlich: (a) negative Druck Air Flow, (b) ein Handschuhfach oder biologische Sicherheit, (c) ein Risiko Gesundheitsmanagement Schranksystem: eine keimtötende UV (UV-C) Beleuchtungssystem, mit 4 Hierarchien der Verteidigung erwiesen 99,7 % der Krankheitserreger zu beseitigen, die gesundheitsbezogenen Infektionen verursachen. Die Anlage ist leicht mit Wasserstoffperoxid oder Natriumhypochlorit (Chlorid) Systeme für effiziente und effektive Dekontamination desinfiziert. 16
Die Sicherung der Qualität der Laborergebnisse hängt ein Bekenntnis zu allen Aspekten der Gesamtheit diagnostische Testverfahren zu beurteilen. Hier präsentieren wir eine Checkliste für den BSL-2 und3 BSL Labor-Workflow und ein Protokoll für schnellen Atemwege Virus diagnostischen Test. Die vorgeschlagenen Diagnose Viruserkrankungen beruht auf dem Nachweis von viraler RNA oder DNA-Probe (Nasenspülflüssigkeit, Blut, Stuhl und Urin, etc.) durch Echtzeit-Reverse Transkription Polymerase-Kettenreaktion (RT-PCR). Die Fähigkeit, schnell zu schätzen Viruslast in einem Exemplar macht PCR ein effizientes Werkzeug für Viruserkrankung screening-17,18. Die Umsetzung des Romans, molekulare Diagnostik-Assays erlaubt Erweiterung der diagnostischen Möglichkeiten für Viren wie Ebola-19,20,21, Grippe8,22und Tuberkulose (TB )23.
Das Ziel dieser Arbeit ist es, eine neuartige modulare und schnell einsetzbaren Laboreinrichtung zu validieren und bieten einen Trainingsleitfaden für Laborpersonal in abgelegenen, ressourcenschonende Umgebungen arbeiten, während einer Epidemie, Naturkatastrophen oder anderen Nothilfe Lage. Hier präsentieren wir Ihnen ein Protokoll für die Atemwege Grippe-Diagnose in diesem innovativen, mobilen Labor.
Protokoll
(1) installation
Hinweis: Nur 2-4 Personen sind erforderlich, die "Lego-Like" Laborgerät bereitstellen. Optimal, 4 Personen bereitstellen verwendet werden würde, aber es ist möglich mit nur 2.
- Nutzen Sie ein Gabelstapler (Abb. 1A,B) oder anderen geeigneten Hebevorrichtung, den Container zu behandeln. Verwenden Sie eine Gabelstapler mit mindestens sieben Tonnen Hubkraft um die beiden Arten von Containern24zu behandeln.
- Um ein Laborgerät einzurichten, wählen Sie einen Patch von ca. 90 x 60 qm (27,4 x 18,3 m2) auf eine flache Landschaft um sicherzustellen, dass keine Hindernisse das richtige Layout zu behindern. Stellen Sie sicher, dass die Website gut durchlässigen Boden, Website Entwässerung zu versichern, wie dadurch entstehen, dass potenzielle Probleme mit Wasser Verlustleistung nach Regen fallen. Verwenden Sie Garten, haben zuvor eingeebnet und das sind harte verdichtetem Boden eine geringe Druckfestigkeit von 10 kN/dm2. Die Umgebung sollte erlauben Zugriff auf erforderliche Ausrüstung für die Einheit von seiner Beförderung Gerät entladen und Platz für die notwendige Unterstützungsausrüstung für die Aufgabe zu erfüllen.
- Legen Sie die Einheit oder Einheiten in der Transport-Modus in der Mitte des ausgewählten Standort und passen Sie die Stufe. Jede Einheit verfügt über vier Leveln Buben Bereitstellung auf einer Website zu ermöglichen, die eine maximale Neigung von 6,5 % (~ 4 Grad) hat. Die Mindesthöhe für die Container ist ~ 6 Zoll um sicherzustellen, dass die Bodenabläufe und Entlastung Rohre einwandfrei funktionieren. Erstrecken Sie sich Buchsen nicht mehr als 12 Zoll. Befestigen Sie die Halterung am Arm des Jack. Sicherstellen Sie, dass der Behälter ist durch die Platzierung einer Richtmaschine Blase in der Mitte der unteren Schienen. Erweitern Sie das Gerät nicht, bis es richtig positioniert wurde!
- Das Gerät durch Öffnen der Platten für die volle Funktionalität zu erweitern. Suchen Sie zuerst die zweiteilige Querstange. Verbinden Sie die Querstange, so dass seine Höhe fast so hoch wie die Containereinheit ist. Der Mast kann der Benutzer öffnen Sie die Systemsteuerung und das Gewicht der Dachplatte zu unterstützen, sobald die Seitentüren geöffnet werden. Es ist ein Sicherheitsclip, der wirkt wie ein Stift auf die Platten verschlossen zu halten. Entfernen Sie die Sicherheitsklammer zuerst, dann heben Sie und ziehen Sie die Cam Lock Pin aus dem Loch. Setzen Sie den Stift hinter den Hebel und aus dem Weg zu den Cam-Hebel befindet sich auf der Unterseite des Behälters (erweiterbar).
- Heben Sie das Dach, das Panel 1 Wenn man bedenkt, dass dieses Panel verfügt über Gas-Federbeine und sobald die Panel-Türen entriegelt werden, erscheint die streben. Dies ermöglicht dem Benutzer, das Dach (Gruppe 1) mit der zweiteiligen Querstange zu erhöhen. Bewegen Sie die Querstange Spitze unter die Dachhaut zu vorübergehend (Abb. 4A) unterstützen.
- Zwar halten sich die Dachhaut mit der Unterstützung Poke, finden die Sicherheitskette, befindet sich im oberen linken Seite des Containers. Ziehen Sie mit Hilfe von 2-3 Personen sorgfältig Panel 2, bis die Sicherheitskette gerade ist, halten das Gewicht der Platte 2 und engagiert.
- Verbinden Sie den Winde Gurt Gürtel an der Lug-Halterung von hand wickelte sie um das äußere der Gasfeder. Beachten Sie, wenn es keine Winde Tool, der vorherige Schritt manuell mit mindestens zwei Personen auf jeder Seite des Fensters manuell halten und senken sie abgeschlossen werden kann.
Achtung: Das Gewicht der Platte ist 260 lb!
- Sicherzustellen Sie, dass keine Personen oder Gegenstände in der Art von Panel 2 und mit der Seilwinde und Bohren Sie, fahren Sie mit das Panel (Abbildung 4 b) zu senken. Wenn Panel 2 vollständig abgesenkt wird, trennen Sie die Winde Gurt und Rolle ihn zurück in die Winde. Entfernen Sie die Winde und legen Sie es auf der gegenüberliegenden Seite des Behälters in Vorbereitung für den Einsatz. Beide Seiten des Referats sind identisch und die gleichen Schritte oben für die andere Seite des Gerätes.
- Zur vollständigen Bereitstellung der ersten Seite auf das Panel (die derzeit dem Boden) zu erreichen Sie und mit mindestens zwei Personen auf jeder Seite, manuell heben Sie Panel 3 nach oben einrasten als die Tür und die Vorderwand der Seite (Abbildung 4). Die beiden Personen bleibt Panel 3, zu halten, während die dritte Person die Querstange entfernt.
Achtung: Niemand sollte im Inneren des Gerätes oder unter dem Dach bis zum Panel 3 Wand ist vorhanden! - Suchen Sie aus dem Inneren des Panel 3 die beiden Laschen und verriegeln sie verwenden das Sicherungsband. Sicherstellen Sie, dass die Gummidichtungen schwarzes Dach-Panel zu Gesicht das Innere der Geräte herausgezogen werden. Dies muss erfolgen, um Regen und andere Eindringen von Wasser in das Gerät zu verhindern.
- Entsperren Sie aus dem Inneren des Behälters Panel 4. Einmal freigeschaltet, push-out Panel 4 (Abbildung 4) so dass es wie eine Tür geöffnet schwingt. Sperre der beiden Sicherheit Verriegelungen an Innenwand. Entsperren Sie Panel 5, und wiederholen Sie die gleichen Schritte für Panel 4. Dieses Panel mit gleichen internen Sicherheitshäkchen zu sichern. Sobald die gesamte Einheit Innenraum gesperrt wurde, wieder anziehen der Spannschraube bis zur Etage und Stirnwände sind versiegelt.
- Sobald beide Seiten des Behälters sicher erweitert werden, überprüfen Sie die Buchsen und stellen Sie alle notwendigen Anpassungen von Verschiebung, die stattgefunden haben können. Überprüfen Sie im Tierheim um wöchentlich sein. Nach extremen Wetterbedingungen (Regen oder Wind) Buchsen am Behälter zu überprüfen und entsprechend anzupassen.
- Erweitern Sie den zweiten Container, wenn die anschließbaren Labormodule für den Einsatz (Abbildung 5) geplant werden.
- Verbinden Sie die Geräte zur Stromversorgung und Wasserversorgung. In der entsprechenden manuellen24finden Sie eine detaillierte Anleitung zur Installation eines Diesel-Generators an den Einheiten durch einen Sicherungskasten angeschlossen.
Hinweis: Die remote Laborgerät ist nun bereitgestellt. Nicht reduzierbare Innenvolumen des Gerätes erlaubt es, mindestens von Ausrüstung und Labor für besondere diagnostische Tests notwendig speichern. Installation von Drucksystem für BSL-3 Modul ist im Detail24 beschrieben und erfordert zusätzliche Qualitätskontrolle. 24
2. Checkliste für Personenschutz und Labor-workflow
Hinweis: Ein Fehler in irgendwelchen der allgemeinen Sicherheit und Laboruntersuchungen Anforderung Phasen kann die Ergebnisse des gesamten Testprozesses ungültig.
- Vor der Vorbereitung auf die installierten Laborgerät, sicherzustellen, dass alle BSL-2 oder BSL-3 Sicherheitsanforderungen berücksichtigt werden: Dressing mit richtigen Personal Schutzausrüstung (PSA), Händewaschen, Handschuhen, und alle Arbeitsbereiche, die Dekontamination verwendet werden.
- Befolgen Sie die Checkliste in Tabelle 1 , die Sicherheitsanforderungen für den Personenschutz bei Tests im Labor BSL-2 und die BSL-3-Modul (der montierten Handschuhfach Zimmer - Unterdruck und PCR Zimmer - Überdruck) ausgeführt enthält.
- Alle Platz zum Arbeiten und Lieferungen im Labor zu dekontaminieren. Wenn Planung Natriumhypochlorit-Lösung (0.5 %), auch bekannt als flüssiges Bleichmittel verwenden, um den Arbeitsbereich und Zubehör, dekontaminieren auch 70 % igem Ethanol verwenden, um alle exponierten um Bleichmittel zu reinigen, kann als Bleichmittel mit anderen Chemikalien im Arbeitsbereich erstellen giftige Dämpfe mischen. Alle Bleach-Produkte in ihr eigenes dafür vorgesehenen Abfallbehälter zu entsorgen.
- Vor Beginn der Arbeiten in der Labor-Einheit, mit seiner Anordnung und Gestaltung vertraut. Es gelten strenge Regeln für die Verarbeitung von Proben im Handschuhfach (GB) Zimmer. Das GB-Zimmer ist Unterdruck! Um eine Glove-Box zu betreiben, überprüfen Sie Anweisungen des Herstellers. Mehrere Quellen geben ausführliche Tutorials über Handschuhfach Betrieb25.
Hinweis: Der Zweck dieses Tests ist zu extrahieren und zu reinigen Ribonukleinsäure (RNA) oder der Desoxyribonukleinsäure (DNA), falls vorhanden, aus Proben. Die extrahierte RNA/DNA wird durch eine Real-Time RT-PCR zur Erkennung der Anwesenheit oder Abwesenheit von gezielten viralen Krankheitserregern - Grippe (INF) getestet werden.
3. schnelle Influenza Virus-Diagnostik mittels RT-PCR in eine Laboreinrichtung BSL-2
- Erhalten und registrieren
- Die Checkliste für PSA gelten (siehe Abschnitt 2). INF ist ein Klasse 2 Agent BSL-2 Praxis erfordern. PSA für BSL-2 Praxis ist erforderlich. Darüber hinaus tragen Sie Schutzbrillen und Handschellen Hülse Laborkittel, potentielle Exposition der Haut zu minimieren.
- Laut Weltgesundheitsorganisation (WHO) Empfehlungen26verwenden Sie sterile Dacron oder Viskose Tupfer mit Kunststoff Wellen für die Probenahme aus den Atemwegen.
Hinweis: Baumwolle oder Kalzium-Alginat-Tupfer oder Tupfer mit Holzstöcken enthalten Verbindungen, die einige Viren inaktivieren und hemmen PCR, Tests26,27. - Wie Patienten Tupfer Probe entnommen werden, transportieren sie an die Laboreinrichtung aus dem Feld oder in der Klinik. Übertragen Sie Proben über die Pass-through-Fenster; Dieses Fenster kann nicht von beiden Seiten geöffnet werden.
- Im Pass-through-Fenster Rohre mit Proben mit Bleichmittel für 1 min, gefolgt von 70 % igem Ethanol sprühen und trocknen um angemessene Dekontamination zu bieten, bevor sie das Laborgerät eingeben. Im Anschluss an das Eintauchen der Zahntechniker im Inneren des Gerätes das Pass-through-Fenster öffnet und sammeln von Proben aus dem Bleichmittel Container registriert werden. In der Regel sind die Übergabe der Probenmaterials und der Person, die Gewinnung der Probenmaterials nicht dasselbe.
- Öffnen Sie das Pass-through-Fenster und Proben Sie die registriert werden. Wischen Sie alle Proben, die in Bleichmittel und Ethanol desinfiziert wurden. Wischen Sie das Innere der Pass-through-Fenster mit Bleichmittel, gefolgt von 70 % Ethanol-Lösung. Registrieren Sie eine Probe innerhalb von interaktiven Tablet-basierten System oder einen Laptop. Identifizieren Sie eine Probe mit den folgenden Informationen:
-Abholtermin
-Beginn Datum
-Patienten-Alter und Geschlecht
-Objekt-Typ (z. B.., Nasenabstrich)
-Eindeutige Kennungen
-Sonstige relevante Informationen - Verwenden Sie Strichcodes für die Kennzeichnung von Rohren. Jede Probenröhrchen und vier leere Rohre bezeichnet, Aliquote fügen Sie Barcode hinzu. Verschieben Sie die Proben an der Abzugshaube. Scannen eines Barcodes auf jedes Rohr und stellen Sie sicher, dass die richtige Probe Identifikationsinformationen auf dem Tablet-basierten System oder Laptop-Bildschirm angezeigt wird. Wenn Barcodes nicht verfügbar sind, verwenden Sie einen alkoholbeständigem Marker. Markieren Sie das Fläschchen selbst immer, nie kann die Kappe als dies bei der Handhabung geschaltet bekommen! Die Registrierung abzuschließen.
- Probe aliquoten
- Einmal Reagenzgläser gekennzeichnet, mit einem zertifizierten Klasse 2 Biosafety Schrank Umgang mit Proben und Aliquote Proben machen. Eine aliquote kann zum sofortigen Testen verwendet werden und die anderen beibehalten für Referenz Zweck oder die Wiederholung der Prüfungen.
- Exemplare mit Nasenabstrich Spitze im viralen Transportmedium angekommen, schüren Tupfer Tipp in das Medium für 30 s und drücken Sie es gegen die Seite des Röhrchens. Entfernen Sie sie dann aus dem Medium und entsorgen Sie es mit einem biogefährlichen Abfällen Protokoll (passend zu verwerfen, Autoklaven oder hängen Sie in 1: 100-Chlor-Lösung).
Hinweis: Das kleinste Volumen des Mediums, die gespeichert werden sollen ist 0,5 mL. So kann eine 3 mL Probe in sechs Aliquote (Teilproben) unterteilt werden. Verwenden Sie 1 mL Cryo-Lagerung-Tube für jede Probe von 0,5 mL, extra Volumen für gefrorene Medium bereitzustellen. - Bei der Einnahme von Aliquote frische sterile oder Einweg-Pipetten für jede Probe und verwerfen sie in biogefährlichen Abfallbehälter um Kreuzkontaminationen zu vermeiden. Stellen Sie sicher, jedes Rohr dicht versiegelt und geschlossen ist.
- Nutzen einer Teilprobe pro Probe für sofortige Extraktion und anderen aliquoten im Gefrierschrank aufbewahren (bei-80 ° C als es ist ein Atemwege Exemplar) für eine spätere Verwendung.
- Reinigen Sie vor dem Umzug an den Arbeitsplatz alle Arbeitsbereich Oberflächen und Geräte mit Bleichmittel, gefolgt von 70 % igem Ethanol-Lösung.
- Extraktion und Reinigung
- Zur Sicherung der Qualität der Prüfung, Umzug der Barcode PCR Probe Aliquote von Handhabung Bereich auf dem Arbeitsplatz (BSL-2 Sicherheitsschrank) für die Gewinnung der Proben. Diese Sicherheitsschrank hat einen separaten Satz von Pipetten zur Handhabung der Probe.
- Verwenden Sie das virale RNA-Mini-Kit für die Extraktion von RNA-Proben. Folgen Sie den Anweisungen des Herstellers für die Reinigung der viralen RNA durch Spin-Protokoll. Bereiten Sie master-Mix nach der Anzahl der Proben, die extrahiert werden müssen. Die Probe und Lyse Puffer-master-Mix bei Zimmertemperatur aufbewahren.
- Bereiten Sie die Anzahl der Samples, die extrahiert werden müssen. Kennzeichnen Sie 1,5 mL Mikro-Zentrifuge Röhren mit Barcodenummern oder eindeutiger Bezeichner.
- Die Pipette auf 560 µL. anwenden, werden eine saubere Pipettenspitze. Jedes beschriftete Röhrchen 560 µL des Puffers Lyse hinzufügen. Tipp zu verwerfen. Eine saubere Pipettenspitze anwenden. Fügen Sie 140 µL der Probe. Entsorgen Sie alte und wenden Sie eine saubere Pipettenspitze an. Mit der anderen Probe wiederholen. Eine saubere Pipettenspitze anwenden. Negativkontrolle Rohr 140 µL Puffer hinzufügen. Schließen Sie jedes Rohr fest.
- Puls-Vortex Beispiel aliquoten 1 mit der Lyse-Puffer für 15 S. Wiederholung mit Probe aliquoten 2 und das Steuerrohr. Mikro-Zentrifuge probieren für 5 S. Inkubation die Proben 10 min bei Raumtemperatur.
- Nach 10 min Inkubation, erneut Zentrifugieren der Rohre, um jeden Tropfen aus innerhalb jedes Rohr Deckel zu entfernen. Probe 560 µL Ethanol-Lösung hinzufügen. Ändern Sie die Pipettenspitze. Wiederholen Sie mit jedem restlichen oder zusätzlichen Proben. Jede Probe Tube sicher schließen und Puls-Vortex probieren für 15 S. Mikro-Zentrifuge die Proben für 5 s.
- Übernehmen Sie die Mischung auf die Spin-Spalte. Erhalten Sie saubere 2 mL Röhrchen. Fügen Sie Spin Spalten hinzu, und beschriften Sie sie um die Proben übereinstimmen. Übertragen Sie 630 µL Probe auf übereinstimmende Spalte entsprechend.
- Kappen zu sichern und in die Zentrifuge zu bewegen. Die Proben in Zentrifuge gleichmäßig zu verteilen. Zentrifugieren Sie bei 6.000 × g für 1 min um die Lyse-Puffer zu entfernen. Rückkehr an den Arbeitsplatz. Röhrchen zu ersetzen. Fügen Sie die restlichen Lyse-Puffer und wiederholen Sie den Zentrifugationsschritt. Verwerfen der ursprünglichen aliquoten Probenröhrchen.
- Waschen der Spin-Spalte mit zwei Puffern und entsorgen das Eluat. Gelten Sie 500 µL Buffer AW1. Wiederholen Sie dies mit jeder Probe. Sichern Sie Kappen jeder Probe und Zentrifuge bei 6.000 × g für 1 Minute. Wiederholen Sie mit den zweiten Buffer AW2 und 20.000 × g für 3 min zentrifugieren.
- Schließlich eluieren Sie RNA durch Zugabe von Elution Puffer. Legen Sie die Spalte in eine saubere 1,5 mL-Tube, öffnen Sie die Spalte und fügen Sie 60 µL Puffer Ave inkubieren bei Raumtemperatur für 1 min und Zentrifuge bei 6.000 X g für 1 min. Die Proben sind nun bereit für die PCR-Analyse.
- PCR-Amplifikation und Detektion
- Führen Sie die PCR-Amplifikation in einem separaten Bereich für PCR bezeichnet. Führen Sie die PCR Verstärkung des viralen Ziels mit PCR-Protokoll für ein-Schritt-Verfahren gemäß den Anweisungen des Herstellers. Beachten Sie, dass ein master-Mix mit viralen spezifischen Primer, Sonden, 2 X RT-PCR-Puffer und RT-PCR Enzym hergestellt wird. Die master-Mix, Platten oder Rohren und dann fügen Sie hinzu und mischen Sie einzelne Samples (siehe Abschnitt 4.4).
- Die Platte auf die PCR-Maschine übertragen und gemäß der viralen Verstärkung Bedingungen ausgeführt. Sobald Proben auf das PCR-Gerät geladen werden, dauert es ca. 90 Minuten zur Vervollständigung der Strecke.
- Wartung nach der Nutzung
- Führen Sie regelmäßige und regelmäßige Wartung nach der Nutzung entsprechend der Tabelle 2.
(4) schnelle Influenza Virus-Diagnostik mittels RT-PCR in eine Laboreinrichtung BSL-3
Hinweis: BSL-3 Bedingungen des experimentellen Protokolls bleibt gleich, aber Sicherheitsmaßnahmen werden Vorrang vor allem. Vor dem Eintritt in das Labor BSL-3, durch das transparente Fenster schauen Sie um sicher zu sein, dass Unterdruck in der Glove-Box-Einheit eingerichtet wurde. Es wird offensichtlich, dass Unterdruck hergestellt wurde, wenn ein rosa Ball in einer Wand sichtbar ist.
- Erhalten und registrieren
- Sobald Unterdruck hergestellt wurde, öffnen Sie die Tür und geben Sie die Einheit. Sofort die Hände waschen und dann mit der PSA. Die Checkliste für PSA und Workflow BSL-3 gelten (siehe Abschnitt 2).
- Fahren Sie mit PPE aufsetzen, in der folgenden Reihenfolge: unter Kleid, Überschuhe, Maske, Gesichtsschutz, Handschuhe, zweites Paar Handschuhe. Tragen eine vollständige Kleid, die den ganzen Körper schützt wird empfohlen.
- Die Maschine einschalten und Druck im Handschuhfach zu stabilisieren lassen. Verwenden Sie ein Bleichmittel Sprühlösung, um alle Bereiche und Lieferungen innerhalb und außerhalb der Glove-Box verwendet werden zu dekontaminieren. Bleichmittel Abfallprodukte in einem Bleichmittel nur Container entsorgen. 70 % igem Ethanol Lösung, sauber aus allen Bereichen für Bleach wurde verwendet.
- Übertragen Sie die Probe über die Pass-through-Fenster.
Hinweis: Vor dem Herunterfallen auf Pass-through-Fenster, Röhrchen mit Proben durch Eintauchen in ein Hypochlorit-Bad für 1-2 min. besonders zu desinfizieren, spray Proben mit einem Bleichmittel-Lösung und lassen Sie allein für mindestens 1 min und Pass-Through-vor Erhalt im Inneren des Gerätes BSL-3. Vorbei an der Probe von außen als auch der Beschenkte Person sollte Extraktion der Probe im Labor BSL-3 nicht dasselbe sein. - Empfangen Sie die Proben im BSL-3 Gerät und reinigen Sie sie bevor Sie fortfahren, um die Registrierung und Kennzeichnung Schritte.
- Registrieren Sie eine Probe mit dem interaktiven Tablet-basierten System oder einen Laptop. Ein Beispiel mit den folgenden Informationen zu identifizieren (siehe Abschnitt 3.1.5).
- Verwenden Sie Strichcodes für die Kennzeichnung von Rohren. Wenn Barcodes nicht verfügbar sind, verwenden Sie einen alkoholbeständigem Marker.
Hinweis: Markieren Sie das Fläschchen selbst, nie die Kappe immer, wie dies bei der Handhabung geschaltet bekommen kann!
- Probe aliquoten
- Einmal Proben registriert sind und Rohre wurde mit dem Label, legen Sie die Proben in der zertifizierten Glove-Box über die Luft verschlossenen Fach Proben innerhalb der Glove-Box abrufen. Schließen Sie die Tür. Öffnen Sie dann die andere Tür durch das Handschuhfach abzurufenden Proben. Nicht beide Türen gleichzeitig geöffnet. Öffnen Sie und schließen Sie jede Tür in zwei verschiedenen Stufen für Sicherheitshinweise. UV-C Licht einschalten.
- Wenn Proben sicher in das Innere der Glove-Box verschoben wurden, befolgen Sie die Schritte, die zuvor für die Erstellung von Probe Aliquote in einem Handschuhfach. Ein Aliquot der Probe kann zur sofortigen Prüfung verwendet werden und die anderen beibehalten für Referenz Zweck oder die Wiederholung der Prüfungen. Exemplare ankommen mit Nasenabstrich Tipp im viralen Transportmedium. Nehmen Sie Proben zu und setzen Sie in jedes Fläschchen. Das Medium für 30 s und drücken Sie den Tupfer Tipp unterrühren es gegen die Seite des Röhrchens vor vom Medium entfernen und entsorgen es unter Verwendung eines biogefährlichen Abfällen Protokolls (passend zu verwerfen, Autoklaven oder hängen Sie in 1: 100-Chlor-Lösung).
Hinweis: Das kleinste Volumen des Mediums, die gespeichert werden sollen ist 0,5 mL, Einsatz 1 mL Fläschchen für diesen Zweck. So kann eine 3 mL Probe in sechs Aliquote (Teilproben) unterteilt werden. - Verwenden Sie frische sterile oder Einweg-Pipetten für jede Probe und als biogefährlichen Abfällen zu verwerfen. Einmal Proben sind regelmÄÑig, die Proben in luftdichten Behälter zu bewegen. Schließen Sie Fläschchen mit Schutz und entfernen Sie aus dem Handschuhfach.
- Innerhalb der Glove-Box schließen Sie die Biohazard Auffangbeutel und bereiten Sie eine neue Auffangbeutel um Kreuzkontaminationen zu vermeiden. Dekontaminieren des Glove-Box-Arbeitsbereichs Bleichmittel für 5 min und 70 % Ethanol Lösung danach anwenden.
- Nutzen Sie einer Teilprobe pro Probe zur sofortigen Untersuchung und speichern Sie andere im Gefrierschrank bei-80 ° C zu, wie es einer respiratorischen Probe ist. Nach der Dekontamination behalten ein Aliquot zum testen, bewegen Sie sich alle Proben aus Glove-Box zur Aufbewahrung in-80 ° C Gefrierschrank.
- Extraktion und Reinigung
- Bewegen Sie nach der Dekontamination den Barcode Probe Aliquote für PCR-Analyse von der Handhabung Bereich wieder in das Handschuhfach der Proben benötigt.
- Im Handschuhfach alle Schritte Lyse für Extraktionsverfahren. Verwenden Sie das virale RNA-Mini-Kit für die Extraktion von RNA-Proben nach den Anweisungen des Herstellers. Folgen Sie den Anweisungen für die Reinigung der viralen RNA durch Spin-Protokoll in den Anweisungen des Herstellers.
- Bereiten Sie die Anzahl der Samples, die extrahiert werden müssen. Kennzeichnen Sie 1,5 mL Mikro-Zentrifuge Röhren mit Barcodenummern oder eindeutiger Bezeichner.
- 140 µL der Probe und Puls Vortex 560 µL des Puffers Lyse hinzufügen. 10 Minuten bei Raumtemperatur inkubieren.
Hinweis: Die Inaktivierung Verfahren kann variieren je nach Art des Erregers BSL-3, die extrahiert wird und in einigen Fällen weitere Inaktivierung kann erforderlich sein. - Nach der Lyse Schritt fest verschließen die Kappen auf jede Probe und legen in der Druckluft gesperrt-Passage (wenn die Zentrifuge sich außerhalb der Glove-Box befindet). Übertragen Sie die lysierten Proben in Biosafety Schrank für den Rest des Verfahrens.
Hinweis: Das Verfahren zur Extraktion und Reinigung von RNA kann im Handschuhfach oder in einem Handschuhfach gefolgt von Bio-Sicherheitsschrank je nach Erreger BSL-3 und Protokolle erforderlich abgeschlossen werden. - Achten Sie darauf, den Arbeitsbereich und Lieferungen im Handschuhfach wieder mit Bleichmittel zu dekontaminieren, und 70 % Ethanol-Lösung für alle Bereiche reinigen ausgesetzt zuvor um zu bleichen.
- Befolgen Sie die Schritte im Abschnitt 3.3.6 - 3.3.10 für Wäsche und Reinigung der RNA.
- Übertragen Sie nach der Extraktion die Proben an das Pass-through-Fenster für PCR-Analysen.
- Nachdem Proben entfernt und übertragen wurde, dekontaminieren des Labor-Arbeitsbereichs außerhalb der Glove-Box nach Abschnitt 2.
- Vor dem Entfernen der PPE warten Sie, bis die Luftzirkulation im Gerät sicher die richtige Anzahl von Zyklen vor Beginn die EVP zu entfernen-Filterung erreicht hat. Sofort nach dem entfernen und entsorgen alle PSA in der EVP Abfallbehälter, fahren Sie mit Händewaschen im Labor mit Wasser und Seife vor dem Beenden der Einheit gemäß Abschnitt 2.
- PCR-Amplifikation und Detektion
Hinweis: Die PCR-Amplifikation erfolgt in einem separaten Bereich für PCR und verbunden mit dem Handschuhfach über Pass-through-Fenster. Der Arbeitsbereich und Zubehör müssen vor einem Test dekontaminiert werden.- Entfernen Sie die extrahierten RNA-Proben aus dem Pass-through-Fenster.
- Führen Sie die PCR Verstärkung des viralen Ziels mit einstufigen PCR-Protokoll. Bereiten Sie einen master-Mix mit viralen spezifischen Primer, Sonden, 2 X RT-PCR-Puffer und RT-PCR-Enzym. Verwenden Sie eine 1,5 mL-Tube mit die folgende Komponente für jede gezielte Assay: Wasser, Primer und Sonden, 2 X Puffer und RT-PCR-Enzym. Wirbel und Spin master-Mix.
- Aliquot der master-Mix in jedes Streifens Rohre. Das PCR-Kit Lagerung bei der empfohlenen Temperatur zurück, nachdem der master-Mix vorbereitet wurden.
- Die einzelnen Samples hinzu kommt jedes Streifens Rohre mit einer separaten Spitze zwischen jedem Streifen-Röhrchen. Drehen Sie die Probenteller oder Schläuche bei 1.500 u/min für 1 min. Die Proben sind bereit, auf das Real-Time PCR-Gerät geladen werden.
- Die Platte mit Proben an das PCR-Gerät zu übertragen und die Maschine entsprechend der viralen Verstärkung Bedingungen laufen. Es dauert ca. 90 min um einen Lauf zu vervollständigen.
- Entfernen Sie vor dem Sammeln der Ergebnisse und das Labor verlassen PSA zu und Dekontaminieren Sie angemessen jede Arbeitsstation und Vorbereitung für den nächsten diagnostischen Test gemäß Abschnitt 2.
- Wartung nach der Nutzung
- Führen Sie regelmäßige und regelmäßige Wartung nach der Nutzung entsprechend der Tabelle 2.
Hinweis: Die insgesamt diagnostische Bearbeitungszeit beträgt ca. 4 Stunden. Extraktionszeit und PCR Aufbauzeit kann variieren, abhängig von der Anzahl der Proben und der diagnostische Test dauert 4-5 Stunden oder mehr, entsprechend.
- Führen Sie regelmäßige und regelmäßige Wartung nach der Nutzung entsprechend der Tabelle 2.
Ergebnisse
Das Ziel dieser Studie soll zeigen, dass die vorgeschlagenen BSL-2 und BSL-3 mobiles Labor ein angemessenes Umfeld ermöglicht respiratorischen Virus diagnostische Tests mit repräsentativen Ergebnisse identisch mit Prüfungen in hoher Qualität bieten stationäre Laboratorien. Die Laborräume dienen zur Einhaltung der Prüfanforderungen in Occupational Health and Safety (OHS) Empfehlungen gegeben. Sobald der remote Laboreinrichtung eingesetzt (Abbildung 4) und alle Geräte ist und Zubehör installiert sind (Abbildung 5), Labor-Tests ausgeführt werden können.
Gemäß Labor geeigneten operativen Standardverfahren, PSA (Kittel, Sicherheitsschuhe, Handschuhe, erweiterte Maske, Schutzbrille, etc.) für BSL-2 Praxis erforderlich ist. Für die Praxis BSL-3 ist die PCR-Labormodul der Unterdruck mit einem zertifizierten Handschuhfach ausgestattet. Die Laboreinheiten werden von Pass-Through-Außenfenster zum Schutz des Personals bei der Probe Empfang aktualisiert. Die Registrierung kann mit zuvor entwickelten Tablet-basierte Anwendung (Abbildung 3D) vereinfacht werden. Andere annehmbaren Anwendungen, die auf einem Laptop können auch verwendet werden.
Dieser bestimmten Atemwegserkrankungen Virus diagnostischen Test kann durchgeführt werden, in der angeschlossenen Labormodule schieden Schritte des diagnostischen Verfahrens mit Absicht, um Verunreinigungen oder potenziellen Interferenzen zwischen biochemische Reagenzien zu vermeiden, die zu beeinträchtigen die Testergebnisse. Um die Qualität der Diagnose zu maximieren, nutzt die diagnostische Schnelltests Praxis (i) sowohl die grundlegenden Labor BSL-2 und die Traverse verbunden PCR Raum (Abschnitt 3) oder (Ii) die GB und PCR Zimmer durch Pass-through-Fenster (Abschnitt 4) verbunden. Das Diagramm des vorgeschlagenen Labor Workflows auf Abbildung 6 dargestellt und Personenschutz, betont. Das Diagramm erkennt die Bedeutung der einzelnen angegebenen Schritte für Personenschutz, vor allem wenn Laborpersonal in abgelegenen Gebieten minimal ausgebildet ist.
Der rasche diagnostische Test der Influenza wird über die RT-PCR-Technik erreicht. Die Prozedur enthält vier Hauptschritte. Beachten Sie, dass einzelne Arbeitsbereiche für jede Phase des Protokolls zugeordnet sind.
Der erste Schritt ist es, eine Probe und unterteilen es in mehrere Aliquote. Die Aliquote können dann mit Barcodes zur Verbesserung der Wirksamkeit des Daten-Steuerelement markiert und gespeichert in den Gefrierschrank für weitere Untersuchungen. Der zweite Schritt ist, eine Probe im Lyse Puffer zu inaktivieren, durch Zentrifugieren und Heizung. Die erste und zweite Schritte müssen in biologischen Sicherheit Schränke durchgeführt werden. Nutzen Sie individuelle Pipette Sets und Ausrüstung. Ein PCR-Test wird vorgeschlagen, in der PCR-Raum durchgeführt werden, falls vorhanden. Der dritte Schritt ist die Dokumentation der Ergebnisse. Der vierte Schritt ist die Pflege nach der Nutzung, und die Erinnerung an Personenschutz am Ende des Experiments.
Wenn die Probe wird voraussichtlich als BSL eingestuft werden-3 + (e.g.,Ebola, Zika, MERS, TB) die Handschuhfach-Anlage verwendet werden muss. Im abgelegenen Labor hat das GB-Zimmer ein eigenen Pass-through-Fenster zu Proben und ein Laptop oder Tablet für Probe-Registrierung zu erhalten. Die Probe aliquoten und Virus-Inaktivierung müssen alle in der Glove-Box Kammer ausgeführt werden. UV-C Licht empfiehlt sich zur Vermeidung von Kontaminationen während der Prozedur. Nach Inaktivierung einer Probe, weitere Schritte für Protokoll sind ähnlich wie die grundlegenden Labor BSL-2 und BSL-3 Test und folgt Checkliste Teil III (Tabelle 1, Abbildung 6).

Abbildung 1. Labor Einrichtung Prototyp. (A, B) Transport-Modus; (C) Modus bereitgestellt: außen festgelegt werden. (D) Modus bereitgestellt: Innenraum. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 2 . Schaltpläne. (A) die grundlegenden Labor BSL-2; (B) die BSL-3 Modul enthält die Glove-Box und PCR-Labore, die ein gemeinsames Pass-Through-für geschützte Probe übertragen Fenster; (C) angeschlossenen Laboreinrichtungen (A) und (B) mit gemeinsamen Versorgungsunternehmen. (D,E) Fotos von der angeschlossenen Geräte von entgegengesetzten Seiten. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 3. (A) Innenraum der BSL-3 Anlage (1) hat ein Pass-through-Fenster, ein Waschbecken und (2) eine Augenwischerei-Station am Einlass; (B) elektrische Stromanschlüsse, (C) Wasser Anschlüsse; (D) Tablet-basierte Software für Lieferung Tracking und Labor-Ergebnis Dokumentationen. Bitte klicken Sie hier für eine größere Version dieser Figur.
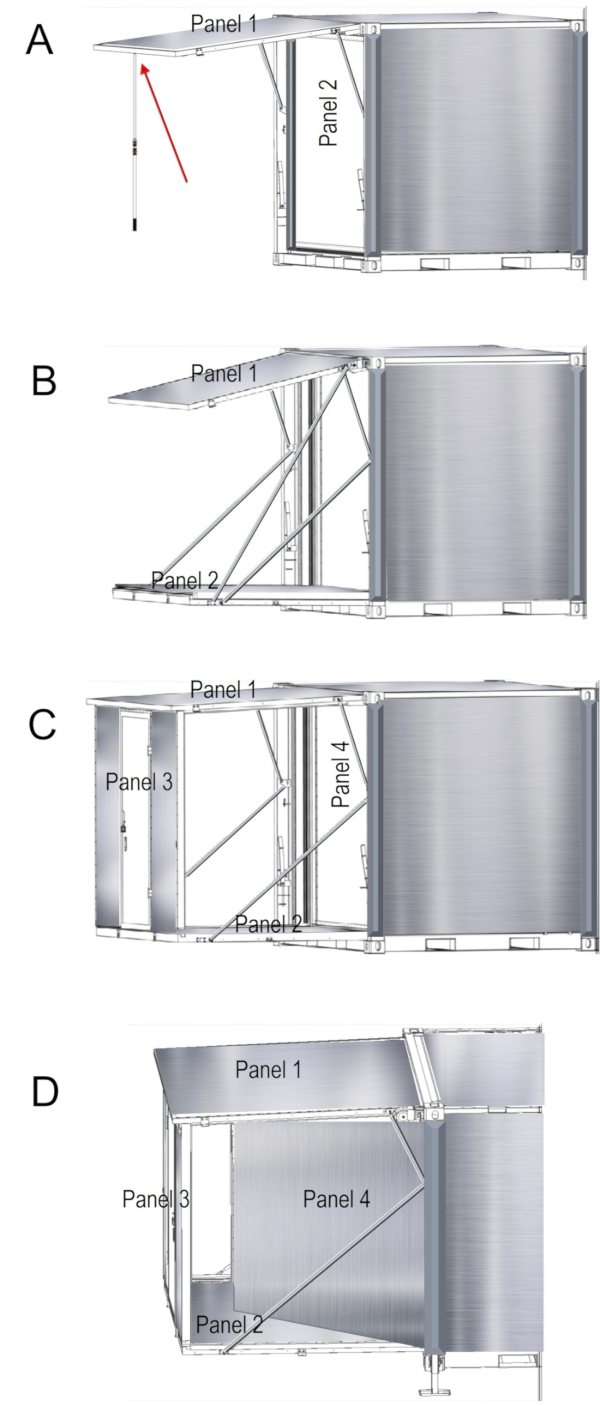
Abbildung 4 . Bereitstellung von der Laboreinrichtung. Anleitung für Panels entfaltet sich auf der einen Seite des Gerätes wie abgebildet (A-D). Bitte klicken Sie hier für eine größere Version dieser Figur.
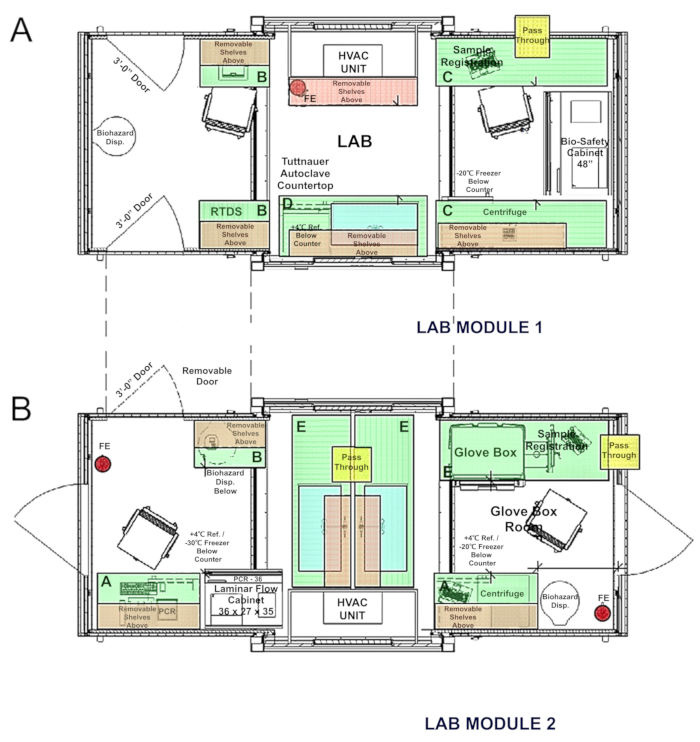
Abbildung 5 . Schaltpläne der anschließbaren Labor: (A) BSL-2 Modul 1; (B) Glove-Box und PCR-Modul 2. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 6 . Flussdiagramm für eine RT-PCR-Diagnosetest respiratorischen Viren in den abgelegenen Laboreinrichtung. Bitte klicken Sie hier für eine größere Version dieser Figur.
| Entfernten Labor BSL-2 | Entfernten Labor BSL-3 |
| Teil I | Teil I |
| i. Lab Tech durch Tür eintreten Eingang beschriftet und Kittel, die an Rack neben Eingangstür hängt aufsetzen. Offene Schuhe sind verboten, erweiterte Masken und Schutzbrillen sind erwünscht. | i. Lab Tech untersuchen Glove-Box Fenster aus außerhalb der Einheit, Unterdruck zu versichern ist aktiviert. (Rosa Ball sollte in der Einheit zu zeigen, dass der Unterdruck funktioniert sichtbar sein). |
| II. Lab Tech Hände im Waschbecken zu waschen, Einweg-Handschuhe anziehen und mit Aufnahme von Proben beginnen. | II. Wenn Unterdruck arbeitet, Lab Tech, treten durch die einzige Tür und legte auf Kittel, die an Rack neben Eingangstür hängt. Offene Schuhe sind verboten, erweiterte Masken und Schutzbrillen sind erwünscht. |
| III. Beispiele, die in Hypochlorit Bad vor dem Herunterfallen auf Pass-through-Fenster eingetaucht waren sitzen im Pass-through für Lab Tech. | III. Lab Tech, Hände im Waschbecken zu waschen auf Einweg-Handschuhe, PSA und beginnen mit der Einnahme von Proben. |
| IV. erhielt Probenannahme. | IV. Proben, die vorher in Hypochlorit Bad vor dem Herunterfallen auf Pass-through-Fenster getaucht waren sitzen im Pass-through für Lab Tech. |
| Teil II | v. erhielt Probenannahme. |
| v. je nach diagnostischen Verfahren Proben nach Biosafety Kabinett und inaktiviert. | Teil II |
| VI. Proben vorbereitet für Mikroskopie, Zentrifuge oder verrottet. | VI. Proben im Handschuhfach inaktiviert. |
| VII. geeignete diagnostische Tests laufen. | VII. Muster für Nukleinsäure-Isolierung ausgeführt. |
| VIII. Lagern Sie Exemplare in 4° C Kühl- oder entsprechende Gefrierschrank. | VIII. nach der Extraktion zog Proben auf Pass-through-Fenster. |
| Teil III | IX. Lab Tech tritt durch Eingang in PCR-Seite des Gerätes (Überdruck). |
| IX. verwenden Sie Spüle für Färbung & Waschen von Elementen. | x. Lab Tech aus Regal neben Eingang Laborkittel anziehen waschen Sie Hände in Waschbecken, Handschuhe anziehen. |
| x. verwenden Sie x. Laptop & Counterpace, Analysen und Dokumentation durchzuführen. | XI. erhalten Sie Proben von Glove-Box Zimmer im Pass-through-Fenster. |
| XI. sterilisieren Sie Ausrüstung durch Ausführen von Autoklaven. | XII. wenn notwendige Proben in Laminar-Flow Kabinett vorbereitet. |
| XII. biogefährlichen Abfall in Biohazard Abfallbehälter entsorgen. | XIII. geeignete Diagnosetests ausführen. |
| XIII. Waschen Sie Hände im Waschbecken. | XIV. Lagern Sie Exemplare in 4° C Kühl- oder entsprechende Gefrierschrank. |
| XIV. Legen Sie Laborkittel zurück auf Gestell auf. | Teil III |
| Verlassen Sie XV durch dieselbe Tür. | XV. verwenden Sie Spüle für Färbung & Waschen von Elementen. |
| XVI. verwenden Sie Laptop & Counterpace, Analysen und Dokumentation durchzuführen. | |
| XVII. Fläschchen in Pass-through-Fenster auf PCR Raum übertragen und Ausrüstung durch Ausführen von Autoklaven sterilisieren. | |
| XVIII. biogefährlichen Abfall in Biohazard Abfallbehälter entsorgen. | |
| XIX. Waschen Sie Hände im Waschbecken. | |
| Verlassen Sie XX durch dieselbe Tür. |
Tabelle 1. Checkliste für den PCR-Diagnostik-Workflow.
| Wartung und Kalibrierung | ||
| Echtzeit-PCR-Systeme | Monatliche | Führen Sie Hintergrund Kalibrierungen jeden Monat |
| 18 Monate | Führen Sie Hintergrund, räumliche und färben Sie Kalibrierungen alle 18 Monateth | |
| Zentrifuge | 1 Jahr | Umdrehungen pro Minute und Temperatur durch externe oder interne Kalibrierung kalibrieren |
| Glove-Box | Tägliche | Überprüfen Sie die Elemente, insbesondere für Schäden, die Sichtflächen der HEPA-Filter, Handschuhe, o-Ringe und Schläuche. Stellen Sie sicher, Rohr-Schellen fest und vorhanden sind. Durchführen Sie Leck-Druckprüfung. Testen Sie den Druck-Alarm. |
| 6 Monate | Ändern Sie den HEPA-filter | |
| 1 Jahr | Das System kalibrieren | |
| Autoklaven | Wöchentliche | Reinigen Sie den Wassertank und Regale mit einem milden nicht scheuernden Reinigungsmittel |
| 3 Monate | Zeitschaltuhr und Messgeräte zu kalibrieren | |
| 1 Jahr oder alle 50 Zyklen | Inspizieren, reinigen, prüfen und kalibrieren | |
| Kühlschrank und Freeezer | 6 Monate | Überprüfen Sie motor, Verdampfer Gebläsekonvektoren, Staubsaugen kondensierende Spulen und Kondensator Filter und ersetzen Sie Batterien nach Bedarf |
| 1 Jahr | Kalibrieren Sie, Gefrierschrank durch interne oder externe Kalibrierdienste | |
Tabelle 2. Real-Time PCR Gerätewartung.
| Obligatorische | Empfohlen |
| Kittel, Sicherheitsschuhe, Handschuhe | Kittel, Sicherheitsschuhe, Handschuhe, Masken, Brillen |
| Kühlschrank 4 ° C,-20 ° C Gefrierschrank | Kühlschrank 4 ° C,-20 ° C, Gefrierschrank Gefriertruhe-80 ° C |
| Eine Reihe von automatischen Pipetten | Drei Sätze von automatischen Pipetten |
| Zentrifuge, Shaker, thermocycler | Robot-system |
| RT-PCR-Maschine, Eisbad | RT-PCR mit Temperaturregelung, eisfreien Kühler |
| Biohazard Müllbeutel | Autoklaven, Biohazard Abfall zu entsorgen |
Tabelle 3. Mindestanforderungen für die RT-PCR respiratorischen Virus diagnostischen test BSL-2.
Diskussion
Die entfernten Laboreinrichtung oben beschriebenen ist logistisch orientierte, erweiterbar, schnell einsetzbare, multifunktionale und basierend auf Human-centered Design-Konzepte, die zum Schutz der Labor-Personal und Arbeitsbereich Effizienz ausgerichtet haben. Das ausführliche Protokoll für schnelle Labor auf- und sichere Atemwege Virusisolierung und Diagnose entwickelt und vorgestellt.
Für optimale Geräte funktionieren, die folgenden Bedingungen eingehalten werden, in den Laboreinheiten: Umgebungstemperatur 21 ± 2 ° C, zulässigen Temperatur von 5 bis 40 ° C, Luftfeuchtigkeit von 14 ± 5 % RH, zulässige maximale Relative Luftfeuchtigkeit von 80 % RH (noncondensing), und einer Höhe von 0 bis 2.000 m über dem Meeresspiegel.
Energieverbrauch ist eines der wichtigsten Parameter für die Verwaltung von einem off-Grid-Labor. Für Kern-Laborgeräte kann die Energieeffizienz 15-40 % variieren. durchschnittlichen Energieverbrauch dürfte jedoch hier um einen entsprechenden Service zu liefern. Die höchste macht Rate (1.500-2.000 W) bezieht sich auf die Klimaanlage, Glovebox System, die PCR-Maschine und der Autoklav Sterilisator. Wenn man 8 Stunden intensiver Arbeit, die Durchführung des Protokolls und 16 Stunden des Kontrollstreifens Labor-Umgebung ist der täglichen Energieverbrauch von Laborgeräten ca. 36 kWh/Tag für BSL-2, ca. 43 kWh pro Tag für BSL-3 und 73 kWh/Tag für die angeschlossenen BSL-2/BSL-3 + Einrichtungen. Für eine Einheit empfehlen wir, die eine Stromquelle mit Kapazität von laufen/Dauerleistung ≥8 kW, Überspannungsschutz/Start Leistung ≥10 kW; für die angeschlossenen Anlage, laufen/Dauerleistung ≥12 kW und Überspannungsschutz/Start Leistung ≥14 kW. Beachten Sie jedoch, dass in der BSL-3 Laboreinrichtung eine backup Energiequelle wird dringend empfohlen, zur Vermeidung versehentlichen Stromausfall und garantieren stetige Arbeit der Glove-Box und Unterdruck-System während eines diagnostischen Tests.
Eine benzinbetriebene Stromgenerator ist eine kostengünstige Lösung für Notenergieversorgung. Davon ausgehen Sie, dass Kraftstoffeffizienz von einem Benzin-Generator ca. 1,5 Gallonen pro Stunde bei 100 % Last. Dann, wenn der durchschnittliche tägliche Energieverbrauch ist 8 Stunden 40 % geladen und 16 Stunden 10 % Last, Laborgerät BSL-2 oder BSL-3 erfordert 7-9 Gallonen Kraftstoff pro Tag, entsprechend, und die angeschlossene Anlage braucht ~ 15 gal/Tag.
Die entfernten Laboreinheiten sollen Möglichkeiten der off-Grid Solar-Panel-Systeme passen. Sonnenkollektoren benötigen keine zusätzlichen Treibstoff und mit hoher Produktivität in den tropischen und subtropischen Regionen Afrikas, Asiens und Lateinamerikas aufgrund der hohen Sonneneinstrahlung betrieben werden können. Derzeit ermöglicht eine Einheit eines im Handel erhältlichen Solar-Panel-Systems eine tägliche Stromverbrauch von bis zu 44 kWh/Tag.
Unabhängig von der gewählten Art der alternative elektrische Energiequelle sind schmutzigen Strom Filter dringend empfohlen und vorinstalliert in den Laboreinrichtungen zur Verbesserung der Netzqualität und Labor-Ausrüstung zu schützen. Quellen starker und ungeschirmte elektromagnetischer Strahlung fernhalten Sie das PCR-System denn starke elektromagnetischer Strahlung mit den ordnungsgemäßen Betrieb des Geräts beeinträchtigen könnten. Es ist auch wichtig verwenden Sie nicht das PCR-System in der Nähe von starken Vibrationen wie eine Zentrifuge oder Pumpe Quellen weil übermäßige Vibrationen Geräteleistung beeinträchtigen wird. Die Laborausstattung kann nur in einer Umgebung installiert werden, Stulpenhandschuhe Schadstoffe wie Staubpartikel oder Hackschnitzel verfügt. Sicherzustellen Sie, dass das Zimmer vom Lüftungsschlitze, die partikuläre Material auf die Instrument-Komponenten vertreiben könnte.
Die Labor-Wasserverbrauch richtet sich nach Anzahl diagnostischer Tests laufen täglich und Laboranten in der Anlage arbeiten. Nuklease freies Wasser für Vorbereitung von Mischern während der diagnostischen Verfahren einschließlich der Extraktion und PCR-Test ist erforderlich und muss im Voraus andere Zubehör und Chemikalien geliefert werden. Mindestens 50 mL des freien Wassers Nuklease ist notwendig, um einen Diagnosetest ausführen; das erforderliche Volumen des freien Wassers Nuklease richtet sich nach Belastung (z. B. auf Anzahl der Proben). Destilliertes Wasser ist zum Ausführen des Autoklav Sterilisators erforderlich. Autoklaven Wasserverbrauch pro Zyklus beträgt 160-180 mL; der Autoklav ist für den täglichen Gebrauch empfohlen. Die meisten Kunststoffe (Rohre, Pipettenspitzen, etc.) sind Einweg, aber einige sind wiederverwendbar und müssen gereinigt werden (große Behälter, Regale usw.). Regelmäßige fließendes Wasser dient zum Händewaschen zwischen den Eingriffen und die minimale Lautstärke ist schätzungsweise 15-20 L täglich. Das Wasser muss für Druck gepumpt werden; Sediment-Vorfilter-System wird die Wasser-Geräte vor die schädigende Wirkung von Sedimenten zu schützen und zur Verbesserung der Qualität von fließendem Wasser empfohlen.
Für die Kühllagerung, mindestens 5,1 Kubikfuß kühl-(+ 4 ° C) und eine 4,9 Kubikfuß (-20 ° C bis-30 ° C) sind in jedem Laborgerät zum Proben speichern erforderlich / RNA.
Labor-Dekontamination umfasst mehrere Ebenen: Reinigung > Antisepsis > Desinfektion > Sterilisation. Einfache Reinigung kann mit Seife und Wasser beim Schrubben mit einem behandschuhten Hand oder einer Bürste durchgeführt werden. Antisepsis beinhaltet waschen mit flüssigen antimikrobielle chemische um das Wachstum und die Vermehrung der Keime zu hemmen. Alkoholische Lösungen (70 %) kann als eine antiseptische Flüssigkeit verwendet werden. Desinfektion ist die Anwendung von flüssigen Chemikalien, fast alle pathogene Mikroorganismen (mit Ausnahme von Bakteriensporen) auf Arbeitsflächen und Geräte zu beseitigen. Exposition gegenüber chemischen Stoffen Zeit, Temperatur und Konzentration des Desinfektionsmittels sind wichtig. Natriumhypochlorit-Lösung (0,5 %) oder Bleichmittel, ist ein effektives Desinfektionsmittel in großem Maßstab für Oberflächen Reinigung und Wasseraufbereitung. Keimtötende UV-Bestrahlung ist eine weitere Methode der Desinfektion. Eine keimtötende Lampe UV-C Licht produziert und führt zur Inaktivierung von Bakterien und Viren. Sterilisation beschäftigt eine physikalische oder chemische Verfahren, alle mikrobielles Leben--einschließlich hochresistente bakterielle-Sporen zu zerstören. Sterilisation erfolgt mit einem Autoklav Sterilisator.
Alle Labor-Abfälle muss zum Zeitpunkt der Erzeugung getrennt werden. Platz solide, nicht scharf, infektiöse Abfälle in auslaufsicheren Müllbeutel als Biohazard gekennzeichnet. Wenn Abfallaufkommen scharf ist, muss es in pannensicher Container platziert werden. Sammeln Sie potentiell infektiösen flüssigen Abfällen in ordentlich beschrifteten Biohazard Behälter für Flüssigkeiten. Behältnisse und Taschen sollten nicht mehr als 2/3 des Volumens gefüllt werden. Die Entsorgung aller Bleichmittel Produkte muss in ihr eigenes dafür vorgesehenen Abfallbehälter sortiert werden. Labor Abfall muss vorsichtig behandelt werden, um zu vermeiden, Erzeugung von Aerosolen und Bruch der Taschen/Container. Taschen/Sammelbehälter mit Biohazard Abfälle müssen versiegelt und Außenflächen, die nach Gebrauch mit 0,5 % Natriumhypochlorit-Lösung dekontaminiert werden. Alle Labor Abfälle sterilisieren im Autoklaven bei 121 ° C für 30 Minuten vor der Verbrennung. Finden Sie funktionierende Handbuch für die ordnungsgemäße Verwendung der Autoklav. Wenn möglich, fügen Sie einen chemischen oder biologischen Indikator den Autoklaven zur ordnungsgemäßen Sterilisation zu gewährleisten hinzu. Alle autoklaviert fester und flüssiger Abfälle muss eindeutig gekennzeichnet sein, wie mit der Einstellung, Datum, Uhrzeit und Betreiber sterilisiert. Die beschriftete Abfälle muss dann in einem sicheren, separaten Bereich vor der Verbrennung platziert werden.
Wie erwartet, hängt Workflow diagnostischen Tests von der Krankheit und Probe. Wenn es für Virus Identifikation Blutproben (z. B. Ebola-19) sammeln empfohlen wird, können Probe Aliquote bei-20 ° C anstelle von-80 ° C (erforderlich für respiratorische Viren) gespeichert werden. Es ist immer besser, mehr als eine Probe zu nehmen, bei der Probennahme von einem Patienten als zu unterteilen Exemplare später. Wenn möglich, für jede Art von Muster müssen mindestens zwei Exemplare in separaten Probe Rohren getroffen werden. Proben müssen unterteilt werden, wenn zusätzliche Probenahme nicht möglich ist.
Wenn alternative Exemplare bei entsprechenden Temperaturen gelagert werden können (z. B. keine Gefrierschränke sind vorhanden), Tupfer sollten gespeichert werden, in reinen (100 %) Ethanol oder 99 % Methylalkohol (Methanol Additive nur). In diesem Fall muss ein Fläschchen mit 1-2 mL Ethanol Tupfer Tipp umgesetzt werden. Beachten Sie, dass solche Exemplare nur für PCR geeignet sind. Darüber hinaus beachten Sie, dass ein gut etablierter Assay ist notwendig für jeden bestimmten Virus Diagnose8,23, unbekannte Virusproben erfolgen und ist an zugewiesenen Laboratorien für weitere Untersuchungen19,20, 21.
Obligatorischen und empfohlenen Anforderungen zur Liste von Laborgeräten für respiratorische Viren diagnostische PCR Tests müssen erkannt werden. Tabelle 3 unterstreicht aus- und minimal (empfohlen) Ausrüstung und Anforderungen für die RT-PCR-Diagnosetest. Für die Praxis BSL-3 ist zusätzliche negative Druck Schutz (z. B. Glove-Box) des Personals wichtig und notwendig.
Die angeschlossenen Labormodule sind vorzuziehen, die Zahl der Mitarbeiter in Labortests und beschleunigen Sie den Zeitaufwand für einen einzigen Test. Ersetzen die zeitraubende manuelle RNA-Extraktion ist möglich mit automatisierten qPCR (z. B. QiaCube). Während dieses Instrument umständlich ist (Breite 65 cm, Länge 62 cm, Höhe 86 cm), es kann den mobilen Labor-Arbeitsbereich nach Umstellung der Möbel in BSL-2 oder BSL-3 Einheiten passen.
Zukünftige Arbeit richtet sich auf die Entwicklung von augmented Reality (AR) und virtuelle Realität (VR) Trainings. AR/VR-Brille werden verwendet, eine interaktive Plattform erforderliche Fähigkeiten, um ein gut ausgebildetes Labor Arbeiter werden zu lehren. Hilfreiche Tipps, um einige der schwierigen, mehrstufigen Verfahren in diagnostischen Laboruntersuchungen durchführen werden in der Software-Guide aufgenommen werden. Dieser Ansatz zur Schulung des Personals sollte die Verbesserung der diagnostischen Test Performance und Management in abgelegenen Laboreinrichtungen, besonders abgelegenen und Ressourcen eingeschränkt.
Offenlegungen
Baylor College of Medicine hält eine provisorische Patentanmeldung US für Mobile Kliniken (US-Patent Anwendung Nr. 15/523.126, # 620078924). Die Autoren erklären, dass sie keine konkurrierendes finanzielles Interesse haben.
Danksagungen
Der Inhalt dieses Artikels spiegelt nicht unbedingt die Ansichten oder die Richtlinien von uns Department of Health And Human Services oder der Organe verbunden mit den Autoren. Diese Forschung wurde von Paul G. Allen Family Foundation "Enhanced Zero-Impact, Notfall-Smart-Pod" unterstützt. Wir schätzen die konstruktive Gespräche und Zusammenarbeit mit den Kollegen vom Baylor College of Medicine, GSS Gesundheit, NASA Johnson Space Center. Wir sind aufrichtig dankbar Thermo Fisher Scientific und seinen Vertretern für ein Darlehen von der RT-PCR-Maschine, Zentrifuge und automatisierte Pipetten zur Durchführung eines respiratorischen Virus diagnostischen Tests in der abgelegenen Laboreinrichtung. Die Autoren sind dankbar, dass Marta Storl-Desmond und Sidney Stephen Sorrell für ihre Unterstützung bei der Vorbereitung Manuskript und Videografie.
Materialien
| Name | Company | Catalog Number | Comments |
| Autoclave Sterilizer 'BioClave' | Benchmark Scientific, Edison, NJ, USA | B4000-16 | 16 liter, Benchtop, Dims: 22x17.5x15.7 in, Fully automatic, Extremely Compact |
| Barcode Scanner | Zebra Technologies ZIH Corp., Lincolnshire, IL, USA | Symbol LS2208 | Handheld, lightweight |
| Breaker Box Panelboard Enclosure | Square D (Schneider Electric), France | MH62WP | NEMA 3R/5/12, Dims: 20 W x 62 H x 6-1/2 in. D, Electrical distribution board |
| Centrifuge - Microcentrifuge 17,000 x g | Thermo Fisher Scientific, Carlsbad, CA, USA | 75002440 | Holds 24 x1.5 or 2 ml tubes, Dims: 8.9x9.6x13.8 in |
| Class II Biological Safety Cabinet | NuAire, Inc., Plymouth, MN, USA | NU-602-400 | 4 Ft. Class II Type A2 Cage Changing Biological Safety Cabinet, 12" Access Opening, HEPEX Pressure Duct |
| Class III Biological Safety Cabinet (Glove box) | Germfree Laboratories, Ormond Beach, FL, USA | Model #PGB-36, Serial #C-2937 | Glove box, Portable, 36", Class III BSC. Dims: 36x20x23.75 in, Includes 2 interior outlets |
| Cryo Coolers | VWR, Radnor, PA, USA | 414004-286 | 0.5 or 1.5 ml tube benchtop coolers |
| Freezer (30°C freezer) | Thermo Fisher Scientific, Carlsbad, CA, USA | Model ULT430A | To occupy 4.9 Cubic feet |
| Laminar Flow Cabinet | NuAire, Inc., Plymouth, MN, USA | NU-126-300 | 3 Ft. Vertical Laminar Airflow Cabinet, 8" Access Opening, HEPA filter supply, 99.99% |
| Mini Centrifuge | Thermo Fisher Scientific, Carlsbad, CA, USA | 75004061 | Dims: 4.1x5.0x6.0 in |
| Pipettes automated | VWR, Radnor, PA, USA | 05-403-151 | Pipet 4-pack (2.5,10, 100 and 1,000μL volume) |
| Pipettes automated 'Finnpipette' | Thermo Fisher Scientific, Carlsbad, CA, USA | 4700880 | Pipet 4-pack (2, 20, 200 and 1,000μL volume), Advanced Volume Gearing(AVG), Ultra durable |
| Power Generator | Cummins Power Generation, Minneapolis, MN, USA | C60 D6 | 60 kW, 60 Hz, 1 Phase, 120/240V, Diesel |
| Refrigerator | BioMedical Solutions, Inc., Stafford, TX, USA | BSI-HC-UCFS-0504W | Standard Undercounter Refrigerators & Freezers |
| Refrigerator | Thermo Fisher Scientific, Carlsbad, CA, USA | 05LRAETSA | To occupy 5.1 Cubic feet |
| RT-PCR machine 'Step-one plus' | Thermo Fisher Scientific, Carlsbad, CA, USA | 4376598 | Holds 96 samples, Dims: 9.7x16.8x20.2 in |
| Vortex Mix | Thermo Fisher Scientific, Carlsbad, CA, USA | 88880017TS | Dims: 6.1x8.3x3.3 in |
| Chemicals | |||
| AgPath-ID One-Step RT-PCR Reagents | Applied Biosystems, Foster City, CA, USA | 4387391 | |
| Ethanol Koptec Pure 200 Proof | Decon Labs, Inc., King of Prussia, PA, USA | V1001 | |
| Nuclease-free Water | Ambion, Inc., Carlsbad, CA, USA | AM9906 | |
| QIAamp Viral RNA Mini Kit | Qiagen, Hilden, Germany | 52906 | |
| SuperScript III Platinum One-Step qRT- PCR Kit | Invitrogen, Carlsbad, CA, USA | 11732-088 | |
| Disposable | |||
| 1 mL cryogenic tubes | Thermo Fisher Scientific, Carlsbad, CA, USA | 03-337-7X | |
| 1.5 mL tubes | VWR, Radnor, PA, USA | 10025-726 | |
| 10 µL Filter Tips | Neptune, VWR, Radnor, PA, USA | Neptune, BT10XLS3 | |
| 20 µL Filter Tips | Multimax, BioExpress, VWR, Radnor, PA, USA | MultiMax, P-3243-30X | |
| 200 µL Filter Tips | ART, Thermo Fisher Scientific, Carlsbad, CA, USA | ART, 2770 | |
| 1000 µL Filter Tips | Phenix Research Products, Candler, NC, USA | TS-059BR | |
| AB custom probes | Thermo Fisher Scientific, Carlsbad, CA, USA | N/A | Custom probes |
| Combitips | Eppendorf, Hauppauge, NY, USA | 89232-972 | |
| Integrated DNA Technology (IDT) custom probes and primer | IDT | N/A | Custom probes |
| MicroAmp Fast Optical 96-Well Reaction Plate | Thermo Fisher Scientific, Carlsbad, CA, USA | 490003-978 CS | |
| MicroAmp Fast Reaction Tubes (8 tubes/strip) | Thermo Fisher Scientific, Carlsbad, CA, USA | 4358293 | |
| MicroAmp Optical 8-Cap Strip | Thermo Fisher Scientific, Carlsbad, CA, USA | 4323032 | |
| MicroAmp Optical Adhesive Film | Thermo Fisher Scientific, Carlsbad, CA, USA | 4311971 | |
| Supplies | |||
| Biohazard waste bags | VWR, Radnor, PA, USA | 14220-046 | 20.3 x 30.5 cm Biohazard bags |
| Gloves | Denville Scientific, Holliston, MA, USA | G4162-250 | Small, meduim or large Nitrile or latex gloves |
| Lab coat | N/A | N/A | Customizable |
| Masks | VWR, Radnor, PA, USA | 414004-663 | Advanced protection mask |
| Protective shoes | N/A | N/A | Customizable |
Referenzen
- World Health Organization (WHO) Ebola Response Team. Ebola virus disease in West Africa - the first 9 months of the epidemic and forward projections. New England Journal of Medicine. 371 (2), 1481-1495 (2014).
- World Health Organization (WHO). . Media Center: Ebola Virus Disease Fact Sheet No. 103. , (2014).
- Fauci, A. S., Morens, D. M. Zika Virus in the Americas - yet another arbovirus threat. New England Journal of Medicine. 374 (7), 601-604 (2016).
- Campos, G. S., Bandeira, A. C., Sardi, S. I. Zika virus outbreak, Bahia, Brazil. Emerging Infectious Diseases. 21 (10), 1885-1886 (2015).
- Aly, M., Elrobh, M., Alzayer, M., Aljuhani, S., Balkhy, H. Occurrence of the Middle East Respiratory Syndrome Coronavirus (MERS-CoV) across the Gulf Corporation Council countries: Four years update. PLoS ONE. 12 (10), e0183850 (2017).
- World Health Organization (WHO). Middle East respiratory syndrome coronavirus (MERS-CoV) - Oman. Media Center: Disease outbreak news. Mar 18. , (2018).
- Ducharme, J., Johnson, D. This flu map shows how the biggest influenza outbreak in years spread across the U.S. Time, Time Health: Public Health. , (2018).
- Gaglani, M., et al. Influenza vaccine effectiveness against 2009 pandemic influenza A(H1N1) virus differed by vaccine type during 2013-2014 in the United States. Journal of Infectious Diseases. 213 (10), 1546-1556 (2016).
- Gates, B. The next epidemic - lessons from Ebola. New England Journal of Medicine. 372 (15), 1381-1384 (2015).
- Mills, A. Health care systems in low- and middle-income countries. New England Journal of Medicine. 370 (15), 552-557 (2014).
- Wölfel, R., et al. Mobile diagnostics in outbreak response, not only for Ebola: a blueprint for a modular and robust field laboratory. Euro Surveillance. 20 (44), 30055 (2015).
- Connelly, S. Through innovation, education and collaboration, Baylor Global Initiatives seeks to transform health and patient care worldwide. TMC Pulse, Global Perspective. , (2015).
- Hersh, D. USAID funds Ebola 'smart pod' project. Federal Times. , (2015).
- Waite, A. Emergency Smart Pods - Transforming Containers into Modern Medical Clinics. DipNote, U.S. Department of State Official Blog. , (2018).
- . . Guide to US Department of Health and Human Services Regulations. , (2015).
- Center for Disease Control and Prevention (CDC). . Website: Clean up after a Disaster. , (2017).
- Flannery, B., et al. Enhanced genetic characterization of influenza A(H3N2) viruses and vaccine effectiveness by genetic group, 2014-2015. Journal of Infectious Diseases. 214 (7), 1010-1019 (2016).
- Spencer, S., et al. Factors associated with real-time RT-PCR cycle threshold values among medically attended influenza episodes. Journal of Medical Virology. 88 (4), 719-723 (2016).
- Cherpillod, P., et al. Ebola virus disease diagnosis by real-time RT-PCR: A comparative study of 11 different procedures. Journal of Clinical Virology. 77, 9-14 (2016).
- Dedkov, V. G., et al. Development and evaluation of a real-time RT-PCR assay for the detection of Ebola virus (Zaire) during an Ebola outbreak in Guinea in 2014-2015. Journal of Virological Methods. 228, 26-30 (2016).
- Cnops, L., et al. Developement, integration of a quantitative reverse-transcription polymerase chain reaction diagnostic test for Ebola virus on a molecular diagnostics platform. Journal of Infectious Diseases. 214 (3), S192 (2016).
- Keitel, W. A., et al. Rapid research response to the 2009 A(H1N1)pdm09 influenza pandemic (Revised). BMC Research Notes. 6, 177 (2013).
- Parsons, L. M., et al. Laboratory diagnosis of tuberculosis in resource-poor countries: challenges and opportunities. Clinical Microbiology Reviews. 24 (6), 314-350 (2011).
- . . Expandable Bicon Shelter. Commercial Manual. Sea Box. , (2019).
- . Lab Safety. Operating the Glovebox. JoVE Science Education Database. , (2018).
- World Health Organization (WHO). . Collecting, preserving and shipping specimens for the diagnosis of avian influenza A(H5N1) virus infection. , (2006).
- Lorenz, T. C. Polymerase Chain Reaction: Basic Protocol Plus Troubleshooting and Optimization Strategies. Journal of Visualized Experiments. (63), e3998 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten