Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Eine hochmoderne Methode zum Erhalt des Restgehörs bei einer Cochlea-Implantat-Operation
In diesem Artikel
Zusammenfassung
Der Erhalt der Cochlea-Strukturen und eines möglichen Restgehörs ist ein wichtiger Faktor, der bei der Cochlea-Implantat-Operation zu berücksichtigen ist. Hier stellen wir Ihnen eine hochmoderne Methode zum Erhalt des Restgehörs bei einer Cochlea-Implantat-Operation unter örtlicher Betäubung vor.
Zusammenfassung
Die Entwicklungen bei den Operationstechniken und dem Design von Cochlea-Implantaten (CI)-Elektroden haben die Indikationen für die CI-Behandlung erweitert. Derzeit können Patienten mit hochfrequentem Hörverlust von CIs profitieren, wenn das niederfrequente Restgehör erhalten werden kann, da dies eine kombinierte elektrisch-akustische Stimulation (EAS) ermöglicht. Zu den möglichen Vorteilen von EAS gehören beispielsweise eine verbesserte Klangqualität, Musikwahrnehmung und Sprachverständlichkeit im Störgeräusch.
Die Risiken eines Innenohrtraumas und einer Verschlechterung oder sogar eines vollständigen Verlustes des Restgehörs variieren je nach Operationstechnik und Art des verwendeten Elektrodenträgers. Kurze, lateralwandige Elektroden mit geringeren winkelförmigen Einstichtiefen haben eine höhere Gehörerhaltung gezeigt als längere Elektroden. Das sehr langsame Einführen des Elektrodenarrays durch das runde Fenster der Cochlea trägt zur Atraumatität des Einführens bei und kann somit zu günstigen Ergebnissen bei der Gehörerhaltung führen. Das Restgehör kann aber auch nach einem atraumatischen Einsetzen verloren gehen.
Die Elektrocochleographie (ECochG) kann verwendet werden, um die Funktion der Haarzellen im Innenohr während des Einführens der Elektrode zu überwachen. Mehrere Forscher haben gezeigt, dass die ECochG-Reaktionen während der Operation die Ergebnisse der postoperativen Gehörerhaltung vorhersagen können.
In einer aktuellen Studie korrelierten wir die subjektive Hörwahrnehmung der Patienten mit gleichzeitig aufgezeichneten intracochleären ECochG-Reaktionen während des Insertions. Dies ist der erste Bericht, in dem der Zusammenhang zwischen intraoperativen ECochG-Reaktionen und der Hörwahrnehmung bei einem Probanden untersucht wird, der sich einer Cochlea-Implantation unter örtlicher Betäubung ohne Sedierung unterzieht. Die Kombination von intraoperativen ECochG-Antworten mit dem Echtzeit-Feedback des Patienten auf Klangreize bietet eine hervorragende Sensitivität für die intraoperative Überwachung der Cochlea-Funktion. In dieser Arbeit wird eine hochmoderne Methode zur Erhaltung des Restgehörs während der CI-Operation vorgestellt. Wir beschreiben dieses Behandlungsverfahren unter besonderer Berücksichtigung der Durchführung der Operation unter örtlicher Betäubung, was es möglich macht, das Gehör des Patienten während des Einführens des Elektrodenarrays zu überwachen.
Einleitung
Die Cochlea-Implantation ist die einzige Behandlung im klinischen Einsatz, die die Funktion eines Sinnesorgans wiederherstellt. Derzeit wird die Cochlea-Implantation zur Behandlung von schwerem bis hochgradigem Schallempfindungsschwerhörverlust bei Kindern und Erwachsenen eingesetzt. Das Cochlea-Implantat-System (CI) besteht aus einem implantierbaren internen Gerät, das mit einem externen Soundprozessor kombiniert wird. Das interne Gerät wird während der Operation durch die Warzenhöhle eingeführt. Die Gesichtsaussparung wird geöffnet, um Zugang zum Mittelohr und zur Cochlea zu erhalten. Das Elektrodenarray wird durch die hintere Tympanotomie und das runde Fenster der Cochlea in die Cochlea eingeführt. Das Elektrodenarray sorgt für die elektrische Stimulation, indem es defekte äußere und innere Haarzellen umgeht und die Ganglienzellen des Hörnervs direkt stimuliert.
Es wurde gezeigt, dass der Erhalt der Integrität der Innenohrstrukturen nach einer CI-Operation zu günstigeren Hörergebnissen beitragen kann im Vergleich zu Elektrodeneinführungen, die strukturelle Schäden am Innenohr verursachen können 1,2. Dies hat zur Entwicklung feinerer Operationstechniken und dünnerer, flexiblerer und damit weniger traumatischer Elektrodenarrays geführt. Diese Entwicklungen haben zu verbesserten Hörergebnissen beigetragen, was zu einer Erweiterung der Indikationen für die CI-Rehabilitation geführt hat. Patienten mit schwerem Hörverlust im Hochfrequenzbereich (>1,5 kHz) können ebenfalls von einer Cochlea-Implantation profitieren, insbesondere wenn ihr natürliches Gehör in den tiefen Frequenzen (<1 kHz) erhalten bleiben kann. Das Hören niedriger Frequenzen nach der Operation ermöglicht es dem Patienten, von der elektroakustischen Stimulation (EAS) zu profitieren3,4. Das EAS ist eine Kombination aus elektrischer Stimulation der hochfrequenten Bereiche der Cochlea, die sich in den basalen Teilen der Cochlea befinden, und akustischer Verstärkung der erhaltenen niederfrequenten Bereiche (typischerweise 125-500 Hz) in den apikalen Teilen der Cochlea.
Die besten Ergebnisse bei der Gehörerhaltungschirurgie wurden mit kürzeren Elektrodenarrays erzielt, die speziell für EAS-Kandidaten entwickelt wurden 4,5,6. Es kann einen großen Nachteil geben, der mit den kurzen Elektrodenarrays verbunden ist - der Verlust des Restgehörs (entweder nach der Operation oder danach). Letztendlich kann der Patient von einem längeren Elektrodenarray profitieren, das einen breiteren Frequenzbereich abdeckt, insbesondere in Fällen, in denen es zu einem unglücklichen Verlust des Restgehörs gekommen ist 5,7. Vor kurzem hat die Einführung des teilweisen Einführens der längeren Seitenwandelektrode bei Patienten mit mittelschwerem Hörverlust bei höheren Frequenzen und normalem oder leichtem Hörverlust bei niedrigeren Frequenzen die Option für eine anfängliche flache Insertion bei EAS-Kandidaten geschaffen, aber auch eine tiefere Einführung mit demselben Array erleichtert, wenn das Restgehör verloren geht8.
Die Elektrocochleographie (ECochG) ist eine Methode, mit der die Cochlea-Funktion während der Cochlea-Implantation überwacht werden kann, und sie wird zunehmend im klinischen Einsatz eingesetzt. Derzeit bieten die drei führenden CI-Hersteller ein klinisch zugelassenes Instrument oder zumindest ein Forschungsinstrument für intracochleäre intraoperative ECochG-Messungen an. Eines bietet eine All-in-One-Lösung, bei der die Aufzeichnung von Stimulation und Reaktion in einem Tool integriert ist, während die Tools der anderen Hersteller einen separaten Stimulator benötigen. ECochG misst die elektrophysiologische Reaktion des Innenohrs und des Hörnervs auf einen akustischen Reiz. Es scheint, dass die Amplituden der ECochG-Antworten, die während des Elektrodeneinführens gemessen werden, die postoperative Hörerhaltung vorhersagen können. Somit scheint die intraoperative ECochG ein vielversprechendes Instrument zur Bereitstellung von Informationen zu sein, die die Prävention von Traumata ermöglichen 9,10,11,12. Aktive Forschung und das gestiegene klinische Interesse an der Beurteilung intraoperativer ECochG-Messungen haben die Frage aufgeworfen, wie die ECochG-Antworten objektiv analysiert werden können und wie auf die Veränderungen in der Amplitude der Reaktion während der Insertion reagiert werden kann.
Die Durchführbarkeit und der Nutzen einer CI-Operation unter örtlicher Betäubung wurden in mehreren Studien berichtet 13,14,15,16. CI-Kandidaten mit signifikanten Komorbiditäten können unter örtlicher Betäubung operiert werden, wodurch die mit einer Vollnarkose verbundenen Risiken vermieden werden. Eine Vollnarkose ist mit einem erhöhten Risiko für eine kognitive Verschlechterung verbunden, insbesondere bei älteren Patienten, und sie wurde auch mit einer höheren Mortalität in diesen Gruppen in Verbindung gebracht17. Wenn eine CI-Operation unter örtlicher Betäubung durchgeführt wird, ist die Genesung von der Operation schneller, und daher verbringt der Patient weniger Zeit im Krankenhaus im Vergleich zu einer ähnlichen Operation, die unter Vollnarkose durchgeführt wird 14,15,18,19. Es wurde auch vorgeschlagen, dass Patienten mit Restgehör in der Lage sein könnten, ihr Gehör während des Einsetzens zu überwachen, was den Chirurgen beim Einsetzen der CI-Elektrode leiten und ein intracochleäres Trauma vermeiden kann14.
Wir haben kürzlich ECochG und subjektive Klangwahrnehmung als Indikatoren für den Erhalt des Gehörs in der CI-Operation unter örtlicher Betäubung verglichen20. Die Ergebnisse zeigten eine gute Vorhersage des Gehörerhalts mit beiden Methoden, und ähnliche Muster wurden zwischen subjektiver Berichterstattung und ECochG-Monitoring beobachtet. Das subjektive Feedback der Patienten zur Klangwahrnehmung, das möglich war, da nur eine Lokalanästhesie verwendet wurde, schien dazu beizutragen, das Risiko eines Traumas des Innenohrs während des Einsetzens zu minimieren, selbst in Fällen, in denen die ECochG-Antworten während des Einsetzens nicht gemessen werden konnten.
Hier stellen wir Ihnen eine hochmoderne Methode zum Erhalt des Restgehörs während einer CI-Operation vor. Wir beschreiben die Behandlungsabläufe, einschließlich der besonderen Überlegungen, die mit der Durchführung der Operation unter örtlicher Betäubung (z.B. ECochG) und dem subjektiven Hörmonitoring verbunden sind.
Access restricted. Please log in or start a trial to view this content.
Protokoll
Das Protokoll wurde vom Institutional Review Board (5551877) und der Forschungsethikkommission des Krankenhausbezirks Nord-Savo (1690/2019) genehmigt und gemäß den Richtlinien der Deklaration von Helsinki durchgeführt. Die Einverständniserklärung wurde von allen Patienten eingeholt, die sich freiwillig für die Studie gemeldet hatten.
1. Präoperative Überlegungen
- Beurteilung der Resthörschwelle
- Stellen Sie sicher, dass die präoperativen Reintonschwellendurchschnitte (PTA) bei 0,250-1 kHz bei ≤75 dB liegen und dass der Patient den Reiz bei 500 Hz oder 1.000 Hz bei ≤100 dB deutlich hören kann (Abbildung 1).
- Patientenbewertung, Ein- und Ausschlusskriterien
- Stellen Sie sicher, dass der Patient für eine CI-Operation geeignet ist, die unter örtlicher Betäubung durchgeführt werden soll. Beurteilen Sie die Eignung anhand der Fähigkeit des Patienten, ruhig zu sein, und verstehen Sie die Kommunikation während der Operation und die Grenzen der Operation. Lassen Sie den operierenden Chirurgen in der Ambulanz ein sorgfältiges Gespräch und eine Untersuchung durchführen, um zu beurteilen, ob der Patient in der Lage sein wird, während der Operation angemessen zu reagieren.
- Prüfen Sie, ob der Patient auf der Grundlage der präoperativen Bildgebung (Magnetresonanztomographie [MRT] und Computertomographie [CT]) eine normale Anatomie im Schläfenbereich aufweist und ob es keine Kontraindikationen (z. B. fehlender Cochlea-Nerv oder obstruktive Cochlea) für die CI-Operation gibt.
- Öffnen Sie die Software für den Bildbetrachter für die CT- und MRT-Bilder und wählen Sie aus dem Dropdown-Menü die Option Multiplanare Rekonstruktion (MPR).
- Identifizieren Sie die wichtigsten anatomischen Orientierungspunkte (Mastoidzellen, Duraplatte der mittleren Fossa, Sinus sigmoideus, Nervus facialis, äußerer Gehörgang, Cochlea, interner Gehörgang) aus dem CT-Bildstapel.
- Öffnen Sie die präoperative MRT-Untersuchung und stellen Sie sicher, dass der Patient für die Cochlea-Implantation geeignet ist: Die Cochlea ist ohne Verschlüsse geöffnet, und bei der MRT-Untersuchung wird ein intakter Cochlea-Nerv festgestellt.
- Bewertung der Einstichtiefe und Elektrodenauswahl in Abhängigkeit von der Größe der Cochlea
- Öffnen Sie den Bildbetrachter und die präoperativen CT-Scans. Wählen Sie dann MPR aus der Dropdown-Leiste aus.
- Erhalten Sie die Cochlea-Ansicht aus den CT-Bildern, indem Sie die Bilder im MPR parallel zur Cochlea ausrichten.
- Beurteilen Sie die A-Maße und B-Maße: die Cochlea-Größe, die Länge vom runden Fenster durch den Modiolus und die Höhe senkrecht zur A-Linie durch den Modiolus, gemäß Escudé et al.21, aus der erhaltenen Cochlea-Ansicht und in einer Einstichtiefe von bis zu 270° vom runden Fenster der Cochlea. Messen Sie den Abstand auf 270°, indem Sie dem äußeren knöchernen Rand der Cochlea folgen.
- Wählen Sie eine Elektrodenlänge so, dass neun intracochleäre Elektrodenkontakte mit einem Einführtiefenwinkel (IDA) von 270° bis 300° vorhanden sind.
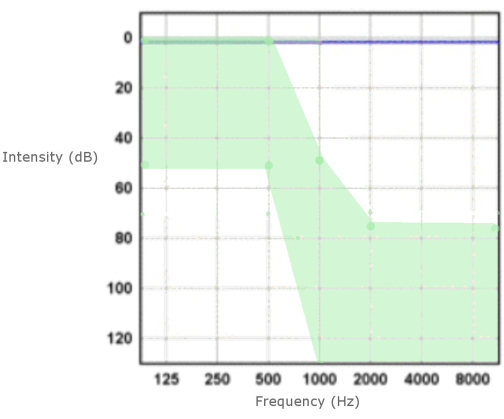
Abbildung 1: Präoperatives Audiogramm. Die Schwellenwerte für die Anzeige werden als grüner Bereich dargestellt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
2. Perioperative Vorbereitungen im Operationssaal (OP)
- Stellen Sie sicher, dass zwischen dem Gesicht des Patienten und dem Tuch ausreichend Platz ist. Prüfen Sie außerdem, ob eine Kommunikation mit dem Patienten mit seinem kontralateralen Hörgerät (HA) möglich ist. Verbinden Sie den HA drahtlos mit einem Remote-Mikrofon, das der Krankenschwester zur Verfügung gestellt wird. Verwenden Sie für den HA ein langes Schallrohr, um unangenehme Rückkopplungen zu vermeiden.
- Wenn der Patient nicht die Möglichkeit hat, eine kontralaterale HA zu erhalten, verwenden Sie alternativ einen Tablet-Computer, um ihm eine schriftliche Kommunikation zu ermöglichen. Testen Sie die Kommunikation mit dem Patienten.
- Verabreichen Sie Antibiotika und Dexamethason (z. B. 1,5 g Cefuroxim und 0,1 mg/kg Dexamethason) intravenös vor dem Hautschnitt.
- Führen Sie den ECochG-Stimulator-Kopfhörer vor dem Schnitt in den äußeren Gehörgang des Patienten ein. Versiegeln Sie den äußeren Gehörgang im Ohrhörer mit Knochenwachs (Abbildung 2).
HINWEIS: Einige Hersteller bieten Schaumstoff-Ohrhörer in steriler Verpackung an. Alternativ kann der Kopfhörer vor dem Drapieren eingeführt werden, und der Schlauch kann unter dem Drapierung zum ECochG-Computer geführt werden. - Legen Sie ein jodförmiges Blatt über den Operationsbereich und richten Sie den Kopfhörer und den Schallschlauch vom Inzisionsbereich weg aus. Achten Sie darauf, dass die iodoforme Abdeckhaube den Schallschlauch während der Aufbereitung nicht verbiegt.
3. Partielle Mastoidektomie, hintere Paukenentfernung und Bohren des Implantatbettes mit einem chirurgischen Bohrer
- Bohren Sie die partielle Mastoidektomie und die hintere Paukenmostomie und bereiten Sie das Implantatbett vor.
4. Einsetzen
- Stellen Sie für die ECochG-Vorbereitung sicher, dass ein Medizinphysiker/klinischer Ingenieur im OP anwesend ist, der hier als ECochG-Bediener bezeichnet wird.
- Bereiten Sie das Gerät für die Durchführung der ECochG-Klangstimulation (siehe Materialtabelle) und die Messung des Ansprechverhaltens durch das CI vor. Das Setup variiert je nach CI-Hersteller leicht.
- Verbinden Sie den Schallschlauch mit dem Stimulator.
- Verbinden Sie die Implantatspule und das Kabel mit dem Messgerät.
- Schrauben Sie die Messspule und das Kabel in die sterile Hülle ein.
- Starten Sie das Messprogramm je nach Hersteller von einem Laptop aus oder verwenden Sie ein Tablet-basiertes System.
- Der Stimulus ist ein Tone-Burst, und die Länge des Bursts hängt von der Stimulusfrequenz ab. Wählen Sie die Stimulusfrequenz (in der Regel Stimuli mit der höchsten erhaltungsfähigen Frequenz von 500 Hz oder 1.000 Hz während des Einführens), den zu verwendenden Schalldruck und die Stimulusamplitude (z. B. 80-100 dB nHL, damit der Stimulus gut gehört und tolerierbar ist) aus der ECochG-Software aus. Behalten Sie je nach Hersteller die anderen Messparameter bei den Standardwerten bei oder ändern Sie sie wie folgt: ein Messfenster von 6,5-9,7 ms mit einer Verzögerung von bis zu 2 ms nach Stimulusbeginn und durchschnittlich 40-150 Aufzeichnungen pro Datenpunkt. Wiederholen Sie im Idealfall den Stimulus mit abwechselnder Polarität und Reaktionen mit Kondensation und subtrahieren Sie die Verdünnungspolarität, um die Cochlea-Mikrofonie-Komponente zu extrahieren (Abbildung 3).
- Verwenden Sie den ersten oder zweiten Kontakt der Elektrode für die ECochG-Messung. Überprüfen Sie die Impedanz des Messkanals kurz nachdem sich der Kontakt in der Cochlea befindet und vor der ersten Messung.
- Bitten Sie den OP-Assistenten, zum Patienten zu gehen und ihm die Anweisungen über die subjektive Berichterstattung über die Veränderungen der Schallreize zu wiederholen.
- Testen Sie die Schallreize und bestätigen Sie dem Patienten, dass er die Reize deutlich hören kann.
- Weisen Sie den Patienten an, über Abweichungen, wie z. B. Abnahme oder Verschwinden der wahrgenommenen Reize, zu informieren.
- Bereiten Sie das Gerät für die Durchführung der ECochG-Klangstimulation (siehe Materialtabelle) und die Messung des Ansprechverhaltens durch das CI vor. Das Setup variiert je nach CI-Hersteller leicht.
- Vorbereitungen des Chirurgen vor dem Einsetzen
- Nehmen Sie das CI-Gerät und platzieren Sie den Empfänger/Stimulator in das Implantatbett.
- Öffnen Sie die runde Fenstermembran der Cochlea. Machen Sie mit einer Injektionsnadel einen Schlitz in die untere Begrenzung des runden Fensters und heben Sie die Membran vorsichtig mit einem mikrochirurgischen Haken nach hinten. Spülen Sie den runden Fensterbereich mit Dexamethason-Lösung.
- Überprüfen Sie die Ausrichtung des CI-Elektrodendrahtes innerhalb der Mastoidkavität, um Rotationskräfte auf die Elektrode und die intracochleären Strukturen des Elektrodendrahts nach dem Einführen zu vermeiden.
- Erreichen Sie eine gute ergonomische Position mit der bestmöglichen Unterstützung der Hände, um ein langsames und kontrolliertes Einführen zu erleichtern.
- Start der Einfügung
- Lassen Sie den Chirurgen das Team darüber informieren, dass das Einsetzen beginnt, und stellen Sie sicher, dass alles bereit ist.
- Nehmen Sie die Elektrode mit der Einführzange und beginnen Sie mit dem Einstechen der Elektrode in die Cochlea durch das runde Fenster.
- Zu Beginn des Einführens führen Sie zuerst die Elektrode direkt in die Cochlea ein (ein oder zwei Kontakte in der Cochlea). Lassen Sie den ECochG-Bediener die Impedanz nach dem Einfügen des ersten und/oder zweiten Kontakts messen. Wenn die Impedanz sehr hoch ist, wechseln Sie den Messkanal.
- Lassen Sie den ECochG-Bediener die Messung nach den Impedanzmessungen starten. Stellen Sie sicher, dass die Elektrode sehr langsam vorangetrieben wird, mit ständigem Feedback von der Person, die die ECochG-Reaktionen beobachtet (Abbildung 4).
HINWEIS: Je nach Hersteller kann es auch eine Option geben, dass das Aufnahmegerät auditives Feedback liefert - einen Ton, der mit zunehmender Reaktion lauter wird. Dieser Ton kann jedoch zusammen mit anderen Geräuschen im OP die subjektive Bewertung des wahrgenommenen Reizes durch den Patienten stören. - Lassen Sie den Chirurgen die Insertion mit 1-2 mm Vorsprüngen (eine Elektrode) fortsetzen. Holen Sie zwischen diesen Fortschritten eine Rückmeldung des Patienten über die Lautstärke der wahrgenommenen Schallreize ein.
- Wenn die ECochG-Reaktionen schwächer werden oder der Patient über eine Abnahme der wahrgenommenen Lautstärke der Schallreize berichtet, bricht die Insertion ab.
- Warten Sie 30-60 s und erkundigen Sie sich dann nach den Reizen des Patienten. Kommunizieren Sie gleichzeitig mit dem ECochG-Betreiber über den aktuellen Status der ECochG-Überwachung (CM-Antwort).
- Wenn sich eine der Reaktionen (ECochG oder subjektive Antworten) nicht erholt, wenn die Elektrode bewegungslos ist, ziehen Sie die Elektrode schrittweise um jeweils ein bis zwei Kontakte zurück (der Wert von ~2 mm hängt davon ab, welche Elektrodenmarke verwendet wird) und warten Sie jedes Mal auf die Antwort. Ziehen Sie die Elektrode gerade so weit zurück, bis sich die Reaktionen erholt haben.
- Wenn die ECochG-Reaktionen oder die wahrgenommene Lautstärke nach dem Einstellen der Insertion nicht wieder ansteigen, aber die gewünschte IDA (270°-300°) (basierend auf präoperativen Messungen und der Anzahl der Elektroden in der Cochlea) erreicht wurde, brechen Sie die Insertion ab. Die Situation wird als abgeschlossene Teileinfügung interpretiert.
- Wenn die Reaktionen wieder zunehmen, setzen Sie das Einfügen wie oben beschrieben fort (Schritte 4.4.5-4.4.7).
- Versiegeln Sie das runde Fenster mit Fettgewebe, das aus dem postaurikulären Schnitt entnommen wurde.
- Verwenden Sie außerdem Fibrinkleber und Knochenstaub, um die Nut für das Elektrodenkabel zwischen dem Empfänger/Stimulator und der Mastoidhöhle abzudichten.
- Fixiere den Elektrodendraht in der Mastoidhöhle mit Knochenstaub und Fibrinkleber.
- Verschließen Sie die Wunde mit chirurgischen Nähten. Überwachen Sie den Patienten nach der Operation während einer Übernachtung auf der Station.
5. Nachsorge
- Überweisen Sie den Patienten an die Cone-Beam-Computertomographie (DVT) zur postoperativen Bildgebung der Implantation.
- Überprüfen Sie die Platzierung der Elektrode anhand der DVT-Bilder.
- Öffnen Sie die DVT-Bilder und wählen Sie MPR aus der Dropdown-Liste.
- Rufen Sie die Cochlea-Ansicht in der MPR ab.
- Überprüfen Sie die IDA und die Position der Elektrode , indem Sie durch die Bilder im MPR scrollen. Überprüfen Sie die Anzahl der intracochleären Elektroden aus der Cochlea-Ansicht , um die Anpassung des CI zu steuern, insbesondere in Fällen, in denen eine teilweise Einführung erfolgt, und identifizieren Sie die stimulierenden Elektroden.
- Überprüfen Sie die Platzierung der Elektrode anhand der DVT-Bilder.
- Überweisen Sie den Patienten für ein postoperatives Audiogramm, um das Restgehör am ersten postoperativen Tag nach der Operation und 1 Monat später zu messen. Messen Sie das Restgehör routinemäßig während der Nachsorge der Anpassung.
HINWEIS: Die Nachbeobachtung von 1 Monat ist in Bezug auf die Ergebnisse der Hörerhaltung zuverlässiger als der erste postoperative Tag.
Access restricted. Please log in or start a trial to view this content.
Ergebnisse
Sowohl die subjektive Überwachung als auch ECochG können dazu beitragen, das Auftreten eines Einführtraumas zu verhindern und somit postoperativ bessere Ergebnisse bei der Gehörerhaltung zu erzielen. Im Audiogramm wird eine Abnahme der PTA (125-500 Hz) innerhalb von 15 dB des präoperativen Hörpegels als Erhalt des Restgehörs und damit als positives Ergebnis nach der Operation angesehen. Ein negatives Ergebnis ist der Verlust des Restgehörs: eine <...
Access restricted. Please log in or start a trial to view this content.
Diskussion
Die optimale Nutzung der Cochlea-Implantation ist wichtig für die effektive Behandlung von Hörverlust. Durch die Erweiterung der Indikationen für die CI-Rehabilitation ist eine Grauzone entstanden, in der individuelle Entscheidungen über die angewandten Rehabilitationsmodalitäten getroffen werden müssen. Heutzutage gibt es bei Patienten mit hochfrequentem Hörverlust einen Trend zur Bereitstellung von CIs. Das Restgehör in den tiefen Frequenzen kann jedoch nicht bei jedem Patiente...
Access restricted. Please log in or start a trial to view this content.
Offenlegungen
Die Autoren berichten von keinen Interessenkonflikten.
Danksagungen
Aarno Dietz erhielt Stipendien der Academy of Finland (Fördernummer 333525) und des North Savo Regional Grant. Pia Linder hat ein Stipendium der finnischen Regierung für Forschung erhalten (Fördernummer 5551877). Matti Iso-Mustajärvi erhielt Zuschüsse von der finnischen Regierung für Forschung (Fördernummer 5551876), der Instrumentarium Science Foundation, dem North Savo Regional Grant und der Finnish Society of Ear Surgery.
Access restricted. Please log in or start a trial to view this content.
Materialien
| Name | Company | Catalog Number | Comments |
| EarPhone and sound tube | AB/Cochlear/Medel | Usually provided by the company in sterile packages, can be inserted in ear without sterility issues | |
| Ecocgh program | AB/Cochlear/Medel | AB and Medel provides software for clinical use. Also Cochlear has software for ECochG, atleas for research purposes. | |
| Equipments for Cochlear implantation | Basic setup and instrumentation for Cochlear implantation, not spesific to the ECoGh or Subjective hearing monitoring | ||
| Laptop/tablet | AB/Cochlear/Medel | AB has tablet consept as "AIM" for intraoperative ECochG measuring. It is provided by the company. Cochlear and Medelare operated with laptop | |
| Sound Processor | AB/Cochlear/Medel | Also company-specific, need for the connection to the electrode and measuring during the insertion |
Referenzen
- Aschendorff, A., Kromeier, J., Klenzner, T., Laszig, R. Quality control after insertion of the nucleus contour and contour advance electrode in adults. Ear and Hearing. 28 (2), 75-79 (2007).
- Holden, L. K., et al. Factors affecting open-set word recognition in adults with cochlear implants. Ear and Hearing. 34 (3), 342-360 (2013).
- Gantz, B. J., Turner, C., Gfeller, K. E., Lowder, M. W. Preservation of hearing in cochlear implant surgery: Advantages of combined electrical and acoustical speech processing. Laryngoscope. 115 (5), 796-802 (2005).
- Lenarz, T., et al. European multi-centre study of the Nucleus Hybrid L24 cochlear implant. International Journal of Audiology. 52 (12), 838-848 (2013).
- Iso-Mustajärvi, M., Sipari, S., Löppönen, H., Dietz, A. Preservation of residual hearing after cochlear implant surgery with slim modiolar electrode. European Archives of Oto-Rhino-Laryngology. 277 (2), 367-375 (2020).
- Roland, J. T., Gantz, B. J., Waltzman, S. B., Parkinson, A. J. Multicenter clinical trial group. United States multicenter clinical trial of the cochlear nucleus hybrid implant system. Laryngoscope. 126 (1), 175-181 (2016).
- Roland, J. T., Gantz, B. J., Waltzman, S. B., Parkinson, A. J. Long-term outcomes of cochlear implantation in patients with high-frequency hearing loss. Laryngoscope. 128 (8), 1939-1945 (2018).
- Lenarz, T., Timm, M. E., Salcher, R., Büchner, A. Individual hearing preservation cochlear implantation using the concept of partial insertion. Otology & Neurotology. 40 (3), 326-335 (2019).
- Calloway, N. H., et al. Intracochlear electrocochleography during cochlear implantation. Otology & Neurotology. 35 (8), 1451-1457 (2014).
- Trecca, E. M., et al. Electrocochleography and cochlear implantation: A systematic review. Otology & Neurotology. 41 (7), 864-878 (2020).
- Mandalà, M., Colletti, L., Tonoli, G., Colletti, V. Electrocochleography during cochlear implantation for hearing preservation. Otolaryngology-Head and Neck Surgery. 146 (5), 774-781 (2012).
- Kim, J. S. Electrocochleography in cochlear implant users with residual acoustic hearing: A systematic review. International Journal of Environmental Research and Public Health. 17 (19), 7043(2020).
- Alzahrani, M., Martin, F., Bobillier, C., Robier, A., Lescanne, E. Combined local anesthesia and monitored anesthesia care for cochlear implantation. European Annals of Otorhinolaryngology, Head and Neck Diseases. 131 (4), 261-262 (2014).
- Dietz, A., Lenarz, T. Cochlear implantation under local anesthesia in 117 cases: Patients' subjective experience and outcomes. European Archives of Oto-Rhino-Laryngology. 279 (7), 3379-3385 (2021).
- Dietz, A., Wüstefeld, M., Niskanen, M., Löppönen, H. Cochlear implant surgery in the elderly: the feasibility of a modified suprameatal approach under local anesthesia. Otology & Neurotology. 37 (5), 487-491 (2016).
- Hamerschmidt, R., Moreira, A. T. R., Wiemes, G. R. M., Tenório, S. B., Tâmbara, E. M. Cochlear implant surgery with local anesthesia and sedation: comparison with general anesthesia. Otology & Neurotology. 34 (1), 75-78 (2013).
- Strøm, C., Rasmussen, L. S. Challenges in anesthesia for elderly. Singapore Dental Journal. 35, 23-29 (2014).
- Kecskeméti, N., et al. Cochlear implantation under local anesthesia: A possible alternative for elderly patients. European Archives of Oto-Rhino-Laryngology. 276 (6), 1643-1647 (2019).
- Shabashev, S., Fouad, Y., Huncke, T. K., Roland, J. T. Cochlear implantation under conscious sedation with local anesthesia; Safety, efficacy, costs and satisfaction. Cochlear Implants International. 18 (6), 297-303 (2017).
- Linder, P., Iso-Mustajärvi, M., Dietz, A. A comparison of ECochG with the subjective sound perception during cochlear implantation under local anesthesia-A case series study. Otology & Neurotology. 43 (5), 540-547 (2022).
- Escudé, B., et al. The size of the cochlea and predictions of insertion depth angles for cochlear implant electrodes. Audiology and Neurotology. 11 (1), 27-33 (2006).
- Gantz, B., et al. Outcomes of adolescents with a short electrode cochlear implant with preserved residual hearing. Otology & Neurotology. 37 (2), 118-125 (2016).
- Suhling, M. -C., et al. The impact of electrode array length on hearing preservation in cochlear implantation. Otology & Neurotology. 37 (8), 1006-1015 (2016).
Access restricted. Please log in or start a trial to view this content.
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten