Method Article
Alto Rendimiento de medición y clasificación de P orgánico en las muestras ambientales
En este artículo
Resumen
Este protocolo describe un método de alto rendimiento de la hidrólisis enzimática que utiliza un lector de microplacas para medir y clasificar el suelo como el fósforo P monoésteres, diésteres P e inorgánicos P. Hasta 96 muestras se puede medir de una sola vez en un laboratorio estándar.
Resumen
Muchos tipos de orgánicos de fósforo (P) existen moléculas en las muestras ambientales 1. Las mediciones tradicionales de P no detectan estos compuestos orgánicos P, ya que no reaccionan con los reactivos colorimétricos 2,3. Hidrólisis enzimática (EH) es un método emergente para caracterizar con precisión las formas de P orgánico en las muestras de 4,5 ambiental. Este método sólo triunfó en la precisión de Fósforo-31 Espectroscopia de Resonancia Magnética Nuclear (RMN-31 P)-un método que es caro y requiere de técnicos especializados training6. Hemos adaptado un método de hidrólisis enzimática capaz de medir tres clases de fósforo (P monoéster, diéster de P y P inorgánico) a un sistema de lector de microplacas 7. Este método ofrece a los investigadores un medio rápido y preciso, asequible y fácil de usar para medir las especies P en suelos, sedimentos, fertilizantes y, si las muestras de concentrado, acuáticos. Este es el único método de alto rendimiento para la medición de las formas y la enzima labilidad de P orgánico que se pueden realizar en un laboratorio estándar. Los datos resultantes proporciona una idea de los científicos que estudian el contenido de nutrientes del sistema y el potencial de eutrofización.
Protocolo
1. Extracción de fósforo
- Prepare una solución de 1 litro de 0,25 M de hidróxido sódico (NaOH, 40,00 g / mol) + 0,05 M de ácido etilendiaminotetraacético (EDTA, 292,24 g / mol).
- Añadir 30 ml de la solución de NaOH + EDTA a 2 g de suelo húmedo o seco / muestra en un tubo cónico de 50 ml.
- Incubar con agitación durante 16 horas a temperatura ambiente.
- Centrífuga 3000 xg durante 3 minutos.
2. Extracto de la muestra de ajuste de pH
- Transferir una alícuota de 0,1 ml a 1,5 ml un micro-tubo de centrífuga.
- Añadir 0,017 ml de 2,5 M de ácido acético, 0,144 ml de solución tampón de acetato 0,4 M (70,5% de acetato de sodio [CH3COONa, 82,03 g / mol] y el 29,5% de ácido acético, pH 5,0), y 0.739 ml de agua destilada.
- El volumen final del extracto de ajuste será de 1 mL y el pH final será 5,0.
3. Foto enzima preparación de la solución
- Prepare 1 litro de acetato de sodio 0,1 M (CH3COONa, 82,03 g / mol) solución, pH 5,0.
- Prepare 2 x 10 ml de ácido soluciones madre fosfatasa en el buffer de acetato de sodio preparado en el paso 3.1 de tal manera que las concentraciones finales son cada 0,5 unidades / ml.
Fosfatasa ácida de tipo I de Triticum aestivum (germen de trigo, GP, por lo general 0,5 U mg-1 sólido, EC 3.1.3.2)
La fosfatasa ácida Tipo IV-S de Solanum tuberosum (papa, PP, en general, 4,6 U mg-1 sólido, EC 3.1.3.2)
* Las unidades de actividad son especificados por el proveedor, donde se define una unidad como la liberación de un micromol de ortofosfato para la solución por hora a 37 ° C. - Reconstituir liofilizado nucleasa P1 (CE 3.1.30.1) de Penicillium citrinum (hongos, NP1, generalmente de 500 U mg -1 sólido) en un ml de agua desionizada, esto ahora se puede almacenar a 4 ° C para su uso futuro.
- Pipeta NP1 en uno de los tubos de 10 ml preparada en la etapa 3.2 de tal manera que la concentración final es de 2,5 unidades / mL NP1, mezclar suavemente invirtiendo varias veces.
- Centrifugar las dos soluciones de la enzima 10 ml 3000 xg durante 30 minutos.
4. P curva de calibración y controles
- Prepare 1 L de 1 mM fosfato de potasio (K2HPO4, 174,18 g / mol) solución de reserva.
- Añadir 1 ml de la 1 mM de potasio solución de reserva de fosfato a un tubo centrífugo de 1,5 ml y llevar a cabo siete diluciones seriadas 0,5 ml.
- Desechar el tubo primero por lo que tiene 7 diluciones que van de 20 nmol, 0,625 nmol P.
- Transferencia de 80 l de cada tubo por duplicado a las filas de B - H de una placa estándar de 96 pocillos.
- Añadir 80 l de tampón de acetato de sodio (punto 3.1) de la fila A de las columnas 11 y 12, este es el punto de calibración 0 nmol P.
- Cada columna 11 y 12 ahora contiene 8 muestras de referencia de 0 a 20 nmol nmol de fosfato inorgánico.
- En la columna 10 contendrá los siguientes controles:
- Añadir 40μL PP + solución de la enzima GP + 40 l tampón acetato de sodio (punto 3.1) a los tres primeros pozos en la columna 10.
- Añadir 40 l PP + GP + NP1 solución de la enzima de búfer + 40 l de acetato de sodio para los próximos tres pozos.
- Añadir 40 l solución de acetato de sodio con 10 nmol de glucosa-6 fosfato (C 6 H 11 Na 2 O 9 P • xH 2 O, 304,1 g / mol) + 40 l PP + solución de la enzima GP a un pozo y al final, así en la columna 10, añadir la solución de acetato de sodio en lugar de solución de enzima.
5. + Muestra la enzima de incubación
- Cada muestra se está probando que ocupan los primeros nueve pozos en una fila de una placa estándar de 96 pocillos.
- Distribución de 40 L de extractos de la muestra de pH ajustado de la Sección 2 de los pozos de 1-9 en un máximo de 8 líneas.
- Después de todas las muestras han sido distribuidos * utilizar una pipeta multicanal para distribuir PP + solución de la enzima GP de columnas 1-3, PP + GP + NP1 a las columnas 4-6 y tampón de acetato sódico (preparado en la sección 3.1) a las columnas 7-9.
* Este paso debe realizarse con rapidez para asegurar todas las muestras de obtener el tiempo de incubación equivalente. - Cubrir la placa de 96 pozos con una tapa y las muestras se incuban + soluciones enzimáticas, los controles y la curva de calibración exactamente 1 hora a 37 ° C.
6. Medición colorimétrica de Lanzamiento y P de fondo inorgánicos
- Prepare 50 ml de cada una de las siguientes soluciones en agua destilada:
Solución A *: 0,1 M de ácido ascórbico (C6H8O6, 176,12 g / mol) + ácido tricloroacético 0,5 M (Cl3, CCOOH, 163,39 g / mol)
Solución B: 0,01 M molibdato de amonio ((NH4) 2MoO4, 196,01 g / mol)
Solución C: 0,1 M de citrato de sodio (HOC (COONa) (CH2COONa) 2 2H2O, 294,10 g / mol) + 0,2 M arseniato de sodio (NaAsO2, 129,91 g / mol) + 5% de ácido acético glacial
(CH3CO2H, 60,05 g / mol) * Solución A debe prepararse diariamente. - Añadir 25 l de solución de SDS, 100 l de solución A, 20 L de la solución B y 50 l de C y la solución a todos los pozos de la pl de 96 pozoscomió. Hacer esto rápidamente con una pipeta multicanal.
- Cubrir la placa e incubar 30 minutos a temperatura ambiente.
- Medir la absorbancia a 850 nm en un micro-ajustable lector de placas.
7. Clasificación de los compuestos de P
- Importar datos en bruto en una hoja de cálculo (por ejemplo Microsoft Excel).
- Trazar la curva de calibración de fósforo inorgánico: 0 a 40 nmol P sobre el eje X y la media de las mediciones de absorbancia por duplicado en el eje.
- Realizar una regresión lineal y encontrar la ecuación de la recta de mejor ajuste.
- Columnas 1-3: se aplica directamente la curva de calibración de fondo-esto es inorgánico P.
- Columnas 4-6: Los valores medios de la muestra por triplicado y restar a los controles (P + enzima solución de fondo inorgánicos) del ingreso bruto absorción, esto es derivado de P hidrolizables monoésteres P.
- Columnas 7-9: Lo mismo que 7.5, excepto los valores de absorbancia resta de las columnas 4-6 - esto es P desde hidrolizables diésteres P.
- Convertir los datos de absorbancia en nmol P liberado mediante la aplicación de la ecuación de calibración.
- nmol P liberado puede relacionarse a mg P / kg de suelo original. Por otra parte, la evaluación de las proporciones de cada clase de P también puede ser un enfoque útil para el análisis de datos.
8. Los resultados representativos:
Una rápida inspección visual de la placa de 96 pozos después de la química colorimétrica ofrecerá pistas sobre si el procedimiento se realizó correctamente. La primera cosa a comprobar es el nivel de líquido en cada pozo de exploración del perfil lateral de la placa. No debe ser exactamente 275 l de reactivos en todos los pozos. A continuación, inspeccione visualmente el color de los pozos de la muestra por triplicado y duplicado los pozos de calibración. Estas técnicas se debe repetir el mismo tono de azul. A continuación, aplicar la curva de calibración de los dos pozos que contienen glucosa-6-fosfato y verificar que todos los liberados nmol 10 de inorgánicos P. Después de P total extraído se ha medido mediante ICP-OES o un método alternativo, asegúrese de que el P total de los valores calculados utilizando este protocolo no superen la cantidad de P que se extrajo.
Nota: una cuidadosa gestión de los datos en la hoja de cálculo le ayudará a evitar errores cuantitativos. Usted tendrá que lidiar con un montón de números a la vez, creando así una plantilla será tiempo bien invertido.
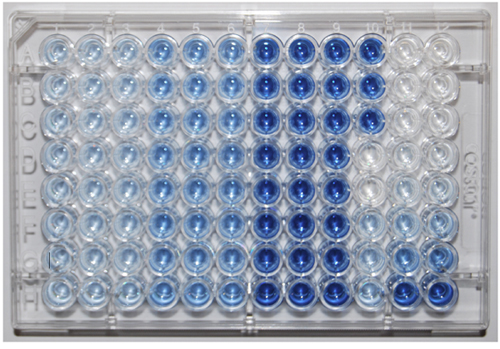
Figura 1. Una placa de 96 pozos que muestra los resultados de 8 muestras (filas AH) y una curva de calibración (columnas 11 y 12). Los controles están en la columna 10. Aumentar la intensidad de color entre las columnas 1-3 y 4-6 se debe a los compuestos hidrolizados monoéster P, entre las columnas 4-6 y 7-9 se debe a los compuestos hidrolizados diéster P.
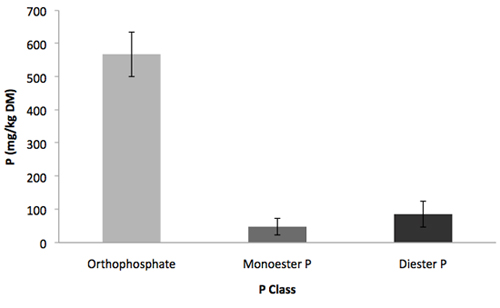
Figura 2. Distribución de las clases de P en un 0,25 M de NaOH 0,05 M de EDTA de extraer una muestra de suelo Vermont con alto rendimiento de la hidrólisis enzimática. Las barras de error indican la desviación estándar, n = 3.
Discusión
Por su propia naturaleza, un método rápido para el uso de volúmenes pequeños requiere mucho cuidado. Por lo tanto, los pasos más importantes son los relacionados con las soluciones de pipeteo en el plato. Precisa, y lo más importante, la técnica consistente pipeta son esenciales para el éxito de este ensayo.
La extracción de NaOH-EDTA permitirá que la mayoría de la P en muchas muestras que se caracteriza en tres clases: ortofosfato, P monoéster y diéster P. Los suelos, los abonos, los sedimentos o cualquier otra muestra del medio ambiente que contiene NaOH-EDTA-P extraíble se puede caracterizar . Formas de P en muestras ambientales no son necesariamente estables y esta técnica se asegurará de muestras se caracterizan antes de las muestras están en peligro sin necesidad de emplear un ejército de investigadores.
Este análisis es especialmente útil cuando un gran número de muestras se van a procesar. Las necesidades de reactivos y las necesidades de espacio se han reducido a un nivel manejable (por ejemplo, 1,5 mL tubos de microcentrífuga en lugar de 50 ml frascos de vidrio). Esta adaptación también limita la producción de residuos.
Divulgaciones
Agradecimientos
Damos las gracias al USGS y de los Recursos de Agua y Vermont Lake Centro de Estudios para proporcionar financiación.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | |
|---|---|---|---|
| NaOH | Sigma-Aldrich | S8045 | |
| EDTA | Sigma-Aldrich | EDS | |
| Ácido acético glacial | Sigma-Aldrich | 242853 | |
| Acetato de sodio | Sigma-Aldrich | S2889 | |
| Trigo fosfatasa ácida | Sigma-Aldrich | P3627 | |
| Papa fosfatasa ácida | Sigma-Aldrich | P1146 | |
| Nucleasa P1 | Sigma-Aldrich | N8630 | |
| Fosfato de Potasio | Sigma-Aldrich | P2222 | |
| Sigma-Aldrich | |||
| Sigma-Aldrich | |||
| La glucosa-6-fosfato | Sigma-Aldrich | G7250 | |
| SDS | Sigma-Aldrich | L4390 | |
| Ácido Ascórbico | Sigma-Aldrich | A5960 | |
| TCA | Sigma-Aldrich | T9159 | |
| Molibdato de amonio | Sigma-Aldrich | A1343 | |
| Citrato de sodio | Sigma-Aldrich | S1804 | |
| Arseniato de sodio | Sigma-Aldrich | S9663 |
Referencias
- Turner, B. L., Frossard, E., Baldwin, D. S. . Organic phosphorus in the environment. , (2005).
- Murphy, J., Riley, J. P. A modified single solution method for determination of phosphate in natural waters. Anal. Chim. Acta. 27, 31-36 (1962).
- Dick, W. A., Tabatabai, M. A. Determination of orthophosphate in aqueous solutions containing labile organic and inorganic phosphorus compounds. J. Environ. Qual. 6, 82-85 (1977).
- He, Z., Toor, G. S., Honeycutt, C. W., Sims, J. T. An enzymatic hydrolysis approach for characterizing labile phosphorus forms in dairy manure under mild assay conditions. Bioresour. Technol. 97, 1660-1668 (2006).
- He, Z., Honeycutt, C. W. A modified molybdenum blue method for orthophosphate determination suitable for investigating enzymatic hydrolysis of organic phosphates. Commun. Soil Sci. Plant Anal. 36, 1373-1383 (2005).
- Cade-Menun, B. J. Characterizing phosphorus in environmental and agricultural samples by 31P nuclear magnetic resonance spectroscopy. Talanta. 66, 359-371 (2005).
- Johnson, N. R., Hill, J. E. Phosphorus species composition of poultry manure-amended soil using high-throughput enzymatic hydrolysis. Soil Sci. Soc. Am. J. 74, 1786-1791 (2010).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados