Method Article
High-Throughput mesure et de classification de P organique dans les échantillons environnementaux
Dans cet article
Résumé
Ce protocole décrit une méthode à haut débit de l'hydrolyse enzymatique qui utilise un lecteur de microplaques pour mesurer et classifier phosphore dans le sol que les monoesters P, P diesters et inorganiques P. Jusqu'à 96 échantillons peuvent être mesurés en une seule fois dans un laboratoire standard.
Résumé
De nombreux types de composés organiques du phosphore (P) de molécules existent dans des échantillons de l'environnement 1. Traditionnelle mesures P ne détecte pas ces composés organiques P, car ils ne réagissent pas avec les réactifs colorimétriques 2,3. L'hydrolyse enzymatique (EH) est une nouvelle méthode pour caractériser avec précision les formes organiques P dans les échantillons environnementaux 4,5. Cette méthode est seulement dans la précision forgées par le phosphore-31 spectroscopie par résonance magnétique nucléaire (31 P-RMN), une méthode qui est coûteux et nécessite spécialisés training6 technique. Nous avons adapté une méthode de l'hydrolyse enzymatique capable de mesurer des trois classes de phosphore (P monoester, diester et P P inorganique) à un système de lecteur de microplaques 7. Cette méthode fournit aux chercheurs un moyen rapide, précis, abordable et convivial pour mesurer les espèces P dans les sols, les sédiments, les engrais et, si elle est concentrée, les échantillons aquatiques. C'est la seule méthode à haut débit permettant de mesurer les formes et les enzymes labilité du P organique qui peut être effectuée dans un laboratoire standard. Les données résultant donne un aperçu de scientifiques qui étudient le contenu du système d'éléments nutritifs et le potentiel d'eutrophisation.
Protocole
1. Extraction du phosphore
- Préparer une solution 1L de 0,25 M d'hydroxyde de sodium (NaOH, 40,00 g / mol) + 0,05 M acide éthylènediaminetétraacétique (EDTA, 292,24 g / mol).
- Ajouter 30 ml de la solution de NaOH + EDTA à 2 g de sol humide ou sec / échantillon dans un tube conique de 50 ml.
- Incuber sous agitation pendant 16 h à température ambiante.
- Centrifugeuse 3000 xg pendant 3 minutes.
2. Ajustement du pH de l'échantillon Extrait
- Transférer une partie aliquote de 0,1 mL à 1,5 mL une micro-centrifugeuse tube.
- Ajouter 0,017 ml de 2,5 M d'acide acétique, 0,144 ml de tampon acétate 0,4 M (70,5% d'acétate de sodium [CH 3 COONa, 82,03 g / mol] et 29,5% d'acide acétique, pH 5,0), et 0,739 ml d'eau déminéralisée.
- Le volume final de l'extrait sera ajusté de 1 mL et le pH final sera 5,0.
3. Préparation de la solution enzymatique Stock
- Préparer 1 L d'acétate de sodium 0,1 M (CH 3 COONa, 82,03 g / mol) en solution, pH 5,0.
- Préparer 2 x 10 ml des solutions d'acide phosphatase stock dans le tampon acétate de sodium préparée à l'étape 3.1 de telle sorte que les concentrations finales sont chacun 0,5 unités / ml.
Phosphatase acide de type I de Triticum aestivum (blé germe; GP, généralement de 0,5 mg U-1 solide, EC 3.1.3.2)
Phosphatase acide de type IV-S de Solanum tuberosum (pomme de terre; PP, généralement 4,6 mg U-1 solide, EC 3.1.3.2)
* Les unités d'activité sont spécifiés par le fournisseur lorsque une unité est définie comme la libération de 1 micromole de l'orthophosphate de la solution par heure à 37 ° C. - Reconstituer lyophilisé nucléase P1 (EC 3.1.30.1) de Penicillium citrinum (champignons; NP1, généralement 500 mg U -1 solide) dans un ml de l'eau déminéralisée, ce qui peut désormais être conservés à 4 ° C pour une utilisation future.
- Pipeter NP1 dans l'un des tubes de 10 ml préparée à l'étape 3.2 telles que la concentration finale est de 2,5 unités / ml NP1; mélanger délicatement en retournant plusieurs fois.
- Centrifuger les deux 10 ml solutions enzymatiques 3000 xg pendant 30 minutes.
4. Courbe d'étalonnage P et contrôles
- Préparer 1 L de phosphate de potassium 1 mM (K2HPO4, 174,18 g / mol) solution stock.
- Ajouter 1 mL de la 1 mM de phosphate de potassium de la solution mère dans un tube à centrifuger de 1,5 ml et 0,5 ml accomplisse sept dilutions successives.
- Jeter le tube d'abord si vous disposez de 7 dilutions allant de 20 nmol-0.625 nmol P.
- Transfert 80 ul de chaque tube en double exemplaire aux lignes B - H d'une plaque standard 96 puits.
- Ajouter 80 ul de tampon acétate de sodium (point 3.1) à la ligne A de colonnes 11 et 12, tel est le point 0 nmol calibration P.
- Chaque colonne 11 et 12 contient maintenant 8 échantillons de référence de 0 à 20 nmol phosphate inorganique nmol.
- Colonne 10 contient les contrôles suivants:
- Ajouter 40μL PP + solution enzymatique GP + 40 ul de tampon acétate de sodium (section 3.1) pour les trois premiers puits dans la colonne 10.
- Ajouter 40 uL PP + GP + solution enzymatique NP1 + 40 ul de tampon acétate de sodium pour les trois prochaines puits.
- Ajouter 40 uL solution d'acétate de sodium contenant 10 glucose-6 phosphate nmol (C 6 H 11 Na 2 O 9 P • xH 2 O, 304,1 g / mol) + 40 uL PP + solution enzymatique GP d'un puits et au bien-finales dans la colonne 10 une solution d'acétate de sodium au lieu d'ajouter la solution d'enzyme.
5. Échantillon + enzyme incubation
- Chaque échantillon testé occuperont les 9 premiers puits dans une rangée d'une plaque standard 96 puits.
- Distribuer 40 ul d'extraits d'échantillons à pH ajusté à la section 2 aux puits 1-9 sur jusqu'à 8 lignes.
- Après tous les échantillons ont été distribués * utiliser une pipette multicanaux pour distribuer PP + solution enzymatique GP à colonnes 1-3, PP + GP + NP1 aux colonnes 4-6 et un tampon d'acétate de sodium (préparée à la section 3.1) dans les colonnes 7-9.
* Cette étape doit être effectuée rapidement afin d'assurer tous les échantillons obtenir du temps d'incubation équivalent. - Recouvrir la plaque de 96 puits avec un couvercle et incuber des échantillons + solutions enzymatiques, les contrôles et courbe d'étalonnage exactement 1 heure à 37 ° C.
6. Mesure colorimétrique de Sortie et P Contexte inorganiques
- Préparer 50 ml de chacune des solutions suivantes dans l'eau déminéralisée:
Solution A *: 0,1 M d'acide ascorbique (C6H8O6, 176,12 g / mol) + 0,5 M d'acide trichloracétique (CI3CCOOH, 163,39 g / mol)
Solution B: 0,01 M molybdate d'ammonium ((NH4) 2MoO4, 196,01 g / mol)
Solution C: 0,1 M citrate de sodium (HOC (COONa) (CH2COONa) 2 2H2O, 294,10 g / mol) + 0,2 M arséniate de sodium (NaAsO2, 129,91 g / mol) + 5% d'acide acétique glacial
(CH3CO2H, 60,05 g / mol) * Solution A doit être préparée chaque jour. - Ajouter 25 ul d'une solution de SDS, 100 pi de solution A, 20 ul de la solution B et 50 pi et de la solution C à tous les puits dans la pl de 96 puitsmangé. Pour ce faire, rapidement avec une pipette multicanaux.
- Couvrir la plaque et laisser incuber 30 minutes à température ambiante.
- Mesurer l'absorbance à 850 nm dans toute accordable micro-lecteur de plaques.
7. Classification des composés P
- Importer des données brutes dans un tableur (par exemple Microsoft Excel).
- Tracer la courbe d'étalonnage de phosphore inorganique: 0 à 40 nmol P sur l'axe des x et la moyenne des mesures d'absorbance en double sur l'axe des y.
- Effectuer une régression linéaire et de trouver l'équation de la droite de meilleur ajustement.
- Colonnes 1-3: appliquer directement la courbe d'étalonnage-ce sont les antécédents inorganiques P.
- Colonnes 4-6: Les valeurs moyennes de l'échantillon en triple et soustraire des contrôles (solution enzymatique + P inorganique de fond) de l'absorbance brute-ce n'est dérivée de P P monoesters hydrolysables.
- Colonnes 7-9: Même chose que 7,5 exception des valeurs d'absorbance soustraire colonnes 4-6 - c'est à partir de diesters P P hydrolysables.
- Convertir les données d'absorbance à nmol P libéré en appliquant l'équation d'étalonnage.
- nmol P libérée peut être liée au retour mg P / kg de sol d'origine. Sinon, l'évaluation des proportions de chaque classe P peut aussi être une approche utile pour l'analyse des données.
8. Les résultats représentatifs:
Une inspection visuelle rapide de la plaque de 96 puits, après la chimie colorimétrique offrira des indices pour savoir si la procédure a été effectuée correctement. La première chose à vérifier est le niveau de liquide dans chaque puits en scannant le profil latéral de la plaque. Il doit être exactement 275 uL de réactifs dans tous les puits. Ensuite, inspecter visuellement la couleur du puits d'échantillon triple et double puits d'étalonnage. Ces techniques devraient être de reproduire la même nuance de bleu. Ensuite appliquer la courbe de calibration pour les deux puits contenant du glucose-6-phosphate et de vérifier, ils sortent tous les 10 nmol de P. Après inorganiques P extrait total a été mesurée en utilisant l'ICP-OES ou une autre méthode, assurez-vous que le P total des valeurs calculées à l'aide de cette protocole de ne pas dépasser la quantité de P qui a été extrait.
Remarque: Attention gestion des données dans le tableur de se prémunir contre des erreurs quantitatives. Vous devrez traiter avec beaucoup de numéros à la fois, afin de créer un modèle sera du temps bien investi.
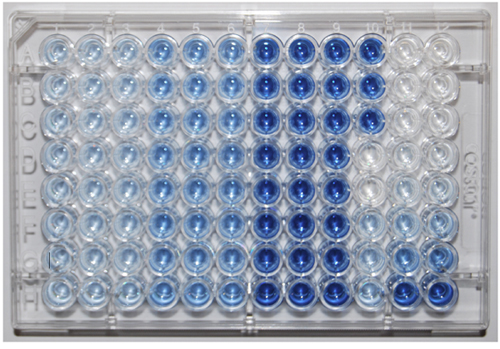
Figure 1. Une plaque de 96 puits montrant les résultats de 8 échantillons (lignes AH) et une courbe de calibration (colonnes 11 et 12). Les contrôles sont dans la colonne 10. Augmentation de l'intensité des couleurs entre les colonnes 1-3 et 4-6 est due à des composés hydrolysés monoester P, entre les colonnes 4-6 et 7-9 est due à des composés hydrolysés P diester.
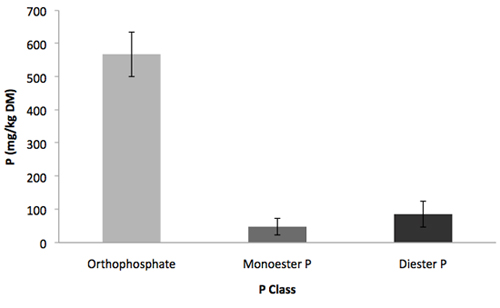
Figure 2. Répartition des classes de P dans un 0,25 M de NaOH 0,05 M d'EDTA extraction d'un échantillon de sol à l'aide du Vermont à haut débit hydrolyse enzymatique. Les barres d'erreur indiquent l'écart type, n = 3.
Discussion
Par sa nature même, une méthode rapide utilisant de petits volumes requiert le plus grand soin. Par conséquent, les étapes les plus critiques sont ceux qui impliquent des solutions de pipetage sur la plaque. Précis, et surtout, la technique de la pipette cohérents sont essentiels pour la réussite de ce test.
L'extraction NaOH-EDTA permettra la plupart du P dans de nombreux échantillons à être caractérisé en trois classes: orthophosphate, monoester et de diester P P. Sols, les engrais, les sédiments ou tout autre échantillon de l'environnement qui contient du NaOH-EDTA-extractibles P peut être caractérisée . Formes de P dans les échantillons environnementaux ne sont pas forcément stables et cette technique va s'assurer que les échantillons sont caractérisés avant que les échantillons sont compromis sans avoir besoin d'employer une armée de chercheurs.
Ce test est particulièrement adapté quand un grand nombre d'échantillons doivent être traitées. Les besoins de réactifs et d'espace ont été revues à la baisse à un niveau gérable (par exemple 1,5 ml microtubes plutôt que 50 flacons en verre ml). Cette adaptation limite également la production de déchets.
Déclarations de divulgation
Remerciements
Nous remercions l'USGS et le Vermont, Ressources en eau et d'études Lac Centre de fournir un financement.
matériels
| Name | Company | Catalog Number | Comments |
| Nom du réactif | Société | Numéro de catalogue | |
|---|---|---|---|
| NaOH | Sigma-Aldrich | S8045 | |
| EDTA | Sigma-Aldrich | EDS | |
| Acide acétique glacial | Sigma-Aldrich | 242853 | |
| Acétate de sodium | Sigma-Aldrich | S2889 | |
| Phosphatase acide blé | Sigma-Aldrich | P3627 | |
| Phosphatase acide de pommes de terre | Sigma-Aldrich | P1146 | |
| Nucléase P1 | Sigma-Aldrich | N8630 | |
| Phosphate de Potassium | Sigma-Aldrich | P2222 | |
| Sigma-Aldrich | |||
| Sigma-Aldrich | |||
| Glucose-6-phosphate | Sigma-Aldrich | G7250 | |
| SDS | Sigma-Aldrich | L4390 | |
| Acide ascorbique | Sigma-Aldrich | A5960 | |
| TCA | Sigma-Aldrich | T9159 | |
| Molybdate d'ammonium | Sigma-Aldrich | A1343 | |
| Citrate de sodium | Sigma-Aldrich | S1804 | |
| Arséniate de sodium | Sigma-Aldrich | S9663 |
Références
- Turner, B. L., Frossard, E., Baldwin, D. S. . Organic phosphorus in the environment. , (2005).
- Murphy, J., Riley, J. P. A modified single solution method for determination of phosphate in natural waters. Anal. Chim. Acta. 27, 31-36 (1962).
- Dick, W. A., Tabatabai, M. A. Determination of orthophosphate in aqueous solutions containing labile organic and inorganic phosphorus compounds. J. Environ. Qual. 6, 82-85 (1977).
- He, Z., Toor, G. S., Honeycutt, C. W., Sims, J. T. An enzymatic hydrolysis approach for characterizing labile phosphorus forms in dairy manure under mild assay conditions. Bioresour. Technol. 97, 1660-1668 (2006).
- He, Z., Honeycutt, C. W. A modified molybdenum blue method for orthophosphate determination suitable for investigating enzymatic hydrolysis of organic phosphates. Commun. Soil Sci. Plant Anal. 36, 1373-1383 (2005).
- Cade-Menun, B. J. Characterizing phosphorus in environmental and agricultural samples by 31P nuclear magnetic resonance spectroscopy. Talanta. 66, 359-371 (2005).
- Johnson, N. R., Hill, J. E. Phosphorus species composition of poultry manure-amended soil using high-throughput enzymatic hydrolysis. Soil Sci. Soc. Am. J. 74, 1786-1791 (2010).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon