Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
El análisis cuantitativo de todos Influenza Tipo A Hemaglutininas viral y neuraminidasas el uso de anticuerpos Universal en simples ensayos Slot Blot
* Estos autores han contribuido por igual
En este artículo
Erratum Notice
Resumen
Un método sencillo slot blot fue desarrollado para la cuantificación de la hemaglutinina y la neuraminidasa viral de la gripe utilizando anticuerpos universales dirigidas a sus secuencias más conservadas identificados a través de análisis de la bioinformática. Este enfoque innovador puede ofrecer una alternativa útil para la determinación cuantitativa de todos los hemaglutinina y la neuraminidasa viral.
Resumen
Hemaglutinina (HA) y neuraminidasa (NA) son dos proteínas de superficie de los virus de influenza que se sabe que juegan un papel importante en el ciclo de vida viral y la inducción de respuestas inmunes protectoras 1,2. Como el principal objetivo de los anticuerpos neutralizantes, HA se utiliza actualmente como el marcador de potencia de la vacuna de la gripe y se mide por inmunodifusión radial simple (SRID) 3. Sin embargo, la dependencia del SRID de la disponibilidad de los antisueros correspondientes subtipos específicos de las causas de un mínimo de 2-3 meses de retraso para la liberación de todas las nuevas vacunas. Por otra parte, a pesar de la evidencia de que NA también induce inmunidad protectora 4, la cantidad de NA en vacunas de la gripe aún no está estandarizado debido a la falta de reactivos adecuados o métodos de análisis 5. Por lo tanto, simples métodos alternativos capaces de cuantificar los antígenos HA y NA son deseables para una liberación rápida y un mejor control de calidad de vacunas contra la influenza.
Regiones universalmente conservadas en todos los de la gripe A disposición de HA y NA secuencias fueron identificados por análisis de la bioinformática 6-7. Una secuencia (designado como Uni-1) fue identificado en el epítopo sólo universalmente conservadas de la HA, el péptido de fusión 6, mientras que dos secuencias conservadas fueron identificados en neuraminidasa, una cerca del sitio activo enzimático (designado como HCA-2) y el otra cerca de la N-terminal (designado como HCA-3) 7. Péptidos con estas secuencias de aminoácidos fueron sintetizados y utilizados para inmunizar a los conejos para la producción de anticuerpos. El anticuerpo contra el epítopo Uni-1 de HA fue capaz de obligar a 13 subtipos de influenza A-HA (H1-H13), mientras que los anticuerpos contra el HCA-2 y HCA-3 regiones de NA fueron capaces de unirse a los 9 subtipos de NA. Todos los anticuerpos mostraron especificidad notable contra las secuencias virales como lo demuestra la observación de que sin reactividad cruzada con las proteínas alantoideo fue detectado. Estos anticuerpos universales fueron utilizados para desarrollar los ensayos de slot blot para cuantificar la HA y NA de la gripe A vacunas sin la necesidad de antisueros específicos 7,8. Muestras de la vacuna se aplica en una membrana de PVDF utilizando un aparato de slot blot, junto con las normas de referencia diluido a diferentes concentraciones. Para la detección de HA, muestra y el patrón se diluye primero en Tris-buffer salino (TBS), que contiene urea 4M, mientras que para la medición de NA que se diluyeron en TBS que contiene 0,01% Zwittergent ya que estas condiciones mejora significativamente la sensibilidad de detección. Tras la detección de los antígenos HA y NA por inmunotransferencia con sus respectivos anticuerpos universales, la intensidad de señal se cuantificaron por densitometría. Las cantidades de HA y NA de las vacunas fueron calculados utilizando una curva estándar establecida con la intensidad de la señal de las distintas concentraciones de las referencias utilizadas.
Dado que estos anticuerpos se unen a epítopos universal en HA o NA, los investigadores interesados puedan utilizarlos como herramientas de investigación en los inmunoensayos que no sea el slot blot solamente.
Protocolo
1. Preparación de los reactivos y equipos
- Antes de iniciar el procedimiento de slot blot, preparar 20_mls de solución de urea 4M en Tris-buffer salino (20 mM Tris, 137 mM NaCl, pH 7,6) (TBS) para la hemaglutinina o HA, slot blot, o 20_mls de un 0,01% Zwittergent solución de TBS de la neuraminidasa, o NA, slot blot. Mientras que la urea 4M debe estar preparado fresco todo el tiempo, una solución al 10% de acciones Zwittergent en dH 2 O es estable durante al menos 6 meses a temperatura ambiente y por lo tanto puede ser diluido al 0,01% en TBS antes de cada ensayo.
- Preparar 2000 ml de tampón de lavado mediante la adición de Tween-20 a una solución de TBS a una concentración final de 0,1%. Prepare 80 ml de tampón de bloqueo mediante la disolución de leche desnatada en polvo (secante grado sin grasa leche en polvo) a una concentración final de 5% w / v en tampón de lavado.
- Activar la membrana de PVDF (pre-cortado a un tamaño de 9 x 12 cm) en metanol durante 15 segundos, seguido de un enjuague en 2 minutos ddH 2 O. Remoje la membrana en TBS hasta su uso. Humedecer previamente 3 hojas de Bio-Dot SF papel de filtro en TBS hasta su uso.
2. Preparación de muestras de vacuna contra la influenza y el estándar de referencia para HA slot blot
Influenza normas para la vacuna con contenido de HA predeterminadas que corresponden a las cepas de vacuna que se prueba se obtuvieron del Centro de Evaluación e Investigación Biológica (CBER / FDA, EE.UU.) o el Instituto Nacional de Estándar Biológica y Control (NIBSC, Reino Unido) y se utilizan para la cuantificación de HA de slot blot. Los investigadores también pueden preparar sus propias normas de antígeno utilizando los procedimientos establecidos como se describe en las referencias 9 y 10.
- De antígenos de referencia de HA y examinar muestras de la vacuna: Diluir el antígeno de referencia HA acciones de la urea 4M / TBS a las siguientes concentraciones: 0, 0,0938, 0,1875, 0,375, 0,75, 1,5, 3 y 6 HA mg / ml. Mezclar bien. Entonces, diluir las muestras de ensayo de vacunas para uso humano obtenido de los productores de vacunas o de fabricación propia para fines de investigación científica en urea 4M / TBS y mezclar bien. Mientras que los duplicados de los antígenos de referencia y muestras de la vacuna se puede ejecutar, por triplicado son las preferidas. Prepare tres diluciones de cada muestra (2 veces la diferencia) para permitir que la concentración de la muestra que caen dentro de la curva estándar. Preparar 450 l l o 650 de cada antígeno de referencia o la vacuna de prueba dilución de la muestra para ejecutar duplicados o triplicados, respectivamente. Monovalente contra la influenza A las vacunas se pueden probar con este método slot blot. El contenido de los antígenos HA de referencia se determinó previamente mediante SRID que es la prueba estándar utilizada actualmente para la preparación de vacunas de la gripe. El contenido de HA determinado por SRID se utilizó como referencia la concentración de antígeno HA acciones iniciales para la preparación de las diluciones de la curva de slot blot estándar.
3. Preparación de muestras de vacuna contra la influenza y el estándar de referencia para NA slot blot
Influenza normas para la vacuna correspondiente a las cepas de vacuna que se prueba se obtuvieron del Centro de Evaluación e Investigación Biológica (CBER / FDA, EE.UU.) o el Instituto Nacional de Estándar Biológica y Control (NIBSC, Reino Unido) y se utilizan para la cuantificación de NA por transferencia de la ranura. El contenido de NA de estas muestras de referencia se determinó mediante análisis SDS-PAGE de las muestras deglicosilada junto con el análisis de densitometría de exploración, como se describió anteriormente 9, con ligeras modificaciones 10. En resumen, las muestras de la vacuna deglicosilada de referencia (5 mg) se mezclaron con tampón de muestra y se cargaron en el gel. El gel se ha ejecutado a 20 mA durante aproximadamente 90 minutos hasta que el colorante de seguimiento acaba de quedarse sin el gel, seguido de la tinción Sypro. Cuantificación de la densitometría de las proteínas se llevó a cabo mediante un sistema de documentación FluorChem gel (Alpha Innotech). La cantidad de NA se determinó sobre la base de la relación de las proteínas de NA a las proteínas totales según lo determinado por el ensayo de Lowry. Las muestras de referencia preparadas con este método se puede utilizar en slot blot para la cuantificación del contenido de NA en las muestras de vacuna a partir de los fabricantes de vacunas.
- De antígenos de referencia NA y examinar muestras de la vacuna: Diluir la referencia NA acciones antígeno en 0,01% Zwittergent / TBS a las siguientes concentraciones: 0, 0,039, 0,078, 0,1562, 0,3125, 0,625, 1,25, 2,5, 5 y 10 mg NA / ml. Mezclar bien. Entonces, diluir las muestras de ensayo de vacunas para uso humano obtenido de los productores de vacunas o de fabricación propia para fines de investigación científica en el 0,01% Zwittergent / TBS y mezclar bien. Mientras que los duplicados de los antígenos de referencia y muestras de la vacuna se puede ejecutar, por triplicado son las preferidas. Prepare tres diluciones de cada muestra (2 veces la diferencia) para permitir que la concentración de la muestra que caen dentro de la curva estándar. Preparar 450 l l o 650 de cada antígeno de referencia o la vacuna de prueba dilución de la muestra para ejecutar duplicados o triplicados, respectivamente. Monovalente contra la influenza A las vacunas se pueden probar el ingenioh este método slot blot.
4. Asamblea del aparato de microfiltración Bio-Dot SF y secante de las muestras sobre la membrana de PVDF
- Montar una previamente limpia y seca Bio-Dot aparato de microfiltración SF. Coloque la placa de apoyo de la junta en el colector de vacío y lugar de la junta de estanqueidad en los 3 top.Place humedecido hojas de Bio-Dot SF papel de filtro sobre la junta, seguido por la membrana pre-empapado PVDF. Coloque la plantilla de la muestra en la parte superior de la membrana y apriete con los dedos los cuatro tornillos con un patrón diagonal cruzando a garantizar la aplicación uniforme de la presión en la superficie de la membrana.
- Verifique que la válvula de 3 vías se establece para exponer el colector de vacío a la fuente de vacío, sólo antes de encender la bomba y la conexión del vacío.
- Encienda la bomba y conectar con el aparato Bio-Dot. Asegúrese de que la válvula reguladora de caudal se sitúa en un nivel por debajo de los pozos de la muestra para un drenaje rápido y adecuado de las muestras en los siguientes pasos.
- Repita el paso tornillo de apriete utilizando el patrón diagonal que atraviesa. Apretar los tornillos mientras se aplica el vacío asegura un sellado más hermético y evita la contaminación cruzada entre los pozos.
- Cambiar la válvula de flujo para exponer el colector de vacío de aire y apagar la bomba.
- Aplicar 100 l de TBS a todos los pocillos utilizando una pipeta multicanal para rehidratar la membrana asegurando unión uniforme del antígeno. Se debe tener cuidado para evitar la formación de burbujas y para aplicar la solución en la mitad del pozo, ya que cerca del fondo como sea posible, a fin de cubrir la ranura de manera uniforme. Ráfaga de cualquier burbuja de aire introducido accidentalmente con una punta de pipeta.
- Cambiar la válvula de flujo para exponer el colector al aire y al vacío, gire a la bomba, y suavemente drenar el buffer de los pozos, poniendo un dedo sobre el puerto se expone al aire para regular la cantidad de vacío.
- Cambiar la válvula de flujo para exponer el colector al aire tan pronto como el buffer se ha drenado completamente de todos los pozos. Apague la bomba o desconectar el vacío.
- Aplicar 200 l de cada dilución de la muestra estándar o bien por la vacuna. Muestras de una pipeta a la vez, en el centro de cada uno, así como cerca del fondo como sea posible, teniendo cuidado de no introducir burbujas de aire. Ráfaga de cualquier burbuja de aire introducido accidentalmente con una punta de pipeta. Poner 200 ul de buffer de dilución de la muestra (4 millones de urea / TBS o 0,01% Zwittergent / TBS) en los pozos utilizados para asegurar vacío adecuado a los pozos en uso.
- Ajustar la válvula de flujo para exponer el colector al aire y el vacío. Encienda la bomba (o vuelva a conectar el vacío) y permitir que las muestras suavemente para drenar por completo de los pozos mediante el control de la cantidad de vacío con un dedo a través del puerto se expone al aire. Quitar el dedo del puerto para liberar el vacío tan pronto como todas las muestras se han agotado.
- Inmediatamente añadir 200 l de TBS a cada pocillo utilizando una pipeta multicanal. Aplicar una succión suave para drenar y lavar los pocillos mediante el control de la cantidad de vacío con un dedo a través del puerto se expone al aire.
- Repita el paso de lavado descrito en el paso 4.11. Tan pronto como los pozos se han agotado por completo, aflojar los tornillos de la plantilla de la muestra y apagar el vacío para evitar el secado excesivo de los pozos. Proceder de inmediato a eliminar la membrana.
- Colocar la membrana en tampón de bloqueo y se incuba durante la noche a 4 ° C, con suave balanceo. Use suficiente tampón de bloqueo para cubrir completamente la membrana.
5. Inmunotransferencia de antígenos HA y NA
- Después de la incubación durante la noche en tampón de bloqueo, lavar la membrana dos veces durante 5 minutos con TBS/0.1% Tween-20 tampón de lavado. Para todos los lavados e incubaciones, garantizar la membrana está completamente cubierto con la solución.
- Incubar la membrana con un anticuerpo de conejo universal contra la HA (como Uni-1) o NA (como HCA-2 o HCA-3) diluido en un 5% w / v BSA en tampón de lavado durante una hora a temperatura ambiente, con suaves mecedora. Las concentraciones óptimas de anticuerpos necesario que se determine para cada acción de anticuerpos. Diluciones de 1:4000 de conejo anti-suero dio resultados óptimos para los anticuerpos antes mencionados.
- Lavar la membrana tres veces, a temperatura ambiente con suave balanceo de 15 minutos cada vez, para eliminar cualquier anticuerpos no unidos primaria.
- Incubar la membrana con un HRP-conjugado anti-conejo secundaria de anticuerpos. Use una dilución 1:50000 de la Cabra Thermo ImmunoPure IgG anti-conejo, el anticuerpo conjugado con peroxidasa en tampón de bloqueo e incubar a temperatura ambiente durante 30 minutos con el suave balanceo.
- Lavar la membrana tres veces, tu ritmo durante 15 minutos cada vez, a temperatura ambiente con tampón de lavado para eliminar los anticuerpos no unidos secundaria.
- Lavar la membrana con TBS durante 5 minutos con balanceo suave para eliminar los restos de detergente Tween-20 de la superficie de la membrana.
- Prepare la superficie con 3 ml de cada reagent de la Supersignal kit West Dura ampliada Duración Substrato de Thermo Scientific y mezclar bien.
- Colocar la lámina sobre un pañuelo de papel seco para eliminar suavemente el exceso de tampón TBS.
- La transferencia de la membrana de un recipiente seco y añadir el sustrato para cubrir toda la membrana. Incubar 5 minutos con el suave balanceo, a temperatura ambiente.
- Retire el exceso de sustrato con cuidado secante de la membrana sobre un papel absorbente.
- Exponer la membrana a una película de quimioluminiscencia. La duración de la exposición tendrá que ser optimizado para evitar la saturación de la señal, pero por lo general van desde 10 segundos a 10 minutos.
- Realizar análisis de densitometría en la película desarrollada usando un aparato de imágenes de gel, como el sistema de documentación FluorChem gel (Alpha Innotech) siguiendo las instrucciones del fabricante. Los valores de densidad para cada conjunto de réplicas de antígenos de referencia y las muestras de prueba de la vacuna se promedian. Si bien las normas de antígenos y muestras de la vacuna se puede ejecutar en los duplicados, triplicados son las preferidas. Los valores de densidad de las réplicas deben ser muy similares. Diferencias significativas entre las réplicas indicar un problema probable técnica durante el procedimiento. Una curva estándar dependiente de la concentración se establece mediante el trazado de los valores de densidad promedio en comparación con la cantidad (en ng) de HA o antígeno NA poner en cada ranura, de la norma de referencia. El uso apropiado adecuada curva de calibración en los inmunoensayos es fundamental para la cuantificación de HA y NA con precisión. Regresión lineal, que se obtiene mediante el trazado de la respuesta (y) frente a la concentración (x) utilizando la parte lineal de la curva de respuesta (y = mx + b) es el método más simple para la cuantificación de los analitos. Si una gama más amplia de los analitos se considera para el cálculo de la concentración, la logística de cuatro parámetros (4PL) modelo actualmente aceptado para los inmunoensayos se debe utilizar. Una gran variedad de software está disponible para los investigadores interesados a considerar. En el caso del ensayo de slot blot descrito, la conversión de los valores del eje X a escala logarítmica permite la curva para adaptarse a un modelo de 4-PL y el uso de una pendiente variable regresión no lineal para el cálculo de las cantidades borrado de HA y NA en las muestras de la vacuna en cuestión es por tanto posible. Por lo tanto, habitualmente utilizan este modelo para nuestro análisis. Como las muestras de la vacuna de prueba se diluyeron en cualquiera de urea 4M / TBS o 0,01% Zwittergent / TBS antes de ser borrado en la membrana, el factor de dilución para cada muestra se debe tener en cuenta para determinar la HA y NA contenido de la prueba original muestras de la vacuna. Se sugiere que cada muestra de la vacuna de prueba se ejecutará en tres diferentes diluciones (2 veces de diferencia) con el fin de un conjunto de valores de densidad de caer dentro de la curva estándar. Los valores de densidad más alta que el rango de la curva estándar para todas las diluciones a prueba de las muestras de la vacuna debe ser diluida para HA o cuantificación exacta de NA. Si los valores de densidad por debajo del extremo inferior de la curva, las muestras de ensayo deben ser diluidas en un factor de dilución inferior.
6. Los resultados representativos:
Los análisis bioinformáticos de todos los de la gripe A disponibles secuencias HA confirmó la N-terminal de la subunidad HA2 (el péptido de fusión) como la única región conservada de la HA. La figura 1 muestra la tasa de conservación para cada posición de aminoácidos de la secuencia de consenso identificados. Dos variaciones se identificaron en las posiciones 2 (L-> I) y 12 (G-> N) de los 14 N-terminal de aminoácidos de HA2, pero estas variaciones se constató que no afecta a la unión entre los anticuerpos y las variantes del péptido 6 . El epítopo Uni-1 (GLFGAIAGFIEGGW) fue elegida para desarrollar un anticuerpo universal contra la HA. Este anticuerpo demostró una especificidad notable de las secuencias virales y es capaz de unirse a los 13 subtipos de influenza A-HA (H1-H13) (Figura 2).
Utilizando un enfoque similar, dos secuencias universalmente conservadas fueron identificados en todos los de la influenza A NA, uno cerca del lugar enzimáticamente activa (HCA-2) (Figura 3) y el otro en la N-terminal (HCA-3) (Figura 3B) . Péptidos con estas secuencias de aminoácidos fueron utilizados como antígenos para generar anticuerpos contra la NA universales. Los anticuerpos contra epítopes eran capaces de unirse a los 9 subtipos de NA y mostró muy poca reactividad cruzada con proteínas alantoideo o celular, lo que demuestra una alta especificidad de las secuencias virales NA (Figura 4).
Figura 5 se muestra una visión general del método de slot blot para la cuantificación de la gripe HA y NA.
Ejemplos de HA y NA antígeno análisis slot blot se muestran en las figuras 6 y 7. Figura 6a y 6c muestra resultados representativos después de la detección del antígeno HA en un estándar para la vacuna de la gripe y las muestras de vacuna, respectivamente. Cada muestra (estándar o de la vacuna) se realizaron por duplicado, en pozos adyacentes. Duplicados se muestran similar la intensidad después de la detección. Optimización de las diluciones de anticuerpos, la incubación y el tiempo de exposición puede ser necesaria en función de los anticuerpos utilizados.
Un ejemplo de una curva típica estándar obtenida tras la detección de varias concentraciones de HA de una muestra de la vacuna estándar de referencia se muestra en la Figura 6B. La concentración de antígeno HA es proporcional a la intensidad de la señal después de la detección de quimioluminiscencia del slot blot y se ajusta a la modelo de la curva 4-PL apropiado para este intervalo de concentraciones (0,0938 a 6 mg de HA / ml).
La figura 7 muestra los resultados representativos de la detección del antígeno de NA en un estándar para la vacuna de la gripe y en muestras de la vacuna. Análisis de la densidad mostraron que la intensidad de la señal obtenida mediante la detección del antígeno de NA en diferentes diluciones de un estándar para la vacuna de slot blot es proporcional a la concentración de NA (Fig. 7A). La curva estándar resultante se ajusta a un modelo de 4-PL para este rango de concentración (0,039 a 10 microgramos NA / ml), como se muestra en la Figura 7B. Figura 7C muestra un ejemplo de un análisis de transferencia ranura del contenido de NA en las muestras de vacuna contra la influenza. Cada muestra se analizó por duplicado, en pozos adyacentes.

Figura 1. Tasa de Conservación de la epítopo Uni-1 en la región del péptido de fusión de la influenza A-HA.
Los análisis bioinformáticos de todos los de la gripe A disponibles secuencias HA confirmó que el péptido de fusión (que se encuentra en la N-terminal de la subunidad HA2) es la única región universalmente conservadas de HA. Tenga en cuenta que las dos variaciones en la posición 2 (L-> I) y 12 (G-> N) se constató que no afectan a la unión de los anticuerpos 6. Un anticuerpo universal, capaz de unir 13 diferentes subtipos de influenza A-HA (H1-H13) se ha desarrollado utilizando la Uni-1 epítopo (GLFGAIAGFIEGGW).
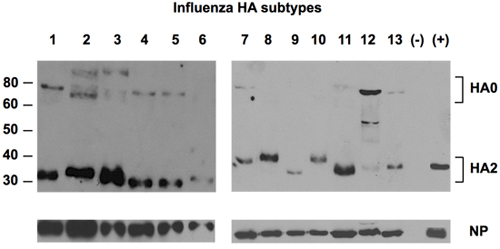
Figura 2. Detección de 13 subtipos de HA de anticuerpos contra la HA universales.
Fluidos alantoideo de 13 subtipos de virus de influenza propagados en huevos embrionados fueron fraccionadas en SDS-PAGE, seguida de la detección de las proteínas HA, utilizando el anticuerpo universal contra el epítopo Uni-1 de la HA. Proteínas NP se detectó como control de carga con un anticuerpo policlonal de conejo NP-anticuerpo específico. Control negativo (-) fue fluido alantoideo de los huevos infectados. Control positivo (+) era una norma de referencia de H1 de NIBSC, Reino Unido
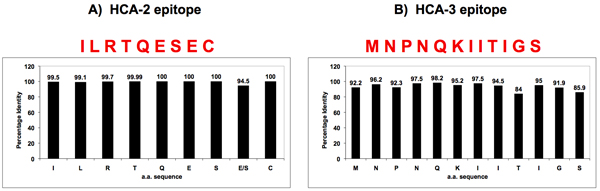
Figura 3. Homología de secuencia de la gripe A de NA cerca del lugar enzimáticamente activa y la N-terminal.
Dos secuencias universalmente conservadas fueron identificados en la gripe A de NA por la bioinformática, uno situado cerca del sitio activo enzimático (HCA-2) (Grupo A), y el otro en la N-terminal (HCA-3) (Grupo B). Péptidos con estas secuencias de aminoácidos conservados fueron sintetizados y utilizados para generar anticuerpos contra la NA universales.

Figura 4. Detección de 9 subtipos de NA NA por los anticuerpos.
Fluidos alantoideo de los nueve subtipos de NA de virus de influenza propagados en huevos embrionados fueron fraccionadas en SDS-PAGE, seguida de la detección de las proteínas de NA con el HCA-2 (Grupo A) y el IICA-3 (Grupo B) anticuerpos. Proteínas NP se detectó como control de carga con un anticuerpo policlonal de conejo NP-anticuerpo específico (Grupo C). Control negativo (-) fue fluido alantoideo de los huevos infectados. Control positivo (+) se enriquece con fluido alantoideo ARN1 de A / New Caledonia/20/99 y probaron con los antisueros correspondientes.

Figura 5. Diagrama de flujo del procedimiento de slot blot para la cuantificación de los antígenos HA y NA de las vacunas antigripales.
Los buffers necesarios para la dilución de la muestra, así como para el lavado y el bloqueo de la membrana de slot blot se prepara en primer lugar y la membrana de PVDF y papeles de filtro necesaria para el montaje del aparato de microfiltración Bio-Dot SF son pre-empapado. Vacuna contra la influenza y las muestras de referencia estándar se diluyen en los buffers óptima para la detección de HA o NA por slot blot. El aparato Bio-Dot SF microfiltración se arma de acuerdo a las instrucciones del fabricante y las muestras se aplica sobre la membrana de PVDF. HA y NA son antígenos detectados utilizando los anticuerpos universal contra cada antígeno. Análisis de densitometría se realiza en las señales de quimioluminiscencia obtenidos para la cuantificación de HA y NA en las muestras analizadas.
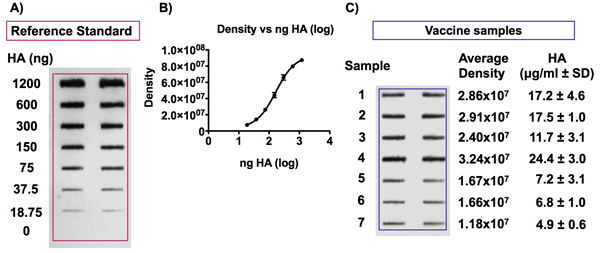
Figura 6. Detección del antígeno HA en las muestras de vacuna contra la influenza y se refierencia estándar.
El panel A muestra una mancha representativos obtenidos tras la inmunodetección del antígeno HA. El antígeno de referencia de HA se diluye a concentraciones de 0 a 6 g de HA / ml y las vacunas se diluyeron a una concentración de 0.375 mg de HA / ml en urea 4M / TBS antes de ser aplicados a una membrana de PVDF con un aparato de microfiltración Bio-Dot SF . El antígeno HA se detectó a continuación, utilizando el anticuerpo Uni-1 universal. El panel B muestra un ejemplo de una curva estándar obtenida mediante la detección de las señales de las concentraciones de HA diferentes de un estándar para la vacuna. La intensidad de la señal es proporcional a la concentración de HA y la curva se ajusta a un modelo de 4-PL.
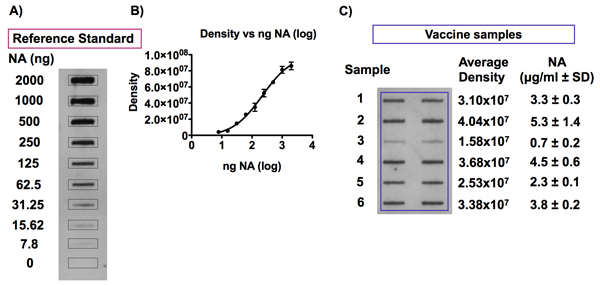
Figura 7. Detección del antígeno NA en las muestras de vacuna contra la influenza y el patrón de referencia.
Grupo A y B representante mostrar señales obtenidas tras la detección de NA en un estándar de referencia de la gripe vacuna diluida a las concentraciones de NA varía de 0 a 10 mg NA / ml en el 0,01% Zwittergent / TBS y el resultado de 4 PL curva estándar después de los análisis de densitometría. Un ejemplo típico de las señales de quimioluminiscencia detectado después de un análisis de transferencia de la ranura del antígeno NA en las muestras de vacuna contra la influenza se muestra en el panel de muestras de la vacuna de influenza C se diluye a una concentración de 1 mg de HA / ml en el 0,01% Zwittergent / TBS y se transfirieron a una membrana de PVDF utilizando un aparato Bio-Dot SF microfiltración. Diluciones del patrón de la vacuna de referencia correspondiente, con concentraciones de 0 a 2,5 g NA / ml, fueron incluidas en la misma mancha en el fin de establecer una curva estándar para la cuantificación del antígeno NA en las muestras de la vacuna. El antígeno NA se ha detectado con el anticuerpo HCA-2 universal contra la NA y análisis de densitometría de las señales de quimioluminiscencia obtenidos se llevó a cabo. La cantidad de NA en cada muestra de la vacuna se puede calcular en la curva 4-PL estándar obtenidos mediante el trazado de los valores de intensidad de señal frente a la concentración de NA para el estándar para la vacuna.
Discusión
La determinación cuantitativa de la influenza viral HA y NA son críticos para la investigación y desarrollo de vacunas ya que estas dos proteínas de superficie son los componentes virales más importantes de inducir respuestas inmunes 06.11. Se informó anteriormente los métodos inmunológicos para la detección de anticuerpos contra estas proteínas requieren cepa específica. El método de ranura mancha simple, reproducible y rápido para cuantificar los antígenos HA y NA aquí descritos son adecuados...
Divulgaciones
Agradecimientos
Los autores desean agradecer a la Sra. Monika Tocchi para la revisión editorial del manuscrito. AMH es apoyado por una beca de la Universidad King Abdulaziz, de Arabia Saudita a través de la Oficina Cultural de Canadá.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo o equipo | Empresa | Número de catálogo | Comentarios |
|---|---|---|---|
| Bio-Dot SF aparato de microfiltración | Bio-Rad | 170-6542 | |
| Bio-Dot SF filtro de papel | Bio-Rad | 162-0161 | |
| Immobilon-FL transferencia de membrana (PVDF) | Millipore | IPFL00010 | |
| Bomba de vacío | Millipore | WP6111560 | |
| Quimioluminiscencia BioMax Cine Luz | Kodak | 178 8207 | |
| FluorChem Gel Sistema de Documentación | Alpha Innotech | 29 a 008-1896X | |
| Anticuerpos de conejo contra la HA universales y los antígenos NA | Uni-1 (HA) HCA-2, HCA-3 (NA) | Los anticuerpos están disponibles a través del MTA o pueden ser generados por los investigadores interesados de acuerdo con los procedimientos descritos anteriormente 6,7. | |
| Vacuna contra la influenza de referencia de antígenos | CBER / FDA o NIBSC | ||
| Muestras de vacunas contra la influenza | Comúnmente disponibles en la mayoría de los países | ||
| Urea | Sigma-Aldrich | U1250 | |
| Zwittergent 3.14 Detergente | Calbiochem | 693017 | |
| Tween-20 | Fisher Scientific | BP337-500 | |
| Secante bloqueador de grado bajo en grasa de leche en polvo | Bio-Rad | 170-6404 | |
| ImmunoPure cabra anti-conejo IgG (H + L), conjugada con peroxidasa | Thermo Scientific | 31460 | |
| SuperSignal West Dura ampliada Duración Substrato | Thermo Scientific | 34075 |
Referencias
- Webster, R. G., Bean, W. J. Genetics of influenza virus. Annu Rev Genet. 12, 415-431 (1978).
- Skehel, J. J., Wiley, D. C. Receptor binding and membrane fusion in virus entry: the influenza hemagglutinin. Annu Rev Biochem. 69, 531-569 (2000).
- Wood, J. M. The influence of the host cell on standardisation of influenza vaccine potency. Dev Biol Stand. 98, 183-188 (1999).
- Sylte, M. J., Suarez, D. L. Influenza neuraminidase as a vaccine antigen. Curr Top Microbiol Immunol. 333, 227-241 (2009).
- Bright, R. A., Neuzil, K. M., Pervikov, Y., Palkonyay, L. WHO meeting on the role of neuraminidase in inducing protective immunity against influenza infection. Vaccine. 27, 6366-6369 (2008).
- Chun, S. Universal antibodies and their applications to the quantitative determination of virtually all subtypes of the influenza A viral hemagglutinins. Vaccine. 26, 6068-6076 (2008).
- Gravel, C. Qualitative and quantitative analyses of virtually all subtypes of influenza A and B viral neuraminidases using antibodies targeting the universally conserved sequences. Vaccine. 28, 5774-5784 (2010).
- Li, C. A simple slot blot for the detection of virtually all subtypes of the influenza A viral hemagglutinins using universal antibodies targeting the fusion peptide. Nat Protoc. 5, 14-19 (2010).
- Harvey, R., Wheeler, J. X., Wallis, C. L., Robertson, J. S., Engelhardt, O. G. Quantitation of haemagglutinin in H5N1 influenza viruses reveals low haemagglutinin content of vaccine virus NIBRG-14 (H5N1). Vaccine. 26, 6550-6554 (2008).
- Li, C. Application of deglycosylation and electrophoresis to the quantification of influenza viral hemagglutinins facilitating the production of 2009 pandemic influenza (H1N1) vaccines at multiple manufacturing sites in China. Biologicals. 38, 284-289 (2010).
- Johansson, B. E., Pokorny, B. A., Tiso, V. A. Supplementation of conventional trivalent influenza vaccine with purified viral N1 and N2 neuraminidases induces a balanced immune response without antigenic competition. Vaccine. 20, 1670-1674 (2002).
- Hashem, A. Universal antibodies against the highly conserved influenza fusion peptide cross-neutralize several subtypes of influenza A virus. Biochem Biophys Res Comm. , (2010).
Erratum
Formal Correction: Erratum: Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays
Posted by JoVE Editors on 11/13/2012. Citeable Link.
An author's affiliation was omitted from the publication of Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados