Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Quantitative Analysen aller Influenza Typ A Viral Hämagglutininen und Neuraminidasen mit Universal Antikörper in Einfache Slot Blot Assays
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Erratum Notice
Zusammenfassung
Ein einfaches Slot-Blot-Methode wurde für die Quantifizierung von Influenza Virus Hämagglutinin und Neuraminidase mit universellen Antikörper, die gegen ihre stärksten konservierten Sequenzen durch bioinformatische Analysen identifiziert entwickelt. Dieser innovative Ansatz kann eine sinnvolle Alternative zu quantitativen Bestimmung aller viralen Hämagglutinin und Neuraminidase.
Zusammenfassung
Hämagglutinin (HA) und Neuraminidase (NA) sind zwei Oberflächenproteine von Influenza-Viren, die bekanntlich eine wichtige Rolle im viralen Lebenszyklus und die Induktion von schützenden Immunantworten 1,2 zu spielen. Als Hauptzielgruppe für neutralisierende Antikörper, ist HA derzeit als das Influenza-Impfstoff Potenz Marker verwendet und wird durch einzelne radiale Immundiffusion (SRID) 3 gemessen. Allerdings verursacht die Abhängigkeit der SRID von der Verfügbarkeit der entsprechenden Subtyp-spezifischen Antiseren mindestens 2-3 Monate Verzögerung für die Veröffentlichung von jedem neuen Impfstoff. Darüber hinaus, obwohl es Belege, dass die NA auch induziert eine schützende Immunität 4, die Höhe der NA in Influenza-Impfstoffen ist noch nicht standardisiert durch einen Mangel an geeigneten Reagenzien oder analytische Methode 5. So sind einfache Alternative Methoden in der Lage Quantifizierung HA und NA-Antigenen wünschenswert für die schnelle Freigabe und bessere Qualitätskontrolle von Influenza-Impfstoffen.
Universell konservierten Regionen in allen verfügbaren Influenza-A-HA und NA-Sequenzen wurden von einer leistungsfähigen Bioinformatik-Analysen 6-7 identifiziert. Eine Sequenz (bezeichnet als Uni-1) wurde in die einzige universell konservierte Epitop des HA, das Fusionspeptid 6 identifiziert, während zwei konservierte Sequenzen in Neuraminidasen, einer in der Nähe der enzymatisch aktiven Stelle (bezeichnet als HCA-2) und die identifiziert wurden, andere in der Nähe des N-Terminus (bezeichnet als HCA-3) 7. Peptide mit dieser Aminosäure-Sequenzen wurden synthetisiert und verwendet, um Kaninchen für die Produktion von Antikörpern zu immunisieren. Der Antikörper gegen das Uni-1-Epitop von HA konnte auf 13 Subtypen von Influenza-A-HA (H1-H13) zu binden, während die Antikörper gegen die HCA-2 und HCA-3-Regionen von NA wurden binden alle 9 NA-Subtypen. Alle Antikörper zeigten bemerkenswerte Spezifität gegen die viralen Sequenzen als durch die Beobachtung, dass keine Kreuzreaktivität zu Allantois Proteine erkannt wurde nachgewiesen. Diese universellen Antikörper wurden dann verwendet, um Slot-Blot-Assays zu entwickeln, HA und NA in Influenza-A-Impfstoffe ohne die Notwendigkeit für spezifische Antiseren 7,8 quantifizieren. Vaccine Proben wurden auf eine PVDF-Membran mit einer Slot-Blot-Apparatur mit Referenzstandards verdünnt, um verschiedenen Konzentrationen angewendet. Für den Nachweis von HA, wurden die Proben und Standard-First in Tris-gepufferter Kochsalzlösung (TBS) mit 4M Harnstoff, während für die Messung von NA sie in TBS verdünnt wurden mit 0,01% Zwittergent diese Bedingungen deutlich verbessert die Nachweisempfindlichkeit. Nach der Erkennung des HA und NA-Antigenen durch Immunoblot mit ihren jeweiligen universellen Antikörper wurden Signalintensitäten durch Densitometrie quantifiziert. Mengen von HA und NA in den Impfstoffen wurden dann anhand einer Standardkurve mit den Signalintensitäten der verschiedenen Konzentrationen der Referenzen verwendet etabliert.
Da diese Antikörper binden an universellen Epitope in HA oder NA konnten sich Interessierte Forscher sie als Werkzeuge der Forschung Verwendung in Immunoassays andere als die Slot-Blot nur.
Protokoll
1. Vorbereitung der Reagenzien und Geräte
- Vor Beginn der Slot-Blot-Verfahren, bereiten 20_mls 4M Harnstoff-Lösung in Tris-gepufferter Kochsalzlösung (20 mM Tris, 137 mM NaCl, pH 7,6) (TBS) für die Hämagglutinin-oder HA, Slot-Blot-oder 20_mls einer 0,01% Zwittergent Lösung in TBS für die Neuraminidase-oder NA, Slot-Blot. Während 4M Harnstoff jedes Mal frisch zubereitet werden sollte, ist eine 10% ige Zwittergent Stammlösung in dH 2 O für mindestens 6 Monate bei Raumtemperatur stabil und kann daher auf 0,01% in TBS werden vor jedem Assay verdünnt.
- Bereiten 2000 MLS Waschpuffer durch Zugabe von Tween-20 zu einer TBS-Lösung auf eine Endkonzentration von 0,1%. Bereiten Sie 80 ml Blocking-Puffer durch Auflösen von Magermilchpulver (Blotting grade fettfreie Trockenmilch) bis zu einer Endkonzentration von 5% w / v in Waschpuffer.
- Aktivieren Sie die PVDF-Membran (eine 9 x 12 cm Größe pre-cut) in Methanol für 15 Sekunden, durch eine 2 Minuten, gefolgt spülen in ddH 2 O. Weichen Sie die Membran in TBS bis zur Verwendung. Vornässen 3 Blatt Bio-Dot SF Filterpapier in TBS bis zur Verwendung.
2. Vorbereitung der Influenza-Impfstoff Proben und Referenz-Standard für HA-Slot-Blot-
Influenza-Impfstoff Referenzstandards mit vorgegebenen HA-Gehalt entsprechend der Impfstämme zu prüfenden wurden aus dem Zentrum für Biologics Evaluation and Research (CBER / FDA, USA) oder dem National Institute for Biological Standard and Control (NIBSC, UK) erhalten und sind für die HA Quantifizierung durch Slot-Blot verwendet. Die Ermittler konnten bereiten auch ihre eigenen Antigen-Standards unter Verwendung etablierter Verfahren wie in Verweise 9 und 10 beschrieben.
- Für HA Referenz-Antigene und testen Impfstoff Proben: Verdünnen Sie die HA Referenz Antigen Lager in 4 M Harnstoff / TBS zu den folgenden Konzentrationen: 0, 0,0938, 0.1875, 0,375, 0,75, 1,5, 3 und 6 ug HA / ml. Gut mischen. Dann verdünnt Testimpfstoff Proben für den menschlichen Gebrauch von Impfstoff-Herstellern erhalten oder aus in-house zu wissenschaftlichen Zwecken in 4 M Harnstoff / TBS und gut mischen. Während Duplikate der Referenz-Antigen-und Impfstoffbank analysiert werden können, sind dreifach bevorzugt. Bereiten Sie 3 Verdünnungen jeder Probe (2-fache Differenz), damit die Konzentration der Probe innerhalb der Standardkurve fallen. Bereiten Sie 450 ul oder 650 ul jeder Verweis Antigen oder testen Impfstoff Probenverdünnung, um Duplikate zu laufen oder dreifach jeweils. Monovalenten Influenza-A-Impfstoffe können mit diesem Slot-Blot-Methode untersucht werden. Der HA-Gehalt des Referenz-Antigene wurde zuvor anhand SRID die derzeit verwendeten Standard-Test für Influenza-Impfstoff Vorbereitungen ist. Der HA-Gehalt durch SRID bestimmt war, als die erste Referenz-Antigen Lager HA-Konzentration für die Vorbereitung der Verdünnungen für die Slot-Blot-Standardkurve verwendet.
3. Vorbereitung der Influenza-Impfstoff Proben und Referenz-Standard für NA Slot-Blot-
Influenza-Impfstoff Referenzstandards entsprechend der Impfstämme zu prüfenden wurden aus dem Zentrum für Biologics Evaluation and Research (CBER / FDA, USA) oder dem National Institute for Biological Standard and Control (NIBSC, UK) erhalten und sind für die NA Quantifizierung verwendet durch Slot-Blot. Die NA Inhalt dieser Referenzproben durch SDS-PAGE-Analyse von deglykosylierter Proben in Verbindung mit Densitometrie Scan-Analyse bestimmt wurde, wie zuvor beschrieben 9, mit leichten Modifikationen 10. Kurz gesagt, wurden die deglykosylierter Impfstoff Referenzproben (5 ug) mit Probenpuffer gemischt und auf dem Gel. Das Gel wurde bei 20 mA für ca. 90 min laufen, bis die Verfolgung Farbstoff nur aus dem Gel laufen, gefolgt von Sypro Färbung. Densitometrie Quantifizierung von Proteinen erfolgte mit einem Fluorchem Geldokumentationssystem (Alpha Innotech) durchgeführt. Die Höhe der NA wurde basierend auf dem Verhältnis der NA-Proteine an die gesamten Proteine, wie Lowry-Assay ermittelt. Referenzproben hergestellt unter Verwendung dieser Methode kann dann in Slot-Blot zur Quantifizierung von NA Inhalte in Impfstoff Proben von Impfstoffen Hersteller verwendet werden.
- Für NA Referenz-Antigene und testen Impfstoff Proben: Verdünnen Sie die NA Referenz Antigen Lager in 0,01% Zwittergent / TBS zu den folgenden Konzentrationen: 0, 0,039, 0,078, 0,1562, 0,3125, 0,625, 1,25, 2,5, 5 und 10 pg NA / ml. Gut mischen. Dann verdünnt Testimpfstoff Proben für den menschlichen Gebrauch von Impfstoff-Herstellern erhalten oder aus in-house zu wissenschaftlichen Zwecken in 0,01% Zwittergent / TBS und gut mischen. Während Duplikate der Referenz-Antigen-und Impfstoffbank analysiert werden können, sind dreifach bevorzugt. Bereiten Sie 3 Verdünnungen jeder Probe (2-fache Differenz), damit die Konzentration der Probe innerhalb der Standardkurve fallen. Bereiten Sie 450 ul oder 650 ul jeder Verweis Antigen oder testen Impfstoff Probenverdünnung, um Duplikate zu laufen oder dreifach jeweils. Monovalenten Influenza A-Impfstoffe können wit getestet werdenh diesem Slot-Blot-Methode.
4. Versammlung der Bio-Dot SF Mikrofiltration Apparate und Blotting von Proben auf PVDF-Membran
- Bauen Sie eine zuvor gereinigt und getrocknet Bio-Dot SF Mikrofiltration Apparat. Legen Sie die Dichtung Trägerplatte in die Vakuumkammer und legen Sie die Dichtung auf top.Place die 3 befeuchtet Blatt Bio-Dot SF Filterpapier über die Dichtung, gefolgt von der Pre-getränkte PVDF-Membran. Legen Sie die Probe Vorlage auf der Membran und den Finger ziehen Sie die vier Schrauben mit einem diagonal kreuzweise um die einheitliche Anwendung von Druck auf die Membran-Oberfläche zu gewährleisten.
- Stellen Sie sicher, dass die 3-Wege-Ventil eingestellt ist, dass die Vakuumkammer, um das Vakuum Quelle freizulegen nur vor dem Einschalten der Pumpe und Anschluss des Vakuums.
- Schalten Sie die Pumpe und die Verbindung zum Bio-Dot Apparat. Stellen Sie sicher, dass der Fluss Ventil auf einem Niveau unterhalb der Probe Brunnen für eine rasche und angemessene Entwässerung der Proben in den folgenden Schritten positioniert ist.
- Wiederholen Sie die Schraubenanzug Schritt mit der Diagonalen kreuzweise. Das Anziehen der Schrauben während der Vakuum angelegt sorgt für eine sichere Abdichtung und verhindert Kreuzkontaminationen zwischen den Wells.
- Ändern Sie den Flow Ventil, um die Vakuumkammer der Luft ausgesetzt, und schalten Sie die Pumpe.
- Apply 100 ul TBS in alle Vertiefungen mit einer Mehrkanalpipette, um die Membran somit eine einheitliche Bindung des Antigens rehydrieren. Es muss darauf geachtet, die Bildung von Blasen zu vermeiden und die Lösung in der Mitte der gut anwenden, als an der Unterseite nahe wie möglich sein, um den Schlitz gleichmäßig abdecken. Burst keine Luftblase aus Versehen mit einer Pipette Spitze eingeführt.
- Ändern Sie den Flow Ventil, um die vielfältigen sowohl Luft und das Vakuum ausgesetzt, schalten Sie die Pumpe, und sanft drain der Puffer von den Brunnen, indem sie einen Finger über den Hafen der Luft ausgesetzt, um die Menge von Vakuum zu regulieren.
- Ändern Sie den Flow Ventil, um den vielfältigen Luft, sobald der Puffer komplett aus allen Vertiefungen abgelassen aussetzen. Schalten Sie die Pumpe oder trennen Sie das Vakuum.
- Apply 200 ul jeder Standard-oder Impfstoff Probenverdünnung pro Vertiefung. Pipet Proben ein zu einer Zeit, in der Mitte eines jeden gut, wie auf den Boden wie möglich zu schließen, wobei darauf zu achten Einführung Luftblasen. Burst keine Luftblase aus Versehen mit einer Pipette Spitze eingeführt. Legen Sie 200 ul Verdünnungspuffer (4 M Harnstoff / TBS oder 0,01% Zwittergent / TBS) in ungenutzten Brunnen, um die ordnungsgemäße Vakuum an den Brunnen in Betrieb zu gewährleisten.
- Stellen Sie den Flow Ventil, um die vielfältigen sowohl Luft und das Vakuum ausgesetzt. Schalten Sie die Pumpe (oder schließen Sie das Vakuum) und schonend möglich, die Proben vollständig aus den Vertiefungen drain durch die Steuerung der Menge an Vakuum mit einem Finger über den Hafen der Luft ausgesetzt. Entfernen Sie die Finger vom Hafen, um das Vakuum, sobald alle Proben wurden entwässert freizugeben.
- Sofort mit 200 ul von TBS in jede Vertiefung mit einer Mehrkanalpipette. Anwenden eines leichten Vakuums abtropfen und waschen Sie die Bohrlöcher durch die Steuerung der Menge an Vakuum mit einem Finger über den Hafen der Luft ausgesetzt.
- Wiederholen Sie den Waschvorgang in Schritt 4.11 beschrieben. Sobald der Brunnen komplett entleert, lösen Sie die Schrauben der Mustervorlage und Ausschalten des Vakuums zu vermeiden Übertrocknung die Vertiefungen geben. Unmittelbar vor der Membran zu entfernen.
- Legen Sie die Membran in Blocking-Puffer und Inkubation über Nacht bei 4 ° C, unter leichtem Schütteln. Verwenden Sie ausreichend Blocking-Puffer vollständig bedecken die Membran.
5. Immunoblotting von HA und NA-Antigenen
- Nach der Inkubation über Nacht in Blocking-Puffer, waschen Sie die Membran zweimal für 5 Minuten mit TBS/0.1% Tween-20 Waschpuffer. Für alle Waschungen und Inkubationen sicher, dass die Membran vollständig mit Lösung bedeckt.
- Inkubieren Sie die Membran mit einem Universal-Kaninchen-Antikörper gegen HA (wie Uni-1) oder NA (wie HCA-2 oder HCA-3) in 5% w / v BSA in Waschpuffer für 1 Stunde bei Raumtemperatur verdünnt, mit sanften rocking. Optimale Antikörper-Konzentrationen müssen für jeden Antikörper Lager bestimmt werden. Verdünnungen von 1:4000 Kaninchen-anti-Serum gab optimale Ergebnisse für den oben genannten Antikörpern.
- Waschen Sie die Membran drei Mal, bei Raumtemperatur unter leichtem Schütteln für jeweils 15 Minuten Zeit, um alle ungebundenen primären Antikörper zu entfernen.
- Inkubieren Sie die Membran mit einem HRP-konjugierten Anti-Kaninchen-Sekundärantikörper. Verwenden Sie einen 1:50000 Verdünnung des Thermo ImmunoPure Ziege Anti-Kaninchen-IgG, Peroxidase konjugierten Antikörper in Blocking-Puffer und Inkubation bei Raumtemperatur für 30 Minuten auf dem Schüttler.
- Waschen Sie die Membran drei Mal, Schaukeln für jeweils 15 Minuten Zeit, bei Raumtemperatur mit Waschpuffer, um alle ungebundenen Sekundärantikörper zu entfernen.
- Waschen Sie die Membran mit TBS für 5 Minuten auf dem Schüttler, um restliches Tween-20 Detergens aus der Membran-Oberfläche zu entfernen.
- Bereiten Sie das Substrat mit 3 ml eines jeden reAgent aus dem Supersignal West Dura Erweiterte Duration Substrate Kit von Thermo Scientific und gut mischen.
- Legen Sie die Membran auf einem trockenen Papiertuch zu entfernen sanft überschüssiges TBS-Puffer.
- Übertragen Sie die Membran in einem trockenen Behälter und fügen das Substrat, auf die gesamte Membran abzudecken. Inkubieren 5 Minuten unter leichtem Schütteln bei Raumtemperatur.
- Entfernen Sie das überschüssige Substrat durch vorsichtiges Abtupfen der Membran auf Seidenpapier.
- Expose die Membran auf eine Chemilumineszenz-Film. Die Länge der Exposition müssen optimiert werden, um Sättigung zu vermeiden, sondern wird in der Regel zwischen 10 Sekunden und 10 Minuten liegen.
- Führen Densitometrie analysiert auf dem entwickelten Film mit einem Gel Imaging Apparaturen wie die Fluorchem Geldokumentationssystem (Alpha Innotech) nach den Anweisungen des Herstellers. Die Dichte-Werte für jeden Satz von Wiederholungen Bezug Antigene und testen Impfstoff Proben werden dann gemittelt. Während die Antigen-Standards und Impfstoff-Proben in Duplikaten ausgeführt werden können, sind dreifach bevorzugt. Dichte-Werte für Replikate sind sehr ähnlich sein. Signifikante Unterschiede zwischen Wiederholungen deuten auf eine wahrscheinlich technische Probleme während des Verfahrens. Eine konzentrationsabhängige Standardkurve durch Auftragen der gemittelten Dichte Werte gegen die Menge (in ng) von HA oder NA-Antigen in jedem Slot gesteckt, aus dem Referenz-Standard etabliert. Mit entsprechender Kalibrierung Kurvenanpassung bei Immunoassays ist entscheidend für die Quantifizierung von HA und NA genau. Lineare Regression, indem man die Reaktion (y) gegen die Konzentration (x) mit Hilfe des linearen Teils der Response-Kurve (y = mx + b) erhalten ist die einfachste Methode zur Quantifizierung der Analyten. Wenn ein breiteres Spektrum von Analyten für die Konzentration der Berechnung berücksichtigt wird, sollten die vier Parameter Logistik (4PL) Modell für Immunoassays derzeit akzeptiert werden. Eine Vielzahl von Software ist für interessierte Forscher zu prüfen erhältlich. Im Falle der beschriebenen Slot-Blot-Assay, Umwandlung der x-Achse Werte zu skalieren log ermöglicht die Kurve zu einem 4-PL-Modell und die Verwendung einer variablen Steigung nicht-linearen Regression passt die ausgelöscht Mengen von HA und NA in berechnen der getesteten Impfstoff Proben ist somit möglich. Deshalb regelmäßig nutzen dieses Modell für unsere Analysen. Da der Test-Impfstoff Proben entweder in 4 M Harnstoff / TBS oder 0,01% Zwittergent / TBS, bevor sie auf der Membran geblottet verdünnt wurden, muss der Verdünnungsfaktor für jede Probe zu berücksichtigen sein, um die HA und NA Inhalt der Original-Test zu ermitteln Impfstoff Proben. Es wird vorgeschlagen, dass jeder Test-Impfstoff Probe bei drei verschiedenen Verdünnungen (2-fache Differenz), um für einen Satz von Dichtewerten ausgeführt werden, um innerhalb der Standardkurve fallen. Dichte-Werte höher als die Standardkurve Bereich für alle getesteten Verdünnungen des Impfstoffs Proben müssen weiter verdünnt werden für eine genaue HA oder NA Quantifizierung. Wenn die Dichte-Werten unterhalb des untersten Ende der Kurve sind, sollten Proben mit einer niedrigeren Verdünnungsfaktor verdünnt werden.
6. Repräsentative Ergebnisse:
Bioinformatik-Analysen aller verfügbaren Influenza-A-HA-Sequenzen bestätigte die N-Terminus der HA2 Untereinheit (die Fusion Peptid) als einzige konservierte Region von HA. Abbildung 1 zeigt die Erhaltung für jede Aminosäure-Position der identifizierten Konsensussequenz. Zwei Varianten wurden an den Positionen 2 (L-> I) und 12 (G-> N) der 14 N-terminalen Aminosäuren von HA2 identifiziert, aber solche Veränderungen gefunden wurden nicht auf die Bindung zwischen den Antikörpern und dem Peptid-Varianten 6 beeinflussen . Die Uni-1-Epitop (GLFGAIAGFIEGGW) wurde gewählt, um eine universelle Antikörper gegen HA entwickeln. Dieser Antikörper nachgewiesen bemerkenswerte Spezifität für virale Sequenzen und in der Lage ist die Bindung an 13 verschiedenen Subtypen von Influenza-A-HA (H1-H13) (Abbildung 2).
Mit einem ähnlichen Ansatz wurden zwei universell konservierten Sequenzen in allen Influenza-A-NA ist, ein in der Nähe des enzymatisch aktiven Zentrums (HCA-2) (Abbildung 3A) und die andere am N-Terminus (HCA-3) (Abbildung 3B) identifiziert . Peptide mit dieser Aminosäure-Sequenzen wurden als Antigene verwendet werden, um universelle Antikörper gegen NA zu generieren. Die Antikörper gegen beide Epitope binden können, um alle 9 Subtypen der NA und zeigte sehr wenig Kreuzreaktivität zu Allantois oder zellulären Proteinen und bewiesen damit, eine hohe Spezifität für virale NA-Sequenzen (Abbildung 4).
Abbildung 5 zeigt einen Überblick über die Slot-Blot-Verfahren für die Quantifizierung von Influenza-HA und NA.
Beispiele für HA und NA-Antigen-Slot-Blot-Analyse sind in den Abbildungen 6 und 7 dargestellt. Abbildung 6A und 6C zeigt repräsentative Ergebnisse nach der Erkennung des HA-Antigen in einer Influenza-Impfstoff Referenzstandard und Impfstoff Proben. Jede Probe (Standard-oder Impfstoff) wurde in Doppelbestimmung durchgeführt, in benachbarten Vertiefungen. Duplikate sollen zeigen similar Intensitäten nach der Aufdeckung. Optimierung der Antikörper-Verdünnungen, Inkubation und Belichtungszeit kann je nach Bedarf und Antikörpern verwendet werden.
Ein Beispiel für eine typische Standardkurve erhalten nach der Aufdeckung von verschiedenen Konzentrationen von HA von einem Impfstoff Referenzstandard Probe wird in Abbildung 6B gezeigt. Die Konzentration von HA-Antigen ist proportional zur Signalintensität folgenden Chemilumineszenzdetektion der Slot-Blot und passt die 4-PL Kurvenanpassung Modell für diesen Konzentrationsbereich (0,0938 bis 6 pg HA / ml).
Abbildung 7 zeigt repräsentative Ergebnisse der Erkennung der NA-Antigen in einer Influenza-Impfstoff Referenzstandard und in Impfstoff-Proben. Density-Analyse zeigte, dass die Intensität des Signals durch den Nachweis der NA-Antigen in verschiedenen Verdünnungen eines Impfstoffs Referenzstandard durch Slot-Blot erhalten proportional zur Konzentration des NA (Abb. 7A) ist. Die daraus resultierende Standardkurve passt ein 4-PL Modell für diesen Konzentrationsbereich (0,039 bis 10 pg NA / ml), wie in Abbildung 7B gezeigt. Abbildung 7C zeigt ein Beispiel einer Slot-Blot-Analyse der NA-Gehalt in Grippeimpfstoff Proben. Jede Probe wurde in Doppelbestimmung durchgeführt, in benachbarten Vertiefungen.

Abbildung 1. Conservation Rate der Uni-1-Epitop in der Fusionspeptid Region des Influenza-A HA.
Bioinformatik-Analysen aller verfügbaren Influenza-A-HA-Sequenzen bestätigt, dass die Fusionspeptid (am N-Terminus der HA2 Untereinheit) das einzige universell konservierte Region von HA ist. Beachten Sie, dass die beiden Varianten an Position 2 (L-> I) und 12 (G-> N) gefunden wurden, nicht an den Antikörper Bindung 6 beeinflussen. Eine universelle Antikörper binden können 13 verschiedene Subtypen des Influenza-A-HA (H1-H13) wurde mit Hilfe der Uni-1-Epitop (GLFGAIAGFIEGGW).
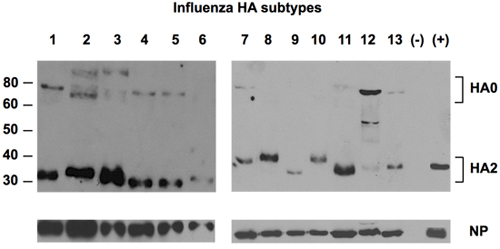
Abbildung 2. Erkennung von 13 Subtypen des HA durch allgemeine Antikörper gegen HA.
Allantois Flüssigkeiten von 13 Subtypen von Influenza A-Viren vermehrt in bebrüteten Eier wurden fraktioniert in SDS-PAGE, gefolgt von einem Nachweis der HA-Proteine mit der Universal-Antikörper gegen das Uni-1-Epitop von HA. NP-Protein wurde als Ladekontrolle mit einem polyklonalen Kaninchen-NP-spezifische Antikörper nachgewiesen. Negative Kontrolle (-) war Allantoisflüssigkeit aus infizierten Eiern. Positive Kontrolle (+) war ein Referenz-Standard von H1 aus NIBSC, UK
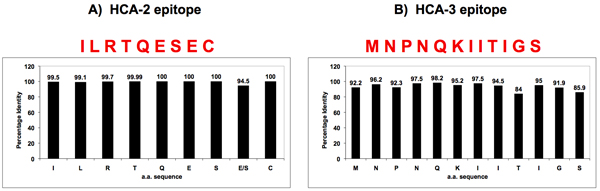
Abbildung 3. Sequenzhomologie von Influenza-A-NA in der Nähe des enzymatisch aktiven Zentrums und der N-Terminus.
Zwei universell konservierten Sequenzen wurden in Influenza-A-NA von einer leistungsfähigen Bioinformatik, einer in der Nähe der enzymatisch aktiven Stelle (HCA-2) befindet (Panel A), die andere am N-Terminus (HCA-3) (Panel B) identifiziert. Peptide mit diesen konservierten Aminosäure-Sequenzen wurden synthetisiert und verwendet werden, um universelle Antikörper gegen NA zu generieren.

Abbildung 4. Erkennung von 9 Subtypen der NA von NA-Antikörper.
Allantois Flüssigkeiten von neun NA-Subtypen von Influenza A-Viren vermehrt in bebrüteten Eier wurden fraktioniert in SDS-PAGE, gefolgt von einem Nachweis der NA-Proteine mit der HCA-2 (Panel A) und HCA-3 (Panel B) Antikörper. NP-Protein wurde als Ladekontrolle mit einem polyklonalen Kaninchen-NP-spezifischen Antikörper (Panel C) nachgewiesen. Negative Kontrolle (-) war Allantoisflüssigkeit aus infizierten Eiern. Positive Kontrolle (+) war Allantoisflüssigkeit mit rNA1 von A / New Caledonia/20/99 versetzt und sondiert mit den entsprechenden Antiseren.

Abbildung 5. Flussdiagramm der Slot-Blot-Verfahren für die Quantifizierung von HA und NA-Antigenen in Influenza-Impfstoffen.
Der Puffer für Probenverdünnung sowie für Wasch-und Blockierung der Slot-Blot-Membran benötigt werden zuerst hergestellt und die PVDF-Membran und Filterpapiere für die Montage des Bio-Dot SF Mikrofiltration Apparat benötigt werden eingeweicht. Influenza-Impfstoff und Referenz-Standard-Proben sind in der optimalen Puffer für HA-oder NA-Erkennung durch Slot-Blot-verdünnt. Die Bio-Dot SF Mikrofiltration Gerät ist gemäß den Anweisungen des Herstellers und die Proben werden auf die PVDF-Membran aufgebracht montiert. HA und NA-Antigene werden unter Verwendung des universellen Antikörper gegen jedes Antigen. Densitometrie Analyse basiert auf der Chemilumineszenz-Signale für die Quantifizierung von HA und NA in den untersuchten Proben erhalten wurden, durchgeführt.
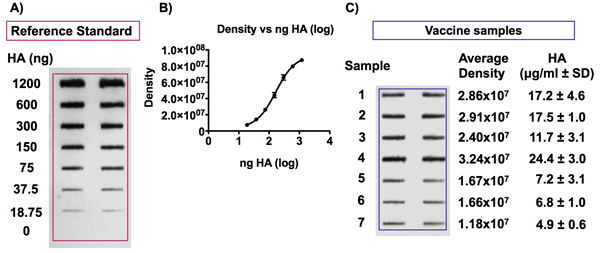
Abbildung 6. Nachweis der HA-Antigen in Grippeimpfstoff Proben und beziehenrenzstandard.
Panel A zeigt einen repräsentativen Blot erhalten folgende Immundetektion der HA-Antigen. Die HA Referenz Antigen wurde auf Konzentrationen von 0 bis 6 pg HA / ml und die Impfstoffe zu einer Konzentration von 0,375 Mikrogramm Hämagglutinin / ml in 4 M Harnstoff / TBS, bevor sie auf eine PVDF-Membran mit einer Bio-Dot SF Mikrofiltration Vorrichtung aufgebracht wurden verdünnt verdünnt . Die HA-Antigen wurde dann unter Verwendung des Uni-1 Universal-Antikörper. Panel B zeigt ein Beispiel für eine Standardkurve durch Erfassen von Signalen von verschiedenen HA-Konzentrationen von einem Impfstoff Referenzstandard erhalten. Die Signalintensität ist proportional zur Konzentration des HA und die Kurve passt ein 4-PL-Modell.
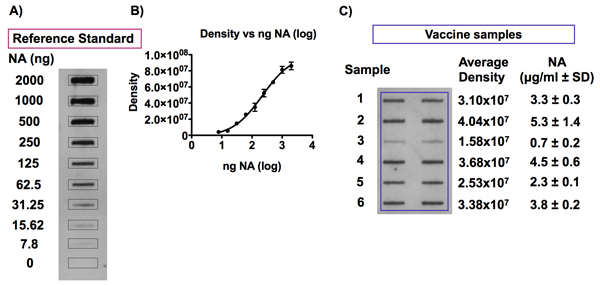
Abbildung 7. Nachweis der NA-Antigen in Grippeimpfstoff Proben und Referenz-Standard.
Panel A und B zeigen repräsentative Signale erhalten nach der Aufdeckung von NA in einer Influenza-Impfstoff Referenzstandard verdünnt, um NA-Konzentrationen im Bereich von 0 bis 10 pg NA / ml in 0,01% Zwittergent / TBS und die daraus resultierenden 4-PL Standardkurve folgenden Densitometrie analysiert. Ein Beispiel für typische Chemilumineszenz detektiert nach einer Slot-Blot-Analyse der NA-Antigen in Grippeimpfstoff Proben ist in Panel C Influenza-Impfstoff Proben gezeigt wurden auf eine Konzentration von 1 ug HA / ml in 0,01% Zwittergent / TBS verdünnt und wurden auf einen ausgelöscht PVDF-Membran mit einem Bio-Dot SF Mikrofiltration Apparat. Verdünnungen der entsprechenden Impfstoff Referenzstandard, mit Konzentrationen im Bereich von 0 bis 2,5 pg NA / ml, wurden auf dem gleichen Fleck enthalten, um eine Standardkurve für die Quantifizierung der NA-Antigen in der Impfstoff-Proben zu etablieren. Die NA-Antigen wurde mit dem HCA-2 universal-Antikörper gegen NA und Densitometrie Analyse der Chemilumineszenzsignale erhalten wurde, durchgeführt erkannt. Die Höhe der NA in jedem Impfstoff Probe kann gegen die 4-PL Standardkurve durch Auftragen der Signalintensität Werte gegenüber der NA-Konzentration für den Impfstoff Referenzstandard erhalten wird, berechnet werden.
Diskussion
Quantitative Bestimmung des Influenza Virus HA und NA sind entscheidend für die Impfstoff-Forschung und Entwicklung, da diese beiden Oberflächenproteine wichtigsten viralen Komponenten induzieren Immunreaktionen 6-11 sind. Zuvor berichtete immunologische Methoden zum Nachweis dieser Proteine benötigen Belastung spezifischen Antikörpern. Die einfache, reproduzierbare und schnelle Slot-Blot-Methode, um die HA und NA-Antigenen hier beschriebenen Quantifizierung eignen sich für alle Influenza-A-V...
Offenlegungen
Danksagungen
Die Autoren bedanken sich bei Frau Monika Tocchi für redaktionelle Durchsicht des Manuskripts danken. AMH wird durch ein Stipendium von King Abdulaziz Universität unterstützt wird, durch den saudi-arabischen Kulturbüro in Kanada.
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes oder Ausrüstung | Firma | Katalog-Nummer | Kommentare |
|---|---|---|---|
| Bio-Dot SF Mikrofiltration Apparatus | Bio-Rad | 170-6542 | |
| Bio-Dot SF Filterpapier | Bio-Rad | 162-0161 | |
| Immobilon-FL Transfer-Membran (PVDF) | Millipore | IPFL00010 | |
| Vakuumpumpe | Millipore | WP6111560 | |
| Chemilumineszenz BioMax Light Film | Kodak | 178 8207 | |
| FluorChem Gel-Dokumentations-System | Alpha Innotech | 29 bis 008-1896X | |
| Universal-Kaninchen-Antikörper gegen HA und NA-Antigenen | Uni-1 (HA) HCA-2, HCA-3 (NA) | Antikörper sind durch MTA erhältlich oder können von interessierten Forschern nach den Verfahren zuvor beschriebenen 6,7 erzeugt werden. | |
| Influenza-Impfstoff-Antigen Referenz | CBER / FDA oder NIBSC | ||
| Influenza-Impfstoff Proben | Häufig in den meisten Ländern | ||
| Harnstoff | Sigma-Aldrich | U1250 | |
| Zwittergent 3-14 Waschmittel | Calbiochem | 693017 | |
| Tween-20 | Fisher Scientific | BP337-500 | |
| Blotting Grade Blocker Non-Fett-Trockenmilch | Bio-Rad | 170-6404 | |
| ImmunoPure Goat Anti-Rabbit IgG (H + L), Peroxidase-konjugierten | Thermo Scientific | 31460 | |
| SuperSignal West Dura Erweiterte Duration Substrate | Thermo Scientific | 34075 |
Referenzen
- Webster, R. G., Bean, W. J. Genetics of influenza virus. Annu Rev Genet. 12, 415-431 (1978).
- Skehel, J. J., Wiley, D. C. Receptor binding and membrane fusion in virus entry: the influenza hemagglutinin. Annu Rev Biochem. 69, 531-569 (2000).
- Wood, J. M. The influence of the host cell on standardisation of influenza vaccine potency. Dev Biol Stand. 98, 183-188 (1999).
- Sylte, M. J., Suarez, D. L. Influenza neuraminidase as a vaccine antigen. Curr Top Microbiol Immunol. 333, 227-241 (2009).
- Bright, R. A., Neuzil, K. M., Pervikov, Y., Palkonyay, L. WHO meeting on the role of neuraminidase in inducing protective immunity against influenza infection. Vaccine. 27, 6366-6369 (2008).
- Chun, S. Universal antibodies and their applications to the quantitative determination of virtually all subtypes of the influenza A viral hemagglutinins. Vaccine. 26, 6068-6076 (2008).
- Gravel, C. Qualitative and quantitative analyses of virtually all subtypes of influenza A and B viral neuraminidases using antibodies targeting the universally conserved sequences. Vaccine. 28, 5774-5784 (2010).
- Li, C. A simple slot blot for the detection of virtually all subtypes of the influenza A viral hemagglutinins using universal antibodies targeting the fusion peptide. Nat Protoc. 5, 14-19 (2010).
- Harvey, R., Wheeler, J. X., Wallis, C. L., Robertson, J. S., Engelhardt, O. G. Quantitation of haemagglutinin in H5N1 influenza viruses reveals low haemagglutinin content of vaccine virus NIBRG-14 (H5N1). Vaccine. 26, 6550-6554 (2008).
- Li, C. Application of deglycosylation and electrophoresis to the quantification of influenza viral hemagglutinins facilitating the production of 2009 pandemic influenza (H1N1) vaccines at multiple manufacturing sites in China. Biologicals. 38, 284-289 (2010).
- Johansson, B. E., Pokorny, B. A., Tiso, V. A. Supplementation of conventional trivalent influenza vaccine with purified viral N1 and N2 neuraminidases induces a balanced immune response without antigenic competition. Vaccine. 20, 1670-1674 (2002).
- Hashem, A. Universal antibodies against the highly conserved influenza fusion peptide cross-neutralize several subtypes of influenza A virus. Biochem Biophys Res Comm. , (2010).
Erratum
Formal Correction: Erratum: Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays
Posted by JoVE Editors on 11/13/2012. Citeable Link.
An author's affiliation was omitted from the publication of Quantitative Analyses of all Influenza Type A Viral Hemagglutinins and Neuraminidases using Universal Antibodies in Simple Slot Blot Assays.
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten