Method Article
LabVIEW operado Novela Osmometer nanolitros de Investigaciones de hielo de fijación con proteínas
En este artículo
Resumen
Proteínas de unión de hielo (IBP), también conocidas como proteínas anticongelantes, inhibir el crecimiento del hielo y son un aditivo prometedor para su uso en la crioconservación de tejidos. La principal herramienta utilizada para investigar los IBP es el osmómetro nanolitros. Hemos desarrollado un hogar diseñado etapa de enfriamiento montado en un microscopio óptico y se controla utilizando una rutina de costumbre-construido LabVIEW. El osmómetro nanoliter descrito aquí manipulado la temperatura de la muestra de una manera ultra-sensible.
Resumen
Ice-binding proteins (IBPs), including antifreeze proteins, ice structuring proteins, thermal hysteresis proteins, and ice recrystallization inhibition proteins, are found in cold-adapted organisms and protect them from freeze injuries by interacting with ice crystals. IBPs are found in a variety of organism, including fish1, plants2, 3, arthropods4, 5, fungi6, and bacteria7. IBPs adsorb to the surfaces of ice crystals and prevent water molecules from joining the ice lattice at the IBP adsorption location. Ice that grows on the crystal surface between the adsorbed IBPs develops a high curvature that lowers the temperature at which the ice crystals grow, a phenomenon referred to as the Gibbs-Thomson effect. This depression creates a gap (thermal hysteresis, TH) between the melting point and the nonequilibrium freezing point, within which ice growth is arrested8-10, see Figure 1. One of the main tools used in IBP research is the nanoliter osmometer, which facilitates measurements of the TH activities of IBP solutions. Nanoliter osmometers, such as the Clifton instrument (Clifton Technical Physics, Hartford, NY,) and Otago instrument (Otago Osmometers, Dunedin, New Zealand), were designed to measure the osmolarity of a solution by measuring the melting point depression of droplets with nanoliter volumes. These devices were used to measure the osmolarities of biological samples, such as tears11, and were found to be useful in IBP research. Manual control over these nanoliter osmometers limited the experimental possibilities. Temperature rate changes could not be controlled reliably, the temperature range of the Clifton instrument was limited to 4,000 mOsmol (about -7.5 °C), and temperature recordings as a function of time were not an available option for these instruments.
We designed a custom-made computer-controlled nanoliter osmometer system using a LabVIEW platform (National Instruments). The cold stage, described previously9, 10, contains a metal block through which water circulates, thereby functioning as a heat sink, see Figure 2. Attached to this block are thermoelectric coolers that may be driven using a commercial temperature controller that can be controlled via LabVIEW modules, see Figure 3. Further details are provided below. The major advantage of this system is its sensitive temperature control, see Figure 4. Automated temperature control permits the coordination of a fixed temperature ramp with a video microscopy output containing additional experimental details.
To study the time dependence of the TH activity, we tested a 58 kDa hyperactive IBP from the Antarctic bacterium Marinomonas primoryensis (MpIBP)12. This protein was tagged with enhanced green fluorescence proteins (eGFP) in a construct developed by Peter Davies' group (Queens University)10. We showed that the temperature change profile affected the TH activity. Excellent control over the temperature profile in these experiments significantly improved the TH measurements. The nanoliter osmometer additionally allowed us to test the recrystallization inhibition of IBPs5, 13. In general, recrystallization is a phenomenon in which large crystals grow larger at the expense of small crystals. IBPs efficiently inhibit recrystallization, even at low concentrations14, 15. We used our LabVIEW-controlled osmometer to quantitatively follow the recrystallization of ice and to enforce a constant ice fraction using simultaneous real-time video analysis of the images and temperature feedback from the sample chamber13. The real-time calculations offer additional control options during an experimental procedure. A stage for an inverted microscope was developed to accommodate temperature-controlled microfluidic devices, which will be described elsewhere16.
The Cold Stage System
The cold stage assembly (Figure 2) consists of a set of thermoelectric coolers that cool a copper plate. Heat is removed from the stage by flowing cold water through a closed compartment under the thermoelectric coolers. A 4 mm diameter hole in the middle of the copper plate serves as a viewing window. A 1 mm diameter in-plane hole was drilled to fit the thermistor. A custom-made copper disc (7 mm in diameter) with several holes (500 μm in diameter) was placed on the copper plate and aligned with the viewing window. Air was pumped at a flow rate of 35 ml/sec and dried using Drierite (W.A. Hammond). The dry air was used to ensure a dry environment at the cooling stage. The stage was connected via a 9 pin connection outlet to a temperature controller (Model 3040 or 3150, Newport Corporation, Irvine, California, US). The temperature controller was connected via a cable to a computer GPIB-PCI card (National instruments, Austin, Texas, USA).
Protocolo
0. Procedimientos preliminares
- Capilar de vidrio para inyección solución. Usando un extractor capilar (Narishige, Tokyo, Japón), preparar una pipeta agudo con una abertura fina de un tubo capilar de vidrio micro (Marca GMBH, Wertheim, Alemania). El tamaño de la abertura debe ser verificada haciendo pasar aire a través del capilar para obtener burbujeo fino en agua limpia. Si el capilar se cierra, entonces se puede abrir rompiendo su borde. Esto puede conseguirse pulsando o rascarse suavemente contra el agua que contiene paredes de los tubos. Preparar el capilar tal que la abertura está casi bloqueado, pero es lo suficientemente abierto para permitir la formación de burbujas de menos de un milímetro.
- Limpieza Cobre disco. Sonicar los discos de cobre durante 10 minutos en 0,1% Micro-90 jabón (Cole-Parmer, Vernon Hills, Illinois, EE.UU.), luego lavar con agua doblemente destilada. Introducir los discos en una mezcla de isopropanol (técnico) y sonicar solución de nuevo durante 10 min. Aletaaliado, se secan los discos con aire filtrado. Esta etapa de limpieza es crítica para evitar la contaminación IBP entre los experimentos.
- Doble capa de montaje cubreobjetos. Un conjunto de cubreobjetos se preparó para permitir la observación de la muestra sin condensación de humedad sobre la superficie de vidrio cubierta. Esto se logró mediante la colocación de un Drierite (WA Hammond Drierite, Xenia, Ohio, EE.UU.) partícula (2 mm de diámetro) entre dos cubreobjetos que fueron pegados a continuación con una pistola de pegamento caliente. Esta configuración impide la condensación que podría bloquear la vista cuando la muestra se enfrió a bajas temperaturas y elimina la necesidad para soplar aire seco a la ventana de observación.
1. Etapa de enfriamiento Set-up
- Conectar la entrada de flujo de agua y la salida de la etapa de enfriamiento a 4 mm de diámetro interno Tygon tubos (Saint-Gobain, París, Francia), y conecte el flujo de agua del tubo de entrada a una bomba de agua.
- Conectar un tubo de 4 mm interior Tygon diámetro a la entrada de la etapa de enfriamiento to suministrar aire seco. El aire se secó usando una columna en línea de Drierite.
- Operar las bombas de aire y agua. Tenga en cuenta que los elementos de refrigeración no debe funcionar sin un disipador de calor.
- Encienda el controlador de temperatura, cámara, y la rutina de LabVIEW.
2. Preparación de la muestra
- Colocar una gota de 3-4 l de aceite de inmersión B (Cargille laboratorios, Cedar Grove, Nueva Jersey, EE.UU.) en el lado posterior de un disco de diámetro de cobre de 7 mm que tiene 500 agujeros perforados mu m a través del disco.
- Colocar el disco de cobre en la etapa de enfriamiento con el lado del aceite de inmersión hacia abajo.
- Conectar el tubo capilar (el borde romo) a un 0,7 mm de diámetro interior del tubo Tygon conectado en el otro extremo a una jeringa de 2 ml, de vidrio (Poulten-Graf, Wertheim, Alemania).
- Antes de utilizar el tubo capilar, visita de la pequeña abertura de la capilaridad para asegurar que la abertura es un tamaño apropiado (véase los procedimientos preliminares).
- Inserte lentamente la glass capilar en el tubo de muestra preparada IBP proteína (2,4 mM Mp IBP-GFP en 20 mM de CaCl 2 y 25 mM Tris-HCl a pH 8, véase la referencia 10 para los detalles de preparación) y tirar de la jeringa de vidrio hasta que el capilar de vidrio contiene 0,1 l de la solución de proteína.
- Comienza la grabación de vídeo a través del software LabVIEW.
- Insertar el borde afilado de la capilar de vidrio (que contiene la solución de proteína) en uno de los agujeros en el disco de cobre en la etapa de enfriamiento.
- Mientras observa a través del microscopio (Olympus, Tokio, Japón, objetivo 10x), cuidadosamente penetrar en la capa de inmersión en aceite con la punta capilar de vidrio, y presione la jeringa de vidrio (muy delicadamente) para suministrar una cantidad pequeña (~ 10 nl) de la proteína solución para crear una gotita 200 micras.
- Cubrir el agujero en la etapa de enfriamiento con el conjunto de capa doble cubreobjetos (véase los procedimientos preliminares).
3. TH de medición de actividad
- Press el botón de refrigeración y la temperatura a -40 ° C.
- Inicialmente, la gota de solución será clara. A temperaturas bajas, típicamente en el rango de -30 ° C a -35 ° C, el color gotita cambios, lo que indica que la solución ha sido congelado. Inmediatamente después de la muestra se ha congelado, aumentar la temperatura lentamente hasta que la mayor parte de hielo comienza a derretirse. Un aumento gradual de la temperatura es necesario para evitar el rebasamiento de la temperatura que podría resultar en la fusión completa de la muestra.
- Cambiar a un objetivo 50x y comienzan a fundir el hielo mediante el ajuste de la temperatura. Este ajuste es interactivo, y los pasos finales se realiza normalmente con pequeños pasos de temperatura de 0,002 ° C. Continúe hasta que se derrita un cristal único que queda. El tamaño final del cristal debe ser alrededor de 10 micras. La temperatura más alta a la que ha dejado de fusión se determina que el punto de fusión y se determina con precisión en la etapa de análisis de vídeo más tarde.
- Ajustar la temperatura a unas pocas centésimas de un grado centígrado por debajo del punto de fusión del cristal y comenzar una rampa de temperatura con un retraso de 10 min. Ajustar la velocidad de rampa según se desee. Durante este tiempo, el cristal estará expuesto a los IBP.
- Al finalizar el tiempo de 10 min de exposición, la temperatura disminuirá de forma automática bajo el control de la rutina de LabVIEW.
- Observar la forma de los cristales a medida que disminuye la temperatura. En algún momento, la ráfaga repentina de los cristales de hielo pueden ser observados. La temperatura a la que ocurre esto se observa como la temperatura ráfaga cristal.
- El uso de análisis de vídeo para determinar el punto de fusión y la temperatura precisa de ráfaga. En primer lugar, mediante el uso de análisis de vídeo, encontrar el punto de fusión exacto. Recordemos que la temperatura más alta a la que ha dejado de fusión se determina que el punto de fusión. Documentar este punto de fusión en un programa de hoja de cálculo. Entonces, determinar la temperatura exacta cristal ráfaga, y documentar este valortambién. La diferencia entre el punto de fusión y el punto de congelación, o la temperatura ráfaga de cristal, es la actividad de histéresis térmica de la solución de IBP.
4. Medida de la actividad TH en función del tiempo
- Seguir el protocolo descrito en las Secciones 3.1-3.3 para preparar un solo cristal de hielo.
- Después de la formación de los cristales, ajuste el tiempo de retardo de la rampa como desee y, a su vez en la rampa.
- La temperatura disminuye a una tasa fija (de acuerdo con los requisitos de los operadores) de forma automática una vez que el tiempo de retardo de rampa ha pasado.
- Documentar la temperatura a la que se produce la ráfaga de cristal. Calcular el tiempo de exposición (el tiempo entre la formación de cristales y la ráfaga de cristal).
- Repetir el experimento para tiempos de retardo diferentes y representar gráficamente la actividad TH como una función del tiempo de exposición para evaluar la dependencia del tiempo de la actividad TH.
Resultados
La medición de la dependencia del tiempo TH
El osmómetro LabVIEW operado nanolitros facilita la realización de mediciones precisas de la actividad TH. La tasa de reducción de temperatura constante permite la medición de la dependencia del tiempo TH. El control preciso de la temperatura activado por el osmómetro de nanolitros era crucial para estos experimentos. El tiempo de exposición de un cristal de hielo a los IBP en solución se define como el periodo de tiempo desde la formación del cristal (el final del proceso de fusión) hasta que el crecimiento repentino de hielo alrededor del cristal (cristal ráfaga). Se encontró que el tiempo de exposición de los cristales de hielo a los IBPs afectado de forma crucial la actividad TH. Los períodos cortos de exposición a IBP (unos pocos segundos) produjo una actividad TH baja en el Mp IBP-GFP solución (2,4 mM) (Figura 5). La actividad TH aumentó con el tiempo de exposición IBP hasta que alcanzó una meseta a 4 min de exposición IBP. A concentraciones más altas de IBP, la placaau se alcanzó a los tiempos más cortos.
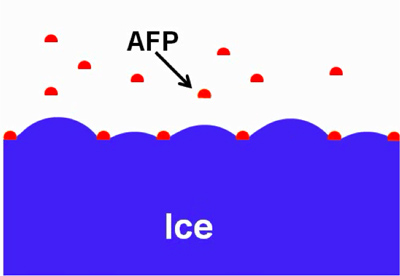
Figura 1. IBPs diagrama esquemático que ilustra adsorbido en hielo. Aprobada con permiso de 10.
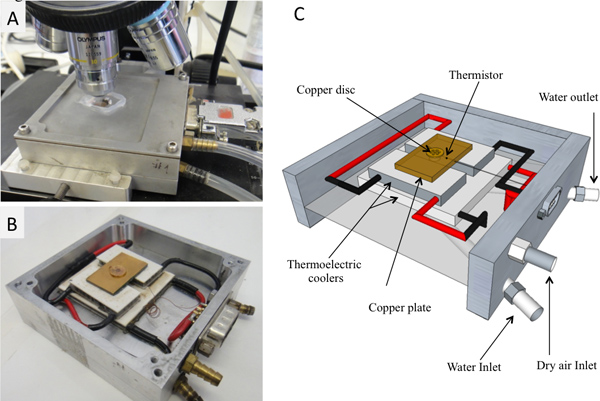
Figura 2. La etapa de enfriamiento. A) conectado a los tubos en el microscopio. B) Sin el liderazgo superior. C) Diagrama esquemático.
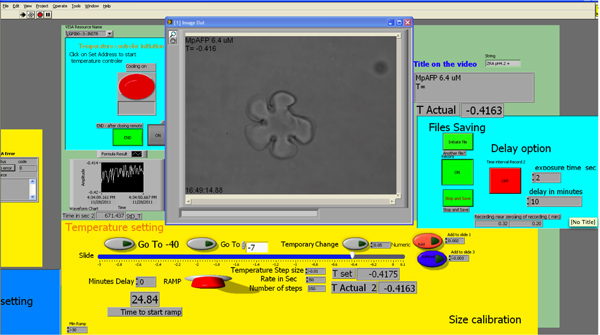
Figura 3. Captura de pantalla de la interfaz de LabVIEW. Click aquí para ampliar la figura.
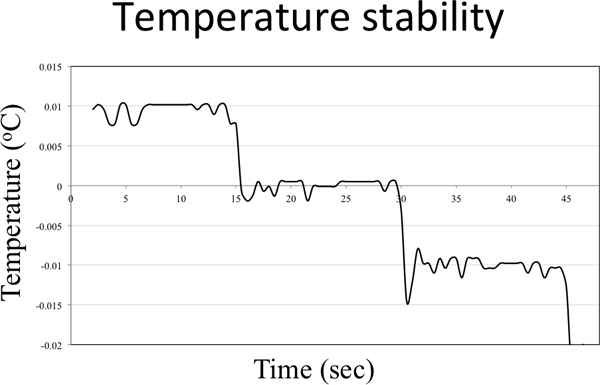
Figura 4. Gráfico de temperatura estabilidad. El controlador de temperatura se ajustó a bajar la temperatura de 0,01 ° C cada 15 seg.
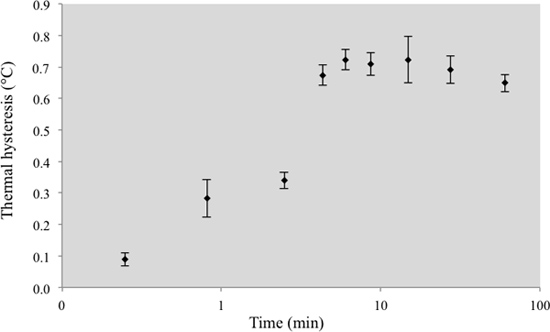
Figura 5. Mp actividad TH IBP como una función del tiempo de exposición de cristales de hielo a los IBP. Cada punto de tiempo es la media de 3-6 experimentos.
Discusión
Este trabajo demuestra el funcionamiento de un osmómetro de nanolitros controlado por computadora que permite mediciones precisas de la actividad TH con control de temperatura extraordinaria. En cualquier sistema sensible a la temperatura, gradientes de temperatura no deseados deben ser evitados. Para evitar gradientes de temperatura en el aparato que aquí se presenta, la gota de solución de ensayo debe ser posicionado en el centro de un agujero en la etapa de refrigeración de cobre del disco (paso 2,7). Adicionalmente, el monocristal debe estar en el centro de la gotita en lugar de cerca de los bordes (en la mayoría de los casos, esto sucederá de forma espontánea). La dependencia del tiempo descrito indica que la velocidad de enfriamiento puede influir en las lecturas de TH. Por lo tanto, se sugiere incluir un informe del tiempo durante el cual el cristal fue expuesta a la solución antes de la refrigeración, así como la velocidad de enfriamiento. Normalmente nos esperó 10 min antes de la rampa descendente de la temperatura a 0,01 ° C pasos cada sec 4.
Los co-LabVIEW controladosetapa Oling fue adaptado para uso con un microscopio invertido en el que los dispositivos de microfluidos podría ser térmicamente manipulado. Este sistema facilita la realización de experimentos de intercambio de soluciones que implican cristales de hielo y IBPS etiquetados con eGFP 9, 10, 16. El sistema LabVIEW controlado puede ser adaptado a una etapa Clifton conectando el controlador de temperatura 3040 a través de un circuito de adaptación designado eléctrica. Tal sistema es operado en el laboratorio Davies 17. El software LabVIEW y el diseño de la adaptación designado circuito eléctrico para la etapa de Clifton están disponibles bajo petición.
En conclusión, se describe un osmómetro de nanolitros que facilita el control sensible y manipulación de la temperatura y la tasa de aumento de la temperatura y disminución (con 0,002 ° C sensibilidad), coordinado con un interfaz de vídeo a través de una rutina de LabVIEW para análisis en tiempo real. Este sistema puede realizar reproducibles de velocidad controlada experimentos que son Important para investigar la cinética de la interacción IBP con hielo. Tales experimentos pueden abordar varios largamente debatido cuestiones relacionadas con el mecanismo de acción de los IBP.
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Esta investigación fue apoyada por la ISF, NSF, y ERC. Queremos reconocer la ayuda técnica con la etapa de temperaturas de Randy Milford, Michael Koren, Shafer Doug y Jeremy Dennison. Asistencia en el desarrollo de software fue proporcionado por O Chen, Xu Di, Sannareddy Rajesh, y Bhattachary Sumit. Nos gustaría agradecer a nuestros colaboradores el profesor Peter L. Davies y el Dr. Laurie A. Graham para la proteína de fusión IBP y útiles debates. También queremos agradecer a los miembros del laboratorio del Dr. Maya Bar-Dolev, Qin Yangzhong, Dr. Yeliz Celik, el Dr. Natalya Pertaya, Mizrahy Ortal, y Guy Shlomit por su retroalimentación de los usuarios.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre | Empresa | Número de catálogo / modelo | Comentarios |
| Aceite de inmersión tipo B | Cargille Laboratorios | 16484 | |
| Drierite | WA Hammond Drierite | 043063 2270g | |
| Micro 90 solución de limpieza | Cole-Parmer | EW-18100-11 | |
| Capilar extractor | Narishige | PB-7 | |
| Tubos capilares de cristal | Marca GnbH Persona | 7493 21 | 75 mm de largo, 1,15 de diámetro |
| Temperaturacontrolador | Newport, Irvine, California, Estados Unidos | Modelo 3040 | Modelo 3040 |
| Microscopio de luz | Olimpo | Modelo BH2 | |
| Objetivo de 10x | Olimpo | S Plan 10, 0,3, 160/0.17 | |
| Objetivo 50x | Nikon | CF plan, 50X/0.55 EPI ELWD | |
| Cámara CCD | Provideo | CVC-140 | |
| Tubos Tygon | Saint-Gobain, París, Francia | Formulación Tygon S-50-HL Tubería | |
| Vidrio de la jeringa (2 ml) | Poulten-Graf, Wertheim, Alemania | 7 10227 | |
| Tarjeta PCI GPIB- | National Instruments, Austin, Texas, EE.UU. | 778032-01 | |
| Vídeo marco grabBER IMAQ PCI-1407 | National Instruments, Austin, Texas, EE.UU. | 322156B-01 | |
| LabVIEW System Software Design | National Instruments, Austin, Texas, EE.UU. | Versión 8 | |
| Software DivX Author | DiVx LLC, San Diego, CA, EE.UU. |
Referencias
- DeVries, A. L. Glycoproteins as biological antifreeze agents in antarctic fishes. Science. 172, 1152-1155 (1971).
- Worrall, D., Elias, L., Ashford, D., Smallwood, M., Sidebottom, C., Lillford, P., Telford, J., Holt, C., Bowles, D. A carrot leucine-rich-repeat protein that inhibits ice recrystallization. Science. 282, 115-117 (1998).
- Raymond, J. A., Knight, C. A. Ice binding, recrystallization inhibition, and cryoprotective properties of ice-active substances associated with Antarctic sea ice diatoms. Cryobiology. 46, 174-181 (2003).
- Tomchaney, A. P., Morris, J. P., Kang, S. H., Duman, J. G. Purification, composition, and physical properties of a thermal hysteresis "antifreeze" protein from larvae of the beetle, Tenebrio molitor. Biochemistry. 21, 716-721 (1982).
- Kiko, R. Acquisition of freeze protection in a sea-ice crustacean through horizontal gene transfer. Polar Biology. 33, 543-556 (2010).
- Robinson, C. H. Cold adaptation in Arctic and Antarctic fungi. New Phytol. 151, 341-353 (2001).
- Gilbert, J. A., Hill, P. J., Dodd, C. E., Laybourn-Parry, J. Demonstration of antifreeze protein activity in Antarctic lake bacteria. Microbiology. 150, 171-180 (2004).
- Raymond, J. A., DeVries, A. L. Adsorption inhibition as a mechanism of freezing resistance in polar fishes. Proc. Natl. Acad. Sci. U.S.A. 74, 2589-2593 (1977).
- Pertaya, N., Marshall, C. B., DiPrinzio, C. L., Wilen, L., Thomson, E. S., Wettlaufer, J. S., Davies, P. L., Braslavsky, I. Fluorescence microscopy evidence for quasi-permanent attachment of antifreeze proteins to ice surfaces. Biophys. J. 92, 3663-3673 (2007).
- Celik, Y., Graham, L. A., Mok, Y. F., Bar, M., Davies, P. L., Braslavsky, I. Superheating of ice crystals in antifreeze protein solutions. Proc. Natl. Acad. Sci. U.S.A. 107, 5423-5428 (2010).
- Gilbard, J. P., Farris, R. L., Santamaria, J. Osmolarity of tear microvolumes in keratoconjunctivitis sicca. Arch. Ophthalmol. 96, 677-681 (1978).
- Gilbert, J. A., Davies, P. L., Laybourn-Parry, J. A hyperactive, Ca2+-dependent antifreeze protein in an Antarctic bacterium. FEMS Microbiol. Lett. 245, 67-72 (2005).
- Soriano, J., Braslavsky, I., Xu, D., Krichevsky, O., Stavans, J. Universality of persistence exponents in two-dimensional ostwald ripening. Phys. Rev. Lett. 103, (2009).
- Tomczak, M. M., Marshall, C. B., Gilbert, J. A., Davies, P. L. A facile method for determining ice recrystallization inhibition by antifreeze proteins. Biochem. Bioph. Res. Co. 311, 1041-1046 (2003).
- Knight, C. A., Hallett, J., Devries, A. L. Solute Effects on Ice Recrystallization - an Assessment Technique. Cryobiology. 25, 55-60 (1988).
- Celik, Y., Drori, R., Pertaya-Braun, N., Altan, A., Barton, T., Bar-Dolev, M., Groisman, A., Davies, P. L., Braslavsky, I. Microfluidic experiments reveal that antifreeze proteins bound to ice crystals suffice to prevent their growth. Proc. Natl. Acad. Sci. U.S.A. 110, 1309-1314 (2013).
- Middleton, A. J., Marshall, C. B., Faucher, F., Bar-Dolev, M., Braslavsky, I., Campbell, R. L., Walker, V. K., Davies, P. L. Antifreeze protein from freeze-tolerant grass has a beta-roll fold with an irregularly structured ice-binding site. J. Mol. Biol. 416, 713-724 (2012).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados