Method Article
Análisis comparativo de la hormona de crecimiento humano en suero utilizando SPRI, Nano-SPRI y ELISA Ensayos
En este artículo
Resumen
El trabajo propuesto se evalúa el potencial de diagnóstico de imagen directa y amplificada por resonancia de plasmones superficiales ensayos (SPRI), sobre todo para la detección de la hormona recombinante del crecimiento humano en el suero humano de pinchos, mediante la comparación de SPRI se traduce directamente con comercialmente disponibles inmunoensayo enzimático (ELISA) equipo.
Resumen
Métodos sensibles y selectivos para la detección de la hormona de crecimiento humana (hGH) durante un amplio intervalo de concentraciones (niveles altos de de 50-100 ng ml - 1 y niveles mínimos de 0,03 ng ml - 1) en la sangre circulante son esenciales como los niveles variable puede indicar la fisiología alterada. Por ejemplo, trastornos del crecimiento que se producen en la infancia pueden ser diagnosticadas mediante la medición de los niveles de hGH en sangre. Además, el mal uso de la hGH recombinante en el deporte no sólo plantea una cuestión ética también presenta amenazas sanitarias graves para el abusador. Una estrategia popular para medir la hGH mal uso, se basa en la detección de la relación de 22 kDa de hGH total hGH, como los niveles endógenos no 22 kDa se reducen después de hGH (rhGH) la administración exógena recombinante. Superficie resonancia de plasmones (SPRI) es una herramienta analítica que permite la monitorización directa (sin etiqueta) y visualización de interacciones biomoleculares mediante el registro de cambios de la ind refracciónex adyacente a la superficie del sensor en tiempo real. En contraste, el método colorimétrico de uso más frecuente, ensayo de inmunoabsorción ligado a enzimas (ELISA) utiliza marcado con enzima anticuerpos de detección para medir indirectamente la concentración de analito después de la adición de un sustrato que induce un cambio de color. Para aumentar la sensibilidad de detección, amplificada SPRI utiliza un formato de ensayo sándwich y puntos cuánticos infrarrojo cercano (QDs) para aumentar la intensidad de la señal. Después de la detección directa de SPRI rhGH recombinante en suero humano de pinchos, la señal de SPRI se amplifica por la inyección secuencial de anticuerpo de detección revestido con puntos cuánticos en el infrarrojo cercano (Nano-SPRI). En este estudio, el potencial diagnóstico de SPRI directa y amplificado se evaluó para medir rhGH claveteado en el suero humano y se compara directamente con las capacidades de un kit ELISA disponible comercialmente.
Introducción
Hormona de crecimiento humano (hGH) es un péptido de 191 aminoácidos (22 kDa) producida por la glándula pituitaria y directamente liberada en el torrente sanguíneo. Las interacciones entre el hipotálamo crecimiento péptido hormona liberadora de la hormona (GHRH) y la somatotropina inducen secreciones pulsátiles de hGH. Como resultado, los niveles de la hGH varían desde los máximos en los 50-100 ng / ml a los mínimos en el rango de 0,03 ng / ml 1. Deficiencia o exceso de hGH en el cuerpo pueden provocar una amplia gama de síntomas fisiológicos anormales. Por ejemplo, el exceso de los niveles de HGH puede dar lugar a gigantismo 2 y la diabetes 3. Niveles de agotamiento de la hGH causan el azúcar bajo en la sangre en los recién nacidos, y débil densidad ósea y la depresión en adultos 4.
La administración de la forma recombinante de la hGH (rhGH) mejora la masa muscular magra, mientras que la reducción de grasa corporal. Como tal, esta sustancia se convirtió en la droga de elección para atletas profesionales y aficionados, ya que mejora la fuerza física que confiere un advantage en deportes competitivos. rhGH está prohibido por la Agencia Mundial Antidopaje (AMA) 5,6 y mucho esfuerzo por parte de los investigadores internacionales se ha centrado en el desarrollo de pruebas que pueden detectar su presencia o efecto anabólico.
Ensayo de inmunoabsorción ligado a enzimas (ELISA) ha sido el método preferido para la determinación de la hGH en sangre entera 7. Aunque, ELISA es una técnica fiable que ofrece una buena sensibilidad y selectividad, es relativamente mucho tiempo y mano de obra intensiva. Además, ELISA se basa en la detección indirecta de la hGH mediante el empleo de etiquetas enzimáticas. En contraste, la resonancia de plasmón superficial (SPR) permite la detección de la hGH directamente sin el uso de etiquetas en tiempo real. El principio detrás de detección SPR implica una superficie de detección que consta de un prisma que está recubierto con una capa delgada de metal (oro o plata); cuando una luz polarizada monocromática interactúa con la superficie del metal, se generan "plasmones de superficie". La unión de un analitoa un receptor de la superficie inmovilizada sobre la superficie del metal perturba las condiciones de resonancia resultantes en un baño de resonancia desplazado, que luego puede ser correlacionada con la concentración de analito. Biosensores basados en SPR ya están disponibles en el mercado que ofrecen un tiempo real, técnica libre etiqueta para supervisar los eventos de unión biomoleculares y reacciones bioquímicas 8-10. Más recientemente, SPRI fue desarrollado en respuesta a la necesidad de multiplexación (es decir, el seguimiento de múltiples eventos de unión a la vez), lo cual no era posible en biosensores SPR clásicos. Por lo tanto, SPRI ha surgido como una herramienta para monitorear varios eventos de unión al mismo tiempo. SPRI sistemas actuales se basan en imágenes microscópicas de la superficie que se excita con la luz en un ángulo y longitud de onda específica 10. La imagen se captura luego en un dispositivo (CCD) matriz de carga acoplada.
Hasta la fecha, se han realizado unos ensayos basados en SPR desarrollados para detectar la hGH 11-14. Una estrategia particular, Conocido como el método isoforma 15, se basa en la detección de la relación de 22 kDa de hGH total hGH, como los niveles endógenos no de 22 kDa se reducen después de la administración exógena de rhGH. Recientemente, de Juan-Franco et al. 11 informó sobre el desarrollo de un inmunosensor basados en SPR para la detección selectiva de la 22 kDa y 20 kDa isoformas de hGH en muestras de suero humano. Los anticuerpos monoclonales específicos de cada isoforma fueron inmovilizados directamente en el sensor de oro que permite la medición de ambas isoformas de forma simultánea en una sola inyección con un límite de detección de 0,9 ng ml en -1. Alternativamente, SPR se ha utilizado para detectar anticuerpos con alta especificidad a la hGH 13. Si la concentración de analito objetivo cae por debajo del límite del sistema SPRI de detección (de 16-19 para vtipos arios de analito y superficies.
En este trabajo, se examinó el potencial analítico de SPRI y Nano-SPRI biosensores basados, sobre todo para la detección de rhGH en suero humano de pinchos, y la comparación de su capacidad de detección directamente a ELISA. Los siguientes parámetros serán revisados y considerados: tiempo de detección, la sensibilidad, el perfil cinético, reproducibilidad y especificidad.
Protocolo
1. Preparación de Soluciones y Proteína muestras para SPRI
- Preparar 100 ml de tampón fosfato salino (PBS) Solución de bajo contenido de sal que contiene fosfato 10 mM, cloruro sódico 150 mM, pH 7,4 y.
- Preparar 50 ml de solución de PBS que contiene alta concentración de sal de fosfato 10 mM, cloruro sódico 750 mM, pH 7,4 y.
- Preparar 5 ml de acetato de sodio 10 mM.
- Preparar un stock de 5 mg / ml de albúmina de suero bovino (BSA) diluido en solución de PBS baja en sal.
- Preparar una solución madre de la hormona del crecimiento humana recombinante (rhGH) a una concentración de 1 g / ml en solución PBS baja en sal.
- Preparar soluciones madre de anti-rhGH y el anticuerpo control negativo a una concentración de 100 mg / ml.
2. Prepare SPRI chip de matriz de anticuerpos
- Limpiar el chip mediante sonicación en 120 ml de solución Piranha estabilizado (3: 1 de peróxido de hidrógeno ácido sulfúrico concentrado al 30%) durante 90 min a 50 ° C y siga enjuagandoy sonicación con agua durante 5 min. Luego, enjuague chip con etanol y secar con una corriente de nitrógeno.
- Coloque el chip de oro en una cámara de UV / ozono durante 30 min para eliminar cualquier contaminante.
- Añadir 150 mg de ácido 11-mercaptoundecanoico a 20 ml de etanol en un tubo de ensayo que contiene una barra de agitación y una tapa del tubo.
- Coloque el chip en el tubo tubo de ensayo y de microondas / chips a 50 W y 50 ° C durante 5 min.
- Enjuague chip con etanol y remojo en etanol durante 5 min.
- Siga por un enjuague con agua y remojar en agua durante 5 minutos.
- Añadir 150 mg de 1-etil-3- (3-dimetilaminopropil) carbodiimida a 20 ml de agua en un tubo de ensayo que contiene una barra de agitación y una tapa del tubo. Chip de microondas como en el paso 2.4.
- Enjuague chip con agua y remojar en agua durante 5 minutos.
- Añadir 150 mg de N-hidroxisuccinimida en 20 ml de agua en un tubo de ensayo que contiene una barra de agitación y una tapa del tubo. Chip de microondas como en el paso 2.4.
- Enjuague chip con agua y remojar en agua durante 5 minutos.
- Prepare polietilenglicol 250 mM (PEG, 800 Da) en 20 ml de agua en un tubo de ensayo que contiene una barra de agitación y una tapa del tubo. Chip de microondas como en el paso 2.4.
Nota: El microondas PEG800 sobre la superficie del sensor se realiza como una etapa de bloqueo para evitar la unión no específica de proteínas séricas y complejos de punto cuántico más tarde utilizaron en el experimento. Esto se logra mediante PEG800 reaccionar con los sitios de oro desnudas no ocupados en el chip. - Enjuague chip con agua y remojar en agua durante 5 minutos.
- Preparar 15 g / ml de solución de anticuerpo anti-rhGH y solución de control negativo de anti-inmunoglobulina G (IgG anti-) y añadir 10 l de cada solución de anticuerpo a un pocillo en la placa de 384 pocillos.
- Diseñar el patrón de manchas en el microarrayer (4 x 7 cuadrantes para cada muestra) y el chip lugar con anticuerpos usando un 500 micras con punta de teflón pin.
- Incubar chip de manchado durante 2 horas a RT y bajo una atmósfera húmeda de 75% o mayor.
- Enjuague y disfrutar de chips en agua durante5 minutos. Entonces, viruta seca con corriente de nitrógeno.
3. SPRI Configuración Experimento y bloqueo
- Inicializar el instrumento y seleccione el directorio. Seleccione la cámara en tiempo real y empezar la bomba de jeringa a 1 ml / min durante 10 ml de agua desgasificada. Inserte el chip en el instrumento y mantener la inyección de agua hasta que se eliminen todas las burbujas.
- Después de aclarar chip con 10 ml de agua, iniciar la adquisición de imágenes, y siga cambiando el búfer de baja en sal PBS y permitir que se ejecute a 1 ml / min durante 5 ml y caudal a continuación lenta hasta 20 l / min durante 20 min .
- Seleccione la imagen de alto contraste, que muestra los anticuerpos inmovilizados manchado en el chip.
- Seleccionar y definir las 400 micras manchas circulares individuales correspondientes a los anticuerpos inmovilizados.
- Después de que el instrumento traza las curvas de plasmones, elegir un ángulo de trabajo que tiene la mayor inclinación en las curvas de reflectividad.
- El flujo de un tampón de desarrollo a 20 l / min de s bajosalt PBS a través del sistema hasta que la señal de todos los puntos seleccionados se estabilice.
- Cargar el BSA (100 mg / ml) en tampón en el bucle de muestra (150 l) con la válvula de inyección en la posición de carga. Luego cambiar la válvula a la posición de inyección para inyectar la solución a la celda de flujo.
Nota: BSA se inyecta para unirse covalentemente a la superficie reactiva amina, los restantes no unido BSA se lave fuera de la superficie a través de enjuague buffer. - Inyectar 150 l de una solución de acetato de sodio 10 mM sobre la superficie y seguir por una inyección de 150 l de sal de alta PBS.
- Inyectar 150 l de etanolamina (1 mM) para desactivar la superficie reactiva amina.
- Inyectar 150 l de acetato de sodio 10 mM para lavar la superficie.
- A continuación, conmutar el funcionamiento de amortiguación de PBS con 50 mg / ml de BSA a un caudal de 250 l / min para un total de 5 ml.
Nota: 50 mg / ml de BSA se añade al tampón de ejecución para el bloqueo adicional del surpor la cara no covalentemente ocupando los sitios no específicos y esto se hace para reducir aún más la unión no específica de proteínas de suero a la superficie. - Caudal Cambiar a 5 l / min y deje que se estabilice durante 20 min.
4. Detección de SPRI de hormona de crecimiento humano
- Preparar una solución de una concentración conjunto de rhGH (30.000 pg / ml; 250 pg / ml; 25 pg / mL; 2,5 pg / ml y 0,25 pg / ml) en 10% de suero y se diluyeron en PBS que contenía 1 mg / ml de BSA.
- Preparar una solución 2: 1 mediante la adición de 1 l de biotina etiquetados anticuerpos de detección anti-rhGH (6 m) a 3 l de estreptavidina recubiertas cerca de puntos cuánticos infrarrojos (1 M) en un tubo de microcentrífuga de 0,5 ml y se incuba durante 30 min para el acoplamiento eficaz .
- Inyectar 150 l de la solución de hGH se dispararon suero humano en el bucle de inyección. Esto se traduce en un fuerte aumento de la señal seguida de una lenta gota a partir del suero unido no específicamente enjuagar la superficie.
- Una vez que el signoal estabiliza, lavar la superficie con una solución de cloruro de sodio 450 mM añadido al tampón de ejecución.
- Diluir la solución de anticuerpos de detección anti-rhGH y puntos cuánticos a una concentración de 10 nM (2: 1) con tampón (PBS con 50 mg / ml de BSA) y se inyecta en la célula de flujo.
5. Análisis de Datos SPRI
Nota: Después de la inyección de la rhGH claveteado suero humano y potenciador de punto cuántico, un aumento en el cambio de reflectancia produce debido al cambio amplificado de las curvas de plasmones. Esto da como resultado una imagen de diferencia que muestra una imagen en escala de grises en correlación con la señal de en el chip en.
- Importe los datos en un programa de análisis de datos. Trazar la señal de SPRI (% de reflectividad) frente al tiempo (s) y determinar la diferencia entre el anti-rhGH y puntos negativos anticuerpo de control después del lavado alta en sal.
6. Protocolo ELISA (Día 1)
- Almacene todos los componentes del ensayo incluyeron in el kit ELISA rhGH a 2-8 ° C. Esto incluye el anticuerpo anti-rhGH placas recubiertas así, estándares (0-5) en suero de oveja, los controles (1 y 2) en el suero humano, tampón de conjugado, (200x) tampón de lavado, cromógeno TMB (tetrametilbencidina) y dejar de reactivo.
- Configuración de los reactivos y seguir los métodos como se describe en el protocolo comercial kit ELISA.
- En primer lugar, permiten que el anticuerpo anti-rhGH recubierto de 96 pocillos calentar a TA antes de abrir el paquete de papel de aluminio.
- A continuación, retire el número deseado de tiras de 8 pocillos para el ensayo y vuelva a sellar el paquete de aluminio que contiene los pozos restantes y se almacena a 2-8 ° C.
- Preparar normas por reconstitución en 2 ml de agua destilada para estándar # 0, en 1 ml de agua destilada para los estándares (1-5), y en 1 ml de agua destilada para los controles (1 y 2). A continuación se muestra una tabla de las concentraciones correspondientes de las normas y los controles (Tabla 1):
| Normas | Concentración (ng / ml) |
| 0 | 0 |
| 1 | 0.17 |
| 2 | 0.94 |
| 3 | 2.63 |
| 4 | 10.4 |
| 5 | 26.9 |
| Control n ° 1 | 1,22 ± 0,33 ng / ml |
| Control nº 2 | 4,97 ± 1,25 ng / ml |
Tabla 1. Las concentraciones de los estándares y controles incluidos en el kit ELISA comercial.
- Preparar las muestras que se componen de la hormona rhGH en 10% de suero humano en las siguientes concentraciones (Tabla 2):
| Muestra | Concentración (ng / ml) |
| 1 | 0,025 |
| 2 | 0.2 |
| 3 | 0.5 |
| 4 | 2.5 |
| 5 | 10 |
| 6 | 30 |
Tabla 2. Las concentraciones de las muestras de rhGH preparados en 10% de suero.
- Añadir 50 l de cada estándar, control y muestra a cada pocillo (por triplicado). Selle los pocillos e incubar con las normas, controles y muestras de rhGH O / N a 4 ° C bajo agitación suave.
7. Protocolo ELISA (Día 2)
- Retirar la placa de la coctelera y deje que se caliente a temperatura ambiente (15 a 20 minutos) antes de proceder con el análisis.
- Retire el Anti-rhGH-HRP, tampón conjugado, tampón de lavado (200x), cromógeno TMB (tetrametilbencidina), und reactivo de parada de la nevera y deje de calentar a RT.
- Preparación de los reactivos: (de acuerdo con las especificaciones del fabricante)
- Diluir la Anti-rhGH-HRP 40x con el tampón conjugado. Preparar el tampón de lavado diluyendo 200x con agua destilada.
- Añadir 50 l de anti-rhGH-HRP en cada pocillo, sellar los pozos y se incuba a temperatura ambiente durante 30 minutos mientras se agita suavemente.
- Decantar la solución de los pozos e invierta la placa y toque seco sobre un papel absorbente. A continuación, añadir 200 l de tampón de lavado en cada pocillo.
- Decantar la solución de lavado y toque seco sobre un papel absorbente. Repita este paso 3 veces.
- Añadir 100 l de cromógeno en cada pocillo dentro de 15 min después de la etapa de lavado. Incubar durante 30 minutos a temperatura ambiente en la oscuridad mientras se agita suavemente. Las soluciones se vuelven de incoloro a azul.
- Añadir 100 l de la reactivo de parada en cada pocillo. Las soluciones se vuelven de azul a amarillo. Inmediatamente, lea ªe absorbancia de cada pocillo a 450 nm usando un lector de microplacas.
- Trazar la curva estándar para los estándares previstos (0-5). A continuación, trazar la densidad óptica de la rhGH en 10% las muestras de suero frente a la concentración de cada muestra.
Resultados
El rendimiento de SPRI y Nano-SPRI (SPRI empleando los NanoEnhancers) se comparó con ELISA para la detección de rhGH en un entorno complejo. Las diferencias en la configuración de estos métodos se describen aquí brevemente. Para SPRI (detección directa, la Figura 1), el anticuerpo de captura se inmoviliza sobre la superficie y luego se inyecta la muestra y la unión del analito a la superficie del sensor se mide directamente en tiempo real y de manera libre de etiquetas. Sin embargo, con Nano-SPRI (Figura 1), después de que el analito se une a la superficie del sensor, una inyección consecutiva se sigue con puntos cuánticos recubiertas con anticuerpos de detección para amplificar la señal SPRI.
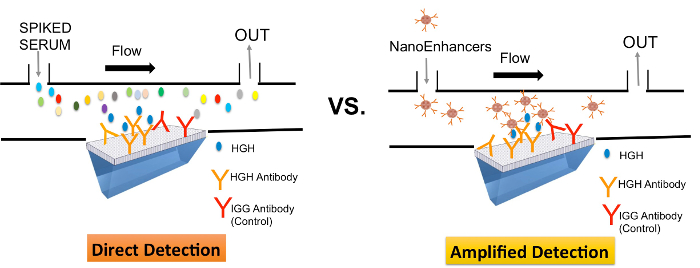
Figura 1. Representación esquemática comparar en modo directo (SPRI) y en modo amplificado (Nano-SPRI) de detección de rhGH en c muestras groseros. ligandos (rhGH o anticuerpos IgG específicos) se inmovilizaron en un formato de matriz en el biochip SPRI. Proteína diana (rhGH) se disparó en el suero humano introducido en la superficie del sensor se detectan directamente (SPRI) y secuencialmente destaca con NanoEnhancers (Nano-SPRI). Haga clic aquí para ver una versión más grande de esta figura.
En cuanto a ELISA, las placas de múltiples pocillos llegan ya pre-funcionalizados con anticuerpo de captura y luego la muestra se introduce, el analito de interés se unirán. Un anticuerpo de detección se introduce seguido de la adición de sustrato. La densidad óptica se mide a continuación a 450 nm. En este estudio, se utilizó un kit ELISA comercial (Figura 2) para medir la rhGH se disparó en el 10% de suero humano.
8 / 53508fig2.jpg "/>
Figura 2. Una representación esquemática del procedimiento de ensayo ELISA. proteína rhGH (óvalos azules) se introduce a los pocillos que han sido pre-funcionalizados con anticuerpos monoclonales (amarillo) específicas para rhGH. Las interacciones no específicas se eliminan por lavado los pocillos con tampón de lavado seguido por la introducción de un anticuerpo de detección prefuncionalizado con peroxidasa de rábano (HRP, púrpura). La solución cambiará de color después de añadir el sustrato tetrametilbenzidina (TMB, oro). Por favor, haga clic aquí para ver una versión más grande de esta figura.
La Figura 3 representa la curva de titulación de rhGH se disparó en 10% de suero humano y se representa frente a la DO obtenida a 450 nm. Se observó una buena respuesta lineal y el límite de detección se determinó que era 1 ng / ml. El coeficiente de variation (CV) fue de 6.5% lo que sugiere una buena reproducibilidad.
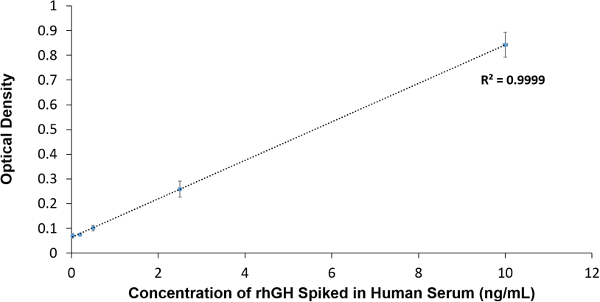
Figura 3. Análisis de datos de ELISA. Concentración de rhGH se disparó en el suero se traza contra la DO obtenida a 450 nm. Por favor haga clic aquí para ver una versión más grande de esta figura.
A continuación, la detección de rhGH enriquecida en el suero humano se evaluó con SPRI. La detección directa de rhGH resultó con la curva de gradiente de concentración correspondiente (Figura 4), cada punto representa el valor medio de la diferencia de reflectividad calculada a partir de tres curvas cinéticas SPRI para cada concentración. El límite de detección (LOD) se determinó que era 3,61 ng / ml. El ensayo de detección directa SPRI era altamente reproducible como el CV del ensayofue sólo del 4,1%.
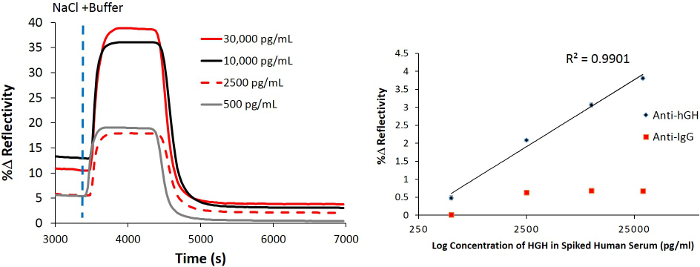
Figura 4. directa SPRI detección de la hGH se disparó en 10% de suero humano. La trama normalizado SPRI cinética resultante después de la inyección de varias cantidades de la hGH se disparó en el suero humano seguido por la inyección de un tampón de alto contenido de sal (línea vertical discontinua) para eliminar la no interacciones específicos de. Una curva de gradiente de concentración que representa la unión de diversas cantidades de la hGH se disparó en el suero humano a la superficie del sensor que se ha prefuncionalizado con biotina-hGH específicos de anticuerpos. Por favor haga clic aquí para ver una versión más grande de esta figura.
Para aumentar la sensibilidad del biosensor SPRI, NanoEnhancers (puntos cuánticos pre-funcionalizados con anticuerpos de detección) se secuencialmente enintrodujo a la superficie del sensor con el fin de destacar la presencia de rhGH pinchos en suero humano. Después de sustracción de fondo, los NanoEnhancers fueron capaces de amplificar la respuesta biosensor hasta el 7,9%, sin embargo, con el cambio de señal mínima (inmunoglobulina G (IgG) anticuerpo específico de, cambio de 0,38% en la reflectividad; Figura 5 en regiones controladas de interés de imágenes de. la superficie del sensor reveló que sólo las regiones de interés que tienen anticuerpos rhGH específicos inmovilizados experiencia el mayor cambio contraste corroborar directamente con la respuesta sensograma cinética.
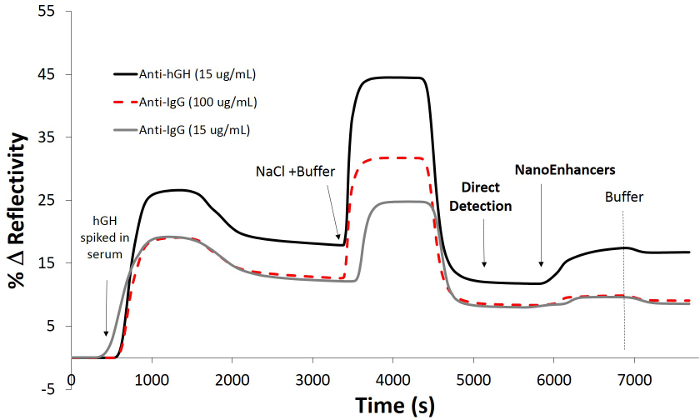
Figura 5. Detección de rhGH usando un ensayo de sándwich de pinchos en 10% de suero humano. SPRI parcela cinética después de la inyección de rhGH (30 ng / ml) en tampón (PBS 10 mM, cloruro sódico 150 mM, pH = 7,4) sobre una pre chip de -functionalized con ácido 11-mercaptoundecanoico / rhGH-anticuerpo específico y controlar IgG-anticuerpo después se bloquearon con BSA seguido de la adición de detección de anticuerpos recubiertos de puntos cuánticos (NanoEnhancers). Haga clic aquí para ver una versión más grande de esta figura.
Para demostrar la viabilidad del biosensor Nano-SPRI, se evaluó el rango de medición de rhGH en muestras de crudo. Un rango de trabajo ampliado de 30.000 pg / ml a 0,25 pg / ml dio lugar como una respuesta a la adición de NanoEnhancers (Figura 6). Vale la pena señalar que cada punto de la curva de titulación se promedia a partir de tres experimentos independientes. En consecuencia, se calculó el límite inferior de detección para ser 9,20 pg / ml y el coeficiente de variación fue de 20%.
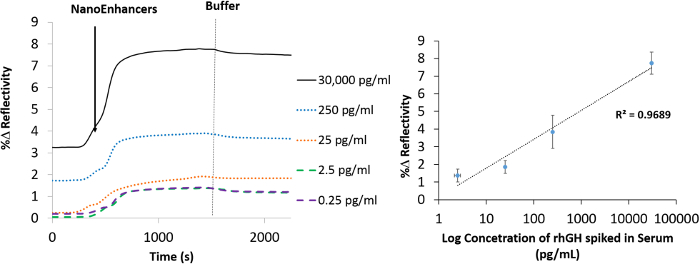
La Figura 6.Detección de Nano-SPRI de la hGH se disparó en el suero humano. Normalizada SPRI representación gráfica cinética de señal amplificada puntos cuánticos-hGH_specific_Anti de muestras de suero humano disparó con diferentes concentraciones de hGH. Una línea vertical discontinua (gris) representa el punto de la memoria intermedia de funcionamiento de la inyección. (b) Una curva de gradiente de concentración que representa la unión de NanoEnhancers (hGH_specific_Anti-puntos cuánticos) después de la inyección de varias cantidades de la hGH se disparó en suero humano a la superficie del sensor que ha sido prefuncionalizado con el anticuerpo de ácido 11-mercaptoundecanoico / hGH-específica. Por favor, haga clic aquí para ver una versión más grande de esta figura.
A continuación, se comparó el cambio que se produce en la curva de reflectividad SPR como una función de la concentración entre el directo y el método de bioensayo NanoEnhancer (Figura 7). Para el de directatécnica de protección entre 25 y 0,25 pg / ml, la señal comenzó a estabilizarse y esto no es sorprendente, ya que estas concentraciones están por debajo del límite de detección de 3 ng / ml (Figura 7). Del mismo modo, para la técnica de amplificación, concentraciones por debajo del límite de detección de la señal / ml 9,2 pg comenzaron a meseta y mostraron prácticamente sin variación.
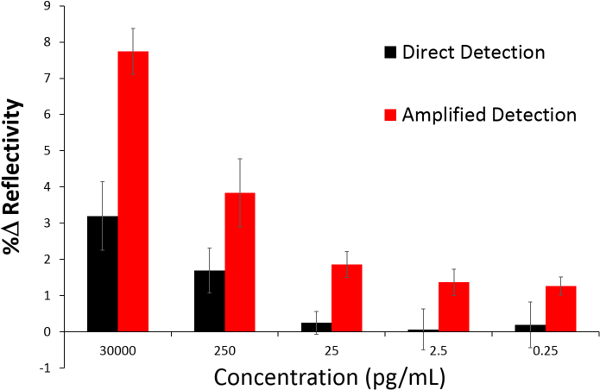
Figura 7. Un análisis comparativo de SPRI con Nano-SPRI. Este gráfico de barras representa el porcentaje de cambio en la reflectividad (% R) después de la introducción de rhGH enriquecida en el suero humano (detección directa), seguido por la inyección de NanoEnhancers (detección amplificada) para 30.000 pg / ml, 250 pg / ml, 25 pg / ml, 2,5 pg / ml y 0,25 pg / ml. Haga clic aquí para ver una versión más grande de esta figura.
Además, se evaluó la especificidad del biosensor Nano-SPRI. Similar a la insulina factor de crecimiento 1 (IGF-1) se disparó en el suero humano se inyectó como control ya que la hGH estimula la secreción de IGF-1 a través del receptor de la hormona de crecimiento en la membrana de los hepatocitos. Después de la inyección de la IGF-1 en el suero, los NanoEnhancers se inyectaron secuencialmente y la respuesta de la señal SPR no mostraron ninguna unión específica (Figura 8). Sin embargo, cuando se disparó rhGH en muestra de suero se inyectó al mismo lugar funcionalizado con anticuerpo rhGH, se observó aumento de la señal. En conclusión, la plataforma Nano-SPRI ha demostrado una excelente especificidad y selectividad para rhGH.
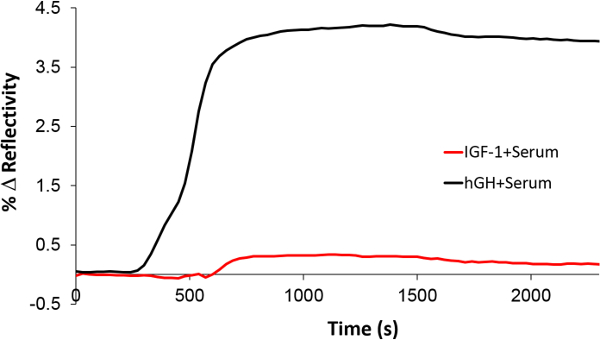
Figura 8. Evaluación de la Nano-SPRI selectividad hacia rhGH. La respuesta biosensor Nano-SPRI después de la inyección de rhGH (negro) y el IGF-1 (roja) en ssuero piked. Haga clic aquí para ver una versión más grande de esta figura.
Se realizó un análisis de correlación mediante el coeficiente de correlación de Pearson para determinar la correlación entre la intensidad de la señal SPRI y valores de densidad óptica de ELISA (Figura 9). Un valor de p <0,01 fue considerado significativo. Como se ilustra en este gráfico, hay una buena correlación entre los niveles de rhGH en suero humano con púas medidos por SPRI y ELISA. El valor r fue 0,9263 durante 9 muestras diferentes.
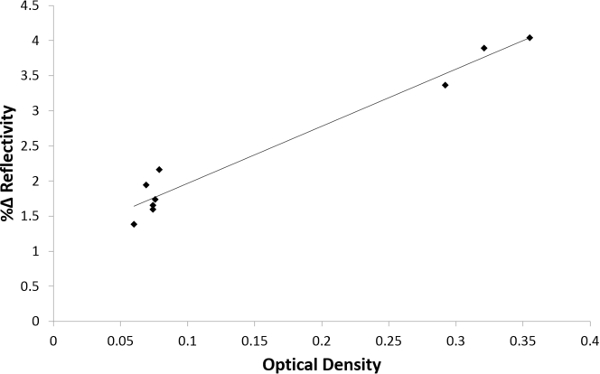
Figura 9. análisis de correlación de Pearson entre ELISA y Nano-SPRI. La trama se correlaciona intensidad de la señal de Nano-SPRI (eje y) con la densidad óptica ELISA (eje x) valores. (Perasel coeficiente de correlación n = 9, r = 0,9263, p = 0,00000183). Haga clic aquí para ver una versión más grande de esta figura.
La constante de disociación en equilibrio (K D) se determinó utilizando el software GraphPad para ELISA. El valor calculado K D fue de aproximadamente 79 nM (Tabla 3). Los de (Ka) y desactivación (K d) las tasas no se pudo determinar por ELISA. Sin embargo, utilizando el software de análisis de datos, el método de detección directa con K dio como resultado el valor D de 23 pM usando la masa molecular de 22 kDa que corresponde a una molécula de rhGH. El encendido y apagado tasas se calcularon para ser 6.1 x10 7 M -1 s -1 y 1,33 x 10 -3 s -1, respectivamente. Esto se traduce inherentemente que 0.13% de la rhGH y anticuerpo desintegración por segundo. En cuanto a la unamplified SPRI experimento, se observó una interacción global más fuerte entre NanoEnhancers y rhGH como la afinidad de unión calculada se determinó que era 16:03. Además, se observó una tasa de asociación más fuerte para NanoEnhancers y rhGH que el anticuerpo de captura / rhGH, sin embargo la tasa de disociación sugiere que 0,26% de NanoEnhancer / rhGH / Captura de decaimiento anticuerpo por segundo.
| Método | K D (Affinity) | K a (tasa on-) | K d (off-rate) | LOD |
| ELISA | 79,45 x 10 -9 M | N / A | N / A | 1 ng / ml |
| SPRI | 23,2 x 10 -12 M | 6,1 x 10 7 M -1 s -1 | 1.33 x10 -3 s -1 | 3,61 ng / ml |
| Nano-SPRI | 4,33 x 10 -12 M | 7.54 x10 8 M -1 s -1 | 2.62 x10 -3 s -1 | 0,0092 ng / ml |
Tabla 3. análisis de datos cinética completa. Evaluación de la afinidad, on-off-tasa y tasa de las respuestas de anticuerpos utilizando GraphPad (ELISA) y análisis de datos software (SPRI y Nano-SPRI). Se eligió La determinación de la avidez usando la masa molecular de 22 kDa que corresponde a una molécula de rhGH. Los límites de detección se determinaron para los tres estudios que utilizan Excel.
Discusión
Niveles irregulares de hGH, una hormona natural, se han relacionado con numerosos trastornos médicos que afectan el crecimiento y el desarrollo humano. Por otra parte, la administración exógena de rhGH es comúnmente utilizado por los atletas, a pesar de que está prohibido, como un agente de dopaje para mejorar su rendimiento. Desafíos en la detección de mal uso rhGH resultado de la dificultad de distinguir exógena de hGH de forma endógena. Como tal, la técnica actual aprobado para la detección de la hGH exógena se basa en la medición de la relación de la hGH de 22 kDa isoforma en relación con la isoforma 20 kDa. Dado que las demandas de prueba isoforma para la medición de múltiples isoformas de hGH simultáneamente dentro de un corto período de tiempo en un amplio rango de concentraciones, por lo tanto, hemos considerado la plataforma SPRI como una combinación perfecta. Además, el nivel de la hGH endógena fluctuar a un nivel muy bajo (0,03 ng / ml) en el torrente sanguíneo, por tanto, el sistema de detección debe ser capaz de medir esta gama cómodamente con alta specificity. Como resultado de ello, que también investigó en este estudio el potencial de las nano-SPRI como una herramienta de diagnóstico para la hGH y comparamos directamente con SPRI y el inmunoensayo ELISA clásica.
Basándose en los resultados obtenidos de este estudio, la principal ventaja del método SPRI y Nano-SPRI es que las concentraciones de rhGH se pueden medir de una manera más rápida en comparación con el método más convencional ELISA. Una duración estándar para medir los niveles de rhGH en una muestra con el método de detección directa era 1 hr mientras que el Nano-SPRI requiere 2 hr debido a los pasos adicionales en el proceso. En general, con SPRI y Nano-SPRI experimentos, antes de la inyección de una muestra, es muy recomendable un paso de calibración. Además, la inyección de una muestra bruta como resultados de suero humano en algunas interacciones no específicas, como consecuencia, es imperativo para inyectar un tampón de lavado de alta sal a sólo revelan interacciones específicas. También vale la pena señalar que una etapa de lavado es absolutamente necesariodespués de la introducción de bloquear las moléculas a la superficie del sensor, para eliminar las moléculas no unidas. En cuanto a los requisitos de tiempo de ELISA son mucho mayores (~ 16-18 de hr) para el análisis de una muestra. Se necesita un tiempo de incubación más largo que la sensibilidad del ensayo es mejorada especialmente para este estudio, ya que el objetivo era comparar el límite inferior de detección.
La elección de la química de superficie puede variar de una aplicación a otra y esto podría ser realizado como una de la limitación de la técnica de SPRI. En este estudio, se evaluaron una amplia gama y combinación de enlazadores químicos y moléculas de bloqueo para alcanzar la combinación correcta con el fin de observar la eficiencia de unión óptima de rhGH a la superficie del sensor. Por ejemplo, en este estudio, la combinación de BSA y PEG sirvió bien en la minimización de las interacciones no específicas. Sin embargo, en un estudio previo 17, en el que el ligando de captura fue un aptámeros, PEG solo sirvió como la mejor molécula de bloqueo. Las variablesque la eficiencia afectar a la unión del analito a ligando también son dependientes de pH, tampón y temperatura. Por lo tanto, con cualquier aplicación, estas variables deben ser optimizado. Además, es crítico para determinar la concentración óptima manchado del ligando a la superficie del chip. Un experimento de valoración con un intervalo de concentraciones de ligandos inmovilizados se realiza antes de iniciar el estudio. En cuanto a ELISA, un paso crucial en el procedimiento fue decantar el tampón de lavado de los pozos tocando la microplaca ya que esto garantiza ningún líquido residual es de sobra. Extracción del tampón de lavado con pipeta no era suficiente como cualquier líquido residual interfirió con la lectura de la señal de la muestra objetivo.
En referencia a la sensibilidad, ELISA (1 ng / ml) es comparable a SPRI (3,61 ng / ml), pero nano-SPRI (9,20 pg / ml) mejora la sensibilidad por tres órdenes de magnitud, lo que permite mediciones en los niveles biológicos inferiores de rhGH 0,03 ng / ml. Como ya se informó 16,17, la mejora de la señal impartida por el NanoEnhancers se atribuye a un efecto de carga masiva y el fuerte acoplamiento que existe entre fluoróforos NIR y propagan plasmones de superficie de nanoestructuras de cine de oro. A pesar de que, Nano-SPRI agrega un paso adicional para el procedimiento, este nivel de sensibilidad puede ampliar las aplicaciones de la tecnología de SPRI en diversos puntos de venta.
SPRI ofrece a los científicos un perfil cinético completo (K D, K a y K d) de anticuerpo / interacción rhGH mientras que ELISA puede informar sólo los valores de afinidad. El coeficiente de variación (CV) fue inferior a 10% para SPRI (4,1%) y ELISA (6,5%), lo que sugiere una buena reproducibilidad. Los valores de afinidad ELISA y SPRI son diferentes debido a que los anticuerpos de captura inmovilizados en el chip sensor son diferentes de anticuerpos inmovilizados en la placa de 96 pocillos ELISA. En cuanto a Nano-SPRI se observó un valor CV más alto (20%). Existen varios parámetros que pueden contribuir como fuente de erroRS CV determinación. Por ejemplo, con el experimento Nano-SPRI se está midiendo una concentración mucho más baja de analito, la adición de NanoEnhancers añade otro paso en el procedimiento y el experimento se realizó manualmente. Una muy buena correlación entre Nano-SPRI y ELISA se logró para la detección de rhGH en suero humano púas. Finalmente, ELISA puede ser una técnica fiable sin embargo, el método en sí es mucho tiempo que hace que sea difícil de utilizar en situaciones que requieren monitorización en tiempo real y la multiplexación, como es el caso con hGH. Además, una característica más atractiva que no se investigó directamente en este estudio que SPRI ofrece más de ELISA, es la capacidad de medir cientos de interacciones simultáneamente en tiempo real. Por lo tanto en el futuro, el método Nano-SPRI será evaluado para detectar múltiples biomarcadores simultáneamente en tiempo real (Multiplexing) presentes en el suero a diversas concentraciones con el fin de examinar su potencial como herramienta de diagnóstico clínico viable.
Divulgaciones
M.G. Sandros is a consultant for Horiba Scientific. She has received honoraria for participation in oral presentations from: Horiba Scientific and Syngenta. The authors have no other relevant affiliations or financial involvement with any organization or entity with a financial interest in or financial conflict with the subject matter or materials discussed in the manuscript apart from those disclosed. No writing assistance was utilized in the production of this manuscript
Agradecimientos
NanoManufacturing Innovation Consortium for funding support.
Materiales
| Name | Company | Catalog Number | Comments |
| Somatotropin Growth Hormone (GH1) capture antibody | Acris Antibodies | DM1015 | |
| Bovine Serum Albumin | Fisher Bioreagents | BP671-10 | |
| Biotin labeled Somatotropin Growth Hormone (GH1) detection antibody | Acris Antibodies | AM09304BT-N | |
| 1-ethyl-3-(3-dimethylaminopropyl) carbodiimide | TCI America | D1601 | |
| Ethanolamine | Acros Organics | 141-43-5 | |
| Ethanol | Fisher Chemicals | BP2818-4 | |
| Human HGH ELISA Kit | invitrogen | KAQ1081 | |
| Human Serum | Sigma Aldrich | H4522 | |
| Rabbit IgG Antibody | Sigma Aldrich | I5006 | |
| 11-mercaptoundecanoic acid | Sigma Aldrich | 450561 | |
| Nanostrip | Cyantek | ||
| N-hydroxysuccinimide | Sigma Aldrich | 130672 | |
| Phosphate Buffer Saline | Invitrogen | 00-3002 | |
| Polyethylene glycol (800 Da) | Sigma Aldrich | 729108 | |
| Recombinant Human Growth Hormone | Calbiochem | 869008 | |
| Sodium Acetate | Sigma Aldrich | 127-09-3 | |
| Sodium Chloride | Fisher Chemicals | 7647-14-5 | |
| Streptavidin coated near infrared quantum dots | Life Technologies | Q10171MP | |
| UV/Ozone Procleaner | Bioforce Nanosciences | ||
| Microwave reactor | CEM Corporation | Discover system | |
| SPRi-Arrayer | LabNext Xactll Microarray System | ||
| SPR biochip | HORIBA | ||
| SPRi-Lab+ | HORIBA | ||
| Synergy Mx Multimode Microplate reader | BioTek | ||
| ScrubberGen | HORIBA | Data Analysis software |
Referencias
- Popii, V., Baumann, G. Laboratory measurement of growth hormone. Clinica Chimica Acta. 350 (1-2), 1-16 (2004).
- Higham, C. E., Trainer, P. J. Growth hormone excess and the development of growth hormone receptor antagonists. Exp Physiol. 93 (11), 1157-1169 (2008).
- Sönksen, P., Salomon, F., Cuneo, R. Metabolic effects of hypopituitarism and acromegaly. Horm Res. 36, 27-31 (1991).
- Molitch, M., et al. Evaluation and Treatment of Adult Growth Hormone Deficiency: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 91 (5), 1621-1634 (2006).
- . . The World Anti-Doping Code: The 2015 Prohibited List International Standard. , (2015).
- . . The 2014 prohibited list world anti-doping code. , (2014).
- Langkamp, M., Weber, K., Ranke, M. B. Human growth hormone measurement by means of a sensitive ELISA of whole blood spots on filter paper. Growth Horm IGF Res. 18 (6), 526-532 (2008).
- Rich, R. L., Myszka, D. G. Survey of the year 2007 commercial optical biosensor literature. J Mol Recognit. 21 (6), 355-400 (2008).
- Homola, J. Present and future of surface plasmon resonance biosensors. Anal Bioanal Chem. 377 (3), 528-539 (2003).
- Hoa, X. D., Kirk, A. G., Tabrizian, M. Toward Integrated Surface Plasmon Resonance Biosensors: A Review of Recent Progress. Biosens Bioelectron. 23 (2), 151-160 (2007).
- de Juan-Franco, E., Rodrìguez-Frade, J. M., Mellado, M., Lechuga, L. M. Implementation of a SPR immunosensor for the simultaneous detection of the 22K and 20K hGH isoforms in human serum samples. Talanta. 114, 268-275 (2013).
- de Juan-Franco, E., Caruz, A., Pedrajas, J. R., Lechuga, L. M. Site-directed antibody immobilization using a protein A-gold binding domain fusion protein for enhanced SPR immunosensing. Analyst. 138 (7), 2023-2031 (2013).
- Du, H., et al. Immunological screening and characterization of highly specific monoclonal antibodies against 20 kDa hGH. Bioanalysis. 4 (17), 2161-2168 (2012).
- Treviño, J., Calle, A., Rodrìguez-Frade, J. M., Mellado, M., Lechuga, L. M. Surface plasmon resonance immunoassay analysis of pituitary hormones in urine and serum samples. Clin Chim Acta. 403 (1-2), 56-62 (2009).
- Wu, Z., Bidlingmaier, M., Dall, R., Strasburger, C. J. Detection of doping with human growth hormone. Lancet. 353 (9156), 895 (1999).
- Malic, L., Sandros, M. G., Tabrizian, M. Designed biointerface using near-infrared quantum dots for ultrasensitive surface plasmon resonance imaging biosensors. Anal. Chem. 83 (13), 5222-5229 (2011).
- Vance, S. A., Sandros, M. G. Zeptomole Detection of C-Reactive Protein in Serum by a Nanoparticle Amplified Surface Plasmon Resonance Imaging Aptasensor. Sci. Rep. 4 (5129), 1-7 (2014).
- Uludag, Y., Tothill, I. E. Cancer biomarker detection in serum samples using surface plasmon resonance and quartz crystal microbalance sensors with nanoparticle signal amplification. Anal. Chem. 84 (14), 5898-5904 (2012).
- Špringer, T., Homola, J. Biofunctionalized gold nanoparticles for SPR-biosensor-based detection of CEA in blood plasma. Anal Bioanal Chem. 404 (10), 2869-2875 (2012).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados