Method Article
La neuraminidasa Ensayo de inhibición basado en la fluorescencia para evaluar la susceptibilidad de los virus de la influenza a El Inhibidor de la neuraminidasa clase de antivirales
En este artículo
Resumen
Se describe el uso de un ensayo de inhibición de la neuraminidasa basada en fluorescencia fenotípico para evaluar la susceptibilidad de los virus de influenza A y B a la clase de inhibidor de la neuraminidasa de los antivirales.
Resumen
Los inhibidores de la neuraminidasa (NA) son la única clase de antivirales aprobados para el tratamiento y profilaxis de la gripe que son eficaces contra las cepas que circulan actualmente. Además de su uso en el tratamiento de la gripe estacional, los inhibidores de NA han sido almacenadas por un número de países para uso en el caso de una pandemia. Por tanto, es importante controlar la susceptibilidad de los virus circulantes de la gripe a esta clase de antivirales. Hay diferentes tipos de ensayos que se pueden utilizar para evaluar la susceptibilidad de los virus de la gripe a los inhibidores de la NA, pero los ensayos de inhibición de la enzima usando un sustrato fluorescente o un sustrato quimioluminiscente son los más ampliamente usado y recomendado. Este protocolo describe el uso de un ensayo basado en fluorescencia para evaluar la susceptibilidad del virus influenza a los inhibidores de NA. El ensayo se basa en la enzima NA escindir el 2 '- (4-metilumbeliferil) -α-D- ácido -acetylneuraminic N (Munana) Sustrato para liberar el producto fluorescente 4-metilumbeliferona (4-MU). Por lo tanto, el efecto inhibidor de un inhibidor de NA en el virus de la gripe NA se determina basándose en la concentración del inhibidor de NA que se requiere para reducir el 50% de la actividad de NA, dada como un valor de CI50.
Introducción
La hemaglutinina (HA) y neuraminidasa (NA) son los dos principales glicoproteínas de superficie de influenza virus A y B. HA se une al ácido siálico-galactosa de las glicoproteínas de la superficie celular o glicolípidos, mientras que la NA libera virus mediante la escisión del ácido siálico de la galactosa sobre la superficie celular 1. Los inhibidores de la NA son una clase de antivirales contra la influenza que fueron racionalmente diseñados para unirse fuertemente al sitio activo NA enzimática, lo que impide la liberación y la propagación de la progenie de virus. Oseltamivir y zanamivir son dos inhibidores de la NA que han sido aprobados en muchos países en todo el mundo para el tratamiento y profilaxis de la gripe. En los últimos años, dos inhibidores adicionales NA, peramivir y Laninamivir, han sido aprobados para su uso en un número limitado de países. Proyección de virus de la gripe para la susceptibilidad a inhibidores de NA y la identificación de mutaciones que confieren resistencia son importantes en la determinación y el control de la effectiveness de esta clase de antivirales.
En los últimos 16 años, el ensayo de inhibición de NA basado en la fluorescencia ha sido realizada de forma rutinaria en el Centro Colaborador para Referencia e Investigación sobre la Gripe, Melbourne (Melbourne WHOCCRRI) para supervisar el cambio de tendencia de la susceptibilidad antiviral entre los virus de influenza circulante. Anualmente, más de 2.000 virus de la gripe se prueban para la susceptibilidad antiviral. En la mayoría de las temporadas de gripe,> 98% de los virus son sensibles a los cuatro inhibidores de la NA 2, 3, 4, aunque durante la temporada hemisferio norte influenza 2007-2008, hubo un aumento en el número de ex virus estacionales A (H1N1) que habían reducido la susceptibilidad a oseltamivir 5. Este grupo de virus, que contenía el H275Y sustitución de aminoácidos NA, se extendió al resto del mundo a finales de 2008, haciendo inappropri oseltamivircomió a nivel mundial para el tratamiento de este virus. La gran mayoría de los virus influenza B, influenza A (H3N2) y la influenza A (H1N1) cepas pdm09 son susceptibles a oseltamivir, aunque grupos de comunidades de A (H1N1) variantes pdm09 que contienen el H275Y sustitución de aminoácidos NA que confiere oseltamivir reduce y susceptibilidad peramivir, se han reportado en diversas partes del mundo, 6, 7.
Debido a la necesidad de un suficientemente alto título de virus, los especímenes clínicos (incluyendo los lavados nasales de los animales) se deben a pases en cultivo celular, ya sea o huevos de pollo antes de la prueba de susceptibilidad antiviral embrionados. El ensayo de inhibición de NA descrito en este artículo se puede dividir en tres secciones:
La determinación de la gama lineal para el producto fluorescente 4-metilumbeliferona (4-MU) en un fluorómetro en particular
Debido a las diferencias inherentes entre fluorómetros, tél intervalo lineal para el producto final fluorescente, 4-MU, y la unidad de fluorescencia relativa (RFU), necesita ser establecido. Una vez establecido el intervalo lineal para 4-MU, se selecciona la señal objetivo óptimo, a la que se ajusta la concentración de los virus de la gripe en el ensayo de actividad de NA. Una vez completado para un fluorómetro particular, esto no debería ser necesario repetir.
La determinación de la actividad de NA de los virus
El ensayo de actividad de NA es un ensayo simple que implica la adición de la 2 '- (4-metilumbeliferil)-D- -α N ácido -acetylneuraminic (Munana) de sustrato a los virus diluido en serie. La cantidad de fluorescencia del producto final 4-MU generada a partir de la escisión de Munana por la NA se mide usando un fluorómetro. La dilución de virus apropiado para utilizar en el ensayo de inhibición de NA se selecciona mediante el trazado de unidades de fluorescencia frente a la dilución de virus. De la curva sigmoidal producido, el punto medio de la sección lineal debe corresponder ael intervalo lineal 4-MU del fluorómetro determina en el apartado 1 e informará a la concentración apropiada de virus para ser utilizado en la sección 3.
La evaluación de la susceptibilidad del virus a los inhibidores de NA utilizando el ensayo de inhibición de NA
Para evaluar la susceptibilidad de los virus a un inhibidor de NA en particular, los virus a la dilución determina en el apartado 2 se incuban con una gama de concentraciones de inhibidor de NA. Después de una incubación posterior con Munana, el 4-MU generada por virus no inhibidas se mide en RFU por el fluorómetro. El efecto inhibidor del inhibidor de NA sobre la actividad enzimática de NA de un virus se calcula de acuerdo a la concentración de inhibidor NA requerida para reducir el 50% de la actividad de NA, dada como un valor de CI50.
Protocolo
1. Determinación del rango lineal del producto fluorescente 4-MU en un fluorómetro
- Preparar 10 ml de mM 4-MU solución madre de 6,4 disolviendo 11,3 mg de 4-MU en 5 ml de etanol absoluto. Añadir 5 ml de NaCl al 0,9% (w / v) a la solución madre para hacer 10 ml. Preparar una 640? M de solución de trabajo diluyendo 1 ml de 6,4 mM 4-MU en 9 ml de 1x tampón de ensayo (ácido 33,3 mM de ácido 2- (N-morfolino) etanosulfónico (MES) y CaCl2 4 mM, pH 6,5).
NOTA: Preparar el tampón de ensayo 2x mediante la adición de 13 g de MES y 8 ml de 1 M CaCl2 para 992 ml de agua destilada. Ajustar el pH a 6,5 usando 10 M de NaOH. Filtrar el tampón utilizando un filtro de acetato de celulosa estéril de tamaño de poro 0,2 m. ¡Precaución! El hidróxido de sodio es cáustico y puede causar quemaduras químicas en la piel y los ojos. Asegúrese de que el equipo de protección personal completo está desgastado. - Preparar 5 ml de una gama de concentraciones de 4-MU (es decir, 5? M, 10? M, 20? M, 40? M, 80? M, 160 & #181; M, y 320? M) a través de una dilución en serie de dos veces de 640? M 4-MU usando tampón de ensayo 1x.
- Dispensar 50 l de cada dilución en serie de 4-MU (es decir, 5? M, 10? M, 20? M, 40? M, 80? M, 160? M, 320? M y 640? M) (dos pocillos por dilución) en un claro, 96- así placa de fondo plano y 50! l de tampón de ensayo 1x en los pocillos restantes (que sirven como espacios en blanco para medir señales de fondo).
NOTA: Las concentraciones finales de 4-MU en el volumen de reacción (50! L 4-MU + 50! L 300 mM Munana) son 2,5 M, 5 M, 10? M, 20? M, 40? M, 80? M, 160? M y 320? M . - Preparar una mM MUNANA solución madre de 2,5 mediante la reconstitución de 25 mg de Munana en 20 ml de agua destilada. Mezclar 0,72 ml de Munana 2,5 mM con 5,28 ml de 1x tampón de ensayo para obtener un 300? M Munana solución de trabajo (volumen suficiente para una placa). Cubrir el tubo que contiene la Munana workin 300 Mg de solución con papel de aluminio y mantenerlo en hielo si no se utiliza inmediatamente. Descarte cualquier materiales sobrantes.
NOTA: El mM MUNANA solución madre de 2,5 se puede almacenar a -20 ° C durante 1 mes y debe ser utilizado dentro del ciclo / descongelación uno congelación. Las 4-MU soluciones y Munana son sensibles a la luz y deben ser protegidos de la exposición a la luz prolongado. - Añadir 50 l de 300 Munana M a cada pocillo, golpee suavemente para mezclar, y se incuba a 37 ° C durante 30 min. Cubrir la placa con un sellador de placas para evitar la evaporación.
NOTA: Este paso es para tener en cuenta la fluorescencia de fondo en el ensayo de inhibición de NA. - Preparar la solución de parada mediante la mezcla de 11 ml de etanol absoluto con 2,225 ml de NaOH 0,824 M (volumen suficiente para una placa).
- Añadir 100! L de solución de parada a cada pocillo para detener la reacción y golpear suavemente para mezclar.
- Leer la placa usando un fluorómetro con un ajuste de longitud de onda de excitación de 355 nm y un ajuste de longitud de onda de emisión de 460 nm, como per las instrucciones del fabricante.
- Calcular la media de la señal de fondo usando señales de fluorescencia de todos los pocillos que no contienen 4-MU. Restar esta señal media de fondo de cada uno de los pocillos que contienen 4-MU y calcular las señales de promedio (RFU) para cada concentración de 4-MU. Trazar una curva estándar de RFU frente a la concentración de 4-MU (M), como se muestra en la Figura 1a; una sección lineal de primer plano de la curva se muestra en la Figura 1b.
- Visualizar la trama de RFU contra 4-MU concentración (M) para determinar el intervalo lineal y la señal objetivo óptimo; el intervalo lineal es donde la señal de fluorescencia aumenta en proporción al aumento de las concentraciones de la 4-MU en el terreno, mientras que la señal objetivo óptimo es una concentración de 4-MU arbitrario dentro del rango lineal.
NOTA: El intervalo lineal y la señal objetivo óptimo son-fluorómetro específico. Por ejemplo, el fluorómetro en el Melbourne WHOCCRRI tiene un rango lineal de 20,5 a 40? M 4-MU y una señal objetivo óptimo de ~ 30? M 4-MU, que corresponde a ~ 1.500 RFU.
2. La determinación de la actividad de NA de los virus
NOTA: Los virus de influenza son cultivadas a títulos suficientes en Madin-Darby Canine Kidney células (MDCK) o huevos de pollo embrionados 8.
- Dispensar 120 l por pocillo de virus de influenza en cultivo sin diluir en la columna 1 y 60! L de tampón de ensayo 1x que contienen 0,1% de NP-40 en las 11 columnas restantes de un de 96 pocillos, la placa de fondo en U.
- En serie realizar dilución de dos veces de los virus a través de la placa (es decir, la transferencia de 60! L de la columna 1 a la columna 2 y así sucesivamente, hasta la columna 11) usando una pipeta multicanal, sale de la columna 12 como un blanco que contiene tampón de ensayo solamente 1x.
- Transferir 50! L de cada uno de los pocillos (virus y espacios en blanco diluido) en un 96 pocillos, la placa transparente, de fondo plano.
NOTA: No es necesario cconsejos hange pipeta si los materiales se transfieren desde la columna 12 a través de a la columna 1. - Añadir 50 l de 300 mM Munana (preparado como en la etapa 1.4) por pocillo y golpear suavemente la placa para mezclar. Incubar la placa a 37 ° C durante 1 h. Cubrir la placa con un sellador de placas para evitar la evaporación.
- Añadir 100! L de solución de parada (preparado como en la etapa 1.6) por pocillo para terminar la reacción y golpear suavemente la placa para mezclar.
- Leer la placa usando un fluorómetro.
- Utilice un ajuste de la longitud de onda de excitación de 355 nm y un ajuste de la longitud de onda de emisión de 460 nm.
- Determinar la señal de fondo promedio basado en las lecturas de fluorescencia de la columna 12 y restar la señal de fondo promedio de cada pocillo. Trazar un gráfico de RFU frente a diluciones de virus.
NOTA: Los valores de fondo para 100 Munana M en el WHOCCRRI Melbourne son típicamente entre 50 y 120 RFU, pero estos serán diferentes dependiendo de la bei fluorómetrong utiliza. - Ver la trama de RFU contra diluciones de virus para determinar el punto medio de la sección lineal de la curva para cada virus (Figura 2). Utilice la señal objetivo óptimo (determinado en el paso 1) como el punto de referencia.
NOTA: Este debe corresponder con el intervalo lineal 4-MU del fluorómetro determina en el apartado 1 y proporcionará la concentración apropiada de virus para ser utilizado en la sección 3.
3. Estimación de la susceptibilidad Virus de NA inhibidores usando el Ensayo de inhibición de NA
- Preparar lotes maestros de inhibidores de NA a concentraciones de 300? M.
- Preparar 300 M zanamivir (peso molecular, PM = 332,32 g / mol) por disolución de 5,0 mg de zanamivir en tampón de ensayo 50 ml de 2x (MES 66,6 mM y 8 mM de CaCl2, pH 6,5).
- Preparar 300 M carboxilato de oseltamivir (D-tartrato; PM = 386,44 g / mol) por disolución de 5,8 mg en 50 ml de tampón de ensayo 2X.
- Preparar300? M peramivir trihidrato (PM = 382,45 g / mol) por disolución de 5,7 mg en 50 ml de tampón de ensayo 2X.
- Preparar 300 M Laninamivir (PM = 346,34 g / mol) por disolución de 5,2 mg en 50 ml de tampón de ensayo 2X.
NOTA: Los lotes maestros de inhibidor de NA se pueden almacenar a -20 ° C durante 12 meses. Compruebe el MW de los inhibidores de NA para asegurar los pesos y volúmenes correctos se utilizan en la reconstitución. El carboxilato de oseltamivir es el compuesto activo del fosfato profármaco oseltamivir. Por lo tanto, sólo el carboxilato de oseltamivir se debe utilizar en el ensayo de inhibición de NA.
- A partir de los lotes maestros, preparar stocks de diez veces diluciones en serie de los inhibidores de NA en 50 tubos de centrífuga mL trabajar a concentraciones de 0,03 nM, 0,3 nM, 3 nM, 30 nM, 300 nM, 3000 nM, y 30.000 nM en el ensayo de 2x tampón (MES 66,6 mM y 8 mM de CaCl2, pH 6,5); esto es para uso a través de múltiples ensayos.
NOTA: Las concentraciones finales de inhibidores de NA en la volum reaccióne (50? l de dilución de virus + 50 l de NA inhibidor + 50 l de 300 Munana M) son 0,01 nM, 0,1 nM, 1 nM, 10 nM, 100 nM, 1000 nM, y 10 000 nM, respectivamente. La concentración final no incluye los 100 l de solución de parada. Almacenar todos los inhibidores de diluciones de NA a 2-8 ° C. La fecha de caducidad es el mismo que el de los lotes maestros. - Preparar las diluciones de virus en tampón de ensayo 1x que contienen 0,1% de NP-40 tensioactivo en un bloque de 96 pocillos profundos. El uso de diluciones de virus a partir de los resultados del ensayo de actividad de NA derivados de la sección 2. Utilizar un volumen total de 2 ml por virus para probar cuatro inhibidores de NA.
NOTA: Preparar dos pozos (1 ml por pocillo) por virus en un bloque de 96 pocillos profundos. Ejemplos de diluciones de virus para el virus de 1, 2, y 3 se muestran en la Tabla 1. - Dispensar el volumen requerido de inhibidores de la NA (preparado como en la etapa 3.2) en un depósito 8 de pozo profundo. A partir de ahí, dispensar 50 l de inhibidores de la NA a diluciones que varían de 0 nM (2x ensayo bsolamente Uffer) a 30.000 nM en las filas A a H en una de 96 pocillos, la placa transparente, de fondo plano.
NOTA: La disposición de la placa se ilustra en la Figura 3. - Añadir 50 l de virus de ensayo diluidos por pocillo a las columnas 1-11 y 50 l por pocillo de tampón de ensayo 1x solamente a la columna 12. Golpear suavemente la placa para mezclar e incubar a temperatura ambiente durante 45 min. Cubrir la placa con un sellador de placas para evitar la evaporación.
- Añadir 50 l de 300 mM Munana (preparado como en la etapa 1.4) por pocillo y golpear suavemente la placa para mezclar. Incubar la placa a 37 ° C durante 1 h. Cubrir la placa con un sellador de placas para evitar la evaporación.
- Añadir 100! L de solución de parada (preparado como en la etapa 1.6) a cada pocillo y golpear suavemente la placa para mezclar.
- Leer la placa usando un fluorómetro.
- Utilice una longitud de onda de excitación de 355 nm y una longitud de onda de emisión de 460 nm, como se describe anteriormente.
4. Cálculo deLos valores de CI50
NOTA: El v1.2 JASPR es un software de ajuste de curvas que permite el cálculo de los valores de CI50. El software fue desarrollado por la División de Influenza de los CDC, Atlanta, EE.UU.. El software utiliza la ecuación: V = V max x (1 - ([I] / (K i + [I]))), donde V max es la tasa máxima de metabolismo, [I] es la concentración de inhibidor, V es la respuesta se inhibió, y K i es el IC 50 para la curva de inhibición.
- Copiar y pegar los datos en bruto que salen de la fluorómetro en una hoja de cálculo en un formato de placa de 12 columna (96 pocillos), a partir de la celda A1.
NOTA: Raw datos de cada placa posterior debe ser escalonada por una fila vacía. Si cada virus ha sido probado contra cuatro inhibidores de la NA, pegar los datos en bruto en un conjunto de cuatro (con una fila vacía entre cada placa). - Abra el software de adaptación y click en la pestaña "Experimento". Elija "alternativos 2-fármaco Fluoro 11 muestras."
- Haga clic en la pestaña "Opciones" y marca "generar gráficos."
- Haga clic en "Opciones" de nuevo y haga clic en la pestaña "Nueva clave". Guarde el archivo .csv "inhibition_key" en la misma carpeta que el archivo de la hoja de datos en bruto.
- En el archivo inhibition_key, listar todos los nombres de las muestras por debajo de la ID. Cada nombre de la muestra debe ser único.
- Si se probaron cuatro inhibidores de la NA, insertar espacios para dos filas adicionales a continuación Oseltamivir y el tipo de "Peramivir" y "Laninamivir." Guardar los cambios realizados en el archivo inhibition_key.
- Volver a la "jaspr v 1.2-Inhibición Ajuste de curvas" de la ventana y seleccione el archivo de datos brutos como el "Experimento Archivo" y inhibition_key como el "archivo de clave." Ejecutar el análisis. Guardar los resultados en formatos .csv y .pdf.
Nota: El software trazará automáticamente una curva de inhibición (RFU agaiNST NA concentraciones de inhibidor), como se muestra en la Figura 4. El programa también calcula los valores de IC50 para cada virus frente a un particular inhibidor de NA (Figura 4). Además, JASPR presenta los valores de CI 50 y el fondo de señal a (S / B) relación en formato de hoja de cálculo. Los valores de fondo pueden diferir de un laboratorio a otro dependiendo del fluorómetro usado. Al Melbourne WHOCCRRI, el fondo valora para la gama Munana 100? M de 50 a 120 RFU. Para un valor fiable IC 50, se prefiere una relación de S / B de ≥10, aunque una proporción de menos de 10 es todavía aceptable, en particular para los virus mutantes que tienen una actividad muy baja NA. - Inspeccionar los valores de IC50 y las formas de las curvas generadas por el software. Todos los puntos de datos deben caer sobre o cerca de la curva; si no lo hacen, repetir el ensayo de inhibición de NA.
NOTA: Para los virus que muestran inusualmente altos valores de CI 50, el ensayo debe ser de repeticióned para confirmar el resultado.
Resultados
El uso de directrices normalizadas del Grupo de Trabajo de la OMS sobre Vigilancia de Influenza Antiviral Susceptibilidad 9, se informó de la susceptibilidad de los virus de la gripe a los inhibidores de la NA utilizando los términos inhibición normal (Ni), inhibición reducida (RI), y altamente reducido de inhibición (HRI) . Virus de NI son aquellos con valores de IC50 de menos de 10 veces en comparación con la mediana de referencia del IC 50 para virus de influenza A (o menos de 5 veces para el virus de influenza B). Virus de RI son aquellos con valores de CI50 entre 10 y 100 veces por encima de la mediana de referencia del IC 50 para los virus de influenza A (o de 5 y de 50 veces para la gripe B). Virus HRI son aquellos con valores de IC50 de 100 veces por encima de la mediana de referencia del IC 50 para virus de influenza A (o por encima de 50 veces para el virus de influenza B); véase la Tabla 2.
La mediana de referencia valores de CI50 para A (H1N1) pdm09, A (H3N2), y los virus B Yamagata / B Victoria se calculan y actualizan anualmente en el Melbourne WHOCCRRI para reflejar los cambios menores en los valores de IC50 de cepas de la gripe circulantes a los inhibidores de NA (Tabla 3). La mediana de los valores de IC50 en la influenza A (H1N1) virus pdm09 son casi los mismos en los cuatro inhibidores de la NA, pero el zanamivir mediana y Laninamivir valores de CI50 para los virus A (H3N2) son de 2 a 4 veces mayor en comparación con oseltamivir y peramivir valores de CI50 (Tabla 3). El oseltamivir mediana IC 50 valor de virus de influenza B es generalmente de 5 a 10 veces mayor que el zanamivir, peramivir, y Laninamivir valores de CI50 (Tabla 3).
El ensayo de inhibición de NA es un ensayo fenotípico que no proporciona información sobre los cambios genéticos Associado con RI o HRI. Por lo tanto, es importante que el análisis genético se realiza después de la identificación de los virus con RI o HRI. Al Melbourne WHOCCRRI, el gen NA de variantes se analizó utilizando la secuenciación de Sanger y piro-secuenciación. Una lista representativa de sustituciones de aminoácidos que se pueden encontrar en el gen NA de los virus con variantes de RI y HRI se presenta en la Tabla 4. Una lista más extensa de sustituciones de aminoácidos que puede alterar NAI susceptibilidad también está disponible en el sitio web de la OMS 10.
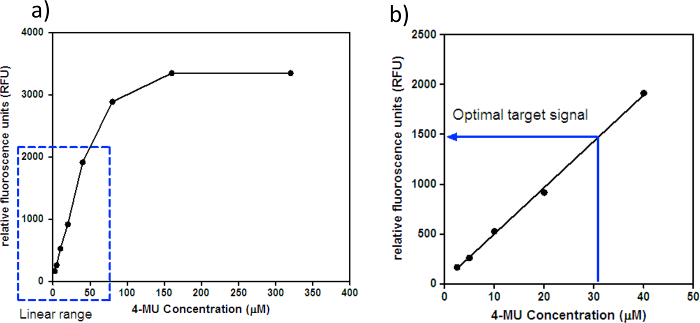
Figura 1: RFU frente a la concentración de 4-MU. (A) Curva estándar de RFU contra 4-MU concentración (M). La caja de puntos muestra el intervalo lineal de 4-MU para el fluorómetro. Las señales de fluorescencia por encima del rango lineal puede ser saturado, y por tanto, cualquier scambios en la fluorescencia de centros comerciales no pueden ser detectadas por el fluorímetro. (B) sección lineal Primer plano de la curva estándar de la figura 1a para la identificación de la "señal objetivo óptimo." El fluorómetro en el Melbourne WHOCCRRI tiene un rango lineal de 2,5-40? M 4-MU y una señal objetivo óptimo de ~ 30? M 4-MU, que corresponde a ~ 1.500 RFU. Haga clic aquí para ver una versión más grande de esta figura.
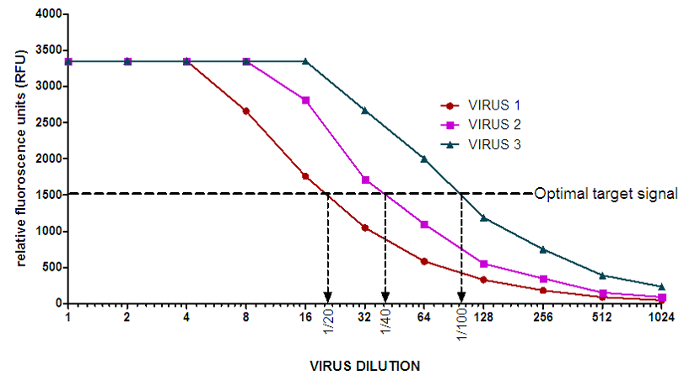
Figura 2: Ejemplo de las curvas de actividad de NA de los virus de influenza. El valor medio de fondo de 50,61 RFU se ha restado de cada punto de dilución en las curvas de actividad de NA. Las flechas indican la dilución de virus apropiado para utilizar en el ensayo de inhibición de NA para cada virus. Para la preparación más fácilaración de diluciones de virus, se puede elegir para llevar a cabo una dilución 1/100 para VIRUS 3 en lugar de una dilución 1/96. Haga clic aquí para ver una versión más grande de esta figura.
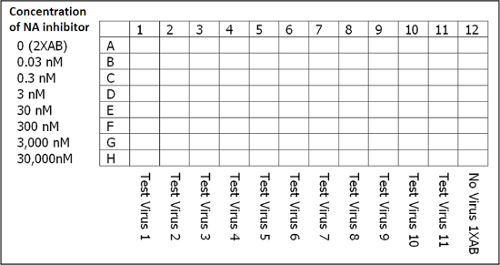
Figura 3: disposición de la placa para la configuración del ensayo de inhibición de NA. Cada placa incluye la última columna, que actúa como un control negativo que no contiene virus pero tampón de ensayo solamente 1x (AB), inhibidor de NA, Munana, y solución de parada. NOTA: JASPR utiliza las lecturas de la columna 12 de cada placa para determinar la señal en blanco promedio se utiliza en el cálculo de los valores de CI50. Haga clic aquí para ver una versión más grande de esta figura.
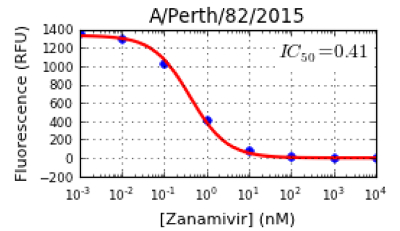
Figura 4: Ejemplo de una curva de inhibición e IC 50 valor de una A (H1N1) virus pdm09, A / Perth / 82/2015. El software JASPR presenta la curva de inhibición como fluorescencia (RFU) en contra de la creciente concentración (nM) de inhibidor de NA, con cada ajuste punto dentro de la curva. Sobre la base de la curva de inhibición, el valor de IC 50 se determina como la concentración de inhibidor de NA para reducir el 50% de la actividad de NA de virus. Haga clic aquí para ver una versión más grande de esta figura.
| Virus | dilución de virus requiere | 1x volumen de tampón de ensayo (l) | Tensioactivo-Amps-NP-40 (10%) (ml) | volumen Virus (mL) |
| 1 | 1/20 | 940 | 10 | 50 |
| 2 | 1/40 | 965 | 10 | 25 |
| 3 | 1/100 | 890 | 10 | 10 |
Tabla 1: Preparación de diluciones de virus para el virus de 1, 2, y 3 en el ensayo de inhibición de NA.
| Tipo de Virus / subtipo / linaje | la inhibición de la normalidad | la inhibición reducida | inhibición altamente reducida |
| (NI) | (RHODE ISLAND) | (HRI) | |
| A (H1N1) pdm09 | <10 veces | 10-100 veces | > 100 veces |
| A (H3N2) | y# 60; 10 veces | 10-100 veces | > 100 veces |
| B Yamagata y B Victoria | <5 veces | 5-50 veces | > 50 veces |
Tabla 2: El Grupo de Trabajo antiviral directrices de la OMS recomienda para la clasificación de la susceptibilidad al virus de la gripe inhibidores de la NA.
| Tipo de Virus / subtipo / linaje | norte | zanamivir | oseltamivir | peramivir | Laninamivir |
| La mediana (rango) IC 50 nM | La mediana (rango) IC 50 nM | La mediana (rango) IC 50 nM | La mediana (rango) IC 50 nM | ||
| A (H1N1) pdm09 | 1326 | 0,42 (0,1 a 3,43) | 0,36 (0,01 a 3,48) | 0,19 (0,07 a 1,60) | 0,55 (0,05 a 2,29) |
| A (H3N2) | 1654 | 0,9 (0,11 a 4,0) | 0,38 (0,01 a 3,65) | 0,33 (0,12 a 3,06) | 1,38 (0,01 a 9,38) |
| B Yamagata y B Victoria | 1115 | 2,2 (1,24 a 10,72) | 15,12 (2.39-70.75) | 1,36 (0,57 a 6,67) | 2,89 (1,62 a 9,15) |
Tabla 3: La mediana de IC 50 y IC 50 gama de inhibición normal (NI) los virus de 2015 derivó en la CCRIG de la OMS, Melbourne.
| sustitución de aminoácido | Tipo / subtipo / linaje | IC 50 veces de cambio compared para hacer referencia a la mediana de los valores de CI50. | |||
| zanamivir | oseltamivir | peramivir | Laninamivir | ||
| H275Y | A (H1N1) pdm09 | 1 | 557 (HRI) | 123 (HRI) | 2 |
| E119V | A (H3N2) | 1 | 63 (RI) | 1 | 1 |
| H134Y | B Victoria | 1 | 4 | 76 (HRI) | 2 |
| N151T | B Victoria | 4 | 4 | 42 (HRI) | 1 |
| G104E | B Victoria | 1220 (HRI) | 87 (HRI) | 17724 (HRI) | 701 (HRI) |
| E105K | B Victoria | 3 | 5 (RI) | 59 (HRI) | 2 |
| I222T | B Victoria | 2 | 7 (RI) | 8 (RI) | 3 |
| H273Y | B Yamagata | 1 | 230 (HRI) | 377 (HRI) | 2 |
| D197N | B Yamagata | 4 | 7 (RI) | 32 (RI) | 3 |
Tabla 4: Lista representativa de sustituciones de aminoácidos unidos a la reducción de la inhibición (RI) o muy reducido de inhibición (HRI) a los inhibidores de NA.
| Problema | Posibles razones) | Solución (s) |
| No o baja actividad de NA | Ningún virus fue el rendimiento de virus presente o baja. | Espécimen clínicos deben ser cultivados en líneas celulares (es decir, células de riñón Madin-Darby Canine) o en huevos de gallina embrionadosa una carga de virus más alta para su uso en el ensayo de inhibición de NA. |
| Algunos virus mutantes tienen una actividad muy baja a pesar de NA a carga alta de virus. | Utilice concentración de virus ordenada para la prueba. Tampón de ensayo pH inferior (por ejemplo pH 5,3) puede ser utilizado. Sin embargo, se debe tener cuidado al comparar los datos. | |
| No o baja actividad de NA en ensayo de inhibición de NA | No se añadió el virus. | Vuelva a diluir el virus. Asegúrese de que el virus se añade directamente en el tampón de ensayo 1x. |
| se usó dilución de virus incorrecto. | Repetir el ensayo de actividad de NA. | |
| tiempo de incubación insuficiente. | Asegúrese de que el tiempo de incubación es seguida. | |
| Los puntos de datos caen fuera de la curva IC 50 | La contaminación cruzada de inhibidor de NA de mayor concentración. | Asegúrese de que las puntas no están en contacto con la inhibi NAtor al dispensar virus diluido en la placa de 96 pocillos. |
| Si se ha utilizado un depósito 8 de pozo profundo, deseche y re-dispensar la NA concentraciones de inhibidor en un depósito de pozo profundo fresco 8. | ||
| El volumen del inhibidor de NA o Munana o virus diluido no se añadió igualmente en cada pocillo. | Repetir el ensayo con una pipeta multicanal calibrada. Asegúrese de un volumen igual de cada reactivo se dispensa en cada pocillo. | |
| Inusualmente altos valores de CI50 | se añadió demasiado alta concentración de virus. | Repetir el ensayo de actividad de NA y ensayo de inhibición de NA. |
| Muestra de ensayo contenía mezclas de influenza A e influenza B. | Realizar PCR en tiempo real para identificar la presencia de mezclas de virus. | |
| La contaminación bacteriana en la muestra | virus Cultura en la condición estéril con la presencia de antibiótico. | |
| señal de fluorescencia de fondo alto | sustrato Munana puede degradarse con el tiempo. | Utilizar un nuevo lote de Muñana subtrate. |
| La detección de fluorescencia de los pozos vecinos. | Utilizar el negro placas de 96 pocillos de fondo plano |
Tabla 5: Solución de problemas para los problemas potenciales en el ensayo de inhibición de NA.
Discusión
La supervisión global de la susceptibilidad del virus influenza a los inhibidores de NA actualmente está siendo realizado por una serie de laboratorios ya sea utilizando ensayos fluorescentes o de inhibición de NA quimioluminiscente 11, 12. El ensayo de fluorescencia se utiliza más comúnmente que el ensayo quimioluminiscente. Aunque ambos ensayos son robustos y reproducible, los valores de CI50 obtenidos a partir del ensayo basado en la fluorescencia son a menudo más alto que el ensayo basado en quimioluminiscencia, haciendo una comparación directa de los datos de los dos ensayos difíciles 13. Incluso con el uso del mismo protocolo, los datos generados de un laboratorio pueden variar de otro. Debido a estas variaciones entre los laboratorios, el Grupo de Trabajo de la OMS sobre Vigilancia de Influenza Antiviral Susceptibilidad produjo una guía para ayudar en las comparaciones entre laboratorios. En lugar de comparar los absolutos valores de CI50, este uso directrizcomparación sa basado en el IC 50 veces de diferencia a la mediana IC 50 de los virus de la gripe de NI ensayados en cada laboratorio particular. La capacidad de comparar los datos de los cinco centros de colaboración se ha traducido en la publicación anual de la gripe mundial de datos de susceptibilidad antiviral 2, 3, 4. La disponibilidad de la gran cantidad de datos de susceptibilidad de la influenza en el dominio público permite a los investigadores comparar IC 50 datos de los estudios con la generada en sus propios laboratorios.
Otros ensayos de inhibición de NA que adoptan un concepto similar también están disponibles comercialmente. Estos kits comerciales que contienen reactivos listos para el uso (NA no inhibidores incluido) son igualmente reproducible. Sin embargo, la casa en ensayo de inhibición de NA es sustancialmente más barato que los kits comerciales, porque la mayoría de los reactivos puede ser hecho en casa encantidades más grandes y el sustrato Muñana, lo que hizo previamente el mayor costo del ensayo, ahora se pueden adquirir de diversas fuentes a precios competitivos. El costo de las pruebas de una cepa de la gripe por fármaco es de aproximadamente $ 1 (USD). Al Melbourne WHOCCRRI, se han realizado mejoras para el ensayo de inhibición de la casa NA después de la incorporación de una plataforma robótica para los componentes de manejo de líquidos del ensayo. Aparte de la preparación manual de diluciones de virus, la mayoría de los procedimientos se llevan a cabo usando el robot de manejo de líquidos. Esto no sólo reducir al mínimo la manipulación manual, pero también aumenta el número de ensayos que se pueden ejecutar en un día.
Aunque el ensayo de inhibición de NA es muy resistente, hay una serie de pasos críticos que deben completarse con la atención adicional. En primer lugar, cualquier irregularidad en las concentraciones de inhibidor de NA pueden desplazar las curvas de inhibición y los valores IC 50; Por lo tanto, una cuidadosa atención debe serpagado en la preparación de las concentraciones de inhibidor de NA. En segundo lugar, los períodos de pipeteado y de incubación precisa precisos son cruciales para mantener resultados consistentes a través de ensayos; esto se puede lograr mediante el uso de pipetas y temporizadores calibrados. La inclusión de los virus de control en cada ensayo también permite la supervisión del rendimiento del ensayo de ensayo a ensayo y durante largos períodos de tiempo. En tercer lugar, debido a que la actividad de la enzima NA de los virus de la gripe estacional es óptima a pH 6,5, el pH correcto del tampón de ensayo es importante. Algunos informes han encontrado que el uso de condiciones más bajos de pH pueden mejora la identificación de variantes de la gripe, tales como la variante A (H7N9) que contiene la mutación R292K 14, 15. Sin embargo, la modificación del pH del tampón de ensayo se desplazará los valores de IC 50, y esto puede complicar la comparación de los datos dentro de los laboratorios y entre laboratorios. Otras modificaciones y solución de problemas que puede ser performed se enumeran en la Tabla 5.
Los inhibidores de la NA son la única clase de antivirales aprobados que están actualmente eficaces contra los virus de influenza en circulación. Hasta que otras clases de antivirales estén disponibles para uso clínico, la vigilancia de la susceptibilidad antiviral del virus de la gripe circulantes se centrará en inhibidores de la NA solo. Debido a la simplicidad y reproducibilidad de los resultados, el uso del ensayo de inhibición de NA para evaluar la susceptibilidad del virus influenza a los inhibidores de NA continuará.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
El Melbourne Centro Colaborador para Referencia e Investigación sobre la Gripe es apoyado por el Departamento de Salud del Gobierno de Australia.
Materiales
| Name | Company | Catalog Number | Comments |
| Influenza A and B viruses | Cultured in MDCK cells or 9 day old embryonated specific pathogen free (SPF) eggs | ||
| Madin-Darby Canine Kidney (MDCK) cells | ATCC | PTA-6500 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Biosynth AG | M-5507 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Sigma | M8639 | |
| 4-Methylumbelliferone (4-MU) | Sigma | M1381-25G | |
| 2-[N-morpholino]ethanesulphonic acid (MES hydrate) (free acid) | Sigma | M8250-250G | |
| Calcium Chloride (Ca Cl2) | APS AJAX Finechem | 127-500G | |
| Surfactant-Amps-NP-40 (10% solution) | Thermo Fisher Scientific | PIE28324 | |
| Sodium Hydroxide (NaOH) | APS AJAX Finechem | 482-2.5KG | |
| Absolute Ethanol | APS AJAX Finechem | 214-2.5L GL | |
| 96-well clear flat-bottom plates | NUNC | 456537 | |
| 96-well U-bottom plates | Greiner Bio-one | 4650101 | |
| 8 channel deep well block | Pacific Laboratory Products | RES-MW8-HP | |
| 96-well deep plates, 2.0 mL square wells | Pacific Laboratory Products | P-2ML-SQ-C | |
| Plate sealers | Thermo Fisher Scientific | 236366 | |
| Bottle-top vacuum filter system (cellulose membrane (nitrate), pore size 0.2 μm, membrane area 33.2 cm2, filter capacity 500 mL) | Sigma-Aldrich | CLS430758-12EA | |
| Single-channel pipettes (1 µL - 1,000 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Multi-channel pipettes | Variety of suppliers (eg. Eppendorf, Sartorius) | 8 or 12 channel electronic and manual pipette (5 - 1250 µL volume) | |
| Pipette tips (1 µL - 1,250 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Disposable pipettes (10 mL and 25 mL) | Greiner Bio-one | P7740-200EA and P7865-200EA | |
| Pipette controller | Eppendorf | 4430000018 | |
| Centrifuge tubes 50 mL | BD Bioscience | 352070 | |
| Racked tubes | Scientific Specialties, Inc. | 1750-00 | |
| Fluorometer with excitation wavelength setting of 355 nm and an emission wavelength setting of 460 nm | TermoFisher Scientific | ASCENT FL 374 | |
| Ascent software | TermoFisher Scientific | 5185410CD | |
| Incubator set at 37 °C | Lab Supply | Biocell 1000 | |
| Zanamivir | GlaxoSmithKline | Request directly from the company | |
| Oseltamivir carboxylate | Roche | ||
| Peramivir (BCX-1812) | BioCryst | ||
| Laninamivir (R-125489) | Daiichi-Sankyo | ||
| JASPR v1.2 | Influenza Division at the CDC Atlanta, USA | freely available upon request (fluantiviral@cdc.gov) |
Referencias
- Moscona, A. Neuraminidase inhibitors for influenza. N.Engl.J.Med. 353 (13), 1363-1373 (2005).
- Hurt, A. C., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 132, 178-185 (2016).
- Meijer, A., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 110, 31-41 (2014).
- Takashita, E., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 117, 27-38 (2015).
- Lackenby, A., et al. Emergence of resistance to oseltamivir among influenza A(H1N1) viruses in Europe. Euro Surveill. 13 (5), (2008).
- Hurt, A. C., et al. Community transmission of oseltamivir-resistant A(H1N1)pdm09 influenza. N Engl J Med. 365 (26), 2541-2542 (2011).
- Takashita, E., et al. Characterization of a large cluster of influenza A(H1N1)pdm09 viruses cross-resistant to oseltamivir and peramivir during the 2013-2014 influenza season in Japan. Antimicrob Agents Chemother. 59 (5), 2607-2617 (2015).
- Eisfeld, A. J., Neumann, G., Kawaoka, Y. Influenza A virus isolation, culture and identification. Nat Protoc. 9 (11), 2663-2681 (2014).
- . Meetings of the WHO working group on surveillance of influenza antiviral susceptibility - Geneva, November 2011 and June 2012. Wkly Epidemiol Rec. 87 (39), 369-374 (2012).
- Okomo-Adhiambo, M., Hurt, A. C., Gubareva, L. V. The chemiluminescent neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 95-113 (2012).
- Hurt, A. C., Okomo-Adhiambo, M., Gubareva, L. V. The fluorescence neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 115-125 (2012).
- Analysis of IC50 data. isirv Antiviral Group (isirv-AVG) Available from: https://isirv.org/site/index.php/methodology/analysis-of-ic50-data (2016)
- Sleeman, K., et al. R292K substitution and drug susceptibility of influenza A(H7N9) viruses. Emerg Infect Dis. 19 (9), 1521-1524 (2013).
- Gubareva, L. V., Robinson, M. J., Bethell, R. C., Webster, R. G. Catalytic and framework mutations in the neuraminidase active site of influenza viruses that are resistant to 4-guanidino-Neu5Ac2en. J Virol. 71 (5), 3385-3390 (1997).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados