Method Article
Basées sur la fluorescence neuraminidase Essai d'inhibition pour évaluer la sensibilité des virus de la grippe à la neuraminidase Inhibiteur Classe de Antiviraux
Dans cet article
Résumé
Nous décrivons l'utilisation d'un test d'inhibition de la neuraminidase par fluorescence phénotypiques pour évaluer la sensibilité des virus grippaux A et B à la classe des inhibiteurs de la neuraminidase de Antiviraux.
Résumé
Les inhibiteurs de la neuraminidase (NA) sont la seule classe d'agents antiviraux approuvés pour le traitement et la prophylaxie de la grippe qui sont efficaces contre les souches actuellement en circulation. En plus de leur utilisation dans le traitement de la grippe saisonnière, les inhibiteurs de NA ont été stockées par un certain nombre de pays pour une utilisation en cas de pandémie. Il est donc important de surveiller la sensibilité des virus grippaux en circulation à cette classe de médicaments antiviraux. Il existe différents types de tests qui peuvent être utilisés pour évaluer la sensibilité des virus grippaux aux inhibiteurs de NA, mais les tests d'inhibition de l'enzyme en utilisant soit un substrat fluorescent ou un substrat chimiluminescent sont les plus largement utilisés et recommandé. Ce protocole décrit l'utilisation d'un test basé sur la fluorescence pour évaluer la sensibilité du virus de la grippe aux inhibiteurs de NA. L'essai est basé sur l'enzyme NA cliver le 2 '- (4-Methylumbelliferyl) -α-D - N -acetylneuraminic acide (Muñana) Le substrat pour libérer le produit fluorescent 4-méthylumbelliférone (4-MU). Par conséquent, l'effet inhibiteur d'un inhibiteur de NA du virus de la grippe NA est déterminée en fonction de la concentration de l'inhibiteur de NA qui est nécessaire pour réduire de 50% de l'activité NA, donnée en tant que valeur CI50.
Introduction
Hémagglutinine (HA) et la neuraminidase (NA) sont les deux principales glycoprotéines de surface de virus grippaux A et B. HA se lie au-galactose en acide sialique des glycoprotéines de surface cellulaire ou des glycolipides, tandis que le NA libère le virus par clivage de l'acide sialique à partir du galactose sur la surface de la cellule 1. Les inhibiteurs de NA sont une classe de médicaments antiviraux de la grippe qui ont été rationnellement conçues pour se lier étroitement au site actif enzymatique NA, empêchant ainsi la libération et la propagation de la descendance virale. Oseltamivir et le zanamivir sont deux inhibiteurs de NA qui ont été approuvés dans de nombreux pays dans le monde entier pour le traitement et la prophylaxie de la grippe. Ces dernières années, deux inhibiteurs de NA supplémentaires, Peramivir et Laninamivir, ont été approuvés pour être utilisés dans un nombre limité de pays. Le criblage de virus de la grippe pour la susceptibilité aux inhibiteurs de NA et l'identification des mutations qui confèrent une résistance sont importantes dans la détermination et le suivi de la effectivEness de cette classe de médicaments antiviraux.
Au cours des 16 dernières années, le test d'inhibition NA par fluorescence a été effectuée régulièrement au Centre collaborateur OMS de référence et de recherche sur la grippe, Melbourne (Melbourne WHOCCRRI) pour surveiller l'évolution de la tendance de la sensibilité aux antiviraux parmi les virus grippaux en circulation. Chaque année, plus de 2000 virus de la grippe sont testés pour la sensibilité aux antiviraux. Dans la plupart des saisons de grippe,> 98% des virus sont sensibles aux quatre inhibiteurs de NA 2, 3, 4, bien que pendant la saison grippale dans l'hémisphère nord 2007-2008, il y a eu une augmentation du nombre d'anciens saisonniers A (H1N1) qui avait une sensibilité réduite à l' oseltamivir 5. Ce groupe de virus, qui contenait la NA substitution d'acide aminé H275Y, se propager au reste du monde d'ici la fin de 2008, ce qui inappropri oseltamivirmangé à l'échelle mondiale pour le traitement de ce virus. La grande majorité des circule actuellement influenza B, de la grippe A (H3N2) et la grippe A (H1N1) souches de pdm09 sont sensibles à l'oseltamivir, bien que les grappes de la communauté de A (H1N1) variants de pdm09 contenant le H275Y de substitution d'acides aminés NA conférant réduite oseltamivir et la sensibilité de peramivir, ont été signalées dans diverses régions du monde 6, 7.
En raison de la nécessité d'un titre viral suffisamment élevé, les échantillons cliniques (y compris les lavages nasaux des animaux) doivent être repiquées dans les deux cultures de cellules ou des œufs de poule embryonnés avant l'essai de sensibilité aux antiviraux. L'essai d'inhibition NA décrit dans cet article peut être divisé en trois sections:
La détermination de la plage linéaire pour le produit fluorescent 4-méthylumbelliférone (4-MU) sur un fluorimètre particulier
En raison des différences inhérentes entre fluorimétres, til plage linéaire de la fluorescence du produit final, le 4-MU, et l'unité de fluorescence relative (RFU), doivent être mis en place. Une fois que la plage linéaire de 4-MU est établi, le signal de cible optimale est sélectionnée, à laquelle la concentration des virus de la grippe est ajustée dans l'essai d'activité NA. Une fois terminé pour un fluorimètre particulier, cela ne devrait pas être répétée.
La détermination de l'activité NA des virus
Le dosage de l' activité NA est un test simple qui consiste à ajouter de la 2 '- (4-Methylumbelliferyl) -α-D - N substrat acide -acetylneuraminic (Muñana) en série de virus dilué. La quantité de fluorescence du produit final 4-MU généré à partir du clivage de Munana par la NA est mesurée en utilisant un fluoromètre. La dilution de virus approprié à utiliser dans l'essai d'inhibition NA est choisi en traçant unités de fluorescence contre la dilution de virus. De la courbe sigmoïde produit, le point médian de la section linéaire doit correspondre àla plage linéaire 4-MU du fluorimètre est déterminé au point 1 et informera la concentration appropriée de virus à utiliser dans la section 3.
L'évaluation de la sensibilité du virus aux inhibiteurs de NA en utilisant le test d'inhibition NA
Pour évaluer la sensibilité des virus à un inhibiteur NA particulier, les virus à la dilution déterminée à l'article 2 sont mis en incubation avec une gamme de concentrations d'inhibiteur de NA. Après une incubation ultérieure avec Muñana, le 4-MU généré par des virus sans inhibition est mesurée en RFU par le fluoromètre. L'effet inhibiteur de l'inhibiteur de NA sur l'activité de l' enzyme NA d'un virus est calculé en fonction de la concentration d'inhibiteur nécessaire pour réduire NA 50% de l'activité NA, donnée en tant que valeur CI50.
Protocole
1. Détermination de la gamme linéaire du produit fluorescent 4-MU sur un Fluorometer
- Préparer 10 ml de 6,4 mM de solution mère de 4-MU par dissolution de 11,3 mg de 4-MU dans 5 ml d'éthanol absolu. Ajouter 5 ml de NaCl à 0,9% (p / v) de la solution mère pour faire 10 ml. Préparer une solution 640 uM de travail en diluant 1 ml de 6,4 mM de 4-MU dans 9 ml de tampon de dosage 1x (33,3 mM de 2- (N-morpholino) éthanesulfonique (MES) et 4 mM de CaCl2, pH 6,5).
NOTE: Préparer le tampon d'essai 2x en ajoutant 13 g de MES et 8 ml de 1 M CaCl 2 à 992 ml d'eau distillée. Ajuster le pH à 6,5 en utilisant de 10 M de NaOH. Filtrer le tampon en utilisant un filtre d'acétate de cellulose stérile de taille de pores de 0,2 um. Mise en garde! L'hydroxyde de sodium est caustique et peut causer des brûlures chimiques sur la peau et les yeux. Assurez-vous que l'équipement complet de protection individuelle est usée. - Préparer 5 ml d'une gamme de concentrations 4-MU ( par exemple, 5 uM, 10 uM, 20 uM, 40 uM, 80 uM, 160 & #181; M, et 320 uM) à travers une série de dilutions deux fois de 640 pM 4-MU en utilisant un tampon de dosage 1x.
- Distribuer 50 uL de chaque dilution en série de 4-MU ( par exemple, 5 uM, 10 uM, 20 uM, 40 uM, 80 uM, 160 uM, 320 uM et 640 uM) (deux puits par dilution) dans un cadre clair, 96- puits d'une plaque à fond plat et 50 ul de tampon d'essai 1x dans les puits restants (qui servent de flans pour mesurer des signaux d'arrière-plan).
NOTE: Les concentrations finales de 4-MU dans le volume de réaction (50 uL 4-MU + 50 uL 300 uM Muñana) sont de 2,5 pM, 5 pM, 10 pM, 20 pM, 40 pM, 80 pM, 160 pM et 320 pM . - Préparer une solution mère 2,5 mM MUNANA en reconstituant 25 mg de Muñana dans 20 ml d'eau distillée. Mélanger 0,72 ml de 2,5 mM MUNANA avec 5,28 mL de tampon de dosage 1x pour obtenir une solution de travail 300 uM Muñana (volume suffisant pour une plaque). Couvrir le tube contenant 300 uM Muñana working de solution avec une feuille d'aluminium et le garder sur la glace à moins utilisé immédiatement. Jetez les restes de matériaux.
NOTE: Le 1 mois solution mère 2,5 mM MUNANA peut être conservé à -20 ° C et doit être utilisé dans un cycle de gel / dégel. Les 4-MU et des solutions Muñana sont sensibles à la lumière et doivent être protégés d'une exposition prolongée lumière. - Ajouter 50 ul de 300 uM Muñana à chaque puits, appuyez doucement pour mélanger et incuber à 37 ° C pendant 30 min. Couvrir la plaque avec un scellant de plaque pour éviter l'évaporation.
REMARQUE: Cette étape est de rendre compte de la fluorescence de fond dans l'essai d'inhibition NA. - Préparer la solution d'arrêt par mélange de 11 ml d'éthanol absolu avec 2,225 ml de NaOH 0,824 M (volume suffisant pour une plaque).
- Ajouter 100 pi de solution d'arrêt à chaque puits pour arrêter la réaction et tapoter doucement pour mélanger.
- Lire la plaque en utilisant un fluorimètre avec un réglage de longueur d'onde d'excitation de 355 nm et un paramètre de longueur d'onde d'émission de 460 nm, comme per les instructions du fabricant.
- Calculer le signal d'arrière-plan en utilisant la moyenne des signaux de fluorescence de tous les puits ne contenant pas de 4-MU. Soustraire ce signal de fond moyen dans chacun des puits contenant 4-MU et calculer les signaux moyens (RFU) pour chaque concentration de 4-MU. Tracer la courbe d' étalonnage de la concentration RFU contre 4-MU (uM), comme représenté sur la figure 1a; une section linéaire gros plan de la courbe est représentée sur la figure 1b.
- Visualiser le tracé de la concentration RFU 4-MU (uM) pour déterminer la plage linéaire et le signal de cible optimal; la plage linéaire est où le signal de fluorescence augmente proportionnellement à la concentration croissante de la 4-MU sur le terrain, tandis que le signal cible optimal est une concentration de 4-MU arbitraire dans la plage linéaire.
NOTE: La gamme linéaire et le signal cible optimal sont spécifiques fluorimètre. Par exemple, le fluorimètre à Melbourne WHOCCRRI a une gamme linéaire de 20,5 à 40 uM 4-MU et un signal de cible optimale d'environ 30 pM de 4-MU, qui correspond à ~ 1500 RFU.
2. Détermination de l'activité NA des virus
NOTE: Les virus grippaux sont cultivées à des titres suffisants dans des cellules ou des œufs de poule embryonnés 8 Madin-Darby Canine Kidney (MDCK).
- Distribuer 120 pl par puits de virus de la grippe en culture non dilués dans la colonne 1 et 60 ul de tampon d'essai 1x contenant 0,1% de NP-40 dans les 11 colonnes restantes d'un 96 puits, une plaque à fond en U.
- Série effectuer une dilution de deux fois des virus à travers la plaque ( par exemple, le transfert de 60 ul de la colonne 1 à la colonne 2 et ainsi de suite, jusqu'à la colonne 11) à l' aide d' une pipette multicanaux, colonne en laissant 12 un vide contenant un tampon d'essai seulement 1x.
- Transférer 50 ul de chacun des puits (virus dilués et blancs) dans un cadre clair, à 96 puits, une plaque à fond plat.
NOTE: Il est nécessaire de cembouts de pipette de hanger si les matériaux sont transférés de la colonne 12 à la colonne 1. - Ajouter 50 ul de 300 uM Muñana (préparé selon l'étape 1.4) par puits et tapoter doucement la plaque pour mélanger. Incuber la plaque à 37 ° C pendant 1 h. Couvrir la plaque avec un scellant de plaque pour éviter l'évaporation.
- Ajouter 100 ul de solution d'arrêt (préparé selon l'étape 1.6) par puits pour arrêter la réaction et tapoter doucement la plaque pour mélanger.
- Lire la plaque à l' aide d' un fluorimètre.
- Utiliser un paramètre de longueur d'onde d'excitation de 355 nm et un paramètre de longueur d'onde d'émission de 460 nm.
- Déterminer le signal de fond moyen sur la base des lectures de fluorescence dans la colonne 12 et soustraire le signal d'arrière-plan moyenne de chaque puits. Tracer un graphique de RFU contre des dilutions de virus.
NOTE: Les valeurs de base pour 100 uM Munana au WHOCCRRI Melbourne se situent généralement entre 50 et 120 RFU, mais ceux-ci diffèrent en fonction du fluorimètre being utilisé. - Voir l'intrigue de RFU contre des dilutions de virus pour déterminer le point médian de la section linéaire de la courbe pour chaque virus (figure 2). Utiliser le signal de cible optimale (déterminée à l'étape 1) en tant que point de référence.
NOTE: Cela devrait correspondre à la plage linéaire 4-MU du fluorimètre déterminé à l'article 1 et fournira la concentration appropriée de virus à utiliser dans la section 3.
3. Évaluation de virus Susceptibilité aux inhibiteurs de NA NA Utilisation du Test d'inhibition
- Préparer les stocks de base des inhibiteurs de NA à des concentrations de 300 uM.
- Préparer 300 uM zanamivir (poids moléculaire, PM = 332,32 g / mol) en dissolvant 5,0 mg de zanamivir dans 50 ml de tampon d'essai 2x (66,6 mM de MES et 8 mM de CaCl2, pH 6,5).
- Préparer 300 uM carboxylate d'oseltamivir (D-tartrate; PM = 386,44 g / mol) par dissolution de 5,8 mg dans 50 ml de tampon d'essai 2x.
- Préparer300 uM de trihydrate d'Peramivir (PM = 382,45 g / mol) par dissolution de 5,7 mg dans 50 ml de tampon d'essai 2x.
- Préparer 300 uM Laninamivir (PM = 346,34 g / mol) par dissolution de 5,2 mg dans 50 ml de tampon d'essai 2x.
REMARQUE: Les stocks de base d'inhibiteurs de NA peuvent être conservés à -20 ° C pendant 12 mois. Vérifier la MW des inhibiteurs de NA pour assurer les poids et les volumes corrects sont utilisés dans la reconstitution. Le carboxylate d'oseltamivir est le composé actif du phosphate d'oseltamivir de promédicament. Par conséquent, seul le carboxylate d'oseltamivir doit être utilisé dans le test d'inhibition NA.
- A partir des valeurs de base, de préparer des stocks de travail de dilutions en série de dix fois des inhibiteurs de NA dans des tubes de centrifugation de 50 ml à des concentrations de 0,03 nM, 0,3 nM, 3 nM, 30 nM, 300 nM, 3000 nM et 30 000 nM dans l'essai 2x tampon MES (66,6 mM et 8 mM de CaCl2, pH 6,5); ceci est pour une utilisation sur plusieurs tests.
NOTE: Les concentrations finales des inhibiteurs de NA dans la réaction volume (50 ul de dilution du virus + 50 ul d'inhibiteur NA + 50 ul de 300 uM Muñana) sont de 0,01 nM, 0,1 nM, 1 nM, 10 nM, 100 nM, 1000 nM et 10 000 nM, respectivement. La concentration finale ne comprend pas les 100 pi de solution d'arrêt. Conserver tous les inhibiteurs de NA dilutions à 2-8 ° C. La date d'expiration est le même que celui des stocks de maître. - Préparer les dilutions de virus dans un tampon de dosage contenant 0,1% 1x agent tensio-actif NP-40 dans un bloc 96 puits profonds. Utiliser des dilutions de virus sur la base des résultats d'analyse de l'activité NA provenant de la section 2. Utilisez un volume total de 2 ml par virus pour tester quatre inhibiteurs de NA.
NOTE: Préparer deux puits (1 ml par puits) par le virus dans un bloc 96 puits profonds. Des exemples de dilutions de virus pour le virus de 1, 2 et 3 sont présentés dans le tableau 1. - Répartir le volume requis d'inhibiteurs de NA (préparé selon l'étape 3.2) dans un réservoir de 8 puits profond. A partir de là, se dispenser 50 pi d'inhibiteurs de NA à des dilutions allant de 0 nM (2x essai buffer seulement) à 30 000 nM dans les rangées A à H de manière claire, à 96 puits, une plaque à fond plat.
REMARQUE: La mise en page de plaque est illustrée à la figure 3. - Ajouter 50 ul de virus d'essai dilué par puits dans les colonnes 1-11 et 50 pl par puits de tampon de dosage 1x seulement à la colonne 12. Tapoter doucement la plaque pour mélanger et incuber à température ambiante pendant 45 min. Couvrir la plaque avec un scellant de plaque pour éviter l'évaporation.
- Ajouter 50 ul de 300 uM Muñana (préparé selon l'étape 1.4) par puits et tapoter doucement la plaque pour mélanger. Incuber la plaque à 37 ° C pendant 1 h. Couvrir la plaque avec un scellant de plaque pour éviter l'évaporation.
- Ajouter 100 ul de solution d'arrêt (préparé selon l'étape 1.6) à chaque puits et tapoter doucement la plaque pour mélanger.
- Lire la plaque à l' aide d' un fluorimètre.
- Utiliser une longueur d'onde d'excitation de 355 nm et une longueur d'onde d'émission de 460 nm, comme décrit précédemment.
4. Calcul de laLes valeurs de CI50
REMARQUE: La v1.2 JASPR est un logiciel d'ajustement de courbe qui permet le calcul des valeurs de CI50. Le logiciel a été mis au point par la Division de la grippe au CDC, Atlanta, États-Unis. Le logiciel utilise l'équation: V = V max x (1 - ([I] / (K i + [I]))), où V max est la vitesse maximale de métabolisme, [I] est la concentration en inhibiteur, V est la réaction étant inhibée, et K i est l'IC 50 pour la courbe d'inhibition.
- Copier et coller les données brutes délivrées par le fluorimètre dans une feuille de calcul dans un format de plaque à 12 colonne (96 puits), en commençant par la cellule A1.
REMARQUE: Les données brutes à partir de chaque plaque postérieure doit être décalée d'une ligne vide. Si chaque virus a été testé contre les quatre inhibiteurs de NA, coller les données brutes dans un ensemble de quatre (avec une ligne vide entre chaque plaque). - Ouvrez le logiciel de montage et clbeurk sur l'onglet « Expérience ». Choisissez "2-médicaments alternatifs Fluoro 11 échantillons."
- Cliquez sur l'onglet « Options » et cochez « Générer des graphiques. »
- Cliquez sur « Options » à nouveau, puis cliquez sur l'onglet « Nouvelle clé ». Enregistrez le fichier .csv « de inhibition_key » dans le même dossier que le fichier tableur de données brutes.
- Dans le fichier inhibition_key, liste de tous les noms d'échantillons ci-dessous l'identifiant. Chaque nom de l'échantillon doit être unique.
- Si quatre inhibiteurs de NA ont été testés, insérer des espaces pour deux lignes supplémentaires ci-dessous Oseltamivir et tapez « Peramivir » et « Laninamivir. » Enregistrez les modifications apportées au fichier inhibition_key.
- Retour à la fenêtre « jaspr v 1.2 Ajustement de la courbe d'inhibition » et sélectionnez le fichier de données brutes comme le « Fichier expérience » et inhibition_key comme le « fichier clé. » Exécutez l'analyse. Enregistrer les résultats dans des formats .csv et .pdf.
REMARQUE: Le logiciel automatiquement une courbe tracer d'inhibition (RFU contnst NA Les concentrations d'inhibiteur), comme le montre la Figure 4. Le programme calcule également les valeurs de CI50 pour chaque virus contre un inhibiteur de NA individuel (Figure 4). En outre, JASPR présente les valeurs de CI50 et du signal à bruit de fond (S / B) rapport dans un format de tableur. Les valeurs de base peuvent différer d'un laboratoire à en fonction du fluorimètre utilisé. Au Melbourne WHOCCRRI, l'arrière-plan des valeurs pour 100 uM plage de Munana de 50 à 120 RFU. Pour une valeur IC 50 fiable, un rapport S / B de ≥10 est préféré, bien qu'un rapport inférieur à 10 est encore acceptable, en particulier pour les virus mutants qui ont une très faible activité NA. - Inspecter les valeurs de CI50 et les formes des courbes générées par le logiciel. Tous les points de données devraient tomber sur ou à proximité de la courbe; si elles ne le font pas, répéter le test d'inhibition NA.
NOTE: Pour les virus qui affichent des valeurs IC 50 anormalement élevées, l'essai doit être répétitioned pour confirmer le résultat.
Résultats
En utilisant des lignes directrices normalisées des rapports du Groupe de travail OMS sur la surveillance de la grippe Antiviral Susceptibilité 9, la sensibilité des virus grippaux aux inhibiteurs de NA sont rapportés en utilisant les termes d' inhibition normale (NI), l' inhibition réduite (RI) et l' inhibition très réduite (IRH) . NI virus sont ceux avec des valeurs de CI50 inférieures à 10 fois par rapport à la référence médiane IC 50 pour les virus de la grippe A (ou moins de 5 fois pour les virus grippaux B). RI virus sont ceux avec des valeurs de CI50 entre 10 et 100 fois supérieure à la médiane de référence CI 50 pour les virus de la grippe A (ou 5 et 50 fois pour l' influenza B). Les virus HRI sont ceux avec des valeurs de CI50 de 100 fois supérieure à la médiane de référence CI 50 pour les virus de la grippe A (ou au- dessus de 50 fois pour les virus influenza de type B); voir le tableau 2.
La référence médiane des valeurs de CI50 pour A (H1N1) pdm09, A (H3N2) et B Yamagata / B virus Victoria sont calculés et mis à jour annuellement au Melbourne WHOCCRRI pour tenir compte des changements mineurs dans les valeurs IC 50 de souches grippales en circulation aux inhibiteurs de NA (tableau 3). La médiane des valeurs de CI50 dans la grippe A (H1N1) de virus de la pdm09 sont presque les mêmes pour les quatre inhibiteurs de NA, mais la médiane zanamivir et Laninamivir valeurs IC50 pour A (H3N2) sont 2 à 4 fois par rapport à l' oseltamivir supérieur et peramivir valeurs de CI50 (tableau 3). Le oseltamivir médian valeur IC 50 pour les virus influenza de type B est généralement de 5 à 10 fois plus élevé que le zanamivir, Peramivir et Laninamivir valeurs de CI50 (tableau 3).
Le dosage d'inhibition de NA est un essai phénotypique qui ne fournit pas d'informations sur la modification génétique associATED avec RI ou HRI. Par conséquent, il est important que l'analyse génétique est effectuée suite à l'identification des virus avec RI ou HRI. A Melbourne WHOCCRRI, le gène NA de variantes est analysé par séquençage Sanger et pyro-séquençage. Une liste représentative des substitutions d'acides aminés qui peuvent être trouvés dans le gène NA de virus avec des variantes RI et HRI est présenté dans le tableau 4. Une liste plus complète des substitutions d'acides aminés qui peuvent modifier la sensibilité NAI est également disponible sur le site Web de l' OMS 10.
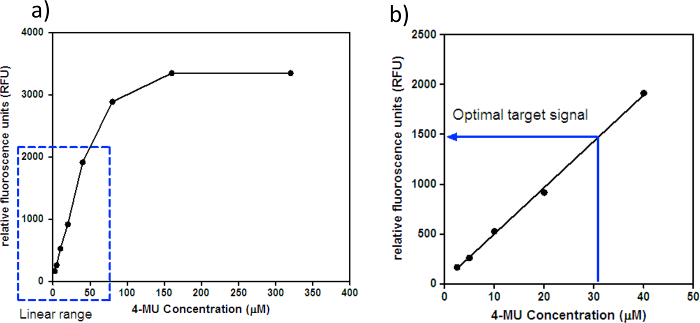
Figure 1: RFU contre concentration 4-MU. (A) Courbe standard de la concentration RFU 4-MU (uM). La boîte en pointillé indique la plage linéaire de 4-MU pour le fluoromètre. Les signaux de fluorescence au-dessus de la plage linéaire peuvent être saturés, et par conséquent, toute schangements de centre commercial en fluorescence ne peuvent pas être détectés par le fluorimètre. (B) section linéaire gros plan , la courbe d' étalonnage de la figure 1a pour l'identification du « signal cible optimale. » Le fluoromètre au Melbourne WHOCCRRI a une plage linéaire de 2,5 à 40 uM 4-MU et un signal de cible optimale d'environ 30 pM de 4-MU, qui correspond à ~ 1500 RFU. S'il vous plaît cliquer ici pour voir une version plus grande de ce chiffre.
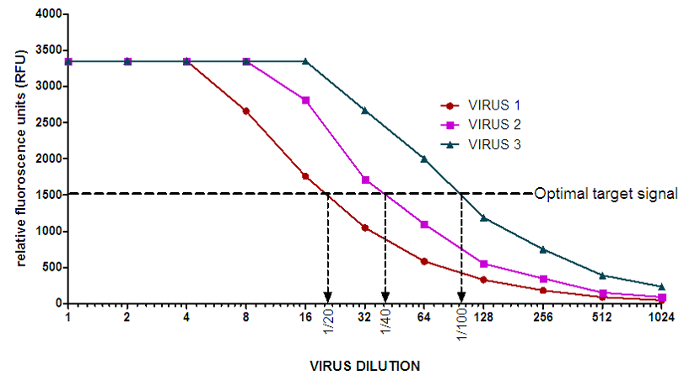
Figure 2: Exemple de courbes d'activité NA du virus de la grippe. La valeur initiale moyenne de 50,61 RFU a été soustraite de chaque point de dilution sur les courbes d'activité NA. Les flèches indiquent la dilution du virus approprié à utiliser dans l'essai d'inhibition NA pour chaque virus. Pour faciliter la préparationaration de dilutions de virus, on peut choisir d'effectuer une dilution 1/100 pour VIRUS 3 au lieu d'une dilution 1/96. S'il vous plaît cliquer ici pour voir une version plus grande de ce chiffre.
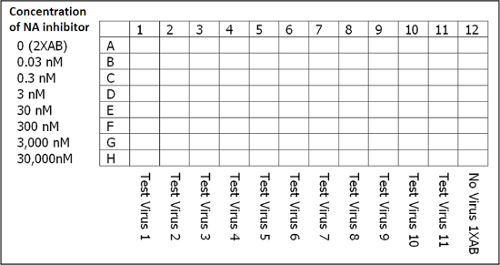
Figure 3: mise à plaques pour la mise en place de l'essai d'inhibition de NA. Chaque plaque comprend la dernière colonne, qui agit comme un témoin négatif qui ne contient pas de virus, mais uniquement du tampon d'essai 1x (AB), l'inhibiteur NA, Munana, et la solution d'arrêt. REMARQUE: JASPR utilise les lectures de la colonne 12 de chaque plaque afin de déterminer le signal de suppression moyen utilisé dans le calcul des valeurs de CI50. S'il vous plaît cliquer ici pour voir une version plus grande de ce chiffre.
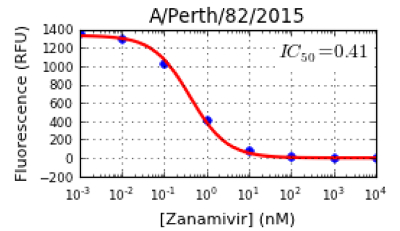
Figure 4: Exemple d'une courbe d'inhibition et de la valeur IC 50 d'un virus de pdm09 A (H1N1), A / Perth / 82/2015. Le logiciel JASPR présente la courbe d'inhibition sous forme de fluorescence (RFU) par rapport à la concentration croissante (nM) de l'inhibiteur de NA, à chaque ajustement de point à l'intérieur de la courbe. Sur la base de la courbe d'inhibition, la valeur IC50 est déterminée comme la concentration de l' inhibiteur pour réduire NA 50% de l'activité du virus NA. S'il vous plaît cliquer ici pour voir une version plus grande de ce chiffre.
| Virus | dilution de virus nécessaire | 1x dosage volume tampon (uL) | Surfactant-ampère-NP-40 (10%) (ml) | Virus volume (ml) |
| 1 | 1/20 | 940 | dix | 50 |
| 2 | 1/40 | 965 | dix | 25 |
| 3 | 1/100 | 890 | dix | dix |
Tableau 1: Préparation de dilutions de virus pour le virus de 1, 2 et 3 dans l'essai d'inhibition de NA.
| Type de virus / sous-type / lignée | inhibition normale | inhibition réduite | inhibition très réduite |
| (NI) | (RI) | (HRI) | |
| A (H1N1) pdm09 | <10 fois | 10-100 fois | > 100 fois |
| A (H3N2) | &# 60; 10 fois | 10-100 fois | > 100 fois |
| B Yamagata et B Victoria | <5 fois | 5-50 fois | > 50 fois |
Tableau 2: Le Groupe de travail OMS a recommandé des lignes directrices pour Antiviral la classification de la sensibilité du virus de la grippe aux inhibiteurs de NA.
| Type de virus / sous-type / lignée | N | zanamivir | oseltamivir | peramivir | Laninamivir |
| Médiane (plage) IC 50 nM | Médiane (plage) IC 50 nM | Médiane (plage) IC 50 nM | Médiane (plage) IC 50 nM | ||
| A (H1N1) pdm09 | 1326 | 0,42 (0,1 à 3,43) | 0,36 (0,01 à 3,48) | 0,19 (0,07 à 1,60) | 0,55 (0,05 à 2,29) |
| A (H3N2) | 1654 | 0,9 (0,11 à 4,0) | 0,38 (0,01 à 3,65) | 0,33 (0,12 à 3,06) | 1,38 (0,01 à 9,38) |
| B Yamagata et B Victoria | 1.115 | 2,2 (1,24 à 10,72) | 15,12 (2,39 à 70,75) | 1,36 (0,57 à 6,67) | 2,89 (1,62 à 9,15) |
Tableau 3: Median gamme IC 50 IC 50 et de l' inhibition normale virus (NI) à partir de 2015 dérivé CCRRI de l'OMS, Melbourne.
| substitution d'acides aminés | Type / sous-type / lignée | IC 50 facteur de variation compared pour faire référence à des valeurs de CI50 médianes. | |||
| zanamivir | oseltamivir | peramivir | Laninamivir | ||
| H275Y | A (H1N1) pdm09 | 1 | 557 (HRI) | 123 (HRI) | 2 |
| E119V | A (H3N2) | 1 | 63 (RI) | 1 | 1 |
| H134Y | B Victoria | 1 | 4 | 76 (HRI) | 2 |
| N151T | B Victoria | 4 | 4 | 42 (HRI) | 1 |
| G104E | B Victoria | 1220 (HRI) | 87 (HRI) | 17724 (HRI) | 701 (HRI) |
| E105K | B Victoria | 3 | 5 (RI) | 59 (HRI) | 2 |
| I222T | B Victoria | 2 | 7 (RI) | 8 (RI) | 3 |
| H273Y | B Yamagata | 1 | 230 (HRI) | 377 (HRI) | 2 |
| D197N | B Yamagata | 4 | 7 (RI) | 32 (RI) | 3 |
Tableau 4: liste représentative des substitutions d'acides aminés liés à une inhibition réduite (RI) ou une inhibition très réduite (HRI) à des inhibiteurs de NA.
| Problème | Raisons possibles) | Solutions) |
| Non ou faible activité NA | Aucun virus n'a été présent ou faible rendement du virus. | Échantillon clinique doivent être cultivées dans des lignées cellulaires (c. -à- Madin-Darby Canine cellules du rein) ou dans des œufs de poule embryonnésà une charge virale plus élevée pour une utilisation dans l'essai d'inhibition de NA. |
| Certains virus mutants ont une activité extrêmement faible NA, malgré une charge élevée de virus. | Utiliser la concentration de virus propre pour les tests. Un tampon inférieur d'essai de pH (par exemple, pH 5,3) peut être utilisé. Cependant, il faut faire preuve de prudence lorsque l'on compare les données. | |
| Aucune ou faible activité NA NA essai d'inhibition | Aucun virus n'a été ajouté. | Rediluer le virus. Assurez-vous que le virus est directement ajouté dans le tampon d'essai de 1x. |
| dilution du virus incorrect a été utilisé. | Répéter le test d'activité NA. | |
| Insuffisant temps d'incubation. | Vérifiez que le temps d'incubation est suivie. | |
| Les points de données tombent en dehors de la courbe IC 50 | La contamination croisée de l'inhibiteur NA de concentration plus élevée. | Assurez-vous que les conseils ne sont pas en contact avec le NA INHIBItor lors de la distribution de virus dilué dans la plaque à 96 puits. |
| Si un réservoir 8 de puits profonde a été utilisé, jeter et re-distribuer le NA concentrations d'inhibiteur dans un nouveau réservoir 8 de puits profonde. | ||
| Le volume de l'inhibiteur NA ou Muñana ou virus dilué n'a pas été ajouté également dans chaque puits. | Répéter l'essai avec une pipette multi-canal calibré. Veiller à volume égal de chaque réactif est distribué dans chaque puits. | |
| Les valeurs de CI50 anormalement élevés | concentration trop élevée du virus a été ajouté. | Répéter le test d'activité NA et essai d'inhibition de NA. |
| l'échantillon d'essai contient des mélanges de grippe A et de la grippe B. | Effectuer la PCR en temps réel pour identifier la présence de mélanges de virus. | |
| La contamination bactérienne dans l'échantillon | le virus de la culture dans l'état stérile avec la présence d'antibiotiques. | |
| signal de fluorescence de fond élevé | Muñana substrat peut se dégrader au fil du temps. | Utilisez un nouveau lot de Munana subtrate. |
| La détection de la fluorescence des puits voisins. | Utiliser le noir à 96 puits de plaques à fond plat |
Tableau 5: résoudre les problèmes potentiels dans l'essai d'inhibition de NA.
Discussion
La surveillance globale de la sensibilité du virus de la grippe à des inhibiteurs de NA est actuellement effectuée par un certain nombre de laboratoires en utilisant soit des essais de fluorescence ou de chimioluminescence inhibition de NA 11, 12. Le dosage fluorescent est plus couramment utilisé à l'essai chimioluminescent. Bien que les deux essais sont robustes et reproductibles, les valeurs de CI50 obtenues à partir de l'essai à base de fluorescence sont souvent plus élevé que le dosage basé sur la chimiluminescence, en faisant une comparaison directe des données des deux essais difficiles 13. Même avec l'utilisation du même protocole, les données générées par un laboratoire peuvent varier d'une autre. En raison de ces variations entre les laboratoires, le Groupe de travail OMS sur la surveillance de la grippe Antiviral Susceptibilité a produit un guide pour aider à des comparaisons inter-laboratoires. Au lieu de comparer les valeurs de CI50 absolus, cette utilisation indicativeComparaison de sa différence par rapport à la fois IC 50 IC à la médiane 50 du virus de la grippe NI testés dans chaque laboratoire particulier. La possibilité de comparer les données des cinq centres collaborateurs a donné lieu à la publication annuelle des données de sensibilité aux antiviraux mondiale de la grippe 2, 3, 4. La disponibilité de la grande quantité de données de susceptibilité de la grippe dans le domaine public permet aux chercheurs de comparer IC 50 données de ces études avec celles générées dans leurs propres laboratoires.
D'autres tests d'inhibition de NA qui adoptent un concept similaire sont également disponibles dans le commerce. Ces kits commerciaux contenant des réactifs prêts à l'emploi (NA, inhibiteurs non inclus) sont également reproductibles. Cependant, dans la maison test d'inhibition NA est sensiblement moins cher que les kits commerciaux, parce que la majorité des réactifs peut être en maisonde plus grandes quantités et le substrat Munana, qui, auparavant constitué le principal coût de l'essai, peuvent désormais être achetés auprès de diverses sources à des prix compétitifs. Le coût de l'essai d'un isolat de la grippe par médicament est d'environ 1 $ (USD). Au Melbourne WHOCCRRI, des améliorations ont été apportées à l'interne essai d'inhibition NA après l'incorporation d'une plate-forme robotique pour les composants de manipulation de liquides du dosage. En dehors de la préparation manuelle des dilutions de virus, la plupart des procédures sont effectuées à l'aide du robot de manipulation des liquides. Non seulement cela minimiser la manutention manuelle, mais il augmente aussi le nombre de tests qui peuvent être exécutés en un jour.
Bien que le test d'inhibition NA est très robuste, il y a un certain nombre d'étapes critiques qui doivent être remplis avec des soins supplémentaires. Tout d' abord, toute irrégularité dans les concentrations d'inhibiteur de NA peut décaler les courbes d'inhibition et les valeurs de CI50; Par conséquent, une attention particulière devrait êtrepayé lors de la préparation des concentrations d'inhibiteur de NA. En second lieu, pipetage précis et des périodes d'incubation précises sont cruciales pour le maintien des résultats cohérents à travers des essais; cela peut être réalisé en utilisant des pipettes et des minuteries calibrés. L'inclusion des virus de contrôle dans chaque essai permet également le suivi des performances du test de dosage à et sur de longues périodes de temps. En troisième lieu, parce que l'activité de l'enzyme NA des virus de la grippe saisonnière est optimale à un pH de 6,5, le pH correct du tampon d'essai est importante. Certains rapports ont montré que l'utilisation de conditions de pH inférieur peut améliorer l'identification des variantes de la grippe, tels que le variant A (H7N9) contenant la mutation R292K 14, 15. Toutefois, la modification du pH du tampon d'essai se déplacera les valeurs de CI50, ce qui peut compliquer la comparaison des données dans les laboratoires et entre les laboratoires. D'autres modifications et dépannage qui peut être performed sont énumérés dans le tableau 5.
Les inhibiteurs de NA sont la seule classe d'antiviraux approuvés qui sont actuellement efficaces contre les virus grippaux circulants. Jusqu'à ce que les autres classes d'antiviraux sont disponibles pour une utilisation clinique, la surveillance de la sensibilité aux antiviraux des virus grippaux en circulation sera concentrée sur les inhibiteurs de NA seul. En raison de la simplicité et la reproductibilité des résultats, l'utilisation du test d'inhibition NA pour évaluer la sensibilité du virus de la grippe aux inhibiteurs de NA continuera.
Déclarations de divulgation
Les auteurs n'ont rien à dévoiler.
Remerciements
Le Centre collaborateur OMS de référence Melbourne et la recherche sur la grippe est pris en charge par le Ministère australien de la Santé.
matériels
| Name | Company | Catalog Number | Comments |
| Influenza A and B viruses | Cultured in MDCK cells or 9 day old embryonated specific pathogen free (SPF) eggs | ||
| Madin-Darby Canine Kidney (MDCK) cells | ATCC | PTA-6500 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Biosynth AG | M-5507 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Sigma | M8639 | |
| 4-Methylumbelliferone (4-MU) | Sigma | M1381-25G | |
| 2-[N-morpholino]ethanesulphonic acid (MES hydrate) (free acid) | Sigma | M8250-250G | |
| Calcium Chloride (Ca Cl2) | APS AJAX Finechem | 127-500G | |
| Surfactant-Amps-NP-40 (10% solution) | Thermo Fisher Scientific | PIE28324 | |
| Sodium Hydroxide (NaOH) | APS AJAX Finechem | 482-2.5KG | |
| Absolute Ethanol | APS AJAX Finechem | 214-2.5L GL | |
| 96-well clear flat-bottom plates | NUNC | 456537 | |
| 96-well U-bottom plates | Greiner Bio-one | 4650101 | |
| 8 channel deep well block | Pacific Laboratory Products | RES-MW8-HP | |
| 96-well deep plates, 2.0 mL square wells | Pacific Laboratory Products | P-2ML-SQ-C | |
| Plate sealers | Thermo Fisher Scientific | 236366 | |
| Bottle-top vacuum filter system (cellulose membrane (nitrate), pore size 0.2 μm, membrane area 33.2 cm2, filter capacity 500 mL) | Sigma-Aldrich | CLS430758-12EA | |
| Single-channel pipettes (1 µL - 1,000 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Multi-channel pipettes | Variety of suppliers (eg. Eppendorf, Sartorius) | 8 or 12 channel electronic and manual pipette (5 - 1250 µL volume) | |
| Pipette tips (1 µL - 1,250 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Disposable pipettes (10 mL and 25 mL) | Greiner Bio-one | P7740-200EA and P7865-200EA | |
| Pipette controller | Eppendorf | 4430000018 | |
| Centrifuge tubes 50 mL | BD Bioscience | 352070 | |
| Racked tubes | Scientific Specialties, Inc. | 1750-00 | |
| Fluorometer with excitation wavelength setting of 355 nm and an emission wavelength setting of 460 nm | TermoFisher Scientific | ASCENT FL 374 | |
| Ascent software | TermoFisher Scientific | 5185410CD | |
| Incubator set at 37 °C | Lab Supply | Biocell 1000 | |
| Zanamivir | GlaxoSmithKline | Request directly from the company | |
| Oseltamivir carboxylate | Roche | ||
| Peramivir (BCX-1812) | BioCryst | ||
| Laninamivir (R-125489) | Daiichi-Sankyo | ||
| JASPR v1.2 | Influenza Division at the CDC Atlanta, USA | freely available upon request (fluantiviral@cdc.gov) |
Références
- Moscona, A. Neuraminidase inhibitors for influenza. N.Engl.J.Med. 353 (13), 1363-1373 (2005).
- Hurt, A. C., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 132, 178-185 (2016).
- Meijer, A., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 110, 31-41 (2014).
- Takashita, E., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 117, 27-38 (2015).
- Lackenby, A., et al. Emergence of resistance to oseltamivir among influenza A(H1N1) viruses in Europe. Euro Surveill. 13 (5), (2008).
- Hurt, A. C., et al. Community transmission of oseltamivir-resistant A(H1N1)pdm09 influenza. N Engl J Med. 365 (26), 2541-2542 (2011).
- Takashita, E., et al. Characterization of a large cluster of influenza A(H1N1)pdm09 viruses cross-resistant to oseltamivir and peramivir during the 2013-2014 influenza season in Japan. Antimicrob Agents Chemother. 59 (5), 2607-2617 (2015).
- Eisfeld, A. J., Neumann, G., Kawaoka, Y. Influenza A virus isolation, culture and identification. Nat Protoc. 9 (11), 2663-2681 (2014).
- . Meetings of the WHO working group on surveillance of influenza antiviral susceptibility - Geneva, November 2011 and June 2012. Wkly Epidemiol Rec. 87 (39), 369-374 (2012).
- Okomo-Adhiambo, M., Hurt, A. C., Gubareva, L. V. The chemiluminescent neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 95-113 (2012).
- Hurt, A. C., Okomo-Adhiambo, M., Gubareva, L. V. The fluorescence neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 115-125 (2012).
- Analysis of IC50 data. isirv Antiviral Group (isirv-AVG) Available from: https://isirv.org/site/index.php/methodology/analysis-of-ic50-data (2016)
- Sleeman, K., et al. R292K substitution and drug susceptibility of influenza A(H7N9) viruses. Emerg Infect Dis. 19 (9), 1521-1524 (2013).
- Gubareva, L. V., Robinson, M. J., Bethell, R. C., Webster, R. G. Catalytic and framework mutations in the neuraminidase active site of influenza viruses that are resistant to 4-guanidino-Neu5Ac2en. J Virol. 71 (5), 3385-3390 (1997).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon