Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Determinación de la eficiencia de los inhibidores químicos contra el crecimiento de toxoplasma intracelular Gondii mediante un ensayo de crecimiento basado en Luciferase
En este artículo
Resumen
Aquí se presenta un protocolo para evaluar la eficacia de la inhibición de los compuestos químicos contra el crecimiento intracelular in vitro de Toxoplasma gondii utilizando un ensayo de crecimiento basado en luciferasa. La técnica se utiliza para confirmar la especificidad de la inhibición mediante la eliminación genética del gen diana correspondiente. La inhibición de LHVS contra la proteasa TgCPL se evalúa como ejemplo.
Resumen
El toxoplasma gondii es un patógeno protozoario que afecta ampliamente a la población humana. Los antibióticos actuales utilizados para tratar la toxoplasmosis clínica son limitados. Además, exhiben efectos secundarios adversos en ciertos grupos de personas. Por lo tanto, el descubrimiento de nuevas terapias para la toxoplasmosis clínica es imperativo. El primer paso del desarrollo de antibióticos novedosos es identificar compuestos químicos que muestren una alta eficacia en la inhibición del crecimiento del parásito utilizando una estrategia de cribado de alto rendimiento. Como patógeno intracelular obligatorio, el toxoplasma sólo puede replicarse dentro de las células huésped, lo que prohíbe el uso de mediciones de absorbancia óptica como un indicador rápido de crecimiento. Aquí se presenta un protocolo detallado para un ensayo de crecimiento basado en luciferasa. Como ejemplo, este método se utiliza para calcular el tiempo de duplicación de los parásitos toxoplasma de tipo salvaje y medir la eficacia de morpholinurea-leucyl-homophenyl-vinyl sulfone phenyl (LHVS, un compuesto de cisteína proteasa-targeting) con respecto a la inhibición del crecimiento intracelular del parásito. También se describe un protocolo de eliminación de genes basado en CRISPR-Cas9 en Toxoplasma que utiliza regiones homólogas de 50 bp para la recombinación dependiente de la homología (HDR). Al cuantificar las eficacias de inhibición de LHVS en parásitos de tipo salvaje y TgCPL (Toxoplasma catepsina L-como proteasa) -parásitos deficientes), se muestra que LHVS inhibe el crecimiento de parásitos de tipo salvaje de manera más eficiente que el crecimiento de la écpl, lo que sugiere que TgCPL es un objetivo al que LHVS se une en Toxoplasma. La alta sensibilidad y fácil operación de este ensayo de crecimiento basado en luciferasa lo hacen adecuado para monitorear la proliferación de Toxoplasma y evaluar la eficacia de los fármacos de una manera de alto rendimiento.
Introducción
El toxoplasma gondii es un parásito intracelular obligado de gran éxito que infecta aproximadamente un tercio de la población humana. Su alta tasa de transmisión se debe principalmente a sus diversas vías de transmisión, incluyendo el consumo de carne poco cocida, la exposición a los reservorios de mamíferos y la transmisión congénita durante el nacimiento. T. gondii provoca principalmente infecciones oportunistas que pueden conducir a una morbilidad y mortalidad graves en individuos inmunocomprometidos1,2,3,4,5,6. Los antibióticos utilizados actualmente para el tratamiento de la toxoplasmosis aguda son particularmente ineficientes en el tratamiento de infecciones congénitas y latentes y causan reacciones graves en algunos individuos3,7,8. Por lo tanto, existe una necesidad urgente de identificar nuevas terapias. Comprender las diferencias en los procesos subcelulares dentro de Toxoplasma y su huésped ayudará a identificar posibles objetivos farmacológicos. Por lo tanto, se requieren técnicas de manipulación del genoma eficientes y convenientes para estudiar las funciones de los genes individuales dentro de Toxoplasma. Además, Toxoplasma pertenece al phylum Apicomplexa, que incluye varios otros patógenos humanos significativos, como Plasmodium spp. y Cryptosporidium spp. Por lo tanto, toxoplasma se puede utilizar como un organismo modelo para ayudar a estudiar la biología básica en otros parásitos apicomplexanos.
Para identificar nuevos antibióticos contra patógenos microbianos, se realiza inicialmente un cribado de alto rendimiento de una biblioteca de compuestos químicos para determinar su eficacia en la represión del crecimiento microbiano. Hasta ahora, se han desarrollado varios ensayos de crecimiento basados en microplacas para medir el crecimiento intracelular de T. gondii (es decir, cuantificación radiactiva basada en la incorporación de 3H-uracil9, detección cuantitativa de parásitos basada en ELISA utilizando anticuerpos específicos de T. gondii10,11, medición basada en proteínas de reportero utilizando cepas de toxoplasma 12,,13y un ensayo de imágenes de alto contenido desarrollado recientemente14).
Todas estas estrategias individuales tienen ventajas únicas; sin embargo, ciertas limitaciones también restringen sus aplicaciones. Por ejemplo, dado que el toxoplasma sólo puede replicarse dentro de células animales nucleadas, la autofluorescencia y la unión no específica de anticuerpos anti-T.gondii a las células huésped causan interferencia en las mediciones basadas en fluorescencia. Además, el uso de isótopos radiactivos requiere un cumplimiento de seguridad especial y posibles problemas de seguridad. Algunos de estos ensayos son más adecuados para evaluar el crecimiento en un solo punto de tiempo en lugar de un monitoreo continuo del crecimiento.
Aquí se presenta un protocolo basado en la luciferasa para la cuantificación del crecimiento intracelular del toxoplasma. En un estudio anterior, el gen NanoLuc luciferase fue clonado bajo el promotor de la tubulina Toxoplasma, y esta construcción de expresión de luciferasa fue transfigurada en parásitos de tipo salvaje (cepa dehúmúxtas RHku80)para crear una cepa deRH-ku80-hxg::NLuc (denominada RHku80::NLuc en adelante)15. Esta cepa sirvió como la cepa parental para la determinación del crecimiento intracelular y la eliminación de genes en este estudio. Usando elRH ku80::Cepa NLuc, el crecimiento del parásito en fibroblastos de prepucio humano (HHF) fue monitoreado durante un período de 96 horas después de la infección para calcular el tiempo de duplicación del parásito.
Además, la eficacia de inhibición de LHVS contra el crecimiento de parásitos se puede determinar trazando las tasas de crecimiento de Toxoplasma contra las concentraciones seriales de LHVS para identificar el valor IC50. La literatura anterior ha informado de que TgCPL es un objetivo importante de LHVS en parásitos y que el tratamiento con LHVS disminuye el desarrollo de infecciones agudas y crónicas por toxoplasma 16,,17,18,19. Además, RHku80::NLuc se utilizó como la cepa parental para la modificación del genoma para generar una cepa deficiente de TgCPL(RHs ku80ácpl::NLuc), y la inhibición de LHVS se midió contra este mutante. Al observar un cambio ascendente de valores IC50 para LHVS en los parásitos con deficiencia de TgCPLen comparación con la cepa WT, se validó que TgCPL está dirigido por LHVS in vivo.
En este protocolo, RHku80::NLuc se utiliza como cepa parental, que carece de una vía de unión final no homóloga eficiente (NHEJ), facilitando así la recombinación dependiente de la homología de doble cruce (HDR)20,21. Además, las regiones homólogas de 50 bp están flanqueadas en ambos extremos de un casete de resistencia a fármacos por PCR. El producto PCR sirve como plantilla de reparación para eliminar todo el origen genético a través de HDR utilizando herramientas de edición del genoma basadas en CRISPR-Cas9. Estas regiones homolometales cortas se pueden incorporar fácilmente en las imprimaciones, proporcionando una estrategia conveniente para la producción de la plantilla de reparación. Este protocolo se puede modificar para realizar la eliminación universal de genes y el etiquetado genético endógeno.
Por ejemplo, en nuestra publicación más reciente, tres genes de proteasa, TgCPL, TgCPB (Toxoplasma catethepsin A B-like protease), y TgSUB1 (Toxoplasma subtilisina-like protease 1), fueron genéticamente ablados en TgCRT (Toxoplasma chloroquine-resistance transporter) -parásitos deficientes utilizando este método15. Además, TgAMN (a putative aminopeptidase N [TgAMN, TGGT1_221310]) fue etiquetado endógenamente15. El laboratorio de Lourido también informó utilizando regiones homoólogas cortas en el rango de 40-43 bp para la introducción de la mutación genética dirigida por el sitio y el etiquetado genético endógeno en el genoma de Toxoplasma utilizando un método similar22. Estas modificaciones exitosas del genoma sugieren que una región homóloga de 40-50 bp es suficiente para una recombinación eficiente del ADN en la cepa deficiente de TgKU80,lo que simplifica en gran medida la manipulación del genoma en Toxoplasma gondii.
Protocolo
El toxoplasma gondii se clasifica en el Grupo de Riesgo 2 y debe manejarse en un Nivel de Bioseguridad 2 (BSL-2). El protocolo ha sido revisado y aprobado por el Comité Institucional de Bioseguridad de la Universidad de Clemson.
1. Ensayo de crecimiento de Toxoplasma basado en Luciferasa
- Fibroblastos de prepucio humano de semilla (HHF) 1 semana antes de la inoculación del parásito para asegurar que las células huésped sean completamente confluentes. Realice un ensayo simulado en una placa transparente para asegurarse de que los parásitos permanezcan intracelulares durante todo el período de evaluación.
NOTA: Aquí, el ensayo se lleva a cabo en 96 microplacas de pozo. Según las necesidades experimentales, se puede escalar hasta 384 o 1536 microplacas de pozo. - Pasar los parásitos toxoplasma a los FHF confluentes 2 días antes de su uso mediante la transferencia de 0,3 a 0,4 ml de parásitos completamente lisados en un matraz T25. Incubar células huésped infectadas a 37 oC con 5% deCO2 durante 2 días.
- Jeringa de 5 ml de parásitos recién lisados a través de una aguja de seguridad de 21 G 5x para liberar parásitos intracelulares, luego pasa a través de un filtro de 3 m para eliminar los desechos de células huésped. Enjuague los parásitos residuales fuera del matraz usando 7 ml de medio D10 libre de fenol y, a continuación, pase a través del filtro de nuevo.
- Parásitos centrífugos a 1000 x g durante 10 min a temperatura ambiente (RT). Vierta el sobrenadante y resuspenda el pellet en 10 ml de medios D10 libres de fenol.
- Cuente los parásitos usando un hemocaquímetro para determinar la concentración.
- Diluir los parásitos a 1 x 104 parásitos/ml para la cepa de tipo silvestre (WT). Para cepas de parásitos con deficiencia de crecimiento, aumentar la concentración en consecuencia para observar un aumento significativo en las señales de luciferasa.
- Aspirar los medios cuidadosamente de 96 microplacas de pozo pre-sembradas con FFC e inocular 150 ol de resuspensión de parásitos en pozos en un formato de tres columnas y cinco filas, lo que representa tres réplicas técnicas y cinco puntos de tiempo.
- Incubar la microplaca a 37oC y 5%CO2 durante 4 h.
- Aspirar los medios cuidadosamente de los pozos para eliminar los parásitos no invasivos, a continuación, llenar los pozos con RT fenol rojo-libre de medios en cada fila (excepto para la primera fila).
- Mezclar volúmenes iguales de PBS y 2x tampón de ensayo luciferasa y diluir el sustrato de luciferasa a 12,5 m.
- Añadir 100 l de sustrato diluido de luciferasa en cada pocal de la fila superior. Incubar las microplacas a RT durante 10 minutos para permitir que las células se alimenten por completo.
- Mida la actividad de la luciferasa con un lector de microplacas. Los ajustes del lector de placas se enumeran en la Tabla 1. Cada lectura representa el número inicial de parásitos invasores a 4 h después de la infección.
- Repita los pasos 1.9-1.12 para cada fila cada 24 h durante 4 días sin cambiar el medio. Estas lecturas reflejan el número total de parásitos replicados a 24 h, 48 h, 72 h y 96 h después de la infección.
- Calcule las lecturas promedio en cada punto de tiempo y divídalas por las lecturas promedio a 4 h para determinar los cambios de pliegue en el crecimiento del parásito a lo largo del tiempo.
- Trazar los datos utilizando el software de gráficos. En la Figura 1A,Bse muestra una tabla de lectura de crecimiento representativa y parcelas de RHku80:: Los parásitosNLuc.
- Para calcular el tiempo de duplicación, trace los valores log2 de los cambios de pliegue en los puntos de tiempo individuales durante el tiempo de incubación. Utilice una función de regresión lineal para calcular la pendiente, que representa el tiempo de duplicación de cada deformación unitaria(Figura 1A,C).
2. Evaluación de la eficacia de la inhibición de compuestos químicos contra el crecimiento de Toxoplasma
NOTA: Aquí, la evaluación de la inhibición de LHVS en el crecimiento de Toxoplasma se presenta como un ejemplo. Se prueban ocho concentraciones diferentes de LHVS, y se realizan tres réplicas técnicas para cada una de las tres réplicas biológicas tanto para RHku80::NLuc como para RHku80cpl::NLuc strains.
- Antes de la infección por parásitos, semilla SFC a 96 microplacas de pozo en el formato de tres filas y nueve columnas para una réplica biológica por compuesto por cepa. Las células anfitrionas podrán crecer durante al menos 7 días antes de su uso.
- Pasar RHku80::NLuc y RHku80ácpl::NLuc parásitos durante 2 días antes de su uso. Siga los pasos 1.2-1.6 para la purificación y cuantificación de parásitos. Resuspender parásitos en medios libres de rojo fenol a 1 x 104 parásitos/ml.
- Aspirar los medios de una placa que contenga FHF confluentes e inocular cada pozo con 150 l de resuspensión del parásito. Incubar la microplaca a 37oC y 5%CO2 durante 4 h.
- Preparar LHVS a ocho concentraciones diferentes en un depósito de 12 poques por dilución en serie. Generalmente, las concentraciones se reducen por tres veces de forma de dilución en serie.
NOTA: La concentración más baja se reduce en 6.561 veces en comparación con la concentración más alta. El cambio de plegado de la dilución se puede ajustar en consecuencia en función de las diferentes propiedades de los compuestos individuales. - A 4 h después de la infección, aspirar medios para eliminar parásitos no invasivos y llenar cada pozo de las columnas 2-9 con 150 l de medios complementados con LHVS a diferentes concentraciones. Deje la primera columna llena de medio regular para servir como un control no tratado.
- Incubar la microplaca a 37oC y 5%co2 durante 96 h adicionales.
- Realice los pasos 1.9-1.11 y mida la actividad luciferasa de los pozos individuales.
- Promedio de las actividades de luciferasa de tres réplicas técnicas de los pozos de cada concentración individual de LHVS.
- Divida la actividad media de luciferasa para cada concentración de LHVS por la actividad media de luciferasa derivada de parásitos no tratados para calcular la actividad luciferasa normalizada como un porcentaje.
- Trazar las actividades de luciferasa normalizadas contra las concentraciones individuales de LHVS utilizando un software de gráficos(Figura 2). La inhibición de la pirimetamina contra el crecimiento del parásito también se mide como un control. La pirimetamina es un antibiótico clínico utilizado para tratar la toxoplasmosis aguda mediante la inhibición del metabolismo del ácido fólico en toxoplasma.
- Calcule los valores de IC50 para compuestos individuales utilizando el método integrado en el software de gráficos, respuesta normalizada frente a [inhibidor], bajo el programa de regresión "dosis-respuesta-inhibición". El IC50 se calcula utilizando la siguiente fórmula:
Y 100/(1 + X/IC50)
Dónde: Y representa las actividades de luciferasa normalizadas de las células infectadas bajo diferentes concentraciones de inhibidor, y X representa las concentraciones individuales de inhibidor.
3. Deleción de genes basada en CRISPR-Cas9 en parásitos toxoplasma
- Generación de una construcción plásmida que expresa ARN guía (sgRNA) y Cas9 para eliminar un gen de interés
- Vaya a www.ToxoDB.org y recupere toda la secuencia de codificación genética, incluidos los intrones y exons, junto con 1,5 kb 5'-UTRs y 3'-UTRs (regiones no traducidas).
NOTA: Aquí, TgCPL (TGGT1_321530) está dirigido como un ejemplo representativo. - Copie la secuencia TgCPL recuperada en el software de análisis de secuencia (consulte Tabla de materiales para el nombre y la versión) y etiquete las regiones 5'- y 3'-UTR.
- Seleccione el icono Herramientas en la barra de menús superior y, a continuación, seleccione Clonación . Encontrar SITIOS CRISPR.
- Elija 3'(Cas9)' para la ubicación del sitio PAM y seleccione la carpeta que contiene la secuencia del genoma de Toxoplasma en la sección de puntuación de especificidad. Deje el resto de la configuración como valores predeterminados.
- Elija un sgRNA con los siguientes dos criterios: 1) que muestre una puntuación de especificidad alta, generalmente >98%, y 2) que carece de una G después de la NGG, una secuencia de motivos adyacentes protoespaciales (PAM). El sgRNA seleccionado se encuentra generalmente en sitios cercanos al inicio y detención de los codones del gen de interés.
- Copie la secuencia del sgRNA seleccionado y péguelo en la siguiente plantilla de imprimación.

La parte en rojo representa la secuencia de sgRNA TgCPL seleccionada. Se puede reemplazar con diferentes sgRNA para varios genes de interés.
NOTA: Si el sgRNA seleccionado no comienza con G, agregue G al principio del sgRNA para ayudar a mejorar su expresión. - Realizar una reacción de PCR para modificar el plásmido preexistente que expresa el ARNNM (Figura 3A) que se dirige algen Toxoplasma uracilfosiltransferasa (TgUPRT) utilizando una premezcla de PCR con los ajustes proporcionados en el Cuadro 2.
- Ejecute el producto PCR en un gel de agarosa para confirmar la amplificación exitosa. Se espera que se amplíe un producto PCR de 10 kb(Figura 3B).
- Extraiga el producto PCR utilizando un kit de extracción de gel de ADN y orizarlo utilizando un kit de mutagénesis dirigido por el sitio. Consulte la Tabla 3 para ver la receta. Incubar la reacción durante 10-20 min a RT.
- Transforme el producto PCR circularizado en E. coli y elija 10 clones para una mayor verificación de la incorporación de sgRNA diseñado.
- Cultiva dos clones y extrae plásmidos. Corte los plásmidos purificados con BamHI y EcoRV. Los plásmidos candidatos producirán dos bandas a 2,4 kb y 7,2 kb(Figura 3C).
- Envíe los plásmidos para la secuenciación de Sanger utilizando imprimaciones inversas M13 para confirmar el reemplazo exitoso de sgRNA TgUPRT con el sgRNA diseñado(Figura 3D).
- Vaya a www.ToxoDB.org y recupere toda la secuencia de codificación genética, incluidos los intrones y exons, junto con 1,5 kb 5'-UTRs y 3'-UTRs (regiones no traducidas).
- Generación de plantilla de reparación para la eliminación de genes a través del mecanismo HDR
- De acuerdo con los sitios de destino del sgRNA seleccionado, localice 50 bp de 5'-UTRs o 3'-UTRs del gen objetivo para la recombinación dependiente de la homología (HDR, ver sección de discusión). La selección de regiones sigue los criterios enumerados a continuación, dependiendo de la ubicación en la que se dirige el ARNS SgRNA.
- Si el sitio de escote de Cas9 se encuentra aguas arriba desde el codón de inicio, seleccione lo siguiente: una secuencia de ADN de 50 bp aguas arriba del sitio de escisión como la región HDR izquierda y una secuencia de ADN de 50 bp aguas abajo del codón de parada como la región HDR derecha.
- Si el sitio de escote de Cas9 está entre los codones de inicio y parada, seleccione lo siguiente: una secuencia de ADN de 50 bp aguas arriba desde el codón de inicio como la región HDR izquierda y una secuencia de ADN de 50 bp aguas abajo del codón de parada como la región HDR derecha.
- Si el sitio de escote de Cas9 se encuentra aguas abajo del codón de la parada, seleccione lo siguiente: una secuencia de ADN de 50 bp aguas arriba desde el codón de inicio como la región HDR izquierda y una secuencia de ADN de 50 bp aguas abajo del sitio de escisión como la región HDR derecha.
NOTA: Para el gen TgCPL, el sitio de escote se encuentra entre los codones de inicio y parada. Por lo tanto, los siguientes imprimadores están diseñados para amplificar la plantilla de reparación utilizando pMDC64 como plantilla, que codifica un casete de resistencia a la pirimetamina. Las secuencias en negro anneal al plásmido pMDC64 para amplificación de PCR. Las regiones etiquetadas en rojo son secuencias específicas de TgCPLpara la recombinación homóloga.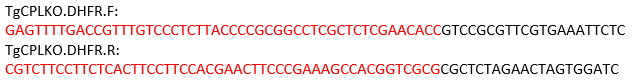
- Realice el PCR utilizando una premezcla de PCR en las condiciones PCR descritas en el Cuadro 4.
- Ejecute el producto PCR en un gel de agarosa(Figura 3E),seguido de la extracción de gel y los procedimientos estándar de cuantificación de ácido nucleico.
NOTA: Si la banda esperada no se puede amplificar correctamente, optimice las condiciones de PCR y/o cambie los pares de imprimación.
- De acuerdo con los sitios de destino del sgRNA seleccionado, localice 50 bp de 5'-UTRs o 3'-UTRs del gen objetivo para la recombinación dependiente de la homología (HDR, ver sección de discusión). La selección de regiones sigue los criterios enumerados a continuación, dependiendo de la ubicación en la que se dirige el ARNS SgRNA.
- Toxoplasma transfección
- Pase RHku80::Parásitos NLuc durante 2 días en un matraz T25 que contiene HIF confluentes. Un matraz T25 de parásitos completamente lisados es suficiente para dos o tres transfecciones.
- Jeringa y parásitos de purificación de filtros como se describe en el paso 1.2. Resuspenda los parásitos en el tampón de citomezcla y gire hacia abajo a 1.000 x g durante 10 min a RT.
- Lavar los parásitos peletizaron con 10 ml de tampón de citomezcla y espíre los parásitos a 1.000 x g durante 10 min a RT.
- Vierta cuidadosamente el sobrenadante y resuspenda los parásitos en el mismo tampón a una concentración de 1 x 108 parásitos/ml.
- Mezclar 2 g de ADN de la plantilla de reparación con 20 g de los plásmidos de expresión sgRNA/Cas9 (relación de masa 1:5, equivalente a una relación molar de 1:3). Si el rendimiento de amplificación de la plantilla de reparación es bajo, reduzca la entrada de ambas piezas de ADN en consecuencia. Se puede utilizar un mínimo de 0,5 g de plantilla de reparación.
- Mezclar 400 l de resuspensión de parásitos, ADN y 5 l de 200 mM de glutatión reducido (GSH) en un tubo de centrífuga de 1,5 ml. Lleve el volumen total a 500 ol con tampón de citomezcla, si es necesario.
- Transfiera la mezcla de parásitos y ADN a una cubeta de electroporación (4 mm de ancho de brecha) y realice la electroporación (voltaje de 2 kV, resistencia de 50o) utilizando un aparato de electroporación.
- Transfiera parásitos electroportados a un matraz T25 que contenga HIF confluentes en medio D10 fresco. Aplicar antibiótico adecuado para la selección de medicamentos después de las 24 h.
- Mantenga la presión selectiva del fármaco hasta que el crecimiento de los parásitos transgénicos sea estable.
- Purificar el ADN genómico de la población eliminatoria y comprobar la integración del casete de resistencia a la pirimetamina en el locus TgCPL por PCR. Después de verificar, proceda a la sección 3.4. Si no es así, realice otra ronda de transfección de parásitos y selección de medicamentos. La incapacidad para detectar la correcta integración del casete de resistencia a los fármacos suele sugerir que el gen objetivo es esencial o que el locus genético no es accesible.
- Clonación de parásitos nocaut
- Semilla dos microplacas de 96 pocillos con células HFF e incubar a 37oC y 5%CO2 durante 1 semana antes de clonar parásitos.
- Pasar 0,3-0,4 ml de la población de parásitos transgénicos en un matraz T25 que contenga FHF confluentes y cultivarlos durante 2 días. Considere la posibilidad de pasar más parásitos si el mutante muestra defectos de crecimiento.
NOTA: Para lograr el mejor rendimiento y viabilidad, las células huésped están fuertemente infectadas por los parásitos, y la mayoría de los parásitos se mantienen en la etapa intracelular. - Células huésped infectadas por jeringas y parásitos recién lisados con filtro como se menciona en el paso 1.3. Resuspende los parásitos en el medio D10 y gíralos a 1.000 x g durante 10 min a RT.
- Resuspender los parásitos peletizares en 10 mL de medio D10.
- Cuente los parásitos usando un hemocitómetro para determinar la concentración del parásito.
- Realizar una dilución en dos pasos para llevar la concentración a 10 parásitos/ml en medio D10 complementado con el antibiótico adecuado. Por lo general, la resuspensión inicial del parásito se diluye por 1.000 veces, seguida de una segunda dilución a 10 parásitos/ml.
- Aspirar medios de microplacas de 96 pozos que contengan FHF confluentes e inocular 150 ol de parásitos diluidos en cada poca.
- Incubar placas a 37oC con 5% deCO2 durante 7 días sin perturbaciones para permitir la formación de placas. El período de incubación puede ser más largo si los parásitos transgénicos presentan defectos de crecimiento.
- Realice una pantalla de las placas con un microscopio de contraste de fase y marque solo los pocillos que contienen una sola placa.
- Realice la PCR de la colonia para identificar los clones correctos.
- Utilice puntas de pipeta para raspar la parte inferior de cada pozo para levantar las monocapas HFF infectadas.
- Pipet 75 l de la resuspensión celular de cada uno marcado bien en tubos de microcentrífuga de 1,5 ml.
- Tubos de centrífuga durante 10 minutos a velocidad máxima a RT. Aspirar cuidadosamente el sobrenadante y resuspender el pellet en 10,25 l de tampón de lisis que contiene tampón de dilución y aditivo de liberación de ADN proporcionado en el kit(Tabla de materiales).
- Incubar las muestras durante 4 min a RT, luego 2 min a 98oC. Después, las muestras se pueden utilizar para PCR o almacenarse a -20 oC hasta su uso. Se utilizan tres conjuntos de reacciones pcR para comprobar la integración del casete de resistencia a los fármacos y la pérdida del gen de interés(Figura 4A). Refiera al cuadro 5 para la configuración de la reacción PCR y a la tabla 6 para las configuraciones del termociclador.
- Identifique los clones correctos y transfiera cuatro clones a matraces T25 que contengan HIF confluentes.
- Después de que los clones individuales lisen las células huésped, purifique el ADN genómico para una mayor verificación de LA PCR.
- Si hay disponible un anticuerpo que reconoce la proteína de interés, siga un procedimiento de inmunoblotting estándar para verificar la pérdida de la proteína diana en los golpes correctos de Toxoplasma. En la Figura 4B,Cse muestran imágenes representativas para la detección de un mutante de eliminación de TgCPL.
Resultados
La Figura 1 representa un ejemplo de una curva de crecimiento para la tensión RHku80::NLuc y el cálculo derivado para su tiempo de duplicación. Generalmente, el ensayo se realiza en tres réplicas técnicas para cada una de las tres réplicas biológicas para tener en cuenta las variaciones de las lecturas de actividad de la luciferasa. Con el fin de calcular el cambio de pliegue normalizado del crecimiento del parásito, cada lectura a 2...
Discusión
++Este protocolo describe un protocolo basado en la luciferasa para evaluar el crecimiento de Toxoplasma intracelular y evaluar la eficacia de inhibición de los compuestos químicos contra el crecimiento del parásito. En comparación con las estrategias existentes disponibles para medir el crecimiento de Toxoplasma intracelular, este método presenta alta sensibilidad y especificidad. Mientras se supervisa el crecimiento del parásito, se recomienda un ensayo simulado en una microplaca transparente de...
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Los autores desean dar las gracias a los Doctores Sibley y Carruthers por compartir los anticuerpos pSAG1-Cas9-sgRNA-TgUPRT y anti-TgCPL y TgActin. Este trabajo fue apoyado por el fondo Clemson Startup (a Z.D.), Knights Templar Eye Foundation Pediatric Ophthalmology Career-Starter Research Grant (a Z.D.), una subvención piloto de una subvención NIH COBRE P20GM109094 (a Z.D.), y NIH R01AI143707 (a Z.D.). Los funderos no tenían ningún papel en el diseño del estudio, la recopilación y el análisis de datos, la decisión de publicar o la preparación del manuscrito.
Materiales
| Name | Company | Catalog Number | Comments |
| Agarose gel extraction kit | New England BioLabs | T1020L | |
| BamHI | New England BioLabs | R0316S | |
| Biotek Synergy H1 Hybrid Multi-Mode Microplate Reader | BioTek Instuments | ||
| BTX Gemini Twin Waveform Electroporation System | Harvard Apparatus | ||
| Chemically competent E. coli cells | New England BioLabs | C29871 | |
| CloneAmp HiFi PCR premix | Takara Bio | 639298 | |
| Coelenterazine h | Prolume | 301-10 hCTZ | |
| EcoRV | New England BioLabs | R3195S | |
| Phire Tissue Direct PCR Master Mix | Thermo Scientific | F170L | |
| Plasmid miniprep kit | Zymo Research | D4054 | |
| Q5 Site-Directed Mutagenesis kit | New England BioLabs | E0554S | |
| Software | |||
| Geneious software for sgRNA design (version: R11) | |||
| GraphPad Prism software (8th version) | |||
| SnapGene for molecular cloning (version: 4.2.11) |
Referencias
- Blader, I. J., Coleman, B. I., Chen, C. T., Gubbels, M. J. Lytic Cycle of Toxoplasma gondii: 15 Years Later. Annual Review of Microbiology. 69 (1), 1-23 (2014).
- Jones, J. L., Kruszon-Moran, D., Rivera, H., Price, C., Wilkins, P. P. Toxoplasma gondii Seroprevalence in the United States 2009-2010 and Comparison with the Past Two Decades. The American Journal of Tropical Medicine and Hygiene. 90 (6), (2014).
- Kieffer, F., Wallon, M. Congenital toxoplasmosis. Handbook of Clinical Neurology. 112, 1099-1101 (2013).
- Hoffmann, S., Batz, M. B., Morris, G. J. Annual cost of illness and quality-adjusted life year losses in the United States due to 14 foodborne pathogens. Journal of Food Protection. 75 (7), 1292-1302 (2012).
- Dubey, J. Toxoplasmosis. Journal of the American Veterinary Medical Association. 205 (11), 1593-1598 (1994).
- Lindsay, D., Dubey, J. Toxoplasma gondii: the changing paradigm of congenital toxoplasmosis. Parasitology. 138 (14), 1-3 (2011).
- Deng, Y., Wu, T., Zhai, S., Li, C. Recent progress on anti-Toxoplasma drugs discovery: Design, synthesis and screening. European Journal of Medicinal Chemistry. 183, 111711 (2019).
- Butler, N. J., Furtado, J. M., Winthrop, K. L., Smith, J. R. Ocular toxoplasmosis II: clinical features, pathology and management. Clinical & Experimental Ophthalmology. 41 (1), 95-108 (2013).
- Pfefferko, E., Pfefferko, L. C. Specific Labeling of Intracellular Toxoplasma gondii with Uracil. Journal of Eukaryotic Microbiology. 24 (3), 449-453 (1977).
- Merli, A., Canessa, A., Melioli, G. Enzyme immunoassay for evaluation of Toxoplasma gondii growth in tissue culture. Journal of Clinical Microbiology. 21 (1), 88-91 (1985).
- Derouin, F., Chastang, C. Enzyme immunoassay to assess effect of antimicrobial agents on Toxoplasma gondii in tissue culture. Antimicrobial Agents and Chemotherapy. 32 (3), 303-307 (1988).
- McFadden, D., Seeber, F., Boothroyd, J. Use of Toxoplasma gondii expressing beta-galactosidase for colorimetric assessment of drug activity in vitro. Antimicrobial Agents and Chemotherapy. 41 (9), 1849-1853 (1997).
- Gubbels, M. J., Li, C., Striepen, B. High-Throughput Growth Assay for Toxoplasma gondii Using Yellow Fluorescent Protein. Antimicrobial Agents and Chemotherapy. 47 (1), 309-316 (2003).
- Touquet, B., et al. High-content imaging assay to evaluate Toxoplasma gondii infection and proliferation: A multiparametric assay to screen new compounds. PLoS ONE. 13 (8), e0201678 (2018).
- Thornton, L. B., et al. An ortholog of Plasmodium falciparum chloroquine resistance transporter (PfCRT) plays a key role in maintaining the integrity of the endolysosomal system in Toxoplasma gondii to facilitate host invasion. PLOS Pathogens. 15 (6), e1007775 (2019).
- Larson, E. T., et al. Toxoplasma gondii cathepsin L is the primary target of the invasion-inhibitory compound morpholinurea-leucyl-homophenyl-vinyl sulfone phenyl. The Journal of Biological Chemistry. 284 (39), 26839-26850 (2009).
- Dou, Z., McGovern, O. L., Cristina, M., Carruthers, V. B. Toxoplasma gondii Ingests and Digests Host Cytosolic Proteins. mBio. 5 (4), e01188-14 (2014).
- Cristina, M., et al. Toxoplasma depends on lysosomal consumption of autophagosomes for persistent infection. Nature Microbiology. 2, 17096 (2017).
- Parussini, F., Coppens, I., Shah, P. P., Diamond, S. L., Carruthers, V. B. Cathepsin L occupies a vacuolar compartment and is a protein maturase within the endo/exocytic system of Toxoplasma gondii. Molecular Microbiology. 76 (6), 1340-1357 (2010).
- Huynh, M. H., Carruthers, V. B. Tagging of endogenous genes in a Toxoplasma gondii strain lacking Ku80. Eukaryotic cell. 8 (4), 530-539 (2009).
- Fox, B. A., Ristuccia, J. G., Gigley, J. P., Bzik, D. J. Efficient gene replacements in Toxoplasma gondii strains deficient for nonhomologous end joining. Eukaryotic Cell. 8 (4), 520-529 (2009).
- Sidik, S. M., Hackett, C. G., Tran, F., Westwood, N. J., Lourido, S. Efficient Genome Engineering of Toxoplasma gondii Using CRISPR/Cas9. PLoS ONE. 9 (6), e100450 (2014).
- Shen, B., Brown, K. M., Lee, T. D., Sibley, D. L. Efficient Gene Disruption in Diverse Strains of Toxoplasma gondii Using CRISPR/CAS9. mBio. 5 (3), e01114-14 (2014).
- Radke, J. R., et al. Defining the cell cycle for the tachyzoite stage of Toxoplasma gondii. Molecular and Biochemical Parasitology. 115 (2), 165-175 (2001).
- Ran, A. F., et al. Genome engineering using the CRISPR-Cas9 system. Nature Protocols. 8 (11), 2281-2308 (2013).
- Labun, K., Montague, T. G., Gagnon, J. A., Thyme, S. B., Valen, E. CHOPCHOP v2: a web tool for the next generation of CRISPR genome engineering. Nucleic Acids Research. 44 (W1), W272-W276 (2016).
- Heigwer, F., Kerr, G., Boutros, M. E-CRISP: fast CRISPR target site identification. Nature Methods. 11 (2), 2812 (2014).
- Peng, D., Tarleton, R. EuPaGDT: a web tool tailored to design CRISPR guide RNAs for eukaryotic pathogens. Microbial Genomics. 1 (4), e000033 (2015).
- Doench, J. G., et al. Rational design of highly active sgRNAs for CRISPR-Cas9-mediated gene inactivation. Nature Biotechnology. 32 (12), 1262-1267 (2014).
- Sidik, S. M., et al. A Genome-wide CRISPR Screen in Toxoplasma Identifies Essential Apicomplexan Genes. Cell. 166 (6), 1423-1435 (2016).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados