Method Article
Génération et quantification 3-Dimensional des lésions artérielles chez la souris utilisant la tomographie optique de projection
Dans cet article
Résumé
Ex vivo analysis of arterial lesions from animal models of cardiovascular disease classically relies on histological and immunohistochemical techniques. These provide 2-dimensional measurements in 3-dimensional lesions. This manuscript describes the generation of arterial lesions for quantitative analysis in 3-dimensions using optical projection tomography.
Résumé
La génération et l'analyse des lésions vasculaires dans des modèles animaux appropriés est une pierre angulaire de la recherche sur les maladies cardiovasculaires, générant d'importantes informations sur la pathogenèse de la formation de la lésion et l'action de nouvelles thérapies. L'utilisation de l'athérosclérose sujettes souris, les méthodes chirurgicales de induction de la lésion, et modification du régime alimentaire a considérablement amélioré la compréhension des mécanismes qui contribuent au développement de la maladie et le potentiel de nouveaux traitements.
Classiquement, l'analyse des lésions est effectuée ex vivo en utilisant des techniques histologiques 2 dimensions. Cet article décrit l'application de tomographie par projection optique (OPT) pour la quantification trois dimensions des lésions artérielles. Comme cette technique est non destructive, elle peut être utilisée comme traitement d'appoint à des analyses histologiques et immunohistochimiques standard.
Néointimales lésions ont été induites par insertion de fil ou une ligature de l'art fémorale de la sourisery tandis que les lésions athérosclérotiques ont été générées par l'administration d'un régime atherogene à des souris déficientes en ApoE.
Les lésions ont été examinées en utilisant l'imagerie de l'OPT de autofluorescente émission suivie par histologique complémentaire et analyse immunohistochimique. OPT lésions clairement distingués de la paroi vasculaire sous-jacente. taille de la lésion a été calculée dans les sections 2 dimensions en utilisant planimétrie, permettant le calcul du volume de la lésion et la zone de section transversale maximale. Les données générées à l'aide OPT étaient en accord avec les mesures obtenues en utilisant l'histologie, ce qui confirme l'exactitude de la technique et son potentiel en tant que complément (plutôt que de remplacement) des méthodes traditionnelles d'analyse.
Ce travail démontre le potentiel de l'OPT pour l'imagerie des lésions athérosclérotiques et néointimales. Il fournit un, si nécessaire ex vivo technique rapide pour la quantification en 3 dimensions de routine de remodelage vasculaire.
Introduction
La formation de lésions artérielles est au cœur du taux élevé de morbidité et de mortalité associé aux maladies cardiovasculaires 1. la formation de la lésion est considérée comme causée par une réponse inflammatoire sans entrave aux blessures artérielle 2. Les lésions athéroscléreuses forment lentement en réponse à une blessure chronique à la paroi artérielle alors que les lésions resténotiques développer rapidement suite à une avarie mécanique aiguë (par exemple, après l'implantation du stent). Les mécanismes qui contribuent au développement de lésions artérielles ont été considérablement clarifié par l'utilisation de modèles animaux appropriés, souvent en combinaison avec des manipulations génétiques pertinents 1.
Analyse de la taille de la lésion et la composition classique a beaucoup dépendu ex vivo, l'histologie 2 dimensions (bien que cela change avec le développement de méthodes améliorées in vivo et ex vivo détection et l'analyse des lésions chez les petits animaux 3). L'analyse histologique des lésions artérielles est de main-d'œuvre, de temps et fournit des informations limitées de la structure en 3 dimensions. Par exemple, la charge de la lésion est généralement évaluée en mesurant la surface de section transversale d'une lésion (que ce soit au niveau de sites sélectionnés de façon aléatoire ou au site d'occlusion maximale). Ceci fournit une analyse incomplète de la charge globale de la lésion. Whole-mount technologie d'imagerie en 3 dimensions offre une solution possible à ce problème, mais étonnamment peu d'approches appropriées ont été décrits. Cela peut être dû principalement à la taille des artères de souris qui sont trop grands pour photon unique microscopie confocale mais trop petit pour l'imagerie par résonance magnétique (IRM) 4 et X-ray tomodensitométrie (TDM) 5. Application de l'IRM et ex vivo micro CT à l'étude des lésions d'athérosclérose chez la souris suggère qu'ils offrent une résolution limitée, même à relativement grosses artères. Ajouté à cela, les temps d'acquisition relativement longs nécessaireslimiter le débit (et augmenter les coûts de numérisation) 4,6.
Développement de nouvelles modalités d'imagerie optique (comme tomographie par cohérence optique 3,7 et photo-acoustique tomographie 8) offre beaucoup de potentiel pour améliorer l'imagerie des lésions dans les artères murins. Potentiel similaire est représenté par tomographie optique de projection (OPT) qui a été développé pour permettre une analyse des embryons de souris. OPT a été conçu pour les spécimens d'image allant de ~ 0,3-10 mm de diamètre 9. Imagerie Transmission enregistre l'opacité d'un échantillon semi-translucide à la lumière visible polychromatique et peut être utilisé pour l'identification de structures anatomiques. Emission dossiers d'imagerie émission de lumière après excitation à des longueurs d'onde spécifiques de endogène (par exemple, le collagène, élastine) et fluorophores exogènes dans l'échantillon. Cela peut également fournir des informations anatomiques (depuis différents composants tissulaires peuvent différer dans le type et la densité des espèces autofluorescentesprésent). En outre, la distribution de l'immunoréactivité ou l'expression du gène peut être déterminé à l'aide de sondes fluorescentes appropriées 10. Pour que soit le mode d'imagerie (transmission ou l'émission), la lumière est focalisé sur un dispositif à couplage de charge pour permettre la capture d'image itératif de la rotation échantillon (généralement 400 images à 0,9 ° incréments). Ceux-ci peuvent être utilisés pour le calcul du volume par des procédés de reconstruction tomographique standards (tels que rétroprojection filtrée (à l'aide d'un algorithme de cône) ou reconstruction itératif).
Cette vidéo démontre notre nouvelle application de l'OPT pour l'analyse en 3 dimensions rapide, quantifiable et rentable des lésions athérosclérotiques et néointimales, comme décrit précédemment dans Kirkby et al. 11. La technique a été montré pour être adapté pour quantifier la taille des lésions en trois modèles couramment utilisés: (i) l'artère fil de blessures fémorale; (Ii) ligature de l'artère fémorale, et (iii) l'athérosclérose induite par l'alimentation en apolipoprotein E déficient (ApoE - / -) chez la souris.
Protocole
1. Induction chirurgicale des lésions néo-intimale dans l'artère fémorale de la souris
- Des expériences utilisant des animaux doivent être effectuées en conformité avec les exigences d'éthique nationaux et institutionnels. Toute chirurgie doit être réalisée en utilisant une technique aseptique appropriée. L'induction de lésions néointima est réalisé en utilisant une modification de la technique décrite par Roque et al. 12 et Sata et al. 13.
- Peser mâle C57BL6 / J souris (Age 10-12 semaines; poids 25-30 g), puis anesthésier en livrant 4-5% d'isoflurane dans une chambre d'induction. Une fois l'anesthésie a été induite, transférer la souris pour un tapis chauffant pour maintenir la température du corps à 37 ° C. Continuer administration de l'isoflurane (2-3%) par l'intermédiaire d'un masque.
- Une fois un niveau approprié de l'anesthésie a été induite (absence de réponse à pincement de l'orteil), fournir une couverture analgésique par l'administration de la buprénorphine (0,1 mg / kg -1). Ensuite, placez la souris dans une position couchée sur le dos d'unD raser la surface ventrale de la patte arrière gauche.
- Faire une incision pour exposer les muscles de la patte arrière supérieure et, entre la bifurcation avec l'artère poplitée et la paroi abdominale, utilisez dissection d'isoler l'artère et la veine fémorale du nerf fémoral. Irriguer la plaie au besoin en utilisant 1% p / v lidocaïne.
- Placez proximale (à proximité de la paroi abdominale) et distale (juste en dessous de la branche avec l'artère poplitée) ligatures temporaires (6/0 Mersilk) autour de l'artère et la veine fémorales pour contrôler le flux de sang. Puis isoler l'artère poplitée (environ 2-5 mm en aval de la branche avec l'artère fémorale) et ligaturer distale. Placez une seconde, ligature déliée sous l'artère poplitée.
- Faire une petite incision (artériotomie) dans l'artère poplitée, immédiatement en aval de la branche avec l'artère fémorale, et prévenir les saignements en appliquant une pression à la ligature temporaire proximale. Avancer d'une droite, jailli 0,014 "fil guide1-1,5 cm le long de l'artère fémorale dans la direction de la paroi abdominale et laisser en place pendant 30 sec (figure 1A).
- Retirer le fil de guidage et ligaturer l'artère poplitée l'artériotomie dessus, en utilisant la ligature placée à cet effet, et en prenant soin de ne pas occlure l'artère fémorale.
NOTE: Pour les lésions induites par ligature. Néointimale remodelage sans préjudice intraluminal peut être induite par la ligature des artères fémorales ou poplitées (Figure 1B et 1C). Pour atteindre cet objectif, suivez les étapes 1.1-1.5. Cependant, ne faites pas l'artériotomie mais (en évitant l'étape 1.6) soit (i) ligaturer l'artère poplitée distale immédiatement à l'artère fémorale ou (ii) ligaturer l'artère fémorale commune au point avec l'artère poplitée de branche. Puis passez à l'étape 1.8. - Supprimer les ligatures temporaires, fermer la plaie avec une suture externe discontinue (5/0 Mersilk) et appliquer la crème EMLA (lidocaïne 2,5%, 2,5% de prilocaïne). Laissez les animaux de re gagner la conscience (habituellement 5-10 min) et veiller à ce qu'ils se déplacent librement autour de leur cage (légère boiterie peut être évident dans la jambe touchée mais cela devrait résoudre au cours des 2-3 premiers jours après la chirurgie) avant de retourner vers les salles. Les souris ne doivent pas être logés séparément après la chirurgie.
- Permettre aux animaux de récupérer jusqu'à 3 mois. Petites lésions commencent à apparaître ~ 7 jours après la blessure de fil et atteindront une taille maximale stable après ~ 21-28 jours.
2. Induction de lésions athérosclérotiques dans le apolipoprotéine E - / - Mice
- Administrer alimentation occidentale (0,2% de cholestérol; Research Diets, USA) en mâle, âgées de 6 semaines les souris ApoE nul (élevés dans la maison) pendant 12 semaines.
- Les lésions athéroscléreuses sont souvent visibles sur l'inspection brut de la crosse de l'aorte et de ses branches principales (figure 2).
3. Analyser artérielle lésions par projection optique tomographie (OPT)
nt "> NOTE: les images de l'OPT de lésions dans les artères fémorales murins et des échantillons de l'arc aortique ont été obtenus en utilisant une projection tomographe optique.- Euthanasier souris par fixation de perfusion transcardiaque et exsanguination sous anesthésie terminale (80 mg / kg de pentobarbital de sodium), en utilisant héparine (10 U / ml) une solution saline tamponnée phosphate (PBS), suivi par 10% de formaline tamponnée neutre.
- Isoler artères fémorales ou la crosse aortique et ses branches principales (gauche de l'artère carotide, l'artère sous-clavière gauche, le tronc brachiocéphalique), le cas échéant, et de retirer le matériau péri-adventitielle étrangère. Post-fix dans 10% formol tamponné O / N, avant stockage dans 70% d'éthanol jusqu'à ce que nécessaire.
- Intégrer dans les artères de 1,5% agarose bas point de fusion, de pré-filtrés Whatman 113 V papier. Fixez chaque échantillon à un OPT fixation magnétique avec de la colle cyanoacrylate avec l'axe du navire en ligne avec celui de la montagne. Coupez l'excédent agarose à une forme conique. Déshydrater dans 100% de methanol pendant au moins 12 heures.
- CLear navires par immersion (par 12-24 h) à un mélange d'alcool benzylique et le benzoate de benzyle (1: 2 v / v).
- Placez échantillons compensés dans un tomographe calibré. Définition de la résolution de 1024 x 1024, et déterminer un grossissement optique qui permet l'ensemble de la zone d'intérêt pour être vu. Le volume OPT est isotrope de l'axe z est reconstruite à la même résolution (par exemple, 1024 x 1024 x 1024), taille de voxel ~ 200 um. Cela peut représenter une surestimation de la résolution car il sont susceptibles d'être des artefacts de reconstruction. Ajustez la position de l'échantillon de sorte qu'il tourne sur son propre axe dans le centre du champ de vue dans le champ lumineux, canal de transmission.
- Dans le canal d'émission de filtre GFP1 (filtre d'excitation 425 nm avec 40 nm passe-bande; filtre d'émission: 475 nm passe de long), concentrer l'échantillon et ajuster le temps d'exposition afin de maximiser la plage dynamique de l'image résultante (éviter la sur-saturation). Scannez le navire dans le chenal d'émission de GFP1 seulement, avec une étape à 0,9 ° de rotation.
- À la fin, confirmer la qualité de l'acquisition de données en utilisant un logiciel DataViewer. Retirer l'échantillon à partir du scanner.
- Pour permettre une analyse histologique ultérieure, placer l'échantillon dans 100% de méthanol pour> 24 heures avant le traitement à la cire paraffine comme normal.
La reconstruction et de l'analyse 4. image
Tomographique reconstruction par rétroprojection filtrée est réalisée en utilisant le logiciel de NRecon ou similaire. Reconstructions peuvent être effectuées sans surveillance, dans les lots.
- Améliorer la qualité de l'image en compensant le défaut d'alignement et le réglage des niveaux d'intensité de l'image.
- Vérifier la qualité de la reconstruction de l'image en utilisant un logiciel DataViewer.
- Identifier la section appropriée de l'échantillon pour analyse. Gardez cette longueur cohérente entre les navires si les dimensions luminal doivent être enregistrées.
- Définir le contour des lésions en traçant manuellement la frontière appropriée pour 1 sur 50 re-construit des sections.
- Vérifiez chaque section entrelacés pour assurer interpolations générées par ordinateur sont corrects. Ajuster manuellement la frontière si nécessaire.
- Fixer le seuil de niveau de gris de sorte que seule la lésion est sélectionnée et exporter les données de mesure.
- Pour chaque analyse, définir une zone verticale d'intérêt contenant la lésion et de tracer la frontière entre les médias et la néo-intima (ie., La position de la limitante élastique interne) pour chaque 50 ème ligne de balayage. Interpoler frontières intima / média pour les lignes de balayage entrelacés, dans le logiciel, et vérifier et corriger l'ajustement si nécessaire. Autre segment défini ce volume tridimensionnel à un seuil d'intensité définie manuellement pour produire une image ensemble binaire dans laquelle les pixels blancs représentent néo-intima et les pixels noirs représentent lumière de brevet.
- Les mesures prises comprennent: volume total de lésion (volume de l'objet), le volume luminal (volume total - volume de l'objet) et la distribution de la lésion et de lumière contre-secteional zone le long de la longueur axiale du récipient étudié.
Résultats
Numérisation préliminaire de santé (non lésé) artères fémorales murins (n = 5) a démontré que l'imagerie de transmission n'a pas fourni des images utiles. Ceci est une conséquence des artères deviennent trop compensés transparent (plutôt que trop opaque) pour la transmission imaging.However, ce qui est bénéfique pour l'imagerie par émission comme il n'y a pas d'absorption / diffusion du signal émis. En revanche, les artères fémorales autofluorescence fortement dans le canal d'émission, avec le plus grand signal de suivi de l'excitation à 405-445 nm (en conformité avec une excitation 410 nm pic de l'élastine 14). Tranches 2 dimensions reconstruites à partir de ces images distinguer nettement les médias de la lumière et de l'adventice et de la lumière.
Dans les artères fémorales murins récolté 28 jours après Wireless (n = 6) ou ligation- (n = 5) lésion induite néo-intimale épaississement était évident dans les projections d'émission non-tomographiques (figure 3A). Dans reconstruites 2-dimenstranches ional, lésions néointimales concentriques pouvaient être distingués des médias par leurs émissions plus faibles (figure 3B et la figure S1).
Images OPT d'émission des échantillons entiers de montage de l'arc aortique et de ses principales branches de souris d'athérosclérose (n = 8) lésions identifiées avec la distribution anatomique anticipée (ie., Dans la petite courbure de l'arc aortique, l'artère brachiocéphalique, et les origines de la carotide gauche et gauche artères sous-clavière (figure 4A). images transversales ont indiqué que ceux-ci étaient généralement des lésions excentriques et ont été facilement distingués des médias et de lumière (figure 4B, les figures S2 et S3).
Artères de traitement pour l'analyse histologique suivante OPT confirmé le caractère non destructif de l'OPT, avec des sections colorées avec succès en utilisant histologique (États-Unis trichrome, PICROsirius rouge) et immunohistochimique (α-SMA, Mac-2) techniques (figures 3C et 4C).
Mesure de la taille de la lésion en utilisant OPT a été montré pour être compatible avec les mesures obtenues en utilisant l'analyse d'images de coupes histologiques prises à partir de la même artère 11.
Mesures planimétriques de la zone de la lésion obtenus par l'OPT et histologie étroitement corrélée par régression linéaire pour Wireless (R 2 = 0,92) et induite ligature (R 2 = 0,89) et de lésions néointimales plaques d'athérosclérose (R 2 = 0,85). Un avantage important de l'OPT est sa capacité à permettre une analyse en 3 dimensions. En développant la quantification volumétrique de lésions avec cette technique, nous avons pu enregistrer des volumes de lésion dans Wireless (0,1100 ± 0,0091 mm 3; n = 6) et les artères fémorales ligature blessé (0,0200 ± 0,0089 mm 3; n = 5) et aussi dans les artères brachiocéphaliques athérosclérotiques (0.180 ± 0,018 mm 3; n = 8). Les mesures étaient hautement reproductibles (coefficient de variation de 5,4%, 11,4% et 4,8%, respectivement, n = 4) pour tous les types de lésion. Lésions néo-intimale dans les vaisseaux de fil blessés étaient plus grandes (p <0,0001) que ceux produits par ligature, compatible avec le plus grand degré de dégâts infligés par l'ancien.
Les données générées pourraient également être exprimé sous forme de profils de lésions (Figure 5) et rendus pour l'évaluation dynamique, qualitative (voir les figures S1 - S3). Cette approche a clairement démontré l'importance de la formation de la lésion en réponse à des procédures de blessures différentes et a souligné la répartition inégale de la formation de lésions dans les vaisseaux blessés.

Figure 1: Méthodes pour initier la formation de la lésion dans l'artère fémorale murin & #.160: (A) l'insertion rétrograde d'un fil guide d'angioplastie dans l'artère fémorale, au moyen d'une artériotomie dans l'artère poplitée stimule la formation de lésions en réponse à l'étirement et l'enlèvement des blessures de l'endothélium. La circulation sanguine est rétablie sur la section blessée du navire. (B) la prolifération néo-intimale, en l'absence d'étirage intraluminal, dénudation ou interruption de la circulation sanguine peut être induite par ligature de l'artère fémorale ou l'autre ou l'artère poplitée immédiatement en aval de la bifurcation de l'artère fémorale. (C) Un non-dénudant une réaction plus grave blessure / prolifération peut être induite par ligature les deux artères fémorales et poplitées à travers le point de l'artère fémorale commune de branche. Cette technique sera également bloquer l'écoulement de sang dans la partie distale de l'artère fémorale.
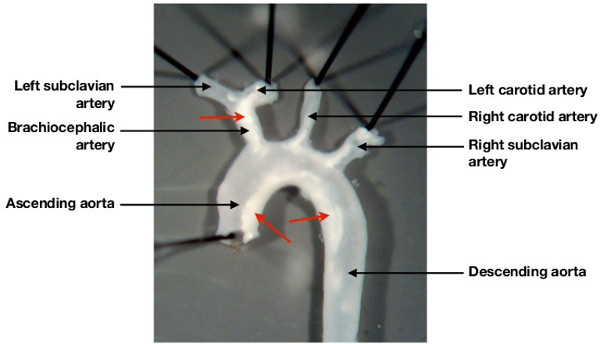
Figure 2:. Dépôt Caractéristique de l'athérome dans l'arc aortique de souris athérosclérose enclins (Apolipopotein E de souris déficientes) nourris avec un régime alimentaire occidental riche en cholestérol pendant 12 semaines à développer un modèle caractéristique de dépôt de lésion dans la crosse de l'aorte et de ses branches principales. Comme il est démontré, les lésions sont visibles (flèches), par inspection brut sous un microscope à dissection, dans la crosse de l'aorte, l'artère brachiocéphalique, et dans les orifices de l'artère carotide gauche et artère sous-clavière gauche.
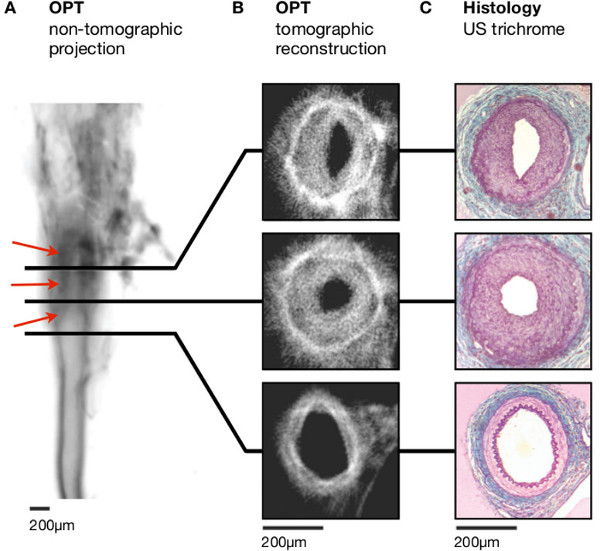
Figure 3:. La formation de lésions suite à la ligature de l'artère fémorale gauche (A) images émission de fluorescence non-tomographiques (inversées pour accroître la clarté - régions sombres correspondent à des émissions plus fort) permettre l'identification de épaississement de l'intima (arrowhe rougeannonces). (B) régions distinctes vasculaires et la lumière peuvent être distingués dans les reconstructions tomographiques. (C) L'analyse histologique (États-Unis trichrome) souligne la nette ressemblance avec des images obtenues à l'aide OPT. Les barres d'échelle dans (AC) sont de 200 mm. Adapté de Kirkby et al. 11 Les barres d'échelle dans (AC) sont de 200 um.
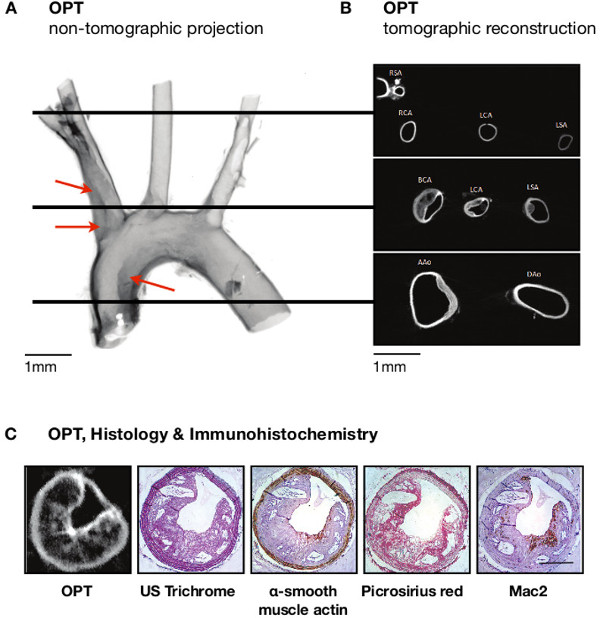
Figure 4:. Imagerie de l'athérome dans la crosse de l'aorte des souris sujettes athérosclérose (A) athérome (flèches rouges) est évidente dans les images non-tomographiques (inversée afin que les régions sombres indiquent émission forte, améliorant ainsi la clarté) de la crosse aortique, dans les sites prédit que athérome portant par inspection au microscope optique (voir Figure 2). (B) Ce modèle de distribution est confirmé dans cr tomographiqueOSS-sections. (C) histologique (États-Unis trichrome) coloration montre une similarité étroite avec coupes tomographiques, et immunohistochimie en utilisant plusieurs anticorps différents met l'accent sur la nature complémentaire de l'OPT avec les approches traditionnelles à l'analyse de la lésion. Les barres d'échelle dans (A-B) sont de 1 mm; La barre d'échelle dans (C) est de 250 um. RSA, l'artère sous-clavière droite; RCA, l'artère carotide droite; LCA, l'artère carotide gauche; LSA, artère sous-clavière gauche; BCA, l'artère brachiocéphalique; AAO, l'aorte ascendante; Dao, l'aorte descendante. Adapté de Kirkby et al. 11
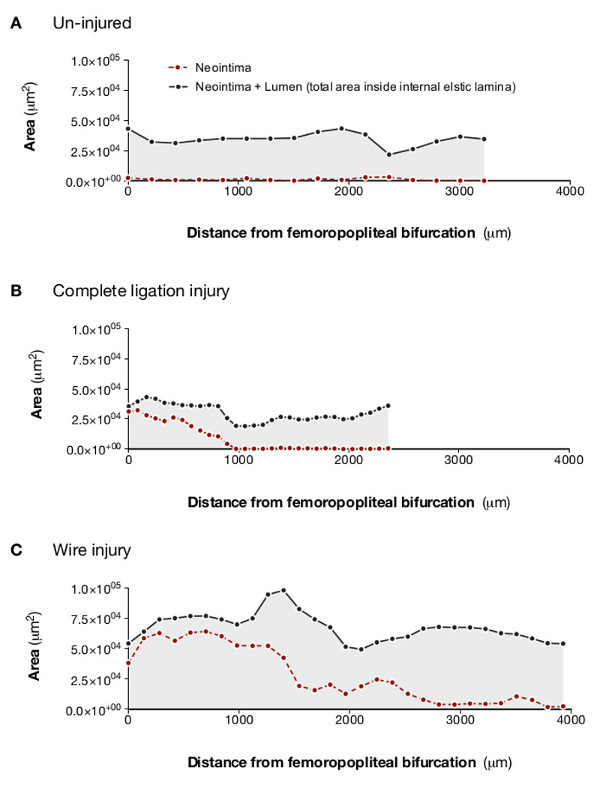
Figure 5: Analyse des profils de lésions et de la lumière indique l'étendue de la prolifération néo-intimale variant en réponse à différentes méthodes de lésion artérielle projection tomographie optique permet lésion et lumière traverser DE MESURE coupe.ts à être relevées en distance le long de l'artère fémorale. Cela démontre clairement que, par rapport à une artère indemne (A), la ligature partielle (B) produit de petites lésions, relativement discrets, tandis que la ligature totale (C) produit une occlusion complète sur le site de la ligature, mais la lésion ne va pas loin le long de l'artère . Blessure de fil intraluminale (D) produit une lésion qui obture presque complètement la partie distale de l'échantillon et se prolonge sur toute la longueur de la zone de lecture de l'artère. Adapté de Kirkby et al. 11
Figure S1. De reconstruction d'images animées transversales obtenues à partir d'une artère fémorale de la souris après une blessure de ligature. Ce type d'image animée est utile à la fois pour l'analyse qualitative et quantitative. Comme l'animation se déplace de l'extrémité proximale aux sections distales de l'artère le développement progressif d'une néo-intima occlusif, disqueernible de la lumière et les médias, est évidente. Les branches latérales peuvent être facilement identifiés et il ya occlusion luminale évident et le remodelage extérieur de l'artère que la lésion augmente en taille. Occlusion complète de la cuve se produit une fois le site de ligature est atteint. Adapté de Kirkby et al. 11
.. Figure S2 de reconstruction animée d'images en coupe transversale d'un arc aortique provenant d'une souris de l'athérosclérose sujettes L'animation commence avec des sections de l'ascendant (de gauche - qui apparaît en premier) et descendant (à droite) aorte. Les petites lésions apparaissent dans l'aorte ascendante comme les mouvements de balayage dans la direction de la crosse aortique. Les images passent ensuite à travers l'arche de montrer l'ostia fortement lésé de l'brachiocéphalique (à gauche), carotide gauche (au milieu) et sous-clavière gauche (à droite) artères. Comme le scanner se déplace de manière distale le long de ces branches les lésions réduisent progressivement et disparaissent, d'abord dans le subcLavian artère, puis dans l'artère carotide et enfin dans l'artère brachiocéphalique. Fait intéressant, la lésion dans les mouvements de l'artère brachiocéphalique sur le diviseur d'écoulement comme ce récipient se divise en la droite de la carotide et des artères sous-clavière droite. Adapté de Kirkby et al. 11
Figure S3. Animées, l'image de volume-rendu d'une crosse de l'aorte à partir d'une souris de l'athérosclérose exposées. Projection optique tomographie permet la génération d'images en 3 dimensions, dans ce cas, démontrant la distribution de la lésion dans la crosse aortique de l'apolipoprotéine E de la souris déficiente. (A) l'athérome est présent dans les sites attendus (tout au long de l'artère brachiocéphalique, dans les orifices de la carotide et des artères sous-clavières gauche et dans la petite courbure de l'arc de l'aorte). (B) La segmentation et le rendu de la lésion (en rouge) portant sections souligne la distribution des plaques quand il est superposé sur l'image originale.Adapté de Kirkby et al. 11
Discussion
Analyse en 3 dimensions a un grand potentiel pour le remplacement ou l'ajout aux techniques histologiques 2 dimensions qui sous-tendent toujours la majorité des enquêtes de la formation de lésions artérielles. Ici OPT est représenté sur les petites artères murins (souris avec artères fémorales représentant probablement les plus petits vaisseaux qui peuvent être analysés avec succès en utilisant cette technique). Il est, cependant, également adapté pour une utilisation avec des artères (lésions) et d'autres espèces, y compris les navires droits de petites et moyennes entreprises; notre groupe a utilisé avec succès la technique pour analyser les lésions de l'aorte de lapin (Bezuidenhout et al;. non publié). OPT promet une analyse plus rapide et accrue par rapport à des informations structurelles histologie classique et présente l'avantage de ne pas empêcher une analyse ultérieure de l'échantillon à la fois en utilisant des techniques histologiques et immunohistochimiques.
Les images produites à l'aide OPT ont donné des détails anatomiques, montrant les sites de formation de la lésionet la taille des lésions dans ces régions. Les artères utilisés dans ces enquêtes sont probablement proches de la limite de la résolution pour la technique et la qualité de l'image est donc altérée à un certain degré par des artefacts (probablement résultant de la rotation désalignement, compensation incomplète, de réflexion / réfraction aux sommets d'agarose et les problèmes de mise au point) . Malgré cela, les informations nécessaires (par exemple, des couches de la paroi du vaisseau) restent discernable et donc la technique est extrêmement utile pour la quantification des couches individuelles. En effet, les images ont pu être quantifiées rapide et reproductible pour fournir des mesures de la lésion et le volume luminal dans les sections plaque portant du navire, ainsi que les zones transversales de la lésion et lumière dans des sites sélectionnés dans l'échantillon. Large (aorte) et de taille moyenne (fémoral, carotide, sous-clavière) des artères de souris - celles généralement utilisées pour l'analyse de la formation de lésions d'athérosclérose chez la souris et neotintimal - ont été avec succèsanalysées en utilisant cette méthode. En effet, nous avons maintenant utilisé OPT pour démontrer l'effet des interventions pharmacologiques et la manipulation génétique de la taille d'athérosclérose et néo-intimale lésion. Par exemple, le blocage des récepteurs de l'endothéline modifié formation de lésion néo-intimale tandis que la suppression sélective du récepteur de l'endothéline B de l'endothélium vasculaire n'a pas 15. Chez les souris sujettes à l'athérosclérose, la deletion génétique des enzymes 11β-HSD-1 ou la galectine 3 16 17 ont été montrés pour réduire la taille des lésions athérosclérotiques.
Quantification du volume de la lésion est un avantage évident de l'OPT. Il donne une indication plus informatif de la charge totale de la lésion dans une artère 4 que l'on obtient généralement avec des méthodes histologiques. L'analyse de la totalité de la lésion réduit biais de sélection et d'erreurs qui vont inévitablement se produire lorsque sections distinctes d'un navire sont choisis pour l'analyse. Production de profils longitudinaux des lésions est un autre point fort de l'OPT, Soulignée par la comparaison des lésions induites par différents types de blessures 13,16 (figure 5). Par exemple, à la fois complète et la ligature d'insertion de fil induites occlusion presque totale proche de la bifurcation de femero-poplitée. blessure de fil, les lésions cependant que produits étendus sur toute la longueur de la zone de lecture, alors que les lésions induites par ligature artérielle diminuée rapidement en taille et disparaissent. Ce modèle est cohérent avec la plus grande mesure du dommage causé par l'insertion du fil guide d'angioplastie. Générer des résultats similaires en utilisant des coupes histologiques est coûteuse, longue et laborieuse.
Les avantages de l'OPT comprennent la qualité des images qu'elle produit et de sa vitesse relative et la simplicité (nous avons régulièrement balayée 20 navires par jour). La qualité d'image apparaît supérieure, ou du moins comparable, à d'autres méthodes pour générer des images en 3 dimensions ex vivo (comme l'IRM et CT micro-), yet OPT nécessite la réduction des temps de balayage (de temps d'intégration pour nos études était généralement 1-2sec / image) et est moins cher. La préparation des échantillons étend sur plusieurs jours, mais nécessite peu de travail, les navires peuvent être préparés en lots, et les données peuvent être acquis en une seule session. En conséquence, le débit est élevé et ne nécessite pas l'utilisation prolongée du scanner. Fait important, la nature non destructive de l'OPT signifie qu'il peut être utilisé pour identifier des sites d'intérêt pour l'examen immunohistochimique; réduisant ainsi la quantité de coupe et de coloration nécessaire. Il est possible que le développement de l'échographie à haute résolution fournira une méthode alternative pour la quantification volumétrique des lésions dans les artères de cette taille, mais les auteurs ne sont pas conscients de toutes les publications qui démontrent cette application.
Peut-être sans surprise, la qualité d'image dans les TPO est inférieur aux techniques microscopiques (qui peut, bien sûr, seulement être effectuées sur des échantillons plus petits). Modifications proposées à reconstruction des données peut adresser cette limitation en permettant l'amélioration future de la qualité d'image 19,20. Une autre préoccupation méthodologique est que le traitement des tissus modifie les caractéristiques de l'échantillon. Par exemple, le caractère lipophile de l'agent de compensation, l'alcool benzylique / benzoate de benzyle (BABB), est susceptible de supprimer lipides à partir de lésions athéroscléreuses, alors que la déshydratation préalable peut provoquer un rétrécissement (même si, bien sûr, de déshydratation et d'élimination des lipides étapes sont également une caractéristique de la préparation d'échantillons pour l'enrobage dans de la cire de paraffine). BABB a été utilisé dans cette étude que, par comparaison avec des agents de compensation hydrophiles (par exemple, glycerol 21) provoque que de faibles changements de morphologie.
Il existe plusieurs possibilités pour la poursuite du développement et le raffinement de l'OPT, en particulier en ce qui concerne le suivi de l'agencement en 3 dimensions des cellules clés et les facteurs impliqués dans le remodelage artériel signalisation. La forte autofluorescence de tissu artériel, qui est teln avantage dans la génération d'images anatomiques, n'a pas été désactivé par des procédés de blanchiment 22 existants et peut limiter l'utilisation de sondes fluorescentes pour évaluer les modèles de distribution de l'ARN et des protéines. L'utilisation de sondes colorimétriques (par exemple β-galactosidase) visualisés par imagerie de transmission peut surmonter cette limitation.
Pour conclure, l'OPT a un grand potentiel pour l'imagerie en 3 dimensions des lésions dans l'intima des artères murins. Il représente un progrès considérable sur les méthodes 2 dimensions qui sont généralement beaucoup de travail et ne représentent pas efficacement le volume totale de la lésion. OPT est relativement rapide, pratique et non destructive. Nouveaux développements dans l'analyse d'image promettent d'augmenter encore la puissance et l'utilité de la technique.
Déclarations de divulgation
The authors have no competing financial interest.
Remerciements
Ce travail a été soutenu par des bourses de l'Université d'Edimbourg (NSK) et Carnegie Trust (LL; Henry régime Dryerre) et le financement de la British Heart Foundation (PWFH, BRW, DJW; RG / 05/008; PG / 05/007; PG / 08/068/25461) et le Wellcome Trust (JRS, BRW, DJW; 08314 / Z / 07 / Z). Les auteurs sont reconnaissants à l'appui pour leur travail fourni par le Centre d'excellence en recherche de l'attribution BHF-financé par le Centre de sciences cardiovasculaires.
Les auteurs sont particulièrement reconnaissants pour conseils du professeur Masataka Sata (Université de Tokushima) et le Dr Igor Chersehnev (dans le groupe de Dr Ernane Reis au Mount Sinai School of Medicine) sur l'établissement de modèles de chirurgie de la production de la lésion néo-intimale. La vidéo produite et mise à disposition par Sata et al. (Http://plaza.umin.ac.jp/~msata/english.htm) a été particulièrement utile.
matériels
| Name | Company | Catalog Number | Comments |
| Operating Microscope | Zeiss, Germany | OPMI Pico i | |
| Anesthetic Machine | Vet Tech, UK | ||
| Fluovac | Harvard Apparatus UK | 340387 | |
| Fluosorber | Harvard Apparatus UK | 340415 | |
| Bead Sterilizer | Fine Science Tools, UK | 1800-45 | |
| Heated Mat | Fine Sceince Tools, UK | 21061-10 | |
| Balance | Mettler Toledo | MS1602S | PB1502 or equivalent |
| Sutures | Ethicon, UK | 5/0 Mersilk | |
| Guidewire | Cook Inc, USA | C-PMS-251 | 0.014” |
| Suture Silk | Fine Science Tools, UK | 18020-60 | 6/0 Mersilk |
| Surgical Tools | Fine Science Tools, UK | 14058-09 | Toughcut Iris scissors |
| Cohan-Vannas Spring Scissors | Fine Science Tools, UK | 15000-01 | |
| Dumont #5/45 Forceps | Fine Science Tools, UK | 11251-35 | |
| Moria Iris Forceps | Fine Science Tools, UK | 11370-31 | |
| Halsted-Mosquito Hemostat | Fine Science Tools, UK | 13008-12 | |
| Bulldog clips | Fine Science Tools, UK | 18050-35 | |
| Bioptonics 3001 Tomograph | Bioptonics, UK | ||
| Magnetic OPT Mount | Bioptonics, UK | ||
| Computer | Dell Inc, UK | ||
| Peristaltic pump | Gilson | F117606 | Minipuls 3 |
| DataViewer software | Skyscan, Belgium | v.1.4.4 | |
| NRecon software | Skyscan, Belgium | v.1.6.8 | |
| CTan software | Skyscan, Belgium | v.1.12 | |
| Isoflurane | Merial Animal Health Ltd, UK | AP/Drugs/220/96 | 100% Inhalation vapor, liquid |
| Medical Oxygen | BOC Medical, UK | UN1072 | |
| Vetergesic | Alstoe Animal Health Ltd, UK | 0.3 mg/ml | |
| 1% Lignocaine | Hamlen Pharmaceuticals, UK | LD1010 | 10 ml ampoule |
| EMLA Cream | Astra Zeneca, UK | ||
| Sodium Pentobarbital | Ceva Animal Health Ltd, UK | ||
| Western Diet | Research Diets, USA | D12079B | 0.2% cholesterol |
| Phosphate Buffered Saline | Sigma UK | P4417 | |
| Heparin (Mucous) | Leo Laboratories, UK | PL0043/003GR | 250,000 Units |
| Neutral Buffered Formalin | Sigma, UK | HT501128 | 10% |
| Ethanol | VWR BDH Prolabo, UK | 20821.33 | Absolute AnalaR |
| Agarose | Invitrogen, UK | 16020050 | Low melting point |
| Filter Paper | GE Healthcare, UK | 113v | Whatman |
| Cyanoacrylate adhesive | Henkel, UK | 4304 | Loctite |
| Benzyl alcohol | Sigma, UK | B6630 | |
| Benzyl benzoate | Sigma, UK | 402834 | |
| Methanol | VWR BDH Prolabo, UK | 20856.296 | 100% |
Références
- Luis, A. J. Atherosclerosis. Nature. 407, 233-241 (2000).
- Ross, R. Atherosclerosis–an inflammatory disease. N Engl J Med. 340, 115-126 (1999).
- Deuse, T. Imaging In-Stent Restenosis: An Inexpensive, Reliable, and Rapid Preclinical Model. J Vis Ex. (31), (2009).
- McAteer, M. A. Quantification and 3D reconstruction of atherosclerotic plaque components in apolipoprotein E knockout mice using ex vivo high-resolution MRI. Arterioscler Thromb Vasc Biol. 24, 2384-2390 (2004).
- Martinez, H. G. Microscopic Computed Tomography-Based Virtual Histology for Visualization and Morphometry of Atherosclerosis in Diabetic Apolipoprotein E Mutant Mice. Circulation. 120, 821-822 (2009).
- Langheinrich, A. C. Atherosclerotic Lesions at Micro CT: Feasibility for Analysis of Coronary Artery Wall in Autopsy Specimens. Radiology. 231, 675-681 (2004).
- Ambrosi, C. M. Virtual histology of the human heart using optical coherence tomography. J Biomed Opt. 14, 054002(2009).
- Ku, G. Photoacoustic microscopy with 2-micron transverse resolution. J Biomed Opt. 15, 021302(2010).
- Sharpe, J. Optical projection tomography as a tool for 3D microscopy and gene expression studies. Science. 296, 541-545 (2002).
- Sharpe, J. Optical projection tomography. Annu Rev Biomed Eng. 6, 209-228 (2004).
- Kirkby, N. S. Quantitative 3-Dimensional Imaging of Murine Neointimal and Atherosclerotic Lesions by Optical Projection Tomography. PloS ONE. 6 (2), e16906(2011).
- Roque, M. Mouse model of femoral artery denudation injury associated with the rapid, accumulation of adhesion molecules on the luminal surface and recruitment of neutrophils. Arterioscler Thromb Vasc Biol. 20, 335-342 (2000).
- Sata, M. A mouse model of vascular injury that induces rapid onset of medial cell apoptosis followed by reproducible neointimal hyperplasia. J Mol Cell Cardiol. 32, 2097-2104 (2000).
- Richards-Kortum, R., Sevick-Muraca, E. Quantitative optical spectroscopy for tissue diagnosis. Annu Rev Phys Chem. 47, 555-606 (1996).
- Kirkby, N. S. Non-endothelial cell endothelin-B receptors limit neointima formation following vascular injury. Cardiovascular Research. 95, 19-28 (2012).
- Kipari, T., et al. 11-hydroxysteroid dehydrogenase type 1 deficiency in bone marrow-derived cells reduces atherosclerosis. FASEB J. 27 (4), 1519-1531 (2013).
- Mackinnon, A. C. Inhibition of galectin-3 reduces atherosclerosis in apolipoprotein E deficient mice. Glycobiology. 23 (6), 654-663 (2013).
- Kumar, A., Lindner, V. Remodeling with neointima formation in the mouse carotid artery after cessation of blood flow. Arterioscler Thromb Vasc Biol. 17, 2238-2244 (1997).
- Walls, J. R. Correction of artefacts in optical projection tomography. Phys Med Biol. 50, 4645-4665 (2005).
- Walls, J. R. Resolution improvement in emission optical projection tomography. Phys Med Biol. 52, 2775-2790 (2007).
- Bucher, D. Correction methods for three-dimensional reconstructions from confocal images: I. tissue shrinking and axial scaling. Journal of Neuroscience Methods. 100, 135-143 (2000).
- Alanentalo, T. Tomographic molecular imaging and 3D quantification within adult mouse organs. Nat Methods. 4, 31-33 (2007).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon