Method Article
Dépistage rapide du VIH de la transcriptase inverse et inhibiteurs de l'intégrase
Dans cet article
Résumé
Nous décrivons ici la cytotoxicité cellulaire et simples essais d'infectivité rondes qui permettent la sélection rapide et précise des composés de déterminer leur cytotoxicité cellulaire (CC 50) et les valeurs IC50 contre WT et VIH-1 résistant médicament.
Résumé
Bien qu'un certain nombre de médicaments anti-VIH ont été approuvés, il ya toujours des problèmes avec la toxicité et la résistance aux médicaments. Cela démontre la nécessité d'identifier de nouveaux composés qui peuvent inhiber l'infection par les résistants aux médicaments souches VIH-1 en commun avec une toxicité minimale. Nous décrivons ici un dosage efficace qui peut être utilisé pour déterminer rapidement la cytotoxicité cellulaire et de l'efficacité d'un composé contre les souches virales WT et mutantes.
La ligne souhaitée de la cellule cible est ensemencé dans une plaque à 96 puits et, après une incubation de 24 h, en série de dilutions des composés à tester sont ajoutés. Pas d'autres manipulations sont nécessaires pour les tests de cytotoxicité cellulaire; Dosages des anticorps anti VIH d'une quantité prédéterminée d'un ou l'autre médicament ou WT VIH-1 résistant vecteur qui exprime la luciférase est ajouté aux cellules. La cytotoxicité est mesurée en utilisant un dosage par luminescence dépendante de l'ATP et de l'impact des composés sur l'infectivité est mesurée en déterminant la quantité de luciferasez en présence ou en l'absence des inhibiteurs putatifs.
Ce test de dépistage prend 4 jours pour compléter et de multiples composés peuvent être criblés en parallèle. Les composés sont criblés en triple exemplaire et les données sont normalisées par rapport à des niveaux infectivité / ATP en absence de composés cibles. Cette technique permet une mesure rapide et précise de l'efficacité et de la toxicité des composés potentiels VIH anti-.
Introduction
La disponibilité de médicaments ciblant plusieurs étapes essentielles du cycle de vie du virus VIH-1 a conduit à la thérapie de combinaison de médicaments (appelée thérapie antirétrovirale hautement active ou HAART) qui a grandement amélioré le traitement du VIH-1 infection, et la survie à long terme des patients. HAART, qui utilise typiquement des combinaisons de deux nucléosides de la transcriptase inverse (RT) et des inhibiteurs non plus un inhibiteur de la protéase ou un inhibiteur non nucléosidique de la RT, a converti une maladie mortelle dans un état de longue durée de vie de 1-5. Cependant, malgré les nombreux succès de la multithérapie dans suppression soutenue de la réplication virale, il a ses limites. HAART n'élimine pas le VIH, de sorte que les patients ne sont pas guéris et le traitement est long de la vie. Il existe des problèmes de toxicité des médicaments et à l'émergence de souches résistantes aux médicaments. Résistance peut se manifester à tous les médicaments contre le VIH anti-approuvés, y compris les médicaments nouvellement approuvés qui ciblent l'intégrase du VIH (EN). La résistance aux médicaments se pose probablement BECAutilisation des mutations spontanées qui se produisent au cours de la replication virale (taux de 3 x 10 -5 cycle de mutations / base / de réplication d'erreur) 6. Lorsque des mutations se produisent dans les gènes codant pour les cibles de médicaments anti-rétroviraux, un petit sous-ensemble de ces mutations se traduira par une réduction de la sensibilité de la souche virale à des médicaments. Pour éviter le développement de la résistance aux médicaments, les concentrations de médicaments doivent être maintenus à des niveaux qui suppriment totalement la réplication du VIH. Une mauvaise observance du régime thérapeutique aggrave le problème, et peut conduire à l'élaboration rapide d'une résistance 7-9. Bien que les concentrations de médicament peuvent varier d'un patient à cause de l'absorption différente, le métabolisme, la distribution et les niveaux d'excrétion, des concentrations élevées de médicaments peuvent conduire à une toxicité 10. Puisque la thérapie continue pour la vie du patient, il existe de graves préoccupations en matière de sécurité au sujet de la toxicité à long terme des anti rétroviraux. Les anti rétroviraux couramment utilisés dans HAART peuvent avoir des effets indésirables d'une il ya eu des cas où les effets secondaires ont été la vie en danger 11-15. Les problèmes rencontrés avec les patients du développement de la résistance et de la toxicité à la base de la nécessité de développer de nouveaux médicaments qui bloquent efficacement la replication des souches communes de médicaments résistantes du virus avec peu ou pas de toxicité à long terme.
Ainsi, il existe un besoin pour un dosage qui peut cribler des composés qui bloquent des étapes essentielles dans le cycle de vie viral rapidement. Nous décrivons ici un dosage efficace qui peut être utilisé pour évaluer la cytotoxicité d'un des composés et leur capacité à bloquer la replication à la fois de WT et des souches de VIH résistantes aux médicaments rapidement et efficacement. Le test que nous utilisons est semblable à un essai qui a été développé pour le dépistage de la résistance aux médicaments dans les virus isolés à partir de patients de 16 à 18.
Bien que le dosage peut être utilisé sans modification pour le dépistage de composés qui peuvent bloquer la transcription inverse du VIH, nous DescrBIE en utilisant le test pour évaluer inhibiteurs de l'IN. IN est une enzyme virale essentielle qui insère l'ADN viral dans le génome cellulaire 19. Bien qu'un certain nombre de promettre inhibiteurs de l'IN sont en cours d'élaboration, dont certains font actuellement l'objet d'essais cliniques, ne Isentress 20, 21 (aussi connu comme le raltégravir ou RAL) et, plus récemment, l'elvitegravir (EVG) 22 et dolutégravir (DTG) 23 ont été approuvé par la FDA. Ces composés sont actifs à la fois contre le VIH sous-types non B et B en culture cellulaire et chez les patients 24, 25. Cependant, le traitement avec RAL sélectionne les souches résistantes du VIH-1 chez les mutants, y compris Y143R, N155H, et G140S/Q148H 24, 26-31. N155H et G140S/Q148H réduisent également l'efficacité des IEV, qui met l'accent sur la nécessité de concevoir et de développer la deuxième génération DANS inhibiteurs de transfert de brin (INSTIs) qui sont efficaces contre ces mutations de résistance.
Protocole
1. Préparation des stocks de Maître
- Faire des stocks de base des composés à tester dans du DMSO. Préparer des stocks à une concentration standard de 20 mM.
Remarque: une concentration supérieure à 10 mm peut être utilisé. Les composés qui peuvent être utilisés comme témoins positifs pour valider ce test comprennent RAL, EVG et DTG. - S'assurer que les composés sont dissous dans du DMSO au vortex les solutions de multiples fois pendant 15 s et en incubant à température ambiante pendant 1 h. Conserver les solutions mM 20 dans l'obscurité à -20 ° C jusqu'à utilisation.
2. Préparation des plaques à 96 puits pour le composé dépistage
- Choisissez la lignée cellulaire à tester (par exemple HOS ou TZM-bl), et ensemencer 100 pi de ces cellules à une densité de 4 x 10 4 cellules / ml (4.000 cellules / puits) dans les médias (par exemple Eagle ou milieu DMEM modifié Dulbecco supplémenté avec 5% (v / v) de sérum de veau fœtal, 5% de sérum de veau nouveau-né, et de la pénicilline (50 unités / ml) plus streptomycin).
3. Génération des stocks de virus
Produire VSV-G-VIH pseudotypé par transfection de cellules 293 (comme le montre la figure 1, étape 1) 32-34.
- Le jour avant la transfection, plaquer les cellules sur des boîtes de 293 100 mm de diamètre à une densité de 1,5 x 10 6 cellules.
- Le jour de la transfection, la transfection de cellules 293 avec 16 ug de type sauvage ou mutant du VIH (pNLNgoMIVR - ΔLUC) et 4 pg de VSV (pHCMV-g) en utilisant le procédé au phosphate de calcium 35.
- Environ 6 heures après le précipité de phosphate de calcium est ajouté, laver 293 cellules deux fois avec du tampon phosphate salin (PBS) et incuber avec du milieu frais pendant 48 heures. [DMEM additionné de 5% (v / v) de sérum de veau fœtal, 5% de sérum de veau nouveau-né, et de la pénicilline (50 unités / ml) et streptomycine (50 ug / ml)].
- Récolter le virus surnageants contenant en enlevant le support du 100 mm de diamètreplats, clarifier les surnageants par centrifugation à faible vitesse à 3000 tours par minute pendant 10 minutes, filtrer le surnageant à travers un filtre de 45 um taille des pores de la seringue, de traiter les surnageants avec Turbo DNase pendant 30 min à température ambiante et diluer le surnageant dans les médias pour la préparation de tests d'infection . Conserver les surnageants viraux congelés, en aliquotes, à -80 ° C.
Note: la quantité de p24 dans le surnageant est déterminée en utilisant un kit d'immuno p24 de HIV-1 dosage lié à une enzyme. La concentration de p24 est utilisé pour contrôler la quantité de virus dans l'échantillon. Environ 500 ng de virus est ajouté aux cellules HOS plaquées sur des boîtes de 60 mm de diamètre à une densité de 1,5 x 10 5 cellules / boîte, le jour avant l'infection. Après une incubation de 48 h, les cellules sont récoltées, recueillies par centrifugation, lavées et remises en suspension dans 100 ul de PBS. Ajouter une quantité égale de Luminescence reporter réactif de dosage génique et mesurer l'activité de la luciférase comme décrit dans les sections 5.4.1 et5.4.2. De là, une dilution appropriée du virus peut être effectuée comme décrit dans l'étape 4.6.
4. Composé dépistage en plaques à 96 puits
Screen chaque composé en triple exemplaire et la moyenne des résultats.
Remarque: l'effet de chaque composé sur la réplication virale est corrigée par normalisation au niveau de la réplication obtenu en l'absence de tout composé.
- Déterminer la gamme de concentration empirique à être projeté.
Remarque: en général, les écrans de 11 dilutions en série sont fabriqués en ajoutant le composé de la colonne de la plaque par colonne et écrans de 7 dilutions en série sont fabriqués en ajoutant le composé par ligne. Une triple série de puits doit être réservé pour le contrôle pas composé. En outre, une colonne ou une ligne doivent rester vierge pour agir comme contrôle négatif / arrière-plan. Enfin, qu'il s'agisse d'une cytotoxicité cellulaire ou un dosage d'infectivité déterminera si le virus est ajouté. - Préparerdilutions en série de la solution stock de 20 mM. Les concentrations sont choisies en fonction de l'intervalle déterminé de manière empirique des concentrations à tester (voir tableau 1). Préparer les dilutions dans les médias à 10x la concentration finale souhaitée, c'est à dire si la concentration finale va être 100 uM, faire un stock de travail 1 mM.
Note: Les composés ayant des CI50 uM 10.5 ci-dessus ne sont généralement pas de bons candidats pour le développement de médicaments. Dans les essais initiaux, nous testons les composés seulement contre le vecteur WT. Composés prometteurs qui inhibent efficacement le vecteur WT sont ensuite testés sur un panel de mutants résistants aux médicaments. - Retirer les plaques de 96 puits à partir de l'incubateur et ajouter des dilutions en série des composés à tester dans les puits, en triple exemplaire (comme le montre la Figure 1, étape 2).
Note: le volume ajouté au puits devrait être de 1/10 de volume de la concentration finale. Ainsi, ajouter 22 ul / puits (volume final pplus de virus ost est de 220 pi) pour les épreuves d'infectivité. Pour les essais de cytotoxicité, ajouter 11 ul / puits (volume final est de 110 ul / puits). - Retourner les plaques à 96 puits à l'incubateur. Pour un écran de cytotoxicité cellulaire, incuber les plaques à 96 puits 48 heures à 37 ° C et pas d'autres manipulations sont nécessaires dans le protocole 4: procéder au protocole 5 Pour les épreuves d'infectivité, continuer en suivant les instructions du protocole 4..
- épreuves d'infectivité seulement. Retirer les plaques de l'incubateur après un minimum de trois heures d'incubation à 37 ° C avec les composés à analyser.
Remarque: cela permet au composé d'être absorbé par les cellules avant l'infection avec le vecteur de VIH. - Préparer une dilution de virus de la 33, 34 (en général environ 1:3) qui va produire un signal de luciférase entre 0,2-1,5 unités relatives (RLU luciférase) dans les cellules non traitées. Une plaque entière prendra environ 10 ml de dilutionvirus de TED. Ajouter 100 ul de virus de chacun des puits, en utilisant soit une pipette multicanaux 8 ou 12. Ne pas ajouter de virus dans les puits de contrôle négatif / fond. Remettre les plaques à 37 ° C incubateur pendant 48 heures.
Remarque: un magasin dilution 1:03 du virus est typique dilution qui va produire un signal de la luciférase entre 0,2 -1,5 RLU en fonction d'un dosage de p24 montre que la concentration virale dans le surnageant est d'environ 500 ng à 1,0 ml.
5. Préparation et évaluation de la cytotoxicité et de l'infectiosité dans des plaques 96 puits
- Aspirer les médias des puits (phénol rouge dans les médias peut interférer avec le signal de la luciférase). Utiliser une pipette de verre avec un embout de pipette de 200 pi attaché à l'extrémité. Commencez par le haut des médias et de travailler lentement vers le coin en bas du puits. Ne pas passer trop de temps au fond du puits, ou des cellules peuvent être retirées du puits.
- Ajouter 100 pi de PBS complété avec 0,5 mMgCl 2 M à chaque puits. Ce qui doit être fait immédiatement après les médias est enlevé de sorte que les cellules ne se dessèchent pas.
- Seulement pour les tests de cytotoxicité, ajouter 5 ml de tampon de substrat à partir de l'essai de détection de la luminescence de l'ATP à chaque flacon de réactif lyophilisé fourni. Un flacon est suffisant pour une plaque de 96 puits.
- Ajouter 50 ul de tampon de lyse de cellules à partir de l'essai de détection de la luminescence de l'ATP à chaque puits. Agiter la plaque de 96 puits à 700 rpm à température ambiante pendant 5 min en utilisant un thermomixer compact.
- Ajouter 50 ul d'reconstitué Luminescence ATP réactif d'essai de détection de tous les puits à l'exception des puits négatifs contrôle / fond. Agiter à 700 rpm à température ambiante pendant 5 min en utilisant un thermomixer compact. Incuber les plaques à température ambiante pendant 20 min pour donner le temps de développement du signal.
- Lire la plaque à 96 puits en utilisant le luminomètre pour microplaques.
Remarque: ouvrir le programme Pro microplaque de luminomètre SoftMax. Assurez-vous que le luminomètre est réglé pour mesurer luminescence à une sensibilité de 5 lectures / puits.
- Seulement pour les épreuves d'infectivité, ajouter 10 ml de tampon de substrat de l'analyse du gène de luminescence de reporter à chaque flacon de réactif lyophilisé fourni. Un flacon est suffisante pour que chaque plaque de 96 puits.
- Ajouter 100 ul de reconstitué Luminescence reporter réactif de dosage de gène à chaque puits. Incuber à température ambiante pendant 20 min pour donner le temps de développement du signal.
- Lire la plaque de 96 puits en utilisant un luminomètre pour microplaques interprété dans la section 5.3.3.
6. Détermination de la CC 50 et IC 50 valeurs pour les composés
- Transférer les données de la luciférase luminomètre pour microplaques dans une feuille de calcul Excel.
- Fois la moyenne des données de la luciférase, en trois exemplaires et les données de signal de fond / contrôle. Soustraire la moyenne du signal de fond / commande du signal de trois exemplaires en moyenne pour l'ensemble de la gamme de concentration.
- Normaliser l'objet d'une correction de signal moyen pour les gammes de concentration de l'activité contre, s'il s'agit d'une cytotoxicité ou d'infectivité, en l'absence de tout composé à déterminer le pour cent d'inhibition.
Remarque: inhibition en pour cent est définie comme l'activité de luciférase en présence de médicament divisé par l'activité de la luciférase en l'absence de médicament, multiplié par 100.
- Utilisez logiciel Kaleidagraph obtenir CC 50 et IC 50 valeurs
- Transférer à la fois la plage de concentration déterminée empiriquement pour cent et l'inhibition de l'activité de la luciférase dans Kaleidagraph.
- Tracer les données de la plage de concentration sur l'axe des x et le pour cent d'inhibition de l'activité de la luciférase sur l'axe y.
Résultats
Si l'essai (figure 1, les étapes 1 et 2) a été effectuée avec succès, les valeurs de luciférase doivent ressembler les données présentées dans le tableau 2 Balayez la gamme de concentration.; un composé potentiellement puissant révélera augmentation de l'activité luciférase à partir de la gauche vers la droite, et le contrôle doit avoir la plus forte activité de la luciférase. Si l'activité de la luciférase ne dépasse pas 0,1 unités de luciférase relatives (RLU) à travers la plage de concentration, ce qui indique généralement que le composé a tué les cellules. Si les données de la luciférase est supérieur ou égal à 2,0 dans tous les RLU des dilutions en série, alors les composés ne sont pas capables d'inhiber les infections du VIH-1 aux concentrations testées.
Traçant la concentration des composés pour cent par rapport à l'inhibition de l'activité luciférase dans Kaleidagraph (tableau 3, partie A), après l'exécution d'une analyse de régression linéaire, va produire des résultats similaires à t Tuyau montre le tableau 3, partie B.

Figure 1. Préparation du VIH-1 stocks viraux et la configuration de cytotoxicité cellulaire et unique tour infectiosité dosages. L'étape 1, les cellules 293T sont transfectées avec pNL4.3ΔEnv.LUC et VSV-G et incubé pendant 48 heures à produire un virus 34 . Le virus est récolté et stocké (congelé à -80 ° C en aliquotes) jusqu'à ce qu'il soit utilisé dans les tests d'infectivité. Pour l'étape 2, les cellules HOS sont ensemencées dans une plaque à 96 puits et incubées pendant 24 heures. Les cellules sont ensuite pré-incubées avec des dilutions en série des composés à tester pendant 3 heures et ensuite infectées avec le virus (soit WT ou résistante aux médicaments). Après une incubation de 48 h, l'activité luciférase est mesurée.
le1.jpg "width =" 300 "/>
Tableau 1. Criblage de médicaments série dilution Prototype. Un dépistage plus rigoureux implique 11 dilutions en série qui commencent généralement à 10 uM et se terminent à 0,0005 uM. Les dilutions en série sont préparées 10x; il existe 100 ul de cellules et 100 pi de virus dans chaque puits). A ce volume et la suite de ces calculs, les dilutions en série sera suffisant pour 3 lignes d'une plaque de 96 puits entier. Les tests de cytotoxicité sont préparés de manière similaire; Mais les 11 dilutions en série commencent à 250 uM et se terminent à 0,05 uM. Seuls 11 pl des dilutions sont ajoutés dans les puits de la plaque qui contient 100 ul de cellules. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
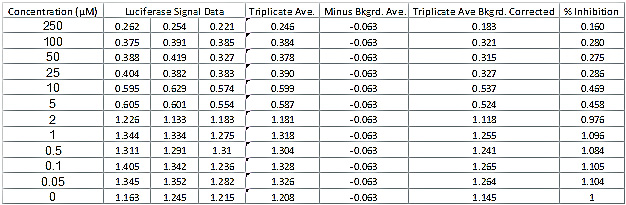
Le tableau 2. Luciferase lecture du signal de données et de détermination de pourcentage d'inhibition de l'activité de la luciférase. La table de données montre un ensemble typique de la luciférase de données pour un composé de succès. Le tableau indique également les calculs nécessaires pour déterminer le pour cent d'inhibition de l'activité de la luciférase et la CC 50 et IC 50 valeurs. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
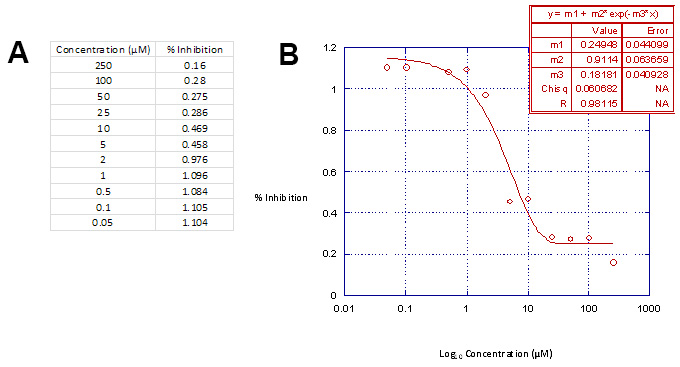
Tableau 3. Analyse de régression linéaire tableau de données. Partie A. Représentation graphique de la gamme de concentration utilisée pour cent par rapport à l'inhibition de l'activité de la luciférase dans Kaleidagraph va produire les courbes d'inhibition appropriées. Partie B, Les courbes d'inhibition sont définis par la 3 paramétriquefonction sigmoïde et ajustement aux données par régression linéaire des analyses 18. Ce tableau de données est ensuite utilisé en conjonction avec Microsoft Excel pour calculer les concentrations de médicament nécessaire pour inhiber l'intégration du virus et de la cytotoxicité cellulaire de 50%, par exemple, IC 50 et CC 50. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Discussion
Nous décrivons un dosage rapide, efficace et reproductible qui peut être utilisé pour cribler des composés pour la cytotoxicité et pour leur capacité à inhiber la replication à la fois de WT et du VIH-1 résistant aux médicaments. La capacité d'identifier rapidement les composés et de tester leur efficacité et leur cytotoxicité est crucial dans le développement de médicaments nouveaux et améliorés contre le VIH-1. Une fois que les composés de plomb sont identifiés, des analogues du composé du plomb peuvent être préparés et testés en utilisant le même dosage. Le dosage est relativement simple. Il ya deux contrôles positifs et négatifs qui permettent à l'utilisateur de diagnostiquer les problèmes les plus courants (composés toxiques, des problèmes avec le vecteur stock). L'utilisation d'un ensemble de triple puits sans composé ajouté montre que l'infection virale s'est produite. Le fait que la cytotoxicité est mesurée dans un test indépendant permet d'éviter une mauvaise interprétation d'une réduction de la luciférase de la cytotoxicité provoquée par un effet spécifique sur la réplication virale.
Les étapes critiquesdans le protocole sont la préparation des plaques de sorte que les cellules sont uniformément réparties dans les puits, ce que les puits ont des concentrations appropriées des composés à tester, en ajoutant la même quantité de virus de chacun des puits, et la mesure de l'activité luciférase à déterminer la CC 50 et IC 50 valeurs.
Le test est sûr, quantitative et reproductible. Le test est sûr parce que le vecteur est déficient pour la replication. Le dosage est quantitatif et reproductible car il est basé sur un vecteur unique ronde qui exprime la luciférase, qui peut être dosé avec précision et commodément. Dans un dosage de réplication de virus tour multi, le CI 50 mesurée en fonction du nombre de cycles de vie viraux; il s'agit d'un problème particulier lorsque les dosages impliquent à la fois des virus WT et résistantes aux médicaments qui peuvent avoir des capacités différentes de façon significative de la réplication.
Il ya eu plusieurs dosages enzymatiques indiqué précédemment que possibleêtre utilisés pour cribler des inhibiteurs IN. Des essais qui impliquent une technologie de PCR en temps réel pour mesurer ADN intégré nécessitent des protéines recombinantes purifiées (s), et sont, en général, à la fois plus de main-d'oeuvre et onéreuse 36, 37. Bien qu'il soit possible d'utiliser des dosages enzymatiques pour mesurer l'impact des composés sur les autres enzymes virales (RT et la protéase), chaque enzyme nécessite son propre système de dosage. Le seul essai de tour vecteur, tel que décrit, peut être utilisé, sans modification, pour dépister les inhibiteurs de la RT. Un dosage similaire peut être utilisée pour cribler des inhibiteurs de la protéase; Cependant, dans un essai d'inhibiteur de la protéase, les composés doivent être ajoutés à des cellules utilisées pour produire les vecteurs. Un dosage liée, en utilisant différentes cellules et des vecteurs, peut également être utilisé pour le dépistage de l'enveloppe (env) et des inhibiteurs de fusion du VIH entrée. Enfin, le dosage peut être utilisé, à plus grande échelle, avec des distributeurs robotiques automatisés. Ainsi, le test peut être utilisé pour cribler de grandes banques de composés contre le WT et le mutant VIH. Toutefois, le fait le test peut détecter un inhibiteur de la réplication du VIH qui agit à différents stades de points de cycle de vie viral à une limitation dans l'interprétation des données. Par lui-même le dosage qui ne définit pas l'étape dans le cycle de vie est bloqué par un composé. Si cette question se pose, il peut être résolu en utilisant des dosages de temps d'addition 38, et en testant le composé contre des protéines virales recombinantes purifiées.
Malheureusement, malgré le succès des médicaments anti-VIH, il ya encore des problèmes à la fois la résistance et la toxicité. En l'absence d'un vaccin anti-VIH efficace, il est nécessaire non seulement pour développer de nouveaux médicaments thérapeutiques qui seront efficaces contre les mutants résistants aux médicaments existants, mais également de développer des médicaments prophylactiques qui peuvent réduire la propagation du virus. Si l'utilisation prophylactique de médicaments anti-VIH incudes le traitement des personnes non infectées, cette approche sera un fardeau spécial sur le développement de médicaments qui sont ont little ou pas de toxicité à long terme.
Déclarations de divulgation
Les auteurs n'ont rien à révéler.
Remerciements
Cette recherche a été financée par le Programme de recherche intra-muros du NCI.
matériels
| Name | Company | Catalog Number | Comments |
| DMSO | Sigma | D2650 | |
| DMEM | Corning Cellgro | 10-017 | |
| ATPlite Luminescence ATP Detection Assay System | Perkin Elmer | 6016941 | |
| Steady Lite Plus High Sensitivity Luminescence Reporter Gene Assay System | Perkin Elmer | 6016751 | |
| Dulbecco's PBS | Gibco-Life Technologies-Invitrogen | 14190-136 | |
| SpectraMax Gemini EM | Molecular Devices | ||
| KaleidaGraph | Synergy Software | ||
| Nunc F96 Microwell White Polystyrene Plate | Thomas Scientific | 12-566-26 | |
| Eppendorf Thermomixer Compact | Sigma Aldrich | T1442-1EA | |
| Turbo DNase | Ambion-Life Technologies-Invitrogen | AM2238 | |
| Millex HA Filter Unit, 0.45 µM | Millipore | SLAHA033SS | |
| Alliance HIV-1 p24 Elisa Kit | Perkin Elmer | NEK050B001KT | |
| HOS cells | ATCC | CRL-1543 | |
| TZM-bl cells | NIH AIDS Reagent Program | 8129 | |
| pNL4.3ΔEnv.LUC | NIH-NCI HIV Drug Resistance Program- Hughes Lab | ||
| VSV-G | NIH-NCI HIV Drug Resistance Program- Hughes Lab | ||
| SoftMax Pro | Molecular Devices | 0200-310 |
Références
- Mouton, Y., et al. Impact of protease inhibitors on AIDS-defining events and hospitalizations in 10 French AIDS reference centres. Federation National des Centres de Lutte contre le SIDA. AIDS. , 101-105 (1997).
- Hammer, S. M., et al. A controlled trial of two nucleoside analogues plus indinavir in persons with human immunodeficiency virus infection and CD4 cell counts of 200 per cubic millimeter or less AIDS Clinical Trials Group 320 Study Team. New Eng. J. Med. 337, 725-733 (1997).
- Hogg, R. S., et al. Improved survival among HIV-infected patients after initiation of triple-drug antiretroviral regimens. Can. Med. Assoc. 160, 659-665 (1999).
- Egger, M., et al. Impact of new antiretroviral combination therapies in HIV infected patients in Switzerland: prospective multicentre study. Swiss HIV Cohort Study. BMJ. 315, 1194-1199 (1997).
- Gulick, R. M., et al. Treatment with indinavir, zidovudine, and lamivudine in adults with human immunodeficiency virus infection and prior antiretroviral therapy. New Eng. J. Med. 337, 734-739 (1997).
- Perelson, A. S., Neumann, A. U., Markowitz, M., Leonard, J. M., Ho, D. D. HIV-1 dynamics in vivo: virion clearance rate, infected cell life-span, and viral generation time. Science. 271, 1582-1586 (1996).
- Simoni, J. M., Amico, K. R., Pearson, C. R., Malow, R. Strategies for promoting adherence to antiretroviral therapy: a review of the literature. Curr. Infect. Dis. Rep. 10, 515-521 (2008).
- Simoni, J. M., Amico, K. R., Smith, L., Nelson, K. Antiretroviral adherence interventions: translating research findings to the real world clinic. Curr. HIV/AIDS Rep. 7, 44-51 (2010).
- Volberding, P. A., Deeks, S. G. Antiretroviral therapy and management of HIV infection. Lancet. 376, 49-62 (2010).
- Acosta, E. P., et al. Novel method to assess antiretroviral target trough concentrations using in vitro susceptibility data. Antimicr. 56, 5938-5945 (2012).
- Rockstroh, J. K., et al. Long-term treatment with raltegravir or efavirenz combined with tenofovir/emtricitabine for treatment-naive human immunodeficiency virus-1-infected patients: 156-week results from STARTMRK. Clin. Infect. Dis. 53, 807-816 (2011).
- Fernandez-Montero, J. V., Eugenia, E., Barreiro, P., Labarga, P., Soriano, V. Antiretroviral drug-related toxicities - clinical spectrum, prevention, and management. Exp. Opin. Drug Safety. , (2013).
- Lunzen, J., et al. Once daily dolutegravir (S/GSK1349572) in combination therapy in antiretroviral-naive adults with HIV: planned interim 48 week results from SPRING-1, a dose-ranging, randomised, phase 2b trial. Lancet Infect Dis. 12, 111-118 (2012).
- Sax, P. E., et al. Co-formulated elvitegravir, cobicistat, emtricitabine, and tenofovir versus co-formulated efavirenz, emtricitabine, and tenofovir for initial treatment of HIV-1 infection: a randomised, double-blind, phase 3 trial, analysis of results after 48 weeks. Lancet. 379, 2439-2448 (2012).
- Sax, P. E., et al. Abacavir/lamivudine versus tenofovir DF/emtricitabine as part of combination regimens for initial treatment of HIV: final results. Infect. Dis. 204, 1191-1201 (2011).
- Kellam, P., Larder, B. A. Recombinant virus assay: a rapid, phenotypic assay for assessment of drug susceptibility of human immunodeficiency virus type 1 isolates. Antimicr. Agents Chemother. 38, 23-30 (1994).
- Hertogs, K., et al. A rapid method for simultaneous detection of phenotypic resistance to inhibitors of protease and reverse transcriptase in recombinant human immunodeficiency virus type 1 isolates from patients treated with antiretroviral drugs. Antimicr. Agents Chemother. 42, 269-276 (1998).
- Petropoulos, C. J., et al. A novel phenotypic drug susceptibility assay for human immunodeficiency virus type 1. Antimicr. Agents Chemother. 44, 920-928 (2000).
- Engelman, A., Mizuuchi, K., Craigie, R. HIV-1 DNA integration: mechanism of viral DNA cleavage and DNA strand transfer. Cell. 67, 1211-1221 (1991).
- Hazuda, D. J., et al. Inhibitors of strand transfer that prevent integration and inhibit HIV-1 replication in cells. Science. 287, 646-650 (2000).
- Nguyen, B. Y., et al. Raltegravir: the first HIV-1 integrase strand transfer inhibitor in the HIV armamentarium. Ann. N.Y. Acad. Sci. 1222, 83-89 (2011).
- Wills, T., Vega, V. Elvitegravir: a once-daily inhibitor of HIV-1 integrase. Exp. Opin. Invest. Drugs. 21, 395-401 (2012).
- Kobayashi, M., et al. In Vitro antiretroviral properties of S/GSK1349572, a next-generation HIV integrase inhibitor. Antimicr. Agents Chemother. 55, 813-821 (2011).
- Cooper, D. A., et al. Subgroup and resistance analyses of raltegravir for resistant HIV-1 infection. Eng. J. Med. 359, 355-365 (2008).
- Briz, V., et al. Raltegravir and etravirine are active against HIV type 1 group O. AIDS Res.Human Retroviruses. 25, 225-227 (2009).
- Fransen, S., et al. Loss of raltegravir susceptibility by human immunodeficiency virus type 1 is conferred via multiple nonoverlapping genetic pathways. J. Virol. 83, 11440-11446 (2009).
- Goethals, O., et al. Primary mutations selected in vitro with raltegravir confer large fold changes in susceptibility to first-generation integrase inhibitors, but minor fold changes to inhibitors with second-generation resistance profiles. Virology. 402, 338-346 (2010).
- Goethals, O., et al. Resistance mutations in human immunodeficiency virus type 1 integrase selected with elvitegravir confer reduced susceptibility to a wide range of integrase inhibitors. J. Virol. 82, 10366-10374 (2008).
- Canducci, F., et al. Dynamic patterns of human immunodeficiency virus type 1 integrase gene evolution in patients failing raltegravir-based salvage therapies. AIDS. 23, 455-460 (2009).
- Ceccherini-Silberstein, F., et al. Characterization and structural analysis of HIV-1 integrase conservation. AIDS Rev. 11, 17-29 (2009).
- Charpentier, C., et al. Drug resistance profiles for the HIV integrase gene in patients failing raltegravir salvage therapy. HIV Med. 9, 765-770 (2008).
- Julias, J. G., et al. Effects of mutations in the G tract of the human immunodeficiency virus type 1 polypurine tract on virus replication and RNase H cleavage. J. Virol. 78, 13315-13324 (2004).
- Hare, S., et al. Structural and functional analyses of the second-generation integrase strand transfer inhibitor dolutegravir (S/GSK1349572). Mol. Pharmacol. 80, 565-572 (2011).
- Adachi, A., et al. Production of acquired immunodeficiency syndrome-associated retrovirus in human and nonhuman cells transfected with an infectious molecular clone. J. Virol. 59, 284-291 (1986).
- Kemp, S. D., et al. A novel polymorphism at codon 333 of human immunodeficiency virus type 1 reverse transcriptase can facilitate dual resistance to zidovudine and L-2',3'-dideoxy-3'-thiacytidine. J. Virol. 72, 5093-5098 (1998).
- Butler, S. L., Hansen, M. S., Bushman, F. D. A quantitative assay for HIV DNA integration in vivo. Nat. Med. 7, 631-634 (2001).
- Brussel, A., et al. Longitudinal monitoring of 2-long terminal repeat circles in peripheral blood mononuclear cells from patients with chronic HIV-1 infection. AIDS. 17, 645-652 (2003).
- Daelemans, D., Pauwels, R., De Clercq, E., Pannecouque, C. A time-of-drug addition approach to target identification of antiviral compounds. Nat. Protoc. 6, 925-933 (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon