Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Comprendre Dissous Matière organique biogéochimie Grâce
Dans cet article
Résumé
La matière organique dissoute constitue une importante source d'énergie et de nutriments aux flux écosystèmes. Ici , nous démontrons une méthode sur le terrain pour manipuler la piscine ambiante de la matière organique dissoute in situ par des impulsions de nutriments facilement réplicables.
Résumé
Dissolved organic matter (DOM) is a highly diverse mixture of molecules providing one of the largest sources of energy and nutrients to stream ecosystems. Yet the in situ study of DOM is difficult as the molecular complexity of the DOM pool cannot be easily reproduced for experimental purposes. Nutrient additions to streams however, have been shown to repeatedly alter the in situ and ambient DOM pool. Here we demonstrate an easily replicable field-based method for manipulating the ambient pool of DOM at the ecosystem scale. During nutrient pulse experiments changes in the concentration of both dissolved organic carbon and dissolved organic nitrogen can be examined across a wide-range of nutrient concentrations. This method allows researchers to examine the controls on the DOM pool and make inferences regarding the role and function that certain fractions of the DOM pool play within ecosystems. We advocate the use of this method as a technique to help develop a deeper understanding of DOM biogeochemistry and how it interacts with nutrients. With further development this method may help elucidate the dynamics of DOM in other ecosystems.
Introduction
La matière organique dissoute (DOM) fournit une source d'énergie et de nutriments importants écosystèmes d'eau douce et est définie comme la matière organique qui passe à travers un filtre de 0,7 um. Dans les écosystèmes aquatiques, DOM peut également influer sur l'atténuation de la lumière et de complexation de métal. DOM est un mélange très diverse et hétérogène de composés organiques avec divers groupes fonctionnels, ainsi que des éléments nutritifs essentiels tels que l'azote (N) et du phosphore (P). Bien que le terme "DOM" décrit toute la piscine, y compris son C, N et P composantes, sa concentration est mesurée en carbone organique dissous (COD). Cependant, la complexité moléculaire inhérente à la piscine DOM crée des défis à son étude. Par exemple, il n'y a aucun moyen direct de mesurer la fraction de la piscine DOM totale composée de nutriments organiques tels que l'azote organique dissous (DON) et phosphore organique dissous (DOP). Au lieu de cela, la concentration des nutriments organiques doit être déterminée par la différence ( par exemple [DON] = [azote total dissous] - [azote inorganique dissous]).
Ajout d'un amendement DOM réaliste à un flux est difficile en raison de la diversité de la piscine DOM ambiante. Des études antérieures ont ajouté des sources de carbone simples (par exemple le glucose, l' urée 1) ou une source particulière telle que la litière de feuilles lixiviat 2 à manipuler des concentrations dans le domaine. Toutefois, ces sources ne sont pas particulièrement représentatif de la piscine DOM ambiante. Essayer d'affiner ou de concentré DOM ambiante pour l' expérimentation ultérieure est également forgé avec des difficultés , y compris la perte de certaines fractions (par exemple des composants hautement labiles) au cours du traitement. En conséquence, il est difficile de comprendre les contrôles sur la piscine DOM ambiante que nous ne possédons actuellement pas de méthode pour manipuler directement la piscine DOM ambiante. Cependant, étant donné que la biogéochimie des DOM est liée aux nutriments couramment dans l'environnement (par exemple nittaux [NO 3 -] 3), nous pouvons ajouter d' autres solutés à flux écosystèmes et de mesurer la réponse de la piscine DOM à ces manipulations. En examinant la façon dont la piscine DOM répond à une large gamme de concentrations en nutriments expérimentalement imposées, nous espérons acquérir une meilleure visibilité sur la façon dont DOM répond aux fluctuations des conditions environnementales.
Une méthode couramment utilisée dans le courant biogéochimie est la méthode d'ajout d'éléments nutritifs. Expériences d'addition d' éléments nutritifs ont traditionnellement été utilisés pour comprendre la cinétique absorption ou le sort de la 4,5,6,7 soluté ajouté. Ajouts d'éléments nutritifs peuvent être à court terme sur l'heure 6 à l' échelle de jour 4 ou manipulations à long terme au cours de plusieurs années 8. Ajouts d'éléments nutritifs peuvent également inclure des éléments nutritifs isotopiquement marqué (par exemple 15 N-NO 3 -) pour tracer des éléments nutritifs ajoutés par des réactions biogéochimiques. Cependant, les études sur la base isotopes sont souvent EXPEnsive et nécessitent des analyses difficiles (par exemple les digestions) des compartiments multiples benthiques où les nutriments marqués par des isotopes peuvent être conservés. L' expérimentation récente a révélé l'utilité des impulsions de nutriments à court terme afin d' élucider les contrôles sur les solutés non-ajoutée et ambiantes telles que DOM 9,10, révélant une nouvelle façon par laquelle d'examiner en temps réel dans les réactions biogéochimiques in situ. Nous décrivons ici et de démontrer les principales étapes méthodologiques à mener des impulsions de nutriments à court terme dans le but de comprendre la biogéochimie couplée de C et N et en particulier les contrôles sur la piscine DOM très diversifié. Cette méthode consiste à ajouter facilement reproductible d' une impulsion de nutriments dans un flux portée expérimentale et mesurer les variations de la concentration à la fois du soluté et de la variable manipulée de réponse d'intérêt (par exemple , DOC, le DON, DOP). En manipulant directement les concentrations de nutriments in situ , nous sommes en mesure de modifier indirectement les DOMpiscine et examiner comment DOM changements de concentration à travers une gamme dynamique de concentrations en éléments nutritifs 10.
Access restricted. Please log in or start a trial to view this content.
Protocole
1. Identification et caractérisation de l'Idéal volet expérimental Portée
- Veiller à ce que flux atteint expérimentaux sont assez longtemps pour favoriser le mélange complet des solutés 11 et assez longues où l' absorption biologique peut se produire. longueurs Reach peuvent varier selon les cours d'eau et des expériences. Dans les petits ruisseaux de tête de premier ordre, atteindre la longueur peut varier de 20 à 150 m (ou plus si le système exige) en fonction de décharge et d'autres propriétés physiques du flux.
- Exclure de grandes piscines atteint expérimentales, car ils retardent le mouvement en aval de solutés, des sections d'écoulement minimales, et les affluents qui diluent la solution ajoutée. Les périodes de faible débit peuvent nécessiter de raccourcir la longueur de portée tout en décharge plus élevée peut nécessiter une plus longue portée.
- Identifier un emplacement en haut du flux portée expérimentale ci-dessus un riffle pour faciliter le mélange des solutés ajoutés. Ce sera le site d'addition. Au bas du volet expérimentalatteindre, identifier un emplacement où l' écoulement est étranglé , et représentant environ 90% du flux total (figure 1). Ce sera le site de collecte de l'échantillon.

Figure 1:. Exemple d'aval d' échantillonnage du site Un site d'échantillonnage idéal est où la majorité des flux est resserrée et facilement accessible sans perturbation du canal de flux et le benthos. Voici un morceau tombé de débris de bois a créé ce point dans un petit cours d' eau d'amont de premier ordre échantillonnage. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
- Obtenir des concentrations de mesure de décharge et de fond en éléments nutritifs des solutés d'intérêt avant les expériences afin de calculer la masse des solutés nécessaires à la manippopu-. S'il vous plaît voir les calculs à l'étape 2.2.1.
- Obtenir des données de concentration de fond pour le soluté cible de manipulation (par exemple NO 3 -) et le chlorure (Cl -) qui est souvent utilisé comme traceur conservateur. Utilisez le traceur conservateur dans le cadre de ces expériences, de suivre l'évolution de la conductivité, qui indiquent l'arrivée de l'impulsion de nutriments à la station d'échantillonnage et de la vitesse à laquelle l'impulsion traverse. Conductivité ou conductance spécifique, est un substitut pour les changements in situ dans la concentration du traceur conservateur.
- Caractériser les propriétés physico-chimiques de la portée expérimentale en recueillant des données auxiliaires telles que la largeur de la portée et de la profondeur, la température, le pH et l'oxygène dissous.
- Effectuer des mesures qui ne peuvent être faites avec l'utilisation d'une sonde de l' environnement (par exemple , la largeur et la profondeur), le jour avant ou immédiatement après l'expérience afin de minimiser toute benthique or perturbation chimique dans le canal de flux. Divisez la portée expérimentale en transects équidistants (par exemple tous les 10 m) où la largeur et au moins 3 mesures de profondeur peuvent être évaluées (par exemple , rive droite, thalweg et rive gauche). Ces données sont utiles pour relier les propriétés physiques d'un flux de mesures biogéochimiques et si les chercheurs sont également intéressés par le calcul de la cinétique et paramètres 6 absorption des éléments nutritifs.
2. Préparation pour l'expérience
- Déterminer la masse (kg) de soluté nécessaire pour la manipulation en utilisant les équations décrites ci-dessous.
Remarque: L'exemple ci - dessous applique à une expérience à base de nitrate avec NO 3 - sous la forme de nitrate de sodium (NaNO 3) et suppose une augmentation ciblée de 3x dessus du fond (équations sont basées sur celles de Kilpatrick et Cobb 12). Dans cet exemple, les hypothèses suivantes ont été faites avec des respect aux conditions de fond: décharge = 10 L / sec; [Cl] = 10 mg / L; [NO 3 -] = 50 pg N / L. En raison de la variation entre les expériences, ajuster les données d'entrée nécessaires.- Calculer l'augmentation ciblée (équation 1):
Ciblée [NO 3 - N ug / L] = augmentation attendue de fond [NO 3 - N ug / L] augmentation * ciblée
150 pg N / L = 50 pg N / L * 3 - Calculer le flux de masse atomique totale (équation 2):
Totale du flux de masse atomique (NO 3 - ig N) = 30 min 60 s * * Q (l / sec) * ciblée [NO 3 - N ug / L] Augmentation
Lorsque 30 minutes est la durée supposée de soluté pic 12 et Q est décharge
2 700 000 * 150 pg N s pg N = 30 min 60 sec * * 10 L / / L - Calculer le flux de masse moléculaire totale (équation 3):
Masse totale moléculaire flux (NO 3 - pg N) = flux total de masse atomique (NO 3 - N pg) / masse atomique (14) * de nous moléculaireight (85)
Lorsque la masse atomique se réfère à N et le poids moléculaire se réfère à NaNO 3.
16,392,857.14 pg N = 2.700.000 pg N / (14 * 85) - Calculer la masse pour ajouter (équation 4):
Mass pour ajouter (g) = flux total de masse moléculaire (NO 3 - pg N) / 1.000.000 g / pg
16,39 g de NaNO 3 = 16,392,857.14 pg N / 1.000.000 g / pg
Remarque: Suivez les calculs ci - dessus pour d'autres solutés , y compris le traceur conservateur (par exemple chlorure de sodium). Assurez-vous de régler les masses atomiques et moléculaires pour le soluté d'intérêt.
- Calculer l'augmentation ciblée (équation 1):
- Préparer tous les solutés un jour avant des expériences de terrain. Peser suffisamment de solutés pour augmenter la concentration ambiante à la fois du traceur biologique et le traceur conservateur trois fois (ou quantité désirée) au-dessus de fond. Il est important que la quantité de solutés ajoutée provoque un changement mesurable au-dessus de la concentration de fond qui est suffisante pour créer awplage dynamique ide de la concentration en éléments nutritifs ajoutés.
- Peser solutés utilisant des échelles d'analyse et de stocker ensuite dans des bouteilles en polyéthylène propres lavés à l'acide à haute densité avec des étiquettes appropriées. Des exemples de traceurs biologiques comprennent: NO 3 -: nitrate de sodium (NaNO 3); NH 4 +: chlorure d'ammonium (NH 4 Cl); PO 4 -3: phosphate de potassium (K 2 HPO 4). Cependant, le choix du traceur biologique sera fonction de la question posée biogéochimique. Les options pour les traceurs conservateurs comprennent le chlorure de sodium (NaCl) et de bromure de sodium (NaBr).
- Collecter les matériaux restants: le livre de champ, bande d'étiquetage et de stylo, bande de mesure de champ, refroidisseur, conductivité mètre, ~ 20 L seau et une grande tige d'agitation (par exemple la bière paddle, des barres d' armature, gros bâton), environ 50 propres et lavés à l' acide 125 ml haute bouteilles en polyéthylène -density. Etiqueter les flacons de 125 ml # 1-50.
Note: Less de 50 échantillons peuvent être prélevés par expérience et des échantillons de fond sont inclus dans les 50 bouteilles au total. - Facultatif: Selon le nombre de personnel de terrain, effectuer un filtrage de l'échantillon sur place (voir la section 5). Si cette option est choisie, apporter 50 propres 60 ml bouteilles en polyéthylène, pré-étiquetés et lavés à l'acide à haute densité dans le champ. Etiqueter les flacons de 60 ml # 1-50 pour faire correspondre les bouteilles 125 de collecte ml.
3. Jour de Set Up
- Déployer le champ compteur de conductivité sur le site de collecte. Placez l'instrument amont (environ 0,5-1,0 m) où les échantillons seront prélevés collection donc l'échantillon ne pas interférer avec les lectures des instruments. Le compteur restera en place pendant toute l'expérience. Un compteur champ de conductivité est meilleure car elle fournit des lectures de conductivité en temps réel, qui sont nécessaires pour déterminer le taux d'échantillonnage (voir étape 5.2) et la filtration et l'ordre d'analyse (étapes 5.3 et 6.1).
- Recueillir 125 ml de fond samples en triple exemplaire au niveau du site d'addition et à l'emplacement de prélèvement de la portée expérimentale avant l'addition de la solution. Ces données seront utilisées pour vérifier au jour de la concentration ambiante et de déterminer la variation de la concentration en soluté le long du tronçon de rivière. Ces données sont également précieuses pour relier la chimie de flux ambiante: - aux mesures biogéochimiques d'intérêt (par exemple DOC NO 3 rapports 13.).
- Notez l'heure et de la conductivité des échantillons de fond recueillies.
- Notez la conductivité du flux de fond avant l'addition de solutions.
4. solutés Ajout
- Verser tous les réactifs (16,39 g NaNO 3 et 1,483 g de NaCl) dans un grand récipient (par exemple 20 L seau) et ajouter de l' eau des cours d'eau suffisante pour dissoudre complètement les solutés. Rincer les navires de réactifs trois fois avec de l'eau des cours d'eau supplémentaire et verser de rinçage dans le récipient de solution. Gardez une trace de quantité d'eau ajoutée.
- Par exemple, utiliser une bouteille de 500 ml à verser de l'eau des cours d'eau dans le récipient. Remuer solution jusqu'à ce que tous les réactifs ont été complètement dissous.
- Recueillir 60 ml d'aliquote de la solution d'addition. Gardez cet échantillon très concentré (par exemple sac zip-lock) séparé de tous les autres échantillons pour réduire au minimum la contamination croisée. Ces échantillons sont importants si nutritifs calcul absorption cinétique 6 est un objectif supplémentaire du projet de recherche que ces échantillons peuvent être utilisés pour déterminer la masse exacte de solutés ajouté.
- Verser la solution dans le site d'addition. Pour ce faire, en versant la solution dans un mouvement fluide et rapide afin de minimiser Voyage temps de latence et les éclaboussures qui pourraient réduire la quantité de réactifs ajoutés. Rincer le contenant et le bâton à mélanger trois fois dans le courant immédiatement après l'addition de garantir tous les réactifs ont été ajoutés au flux.
- Noter le temps a été ajouté la solution: h: min: sec.
- Notez les masses de traceurs ajoutés(Par exemple NaNO 3 et NaCl).
- Après que la solution a été ajoutée, ne perturbent pas le flux. Assurez-vous que tous les Voyage le long du ruisseau se produit sur les banques pour assurer que le benthos de flux et de la solution elle-même ne sont pas perturbés.
5. Champ d'échantillonnage
- Commandez des bouteilles d'échantillonnage dans l'ordre croissant en attendant la solution pour arriver à l'emplacement d'échantillonnage. Temps de Voyage sera fonction du débit et d' atteindre la longueur et peut être déterminée à l' avance (un jour avant) , soit avec une seule injection de NaCl ou rhodamine colorant (qui peut être utilisé pour établir le temps de Voyage 14).
Remarque: Si vous travaillez sur un projet DON thème, évitez d'utiliser la rhodamine colorant comme il est un type de DON et va donc modifier la température ambiante DON piscine si tout reste à la portée de l'étude.

Figure 2:Exemple schématique de soluté Curve Breakthrough (BTC). Un BTC représente des changements de concentration de soluté dans le temps et peut être utilisé pour expliquer le transit et le cycle biogéochimique d'un traceur dans un flux. Des échantillons choisis doivent être prises à travers le BTC avec une fréquence qui donne une représentation égale à la fois ascendant et descendant membres du BTC. S'il vous plaît cliquez ici pour voir une version plus grande de cette figure.
- Collecte d'échantillons
Note: L'objectif primordial de la collecte de l' échantillon, est de représenter adéquatement l' évolution de la concentration de soluté le long des deux branches montantes et descendantes de la rupture à travers la courbe (BTC) (Figure 2).- À l'arrivée de la solution (détectée par une augmentation de la conductivité), prélever des échantillons dans 125 ml de bouteilles à travers le BTC en tenant une bouteille de 125 ml dans le flux principal de l'eau au point d'échantillonnage. Rapidely rincer la bouteille avec de l'eau des cours d'eau et jeter rincer aval et puis prendre l'échantillon. échantillon de Cap et le lieu dans refroidisseur.
- Noter le temps (h: min: sec) et la conductivité de chaque échantillon prélevé le long de la CTB dans un livre de champ (tableau 1).
- Prélever des échantillons en fonction du temps (par exemple des intervalles de 1 min) ou en fonction de la vitesse à laquelle les changements de conductivité. Par exemple, si la conductivité évolue rapidement, échantillonner tous les 30-60 secondes jusqu'à ce que les changements de conductivité lente, au cours de laquelle des échantillons de temps peuvent être prises toutes les 5-10 minutes. Pour les intervalles basés sur la conductivité, prélever des échantillons toutes les 15-30 unités en fonction de la vitesse à laquelle la conductivité change.
- Exemple jusqu'à conductivité retourne à fond ou dans 5 microsiemens / cm de conditions de fond. Intervalles de collecte d'échantillons peuvent être ajustés pendant l'expérience aussi longtemps que le BTC est bien représentée dans les échantillons ponctuels.
| Bouteille # | conductance spécifique | Temps | Remarques |
| 1 | h: min: sec | par exemple fond ( en aval) | |
| 2 | par exemple fond ( en aval) | ||
| 3 | |||
| 4 | |||
| 5 | par exemple , l' échantillon au pic de conductance | ||
| . | |||
| . | |||
| . | |||
| La plus élevée Bouteille # |
Tableau 1PFieldlivre: Exemple Page du Lab Book et renseignements requis
- filtrage Sample
Remarque: Le filtrage des échantillons peut se produire soit sur le terrain ou lors du retour au laboratoire.- Filtrer les échantillons de la branche montante afin de monter la conductivité spécifique jusqu'à ce que le pic de conductivité spécifique. Attendez que l'expérience soit terminée et des échantillons de filtre de la branche tombant dans l' ordre croissant de conductivité spécifique (c. -à commencer par le dernier échantillon et de travailler vers l' arrière vers la conductivité spécifique de pointe).
Remarque: Cette commande d'échantillons évite toute contamination croisée entre les échantillons et permet pour le même filtre, la seringue et le porte-filtre doit être utilisé aussi longtemps que le filtre, la seringue et le porte-filtre sont rincées de manière appropriée entre chaque échantillon (voir les étapes 5.3.2 5.3.4). - Retirer le piston d'une seringue de 60 ml puis fermez le robinet d'arrêt. Versez ~ 10 ml d'échantillon dans la seringue et revenir piston pour seringue. Agiter la seringue de telle sorte que l'échantillonrinçages parois internes de la seringue. seringue Attaché au porte-filtre et ouvert le robinet d'arrêt. Poussez échantillon à travers porte-filtre et jeter rincer.
- Retirer le piston et à proximité du robinet d'arrêt. Versez ~ 30 ml d'échantillon dans la seringue et revenir piston pour seringue. Ouvrir de stock-coq et expulser ~ 10 ml par porte-filtre et dans 60 ml d'échantillonnage bouteille. Boucher le flacon, agiter avec filtrat et les jeter. Répétez cette étape pour un total de 3 rinçages. Cela permettra d'assurer toutes les impuretés ont été retirées du flacon d'échantillon 60 ml et que les parois sont revêtues d'échantillon.
- Retirer le piston et à proximité du robinet d'arrêt. Versez ~ 60 ml d'échantillon dans la seringue et revenir piston pour seringue. Poussez l'échantillon dans le porte-filtre et dans le 60 ml flacon d'échantillonnage. Remplir les bouteilles jusqu'à l'épaule pour empêcher la fissuration des bouteilles lors de la congélation. bouteille Cap et lieu en refroidisseur.
- Répétez les étapes 5.3.2-5.3.4 pour tous les échantillons restants. Changer le filtre entre la hausse et la baisse des échantillons des membres pour minimiser la contamination.
- Transporter les échantillons au laboratoire le même jour et sur la glace.
- Filtrer les échantillons de la branche montante afin de monter la conductivité spécifique jusqu'à ce que le pic de conductivité spécifique. Attendez que l'expérience soit terminée et des échantillons de filtre de la branche tombant dans l' ordre croissant de conductivité spécifique (c. -à commencer par le dernier échantillon et de travailler vers l' arrière vers la conductivité spécifique de pointe).
6. Préparation de l'analyse de laboratoire
- Si le filtrage des échantillons doit se produire dans le laboratoire, suivre le protocole tel que décrit dans la section 5.3.1. Filtrer les échantillons à la fois ascendante et descendante des membres de la CTB afin d'augmenter la conductivité. Changer le filtre entre la hausse et la baisse des membres des échantillons des membres.
- Congeler des échantillons filtrés à -20 ° C jusqu'à l'analyse.
- Veiller à ce que les installations d'analyse sont équipés pour manipuler des échantillons très concentrés.
Remarque: Certains laboratoires ne sont pas équipés pour exécuter des échantillons très concentrés et les soins doivent donc être prises. Incorporer les normes préparées qui capturent cette fin plus élevée des concentrations de soluté attendues. Des normes élevées de concentration contribueront à assurer une courbe standard qui capture la plage attendue de concentrations de soluté manipulées. - Analyser des échantillonsde faible à haute conductivité sur tous les instruments analytiques. Commande des échantillons de faible à élevé conductance spécifique empêche la contamination des échantillons de faible sel / éléments nutritifs par des échantillons élevés sel / éléments nutritifs. Cela signifie des échantillons provenant des membres ascendants et descendants seront mélangés par rapport à la séquence.
- Analyser des échantillons pour le carbone total organique dissous, l' azote total dissous, nitrate et ammonium, bien que la combinaison exacte de l' analyse de soluté sera fonction de la question de recherche (voir Wymore et al. 10 , par exemple).
Analyse 7. Données
- Analyser les données en utilisant la régression linéaire simple. La variable indépendante est la concentration de la substance nutritive ajoutée et la variable dépendante est la concentration DOM soit comme DOC ou DON. Chaque point de la figure représente un échantillon instantané de la courbe de percée et de nutriments de cet échantillon et DOC concentration / DON.
Access restricted. Please log in or start a trial to view this content.
Résultats
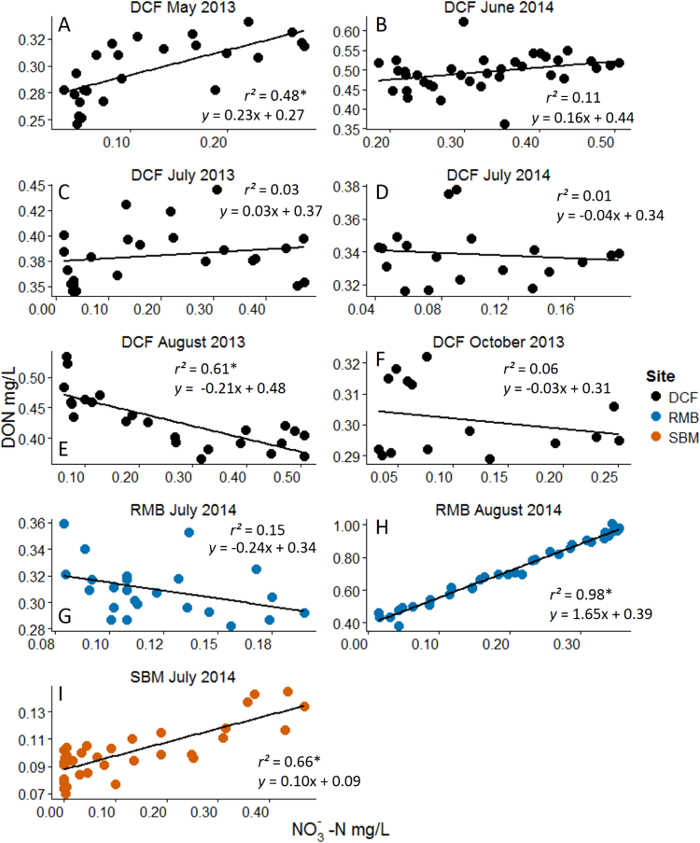
Figure 3: Exemple. Les résultats de Nitrate (NO 3 -) Additions avec Dissous azote organique (DON) comme variable de réponse Des analyses sont des régressions linéaires. Les astérisques représentent une signification statistique à α = 0,05. Noter que la plage dynamique de NO 3 - concentration qui a ?...
Access restricted. Please log in or start a trial to view this content.
Discussion
L'objectif de la méthode d'impulsion des éléments nutritifs, tel que présenté ici, est de caractériser et quantifier la réponse de la piscine très diversifiée de la température ambiante DOM de l'eau des cours d'eau à travers une gamme dynamique d'un nutriment inorganique ajouté. Si le soluté ajouté augmente suffisamment la concentration du soluté réactif, un grand espace déductive peut être créé pour comprendre comment le cycle biogéochimique des DOM est liée à des concentratio...
Access restricted. Please log in or start a trial to view this content.
Déclarations de divulgation
The authors have nothing to disclose.
Remerciements
The authors acknowledge the Water Quality Analysis Laboratory at the University of New Hampshire for assistance with sample analysis. The authors also thank two anonymous reviewers whose comments have helped to improve the manuscript. This work is funded by the National Science Foundation (DEB-1556603). Partial funding was also provided by the EPSCoR Ecosystems and Society Project (NSF EPS-1101245), New Hampshire Agricultural Experiment Station (Scientific Contribution #2662, USDA National Institute of Food and Agriculture (McIntire-Stennis) Project (1006760), the University of New Hampshire Graduate School, and the New Hampshire Water Resources Research Center.
Access restricted. Please log in or start a trial to view this content.
matériels
| Name | Company | Catalog Number | Comments |
| Sodium Nitrate | Any | Any | |
| Sodium Chloride | Any | Any | Store purchased table salt can be used as well, however, it does contain trace levels of impurities |
| Whatman GFF glass-fiber filters | Any | Any | |
| BD Filtering Syringe | Any | Any | |
| EMD Millipore Swinnex Filter Holders | Any | Any | |
| Syringe stop-cock | Any | Any | |
| YSI Multi-parameter probe | Yellow Springs International | 556-01 | |
| Wide mouth HDPE 125 ml bottles | Any | Any | |
| 60 ml HDPE bottles | Any | Any | |
| 20 L bucket | Any | Any | |
| Field measuring tape | Any | Any | |
| Lab labeling tape | Any | Any | |
| Stir stick | Any | Any | |
| Cooler | Any | Any | |
| Sharpie pen | Any | Any | |
| Field notebook | Any | Any | |
| Tweezers | Any | Any | |
| Zip-lock bags | Any | Any |
Références
- Brookshire, E. N. J., Valett, H. M., Thomas, S. A., Webster, J. R. Atmospheric N deposition increases organic N loss from temperate forests. Ecosystems. 10 (2), 252-262 (2007).
- Bernhardt, E. S., McDowell, W. H. Twenty years apart: Comparisons of DOM uptake during leaf leachate releases to Hubbard Brook Valley streams in 1979 and 2000. J Geophys Res. 113, G03032(2008).
- Taylor, P. G., Townsend, A. R. Stoichiometric control of organic carbon-nitrate relationships from soils to sea. Nature. 464, 1178-1181 (2010).
- Mulholland, P. J., et al. Stream denitrification across biomes and its response to anthropogenic nitrate loading. Nature. 452, 202-205 (2008).
- Tank, J. L., Rosi-Marshall, E. J., Baker, M. A., Hall, R. O. Are rivers just big streams? A pulse method to quantify nitrogen demand in a large river. Ecology. 89 (10), 2935-2945 (2008).
- Covino, T. P., McGlynn, B. L., McNamara, R. A. Tracer additions for spiraling curve characterization (TASCC): quantifying stream nutrient uptake kinetics from ambient to saturation. Limnol Oceanogr. 8, 484-498 (2010).
- Johnson, L. T., et al. Quantifying the production of dissolved organic nitrogen in headwater streams using 15 N tracer additions. Limnol Oceanogr. 58 (4), 1271-1285 (2013).
- Rosemond, A. D., et al. Experimental nutrient additions accelerate terrestrial carbon loss from stream ecosystems. Science. 347 (6226), 1142-1145 (2015).
- Diemer, L. A., McDowell, W. H., Wymore, A. S., Prokushkin, A. S. Nutrient uptake along a fire gradient in boreal streams of Central Siberia. Freshwater Sci. 34 (4), 1443-1456 (2015).
- Wymore, A. S., Rodríguez-Cardona, B., McDowell, W. H. Direct response of dissolved organic nitrogen to nitrate availability in headwater streams. Biogeochemistry. 126 (1), 1-10 (2015).
- Stream Solute Workshop. Concepts and methods for assessing solute dynamics in stream ecosystems. J N Am Benthol Soc. 9 (2), 95-119 (1990).
- Kilpatrick, F. A., Cobb, E. D. Measurement of discharge using tracers: U.S Geological Survey Techniques of Water-Resources Investigations. , http://pubs.usgs.gov/twri/twri3-a16 (1985).
- Rodríguez-Cardona, B., Wymore, A. S., McDowell, W. H. DOC: NO3- and NO3- uptake in forested headwater streams. J Geophys Res - Biogeo. 121, (2016).
- Kilpatrick, F. A., Wilson, J. F. Book 3 Chapter A9, Measurement of time of travel in streams by dye tracing. Techniques of Water-Resources Investigations of the United States Geological Survey. , (1989).
- Lutz, B. D., Bernhardt, E. S., Roberts, B. J., Mulholland, P. J. Examining the coupling of carbon and nitrogen cycles in Appalachian streams: the role of dissolved organic nitrogen. Ecology. 92 (3), 720-732 (2011).
- Michalzik, B., Matzner, E. Dynamics of dissolved organic nitrogen and carbon in a Central European Norway spruce ecosystem. Eur J Soil Sci. 50 (4), 579-590 (1990).
- Solinger, S., Kalbitz, K., Matzner, E. Controls on the dynamics of dissolved organic carbon and nitrogen in a Central European deciduous forest. Biogeochemistry. 55 (3), 327-349 (2001).
- Kaushal, S. S., Lewis, W. M. Patterns in chemical fractionation of organic nitrogen in Rocky Mountain streams. Ecosystems. 6 (5), 483-492 (2003).
- Kaushal, S. S., Lewis, W. M. Fate and transport of organic nitrogen in minimally disturbed montane streams of Colorado, USA. Biogeochemistry. 74 (3), 303-321 (2005).
Access restricted. Please log in or start a trial to view this content.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon