Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Calcul de la variabilité de la fréquence cardiaque à partir des données ECG des jeunes atteints de paralysie cérébrale pendant les sessions actives de jeux vidéo
Dans cet article
Résumé
Ce protocole décrit une méthode pour calculer la variabilité de fréquence cardiaque (HRV) des formes d'onde d'électrocardiogramme (ECG). Des formes d'ondes provenant d'enregistrements continus de fréquence cardiaque (HR) pendant les séances actives de jeu vidéo (AVG) ont été utilisées pour mesurer la performance aérobique des jeunes atteints de paralysie cérébrale (CP).
Résumé
L'objectif de cette étude était de générer une méthode de calcul de la variabilité de la fréquence cardiaque (VRC) à partir des formes d'ondes d'électrocardiogramme (ECG). Les formes d'onde ont été enregistrées par un moniteur RH que les participants (jeunes atteints de paralysie cérébrale (CP)) portaient lors de séances de jeux vidéo actifs (AVG). Les séances AVG ont été conçues pour promouvoir l'activité physique et la forme physique (performance aérobique) chez les participants. L'objectif était d'évaluer la faisabilité des AVAN en tant que stratégie d'intervention en physiothérapie (PT). Le HRH maximal (HRM) a été déterminé pour chaque participant et la zone de fréquence cardiaque cible (THRZ) a été calculée pour chacune des trois phases d'exercice de la séance AVG de 20 min : (échauffement à 40-60% mHR, conditionnement à 60-80% mHR, et refroidissement à 40-60% mHR). Chaque participant a joué trois jeux de 20 min au cours de la session AVG. Tous les matchs ont été joués assis sur un banc parce que de nombreux jeunes avec le CP ne peuvent pas se tenir debout pendant de longues périodes de temps. Chaque condition de jeu différait avec les participants utilisant des icônes de main seulement, des icônes de main et de pieds ensemble ou des icônes de pieds seulement pour recueillir des objets. L'objectif du jeu (appelé KOLLECT) est de collecter des objets pour gagner des points et éviter les dangers de ne pas perdre de points. Les dangers ont été utilisés dans les phases d'échauffement et de refroidissement uniquement pour favoriser un mouvement plus lent et contrôlé pour maintenir les RH dans la zone de fréquence cardiaque cible (THRZ). Il n'y avait aucun danger dans la phase de conditionnement pour favoriser des niveaux plus élevés et une activité physique plus intense. Des méthodes analytiques ont été utilisées pour générer des VRC (mesures sélectionnées du domaine temporel et du domaine de fréquence) à partir des données ECG afin d'examiner la charge de travail aérobie. Des applications récentes du VRC indiquent que les mesures à court terme (5 min) sont appropriées et que le biofeedback du VRC peut aider à améliorer les symptômes et la qualité de vie dans une variété de conditions de santé. Bien que les RH soient une mesure clinique bien acceptée pour examiner la performance et l'intensité aérobies dans les interventions de PT, HRV peut fournir l'information des fonctions autonomes de système, de récupération et d'adaptation pendant des sessions d'AVG.
Introduction
La paralysie cérébrale (CP) est l'incapacité physique la plus courante de l'enfance1. Le CP est causé par une insulte neurologique au cerveau en développement et est associé à des déficiences motrices telles que la faiblesse musculaire, la spasticité, le déconditionnement, et la diminution du contrôle moteur et de l'équilibre2,3. Le CP est une maladie non progressive, mais avec l'âge, les enfants deviennent moins actifs physiquement et plus sédentaires que leurs pairs ayant un développement typique (TD) principalement en raison de la demande accrue de croissance de leur systèmes musculo-squelettiques4.
Les jeunes atteints de CP reçoivent habituellement des services de physiothérapie (PT) pour améliorer la mobilité fonctionnelle et promouvoir l'activité physique et la forme physique (p. ex. endurance aérobique et musculaire)2. Souvent, l'accès aux services de PT et aux ressources communautaires est limité pour atteindre et maintenir ces objectifs de PT5,6. Les jeux vidéo actifs (AVA) peuvent être une stratégie réalisable dans les interventions PT axées sur l'activité dans les milieux cliniques, à domicile ou communautaires7,8. Les AVAN commerciaux ont une flexibilité limitée pour adapter le jeu et répondre aux besoins spécifiques et aux objectifs de PT pour les jeunes avec CP9. Cependant, les AVAN personnalisés offrent des paramètres de jeu flexibles pour défier les jeunes atteints de CP tout en favorisant l'activité physique et la condition physique10.
Notre équipe a mis au point un AVG personnalisé (appelé KOLLECT) pour examiner les réponses à l'exercice chez les jeunes (p. ex., l'activité physique et la condition physique). Le jeu utilise un capteur de mouvement pour suivre le mouvement des jeunes pendant le jeu. Le but du jeu est de «collecter» autant d'objets que possible pour un score élevé et d'éviter les dangers pour éviter de perdre des points. Les objets peuvent être collectés avec des icônes de main et/ou de pieds déterminées par le thérapeute dans les paramètres de jeu flexibles.
Concevoir des interventions PT axées sur l'activité qui dilanulel l'intensité de l'activité physique pour promouvoir la condition physique aérobique est essentiel pour les jeunes atteints de CP11. Les AVAN personnalisés peuvent être une stratégie efficace pour doser l'intensité et faire participer les jeunes à l'activité physique afin de promouvoir la forme physique10. Les moniteurs de fréquence cardiaque (HR) sont souvent utilisés dans la pratique clinique de PT pour déterminer la performance aérobie et l'intensité d'activité. Par conséquent, les moniteurs RH aideront à déterminer la faisabilité des AVAN dans le dosage de l'intensité de l'activité physique pour promouvoir la forme physique aérobie9. Les données ECG générées à partir d'un moniteur RH peuvent être utilisées pour calculer la variabilité de la fréquence cardiaque (VRC). Des méthodes analytiques ont été utilisées pour générer des VrC à partir des données ECG afin d'examiner la charge de travail aérobie. Les applications récentes du VRC indiquent que les mesures à court terme (5 min) sont appropriées et que le biofeedback du VRC peut aider à améliorer les symptômes et la qualité de vie dans une variété de conditions de santé32,33,34 . L'application de mesures à court terme de VRC est un moyen approprié d'évaluer la fonction cardiovasculaire pendant les séances d'AVG. Étant donné que le VRC est dérivé de l'intervalle R-R d'un ECG, nous avons utilisé des mesures de domaine temporel et de fréquence sélectionnées. La mesure du domaine temporel du VRC quantifie la quantité de variablilité dans les intervalles interbeat qui représente le temps entre les battements de cœur successifs. Nous avons utilisé l'AVNN (intervalle NN moyen), RMSSD (carré moyen de racine des différences successives), SDNN (écart standard de l'intervalle NN), NN50 (nombre d'intervalles NN -gt;50 ms) et PNN50 (pourcentage d'intervalles NN). Les mesures de domaine de fréquence estiment la distribution de la puissance absolue ou relative en peut-être quatre bandes de fréquence, nous avons spécifiquement abordé sur deux bandes, la puissance de basse fréquence (LF) et la puissance de haute fréquence (HF) avec le rapport LF/HF. Bien que les RH soient une mesure clinique bien acceptée, le VRC peut être utile parce qu'il fournit des informations sur la fonction du système autonome, la récupération, l'adaptation, et fournit une estimation de la charge de travail aérobie au cours d'une session AVG28.
Le but de cette étude était d'examiner la faisabilité d'utiliser des stratégies AVG pour promouvoir l'activité physique et la condition physique. Un deuxième objectif était de présenter le protocole de collecte de données AVG et la méthodologie pour calculer le VRC à partir des données ECG obtenues par l'intermédiaire d'un moniteur RH. Ces mesures et ce protocole peuvent s'avérer pertinents pour les cliniciens pour surveiller et doser les séances d'intervention pt.
Protocole
L'approbation de la Commission d'examen institutionnel a été obtenue. Tous les jeunes ont donné leur assentiment écrit et les parents ont donné leur consentement avant la participation.
1. Sessions de collecte de données AVG
- La session de jeu AVG
- Dans le présent étude, demandez aux jeunes atteints de CP de participer à une séance AVG qui comprend trois jeux de 20 min. Voir tableau 5 pour la démographie des jeunes. On s'attendait à ce qu'un total de 30 matchs soient joués; cependant, 29 jeux ont été complétés parce qu'un sujet n'a joué que 2 jeux dans sa session AVG.
- Demandez aux sujets de porter un moniteur RH tout au long de la session pour enregistrer les réponses RH et ECG.
- Dans la session AVG, demandez aux jeunes de jouer chaque AVG assis sur un banc avec les pieds à plat sur le sol et les genoux et les hanches fléchies à 90 degrés (90/90 assis) pour un soutien postural et la stabilité.
- Utilisez les trois conditions de jeu suivantes pour les objets de collection : 1) icônes manuelles seulement ; 2) icônes de pieds seulement ; et 3) les icônes de la main et des pieds. Utilisez un ordre contrebalancé entre les sujets. Choisissez ces trois conditions pour déterminer qui est le plus efficace dans la promotion de l'activité physique et de la condition physique et pas trop exigeant pour causer une fatigue précoce et indue.
REMARQUE : Chaque jeu a été conçu en utilisant les phases de prescription d'exercice : échauffement, conditionnement et refroidissement. [S'il vous plaît voir le tableau 1]. En outre, il y avait une phase de repos avant que le jeu a commencé à documenter les RH de base et une phase de récupération après le jeu de jeu pour documenter le temps de retour à la ligne de base HR. - Permettre aux sujets une période de repos entre les jeux pour hr de revenir au niveau de base.
- Calcul du VRC à partir des données ECG
- Organiser les données en intervalles de temps de 5 min afin d'assurer des données comparables pour chaque phase. Par conséquent, il y avait 6 phases définies pour ces calculs : 1) Repos; 2) Échauffement; 3) Conditionnement 1 (premier 5 min); 4) Conditionnement 2 (deuxième 5 min); 5) Refroidir (5 min) et 6) Récupération. La division de la phase de conditionnement en deux phases de 5 min permet d'examiner les performances aérobies du sujet à intervalles plus courts pour tenir compte de la fatigue due au déconditionnement 12 (tableau 4).
- Pour calculer correctement les mesures de VRC pour chaque segment de la session d'un sujet, effectuez la détection R-peak sur le signal ECG brut12,13. Utilisez le signal brut pour éviter les manipulations qui pourraient fausser les données.
- Pour traiter les données, obtenir les heures de début de chaque session d'enregistrement et convertir à partir de variables 'datetime' (MM/DD/YYYYY HH:MM:SS. SS) à quelques secondes. Aucune des séances ne s'est déroulée sur deux jours, ce qui a permis d'ignorer la partie MM/DD/YYYY pendant ces calculs. Acquérir l'heure de début du jeu d'intérêt à partir de la table de chronométrage pour localiser chaque session de jeu dans le fichier électrocardiogramme (ECG) ; ce temps a été converti en secondes après qu'il ait été extrait du fichier de synchronisation. Le fichier de chronométrage contenait des heures de début pour chaque phase du jeu ainsi que la fin de la période de récupération (tableau 2).
- Calculez la période de repos comme les 5 minutes avant le début du jeu et la phase de récupération comme la période de 5 minutes après la fin de la phase de refroidissement. Une fois ces temps obtenus, obtenez l'emplacement (S) de la phase de jeu d'intérêt dans le fichier ECG par l'équation suivante :
 (1)
(1)
où la phase est mise au repos, à l'échauffement, au conditionnement 1, au conditionnement 2, au refroidissement ou à la récupération; le temps a été divisé par 1/Fréquence pour tenir compte du taux d'échantillonnage ECG. Le moniteur RH avait un taux d'échantillonnage de 250 Hz et contenait donc une mesure tous les 4 ms.- Modifier ce numéro en modifiant le taux d'échantillonnage avec la première invite du programme Peak-Detection.m pour tenir compte de l'utilisation d'autres dispositifs d'enregistrement. Choisissez le segment de 5 min avec lequel travailler pendant l'exécution du programme de détection de pointe. Cela a été fait via une invite à l'utilisateur. Fixez l'heure de fin à 5 minutes après l'heure de début et prenez en considération la fréquence de l'appareil d'enregistrement.
- Une fois la section de 5 min choisie, calculez un seuil de détection de pointe en fonction de l'écart moyen et standard de la forme d'onde.
- Définir le seuil
 comme mais cela peut être augmenté dans le programme si les données sont uniformes pour réduire la détection faussement positive des pics T qui sont plus élevés que leurs pics R correspondants. Des exemples de ces faux positifs peuvent être vus à la figure 1.
comme mais cela peut être augmenté dans le programme si les données sont uniformes pour réduire la détection faussement positive des pics T qui sont plus élevés que leurs pics R correspondants. Des exemples de ces faux positifs peuvent être vus à la figure 1. - Avec une hauteur minimale pour le pic R, assigner une distance minimale entre les pics pour minimiser la détection des pics incorrects autour de la R. Set cette valeur à 75 qui correspondait à 0,3 s entre les pics ou 200 battements par min (bpm) (cette valeur change avec fréquence). La valeur de 200 bpm est plus élevée que n'importe quel HR atteint par les sujets dans cette étude et peut être changée en fonction de la population étudiée.
- Définir le seuil
- Une fois le seuil calculé, laissez le programme passer à travers la forme d'onde et essayez de discerner tous les R pour les calculs d'intervalle RR et de VRC. Générer une parcelle préliminaire afin que l'utilisateur puisse l'examiner pour décevoir des irrégularités telles que celles indiquées dans la figure 1 ou la figure 2.
- Corriger manuellement ces irrégularités en modifiant la variable de détection qui contient la lecture microvolt (V) du pic dans la colonne 1 et l'emplacement dans la session de jeu en cours (s/0.004) dans la deuxième colonne. Dans la plupart des cas, les pics R appropriés peuvent facilement être trouvés en zoomant sur l'emplacement du problème comme on le voit dans la figure 1. De nombreuses séances de données sont assez uniformes comme le montre la figure 3 et ne nécessiteront donc que quelques corrections. Certains cas, cependant, sont assez désordonnés et nécessitent plus de temps pour examiner et obtenir les emplacements R appropriés.
- Si les fluctuations de la forme d'onde rendent excessivement difficile de localiser correctement un pic, ignorez les petits segments 1-2 s et attribuez aux battements ectopiques qui ne sont pas utilisés dans les calculs DE VRC12.
- Une fois que les R ont été localisés, exécutez le programme DE rh. Calculer les intervalles RR d'abord car ils sont la base des mesures DE VRC utilisées dans cette étude12.
- Obtenir une matrice d'intervalles et ignorer tout intervalle supérieur à 1,5 s (40 bpm) car il était dû aux battements ectopiques susmentionnés étant retirés des calculs. Enregistrez ces intervalles RR pour d'autres calculs et vérification des données. Utilisez ces intervalles pour calculer le carré moyen racine des différences successives (RMSSD) avec l'équation suivante :
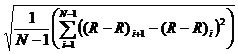 RMSSD (2)
RMSSD (2)
Où N - Nombre d'intervalles RR (R-R)i - Intervalle entre les pics QRS voisins (R-R)i-1 - Intervalle entre l'ensemble suivant de pics
- Obtenir une matrice d'intervalles et ignorer tout intervalle supérieur à 1,5 s (40 bpm) car il était dû aux battements ectopiques susmentionnés étant retirés des calculs. Enregistrez ces intervalles RR pour d'autres calculs et vérification des données. Utilisez ces intervalles pour calculer le carré moyen racine des différences successives (RMSSD) avec l'équation suivante :
- Choisissez cette variable car il a été démontré qu'il est efficace sur les intervalles allant de 1 min à 24 h de longueur13,14,15,16,17 et peut donc être utilisé pour évaluer ces 5 min intervalles dans les phases de jeu. Avec RMSSD, obtenir la déviation standard des intervalles NN pour mesurer les changements dans les RH tout au long de la phase14,16,18.
- Utilisez les intervalles RR pour calculer NN50, le nombre d'intervalles qui diffèrent de l'intervalle précédent par plus de 50 ms12 qui a également été utilisé sur les intervalles allant d'une min à 24 h16,17,19, 20,21.
- Calculer la variable NN50 au moyen d'une fonction de comptage simple qui vérifiait si la différence entre les longueurs d'intervalle RR consécutives était supérieure à 50 ms. Une fois que NN50 a été obtenu de cette manière, diviser par le nombre total d'intervalles pour calculer pNN50 qui est le pourcentage d'intervalles qui diffèrent de plus de 50 ms. Ce calcul a permis de comparer les données mesurées entre les sujets, les jeux et même les sessions de durées variables, car il s'agit d'une variable sans unité13,14, 16 Annonces , 17.
- Calculer la durée moyenne de l'intervalle RR pour chaque phase et sujet comme une mesure distincte DU VRC16,17,19,22,23,24. Utilisez cette mesure pour calculer les RESSOURCES humaines moyennes en divisant l'intervalle MOYEN de RR par 60 s. Ces deux mesures sont facilement comparables à travers les sessions de jeu pour observer la tendance de l'activité du sujet16,17,19,22,23, 24.
- Une fois ces mesures calculées, calculez la densité spectrale à basse fréquence et à haute fréquence (PSD) pour l'ECG brut de l'intervalle de 5 minutes et la matrice d'intervalle RR en obtenant le PSD de Fast-Fourier transforme13,14 , 17 Annonces , 19 ans, états-unis qui , 25. Toutes ces données ont ensuite été stockées dans un tableau, dont un exemple est affiché dans le tableau 4.
2. Acquérir les données ECG du patient
- Préparer la sangle thoracique de moniteur HR et le module Bluetooth pour l'application au sujet.
- Assurez-vous que le module Bluetooth a été entièrement chargé (3 h) à l'aide du berceau de charge.
- Branchez le module dans l'ordinateur de données via le berceau de charge et ouvrez l'outil config. Entrez un nom à des fins d'enregistrement.
- Sélectionnez l'appareil RH, cliquez sur l'onglet Temps et sélectionnez Date/heure de jeu pour synchroniser le module à l'heure et à la date correctes. L'appareil peut maintenant être retiré du berceau de charge.
- Humidifiez les zones conductrices (beige) sur la sangle thoracique de surveillance DES RH en plaçant une main dans l'eau et en frottant les zones conductrices.
- Placez le module Bluetooth de moniteur HR dans la sangle thoracique avec les surfaces conductrices du module alignées avec celles de la sangle de coffre : il cliquera en place.
- Appuyez et maintenez le bouton sur le module jusqu'à ce que les lumières clignotent. Le module est maintenant allumé et l'enregistrement.
- Appliquez la sangle thoracique du moniteur HR (avec module Bluetooth) au joueur avec le module aligné avec la ligne mi-axillaire gauche et la sangle juste sous les muscles pectoraux. Une fois correctement positionné, resserrez l'appareil de sorte qu'il ne se déplace pas pendant la session, mais n'est pas inconfortable pour le joueur.
- Acquérez un signal et affichez le flux en direct.
- Branchez le connecteur dans le port USB de l'ordinateur qui sera utilisé pour afficher les données.
- Ouvrez le programme Live View et entrez le mode de configuration en cliquant sur l'icône avec la clé et le tournevis.
- Choisissez un joueur de la liste s'il y a lieu ou ajoutez un nouveau sujet avec le nouveau bouton dans le coin inférieur gauche de l'écran.
- Entrez les informations du sujet comme vous le souhaitez à des fins d'identification (nom, âge, sexe, taille, poids).
- Cliquez sur l'onglet Matériel et sélectionnez le sujet actuel.
- Cliquez sur Attribuer en bas de l'onglet et sélectionnez l'appareil actuel (listé comme 01 si aucun autre appareil n'est présent). Cliquez ensuite sur attribuer dans la boîte contextuel.
- Cliquez sur l'onglet Équipe. Mettez en surbrillance le sujet, puis cliquez sur le bouton flèche droite pour placer le joueur sur l'équipe A.
- Cliquez sur l'onglet Déploiement, puis déplacez l'équipe nouvellement créée vers le premier onglet.
- Ouvrez l'onglet Mode Live en cliquant sur le symbole Wi-Fi bleu dans le coin supérieur gauche.
- Utilisez l'onglet Mode Live pour surveiller les RH, la fréquence respiratoire et la posture du sujet en temps réel.
REMARQUE : La force du signal, la puissance de la batterie et la confiance des mesures peuvent également être visualisées. - Enregistrez le calendrier précis (MM/DD/YYYYY HH:MM:SS) du début et de la fin de chaque session et phase de traitement.
- Téléchargez les données ECG à partir du moniteur RH.
- Retirez la sangle du lecteur à la fin de la session et retirez le module Bluetooth de la sangle thoracique.
- Placez le module dans le berceau de charge et branchez-le dans un ordinateur avec le logiciel installé.
- Ouvrez le journal.
- Sélectionnez l'appareil dans le menu déroulant. Toutes les sessions actuellement sur l'appareil sont affichées avec les dates et les heures.
- Décochez la case qui indique utiliser l'emplacement d'enregistrement par défaut et choisissez un nouvel emplacement d'enregistrement.
- Cliquez sur Enregistrer. Une barre de progression apparaîtra alors. L'épargne peut prendre jusqu'à une heure en fonction de la durée de la session.
- Renommer la date, une fois qu'elle a été sauvegardée.
3. Analyse des données et calcul des mesures de variabilité de la fréquence cardiaque
- Préparer les fichiers pour le traitement .
- Nommez les fichiers ECG comme étant 'KOLLECT'Subject'AVG4' (p. ex., KOLLECT-01-AVG4.csv').
- Générer une table de synchronisation dans le format variable séparé par virgule (.csv) pour tirer des données de synchronisation pendant le traitement des données. Voir tableau 1 pour un exemple du format correct.
- Importer les données Date-heure du fichier .csv et cliquez à droite sur le nom de la variable nouvellement créée et changez-le en 'Timing.mat'.
- Détection préliminaire du pic R.
- Ouvrez et exécutez Pic - Détection . m.
- Entrez la fréquence de l'appareil d'enregistrement ECG lorsqu'il est invité par le programme.
- Entrez le numéro de joueur pour que les données soient analysées lorsqu'elles sont invitées.
REMARQUE: Certains joueurs n'ont pas terminé le jeu vidéo actif 4 (AVG4) et donc seuls les joueurs 1-10 sont utilisés pour cette étude. D'autres numéros fourniront un message d'erreur. - Entrez le numéro du jeu à analyser (1, 2 ou 3) lorsqu'il est invité.
- Entrez dans la phase à analyser (Repos, Warmup (WU), Conditionnement (Con), Repos ou Récupération).
- Entrez un décalage en quelques minutes si désiré, ou entrez 0 pour aucun décalage.
- Sélectionnez l'outil de grossissement et sélectionnez une zone de l'intrigue qui est sortie pour créer une fenêtre d'une largeur d'environ 2 000 (s/0,004) et d'une hauteur qui affichera la forme d'onde complète comme indiqué à la figure 3. Zoom avant ou arrière si la fenêtre n'est pas facilement inspectée visuellement.
- Inspectez visuellement le graphique pour évaluer si les pics détectés sont correctement étiquetés. Voir La figure 1, par exemple, des pics mal détectés et manqués causés par des données ECG irrégulières (Figure 2).
- Correction de pointe
- Corriger les pics mal détectés ou manquants en localisant la variable de détection et en cliquant doublement dans l'espace de travail.
- Utiliser l'outil data Curseur sur la parcelle de la forme d'onde ECG pour obtenir les coordonnées x et y du pic incorrect; X (temps de fréquence) est la première colonne dans Detection.mat et Y (Voltage) est la deuxième colonne (Figure 3).
- Cliquez à droite sur la boîte de texte qui apparaît et cliquez sur SélectionnezCurseur Update Function .
- Sélectionnez TooltipUpdate.m dans le dossier contenant les fichiers utilisés pour cette analyse. Cela permettra à l'outil d'afficher des valeurs plus exactes.
- Si le point est un faux positif, retirez-le du tableau en cliquant sur sa ligne dans la variable Detection.mat et en appuyant sur le contrôle et la touche Minus. Un exemple de détection faussement positive peut être vu dans la figure 3.
- Modifier les pics mal marqués qui sont adjacents à des pics non marqués, comme le montrent les deux pics T marqués R à la figure 1, en modifiant leurs valeurs pour correspondre à celle du pic non marqué.
- Obtenir la valeur du pic manqué peut être obtenu avec l'outil Data Cursor.
- Ajouter des lignes supplémentaires à La détection. tapis en utilisant le contrôle et la clé plus pour les pics manqués en raison de niveaux de basse tension.
- Entrez les valeurs dans l'ordre numérique afin d'éviter les valeurs négatives pendant le processus de calcul (c.-à-d., ajoutez le pic situé à 11000 entre les pics à 10908 et 11167) (figure 5).
- Assurez-vous que les valeurs sont saisies correctement avant de continuer toute la session, car les nombres sont parfois coupés lorsqu'ils sont entrés.
- Répétez l'étape 2.3 jusqu'à ce que tous les pics aient été vérifiés et/ou corrigés.
REMARQUE : Certains fichiers ont une variabilité limitée dans l'amplitude des formes d'ondes et sont plus rapides à vérifier, comme on le voit dans la figure 4, tandis que d'autres sont plus variables et peuvent nécessiter un zoom plus étroit pour localiser avec précision les pics lors de l'inspection visuelle.
- Obtenir des calculs de mesure DU VRC.
- Enregistrer l'intrigue originale générée à partir de Peak-Detection.m pour une référence ultérieure.
- Exécutez HRV-Measures.m pour générer la parcelle correctement étiquetée. Un échantillon de données corrigées est affiché à la figure 6.
- Modifier le titre de l'intrigue en utilisant Insert Titre sur la fenêtre de l'intrigue et de le changer pour le titre désiré.
- Vérifiez la fenêtre pour la sortie, le programme informera l'utilisateur de l'emplacement incorrectement entré des données s'il y en a.
- Enregistrer l'intervalle nommé variable.
- Ouvrez la variable intitulée HRV à partir de la fenêtre de l'espace de travail pour afficher Mean RR (ms), Moyenne HR (bpm), RMSSD (ms), SDNN (ms), NN50 (compte), pNN50 (%), basse fréquence (LF)/ haute fréquence (HF) (ECG), LF/HF RR, Low Frequency Power RR et High Frequency Power (RR)). Enregistrer les valeurs h de ces variables à un tableau tel que celui indiqué dans le tableau 4.
- Répétez les sections 3.2 - 3.4 pour tous les autres segments, sessions et sujets qui ont besoin d'analyse.
Résultats
Cette méthode fournit des données à utiliser pour analyser l'effet qu'une nouvelle méthode a sur la variabilité de la fréquence cardiaque (VRC) du sujet. Pour ce faire, il localise la partie R de la forme d'onde QRS des données ECG d'un sujet, comme le montre la figure 6, et en calculant diverses valeurs du VRC à partir de celui-ci. Si le contrôleur des RH entre en contact correctement avec le sujet, les données seront uniformes, ce qui réduira con...
Discussion
Dix jeunes atteints de CP ont participé à cette étude (moyenne et DD) [âge (années) 15,53 ans , 3,57; hauteur (cm) 154,8 à 12,6; poids (kg) 50,69 à 11,1; indice de masse corporelle (IMC) 50,46 , 29,2; mHR 9 bpm) 186,8 à 12,4] Veuillez consulter le tableau 5 pour les données démographiques des patients.
Il y a quelques considérations pour l'utilisation des moniteurs rh et les mesures connexes des RH et des HRV qui se rapportent aux modifications et au dépannage. Deu...
Déclarations de divulgation
Pour l'instant, les auteurs (CL et PAS) n'ont rien à divulguer. Dr. O'Neil est un co-fondateur d'enAbleGames, LLC et Kollect est l'un des jeux offerts par cette société basée sur le Web. enAbleGames est en phase de développement de jeux et n'est pas une société ouverte en ce moment (www.enAbleGames.com).
Remerciements
Les auteurs remercient les participants et leurs familles pour leur temps et leurs efforts consacrés à leur participation à l'étude. De plus, les auteurs reconnaissent le Dr Yichuan Liu et le Dr Hasan Ayaz pour leur aide dans le calcul du calendrier de la surveillance des RH et le Dr Paul Diefenbach pour le développement du logiciel KOLLECT Active Video Gaming. Le financement de ces travaux a été fourni par la Fondation Coulter Grants #00006143 (O'Neil; Diefenbach, PIs) et #00008819 (O'Neil; Diefenbach, P).
matériels
| Name | Company | Catalog Number | Comments |
| BioHarness Bluetooth Module (Electronics sensor) | Zephyr | 9800.0189 | Detects Heart Rate, Resiration Rate, Posture, and Skin Temperature. |
| BioHarness Chest Strap | Zephyr | 9600.0189, 9600.0190 | Sizes Small XS-M, Large M-XL |
| BioHarness Charge Cradle & USB Cable | Zephyr | 9600.0257 | Used to Transfer Data from the Module to a Computer for Analysis. |
| BioHarness Echo Gateway | Zephyr | 9600.0254 | Allows for Realtime Viewing of Subject's Heart Rate. |
| MATLAB R2016a | Mathworks | 1.7.0_.60 | Used for All Programming. |
Références
- Winter, S., Autry, A., Boyle, C., Yeargin-Allsopp, M. Trends in the prevalence of cerebral palsy in a population-based study. Pediatrics. 110 (6), 1220-1225 (2002).
- Fowler, E., et al. Promotion of physical fitness and prevention of secondary conditions for children with cerebral palsy: Section on Pediatrics Research Summit Proceedings. Physical Therapy. 87 (11), 1495-1510 (2007).
- Rosenbaum, P., Paneth, N., Leviton, A., Goldstein, M., Bax, M. A report: The definition and classification of cerebral palsy: April 2006. Developmental Medicine & Child Neurology. 49 (s109), 8-14 (2007).
- Hanna, S., et al. Stability and decline in gross motor function among children and youth with cerebral palsy aged 2 to 21 years. Developmental Medicine & Child Neurology. 51 (4), 295-302 (2009).
- Rimmer, J., Rowland, J. Health promotion for people with disabilities: Implications for empowering the person and promoting disability-friendly environments. American Journal of Lifestyle Medicine. 2 (5), 409-420 (2008).
- Feehan, K., et al. Factors influencing physical activity in children and youth with special health care needs: A pilot study. International Journal of Pediatrics. , (2012).
- Fehlings, D., Switzer, L., Findlay, B., Knights, S. Interactive computer play as motor therapy for individuals with cerebral palsy. Seminars in Pediatric Neurology. 20 (2), 127-138 (2013).
- Sandlund, M., Dock, K., Hager, C., Waterworth, E. Motion interactive video games in home training for children with cerebral palsy: parents’ perceptions. Disability & Rehabilitation. 34 (11), 925-933 (2012).
- Howcroft, J., et al. Active video game play in children with cerebral palsy: Potential for physical activity promotion and rehabilitation therapies. Archives of Physical Medicine and Rehabilitation. 93 (8), 1448-1456 (2012).
- Bilde, P., Kliim-Due, M., Rasmussen, B., Petersen, L., Petersen, T., Nielsen, J. Individualized, home-based interactive training of cerebral palsy children delivered through the Internet. BMC Neurology. 11, 32 (2011).
- Kolobe, T., et al. Research Summitt III proceedings on dosing in children with an injured brain or cerebral palsy. Physical Therapy. 94 (7), 907-920 (2014).
- Schipke, J., Pelzer, M., Arnold, G. Effect of respiration rate on short-term heart rate variability. Journal of Clinical and Basic Cardiology. 2 (1), 92-95 (1999).
- Ernst, G. Heart rate variability. Heart Rate Variability. , 1-336 (2014).
- Francis, J., et al. Association between symptoms of depression and anxiety with heart rate variability in patients with implantable cardioverter defibrillators. Psychosomatic Medicine. 71 (8), 821-827 (2009).
- Mendes, R., et al. Is applying the same exercise-based inpatient program to normal and reduced left ventricular function patients the best strategy after coronary surgery? A focus on autonomic cardiac response. Disability and Rehabilitation: An International Multidisciplinary Journal. 36 (2), 155-162 (2014).
- Muralikrishnan, K., Balakrishnan, B., Balasubramanian, K., Visnegarawla, F. Measurement of the effect of Isha Yoga on cardiac autonomic nervous system using short-term heart rate variability. Journal of Ayurveda and Integrative Medicine. 33 (2), 279-283 (2012).
- Yadav, R. K., Gupta, R., Deepak, K. K. A pilot study on short term heart rate variability & its correlation with disease activity in Indian patients with rheumatoid arthritis. Indian Journal of Medical Research. 136 (4), 593-598 (2012).
- Thuraisingham, R. A. Preprocessing RR interval time series for heart rate variability analysis and estimates of standard deviation of RR intervals. Computer Methods and Programs in Biomedicine. 83 (1), 78-82 (2006).
- Alamili, M., Rosenberg, J., Gögenur, I. Day-night variation in heart rate variability changes induced by endotoxaemia in healthy volunteers. Acta Anaesthesiologica Scandinavica. 59 (4), 457-464 (2015).
- Pal, G., et al. Preference for salt contributes to sympathovagal imbalance in the genesis of prehypertension. European Journal of Clinical Nutrition. 67 (6), 586-591 (2013).
- Telles, S., Raghavendra, B. R., Naveen, K. V., Manjunath, N. K., Kumar, S., Subramanya, P. Changes in autonomic variables following two meditative states described in yoga texts. Journal of Alternative and Complementary Medicine. 19 (1), 35-42 (2013).
- Kičmerová, D. . Methods for Detection and Classification in ECG Analysis. Doctoral thesis. , (2009).
- Murai, K., Hayashi, Y. Evaluation of mental workload for ship handling using physiological indices. , 604-608 (2009).
- Taelman, J., Vandeput, S., Spaepen, A., Van Huffel, S. Influence of mental stress on heart rate and heart rate variability. Heart. 29 (1), 1366-1369 (2009).
- Durantin, G., Gagnon, J. F., Tremblay, S., Dehais, F. Using near infrared spectroscopy and heart rate variability to detect mental overload. Behavioural Brain Research. 259, 16-23 (2014).
- Buchheit, M. Monitoring training status with HR measures: Do all roads lead to Rome?. Frontiers in Physiology. 5, (2014).
- Achten, J., Jeukendrup, A. Heart rate monitoring: Applications and limitations. Sports Medicine. 33 (8), 517-538 (2012).
- Amichai, T., Katz-Leurer, M. Heart rate variability with cerebral palsy: Review of literature and meta-analysis. NeuroRehabilitation. 35, 113-122 (2014).
- Billman, G., Haikuri, H., Sacha, J., Trimmel, K. An introduction to heart rate variability: Methodological considerations and clinical applications. Frontiers in Physiology. 6, (2015).
- Beffara, B., Bret, A., Vermeulen, N., Mermillod, M. Resting high frequency heart rate variability selectively predicts cooperative behavior. Physiology & Behavior. 164, 417-428 (2016).
- Fogt, D., Cooper, P., Freeman, C., Kalns, J., Cooke, W. Heart rate variability to assess combat readiness. Military Medicine. 174, 491-495 (2009).
- Kerppers, I. L., Arisawa, E. A. L., Oliveira, L. V. F., Sarmpaio, L. M. M., Oliverira, C. S. Heart rate variability in individual with cerebral palsy. Archives of Medical Science. 5, 45-50 (2009).
- Giggins, O. M., Persson, U. M., Caulfield, B. Biofeedback in Rehabilitation. Journal of Neuroengineering and Rehabilitation. 10, (2013).
- Shaffer, F., Ginsberg, J. P. An overview of heart rate variability metrics and norms. Frontiers in Public Health. 5, 258 (2017).
- Shaffer, F., McCarty, R., Zeir, C. L. A healthy heart is not a metronome: an integrative review of the heart’s anatomy and heart rate variability. Frontiers in Psychology. 5, 1040 (2014).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon