Method Article
Modello di topo per il trapianto di Pancreas usando una tecnica modificata polsino
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Tra trapianto di organo solido addominale, gli innesti del pancreas sono inclini a sviluppare danno lesione-collegata dell'innesto di grave ischemia riperfusione, che conduce alla fine precoce perdita dell'innesto. Questo protocollo descrive un modello di trapianto di pancreas murino usando una tecnica di sutura non polsino, ideale per analizzare questi danni presto, deleteri.
Abstract
Modelli murini hanno diversi vantaggi nella ricerca di trapianto, tra cui maneggevolezza, una varietà di ceppi geneticamente ben definiti e la disponibilità della più vasta gamma di sonde molecolari e reagenti per eseguire in vivo come pure in vitro studi. Basandoci sulla nostra esperienza con i vari modelli di trapianto murino, abbiamo sviluppato un modello di trapianto di pancreas heterotopic in topi con l'intento di analizzare i meccanismi di danno grave ischemia riperfusione lesione-collegata iniziale dell'innesto. In contrasto con precedentemente tecniche descritte utilizzando tecniche di sutura, qui descriviamo una nuova procedura usando una tecnica di sutura non polsino.
Negli ultimi anni, abbiamo effettuato oltre 300 trapianti di pancreas in topi con un tasso di successo globale di > 90%, un tasso di successo mai descritta prima in trapianto di pancreas del mouse. La spina dorsale di questa tecnica di sutura non polsino per la rivascolarizzazione dell'innesto è costituito da due passaggi principali: (I) tirando la nave ricevente sovrapposto a un manicotto di polietilene/poliammide e fissandolo con una legatura della circonferenza e (II) posizionando il vaso donatore la estroflesso nave ricevente e fissandolo con una seconda legatura della circonferenza. La continuità risultante dei risultati strato endoteliale in meno lesioni trombogenico con tariffe alta pervietà e, infine, alti tassi di successo.
In questo modello, anastomosi arteriosa si ottiene tirando l'aorta addominale dell'innesto erogatore sopra l'arteria carotica comune anteverso dell'animale destinatario. Drenaggio venoso dell'innesto si ottiene tirando la vena dell'innesto sopra la vena giugulare esterna estroflesso del destinatario. Questo manoscritto fornisce dettagli e passi fondamentali del recupero di organi e procedure di impianto dell'organo, che permetteranno ai ricercatori con competenze microsurgical svolgere con successo il trapianto nei loro laboratori.
Introduzione
Trapianto simultaneo del rene-pancreas (SPK) rappresenta l'attuale standard di cura per i pazienti affetti da diabete mellito e fine malattia renale di stadio. Riuscito trapianto comporta l'indipendenza di insulina a lungo termine associato con stabilizzazione o addirittura regressione della microangiopatia diabetica e una migliore qualità di vita1. Tuttavia, a differenza di altri comuni trapianti di organi solidi, come rene e trapianto del fegato, del pancreas innesti sono più suscettibili della lesione di ischemia riperfusione (IRI). Incidenze segnalate fino al 35% in pericolo non solo dell'innesto, ma anche paziente, sopravvivenza2,3.
Stress ossidativo, disordini microcircolatori, aumentata espressione di citochine pro-infiammatorie e molecole di adesione risultante infine attivazione endoteliale e la perdita della sua integrità, sono tutti stati attribuiti a questa lesione non-trapianto allogeneic dell'innesto 4. finora, i meccanismi molecolari esatti dell'IRI sono in gran parte sconosciuti e possono variare da organo a organo.
Nonostante importanti progressi utilizzando modelli in vitro , lo sviluppo di modelli animali è fondamentale per approfondire la conoscenza dei meccanismi molecolari coinvolti nelle alterazioni di IRI-collegata dell'innesto dopo trapianto di pancreas. Sono stati sviluppati diversi modelli di trapianto di pancreas in roditori5,6, ma solo uno è riportato in topi7. Il tallone d'Achille di questo altamente esigente procedura microsurgical è il basso tasso di sopravvivenza del 46%. Tuttavia, modelli murini rappresentano il miglior modello per la ricerca correlata al trapianto, poiché la più ampia varietà di strumenti di analisi molecolare può essere applicata a loro. Basato sulla vasta esperienza microchirurgica in topi con differenti dell'organo trapianti8,9,10, abbiamo sviluppato una tecnica nuova, altamente riproducibile per pancreas heterotopic, cervicale trapianto in topi con > 90% tasso di successo utilizzando una tecnica di sutura non polsino. Con questa tecnica, complicanze correlate alla anastomosi sono ridotti al minimo, e un alto tasso di successo può essere raggiunto rispetto alla sutura modello11. Finora, solo un modello del topo con simili tassi di successo è stato descritto da Liu et al.12. Tuttavia, non ci sono studi pubblicati utilizzando questo modello finora.
Protocollo
Al fine di evitare risposte alloimmune e rigorosamente studiare danno ischemia riperfusione ferita-collegata dell'innesto, una coppia donatore-destinatario syngeneic deve essere utilizzata. In questo protocollo, maschio C57BL6 (H2b) 10-12-settimana-vecchi topi 26 a 28 g di peso sono stati usati come coppie donatore-destinatario di pari dimensioni. Tutti gli animali sono stati alloggiati in una struttura di libero agente patogeno di barriera e ha ricevuto la cura umana in conformità con le "entità di laboratorio Animal Care" formulato dalla società nazionale per la ricerca medica e la "Guida per la cura e uso di animali da laboratorio" preparato dalla National Academy of Sciences e pubblicato dalla National Institutes of Health (NIH pubblicazione n. 86-23, rivisto 1985). Ministero dell'istruzione, scienza e cultura ha approvato gli esperimenti descritti in questo manoscritto (BMWF-66.011/0056-II/3b/2011).
1. pancreas appalti
- Anestetizzare l'animale donatore con un'iniezione intraperitoneale (i.p.) di xilazina (5 mg/kg di peso corporeo) e ketamina (100 mg/kg di peso corporeo) utilizzando un ago di calibro 27 (G).
- Radersi i capelli nella regione addominale utilizzando un rasoio elettrico e fissare il mouse sul campo operatorio in posizione supina con fili di nastro.
- Strofinare il campo operatorio tre volte con garza imbevuta di clorexidina.
- Eseguire un'incisione addominale del midline con estensione sottocostale bilaterale con le forbici. Delicatamente esternare i visceri a sinistra con bastoncini di cotone sterile e avvolgerli in una garza inumidita. Sollevare il xyphoid cranialmente con un morsetto di zanzara per fornire la massima esposizione della cavità addominale per la procedura seguente.
- Utilizzando un ago 19 G, iniettare 400 µ l di una sterile soluzione di cloruro di sodio eparina 1:4 per heparinisation in vena cava inferiore (IVC). Dopo aver rimosso l'ago, eutanasia animale transecting dissanguamento dell'aorta.
- Sezionare l'aorta addominale tra l'origine dell'arteria mesenterica superiore e l'arteria renale di destra separando delicatamente il tessuto fibroso utilizzando pinze punta ricurva. Minare l'aorta e legarlo con una legatura di seta 8/0.
- Identificare il legamento epatoduodenale, che corre tra il duodeno postpyloric e hilum del fegato. Dividere il dotto biliare sotto l'entrata del condotto cistico dopo legatura distale e delicatamente sezionare e transetto vena portale distalmente possibile per avere una lunghezza sufficiente per eseguire l'anastomosi nel destinatario.
- Usando il forcipe punta ricurva, senza mezzi termini sezionare l'aorta addominale, a partire dalla legatura precedente (Vedi punto 1.6). Minare il tessuto periaortic usando il forcipe punta ricurva, legarlo con una legatura di seta 8/0 e transetto e con le forbici.
- Utilizzando le pinze bipolari, coagulare tutti i suoi rami lombare e transetto dell'aorta con forbici quanto più possibile al diaframma, al fine di fornire una lunghezza sufficiente per anastomosi di nave. Finalmente, transetto aorta già legato sopra l'arteria renale di sinistra.
- Irrorare il pancreas con una siringa di 19 G con 5 mL di soluzione di istidina-triptofano-chetoglutarato aspersione di 4 ° C in modo antegrade tramite l'aorta addominale, fino a quando c'è un chiaro effluente proveniente dalla vena portale. Applicare una pressione bassa per evitare la formazione di edema.
Nota: Eseguire passaggi 1,5 a 1,9 in modo rapido e standardizzato per evitare qualsiasi pregiudizio da deterioramento ischemico caldo dell'innesto recuperato. - Sostituire i visceri nella cavità peritoneale con bastoncini di cotone sterile.
- Usando il forcipe punta ricurva, separare il pancreas graduale a partire dal duodeno postpyloric e andare avanti fino a raggiungere il legamento di Treitz. Per questi passaggi, identificare le aree di tessuto connettivo avascolare tra il pancreas e la parete duodenale.
- Senza mezzi termini la dissezione queste aree utilizzando pinze punta ricurva al fine di isolare i vasi gettante un ponte fra il pancreas ed il duodeno. Passare una legatura seta 8/0 intorno ogni struttura vascolare isolata e legarlo.
- Infine, transetto la struttura vascolare con forbici verso la parete duodenale. Allo stesso modo, è possibile utilizzare una sutura seta 8/0 per separare il pancreas dal mesentery, colon trasverso e lo stomaco.
Nota: Durante questa procedura, il dotto choledocho-pancreatico è legato.
- Identificare il legamento gastrosplenico in esecuzione dalla milza allo stomaco e i brevi rami gastrici, sollevando lo stomaco cranialmente e tagliandola con le forbici. Lasciare la milza associata all'innesto recuperati.
Nota: Al fine di ridurre al minimo dell'innesto che riscalda, irrigare il pancreas continuamente usando una siringa da 10 mL con un ago 19 G con la soluzione di perfusione istidina-triptofano-chetoglutarato freddo conservata nel ghiaccio. - Infine, rimuovere il pancreas dal sito donatore (Figura 1B) afferrando la milza con il forcipe e trasferirlo nel ricevente.
- In alternativa, per attivare la riperfusione di ischemia severa, memorizzare l'innesto nella sterile, soluzione di perfusione di 4 ° C per 16 h prima l'impianto nell'animale destinatario.
2. destinatario preparazione
- Anestetizzare l'animale destinatario con un'iniezione i.p. di xilazina (5 mg/kg di peso corporeo) e ketamina (100 mg/kg di peso corporeo) utilizzando un ago da 27 G.
- La barba la regione cervicale laterale di destra utilizzando un rasoio elettrico e posizionare il mouse sul campo operatorio in posizione supina. Difficoltà il mouse utilizzando fili di nastro. Evitare pressioni eccessive gli arti anteriori per evitare di compromettere la respirazione.
- Strofinare il campo operatorio tre volte utilizzando garze imbevuta di clorexidina.
- Rendere un giusto paramedian, incisione della pelle leggermente obliqua dall'incisione giugulare fino all'angolo della mandibola di destra.
- Senza mezzi termini individuare e mobilitare i rami laterali della vena giugulare esterna destra. Coagulare li con pinze bipolari e li transetto con le forbici.
- Sollevare il lobo di destra della ghiandola salivare sottomandibolare cranialmente, identificare il pedicle vascolare e cauterizzare utilizzando pinze bipolari. Rimuovi il lobo transecting il pedicle cauterizzato con le forbici.
- In analogia al punto 2.5, identificare tutti i rami mediali della vena giugulare esterna, li cauterizzare con pinze bipolari e li transetto con le forbici.
3. l'impianto
- Posto l'innesto nella regione del collo del destinatario utilizzando la milza come una maniglia, con la testa orientata lateralmente, la coda compresa la milza medialmente ed i ceppi di nave ventro-caudale. Uso bastoncini di cotone per posizionare correttamente l'innesto.
- Tirare delicatamente la vena dell'innesto del pancreas nel corso della vena giugulare esterna dell'animale destinatario, che è stato precedentemente estroflesso, e fissa il bracciale appropriato (Vedi punto 2.10). Risolvere il problema con una legatura di seta 8/0 circolare.
- Accostare il ceppo dell'aorta addominale dell'innesto arteria carotica comune anteverso dell'animale destinatario. Risolvere il problema con una legatura di seta 8/0 della circonferenza (Figura 1).
- Identificare i vasi splenici vicino l'ILO della milza e minare la loro con una pinza a punta ricurva. Legarli con legature seta 8/0 e transetto i vasi splenici per rimuovere la milza. Infine, accorciare i legami.
- Utilizza un morsetto applicando il forcipe, rimuovere prima il morsetto sul polsino venoso. Quindi rimuovere il morsetto arterioso.
Nota: Se il trapianto è stato completato, l'innesto del pancreas sarà reperfused immediatamente mostrando un omogeneo colore rosato e la pulsazione arteriosa visibile (Figura 1). - Inumidire l'innesto con soluzione salina normotermica.
- Rimuovere la maniglia del bracciale venoso usando il forcipe dritto.
- Chiudere la ferita chirurgica con un funzionamento sutura 6/0.
4. postoperatoria (Endpoint)
- Seguendo la procedura, si applicano fino a 0,5 mL di soluzione salina normale per via sottocutanea (s.c.) per la sostituzione della perdita di liquidi intraoperative usando un ago 19g.
- Tenere l'animale destinatario su un rilievo di riscaldamento fino al completo recupero dall'anestesia.
- Una volta sveglio, restituire l'animale destinatario per la struttura alloggiativa, dove può avere cibo e acqua ad libitum.
- Per evitare il dolore postoperatorio, amministrare subito dopo l'operazione (1) Buprenorphin (0,1 mg/kg di peso corporeo) ogni 12 h per i primi 5 giorni e il carprofen (2) 4 mg/kg di peso corporeo ogni 12 h s.c. per la prima settimana.
- Al fine di stimare il corretto apporto nutrizionale, controllare il peso (g) di ogni animale destinatario ogni giorno. Una perdita di peso di più di 10-15% rispetto al peso al giorno di chirurgia, apatia, paralizzante, una schiena molto piegata, come pure le infezioni chirurgiche lato rappresentano gli endpoint.
- In questo caso, come pure dopo il raggiungimento dell'endpoint clinici, sacrificare l'animale mediante inalazione isoflurane terminale.
Risultati
Nell'ultimo decennio, abbiamo fatto più di 300 trapianti di pancreas nei topi. Dopo aver stabilito il protocollo, c'era una sopravvivenza globale di > 90%. Lo spurgo postoperatorio era la principale causa di guasto, seguita da trombosi dell'innesto con pancreatite successive letale innesto necrotico. In entrambi i casi, gli endpoint sono stati raggiunti entro 24 ore e gli animali sono stati sacrificati. Non c'erano qualsiasi disturbi neurologici, sintomi quali disfagia e infezioni chirurgiche lato in questa serie.
Per analizzare la funzione endocrina degli innesti trapiantati e quindi convalidare la pervietà del modello, l'iperglicemia è stata indotta in topi destinatari tramite pretrattamento con una dose singola di streptozotocin intraperitonealmente applicata (312,5 mg/kg di peso corporeo) 4 giorni prima dell'intervento chirurgico. Topi sono stati considerati hyperglycemic se i livelli della glicemia sono stati > 300 mg/dL. La Figura 2A Mostra il glucosio nel sangue di gruppi diversi. I topi che ricevono gli innesti senza un tempo di ischemia fredda prolungata di 16 h raggiunto normogylcemia all'interno di 24 h dopo trapianto e mantenuto questo stato metabolico sopra l'intero periodo di osservazione. Al contrario, gli animali non-trapiantati è rimasto hyperglycemic. Dato che eravamo interessati all'impatto del danno di ischemia riperfusione lesione-collegata dell'innesto sulla funzione endocrina, abbiamo aggiunto un terzo gruppo dove sono stati esposti gli innesti per 16 h prolungato tempo di ischemia fredda (CIT) e 45 min di tempo di ischemia calda (WIT). I topi che ricevono questi innesti non hanno raggiunto il normoglycemia e dovevano essere sacrificato dopo 48 h a causa dello sviluppo di pancreatite severa, che è stato indicato per essere letale in questo modello13.
Questo modello è utile per vari progetti volti a indagare l'ischemia riperfusione lesione-collegata agli inizi dell'innesto del danno. Le indagini successive inclusi, tra gli altri, microscopia di fluorescenza intravital confocal per la quantificazione delle dismutazioni microcircolatorie realizzate 2 h dopo trapianto. Contrasto di microvasi degli innesti è stata migliorata iniettando 0,3 mL di un 0,4% con etichetta isotiocianato di fluorescina destrano (MW 150 000) nella vena del pene. Figura 2B Visualizza un regolare reticolo capillare di un pancreas murino ingenuo e di un innesto del pancreas trapiantato, che non è stato esposto a prolungata CIT (Figura 2). Al contrario, Figura 2D Mostra la composizione della microcircolazione come conseguenza di esporre l'innesto del pancreas al prolungato CIT.
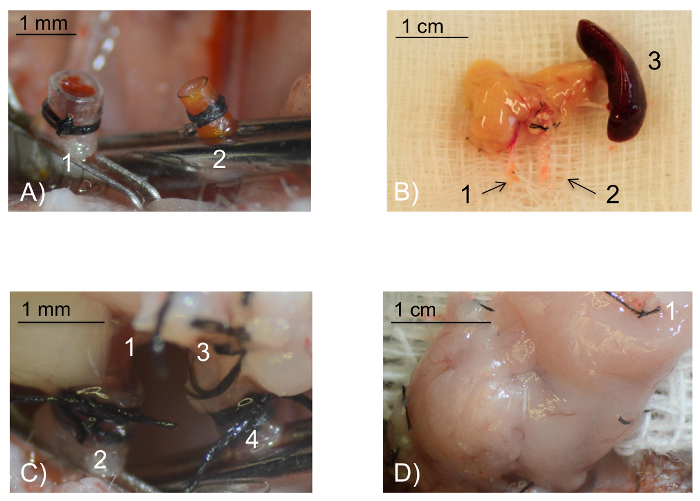
Figura 1 : Immagini intraoperative. (A) i vasi recettivi preparato per anastomosi vista Intraoperative. La vena giugulare esterna (1) è stata rovesciata sopra il polsino di venosa in polietilene e fissata con una legatura di seta 8/0 circolare. In analogia, l'arteria carotica comune (2) è stato rovesciato e fissato sopra il polsino della poliammide arteriosa più piccolo. Scala bar 1 mm. (B) il pancreatica dell'innesto ex situ. La vena portale (1) e il ceppo dell'aorta addominale (2) necessaria per l'anastomosi vascolare. La milza (3) è estratto insieme al pancreas e viene utilizzata come un handle. La milza verrà rimosso prima di riperfusione dell'innesto. Scala bar 1 cm. (C) visualizzazione intraoperatoria delle anastomosi. La vena portale (1) viene tirata sopra il polsino della vena giugulare esterna estroflesso (2) e fissata con una cravatta di seta 8/0 circolare. Allo stesso modo, il moncone aortico dell'aorta addominale (3) è tirato sopra il polsino dell'arteria carotica comune estroflesso (4). Scala bar 1 mm. (D) vista Intraoperative dell'innesto del pancreas perfuso dopo 5 min di riperfusione: dopo la rimozione della vena, quindi la pinza arteriosa, un innesto del pancreas trapiantato con successo viene visualizzato un colore rosato omogeneo. La milza è stata rimossa prima di riperfusione (1: vaso splenico legato). Scala bar 1 cm. per favore clicca qui per visualizzare una versione più grande di questa figura.
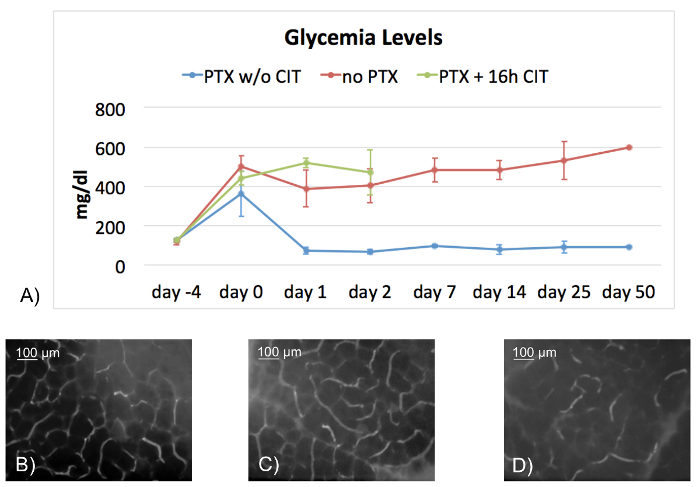
Figura 2 : Funzione endocrina del trapianto pancreatico e confocale in vivo microscopia di fluorescenza. La Figura 2A Mostra un grafico a linee con livelli di glucosio nel sangue dei topi trapiantati senza CIT (n = 10, PTX w/o CIT, linea blu), non trapiantato topi (n = 11, nessun PTX, linea rossa) e i topi che ricevono innesti esposti a prolungata CIT (PTX + 16 h CIT, n = 10, linea verde). Tutti i destinatari sono stati precedentemente resi hyperglycemic con 312,5 mg/kg b.w. streptozotocin i.p. Mentre tutti i destinatari degli innesti senza CIT erano in grado di sopravvivere l'intero periodo di osservazione (50 giorni) con la funzione endocrina intatta, topi trapiantati non è rimasto hyperglycemic durante l'intero periodo di osservazione. I topi che ricevono gli innesti esposti alle 16h CIT non hanno recuperato dalla iperglicemia e dovevano essere sacrificato 48 h dopo l'intervento chirurgico di trapianto, a causa di perdita di peso di più di 10-15%. L'intero periodo di osservazione di sopravvivenza di topi sono stati sacrificati a giorno 50 seguendo una ultima misurazione glicemia. Microcircolazione negli innesti trapiantati è stata valutata da microscopia di fluorescenza intravital confocal 2 h dopo trapianto. Ingenuo pancreas hanno servito da comandi. Figura 2B Mostra un normale modello capillare nel pancreas ingenuo. Una mesh capillare normale è visto anche negli innesti trapiantati non sottoposti a prolungata CIT (Figura 2). Al contrario, una ripartizione del microcircolo è osservata negli innesti trapiantati esposti a prolungata CIT (Figura 2D). Scala bar 100 µm. dati nel grafico vengono espressi come ± deviazione Standard. PTX: trapianto di pancreas; CIT: tempo di ischemia fredda; w/o: senza Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Danni di innesto IRI-collegato sono inerenti al trapianto d'organo solido, ed è caratterizzata da un disturbo del microcircolo. Accumulazione dei metaboliti diversi durante la fase ischemica e iniziazione di cascate infiammatorie mediate principalmente da specie reattive dell'ossigeno e dell'azoto, risultati nel danno tissutale durante riperfusione di innesto4. Questa cascata può compromettere il successo non solo a breve termine, ma anche a lungo termine e, quindi, influenza significativamente la sopravvivenza di pazienti14. Ad oggi, combinati rene pancreas rappresenta la terapia di scelta per i pazienti affetti dal tipo 1 diabete con fine fase malattia renale15. Diversi studi hanno dimostrato che un trapianto di pancreas rene combinato successo non solo ripristinare e proteggere la funzione dell'innesto del rene in diabetici destinatari, ma inoltre stabilizza o inverte anche complicazioni secondarie, compreso la neuropatia come pure Micro - e macroangiopathy16,17,18.
Nonostante il continuo impegno nella riduzione, di sostituzione e raffinatezza (3 R) nella ricerca animale, riproduzione di processi patofisiologici complessi come IRI è semplicemente impossibile in impostazioni in vitro . Pertanto, modelli animali sono ancora considerati di essere lo strumento ideale per la ricerca traslazionale19,20. Modelli di mouse come quello descritto qui hanno diversi vantaggi rispetto al topo o altro animale modelli. Questi includono la disponibilità di una vasta quantità di diversi ceppi di topi inbred geneticamente ben definita (ad es. ceppi transgenici e knock-out), una pletora di strumenti di analisi molecolare, così come un facile e a buon mercato movimentazione21. Un grande vantaggio il modello descritto si trova nella tecnica di sutura non polsino. Utilizzando la tecnica qui presentata, le percentuali di successo di > 90% sono realizzabili, che è drammaticamente meglio rispetto al precedentemente modelli descritti22. Utilizzando questa tecnica di sutura non, abbiamo significativamente ridotto comuni complicazioni come shock ipovolemico, trombosi e stenosi dell' anastomosi12. Un ulteriore vantaggio di questo metodo è costituito dalla posizione extra addominale dell'innesto, che è associato con un rapido recupero postoperatorio del destinatario. Inoltre, la posizione cervicale lo rende perfettamente adatto per le analisi in vivo , quali formazione immagine diretta dell'innesto di exterioration senza alcuna tensione22.
Lo svantaggio principale di questo modello è l'occlusione del dotto pancreatico, che non assomiglia a realtà clinica. In questo modello, drenaggio esocrino è gestito da legatura del dotto choledocho-pancreatico. A lungo termine, causando una profonda fibrosi e atrofia della ghiandola senza che portano alla pancreatite22del trapianto. A causa di questo deterioramento del tessuto esocrino, che abbiamo già osservato come al giorno 30 dopo trapianto, crediamo che questo modello non è adatto per l'osservazione a lungo termine. Al contrario, la funzione endocrina unimpaired rende gylcemic controlli del destinatario un facile strumento per valutazione quotidiana della funzione dell'innesto13,23,24.
Queste caratteristiche lo rende un modello ideale per l'analisi degli infortuni di innesto precoce associati a lunghi periodi di conservazione o con tecniche e soluzioni di conservazione diversi. Per raggiungere il successo ottima con questo modello, devono essere considerati diversi passaggi cruciali. Il pancreas stesso è molto suscettibile alla manipolazione. Di conseguenza, manipolazione delicata utilizzando bastoncini di cotone durante il recupero dell'organo e durante l'impianto minimizza i traumi meccanici. Afferrare diretta della ghiandola con il forcipe dovrebbe essere evitato, poiché inevitabilmente provocherebbe danni severa dell'innesto. Per lo stesso motivo, la milza è recuperata insieme al pancreas e viene utilizzata come un handle. Questo è stabilito anche nella pratica clinica. Un altro trabocchetto coinvolge aspersione freddo, che è realizzato tramite aspersione tramite il moncone aortico usando la soluzione di perfusione di istidina-triptofano-chetoglutarato di 4 ° C. Con la presente, un eccessivo gonfiamento della ghiandola può essere evitato irrorando delicatamente l'innesto. La soluzione di perfusione rimanente deve essere utilizzata per inumidire l'innesto, al fine di mantenere bassa la temperatura durante il recupero dell'organo.
Per quanto riguarda la preparazione destinatario una dissezione accurata della vena giugulare esterna così come l'arteria carotica comune imposta la base per rivascolarizzazione successo. In particolare, completa l'esposizione della vena di rimuovere non solo tutti i tributari, ma anche il tessuto adiposo circostante, è necessario per evitare la compressione esterna e stenosi di tessuto grasso rimanente. La selezione dei diametri polsino appropriato è fondamentale. Sulla base dell'esperienza condivisa, per topi pesano fra 25 a 28 g, un diametro interno di 0,57 mm per il bracciale arterioso e tra 0,75 e 0,8 mm per il bracciale venoso, è appropriato. Preciso, pulito taglio dei bordi dei polsini è obbligatorio per evitare di strappare il ceppo di nave. Dilatazione dei vasi, soprattutto dell'arteria, si ottiene migliore utilizzando dilatatori nave con estremità sottili. Come regola generale, la nave dovrebbe essere in grado di ampliare a due volte il lume del bracciale. Durante il processo di "everting" la nave sopra e fissandolo sul bracciale, si consiglia di stabilizzare pinze vascolari ponendoli sotto un lembo di pelle, come questo facilita questo passaggio cruciale.
Come già accennato, il polsino-tecnica di sutura non rappresenta un metodo semplice per l'anastomosi vascolare e può essere eseguita entro 5 min. Tuttavia, corretto posizionamento dell'innesto nella regione del collo del destinatario è della massima importanza per la corretta rivascolarizzazione. Con la presente, il finale corretto posizionamento dell'innesto nella regione del collo deve essere anticipata al fine di consentire un'anastomosi sicura, dritta e privo di tensione di sia la vena e dell'arteria. Vasi che sono troppo lunghi devono essere evitate, poiché questo può condurre all'ostruzione di uscita a causa di annodamento. Per lo stesso motivo, il polsino-maniglia all'anastomosi venosa dovrebbe essere rimosso dopo riperfusione. In caso di emorragie localizzate dall'innesto del pancreas, hemostasis successo può essere realizzato comprimendo delicatamente il lato di spurgo per 5 min utilizzando bastoncini di cotone. Questo è il modo solo successo per gestire questo tipo di complicazione.Cauterizzazione, anche se altamente selettivo, ha provocato la perdita dell'innesto in quasi tutti i casi, a causa di pancreatite necrotica.
In sintesi, abbiamo sviluppato un metodo per il trapianto di pancreas nei topi utilizzando una tecnica di sutura non polsino, che è tecnicamente fattibile e microsurgically e ha tassi di successo eccellente. Dato la fibrosi progredient del pancreas dovuto l'occlusione del condotto, questo modello è adatta meglio per aree di ricerca, concentrandosi sui primi danni dell'innesto. Questo manoscritto è destinato a permettere ai ricercatori di stabilire in modo sicuro questo modello nei loro laboratori.
Divulgazioni
Gli autori dichiarano di non avere nessun concorrenti interessi finanziari.
Riconoscimenti
Questo lavoro è stato supportato da sovvenzioni n. 2008-1-596 e #UNI-0404/1956 della "Tiroler Wissenschaftsfonds (TWF)" (https://www.tirol.gv.at/en/) e da grant #2013-042018 di "Förderungsprogramm di MUI-Start" dell'università Innsbruck Medical.
Materiali
| Name | Company | Catalog Number | Comments |
| Adventitia Scissors | S&T | S-00102 | Straight |
| Dumont # 7 Forceps | FST | 11271- 30 | Curved Tip 0.17 x 0.1 mm |
| Yasargil Clip Mini Permanent 7mm | Aesculap | FE720K | |
| Micro vessel clip | S&T | B1 00396 V | |
| Vessel dilatator | S&T | D-5a.2, 00125 | |
| Clip applier | S & T | CAF-4 00072 | for venous cuff |
| Clip applier | Aesculap | FE572K | for the arterial cuff |
| Polyethylene tube | Portex Ltd | Inner diameter 0.75 mm for venous cuff | |
| Polymide tubing | Vention Medical | 141-0051 | Inner diameter 0.8 mm (Alternative for polyethylene tube from Portex Ltd) |
| Polymide tubing | Vention Medical | 141-0033 | Inner diameter 0.57 mm for arteriail cuff |
| Bipolar forceps | Micromed | 140-100-015 | |
| 8/0 silk ligatures | Catgut GmbH, Merkuramed | 17209008 | |
| Custodiol HTK solution | Dr. Franz Köhler Chemie | 59997 | |
| Ketamin Graeub | aniMedica GmbH | 32554 | |
| Xylasol Graeub | aniMedica GmbH | 50855 |
Riferimenti
- Gruessner, A. C. 2011 update on pancreas transplantation: comprehensive trend analysis of 25,000 cases followed up over the course of twenty-four years at the International Pancreas Transplant Registry (IPTR). Rev Diabet Stud. 8 (1), 6-16 (2011).
- Troppmann, C. Complications after pancreas transplantation. Curr Opin Organ Transplant. 15 (1), 112-118 (2010).
- Fernández-Cruz, L., et al. Native and graft pancreatitis following combined pancreas-renal transplantation. Br J Surg. 80 (11), 1429-1432 (1993).
- Eltzschig, H. K., Eckle, T. Ischemia and reperfusion-from mechanism to translation. Nat Med. 17 (11), 1391-1401 (2011).
- Konigsrainer, A., Habringer, C., Krausler, R., Margreiter, R. A technique of pancreas transplantation in the rat securing pancreatic juice for monitoring. Transpl. Int. 3 (3), 181-182 (1990).
- Lee, S., Tung, K., Koopmans, H., Chandler, J., Orloff, M. Pancreaticoduodenal transplantation in the rat. Transplantation. 13 (4), 421-425 (1972).
- Tori, M., Ito, T., Matsuda, H., Shirakura, R., Nozawa, M. Model of mouse pancreaticoduodenal transplantation. Microsurgery. 19 (2), 61-65 (1999).
- Oberhuber, R., et al. Murine cervical heart transplantation model using a modified cuff technique. J Vis Exp. (92), e50753 (2014).
- Brandacher, G., et al. Tetrahydrobiopterin compounds prolong allograft survival independently of their effect on nitric oxide synthase activity. Transplantation. 81 (4), 583-589 (2006).
- Zou, Y., Brandacher, G., Margreiter, R., Steurer, W. Cervical heterotopic arterialized liver transplantation in the mouse. J Surg Res. 93 (1), 97-100 (2000).
- Zhou, Y., Gu, X., Xiang, J., Qian, S., Chen, Z. A comparative study on suture versus cuff anastomosis in mouse cervical cardiac transplant. Exp Clin Transplant. 8 (3), 245-249 (2010).
- Liu, X. Y., Xue, L., Zheng, X., Yan, S., Zheng, S. S. Pancreas transplantation in the mouse. Hepatobiliary Pancreat Dis Int. 9 (3), 254-258 (2010).
- Maglione, M., et al. Donor pretreatment with tetrahydrobiopterin saves pancreatic isografts from ischemia reperfusion injury in a mouse model. Am J Transplant. 10 (10), 2231-2240 (2010).
- Drognitz, O., Obermaier, R., von Dobschuetz, E., Pisarski, P., Neeff, H. Pancreas transplantation and ischemia-reperfusion injury: current considerations. Pancreas. 38 (2), 226-227 (2009).
- White, S., Shaw, J., Sutherland, D. Pancreas transplantation. Lancet. 373 (9677), 1808-1817 (2009).
- Morath, C., et al. Simultaneous pancreas-kidney transplantation in type 1 diabetes. Clin Transplant. 23 (Suppl 21), 115-120 (2009).
- Perseghin, G., et al. Cross-sectional assessment of the effect of kidney and kidney-pancreas transplantation on resting left ventricular energy metabolism in type 1 diabetic-uremic patients: a phosphorous-31 magnetic resonance spectroscopy study. J Am Coll Cardiol. 46 (6), 1085-1092 (2005).
- Secchi, A., Caldara, R., La Rocca, E., Fiorina, P., Di Carlo, V. Cardiovascular disease and neoplasms after pancreas transplantation. Lancet. 352 (9121), 65 (1998).
- Kirk, A. D. Crossing the bridge: large animal models in translational transplantation research. Immunol Rev. 196, 176-196 (2003).
- de Jong, M., Maina, T. Of mice and humans: are they the same?--Implications in cancer translational research. J Nucl Med. 51 (4), 501-504 (2010).
- Niimi, M. The technique for heterotopic cardiac transplantation in mice: experience of 3000 operations by one surgeon. J Heart Lung Transplant. 20 (10), 1123-1128 (2001).
- Maglione, M., et al. A novel technique for heterotopic vascularized pancreas transplantation in mice to assess ischemia reperfusion injury and graft pancreatitis. Surgery. 141 (5), 682-689 (2007).
- Cardini, B., et al. Crucial role for neuronal nitric oxide synthase in early microcirculatory derangement and recipient survival following murine pancreas transplantation. PLoS One. 9 (11), e112570 (2014).
- Maglione, M., et al. Prevention of lethal murine pancreas ischemia reperfusion injury is specific for tetrahydrobiopterin. Transpl Int. 25 (10), 1084-1095 (2012).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon