Method Article
Automazione di un positrone-emissione di positroni (PET) radiotraccitore sintesi protocollo per la produzione di clinica
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Positrone-emissione di positroni (PET) imaging siti coinvolti in studi di ricerca clinica precoce più bisogno di capacità di produzione del radiotraccitore robusto e versatile. Utilizzando il radiotraccitore [18F] clofarabina come esempio, illustriamo come automatizzare la sintesi di un radiotraccitore utilizzando un radiosynthesizer flessibile, lettore di cassette e convalidare la sintesi per uso clinico.
Abstract
Lo sviluppo di nuovi rivelatori di positroni (PET) emissione di positroni è abilitazione i ricercatori e i clinici all'immagine una sempre più vasta gamma di bersagli biologici e processi. Tuttavia, il crescente numero di differenti traccianti crea sfide per la loro produzione radiofarmacie. Mentre storicamente è stato pratico di dedicare un radiosynthesizer personalizzato e cella calda per la produzione ripetuta di ogni singolo elemento tracciante, diventa necessario cambiare questo flusso di lavoro. Recenti radiosynthesizers commerciale basato su cassette/Kit monouso per ogni elemento tracciante semplificare la produzione di traccianti multipli con un set di attrezzatura, eliminando la necessità di modifiche personalizzate specifiche del tracciante. Inoltre, alcuni di questi radiosynthesizers consentono all'operatore di sviluppare e ottimizzare i propri protocolli di sintesi oltre all'acquisto di kit disponibili in commercio. In questo protocollo, descriviamo la procedura generale per come la sintesi manuale di un nuovo elemento tracciante PET può essere automatizzata su uno di questi radiosynthesizers e convalidati per la produzione di traccianti di uso clinico. Ad esempio, usiamo il radiosynthesizer ELIXYS, uno strumento flessibile basato su cassetta radiochimica che può sostenere gli sforzi di sviluppo di tracciante PET, nonché produzione di routine clinica sonda sullo stesso sistema, per produrre [18F] clofarabina ([ 18 F] CFA), un tracciante PET per misurare l'attività enzimatica in vivo deossicitidina chinasi (dCK). Tradurre una manuale sintesi coinvolge abbattendo il protocollo sintetico nei processi di radiochimica base che vengono poi tradotte in chimica intuitiva "operazioni unitarie" supportate dal software sintetizzatore. Queste operazioni quindi possono rapidamente essere convertite in un programma di sintesi automatizzata assemblandole utilizzando l'interfaccia drag-and-drop. Dopo il test di base, la procedura di sintesi e purificazione può richiedere ottimizzazione per ottenere la resa desiderata e la purezza. Una volta ottenuta la prestazione desiderata, una convalida della sintesi è effettuata per determinare l'idoneità per la produzione del radiotraccitore per uso clinico.
Introduzione
Una crescente gamma di bersagli biologici possa essere visualizzata in modo dinamico nella vita del soggetto tramite la modalità di imaging molecolare PET. PET fornisce saggi in vivo dei processi biologici, biochimici e farmacologici specifici utilizzando radiotraccianti specifici (molecole etichettati con radionuclidi emettitori di positroni) che vengono iniettate nella materia prima del1di imaging. L'uso aumentato di PET per studiare una vasta gamma di questi processi nella scienza di base e ricerca clinica2,3,4e nella scoperta, sviluppo e l'uso clinico di farmaci nella cura del paziente5, 6, sta portando ad una crescente domanda per diversi radiotraccianti7,8. Per evitare l'esposizione a radiazioni per la radiochemist e per garantire una produzione riproducibile di questi rivelatori di breve durate, essi sono in genere realizzati utilizzando un radiosynthesizer automatizzato operanti all'interno di una "cella calda". Radiosynthesizers recenti utilizzano un'architettura di USA e getta-cassetta/kit per semplificare il compito di adempiere con produzione ad uso clinico, fornendo inoltre la flessibilità necessaria per preparare i tipi multipli di radiotraccianti semplicemente sostituendo cassette9 . Tuttavia, nelle fasi cliniche iniziali, non ci sono solitamente nessun cassette/kit disponibile in commercio per eseguire il radiosynthesis automatizzato; di conseguenza, impianti di produzione di droga PET lottano per personalizzare sistemi per implementare la capacità di produzione di cGMP-grado tracciante entro un lasso di tempo adeguato e ad un costo ragionevole. Così, radiosynthesizers sono stati sviluppati che combinano l'architettura di cassette/kit con caratteristiche per facilitare lo sviluppo e l'ottimizzazione di rivelatori.
Il FLEX/CHEM ELIXYS (ELIXYS) è un esempio di un radiosynthesizer basato su cassetta flessibile con una vasta reazione reagente e solvente temperatura compatibilità10. Ha tre recipienti di reazione e utilizza un meccanismo robotico per configurare dinamicamente il percorso fluido come richiesto da qualsiasi particolare sintesi protocollo11. Il sintetizzatore software permette la creazione di programmi di sintesi (sequenze) diversi traccianti trascinando e rilasciando Operazioni unitarie come Trappola degli isotopi, Isotopo eluire, Aggiungere Reagente, reagire, ed evaporare12. Ogni operazione di unità ha una varietà di parametri programmabili disponibili all'operatore, quali durata, temperaturao gas inerte guida pressione (pressione). Di comprendere la natura di ogni operazione di unità, una sintesi manuale può essere facilmente tradotto in una sequenza di operazioni unitarie e quindi essere modificata durante l'ottimizzazione del protocollo13. In combinazione con il modulo di ELIXYS PURE/modulo, il sistema integrato inoltre possibile eseguire una purificazione automatizzata e formulazione dell'elemento tracciante PET. Utilizzando questo radiosynthesizer, precedentemente abbiamo segnalato la sintesi automatizzata di 24 diverse 18F-etichetta traccianti e gruppi prostetici11,14,15,16, come così come il radiofluorination enzimatica automatizzato di biomolecole17, semplicemente cambiando i reagenti e non la configurazione del sistema. Altri hanno mostrato la sintesi automatizzata di [18F] RO6958948 per l'imaging di tau neurofibrillary tangles18, la sintesi automatizzata del gruppo prostetico [18F] F-Py-TFP con una conseguente etichettatura dei peptidi19 e la sintesi automatizzata di [18F] AM580 per l'imaging della fosfodiesterasi 10a (PDE10A)20. Inoltre, diversi gruppi hanno dimostrato la produzione di traccianti appropriata per uso clinico, tra cui [18F] 4-fluorobenzil-trifenilfosfonio ([18F] FBnTP) per l'imaging della membrana mitocondriale potenziali21, [ 18 F] DCFPyL per l'imaging di membrana prostatico specifico antigene (PSMA)22e [18F] THK-5351 per l'imaging di tau23.
In questo articolo, usiamo la nostra esperienza con [18F] CFA per illustrare come una procedura manuale radiosynthetic può essere tradotto semplicemente e rapidamente in una sintesi automatizzata adatta a produzione di routine seguendo linee guida cGMP. Il tracciante [18F] CFA è stato progettato per l'imaging di dCK attività. Il manuale radiosynthesis di [18F] CFA è stato originariamente descritto da Shu et al. 24 come procedura utilizzando due recipienti di reazione, purificazione cartuccia intermedia silice e una purificazione HPLC finale (vedere Materiale supplementare, sezione 1 per i dettagli). Recenti in vitro e studi preclinici hanno dimostrato l'eccezionale specificità di questo tracciante per dCK, e primo-in-umani hanno dimostrato favorevole biodistribuzione25. C'è un interesse immediato negli studi clinici su più ampia scala per confermare la sensibilità di [18F] PET CFA a variazioni nell'attività dCK e un interesse a lungo termine per le potenziali applicazioni cliniche di questo tracciante26. Può essere un biomarcatore utile per le terapie che attivano attivazione delle cellule T, indurre il danno del DNA o si basano su profarmaci analogico del nucleoside dCK-dipendente. In particolare, [18F] CFA può abilitare la stratificazione dei pazienti per una potenziale risposta al trattamento con la clofarabina. [18F] CFA può anche facilitare lo studio e lo sviluppo di inibitori di dCK che stanno avanzando verso sperimentazioni cliniche. Poiché questo tracciante è tradizionalmente stato sintetizzato manualmente, avanzando tutti questi studi richiede una sintesi affidabile, automatizzata di [18F] CFA appropriata per uso clinico.
Anche se precedentemente abbiamo segnalato una sintesi automatizzata di [18F] CFA per studi preclinici16, questo protocollo si basa più avanti questi sforzi e descrive le modifiche aggiuntive necessarie per la produzione clinica di questo tracciante, compresa l'integrazione di purificazione completamente automatizzata e la formulazione, protocollo convalida e test di controllo qualità. Le procedure generali qui descritte non sono limitate a sviluppare una sintesi automatizzata e clinicamente adatto [18F] CFA, ma può essere generalizzata in modo semplice di sviluppare automatizzati sintesi appropriate per uso clinico di altri radiotraccianti etichettati con fluoro-18.
Protocollo
1. generale procedura per l'automazione e la validazione di un protocollo di Radiosynthesis per la produzione di clinica
-
Analizzare l'ammissibilità del regime di sintesi manuale per la produzione di clinica
- Eseguire analisi del rischio di contaminazione del prodotto con eventuali residui chimici indesiderati.
- Evitare di classe 1 solventi come benzene e sostituirli con appropriati solventi alternativi (classe 2 o classe 3).
- Evitare sostanze chimiche che sarebbero difficile da rilevare nella formulazione finale come impurità residue potenziali.
- Scegliere soli prodotti chimici che sono disponibili in commercio in grado di elevata purezza (il desiderato grado USP o pH. EUR.) e sono forniti con un certificato di analisi.
- Perfezionare lo schema di sintesi se indesiderati prodotti chimici o solventi vengono rilevati attraverso l'analisi di rischio e ripetere la sezione 1.1 fino a nessuno rimanere.
- Eseguire analisi del rischio di contaminazione del prodotto con eventuali residui chimici indesiderati.
-
Automatizzare il protocollo di sintesi
- Se un protocollo automatizzato per il tracer utilizzando il sintetizzatore stesso ha già stato creato e caricato in un archivio online, scaricare una copia del programma di sintesi.
- Se non esiste già un programma di sintesi automatizzata, crearne uno.
- Con carta e penna, suddividere la sintesi manuale in passaggi ad alto livello (ad es., asciugatura/attivazione [18F] fluoruro, riscaldamento per facilitare una reazione radiochimica, esecuzione di una fase di purificazione, ecc.). Suddividere ulteriormente i passaggi più importanti nei processi di basic discreti, che sono necessari. Ad esempio, lo schema di sintesi [18F] CFA è illustrato nella Figura 1, l'identificazione dei passaggi ad alto livello è mostrato in Figura 2Ae le ripartizioni fra processi sono mostrata nella Figura 2B.
- Utilizzando carta e penna, mappare ogni processo in funzionamenti dell'unità individuali fornite dal software sintetizzatore. Ad esempio, un'analisi della mappatura dei processi di base nella sintesi di [18F] CFA per operazioni unitarie adatto a sintetizzatore software13 è mostrato in Figura 2.
- Utilizzando l'interfaccia di programmazione radiosynthesizer, creare un programma vuoto e aggiungere ognuno dei funzionamenti dell'unità identificata nella sequenza facendo clic sul pulsante di Menu (in alto a sinistra) e selezionando sequenzee quindi scegliendo il nuovo Sequenza pulsante. Per ogni operazione di unità identificata nel passaggio 1.2.2.2, trascinare il funzionamento dell'unità dalle operazioni disponibili per la visualizzazione sequenza e clic o il tipo di compilare il valore desiderato di ogni parametro di funzionamento l'unità. La figura 3 Mostra un esempio dell'interfaccia quando tutte le operazioni di sintetizzare [18F] CFA sono stati popolati, e l'utente ha selezionato il funzionamento dell'unità reagire primo di modificare i valori di parametro. Il programma di sintesi finale per [18F] CFA è descritto nel Materiale supplementare, Tabelle S1 e S2.
- Verificare il programma di sintesi.
- Effettuare una prova. Impostare ed eseguire il programma come nei passaggi 2.1-2.3, utilizzando tutti i reagenti e solventi diversi dal radionuclide (ad es., [18F] fluoruro) per verificare il comportamento previsto.
- Se necessario, regolare i valori dei parametri di funzionamento di unità nel programma (ad esempio, il tempo o il differenziale di pressione per trasferire completamente un reagente, il tempo/temperatura per far evaporare il solvente al livello desiderato, ecc.) e ripetere il test. Per regolare i valori dei parametri, in primo luogo, di tornare alla modalità di modifica scegliendo sequenze dal menu principale (in alto a sinistra) e selezionare il programma appena creato. Successivamente, fare clic sull'operazione dell'unità desiderata nella visualizzazione sequenza (in basso dello schermo), selezionare il parametro desiderato e selezionare o digitare il nuovo valore.
- Eseguire un test bassa attività (< 370 MBq) per valutare il programma.
- Ottimizzare la sintesi automatizzata regolando i valori dei parametri per migliorare la resa, tempo di sintesi, ripetibilità e qualsiasi altro risultato misurabile desiderato.
-
Sviluppare il controllo di qualità (QC) procedure di collaudo
- Utilizzare un riferimento non radioattivo del prodotto finale ed esempi di potenziali impurità chimiche, sviluppare un radio-HPLC analitica e/o radio-sottile metodo di cromatografia (radio-TLC) di livello con una separazione sufficiente delle specie per la determinazione del purezza chimica, attività molare, la purezza radiochimica e identità radiochimica. Convalidare i metodi analitici per la ripetibilità e linearità e determinare i limiti di rilevazione e quantificazione.
- Allo stesso modo, sviluppare e validare un metodo di cromatografia in fase gassosa per analizzare impurità volatili (ad es., gli importi residui di solventi utilizzati durante la sintesi).
- Sviluppare e validare saggi analitici che consentono la rilevazione e la quantificazione delle altre impurità (ad es., criptando 222 tramite la prova di punto di colore standard).
- Utilizzare le procedure standard per la determinazione della sterilità, pH, radionuclidica identità, purezza radionuclidica, concentrazione di radioattività, volume del prodotto e livelli di endotossina.
-
Eseguire la convalida di sintesi
- Stabilire procedure operative standard (POS) per la sintesi e QC procedure di collaudo e integrare un materiali e sistema di tracciamento di attrezzature compatibile con buona corrente pratica (cGMP) esigenze produttive.
- Convalidare le procedure di sintesi viene eseguito tramite tre produzione indipendente e consecutivi agli stessi livelli di radioattività come previsto per la clinica produzione seguendo le procedure operative standard. Documentare le prestazioni di sintesi e risultati della prova di controllo.
- Tutte le esecuzioni di convalida consecutivi devono passare ai limiti preimpostati di QC. Se una convalida eseguita ha esito negativo, è possibile ripetere il processo di convalida intero dopo affrontare adeguatamente la causa principale dell'errore.
2. esempio: Automatizzato sintesi di CFA [18F] per uso clinico
- Preparare la radiosynthesizer
- Accendere il radiosynthesizer.
- Garantire la fornitura di gas inerte è attivata con una pressione sufficiente e che le valvole necessarie siano aperte, in modo che il radiosynthesizer è collegato alla rete del gas.
- Installare nuove cassette monouso in reattore #1 e #2 posizioni e inserire recipienti di reazione contenente barre magnetiche. Garantire che ogni tubo di immersione del trasferimento di cassette è puntato dritto verso il basso.
- Preparare i flaconi dei reagenti e installarli in cassette secondo lo schema di Figura 4.
- Installare un vuoto [18O] flaconcino recupero di H2O nella posizione W1 della cassetta n. 1.
- Attivare una cartuccia Metilammonio quaternario (QMA) di primo passaggio 12 mL di una soluzione di3 1m KHCO attraverso di essa, seguita da 12 mL di acqua deionizzata. Condizione di una cartuccia di silice settembre-Pak passando 5 mL di acetato di etile attraverso di essa.
- Collegare le cartucce e fare tutte le connessioni dei tubi cassette come mostrato in Figura 5A. Verificare che nessun tubo cassetta (tra cui tubi inutilizzati) si blocca all'interno, dove può interferire con i movimenti robotici.
- Collegare la linea di origine di fluoruro [18F] dal ciclotrone per la riga di input di fluoruro [18F] su cassetta n. 1.
- Assicurarsi che il contenitore è vuoto. Posizionare le linee dei rifiuti dal sottosistema di purificazione/formulazione nel contenitore dei rifiuti (cioè, linea rifiuti sample loop 1, linea rifiuto di sottosistema HPLC e la linea di scarico pompa siringa).
- Collegare le linee di ingresso di HPLC. Posto HPLC fase mobile ingresso linea "A" in un contenitore di 25 millimetri di acetato di ammonio e HPLC fase mobile ingresso linea "B" in un contenitore di EtOH.
- Equilibrare il sottosistema di purificazione/formulazione e colonna HPLC.
- Aprire la pagina di controllo per il modulo di purificazione/formulazione nel software selezionando HPLC dal menu principale (in alto a sinistra). Per impostazione predefinita, la scheda di purificazione sarà già selezionata. (Questa pagina è illustrata nella Figura 6).
- Impostare la portata a 5,0 mL/min alla composizione definita solvente e scegliere quale posizione di colonna, la colonna di purificazione è installata in. Accendere la pompa HPLC in modalità isocratica per almeno 10 min.
- Sciacquare la linea di prodotti e tutte le linee di raccolta di frazione con la fase mobile, ciascuno per 1 min.
- Sciacquare ogni ciclo del campione HPLC e HPLC campione ciclo trasferimento tubi con 10 mL di fase mobile utilizzando una siringa.
- Collegare le linee di ingresso purificazione/formulazione sottosistema siringa pompa. Uso concentrata di cloruro di sodio (90 mg/mL) per la linea di Elute e soluzione fisiologica 0,9% per la linea di ricostituire .
- Primo il sottosistema di formulazione.
- Passare alla scheda della pagina del controllo purificazione/formulazione formulazione .
- Per primo il cloruro di sodio concentrato (90 mg/mL), selezionare la scheda di Elute Press inizializzare per inizializzare la pompa a siringa. Pipettare 5 mL.
- Per adescare la soluzione fisiologica 0,9%, selezionare il ricostituire Tab. Pipettare 5 mL.
- Collegare le linee di prodotto e prodotto finale dalla parte anteriore del sottosistema purificazione/formulazione in una connessione di T. Collegare l'uscita del T-collegamento a un filtro sterile (0,22 µm) che, a sua volta, è collegato al flaconcino finale prodotto sterile. Inserire un ago di sfiato con un filtro sterile in spazio di testa della fiala di prodotto finale. Una fotografia della messa a punto finale del sistema è mostrata in figura 5B.
- Aggiungere ghiaccio secco ed EtOH o MeOH la trappola a freddo.
- Eseguire il programma di sintesi
- Passare all'elenco dei programmi selezionando sequenze dal pulsante menu principale (in alto a sinistra). Selezionare il programma CFA [18F] e avviare il programma premendo il pulsante Esegui .
- Con attenzione passano attraverso ogni elemento nella lista di controllo pre-esecuzione e spuntare sono stati completati. Parte della lista di controllo pre-esecuzione schermata è illustrato nella Figura 7.
- Premere continua per confermare che la configurazione è completa e causare la sintesi automatizzata iniziare.
- Se si desidera monitorare la sintesi in tempo reale tramite feedback visivo (telecamere reattore), letture del sensore (ad esempio, temperatura, pressione, vuoto, lettura di radiazione, ecc.) e timer conto alla rovescia. Uno screenshot rappresentativo è illustrato nella Figura 8.
- Durante l'operazione di unità di purificazione , selezionare il prodotto quando il picco di prodotto ha cominciato a comparire sul cromatogramma di rivelatore di radiazioni. Un rappresentante screenshot durante questa operazione di unità (contenente un cromatogramma del rivelatore UV e rivelatore di radiazione in uscita) è illustrato nella Figura 9.
- Una volta che il picco di cromatogramma rivelatore di radiazione è tornato alla linea di base, selezionare rifiuti per deviare il percorso del flusso del sottosistema HPLC per il contenitore dei rifiuti.
- Impostare ed eseguire il programma di formulazione
- Dall'elenco dei programmi (sequenza dello schermo), aprire il [18F] formulazione CFA programma.
- Regolare i parametri di funzionamento dell'unità la formulazione.
- Calcolare il volume della frazione prodotto raccolti (Vfrazione) basato sulla portata della pompa HPLC e la durata della raccolta frazione.
- Calcolare il volume supplementare di cloruro di sodio (90 mg/mL) necessaria per ottenere isotonicità e calcolare la quantità di soluzione fisiologica supplementare necessaria per diluire la concentrazione di EtOH inferiore al 10%.
- Modificare il programma con questi valori. Il volume del cloruro di sodio (90 mg/mL) viene immessa per il passo di Elute e il volume di soluzione fisiologica viene immesso per il passo di ricostituire . (I calcoli sono descritte nel Materiale supplementare, Figura S2).
- Salvare il programma.
- Eseguire il programma. Il sistema diluirà la frazione di prodotto purificato raccolti con cloruro di sodio e soluzione fisiologica per garantire l'isotonicità della formulazione e consegnarlo attraverso un filtro sterilizzante nella fiala di prodotto sterile.
- Raccogliere formulato [18F] CFA per controllo qualità e spedizione
- Rimuovere il prodotto CFA formulato [18F] dalla cella calda.
- Utilizzando tecniche di lavoro sterile, prelevare due campioni (300 µ l) per eseguire test di controllo qualità.
- Utilizzare il primo campione per verificare la sterilità della formulazione finale inoculando tioglicolato fluido media e brodo di soia triptico per 14 d senza osservare alcuna crescita.
- Utilizzare il secondo campione per eseguire il controllo di qualità secondo le procedure elaborate nel passaggio 1.3. Le procedure stabilite presso l'UCLA Ahmanson biomedica ciclotrone impianto secondo farmacopea degli Stati Uniti sono descritti di seguito.
- Valutare aspetto mediante ispezione visiva.
- Valutare il pH con una striscia reattiva.
- Valutare il contenuto di endotossine batteriche utilizzando una cinetica cromogenico batterica endotossina Test (scommessa).
- Valutare l'identità radiochimica con radio-HPLC analitici verificando la co-eluizione del campione radioattivo e un composto di riferimento non radioattivo.
- Valutare la purezza radiochimica con radio-HPLC analitica confrontando l'area sotto la curva (AUC) di impurità radioattive nel cromatogramma rilevatore gamma con l'AUC corrispondente al prodotto desiderato.
- Valutare la purezza chimica con HPLC analitica determinando l'AUC nel cromatogramma rivelatore UV di tutte le impurità UV-attivo.
- Valutare attività molare e la massa di vettore con radio-HPLC analitica determinando l'AUC corrispondente al prodotto desiderato nel cromatogramma rivelatore UV.
- Valutare l'emivita della sonda misurando la sua attività in due punti temporali differenti e una curva di decadimento.
- Valutare il contenuto di solvente residuo della formulazione mediante gascromatografia.
- Valutare l'energia del radionuclide usando uno spettrometro gamma.
- Valutare il contenuto di criptando 222 utilizzando un test di spot basati su TLC.
- Se tutti i test passano, rilasciare la formulazione di sonda per la spedizione al sito imaging clinico.
- Post-run e sistema di arresto
- Sciacquare la colonna di purificazione HPLC e tutti i tubi usati per la raccolta del prodotto con il 70% (v/v) EtOH in acqua. Questo dovrebbe essere fatto con la pagina di controllo PURE/modulo, simile al punto 2.1.12.
- Arrestare il radiosynthesizer tramite il pulsante di alimentazione sul software. Una finestra pop-up indicherà quando l'alimentazione del sistema può essere disattivato.
- Disattivare i rifornimenti di aria compressa e gas inerte chiudendo le valvole di arresto appropriato.
- Concedere tempo radioattività residua nella cella calda a decadere (in genere durante la notte).
- Pulire il radiosynthesizer
- Rimuovere e smaltire tutte le cassette, cartucce, flaconi di reattore e i flaconi dei reagenti utilizzati durante la sintesi.
- Svuotare il contenuto della trappola fredda.
- Pulire i percorsi fluidi del sottosistema di purificazione.
- Aprire un programma di pulizia esistente o creare un nuovo programma che contiene una sola operazione di unità di purificazione in modalità di pulizia (cioè con selezionata la casella di pulite ). Vedere Materiale supplementare, Figura S9 per un esempio.
- La pagina di configurazione del parametro, selezionare la colonna che è stata usata per la purificazione e la linea di ingresso fase mobile HPLC è connesso a un flacone contenente 70% EtOH in acqua. Programmare una portata di 2 mL/min, una risciacquo durata per ogni ciclo di iniezione di 5 min e una risciacquo durata per ogni output prodotto e frazione di 30 s. Selezionare Linee asciutte e programmare una durata di 30 s.
- Posizionare tutte le uscite di linea di frazione in un grande contenitore per rifiuti.
- Eseguire il programma.
- Dopo il completamento, svuotare il contenitore.
- Pulire i percorsi fluidi del sottosistema di formulazione.
- Aprire un programma esistente o creare un nuovo programma che contiene una formulazione unità operazione in modalità di pulizia (cioè con la casella di controllo pulite selezionata nella scheda pulita ). Vedere Materiale supplementare, Figura S10 per un esempio.
- Riempire un serbatoio di diluizione pulito (di fronte il sottosistema di purificazione/formulazione) con 100 mL di EtOH.
- Posizionare il sottosistema di purificazione/formulazione Elute riga di input in un serbatoio di EtOH (contenente > 50 mL di EtOH).
- Inserire le righe di input risciacquo e ricostituire in un contenitore per rifiuti insieme alla linea di uscita del prodotto finale.
- Eseguire il programma.
- Dopo il completamento, svuotare il contenitore.
Risultati
Un metodo per automatizzare la produzione di [18F] CFA è stato sviluppato e tre lotti di convalida sono stati sintetizzati. Sintesi, purificazione e formulazione di [18F] CFA è stato raggiunto a 90 ± 5 min (n = 3) e la resa di radiochimica decadimento senza correzione era 8,0 ± 1,4% (n = 3). I rendimenti di attività delle tre piste erano 3,24 GBq, 2,83 GBq e 3.12 GBq, a partire da 34,3 GBq, GBq 41,8 e 41,1 GBq, rispettivamente. Le formulazioni di CFA ottenuti [18F] superato tutti i test di controllo qualità (tabella 1). Attualmente viene utilizzato il protocollo automatizzato per la produzione di uso clinico [18F] CFA per sostenere studi clinici.
| Dati di controllo qualità | Esecuzione 1 convalida | Esecuzione 2 convalida | Convalida di eseguire 3 |
| [requisito per "Pass"] | |||
| Aspetto | Passare | Passare | Passare |
| [chiaro, incolore, priva di particelle] | |||
| Concentrazione di radioattività presso EOS | 213 MBq/mL | MBq/mL 210 | 180 MBq/mL |
| [≤ 740 MBq/mL @ EOS] | |||
| pH | 6 | 5.8 | 6 |
| [5.0-8.0] | |||
| Half-Life | 115 min | 108 min | 112 min |
| [105 – 115 min] | |||
| Purezza radiochimica | 99% | 99% | 99% |
| [> 95%] | |||
| Radiochimica identità dal tempo di ritenzione relativo (RRT) | 1.01 | 1.01 | 1.01 |
| [1,00 < RRT < 1.10] | |||
| Attività di molare | 314 GBq/µmol | > 370 GBq/µmol | > 370 GBq/µmol |
| [≥ 3,7 GBq/µmol] | |||
| Massa totale vettore nel prodotto finale | 3,1 µ g | < 1 µ g | < 1 µ g |
| [≤ 50 µ g/dose] | |||
| Massa totale impurità nel prodotto finale | ND | ND | ND |
| [≤ 1 µ g / dose] | |||
| Volume di iniezione ammissibile massima basata su vettore totale massa ≤ 50 µ g/dose e impurità totali massa ≤ 1 µ g/dose | Intero batch | Intero batch | Intero batch |
| Contenuto residuo di EtOH da GC | 8,90% | 9,50% | 9.60% |
| [≤ 10%] | |||
| Contenuto residuo di EtOAc da GC | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ 5000 ppm] | |||
| Contenuto residuo di MeCN di GC | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ ppm 410] | |||
| K222 residua di prova di punto di colore | Passare | Passare | Passare |
| [< 50 µ g/mL] | |||
| Prova di integrità della membrana del filtro | Passare | Passare | Passare |
| [bubble punto ≥ 50 psi] | |||
| Endotossine batteriche | Passare | Passare | Passare |
| [≤ 175 EU/batch] | |||
| Purezza radionuclidica di spettroscopia gamma | Passare | Passare | Passare |
| [> 99,5%] | |||
| Sterilità | Passare | Passare | Passare |
| [requisiti USP < 71 >] |
Tabella 1: dati di test di controllo qualità (QC) per tre lotti di convalida un riassunto. EOB = fine del bombardamento; EOS = fine della sintesi; ND = non rilevato.
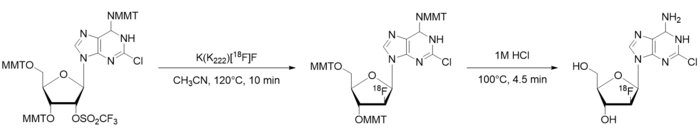
Figura 1: schema di [18F] CFA radiosynthesis. MMT = Monomethoxytrityl. Clicca qui per visualizzare una versione più grande di questa figura.
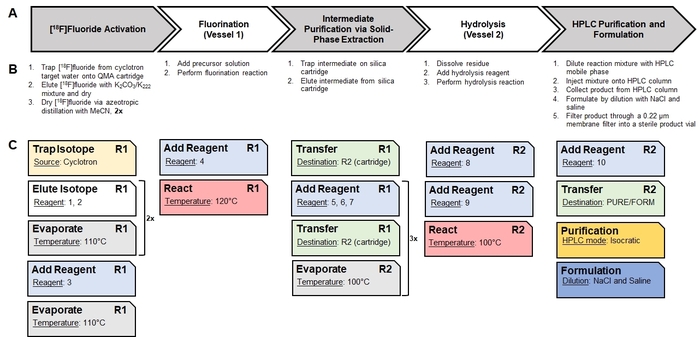
Figura 2: traduzione di una manuale sintesi in una sequenza automatizzata delle operazioni unitarie. (A), questo pannello fornisce una panoramica dei passaggi ad alto livello nella sintesi manuale di [18F] CFA. (B), questo pannello mostra le procedure di base necessarie per eseguire tutti i passaggi ad alto livello. (C) operazioni di unità specifiche per Radiosynthesizer utilizzate per eseguire le procedure di base vengono visualizzate come schede. Ogni operazione di unità ha il proprio insieme di valori di parametri (come evidenziato in figura) che sono configurate tramite il software. La notazione "R1" e "R2" indicano i vasi di reazione #1 e #2, rispettivamente. I reagenti corrispondenti ai numeri di reagente sono identificati nella Figura 4. La serie di operazioni unitarie è salvata come una sequenza ed eseguita dal software per eseguire la sintesi automatizzata. Clicca qui per visualizzare una versione più grande di questa figura.
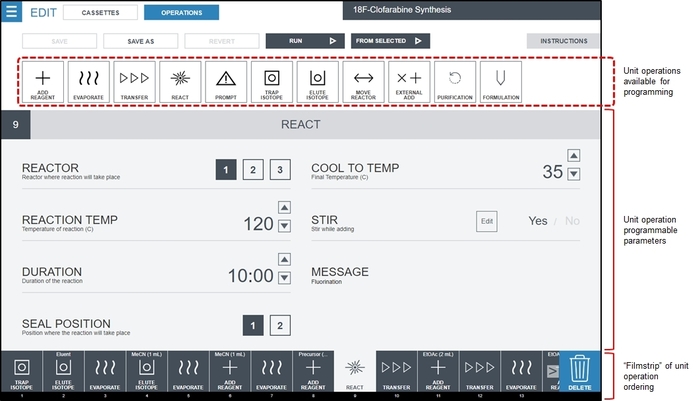
Figura 3: Screenshot dell'interfaccia del software di radiosynthesizer (ELIXYS) per creare un programma di sintesi. Operazioni unitarie sono collocate nell'ordine desiderato nella Filmstrip utilizzando un'interfaccia drag-and-drop. In questa schermata, un'operazione di unità reagire sia selezionata e i suoi valori di parametro modificabile sono mostrati nella parte principale dello schermo. In questo esempio, la reazione di fluorurazione avverrà nel recipiente di reazione #1 (sigillato) a 120 ° C per 10 minuti con agitazione attivo. La nave sarà raffreddata a 35 ° C dopo che è trascorso il tempo di reazione. Dettagli dei valori di parametro che possono essere programmati per altre operazioni di unità sono indicati nel Materiale supplementare, sezione 3. Clicca qui per visualizzare una versione più grande di questa figura.
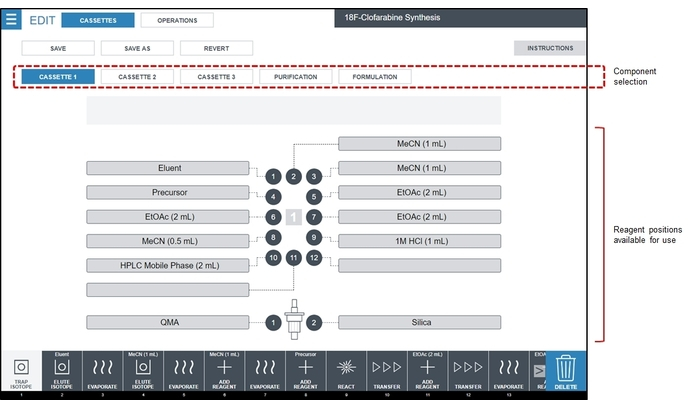
Figura 4: Screenshot della schermata di configurazione di reagente. Per la sequenza di sintesi CFA [18F], tutti i reagenti vengono caricati nella cassetta monouso #1, che viene evidenziato nell'area di selezione del componente. Per la sintesi CFA [18F] descritta qui, eluente è 1,0 mg di K2CO3 + 5,0 mg di K222 in 0,4 mL di H2O/0.5 mL di MeCN, precursore è 6 mg di precursore CFA in 0,6 mL di MeCN e Fase Mobile HPLC è 85: 15 v etanolo: /v 25 mM ammonio acetato. Clicca qui per visualizzare una versione più grande di questa figura.
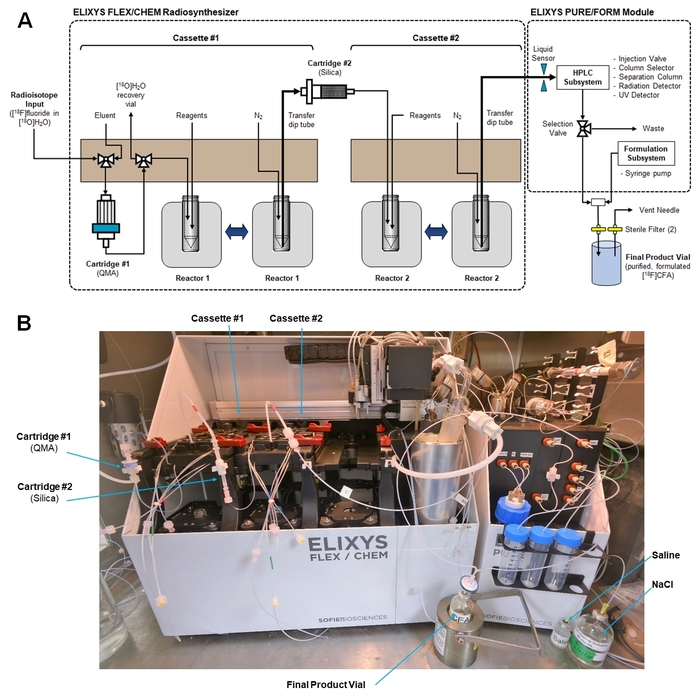
Figura 5: Radiosynthesizer set-up per la sintesi di [18F] CFA. (A) questo è lo schema mostrando percorsi fluido cassetta, connessioni alle cartucce e la connessione per il trasferimento finale prodotto grezzo dal modulo radiosynthesis al modulo purificazione/formulazione. (Entrambi i moduli sono controllati con una singola interfaccia di computer e software). (B) Questa è una fotografia di radiosynthesizer all'interno di una cella calda dopo la preparazione per la sintesi CFA [18F]. Clicca qui per visualizzare una versione più grande di questa figura.
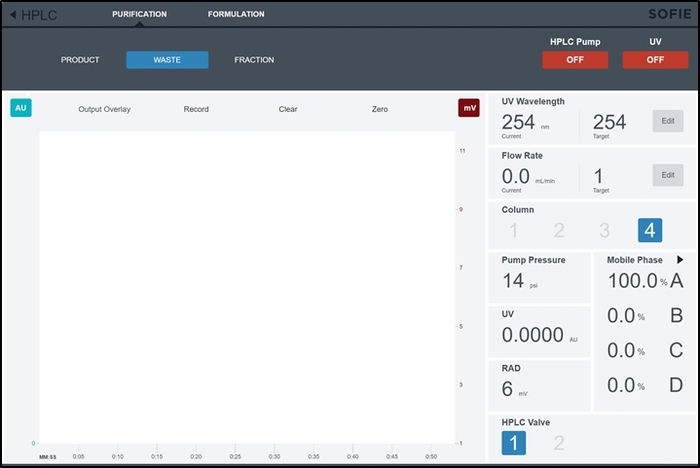
Figura 6: Screenshot dell'interfaccia di controllo del modulo di purificazione/formulazione. Questa schermata è accessibile dall'operatore per controllare manualmente i sottosistemi HPLC e formulazione durante l'installazione di sintesi. Clicca qui per visualizzare una versione più grande di questa figura.
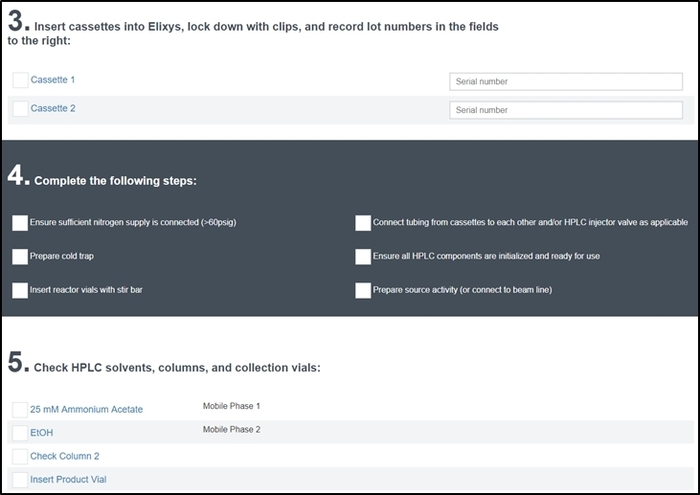
Figura 7: schermata di elenco di controllo pre-esecuzione. L'operatore immette il numero di serie delle cassette installate nel sistema e deve spuntare ogni elemento per garantire il sistema è stato correttamente configurato e preparato per la sintesi. Oltre a queste sezioni, l'operatore è inoltre richiesto per un nome e una descrizione della sintesi eseguire (sezione 1) e lotto numeri per tutti i reagenti utilizzati (sezione 2) e viene chiesto di verificare tutti i feed dei video di reattore funzionino correttamente (sezione 6). Clicca qui per visualizzare una versione più grande di questa figura.
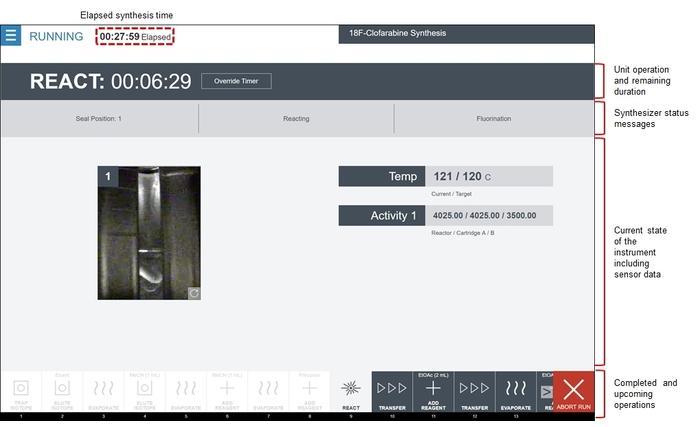
Figura 8: Screenshot del software durante l'esecuzione della sequenza di sintesi CFA [18F] radiosynthesizer. Il software consente di visualizzare l'ordine delle operazioni unitarie nell'area Provino. Operazioni completate sono grigio ed evidenziate in bianco, l'operazione corrente è evidenziata in grigio, e le prossime operazioni vengono mostrate in grigio scuro. L'area centrale dello schermo Mostra lo stato dell'operazione unità attiva, tra cui quali sottocomando è in esecuzione, così come lo stato corrente del sistema (reattore feed video e dati del sensore). Questo particolare reagire funzionamento dell'unità è la reazione di fluorurazione. Nella zona di Temp , è visualizzata la temperatura attuale del reattore accanto la temperatura target (programmato). Di sotto di questo, l'area di attività vengono visualizzati i valori di sensore di radiazione dai tre sensori associati al passaggio di reazione. Infine, un video feed sulla sinistra mostra una vista diretta del flaconcino reattore. Clicca qui per visualizzare una versione più grande di questa figura.
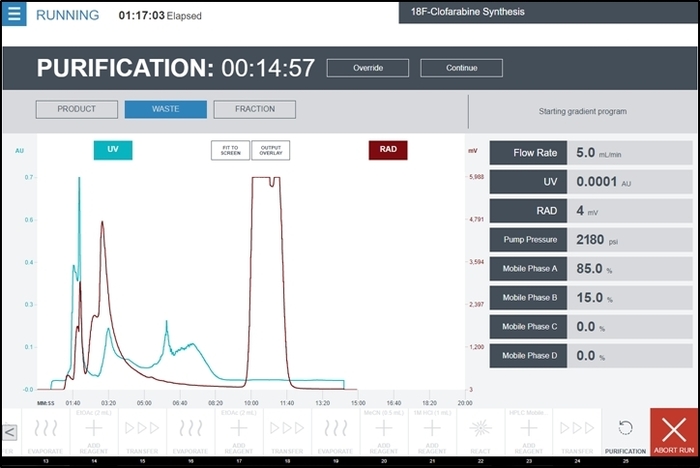
Figura 9: Schermata di radiosynthesizer dell'interfaccia utente durante l'esecuzione il funzionamento di unità di purificazione durante la sintesi dei [18F] CFA. Rivelatore UV the e rilevatore di radiazioni uscite del modulo purificazione/formulazione vengono visualizzati nel grafico centrale in tempo reale. Commenti e suggerimenti aggiuntivi dai rivelatori e pompa HPLC sono mostrati sul lato destro dello schermo. L'operatore raccoglie il picco prodotto temporaneamente selezionando prodotto quando il picco comincia ad apparire e quindi passare al rifiuti dopo il picco completo è stato visto. Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Questo protocollo definisce i passaggi di base che dovrebbero adottare quando si automatizza un protocollo di sintesi manuale per ottenere la produzione di formulazione del tracciante di grado clinico. Il ciclo di sviluppo, compreso lo sviluppo del controllo di qualità, è esemplificato da radiotraccitore [18F] CFA (per l'imaging di dCK attività). Particolare attenzione alla modifica la sintesi automatizzata per garantire l'idoneità di tracciante per uso clinico. La sintesi comporta processi di base quali l'attivazione di fluoro [18F], radiofluorination della molecola del precursore, cartuccia intermedia purificazione, rimozione del gruppo di protezione e purificazione HPLC semi-preparatorio e formulazione per l'iniezione. Questi processi di base comprendono un repertorio standard che è sufficiente per la sintesi della maggior parte dei rivelatori di 18F-etichetta PET.
Durante la progettazione della sintesi, la scelta dei reagenti e garanzia della loro qualità è di particolare importanza per l'uso clinico. Garantire la corretta programmazione e collegamenti corretti eseguendo una finta sintesi (solo solventi) è indispensabile per eliminare errori imprevisti quando la sintesi viene eseguita con la radioattività. Le ottimizzazioni successive sintesi (solventi, volumi, quantità, temperature, tempi di reazione e le condizioni di purificazione) dipendono il tracciante PET specifico nello sviluppo. Durante questi esperimenti, particolare attenzione dovrebbe essere splendeva sulla purezza radiochimica e chimica del prodotto finale che può essere raggiunto, come questi devono soddisfare severi requisiti per l'uso clinico. Una sintesi che produce in modo affidabile un puro prodotto dei rendimenti inferiori ma sufficiente attività è in genere preferita un processo ad alto rendimento che ha un rischio di fallire sporadicamente. Una volta che la sintesi è stata ottimizzata in modo adeguato, il processo finale ha bisogno di sottoporsi a test di convalida (un requisito normativo) per garantire l'idoneità clinica. Il metodo di sintesi convalidato è utilizzabile quindi per produrre il tracciante PET per uso clinico. Quando sintetizzando un tracciante PET secondo un metodo convalidato, le procedure operative standard dovrebbe essere seguite accuratamente. Per garantire il rispetto, il software è programmato per avere l'operatore conferma il completamento dei passaggi chiave tramite una lista di controllo pre-esecuzione dopo aver fatto clic su Esegui per avviare la sintesi. Mentre il sistema eseguirà la sintesi in modo automatico, la fase di purificazione richiede un intervento manuale. L'operatore deve, pertanto, osservare da vicino lo schermo cromatografico durante la fase di purificazione HPLC e inserire manualmente in tempo reale quando di start e stop raccogliendo la frazione di prodotto.
All'interno dei nostri sforzi di automazione e ottimizzazione per la sintesi CFA [18F], abbiamo razionalizzato il metodo di purificazione HPLC semi-preparatorio della miscela utilizzando un sistema solvente iniettabile costituito da soluzione di acetato di ammonio ed EtOH ; il nostro metodo precedente necessaria un ulteriore passaggio per sostituire il solvente dopo purificazione16. La successiva formulazione di processo, così, ha bisogno solo di ridurre il contenuto di EtOH della frazione raccolto ai livelli consentiti e per garantire la sua isotonicità, entrambi i quali può essere compiuti da diluizione. Il passo di formulazione è stato effettuato usando un secondo programma che consiste di una singola operazione di unità di formulazione per consentire aggiunte di volume variabile di NaCl-soluzioni per la frazione prodotto purificato tramite il modulo di formulazione contabilizzare la variabile volume ottenuto dopo purificazione HPLC. Se il volume di frazione del prodotto raccolti è stato impostato per essere costante, invece, il funzionamento dell'unità formulazione potrebbe essere incluso nel programma principale sintesi, evitando la necessità di un programma indipendente. Un approccio alternativo per evitare l'intervento manuale sarebbe quella di utilizzare tutte le funzionalità del modulo formulazione (ad es., diluire il tracer purificato con acqua trappola su una cartuccia di estrazione in fase solida C18, lavarlo, esso eluire con un volume fisso di EtOH e infine, diluirlo con un volume fisso di soluzione fisiologica).
La tecnica qui presentata per l'automazione e la convalida di un protocollo di sintesi per uso clinico è destinata a essere abbastanza generale. Attraverso la scelta di radiosynthesizer (ELIXYS), una vasta gamma di sintesi può essere automatizzata e convalidata. Questo include complesse sintesi 3-pot, o sintesi che coinvolgono alte temperature di solventi volatili. Ottimizzare una sintesi può essere realizzato modificando i parametri del programma software. Il sintetizzatore ha caratteristiche per monitorare l'impatto delle modifiche, ad esempio i vasi di reazione per la rimozione di campioni per analisi radio-TLC o radio-HPLC di posizionamento. Tuttavia, senza modifiche di sistema, il sistema attualmente non consente la gestione di volumi di reagente molto bassa (~ 5-20 µ l), distillazione del prodotto intermedio o la manipolazione di [18F] AlF, 68Ga, o altri radiometalli. Se la sintesi manuale da automatizzare contiene tali passaggi e non può essere eluso, automazione e convalida con un'altra piattaforma di radiosynthesizer potrebbe essere appropriati.
Anche se questo lavoro si è concentrato sullo sviluppo di un protocollo per la produzione automatizzata di [18F] CFA per uso clinico, la sintesi di molti altri traccianti PET potrebbe essere automatizzata in modo adatto per la produzione di clinica, seguendo la stessa logica e metodi. Seguendo il metodo qui presentato, inoltre abbiamo adattato la sintesi automatizzata di 9-(4-[18F] fluoro - 3-[idrossimetilico] butile) guanina ([18F] FHBG) e convalidato per l'uso clinico. Stabilita dall'utente protocolli possono essere caricati e scaricati dalla rete sonda SOFIE, un portale web per la condivisione di programmi di sintesi e connessa documentazione tra radiofarmacia diversi siti27. Questo può evitare una duplicazione degli sforzi della Comunità e facilitare multi-centro studi clinici che coinvolgono imaging PET.
Divulgazioni
I reggenti dell'Università della California hanno concesso in licenza la tecnologia per SOFIE che è stato inventato da Jeffrey Collins e R. Michael van Dam e hanno preso equità in SOFIE come parte della transazione sulle licenze. Inoltre, R. Michael van Dam è un fondatore e consulente di SOFIE. I termini di questo accordo sono stati esaminati e approvati dal Università di California, Los Angeles secondo le proprie politiche di conflitto di interessi. Eric Schopf e Christopher Drake sono dipendenti e gli azionisti di SOFIE.
Riconoscimenti
Quest'opera è stata sostenuta in parte dal National Cancer Institute (R44 CA216539) e dalla Fondazione di UCLA da una donazione fatta da Ralph e Marjorie Crump per l'Istituto di Crump UCLA per Imaging molecolare.
Materiali
| Name | Company | Catalog Number | Comments |
| ELIXYS FLEX/CHEM | Sofie (Culver City, CA, USA) | 1010001 | Radiosynthesizer |
| Radiosynthesizer cassette | Sofie (Culver City, CA, USA) | 1861030400 | Cassette for ELIXYS FLEX/CHEM |
| ELIXYS PURE/FORM | Sofie (Culver City, CA, USA) | 1510001 | Radiosynthesizer purification module |
| [O-18]H2O | IBA RadioPharma Solutions (Reston, VA, USA) | IBA.SP.065 | >90% isotopic purity |
| [F-18]fluoride in [O-18]H2O | UCLA | N/A | Produced in a cyclotron (RDS-112; Siemens; Knoxville, TN, USA) by the (p,n) reaction of [O-18]H2O. Bombardment at 11 MeV using a 1 mL tantalum target with havar foil. |
| Deionized water | UCLA | N/A | Purified to 18 MΩ and passed through 0.1 µm filter |
| Acetonitrile (MeCN) | Sigma-Aldrich (St. Louis, MO, USA) | 271004 | Anhydrous, 99.8% |
| Ethanol (EtOH) | Decon Laboratories, Inc. (King of Prussia, PA, USA) | 2701 | Anhydrous, 200 proof |
| Sodium hydroxide (NaOH) solution | Merck (Burlington, MA, USA) | 1.09137.1000 | 1M solution |
| Hydrochloric acid (HCl) solution | Fisher Chemical (Hampton, NH, USA) | SA48-500 | 1M solution |
| Ethyl acetate (EtAc) | Fisher Chemical (Hampton, NH, USA) | E195SK-4 | HPLC grade |
| Sodium chloride (NaCl) | Fisher Chemical (Hampton, NH, USA) | S-640-500 | USP grade |
| Ammonium acetate | Fisher Chemical (Hampton, NH, USA) | A639-500 | HPLC grade |
| Potassium carbonate (K2CO3) | Fisher Chemical (Hampton, NH, USA) | P-208-500 | Certified ACS |
| CFA precursor | CalChem Synthesis (San Diego, CA, USA) | N/A | Custom synthesis |
| Cryptand 222 (K222; Kryptofix 2.2.2) | ABX Advanced Biochemical Compounds (Radeberg, Germany) | 800.1000 | >99% |
| Sodium chloride (NaCl) solution (saline) | Hospira (Lake Forest, IL, USA) | 0409-4888-02 | 0.9%, for injection, USP grade |
| Silica cartridge | Waters (Milford, MA, USA) | WAT051900 | Sep-pak Classic |
| Quaternary methylammonium (QMA) cartridge | Waters (Milford, MA, USA) | WAT023525 | Sep-pak Light Plus |
| Sterile syringe filter (0.22 µm) | Millipore Sigma (Burlington, MA, USA) | SLGSV255F | Millex-GV |
| Glass V-vial (5 mL) | Wheaton (Millville, NJ) | W986259NG | Used for reaction vessels |
| Septa | Wheaton (Millville, NJ) | 224100-072 | Used for reagent vials |
| Crimp cap | Wheaton (Millville, NJ) | 224177-01 | Used for reagent vials |
| Amber serum vial (2 mL) | Voigt (Lawrence, KS, USA) | 62413P-2 | Used for reagent vials |
| Magnetic stir bar | Fisher Scientific (Hampton, NH, USA) | 14-513-65 | Used for reaction vessels |
Riferimenti
- Phelps, M. E. Positron emission tomography provides molecular imaging of biological processes. Proceedings of the National Academy of Sciences. 97 (16), 9226-9233 (2000).
- Kitson, S., Cuccurullo, V., Ciarmiello, A., Salvo, D., Mansi, L. Clinical Applications of Positron Emission Tomography (PET) Imaging in Medicine: Oncology, Brain Diseases and Cardiology. Current Radiopharmaceuticalse. 2 (4), 224-253 (2009).
- Sengupta, D., Pratx, G. Imaging metabolic heterogeneity in cancer. Molecular Cancer. 15, 4 (2016).
- Rabinovich, B. A., Radu, C. G. Imaging Adoptive Cell Transfer Based Cancer Immunotherapy. Current Pharmaceutical Biotechnology. 11 (6), 672-684 (2010).
- Matthews, P. M., Rabiner, E. A., Passchier, J., Gunn, R. N. Positron emission tomography molecular imaging for drug development. British Journal of Clinical Pharmacology. 73 (2), 175-186 (2012).
- Hargreaves, R. The Role of Molecular Imaging in Drug Discovery and Development. Clinical Pharmacology & Therapeutics. 83 (2), 349-353 (2008).
- Keng, P. Y., Esterby, M., van Dam, R. M., Hsieh, C. -. H. Emerging Technologies for Decentralized Production of PET Tracers. Positron Emission Tomography - Current Clinical and Research Aspects. , 153-182 (2012).
- Lazari, M., Irribarren, J., Zhang, S., van Dam, R. M. Understanding temperatures and pressures during short radiochemical reactions. Applied Radiation and Isotopes. , 82-91 (2016).
- Lazari, M., et al. ELIXYS - a fully automated, three-reactor high-pressure radiosynthesizer for development and routine production of diverse PET tracers. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3 (1), 52 (2013).
- Claggett, S. B., Quinn, K., Lazari, M., Esterby, J., Esterby, M., van Dam, R. M. A new paradigm for programming and controlling automated radiosynthesizer. Journal of Nuclear Medicine. 53 (suppl. 1), 1471-1471 (2012).
- Claggett, S. B., Quinn, K. M., Lazari, M., Moore, M. D., van Dam, R. M. Simplified programming and control of automated radiosynthesizers through unit operations. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3, 53 (2013).
- Lazari, M., et al. Fully Automated Production of Diverse 18F-Labeled PET Tracers on the ELIXYS Multireactor Radiosynthesizer Without Hardware Modification. Journal of Nuclear Medicine Technology. 42 (3), 203-210 (2014).
- Lazari, M., et al. Fully-automated synthesis of 16β-18F-fluoro-5α-dihydrotestosterone (FDHT) on the ELIXYS radiosynthesizer. Applied Radiation and Isotopes. 103, 9-14 (2015).
- Collins, J., et al. Production of diverse PET probes with limited resources: 24 18F-labeled compounds prepared with a single radiosynthesizer. Proceedings of the National Academy of Sciences. 114 (43), 11309-11314 (2017).
- Drake, C., et al. Enzymatic Radiofluorination of Biomolecules: Development and Automation of Second Generation Prosthetic on ELIXYS Radiosynthesizer. Journal of Nuclear Medicine. 58 (supplement 1), 1 (2017).
- Gobbi, L. C., et al. Identification of Three Novel Radiotracers for Imaging Aggregated Tau in Alzheimer's Disease with Positron Emission Tomography. Journal of Medicinal Chemistry. 60 (17), 7350-7370 (2017).
- Ippisch, R., Maraglia, B., Sutcliffe, J. Automated production of [18F]-F-Py-peptides. Journal of Nuclear Medicine. 57, 275 (2016).
- Chen, H., et al. AMG 580: A Novel Small Molecule Phosphodiesterase 10A (PDE10A) Positron Emission Tomography Tracer. Journal of Pharmacology and Experimental Therapeutics. 352 (2), 327-337 (2015).
- Waldmann, C. M., et al. An Automated Multidose Synthesis of the Potentiometric PET Probe 4-[18F]Fluorobenzyl-Triphenylphosphonium ([18F]FBnTP). Molecular Imaging and Biology. 20 (2), 205-212 (2018).
- Ravert, H. T., et al. An improved synthesis of the radiolabeled prostate-specific membrane antigen inhibitor, [18F]DCFPyL. Journal of Labelled Compounds and Radiopharmaceuticals. 59 (11), 439-450 (2016).
- Betthauser, T. J., et al. Characterization of the radiosynthesis and purification of [18F]THK-5351, a PET ligand for neurofibrillary tau. Applied Radiation and Isotopes. 130, 230-237 (2017).
- Shu, C. J., et al. Novel PET probes specific for deoxycytidine kinase. Journal of Nuclear Medicine. 51 (7), 1092-1098 (2010).
- Kim, W., et al. [18F]CFA as a clinically translatable probe for PET imaging of deoxycytidine kinase activity. Proceedings of the National Academy of Sciences. 113 (15), 4027-4032 (2016).
- Barrio, M. J., et al. Human Biodistribution and Radiation Dosimetry of 18F-Clofarabine, a PET Probe Targeting the Deoxyribonucleoside Salvage Pathway. Journal of Nuclear Medicine. 58 (3), 374-378 (2017).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon