Method Article
Accumulazione e l'analisi di ioni rameosi in un solfato di rame in soluzione di placcatura
In questo articolo
Riepilogo
Qui, l'accumulo di ioni rameosi in un solfato di rame placcatura soluzione in un modello sperimentale e un'analisi basata su misurazioni quantitative sono descritti. Questo esperimento riproduce il processo di accumulo di ioni rameosi nel bagno di placcatura.
Abstract
Conoscenza del comportamento degli ioni rameosi (monovalenti ioni rame: Cu(I)) in un bagno di placcatura di solfato di rame è importante per migliorare il processo di placcatura. Con successo abbiamo sviluppato un metodo per misurare quantitativamente e facilmente in cu (i) in una soluzione di placcatura e usato per la valutazione della soluzione. In questa carta, una misura quantitativa dello spettro di assorbimento e una misura di iniezione risolta in tempo di Cu (i) le concentrazioni di una reazione al colore sono descritti. Questa procedura è efficace come un metodo per riprodurre e delucidare il fenomeno che si verifica nel bagno placcatura in laboratorio. In primo luogo, è mostrato il processo di formazione e accumulo di Cu (i) in soluzione mediante elettrolisi di una soluzione di placcatura. L'importo di Cu (i) nella soluzione viene aumentato mediante elettrolisi a più alti valori di correnti che il processo di placcatura usuale. Per la determinazione di Cu (i), BCS (bathocuproinedisulfonic acido, sale disodico), un reagente che reagisce selettivamente con cu (i), viene utilizzato. La concentrazione di Cu (i) può essere calcolata dall'assorbanza di Cu (I)-complesso BCS. Successivamente, la misurazione del tempo di reazione del colore è descritto. La curva di reazione di colore di Cu (i) e BCS misurata con il metodo di iniezione può essere scomposto in una componente istantanea e una componente di ritardo. Dall'analisi di questi componenti, la struttura di holding di Cu (i) può essere chiarita, e questa informazione è importante quando predire la qualità del film placcatura ad essere prodotta. Questo metodo viene utilizzato per facilitare la valutazione del bagno placcatura nella linea di produzione.
Introduzione
Come circuiti stampati diventano più dense e multistrato, gestione di soluzioni di placcatura durante il processo produttivo diventa più importante per mantenere la qualità del prodotto. Nel solfato di rame placcatura elettrolitica, lo ione rame monovalente (ione rameoso: Cu(I)) è stata determinata per essere una delle cause principali della grande rugosità e finitura opaca della superficie ramatura. Il comportamento e il ruolo di Cu (i) in placcatura processo1,2,3,4,5, l'effetto di ogni additivo e la tenuta di struttura6,7, 8 sono stati studiati. È necessario analizzare cu (i) della soluzione di placcatura, ma era difficile quantificare la sua concentrazione a causa dell'instabilità di Cu (i) in una soluzione acquosa. Di conseguenza, l'analisi in loco di Cu (i) nel bagno di placcatura è uno strumento efficace per controllare la soluzione di placcatura.
Abbiamo effettuato analisi colorimetrica utilizzando un reagente chelante acquoso, BCS (bathocuproinedisulfonic acido, sale disodico), per stabilire in loco analisi quantitativa di Cu (i) in un solfato di rame in soluzione di placcatura. Il BCS può essere utilizzato per quantificare la concentrazione di Cu (i) in soluzioni acquose9,10,11. Il reagente di reazione del colore di tipo cuproine, che è stato convenzionalmente utilizzato per la determinazione di Cu (i), è idrorepellente e l'estrazione con alcool è necessario. È stato dimostrato che BCS è idrofila e può direttamente misurare cu (i) in una soluzione acquosa. Due molecole di BCS coordinano a uno cu (i) per formare complessi di 1:2 che assorbono la luce visibile a lunghezze d'onda tra 400 e 550 nm (Vedi Figura 1). Abbiamo stabilito un metodo per determinare la concentrazione di Cu (i) della soluzione di placcatura dalla misurazione dell'assorbanza del Cu (I)-BCS complesso12,13. Nella prima parte del presente protocollo, sono descritto un metodo per accelerare la formazione di Cu (i) in un solfato di rame placcatura soluzione in un sistema sperimentale di modello e la determinazione quantitativa della concentrazione di Cu (i) in una soluzione di placcatura. Questo è fondamentale per chiarire il processo di formazione e accumulo di Cu (i) nel bagno di placcatura.
Inoltre, è stato dimostrato che la reazione al colore di Cu (i) e BCS possa essere suddivisi in componenti di reazione relativamente lenta e rapida reazione. Questo aumenta l'incertezza della misura di assorbanza. Per ovviare a questo problema, abbiamo sviluppato un metodo di misurazione di curve di reazione di un metodo di iniezione14,15. La seconda parte Mostra la misurazione di Cu (i) sulla base del metodo di iniezione. Analizzando i componenti ottenuti con il metodo di iniezione, è possibile approssimare la comprensione del meccanismo di formazione di Cu (i) e struttura portante in soluzione.
Convenzionalmente, è stato sostenuto che cu (i) in una soluzione di placcatura è ossidato istantaneamente agli ioni rameici (Cu(II)). Abbiamo confermato che ci sono parecchi millimoli (mmol/L) di Cu (i) nel bagno di placcatura della linea di produzione12. Secondo questo metodo di esperimento, l'accumulo di Cu (i) simile al bagno di placcatura può essere riprodotto anche nel becher del laboratorio. Si tratta di una tecnologia fondamentale per chiarire il processo di produzione e accumulo di Cu (i) in un solfato di rame placcatura elettrolitica di soluzione, che era sconosciuto14. Inoltre, controllando cu (i) della soluzione di placcatura, è anche possibile prevedere l'effetto di Cu (i) la qualità della placcatura pellicola15.
Protocollo
Nota: Si prega di controllare tutte le relative schede di sicurezza (MSDS). Si prega di indossare dispositivi di protezione quando si sperimenta con la placcatura di solfato di rame.
1. preparazione della soluzione di placcatura del solfato di rame
Nota: Il solfato di rame in soluzione acquosa di placcatura è preparato da acido solforico che unisce (0,5 mol/L), solfato di rame (0,4 mol/L), cloro (Cl, 1.41 mmol/L), polietilenglicole (PEG; MW 4000: 0.025 mmol/L), bisolfuro di bis(3-sulfopropyl) (SPS, 0.003 mmol/L) e Janus Green B (JGB, 0.004 mmol/L) in acqua pura.
- Mettere un ancoretta in un becher da 1 litro e versare 600 mL di acqua pura. Aggiungere acido solforico (95,0%: 49,04 g) in piccole porzioni continuando a mescolare. Lasciare raffreddare la soluzione.
- Aggiungere solfato di rame (99,5%: 99,876 g) alla soluzione poco a poco. Agitare per 30 min.
- Aggiungere 23,7 mL di acido cloridrico (0,02 mol/L), 0,1 g di glicole polietilenico, 1 mL di soluzione SPS di 1 mg/L e 1 mL di soluzione JGB di 2 mg/L.
- Trasferire la soluzione in un matraccio tarato (1 L). Aggiungere acqua pura e regolare a 1 L. trasferimento il solfato di rame placcatura soluzione a un contenitore di polietilene e conservarlo a temperatura ambiente al buio.
2. formazione del Cu (i) della soluzione di placcatura
- Versare 150 mL di solfato di rame placcatura soluzione in un becher da mL 200. Mettete l'ancoretta nel becher e mescolate a 500 giri/min. Lasciare la soluzione di placcatura in anticipo a temperatura ambiente (23 ° C ± 1 ° C) per 1 ora.
- Inserire un filmato in un becher e lasciare che il flusso di azoto (circa 85 mL/min). Deoxygenate la soluzione di placcatura con gas azoto per oltre 30 min.
- Tagliare la piastra di rame spessa 0,3 mm con le cesoie di metallo di dimensioni 9,5 x 2 cm. Tagliare la piastra di platino con uno spessore di 0,1 mm nello stesso modo.
- Lavare la piastra di rame e il platino con etanolo e sciacquare con acqua pura. Asciutto con gas azoto.
- Collegare la piastra rame e platino per la dima di fissaggio, inseriscilo all'interno del bicchiere e fissarlo. L'area immerso di ogni piatto per la soluzione di placcatura è di 4 x 2 cm2 (Vedi Figura 2).
Nota: Il jig è costituito di un becher acrilico fissaggio parte (Figura 3 (1)) e parti di elettrodo metallico (Figura 3 (2)). La parte di elettrodo consiste delle parti per fissare la piastra, e la parte si collega al cavo dalla rete elettrica. - Collegare l'elettrodo (anodo) della piastra di rame per il polo positivo dell'alimentatore (Figura 3 (3)) e l'elettrodo di platino piastra (catodo) alla fine negativa dell'alimentatore (Figura 3 (4)).
- Accendere l'alimentazione elettrica a una costante corrente di 1.0 A (densità di corrente: 62,5 mA/cm2). Cu (i) è formata nella soluzione di placcatura in base al tempo di elettrolisi e concentrazione di Cu (i) (importo accumulato) viene ingrandita in circa 10 min.
Nota: Se la piastra viene inserita mentre l'agitatore ruota, la soluzione di placcatura si disperderanno e cada il bicchiere. Si prega di installare il jig prima di accendere il potere di evitare il pericolo. - Spegnere l'alimentazione dopo 10 min e interrompere l'agitatore. Lasciare per circa 10 minuti fino a quando le particelle si depositano.
3. misura quantitativa della cu (i)
- Preparare la soluzione BCS (10-2 mol/L) sciogliendo 0,36 g della molecola in 100 mL di acqua pura. Agitare la soluzione e sciogliere il BCS in una quantità in eccesso rispetto al rame monovalente. Conservare la soluzione BCS in un contenitore a prova di luce e conservare il contenitore al buio.
Nota: Nella misura, la concentrazione di BCS nella soluzione del campione è regolata a 1.000 volte o più la concentrazione di Cu (i). - Aggiungere 60 mL di acido acetico (1 mol/L) e 25,2 mL di soluzione di NaOH (1 mol/L) 120 mL di acqua pura per preparare una soluzione neutralizzante (soluzione tampone).
- Mettere un ancoretta nella cella di misura di assorbimento (lunghezza del cammino ottico: 1 cm) e versare in 2,5 mL di soluzione di neutralizzazione e 219 μL di soluzione di BCS.
- Mescolare in 22 μL di campione di soluzione (passo 2.9) di placcatura. Mescolare per 20 min.
Nota: Al fine di garantire che la funzione di BCS è normale, il pH della soluzione del campione da misurare non deve scendere di sotto 4. BCS selettivamente forma un complesso con cu (i). Il Cu (I)-BCS complesso assorbe nella regione visibile (400-550 nm), e la soluzione neutralizzante sviluppa un colore arancione (Figura 4). - Misurare gli spettri di assorbimento della soluzione del campione (3.4) con uno spettrofotometro UV/vis (intervallo di lunghezza d'onda: 400-600 nm) (Figura 5e).
Nota: Non esistono apparecchi di misurazione vincolata e condizioni, ed è auspicabile per renderle identiche in serie di un esperimento. - Calcolare la concentrazione di Cu (i) usando la legge di Lambert-Beer:
A = εlc
dove A è l'assorbanza, L è la lunghezza del percorso ottico, ε è il coefficiente di assorbimento molare (BCS: 1,2 × 104 a 485 nm), e c è la concentrazione molare (mol/L) del soluto.
Nota: Poiché la lunghezza del cammino ottico è di 1 cm, la concentrazione di Cu (i) nella cella è semplicemente l'assorbanza diviso per il coefficiente di estinzione molare. Il valore ottenuto moltiplicando il rapporto 125 (la diluizione di piega con la soluzione neutralizzante) è la concentrazione di Cu (i) della soluzione di placcatura.
4. misura iniezione di Cu (i) e BCS colore curve di reazione
- Utilizzare uno spettrofotometro UV/vis con funzione di misura di tempo di più di 20 min per misura di iniezione. Lo spettrometro dovrebbe avere un campione dell'alloggiamento coperchio con una porta di siringa (Figura 6 a sinistra) e un titolare di cella di termostato con un agitatore.
- Utilizzare una cella quadrata di 1 cm x 1 cm per la misura di assorbanza. Mettere ancoretta di s nella cella assorbimento.
- Versare 2,5 mL di soluzione neutralizzata preparata a 3,2 e 219 μL della soluzione di BCS preparata in 3.1 nella cella. Massimizzare la velocità di rotazione di agitatore.
- Impostare il tempo di misurazione di 1.270 s nella modalità di misura volta a 485 nm e inizio. Un minuto dopo l'avvio, iniettare 22 μL del campione di soluzione di placcatura (2,9) con una pipetta dal porto siringa del coperchio del vano. Le curve di reazione di Cu (i) e BCS sarà acquisito (diritto diFigura 6 ).
Risultati
La concentrazione di Cu (i) della soluzione di placcatura può essere determinata dall'assorbanza a 485 nm di Cu (I)-chelato di 2BCS. La figura 5 Mostra gli spettri di assorbimento delle soluzioni di placcatura che erano elettrolizzate per 0, 4, 6, 8 e 10 min. La concentrazione di Cu (i) tende ad aumentare da 0 a 10 min a seconda del tempo di elettrolisi. Tuttavia, a seguito della misurazione risolta in tempo, un componente di ritardo è comparso oltre al componente istantaneo nella reazione tra BCS e Cu (i). Ciò riduce il rapporto segnale-rumore (S/N ratio) del valore di assorbanza e previene accurata determinazione della concentrazione di Cu (i). È preferibile utilizzare il metodo di iniezione per determinare la concentrazione di Cu (i), perché la variazione di assorbanza causata tramite l'iniezione di soluzione di placcatura è misurata dalla decomposizione di tempo (Figura 6).
Informazioni sulla struttura portante della soluzione di placcatura cu (i) vengono ottenute mediante analisi numerica della curva di reazione. In generale, cu (i) è rapidamente ossidato a Cu (II) in soluzione acquosa; ma nella soluzione di placcatura è considerato essere stabilizzata formando un complesso con un additivo (soprattutto PEG)14. La curva di reazione riflette il processo di chelazione di Cu (i) e BCS. La curva di reazione è composto da un componente che aumenta immediatamente dopo l'iniezione di soluzione di placcatura e un componente che aumenta lentamente nel corso di diverse decine di min. Questi componenti suggeriscono che ci sono più strutture di holding di Cu (i) della soluzione di placcatura. Caratteristiche della soluzione di placcatura coinvolta in cu (i) possono essere valutate analizzando la curva di reazione. Supponendo che la reazione di Cu (i) con BCS è una reazione di primo ordine per quanto riguarda la concentrazione di Cu (i), abbiamo ottenuto la cinetica di reazione seguente dell'assorbanza, a:
A = A0 + AL [1-exp (altezza/TL)]
t è il tempo dall'inizio della misurazione, A0 corrisponde a un componente che reagisce istantaneamente (assorbanza a t = 0) e AL corrisponde a un componente che reagisce lentamente (a - A0). TL è la costante di tempo del componente AL. Per simulare la curva di reazione del colore, abbiamo applicato la formula per il software di analisi originale (il software potrebbe essere commercialmente disponibile)13,15. Una curva che simula la variazione di assorbanza della reazione al colore della soluzione elettrolitica è illustrata nella Figura 7. Dalla simulazione, sono quantificati i parametri (A0, AL, TL) relazionati all'accumulo di Cu (i). I risultati di simulazione in questa figura sono stati A0 = 0,053, AL = 0.098, TL = 13,6 min e r2 = 0.998. Figura 8 (tracciati), il valore di A0 della soluzione di placcatura che era elettrolizzata per diverse volte. Anche se il valore di A0 non ha cambiato notevolmente fino a 4 min di elettrolisi, un aumento corrispondente al tempo di elettrolisi è stato visto da 6 min a 10 min.
Placcatura è stato effettuato su un substrato di rame per 10 min con le soluzioni di elettrolisi per studiare l'effetto di Cu (i) la qualità della placcatura rame come rugosità e morfologia. Figura 8 Mostra le immagini di SEM (microscopio elettronico a scansione) della struttura superficiale film depositati con soluzioni di elettrolisi. La struttura del film a 0 min e a 4 min di placcatura di elettrolisi sono quasi indistinguibili. Ci sono particelle fini adsorbite densamente con una dimensione di alcune decine di nanometri e una morfologia di superficie liscia. Dopo 6 min di placcatura di elettrolisi, c'è qualche gonfiore sulla superficie. Dopo 10 min di placcatura di elettrolisi, c'è un grande rugosità grosso.
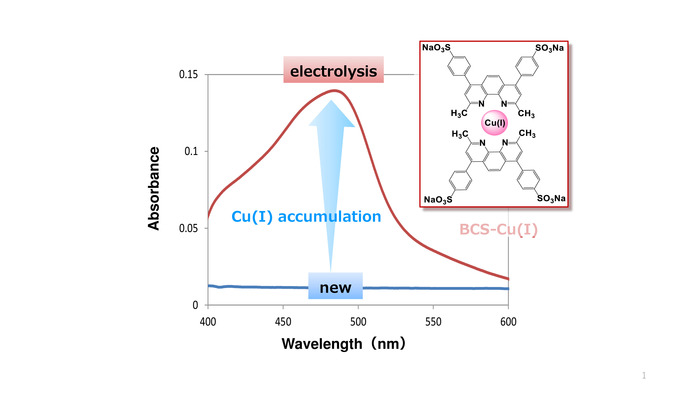
Figura 1: Struttura e spettro di assorbimento di Cu (I)-complesso BCS. Solfato di rame fresco placcatura soluzione e soluzione di elettrolisi. Poiché Cu (i) viene accumulato nella soluzione di placcatura mediante elettrolisi, lo spettro di assorbimento di Cu (I)-complesso BCS è osservato nell'esempio di soluzione di placcatura di elettrolisi. Clicca qui per visualizzare una versione più grande di questa figura.
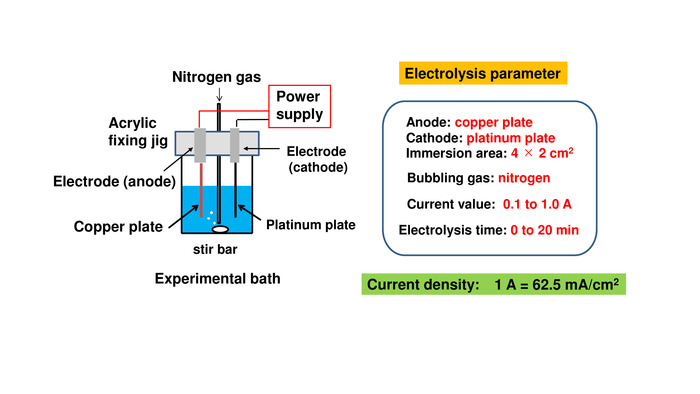
Figura 2: Diagramma schematico delle attrezzature per esperimento di elettrificazione (a sinistra) e rappresentante condizioni dell'elettrolisi sperimentare (a destra). Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3: foto di una combinazioni di parti per essere stimolato nell'esperimento. Fissare la dima con la piastra elettrodo becher di vetro e collegarlo all'alimentazione elettrica. (1) elemento di fissaggio acrilico Becher, parti (2) metallo elettrodo, elettrodo piatto (3) rame (anodo) e (4) platino piastra elettrodo (catodo). Clicca qui per visualizzare una versione più grande di questa figura.

Figura 4: Misurazione dell'assorbimento di Cu (i). Procedura di misurazione di assorbimento (a sinistra) e foto della soluzione campione (a destra). Solfato di rame fresco placcatura soluzione (blu) e soluzione di elettrolisi (arancione). Poiché Cu (i) si accumula nella soluzione di placcatura mediante elettrolisi, è colorata arancione nell'esempio di soluzione di placcatura di elettrolisi. Clicca qui per visualizzare una versione più grande di questa figura.
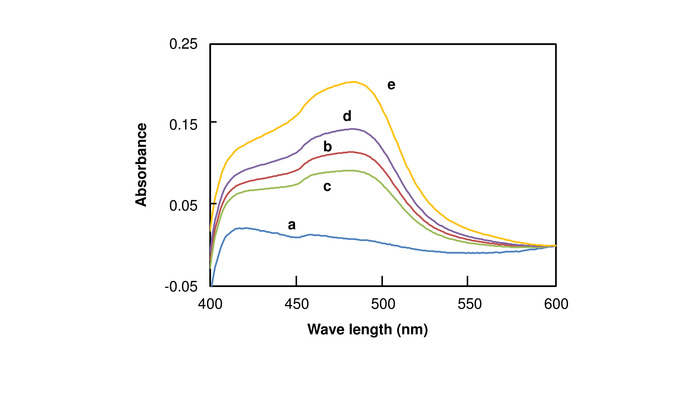
Figura 5: Spettri di assorbimento di Cu (I)-BCS in soluzioni elettrolisi. Tempo di elettrolisi: (un) 0, (b), 4, (c), 6, (d), 8 e (e) 10 min. Poiché l'assorbanza di Cu (I)-BCS generalmente aumenta con il tempo di elettrolisi si allunga, si ritiene che la quantità di Cu (i) accumulato nella soluzione di placcatura è aumentata. Questa figura è una modifica della figura 2 di Koga et al 201815. Clicca qui per visualizzare una versione più grande di questa figura.
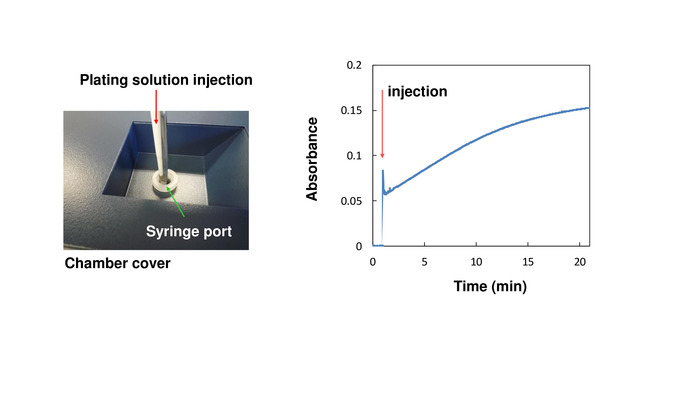
Figura 6: Misura iniezione. A sinistra: Foto di copertina di camera. C'è una porta di siringa nella parte superiore della cella; inserire una pipetta c'e iniettare la soluzione di esempio. Destra: Curva di reazione di placcatura soluzione che è stata elettrolizzata a 1.0 A per 10 min. Si osservano chiaramente un forte aumento di assorbanza immediatamente dopo l'iniezione e un delicato aumento. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 7: Simulazione dell'assorbanza di placcatura soluzione (1.0 A, 10 min).  : punto, linea continua misurato: curva di raccordo. Questa figura è una modifica della figura 4 di Koga et al 201815. Clicca qui per visualizzare una versione più grande di questa figura.
: punto, linea continua misurato: curva di raccordo. Questa figura è una modifica della figura 4 di Koga et al 201815. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 8: Deposizione rispetto al tempo di elettrolisi. (Grafico) Parametri di raccordo normalizzato assorbanza tracciati contro il tempo di elettrolisi, A0. (Immagini) Immagini al SEM della superficie della pellicola di placcatura che sono stati depositati in ogni soluzione di elettrolisi (tempi sopra le immagini sono tempi di elettrolisi). Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Figura 2 illustra schematicamente un sistema per l'esperimento di elettrolisi. Il jig è un articolo ordinato, che consiste di una parte acrilica da fissare a bicchieri e parti metalliche per il fissaggio di piastre e per il collegamento con l'alimentazione. Da questo meccanismo, la zona di immersione delle piastre diventa costante e il rapporto tra il valore corrente e la densità di corrente è mantenuto costante. Nelle nostre condizioni, immersione è 4 cm x 2 cm, e la densità di corrente sarà 62,5 mA/cm2 con una corrente di 1 A. Nella procedura di accumulo di Cu (i), una lastra di rame è collegata all'anodo e una piastra di platino è collegata al catodo. Al fine di aumentare l'efficienza di accumulo di Cu (i), è preferibile di deoxidize la soluzione di placcatura con gas azoto in anticipo.
Misurazione quantitativa di Cu (i) è costituito da una semplice procedura. Versare la soluzione di neutralizzazione e soluzione BCS in cella e miscelare la soluzione di placcatura (Figura 4). È necessario mescolare per più di 20 minuti fino a Cu (i) e BCS reagire sufficientemente. Questo è per assicurare l'accuratezza della misurazione sufficientemente avanzando la reazione. Se cu (i) è contenuta la soluzione di placcatura, la soluzione di esempio appare arancione e uno spettro di assorbimento con un picco a 485 nm è ottenuta. Cambiamenti nel colore della soluzione a causa della formazione di complessa erano drammatici e sorpreso molti tecnici di ramatura.
È confermato che cu (i) si accumula nella soluzione quando una corrente è passata attraverso il solfato di rame placcatura soluzione (Figura 5). Lo spettro di assorbimento Mostra la forma del Cu (I)-complesso BCS, che è adatto per il calcolo della concentrazione di Cu (i) dall'assorbanza a 485 nm. Anche se il valore corrente è arbitrario, cu (i) difficilmente si accumula ad un valore attuale di 0,2 A, e un valore di corrente superiore è richiesto. Anche se la quantità di accumulo di Cu (i) tende ad aumentare con il tempo di elettrolisi, è saturo di corrente eccessiva (ad esempio, elettrolisi per più di 10 min a 1.0 A). La quantità di accumulo di Cu (i) aumentato di elettrolisi per 10 min quando il valore corrente è 0,5-1,0 A14. Quando una corrente eccessiva ha fluito (ad esempio, a 1.0 A per 20 min), la concentrazione di Cu (i) è diminuito. Questo è pensato per essere collegato con la formazione di particelle di rame dovuto il progresso della reazione sproporzionata.
La reazione di Cu (i) e BCS della soluzione di placcatura ha più componenti di tempo, che spesso rendono difficile la determinazione accurata della concentrazione. Per risolvere questo problema, è auspicabile una misurazione di iniezione (Figura 6). In questa misura, l'intensità di assorbimento di Cu (I)-complesso BCS è acquisito come un importo modificato dalla linea di base prima dell'iniezione della soluzione di placcatura, quindi è possibile determinare con maggiore precisione. Inoltre, poiché la curva di reazione può essere analizzata semplicemente numericamente, la concentrazione può essere conosciuta con elevata precisione anche se la reazione non è stata completata. I componenti della curva di reazione sono pensati per riflettere la struttura di ritegno di Cu (i) della soluzione di placcatura14.
È importante modellare la struttura di detenzione di Cu (i) della soluzione di placcatura contro l'asserzione che cu (i) nel bagno di placcatura si ossida istantaneamente cu (II). Vi proponiamo il seguente modello dall'analisi delle caratteristiche della quantità di corrente, la formazione e l'accumulo di Cu (i). Una parte dell'eluito dalla piastra di rame Cu (i) viene mantenuta in soluzione sotto forma di un Cu (I)-complesso di PEG. Nelle prime fasi della formazione del complessa, gli ioni cloruro sono pensati per svolgere un ruolo come stabilizzatore temporaneo per cu (i)6,8. Cu (i) coordinato al PEG è incorporato all'interno della struttura tridimensionale, ed è in un ambiente idrofobico. Quando viene promosso la formazione di Cu (i), cu (i) in eccesso è coordinato per la superficie del perno e può essere in prossimità del liquido. Poiché Cu (i) sulla superficie reagisce prontamente con BCS, rifletterà il componente A0 della curva di reazione. Poiché il Cu (i) all'interno del PEG è protetto dagli attacchi BCS, ha un lento AL componente. È stato sottolineato che il componente di A0 influenza principalmente la qualità della placcatura pellicola15. Questa informazione è importante per la gestione della soluzione di placcatura.
Accelerando la denaturazione della soluzione di placcatura e verificando la concentrazione di Cu (i) accumulata e la struttura di holding, è possibile caratterizzare chiaramente la soluzione di placcatura. Questo è importante non solo per comprendere il processo di placcatura ma anche per predire la qualità del film placcatura ad essere prodotta. Dalla verifica dell'immagine SEM, è stato indicato che la concentrazione di Cu (i), soprattutto la componente di A0, è fortemente coinvolta nella generazione della rugosità del film placcatura (Figura 8). Misurazione in loco di Cu (i) fornisce nuove indicazioni per la gestione dei bagni di placcatura.
Questa ricerca può contribuire alla gestione del bagno placcatura basato su misura ottica. Puntiamo a sviluppare un sistema che consentono di valutare lo stato del bagno placcatura sulla linea di produzione in tempo ed in situ.
Divulgazioni
Non abbiamo nulla di divulgare.
Riconoscimenti
Ringraziamo Hirakawa Miss per il suo grande contributo a questa ricerca.
Materiali
| Name | Company | Catalog Number | Comments |
| Acetic acid | Wako | 016-18835 | |
| BCS | Dojindo | B002 | |
| Copper plate | YAMAMOTO-MS | B-60-P05 | |
| Copper sulfate | Wako | 033-04415 | |
| Hydrochorinic acid | SIGMA-ALDRICH | 13-1750-5 | |
| JGB | Wako | 106-00011 | |
| Magnetic stirrer | Iuchi | HS-30D | |
| NaOH | NACALAI TESQUTE | 31511-05 | |
| PEG4000 | Wako | 162-09115 | |
| Platinum plate | NILACO | PT-353326 | |
| Power supply | TAKASAGO | LX018-28 | |
| SPS | Wako | 327-87481 | |
| Stir bar | AS ONE | 1-5409-01 | |
| Sulfuric acid | Wako | 192-04696 | |
| Syringe port | JASCO | CSP-749 | |
| Thermostat cell holder with a stirrer | JASCO | STR-773 | |
| UV/vis Spectrophotometer | JASCO | V-630 |
Riferimenti
- Kondo, K., Akolkar, R. N., Barkey, D., Yokoi, M. Chap 1. Copper Electrodeposition for Nanofabrication of Electronics Devices. , (2014).
- Kondo, K., Nakamura, T., Okamoto, N. Correlation between Cu (I)-complexes and filling of via cross section by copper electrodeposition. Journal of Applied Electrochemistry. 39, 1789-1795 (2009).
- Healy, J. P., Pletcher, D., Goodenough, M. The Chemistry of the additives in an acid copper electroplating bath, Part II. The instability of 4,5-dithiaoctance-1,8-disulphonic acid in the bath on open circuit. Journal of Electroanalytical Chemistry. 338, 167-177 (1992).
- Frandon, E. E., Walsh, F. C., Campbell, S. A. Effect of thiourea, benzotriazole and 4,5-dithiaoctane-1,8-disulphonic acid on the Kinetics of Copper Deposition from Dilute Acid Sulphate Solution. Journal of Applied Electrochemistry. 25, 574-583 (1995).
- Gabrielli, C., Mocoteguy, P., Perrot, H., Zdunek, A., Sanz, D. N. A Model for Copper Deposition in the Damascene Process Application to the Aging of the Deposition Bath. Journal of The Electrochemical Society. 154 (1), D13-D20 (2007).
- Yokoi, M., Konishi, S., Hayashi, T. Adsorption Behavior of Polyoxyethyleneglycole on the Copper Surface in an Acid Copper Sulfate Bath. Denki Kagaku. 52, 218-223 (1984).
- Pan, S. Z., Song, L. X., Chen, J., Du, F. Y., Yang, J., Xia, J. Noncovalent Interaction of Polyethylene Glycol with Copper Complex of Ethylenediaminetetraacetic Acid and Its Application in Constructing Inorganic Nanomaterials. Dalton Transactions. 40, 10117-10124 (2011).
- Feng, Z. V., Li, X., Gewirth, A. A. Inhibition Due to the Interaction of Polyethylene Glycol, and Copper in Plating Bath: A Surfce-Enhanced Raman Study. The Journal of Physical Chemistry. B. 107, 9415-9423 (2003).
- Palmer, J. Determination of Copper Species in Atmospheric Waters. The Plymouth Student Scientist. 7 (2), 151-184 (2014).
- Faizullah, A., Townshend, A. Spectrophotometric Determination of Copper by Flow Injection Analysis with an On-Line Reduction Column. Analytica Chimica Acta. 172, 291-296 (1985).
- Koga, T., Hirakawa, C., Takeshita, M., Terasaki, N. Quenching Characteristics of Bathocuproinedisulfonic Acid, Disodium Salt in Aqueous Solution and Copper sulfate plating solution. Japanese Journal of Applied Physics. 57, (2018).
- Noma, H., et al. Analysis of Cu(I) in Copper Sulfate Electroplating Solution. Journal of The Surface Finishing Society of Japan. 63, 124-128 (2012).
- Noma, H., et al. Analysis of Cu(I) Complexes in Copper Sulfate Electroplating Solution by Using Reaction Kinetics with a Chelate Regent. ECS Transactions. 58 (17), 77-88 (2014).
- Koga, T., Nonaka, K., Sakata, Y., Terasaki, N. Electrochemical Formation and Accumulation of Cu(I) in Copper Sulfate Electroplating Solution. Journal of The Electrochemical Society. 165 (10), D423-D426 (2018).
- Koga, T., Nonaka, K., Sakata, Y., Terasaki, N. Spectroscopic and Electrochemical Analysis of Cu(I) in Electroplating Solution and Evaluation of Plated Films. Journal of The Electrochemical Society. 165 (10), 467-471 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon