このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
可視光照明下におけるプラスモニック触媒のための銀パラジウム合金ナノ粒子の調製
要約
ここで提示される銀パラジウム(Ag-Pd)合金ナノ粒子(NPs)の合成のためのプロトコルはZrO2(Ag-Pd/ZrO2)でサポートされています。可視光照射からエネルギーを収穫し、分子変換を加速・制御するシステムです。これは、Ag-Pd/ZrO2 NPによって触媒された光照射下でのニトロベンゼン還元によって示される。
要約
局在した表面プラズモン共鳴(LSPR)は、さまざまな分子形変換の選択性を加速および制御することができます。これにより、これらの範囲でLSPR励起を支えるプラズモニックナノ粒子が触媒として採用される場合の反応を駆動し、制御するための持続可能な入力として、可視光または近IR光を使用する可能性が開かれます。残念ながら、パラジウム(Pd)などのいくつかの触媒金属には当てはまりません。この制限を克服する戦略の1つは、プラスモニック金属と触媒金属を含むバイメタルNPを採用することです。この場合、プラスモニック金属中のLSPR励起は、触媒成分によって駆動される加速および制御変換に寄与し得る。本明細書で報告される方法は、プラスモニック触媒系として作用するZrO2(Ag-Pd/ZrO2)で支持されるバイメタル銀パラジウム(Ag-Pd)NPsの合成に焦点を当てている。このNPは、ZrO2支持に対応する金属前駆体を共含浸させ、続いてZrO2支持体に直接バイメタルNPを形成する同時還元によって調製した。次に、Ag-Pd/ZrO2 NPを、LEDランプによる425nmの照明下でのニトロベンゼンの還元のためのプラスモニック触媒として使用した。ガスクロマトグラフィー(GC)を用いて、暗色および光照射条件下での還元反応の変換および選択性をモニタリングすることができ、非プラズモニックPdをプラスモニック金属Agで合金化した後のLSPR励起下での触媒性能の向上および制御を実証する。この技術は、幅広い分子変換およびNPs組成物に適応することができ、変換および選択性の点で異なるタイプの触媒反応のプラズモニック触媒活性の特性化に有用である。
概要
金属ナノ粒子(NPs)のいくつかの用途の中で、触媒は特別な注意を払うに値する。触媒は持続可能な未来において中心的な役割を果たし、エネルギー消費の減少、原材料の利用の改善、よりクリーンな反応条件1、2、3、4に貢献する。したがって、触媒の進歩は、化学プロセスの原子効率を高め、よりクリーンで経済的に実行可能で、より環境に優しいツールを提供することができます。銀(Ag)、金(Au)または銅(Cu)を包含する金属NPsは、これらのシステムが局在面プラズモン共鳴(LSPR)励起5、6、7、8を介してナノスケールで光と相互作用するユニークな方法から生じる可視範囲で興味深い光学特性を表示することができる。これらのNPでは、プラズモニックNPと呼ばれ、LSPRは、電子5、6、7、8の集合運動との(入ってくる電磁波からの)入射光子との共振相互作用を含む。この現象は、環境9、10、11の大きさ、形状、組成、および誘電率に依存する特性周波数で起こる。例えば、Ag、Au、およびCuの場合、これらの周波数は可視から近いIRまで、そのLSPR5、6、7、8、12、13を励起する太陽エネルギーの利用の可能性を開くことができる。
近年、プラスモニックNPsにおけるLSPR励起が、分子変換の速度を加速し、分子変換の選択性を制御するために寄与できることが実証されている5、14、15、16、17、18、19。これは、光からのエネルギーを使用して化学変換を加速、駆動、および/または制御するプラスモニック触媒と呼ばれるフィールドを生み出しました5,14,15,16,17,18,19.この文脈では、プラスモニックNPsにおけるLSPR励起が、LSPR励起熱担体と呼ばれるエネルギー熱電子および正孔の形成につながることが確立されている。これらのキャリアは、電子的または振動的活性化15、16を介して吸着された種と相互作用することができる。反応速度の増加に加えて、このプロセスは、従来の熱化学的に駆動されたプロセスを介してアクセスできない代替反応経路を提供することができ、反応選択性20、21、22、23、24、25を制御するための新しい道を開く。重要なことに、プラズモン崩壊はまた、熱放散につながる可能性があることは注目に値し、また、反応速度15、16の高速化に寄与することができるNPsの近傍の温度上昇につながる。
これらの興味深い特徴により、プラズモニック触媒は、様々な分子変換18に向けてうまく採用されている。それにもかかわらず、重要な課題は残っています。AgやAuなどのプラズモニックNPは、可視および近IR範囲で優れた光学特性を示しますが、その触媒特性は変換の範囲の点で制限されています。つまり、いくつかの変換に対して良好な触媒特性が表示されません。さらに、パラジウム(Pd)や白金(Pt)などの触媒に重要な金属は、可視または近照性の範囲でLSPR励起をサポートしていません。このギャップを埋めるために、プラスモニック金属と触媒金属を含むバイメタルNPは、効果的な戦略20、26、27、28、29を表します。これらのシステムでは、プラスモニック金属をアンテナとして用いて、光励起からLSPRを通してエネルギーを収穫し、触媒金属の分子変換を駆動、加速、制御するために使用することができます。したがって、この戦略は、我々は伝統的なプラズモニック金属NP 20、26、27、28、29を超えてプラズモニック触媒を拡張することができます。
本プロトコルは、プラスモニック触媒反応のためのプラスモニック触媒系として作用することができるZrO2(Ag-Pd/ZrO2)でサポートされるバイメタル銀パラジウム(Ag-Pd)合金NPのファシリティ合成を記述する。Ag-Pd/ZrO2 NPは、ZrO2支持に対応する金属前駆体を共含浸させることにより、次いで同時還元30を行った。このアプローチはZrO2サポートの表面に直接サイズ(直径)の約10 nmのバイメタルNPの形成につながった。このNPは、得られたAg-Pd NPsの光学特性を最大化しながら触媒金属の利用を最小限に抑えるためにPdの1モル%で構成された。ニトロベンゼンの還元のために、Ag-Pd/ZrO2 NPをプラスモニック触媒分解に適用するためのプロトコルが実証された。LSPR励起には425 nm LED照明を採用しました。ガスクロマトグラフィーは、暗色および光照射条件下での還元反応の変換および選択性をモニタリングするために行った。LSPR励起は、純粋に熱駆動条件に対するAg-Pd/ZrO2 NPにおける触媒性能および選択性の制御を強化しました。このプロトコルに記載されている方法は、ガスクロマトグラフィーと結合した単純な光触媒反応設定に基づいており、幅広い分子変換およびNPs組成物に適合させることができる。したがって、この方法は、光触媒活性の特性を、変換および反応選択性の観点から、異なるNPsの、無数の液相変換に対して可能にする。この記事は、新規参入者と現場の経験豊富な科学者の両方に重要なガイドラインと洞察を提供すると信じています。
プロトコル
1. Ag-Pd/ZrO2 NPsの合成
注: この手順では、Ag-Pd の Pd mol% は 1% に対応し、ZrO2 の Ag-Pd ローディングは 3 wt.% に対応しました。
- ZrO2 パウダー1gを250 mLビーカーに入れます。
- AgNO 3(aq)(0.0059 mol/L)の50 mLと9.71 mLのK2PdCl4(aq)(0.00031 mol/L)溶液を室温で激しい磁気攪拌(500 rpm)下でビーカーに加えます。
- 10 mL のリジン (0.53 M) 水溶液を加えます。
- 20分間、激しい攪拌(500rpm)下で混合物を保ちます。
- 20分後、ピペットを使用して、1 mL/minの速度で、新たに調製したNaBH 4(aq)(0.035 M)溶液を滴下して懸濁液10mLに加えます。 プロセス全体を通して懸濁液を撹拌(500 rpm)下に保ちます。
- 混合物を室温で30分間かき混ぜます。
2. 触媒の分離と精製
- 懸濁液を遠心管に移し、10分間3,260 x gで遠心分離して混合物から固形分を分離する。
- 慎重にピペットで液相を除去し、チューブに15 mL脱イオン水を加えます。
- 固体の分散が得られるまで激しく振る。良好な分散が達成されない場合は、5分間超音波浴中にチューブを置きます。
- 3,260 x g で分散液を10分間遠心する。
- 洗浄手順(2.2~2.2.2.)を、脱イオン水を使用してさらに2回繰り返し、水の代わりにエタノールを使用します。
- エタノールを取り出し、オーブンで固体を60°Cで12時間乾燥させます。
- さまざまな顕微鏡、元素、分光技術によって調製されたAg-Pd/ZrO2 のNPを特徴付けます。
3. Ag/ZrO2 NPsの合成
注: この手順では、ZrO2 での Ag の荷重は 3 wt.% に対応しています。
- ZrO2 パウダー1gを250 mLビーカーに入れます。
- AgNO 3(aq)(0.0059 mol/L)溶液を室温で激しい磁気攪拌(500 rpm)下でビーカーに50 mL添加します。
- 10 mL のリジン (0.53 M) 水溶液を加えます。
- 20分間、激しい攪拌(500rpm)下で混合物を保ちます。
- 20分後、ピペットを使用して、1 mL/minの速度で、新たに調製したNaBH 4(aq)(0.035 M)溶液を滴下して懸濁液10mLに加えます。プロセス全体を通して懸濁液を撹拌(500 rpm)下に保ちます。
- 混合物を室温で30分間かき混ぜます。
4. 触媒の分離と精製
- 懸濁液を遠心管に移し、10分間3,260 x gで遠心分離して混合物から固形分を分離する。
- 慎重にピペットで液相を除去し、チューブに15 mL脱イオン水を加えます。
- 固体の分散が観察されるまで激しく振る。良好な分散が達成されない場合は、5分間超音波浴中にチューブを置きます。
- 3,260 x g で分散液を10分間遠心する。
- 洗浄手順(4.2~4.2.2.)を、脱イオン水を使用してさらに2回繰り返し、水の代わりにエタノールを使用します。
- エタノールを取り出し、オーブンで固体を60°Cで12時間乾燥させます。
- 調製されたAg/ZrO2 のNPは、様々な顕微鏡、元素、分光技術によって特徴づけることができます。
5. LSPR励起(光照明)下のニトロベンゼン還元に向けたプラスモニック触媒性能の検討
- 25 mL ラウンドボトムフラスコに30mgの触媒を磁気攪拌棒と一緒に入れる。
- ニトロベンゼン(0.03モル/L)の溶液をイソプロピルアルコール(IPA)に5 mL加えて反応器に加えます。
- 次いで、11.22mgのKOH粉末(0.0002モル)を加える。
- 1分間アルゴン流で懸濁液をバブリングして反応器をパージします。パージ後すぐにフラスコを密封します。
- 温度制御された磁気撹拌機(500rpm)以上の70°Cで加熱したオイルバスに反応器を入れます。
- 光源として425nmの波長を有する4つのLEDランプ、および0.5W/cm2の光強度を用いて管を照射する。ランプから反応フラスコまでの距離は7cmでなければなりません。
- 活発な磁気撹拌(500rpm)下で70°Cで2.5時間反応を進める。
- 次に、ライトを消し、反応器を開き、注射器と針を使用して1mLサンプルを採取します。0.45 μmフィルターを通してフィルター処理し、触媒微粒子を除去し、ガスクロマトグラフィーバイアルに入れ。
LSPR励起(暗い状態)がない場合の反応
- 5に記載されているのと同じ手順に従うが、光照射を行わない。反応管をアルミホイルで包み、光の露出を防ぎます。
ガスクロマトグラフィー(GC)分析製剤
- 約30 mmol/Lニトロベンゼン(NB)、アニリン30ミリモル/L(AN)、アゾベンゼン(AB)30ミリモル/Lを含むIPA溶液を調製します。
- 適切な方法を使用して溶液のGC分析を実行します。カラム温度とガス流量のプログラムを変えることで、さまざまな方法でテストできます。選択した方法は、最小保持期間内の IPA、NB、AN、および AB に対応するピークを分離できる必要があります。
- この方法を選択したら、IPAで50mM、25mM、10mM、5 mM、2.5 mM NBの溶液セットを用意し、同じ濃度のIPAでANとABの別の溶液セットを調製します。
- 準備されたソリューションの GC 分析を実行します。各クロマトグラムは2つのピークを提示する必要があります:高い1つはIPAに対応し、下の1つはNB、AN、またはABに対応します。各クロマトグラムについて、すべてのピークの保持時間とピーク領域をメモします。
- 各サンプルの濃度対ピーク面積をプロットして、NB、AN、およびABのキャリブレーション曲線をトレースします。
8. GC分析
- 手順 5 で収集したサンプルに対して GC 分析を実行します。と6.手順 7.2 で使用したのと同じ方法を使用します。と7.4.
- クロマトグラムごとに、保持時間とピーク面積をメモし、前にプロットしたキャリブレーションカーブを使用して、サンプル中のNB、AN、およびABの濃度を決定します。
- ニトロベンゼン変換、アニリンおよびアゾベンゼンの選択度を計算します。
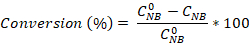
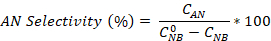
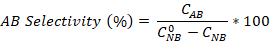
最初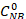 のNB濃度(0.03 mol/L)、およびCNB、C AN、C ABは、それぞれ、GC分析による2.5時間反応後に、NB、AN、およびAB濃度に対応する。
のNB濃度(0.03 mol/L)、およびCNB、C AN、C ABは、それぞれ、GC分析による2.5時間反応後に、NB、AN、およびAB濃度に対応する。
結果
図1Aは、純粋なZrO2酸化物(左)とAg-Pd/ZrO2のNPs(右)を含む固体試料のデジタル写真を示す。この色の色の変化は白色(ZrO2)から茶色(Ag-Pd/ZrO2)に変化し、ZrO2表面でのAg-Pd NPの堆積に関する最初の定性的証拠を提供する。図1Bは、Ag-Pd/ZrO2 NP(青色トレース)とZrO2(黒トレース)およびAg/ZrO2 NP(赤色の...
ディスカッション
この方法で説明した知見は、Pdの固有の触媒活性(または他の触媒的な触媒的な金属ではない)が、バイメタル合金NPs35における可視光照射を介したLSPR励起によって有意に増強できることを示す。この場合、Ag(または別のプラズモニック金属)は、LSPR励起を介して可視光照射からエネルギーを収穫することができる。LSPR励起は、熱電荷キャリア(熱い電子と正孔)と局在?...
開示事項
著者らは開示するものは何もない。
謝辞
この作品は、ヘルシンキ大学とジェーンとアートス・エルッコ財団によって支援されました。S.H.はエラスムス+EUのフェローシップに感謝します。
資料
| Name | Company | Catalog Number | Comments |
| 2-Propanol (anhydrous, 99.5%) | Sigma-Aldrich | 278475 | CAS Number 67-63-0 |
| Aniline (for synthesis) | Sigma-Aldrich | 8.22256 | CAS Number 62-53-3 |
| Azobenzene (98%) | Sigma-Aldrich | 424633 | CAS Number 103-33-3 |
| Ethanol | Honeywell | 32221 | CAS Number 64-17-5 |
| Hydrochloric acid (37%) | VWR | PRLSMC310066 | CAS Number 7647-01-0 |
| L-Lysine (crystallized, ≥98.0% (NT)) | Sigma-Aldrich | 62840 | CAS Number 56-87-1 |
| Nitric acid (65%) | Merck | 100456 | CAS Number 7697-37-2 |
| Nitrobenzene | Sigma-Aldrich | 8.06770 | CAS Number 98-95-3 |
| Potassium hydroxide | Fisher | 10448990 | CAS Number 1310-58-3 |
| Potassium tetrachloropalladate (II) (98%) | Sigma-Aldrich | 205796 | CAS Number 10025-98-6 |
| Silver nitrate (ACS reagent, ≥99.0%) | Sigma-Aldrich | 209139 | CAS Number 7761-88-8 |
| Sodium borohydride (fine granular for synthesis) | Sigma-Aldrich | 8.06373 | CAS Number 16940-66-2 |
| Zirconium (IV) oxide (nanopowder, <100 nm particle size (TEM)) | Sigma-Aldrich | 544760 | CAS Number 1314-23-4 |
参考文献
- Dunn, P. J., Hii, K. K., Krische, M. J., Williams, M. T. . Sustainable Catalysis: Challenges and Pratices for the Pharmaceutical and Fine Chemical Industries. , (2013).
- Tzouras, N. V., Stamatopoulos, I. K., Papastavrou, A. T., Liori, A. A., Vougioukalakis, G. C. Sustainable metal catalysis in C-H activation. Coordination Chemistry Reviews. 343, 25 (2017).
- Polshettiwar, V., Varma, R. S. Green chemistry by nano-catalysis. Green Chemistry. 12 (5), 743 (2010).
- Rodrigues, T. S., da Silva, A. G. M., Camargo, P. H. C. Nanocatalysis by noble metal nanoparticles: controlled synthesis for the optimization and understanding of activities. Journal of Materials Chemistry A. 7 (11), 5857-5874 (2019).
- Linic, S., Christopher, P., Ingram, D. B. Plasmonic-metal nanostructures for efficient conversion of solar to chemical energy. Nature Materials. 10 (12), 911-921 (2011).
- Nam, J. M., Liz-Marzán, L., Halas, N. Chemical Nanoplasmonics: Emerging Interdisciplinary Research Field at Crossroads between Nanoscale Chemistry and Plasmonics. Accounts of Chemical Research. 52 (11), 2995-2996 (2019).
- Brongersma, M. L., Halas, N. J., Nordlander, P. Plasmon-induced hot carrier science and technology. Nature Nanotechnology. 10 (1), 25-34 (2015).
- Smith, J. G., Faucheaux, J. A., Jain, P. K. Plasmon resonances for solar energy harvesting: A mechanistic outlook. Nano Today. 10 (1), 67-80 (2015).
- Hartland, G. V. Optical studies of dynamics in noble metal nanostructures. Chemical Reviews. 111 (6), 3858-3887 (2011).
- Kelly, K. L., Coronado, E., Zhao, L. L., Schatz, G. C. The optical properties of metal nanoparticles: The influence of size, shape, and dielectric environment. Journal of Physical Chemistry B. 107 (3), 668-677 (2003).
- Hermoso, W., et al. Triangular metal nanoprisms of Ag, Au, and Cu: Modeling the influence of size, composition, and excitation wavelength on the optical properties. Chemical Physics. 423, 142-150 (2013).
- Kumar, A., et al. Rational Design and Development of Lanthanide-Doped NaYF4@CdS-Au-RGO as Quaternary Plasmonic Photocatalysts for Harnessing Visible-Near-Infrared Broadband Spectrum. ACS Applied Materials and Interfaces. 10 (18), 15565-15581 (2018).
- Reddy, K. L., Kumar, S., Kumar, A., Krishnan, V. Wide spectrum photocatalytic activity in lanthanide-doped upconversion nanophosphors coated with porous TiO2 and Ag-Cu bimetallic nanoparticles. Journal of Hazardous Materials. 367, 694-705 (2019).
- Ingram, D. B., Linic, S. Water splitting on composite plasmonic-metal/semiconductor photoelectrodes: Evidence for selective plasmon-induced formation of charge carriers near the semiconductor surface. Journal of the American Chemical Society. 133 (14), 5202-5205 (2011).
- Linic, S., Aslam, U., Boerigter, C., Morabito, M. Photochemical transformations on plasmonic metal nanoparticles. Nature Materials. 14 (6), 567-576 (2015).
- Aslam, U., Rao, V. G., Chavez, S., Linic, S. Catalytic conversion of solar to chemical energy on plasmonic metal nanostructures. Nature Catalyst. 1, 656-665 (2018).
- Araujo, T. P., Quiroz, J., Barbosa, E. C. M., Camargo, P. H. C. Understanding plasmonic catalysis with controlled nanomaterials based on catalytic and plasmonic metals. Current Opinion in Colloid and Interface Science. 39, 110-122 (2019).
- Gellé, A., et al. Applications of plasmon-enhanced nanocatalysis to organic transformations. Chemical Reviews. , 986-1041 (2020).
- Shaik, F., Peer, I., Jain, P. K., Amirav, L. Plasmon-Enhanced Multicarrier Photocatalysis. Nano Letters. 18 (7), 4370-4376 (2018).
- Quiroz, J., et al. Controlling Reaction Selectivity over Hybrid Plasmonic Nanocatalysts. Nano Letters. 18, 7289-7297 (2018).
- Peiris, E., et al. Plasmonic Switching of the Reaction Pathway: Visible-Light Irradiation Varies the Reactant Concentration at the Solid-Solution Interface of a Gold-Cobalt Catalyst. Angewandte Chemie - International Edition. 58 (35), 12032-12036 (2019).
- Yu, S., Wilson, A. J., Heo, J., Jain, P. K. Plasmonic Control of Multi-Electron Transfer and C-C Coupling in Visible-Light-Driven CO2 Reduction on Au Nanoparticles. Nano Letters. 18 (4), 2189-2194 (2018).
- Yu, S., Jain, P. K. Plasmonic photosynthesis of C 1 -C 3 hydrocarbons from carbon dioxide assisted by an ionic liquid. Nature Communications. 10, 2022 (2019).
- Zhang, X., et al. Product selectivity in plasmonic photocatalysis for carbon dioxide hydrogenation. Nature Communications. 8, 1-9 (2017).
- Cortés, E. Efficiency and Bond Selectivity in Plasmon-Induced Photochemistry. Advanced Optical Materials. 5 (15), 1700191 (2017).
- de Freitas, I. C., et al. Design-controlled synthesis of IrO 2 sub-monolayers on Au nanoflowers: marrying plasmonic and electrocatalytic properties. Nanoscale. , 23-27 (2020).
- Zhang, C., et al. Al-Pd Nanodisk Heterodimers as Antenna-Reactor Photocatalysts. Nano Letters. 16 (10), 6677-6682 (2016).
- Zhou, L., et al. Light-driven methane dry reforming with single atomic site antenna-reactor plasmonic photocatalysts. Nature Energy. 5, 61-70 (2020).
- Swearer, D. F., et al. Heterometallic antenna-reactor complexes for photocatalysis. Proceedings of the National Academy of Sciences. 113 (32), 8916-8920 (2016).
- Peiris, S., Sarina, S., Han, C., Xiao, Q., Zhu, H. -. Y. Silver and palladium alloy nanoparticle catalysts: reductive coupling of nitrobenzene through light irradiation. Dalton Transactions. 46 (32), 10665-10672 (2017).
- Rahm, J. M., et al. A Library of Late Transition Metal Alloy Dielectric Functions for Nanophotonic Applications. Advanced Functional Materials. 2002122, 02122 (2020).
- Zhang, C., Chen, B. Q., Li, Z. Y., Xia, Y., Chen, Y. G. Surface Plasmon Resonance in Bimetallic Core-Shell Nanoparticles. Journal of Physical Chemistry C. 119 (29), 16836-16845 (2015).
- Liu, Z., Huang, Y., Xiao, Q., Zhu, H. Selective reduction of nitroaromatics to azoxy compounds on supported Ag-Cu alloy nanoparticles through visible light irradiation. Green Chemistry. 18 (3), 817-825 (2016).
- Chaiseeda, K., Nishimura, S., Ebitani, K. Gold nanoparticles supported on alumina as a catalyst for surface plasmon-enhanced selective reductions of nitrobenzene. ACS Omega. 2 (10), 7066-7070 (2017).
- Peiris, S., et al. Metal nanoparticle photocatalysts: emerging processes for green organic synthesis. Catalysis Science and Technology. 6 (2), 320-338 (2016).
- García-García, I., et al. Silver-Based Plasmonic Catalysts for Carbon Dioxide Reduction. ACS Sustainable Chemistry and Engineering. 8 (4), 1879-1887 (2020).
- Agrawal, A., Johns, R. W., Milliron, D. J. Control of Localized Surface Plasmon Resonances in Metal Oxide Nanocrystals. Annual Review of Materials Research. 47 (1), 1-31 (2017).
- Lounis, S. D., Runnerstrom, E. L., Llordés, A., Milliron, D. J. Defect chemistry and Plasmon physics of colloidal metal oxide Nanocrystals. Journal of Physical Chemistry Letters. 5 (9), 1564-1574 (2014).
- Rej, S., et al. Determining Plasmonic Hot Electrons and Photothermal Effects during H2 Evolution with TiN-Pt Nanohybrids. ACS Catalysis. 10 (9), 5261-5271 (2020).
- Barragan, A. A., et al. Photochemistry of Plasmonic Titanium Nitride Nanocrystals. The Journal of Physical Chemistry C. 123 (35), 21796-21804 (2019).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved