このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
肺換気の過偏波 129Xe磁気共鳴画像の取得
要約
過偏波129Xe磁気共鳴画像法(MRI)は、肺機能の局所的に分解された側面を研究するための方法です。この作業は、パルスシーケンス設計、129Xe線量の準備、スキャンワークフロー、および被験者の安全性モニタリングのベストプラクティスに特に注意を払って、肺換気の過分極129XeMRIのエンドツーエンドの標準化されたワークフローを提示します。
要約
過偏波 129Xe MRIは、構造的および機能的な肺イメージング技術のユニークな配列で構成されています。 129XeがMR造影剤として最近FDAに承認され、研究機関や臨床機関の間で 129Xe MRIへの関心が高まっていることを考えると、施設間の技術標準化はますます重要になっています。 129Xe MRI Clinical Trials Consortium(Xe MRI CTC)のメンバーは、 129Xe MRIワークフローの主要な側面のそれぞれについてベストプラクティスに合意しており、これらの推奨事項は最近の出版物にまとめられています。この研究は、Xe MRI CTC の推奨事項に従って、肺換気の 129枚の Xe MR 画像を収集するためのエンドツーエンドのワークフローを開発するための実用的な情報を提供します。MR 研究のための 129Xe の準備と投与について議論し、実証し、研究全体および個々の MR スキャンの適切なガス量の選択、個々の 129Xe 用量の準備と送達、および研究中の被験者の安全性と 129Xe 忍容性を監視するためのベスト プラクティスなどの特定のトピックを使用します。また、パルスシーケンスタイプと最適化されたパラメータ、 129Xeフリップ角度と中心周波数のキャリブレーション、 129Xe MRI換気画像解析など、MRの主要な技術的考慮事項についても説明します。
概要
過偏波129Xe MRIは、肺機能の特定の側面の非侵襲的で空間的に分解された特性評価と定量化のためのエキサイティングなツールです1,2,3。解剖学的陽子線MRIで使用されるものと同様の取得および再構成アプローチにより、肺に吸入された129Xeの画像が得られ、非換気肺領域の視覚化と換気分布の領域分解定量化が可能になります4,5,6,7,8.より高度なパルスシーケンスと分析技術により、分光MRIによる肺胞と肺毛細血管間のガス交換効率の定量化9,10,11,12,13や、拡散強調MRIによる肺胞微細構造の完全性の特性評価14,15,16など、さらに補完的な情報が得られます。
吸入された129Xeは、肺疾患のある被験者を含む成人および小児被験者において安全で忍容性が高いことが証明されています17,18。129回のXe MRIによる肺機能の測定では、慢性閉塞性肺疾患6,10,19、嚢胞性線維症20,21,22、特発性肺線維症23,24,25、喘息7,10など、多くの肺疾患の状況における構造的および機能的変化に対する感受性が示されています、26。129Xe MRIの高い安全性と忍容性を考えると、他の一般的なイメージングアプローチと比較してMRIには電離放射線がなく、129Xe MRIの結果の高い再現性27,28、129Xe MRIは、特に慢性肺疾患の経時的な治療を受けている個人の正確な連続モニタリングに大きな期待が寄せられています。
129Xe MRIの安全性と臨床的有望性により、2022年12月に12歳以上の29歳の人を対象とした肺換気画像検査のFDA承認に至りました。このため、今後数年間で、129回のXe MRIを実施できる研究施設や臨床施設(現在、世界中で~20施設)が大幅に増加すると予想されます。129Xe MRIが新しい施設に広がるにつれて、施設が臨床的に関連性のある129Xe MRI技術を迅速に構築し、スキャンを実行して既存の施設と密接に比較できる結果を生成できるようにするための堅牢な方法論リソースが存在することが重要です。
この作業では、129Xe MRI 臨床試験コンソーシアム (Xe MRI CTC) のメンバー機関によって合意され、最近のポジションペーパー 30 に要約された、肺換気のヒト過分極 129Xe MRI の現在のベスト プラクティスを概説します。トピックには、完全な 129Xe MRI ワークフローに最適なカスタマイズされたパルス シーケンスの準備、過偏波 129Xe ガスの準備と投与、ヒト 129Xe MRI セッション用に最適化されたワークフロー、および MRI セッション中の被験者の安全性と快適性を監視するためのベスト プラクティスが含まれます。
プロトコル
ヒトを対象とするすべての研究は、治験審査委員会(IRB)の承認を受ける必要があります。規制当局が承認した 129Xe MRIの臨床使用には、IRBの関与は必要ありません。調査研究に参加する前に、将来の被験者には承認されたインフォームドコンセント文書を提供する必要があります。同意を得る人は、研究の目的、手順、利点、およびリスクを含む文書の内容を説明し、質問に答える必要があり、インフォームド コンセント文書の被験者の署名によって文書化されたように、研究を進めるために被験者から同意を得る必要があります。小児被験者またはその他の特別な状況の場合、同意を得るための承認された慣行に従う必要があります。.以下に説明するプロトコルは、バージニア大学のIRBのガイドラインに従っており、この原稿の症例例の被験者は、バージニア大学IRBが承認した同意書(IRB 13647、16215、16885、19569)に署名しています。
1. 129Xe MRIのハードウェアとパルスシーケンスの準備
注:ステップ1のプロトコルステップは、ヒト被験者をスキャンする前に実行する必要があります。科目ごとに繰り返す必要はありません。
- MRIスキャナーが 129Xeを含む多核操作に対応していることを確認します。
- 必要に応じて、専用のコイルとスキャナーのインターフェースボックスを使用して、 129Xe無線周波数(RF)コイルをMRIスキャナーに接続できることを確認します。
- スキャナーの製造元から要求されている場合は、 129Xe RFコイルをMRIスキャナーに接続するための適切なソフトウェア(コイルファイルと呼ばれることが多い)がインストールされていることを確認します。
- 以下に説明するように、 129Xeおよび 1Hイメージング用のパルスシーケンスを準備します。
- 129Xeキャリブレーションでは、表1に示すパルスシーケンスパラメータを使用して、一連の自由誘導減衰(FID)を含む局在しない分光シーケンスを準備します。
注:~218 ppm(溶存相周波数)で取得したFIDは、主に溶存相129Xe MRIのパラメータを決定するために使用されますが、本研究では説明しません。ただし、これらのパラメータは、あらゆるタイプの 129Xe MRI スキャンで十分な単一の標準化された 129Xe キャリブレーションを開発できるように与えられています。さらに、129Xe換気画像のみを含む研究の場合、サイトが十分な経験を積めば、個別のキャリブレーションスキャンは必要ない場合があることに注意してください。129Xeの動作周波数は、スキャナが決定した1H周波数を129Xeと1Hのジャイロ磁気比の比でスケーリングすることで正確に推定でき、蓄積された経験と被験者の重量に基づいて送信機のキャリブレーションを推定できます。 - 129Xe換気MRIでは、表2に示すパルスシーケンスパラメータを使用して、2次元(2D)RFスポイドグラジエントエコーシーケンスを準備します。129Xeがターゲット核として選択されていることを確認します。
- 従来の 1時間解剖学的 MRI では、 表 2 に示すパラメーターを使用して、シングルショットのターボ/高速スピンエコーシーケンスまたは RF スポイルドグラジエントエコーシーケンスを準備します。
注: 129Xe換気および 1H解剖学的シーケンスの場合、FOVとスライス数は被験者固有です。これらのパラメータは、スキャンセッションの開始時に、3次元すべてで肺を完全にカバーするように選択してください。- 位相オーバーサンプリングを有効にして、イメージングFOVへのアームのエイリアシングの可能性を軽減します。
- MRIスキャナーのベンダーの制限により、推奨される粗い面内分解能(4 mm x 4 mm)でのシングルショットターボ/高速スピンエコーシーケンスの動作が妨げられる場合があります。その場合は、目的の分解能の整数係数である分解能を使用します(例:2 mm x 2 mm)。
注: 1Hの解剖学的スキャンは、2D RFスポイルドグラジエントエコーシーケンスを使用して取得することもできます。この場合、 表2 に示した換気スキャンパラメータと同じパラメータを使用しますが、位相オーバーサンプリングを有効にして、アームがイメージングFOVにエイリアシングしないようにします。
- 129Xeキャリブレーションでは、表1に示すパルスシーケンスパラメータを使用して、一連の自由誘導減衰(FID)を含む局在しない分光シーケンスを準備します。
- 129Xeスキャンの場合は熱偏光129Xeファントム31、1Hスキャンの場合は1Hファントムのスキャンを実行して、上記のRFコイルとパルスシーケンスの動作を確認します。
| パラメーター | キャリブレーション | ||
| TRの | 15ミリ秒 | ||
| TE (テ) | 0.45 ms(3 T)、0.8 ms(1.5 T) | ||
| RFパルス | ウィンドウ sinc | ||
| RF持続時間 | 0.65-0.69 ms(3 T)、1.15-1.25 ms(1.5 T) | ||
| フリップ角度 | 20° | ||
| RF周波数 | 218ppm(溶存相)、0ppm(気相) | ||
| 滞留時間 | 39マイクロ秒 | ||
| 帯域幅 | 25.6 kHzの | ||
| いいえ。サンプル数 | 256 (使用する場合、オーバーサンプリングは含まない) | ||
| 読み出し期間 | 10ミリ秒 | ||
| FID の数 | 1ノイズ(RFなし)、溶存相周波数で499、気相周波数で20 | ||
| グラデーションの台無し | 少なくとも15 mT/m-msのモーメント(各軸、各FIDの後) | ||
| 期間 | ~8秒 | ||
表1: 129Xeキャリブレーションに推奨されるパルスシーケンスパラメータ。 パラメータは、局在しない分光 129Xe キャリブレーションパルスシーケンスについて示されています。
| パラメーター | 換気 | 解剖 学 的 |
| シーケンスの種類 | RFスポイドグラジエントエコー | 単発ターボ/高速スピンエコー |
| TRの | <10ミリ秒 | 無限 |
| TE (テ) | <5ミリ秒 | <50ミリ秒 |
| エコースペーシング | 該当なし | 3-5ミリ秒 |
| 励起反転角度 | 8-12° | 90° |
| 反転角度の焦点を合わせ直す | 該当なし | ≥90°(SAR制限内で許容される最高) |
| スライスの厚さ | 15ミリメートル | 15ミリメートル |
| スライスギャップ | 何一つ | 何一つ |
| スライスの向き | コロナ | コロナ |
| スライスの順序 | シーケンシャル(前方から後方) | シーケンシャル(前方から後方) |
| 位相符号化順序 | シーケンシャル (左から右) | シーケンシャル (左から右) |
| NEXの | 1 (部分フーリエの 7/8 まで可) | ハーフフーリエ |
| 非対称エコー | 許可 | 該当なし |
| ボクセル サイズ | 4 x 4 x 15 mm3 | 4 x 4 x 15 mm3 |
| エコーごとのサンプリング時間 | 5-7ミリ秒 | 1-1.5ミリ秒 |
| スキャン期間 | 8-12秒 | ≤16秒 |
表2:129Xe換気および1H解剖学的イメージングに推奨されるパルスシーケンスパラメータ。129Xe換気イメージング用の2D RFスポイテッド高速グラジエントエコーシーケンス(1列目)と、1H解剖学的イメージング用の2Dシングルショットターボ/高速スピンエコーシーケンス(2列目)のパラメータが与えられています。解剖学的スキャンは、2D RFスポイドグラジエントエコーシーケンスを使用して取得することもできます。この場合、ここで示す換気スキャンパラメータと同じパラメータを使用しますが、必要に応じて位相オーバーサンプリングを追加して、イメージングFOVへのアームのエイリアシングを回避します。また、受信機の帯域幅を指定する方法はスキャナーの製造元によって異なりますが、エコーごとの特定のサンプリング時間から、どのスキャナーの製造元でも正しい値を計算できることに注意してください。
2. 129Xe MRIの候補のスクリーニングと準備
- MR安全フォームで調査することにより、将来の被験者にMRIの禁忌がないことを確認します。 補足ファイル1 は、バージニア大学で使用されているフォームの例を示しています。
- -将来の被験者が 129Xe MRI検査に固有の除外基準を満たしていないことを確認してください これには、予測されるFEV1 の割合が25%未満、過去6週間以内の非代償性呼吸器状態、胸囲が 129Xe RFコイルの内周よりも大きい、および不安定な心臓病の病歴が含まれますが、これらに限定されません。
注:即時の除外を示すものではないが、慎重な個々の検討を必要とする追加の基準には、ベースラインでの有意な酸素補給の必要性が含まれます(つまり、鼻カニューレによる3 L / minを超える)およびベースライン異常を伴う神経障害の病歴。 - 画像検査中に肺拡散検査(DLCO)または肺活量測定を実施する場合は、被験者に研究訪問当日に炭酸飲料を摂取しないように指示します。被験者が処方された呼吸器薬を使用する場合、研究プロトコルで指定されている場合は、服用を遅らせるか控えるように指示します。
3.過分極129Xe用量の調製
注意: 129Xe偏光子および偏光測定ステーションの詳細な手順は、各ベンダー独自のものであり、固有です。以下の説明は、一般的なスピン交換光ポンピング 129Xe偏光子の動作に関する基本的な要約を含む。
- 被験者の線量を決定します。一般に、すべての被験者に 1 L の総線量が選択され、この総線量量は 129Xe MRI の FDA ラベルに指定されています。ただし、現在のXe MRI CTCの推奨事項30は、総線量(キセノンと窒素またはヘリウムのいずれか)を対象とすべきであることを示唆しています 各被験者が吸入するガスの快適な量を確保し、被験者間の肺容積差に関連する影響を最小限に抑えるために、被験者の強制肺活量(FVC)の1/5を目標とする必要があります。
- 被験者の最近のスパイロメトリー結果が利用可能な場合は、これらを使用してFVCの1 /5を決定します。肺活量測定の結果が利用できない場合は、身長、性別、および人種に基づいて被験者の総肺活量(TLC)を推定し、総線量をTLCの1 /6と推定します。
- 分極するキセノンガスの量を決定します。
注:各用量バッグの目標キセノン容量は、用量当量(DE)容量として示され、概念的には100%濃縮、100%分極された 129Xeガスの等価体積を示します。概念的には、DEボリュームは 129Xeスキャンの予想される信号対雑音比(SNR)に正比例し、推奨されるDEボリュームは、特定の 129Xeスキャンタイプに必要なS/N比に基づいて大きくなったり小さくなったりします。- 所与のキセノン線量のDE体積を次のように計算する32。
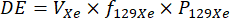
ここで、 VXe は線量中のキセノンガス( 129Xeだけでなく、すべての同位体)の総量であり、 f129Xe は 129Xe同位体濃縮度であり、 P129Xe は 129Xe分極である。 - 実行する 129個の Xe スキャンのセットに必要な DE ボリュームの合計を選択します。個々のキャリブレーションおよび換気スキャンに推奨されるDE容量は75〜150 mLです。
注: 換気イメージングでは、換気された画像ボクセルと換気されていない画像ボクセルを確実に区別するのに十分な SNR が必要です。50mLのDE容量は、少なくとも20の期待されるSNRを達成するための換気画像30 の絶対最小値と考えられる。キャリブレーションスキャンでは、気相信号のみがキャリブレーションされる場合は、25 mL という低い DE 容量が許容される場合があります。気相と溶存相の両方のシグナルを校正する場合は、少なくとも 75 mL を使用する必要があります。
- 所与のキセノン線量のDE体積を次のように計算する32。
- 必要な総 DE 体積、既知の 129Xe のキセノン ガス等方性濃縮度、および以前の偏光実行に基づいて推定 された 129Xe 分極を使用して、分極に必要なキセノン ガスの総体積を計算します。 129Xe同位体濃縮率85%、偏光率20%と仮定した場合の1回の換気スキャン(DE容量 = 75 mL)の計算例を以下に示します32。
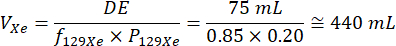
各キセノン用量に対してこの計算を実行して、各用量バッグに分配する分極キセノンガスの正しい量を決定します。.- BMI(<21)が低い被験者は、他の被験者よりも 129Xe吸入後に中枢神経系(CNS)に深刻な影響を与えるリスクが高くなります。低BMIの被験者を画像化する前に医師に相談し、これらの潜在的な問題を回避するために 129回のXe用量を最小限に抑えることを検討してください。.
- 129Xe偏光板は、偏光板メーカーが提供するすべての指示に従って準備します。
- 偏光子のベンダーに応じて、手順には次のものが含まれる場合があります。 ヘルムホルツコイル電源がオンになっていることを確認します。アウトレットマニホールドを排気して、不純物を取り除きます。冷たい指の周り/下に液体窒素デュワーを設定します。レーザーの電源をオンにして、ウォームアップします。オーブンへの空気の流れをオンにし、オーブンコントローラーを使用してオーブンを適切な温度に設定し、オーブンを温めます。
注意: 液体窒素は、皮膚、目、または衣服に接触すると重度の凍傷を引き起こす可能性があり、高強度レーザー光線は、保護せずに目に衝突すると、目の怪我を引き起こす可能性があります。適切な注意を払い、必要に応じて保護具を着用してください。
- 偏光子のベンダーに応じて、手順には次のものが含まれる場合があります。 ヘルムホルツコイル電源がオンになっていることを確認します。アウトレットマニホールドを排気して、不純物を取り除きます。冷たい指の周り/下に液体窒素デュワーを設定します。レーザーの電源をオンにして、ウォームアップします。オーブンへの空気の流れをオンにし、オーブンコントローラーを使用してオーブンを適切な温度に設定し、オーブンを温めます。
- 129Xe偏光測定ステーションの電源がオンになっていて、ソフトウェアが線量偏光を測定する準備ができていることを確認します。
- 過偏波 129Xe の収集を開始するには、次の手順を実行します。
- 冷たい指の加温ジャケットへの窒素の流れを開始します。
- キセノン混合物を冷たい指に流し始めます。偏光子のマニュアルの偏光子性能曲線を参照して、最適な流量を選択してください。
- 冷たい指の周りのデュワーに液体窒素を加えます。
- 偏波開始時間をデータシートに記録して、正確な偏波量を確保します。
- 収集が開始されたら、流量と温度を一定に保つようにフローコントローラーとオーブンコントローラーを調整し、必要に応じて液体窒素を追加してデュワーを満タンに保ちます。
- キセノンの蓄積中は、偏光子出口マニホールドを使用してバッグを少なくとも3回パージおよび排気を繰り返して、バッグ内の不純物および/または脱分極ガスを最小限に抑えることにより、線量収集用のテドラー用量バッグを準備します。
- 所望の過偏光 129Xe ボリュームの収集に適切な時間が経過したら、偏光子のドキュメントの指示に従って過偏光 129Xe 収集を終了します。
- 以下に説明するように、冷たい指に沈殿した凍結した 129Xeを解凍します。
- 129Xe用量バッグをアウトレットマニホールドのキセノンアウトレットに取り付けます。.
- 液体窒素デュワーを慎重に除去し、室温の水が入った解凍容器と交換します。
- 解凍中は、圧力を継続的に監視し、圧力が偏光子のドキュメントに記載されているしきい値に達したら、冷たい指からキセノン出口までフローバルブを開き、圧力が下がったらバルブをすばやく閉じます。
- このようにして、昇華したキセノンガスを投与バッグに投与し続け、投与バッグ内のキセノンの所望の量に達するまで投与する。
- 緩衝ガス(窒素またはヘリウム)を以前にバッグに添加していない場合は、この時点で追加します。
- 必要なキセノンガスと緩衝ガスをすべてバッグに加えたら、バッグチューブのピンチクランプをすばやく閉じ、キセノン出口バルブを閉じ、全用量バッグを偏光子から取り外します。
- 129Xe偏光測定ステーションのヘルムホルツコイルペアによって生成される磁場にバッグをすぐに移動します。
注意: キセノンガスが温められて昇華すると、冷たい指に圧力が急速にかかり、圧力が安全限界を超えて上昇すると、爆発の危険性が生じます。偏光子のドキュメントに記載されているこの手順の指示に正確に従い、この手順を実行する間は目の保護具を着用してください。
- 偏光測定ステーションのベンダーが提供する指示に従って、 129Xe偏光測定ステーションで各線量バッグの偏光を測定して記録します。
- 偏光が測定されたら、被験者に線量を投与する準備ができるまで、偏光測定ステーションのヘルムホルツコイルペアによって生成された磁場に 129個のXe線量バッグを保管します。
4.被験者のスキャン前の準備とコーチング
注:被験者が6分間の歩行テストを含む完全な検査を受ける場合は、129Xe MRIの結果に影響を与える可能性のある方法で被験者を疲労させないように、129Xe MRIが完了するまで歩行を行わないことをお勧めします。これは、心肺疾患の患者に特に関連しています。
- 被験者がステップ2で説明したように、すべての訪問前の指示を正しく実行したこと、および被験者がスクリーニングされてから、研究除外基準を満たしたり、MRI禁忌を構成したりする健康上の変化が発生していないことを確認します。
- 心電図(ECG)を含む、被験者に必要なすべての身体検査を実行します。体温、心拍数、呼吸数、血中酸素飽和度(SpO2)、血圧などのバイタルのコレクション。肺活量測定;そしてDLCOテスト。
- これらのテストを監視して、低SpO2 (<92%)、血圧の上昇、または被験者の既存のベースラインからのテスト結果の大幅な逸脱など、潜在的な警告サインがないか確認します。
注:これらの読み出し、特にベースラインSpO2は、129Xe吸入中に軽度の過渡的な酸素飽和度低下が発生することが予想されるため、チェックされます。ベースラインのSpO2<92%またはその他の警告サインがある被験者の場合、医師に相談して、被験者が129Xe MRI検査に適しているかどうか、および129Xe吸入の間に補助O2を使用するかどうかを確認してください。. - 以下に説明するように、正しい 129Xe吸入手順で被験者を指導します。
- 被験者がスキャナーの外で練習できるように、空気の入ったテドラーバッグを1つ以上用意します。実際の研究中にバッグから吸入されるキセノンとバッファーガスの総量と一致する空気量を使用してください。
- 息止めスキャン中に被験者が着用するノーズクリップを準備します。息を止め始める前に、ノーズクリップを被験者の鼻に取り付けます(練習用と実際のスキャン用の両方)。
- 以下の手順に従って、試行ごとに空気で満たされたバッグを1つ使用して被験者を指導します。被験者は、機能的残存容量の目標量からバッグの吸入を開始する必要があります。以下の手順の間、被験者の胸部を監視して、被験者が与えられた指示を実行していることを確認します。
- バッグを用意しますが、まだ被験者に投与しないでください。被験者に次のことを尋ねます:定期的に息を吸い込みます。息を吐き出してください。定期的に息を吸い込みます。息を吐き出してください。
- テドラーバッグに取り付けられたチューブを被験者の口に入れます。被験者が吸い込める場所にバッグを持ち、バルブを開きます。被験者に「息を吸う」と尋ねます。吸い込む。吸い込む。
- 被験者が袋の中身全体を吸い込んだら、被験者に次のことを尋ねます:息を止めてください。ただちにスキャナーオペレーターに「Go!
注意: 被写体をスキャンする場合、スキャナーのオペレーターは、Go!この指示は被験者を対象としたものではありませんが(つまり、直前に指示されたとおりにじっと息を止め続ける必要があります)、スキャンが差し迫っていることを被験者に警告します。 - スキャンが終了するのを待つか、練習中は、一般的な 129Xeスキャンが経過するのに必要なおおよその時間である10〜15秒のカウントで待ちます。
- 被験者に「呼吸をしてください」と尋ねます。この時点で被験者は息を吐きます。この時点で何度か深呼吸をしたり吐いたりするように被験者を指導し、肺から 129Xeをより早くクリアし、通常の酸素飽和度に早く戻るようにします。
- 被験者がこれらの指示を確実に実行できることを確認します。ガスの全量を吸い込むことができない被験者、息を止めることができない被験者、またはテスト中の息止めの試み中に持続的に咳をする被験者を除外することを検討してください。
注意: このテストの結果は、予想される画像品質を判断するために重要です。信頼できる被験者のコンプライアンスに関するこのチェックは、小児画像および重度の肺疾患の画像診断のコンテキストで特に重要であり、これらのカテゴリのいずれかまたは両方の被験者は、必要な息止めを確実に完了するのに苦労する可能性が高くなります。
5. MRIスキャナー室の準備とスキャナー患者テーブルへの被験者の位置決め
- MRIスキャナー室に入る人、または入る予定の人(被験者および職員)は、スキャナー室に入る前に、ポケットや人からすべての金属および/または電子物を取り除いてください。
- 129Xeベストコイルをスキャナーに差し込み、MRIスキャナーの患者テーブルに置いて準備します。
- 被験者に、足が先の仰臥位(またはスキャナー室のレイアウトに適している場合は頭が先の仰臥位)で患者テーブルに横になるように指示します。被験者と相談して、被験者の頭、膝などの下に枕を置き、被験者が検査中に快適に横になれるようにします。
- 129Xeベストコイルを被験者の胸に固定します。肺の末梢での信号の減少を避けるために、頭足方向のコイルの正中線が被験者の肺の予想される正中線にできるだけ近いように、快適な肺膨張レベルで目指す。
注意: コイルを被験者の足の方向に置きすぎるのはよくあるエラーです。上記のようにコイルを配置すると、コイルが素朴に予想するよりも被験者の頭部に近づく可能性があります。さらに、被験者の胸の直径がこれを必要とする場合、被験者の腕を頭の上に配置し、コイルの外側に配置する必要があるかもしれません。このポジショニングが必要な特定の胸部直径は、特定のスキャナーとコイルのハードウェアによって異なります。小柄な被写体の場合、アームは頭の上とコイルの外側、またはコイルの側面と内側に配置できます。 - MRIスキャナー室の患者テーブルの隣にMRIセーフパルスオキシメータを設置し、パルスオキシメータプローブを被験者に接続します。パルスオキシメータが正しく読み取っていることを確認します。
- 被験者の鼻に鼻カニューレを置き(または、健康な被験者の場合は、スキャナールームに待機させます)、被験者のSpO2 が10%以上低下した場合に使用する酸素源に接続します 用量吸入後2分以上。酸素ボンベとレギュレーターは、地域の安全ポリシーに基づいてMRセーフな方法で、手の届く距離内に配置してください。
- 患者テーブルをMRIスキャナーに進め、コイル/被験者の肺の正中線をスキャナーの等中心に合わせます。
6.スキャン手順
- MRIスキャナーのユーザーインターフェースで、被験者データを入力し、以前に準備した(ステップ1で説明した) 129Xe MRIプロトコルを開きます。
- 129 Xeの分極率を最小限に抑えるために、129Xe線量がステップ3の説明に従って調製され、129Xe線量バッグが偏光測定ステーションのヘルムホルツコイルペア(または同等のデバイス)によって生成された磁場内にあることを確認してください。
- 以下で説明するように、ベンダーが提供する標準プロトコル(3面ローカライザーなど)を使用して、 1時間ローカライザースキャンを実行します。
- 被験者に快適で自然な息を吸い込み、息を止めるように指示します。被験者が息を止めている間に、ローカライザースキャンを実行します。
- ローカライザースキャンの結果をMRIスキャナーインターフェースで表示します。画像にアーティファクトが見られる場合(金属を含む衣服が取り除かれていない場合など)は、問題を解決し、ローカライザーを繰り返します。ローカライザの FOV が被写体の中心に収まらない場合は、被写体の位置を変えて繰り返します。受け入れ可能なローカライザー イメージを取得したら、次の手順に進みます。
- 以下で説明するように、 129Xeスキャンの初期スキャン前調整を実行します。
- ローカライザからの 1H の中心周波数を 3.61529 (1H と 129Xe のそれぞれのジャイロ磁気比の近似比) で割って、初期 129Xe の中心周波数を設定します。
- 129Xe送信機の初期設定は、同様の身体ハビトゥスを持つ以前の被験者からのキャリブレーション結果、1H基準電圧に基づくスケーリング、または被験者の測定体重に基づいて設定します。129Xe送信機設定の詳細は、スキャナーおよび129Xeコイルの製造元に固有です。
- スキャナーのデフォルトのシム設定を、 129Xeの取り込みすべてに使用します。
- 上記のスキャン前の調整を行った後、 129Xeキャリブレーションスキャンを取得して、以下で説明する ように129Xeの中心周波数と送信機の設定を見つけます。
- 準備したプロトコルから 129Xe キャリブレーションシーケンスをロードします。すべてのパルスシーケンスパラメータが希望どおりであることを確認し、ワンクリックでスキャンを実行できるようにスキャン実行設定を設定します。
- 129Xeキャリブレーションスキャン用の129Xe線量バッグを偏光測定ステーションからスキャナールームに持ち込みます。被験体の近くに線量バッグを準備できるように保持または置きます。磁界強度が急激に変化するボア開口部付近の領域は避けてください。
- ステップ4で概説された誘導された吸入手順に従って、被験者がバッグから 129Xe用量を吸入するのを支援します。
- Execute the scan immediately upon hearing Go!被験者を支援する個人によって合図されます。
- スキャンが進行している間、被写体を監視します。被験者が目に見えて息を吐いたり、咳をしたり、動いたりする場合は、可能であればスキャンを繰り返してください。
- スキャンが終了したらすぐに、被験者に息を吐き出し、自由に呼吸するように指示します。
- スキャン後、パルスオキシメータを使用して被験者の心拍数とSpO2 を監視し、被験者との口頭でのコミュニケーションを介して一時的な中枢神経系の影響(めまい、立ちくらみ、陶酔感、感覚異常など)を監視します。
注:ほとんどすべての被験者は、ステップ3.2で言及されているように、体脂肪含有量が少ない被験者を除いて、介入を必要としない非常に軽度のCNS効果を経験します。 - ベースラインからの逸脱が消えるのを待ってから、さらに 129Xe用量を投与します。.ベースラインからの有意な逸脱が発生しない場合は、少なくとも2分待ってから、さらに 129Xe用量を投与します。.
注:酸素の脱飽和化と回復の典型的な時間経過は次のとおりです:脱飽和は 129Xe吸入を完了してから10〜20心拍で始まり、吸入完了後20〜30心拍で最下点が発生し、吸入が完了してから45〜50心拍以内に回復します。ほとんどの不飽和度は 、129Xe吸入から30秒以内に解消し、通常は2分以内に完全に解消すると予想されます。持続的な不飽和度(被験者ベースラインの10%以上)が2分を超えて続く場合は、それ以上の 129回のXe投与を避けたり、研究を終了したりすることをお勧めします。.
- 以下で説明するように、 129Xeキャリブレーション分析を実行します(たとえば、スタンドアロン分析ツールを使用)。
- 最初の気相 FID のスペクトルを使用して 129Xe の中心周波数を決定します。
- 129Xe送信機の調整を以下の手順で決定します。
- 20 個の気相 FID のピーク強度を次の関数30 に当てはめ、反転角 α を解きます。
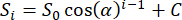
ここで、Siはi番目の励起から生じる信号強度の大きさであり、S0は最初の励起からの信号強度の大きさであり、Cはノイズオフセットパラメータである。 - αが得られたら、表1で推奨されているように、20°を意図したキャリブレーションフリップ角度として使用したと仮定して、後続のスキャンで129Xe送信機の初期設定を20°/αスケーリングします。
- 20 個の気相 FID のピーク強度を次の関数30 に当てはめ、反転角 α を解きます。
- 最終的な 129Xeスキャン前調整が行われ、被験者が次の 129Xe投与の準備ができたら、以下に説明するように 129Xe換気スキャンを実行します。
- 準備したプロトコルから 129Xe換気シーケンスをロードします。すべてのパルスシーケンスパラメータが希望どおりであることを確認し、1回のクリックですぐにスキャンが開始されるようにスキャン実行設定を設定します。
- ローカライザーの結果に基づいて、FOV サイズと中心位置を選択します。視野の中心が3次元すべてで肺の中心と一致することを目指し、視野が両方の肺全体を含む胸腔全体を快適に収容するのに十分な大きさになることを目指します。
- 偏光測定ステーションから129Xe換気スキャン用の129Xe線量バッグをスキャナー室に持ち込みます。被験体の近くに線量バッグを準備できるように保持または置きます。磁界強度が急激に変化するボア開口部付近の領域は避けてください。
- ステップ4で概説された誘導された吸入手順に従って、被験者がバッグから 129Xe用量を吸入するのを支援します。
- Execute the scan immediately upon hearing Go!被験者を支援する個人によって合図されます。
- スキャンが進行している間、被写体を監視します。被験者が目に見えて息を吐いたり、咳をしたり、動いたりする場合は、可能であればスキャンを繰り返してください。
- スキャンが終了したらすぐに、被験者に息を吐き出し、自由に呼吸するように指示します。
- スキャン後、パルスオキシメータを使用して被験者の心拍数とSpO2 を監視し、被験者との口頭でのコミュニケーションを介して一時的な中枢神経系の影響(めまい、立ちくらみ、陶酔感、感覚異常など)を監視します。
- ベースラインからの逸脱が消えるのを待ってから、さらに 129Xe用量を投与します。.ベースラインからの有意な逸脱が発生しない場合は、少なくとも2分待ってから、さらに 129Xe用量を投与します。.
- 以下に説明するように 、1時間の解剖学的スキャンを実行します。
- 準備したプロトコルから 1Hの解剖学的配列をロードします。すべてのパルスシーケンスパラメータが希望どおりであることを確認し、ワンクリックでスキャンを実行できるようにスキャン実行設定を設定します。
- 空気で満たされ、 129Xe換気スキャンに使用される線量バッグの容量に合わせた線量バッグをスキャナー室に持ち込みます。
- ステップ4で概説された誘導された吸入手順に従って、被験者がバッグから空気線量を吸入するのを助けます。
- Execute the scan immediately upon hearing Go!被験者を支援する個人によって合図されます。
- スキャンが進行している間、被写体を監視します。被験者が目に見えて息を吐いたり、咳をしたり、動いたりする場合は、可能であればスキャンを繰り返してください。
- スキャンが終了したらすぐに、被験者に息を吐き出し、自由に呼吸するように指示します。
7. スキャン後の手順
- スキャン手順の前と同じ方法で被験者のバイタルを測定します。バイタルが異常になった場合は、出発する前に、30〜60分、および/またはバイタルがベースライン近くに戻るまで待つように被験者に指示します。
8. 129Xe MRI換気データの解析
注:取得した 129Xe換気画像と 1H解剖学的画像は、ベンダーのデフォルトの画像再構成パイプラインを使用して、MRIスキャナーコンピューターで自動的に再構築する必要があります。
- 129Xe換気と1Hの解剖学的スキャンを、許容される最小レベルの補間(理想的にはなし)を使用してDICOM画像ファイルとしてエクスポートします。
- 換気不良率(VDP)は、プログラミングまたは画像解析ソフトウェアで、次の式8を使用して計算します。
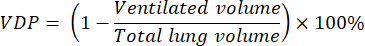
- 129のXe換気スキャンをセグメント化することにより、手動または既存の多くの自動アプローチの1つを使用して、換気量を決定します33。
注: 129Xe画像の2値化セグメンテーションの簡単な方法では、次のように定義されたしきい値を使用します8。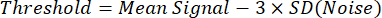
ここで、「平均信号」は、肺内の強い129Xeシグナルのユーザー定義の関心領域内の129Xe信号強度の平均であり、「SD(ノイズ)」は、肺または気管から遠く離れた視野の端付近の領域内の129Xe信号強度の標準偏差です。 - 1Hの解剖学的スキャンをセグメント化することにより、手動または既存の自動アプローチを使用して総肺容積を決定します34。
- これらのセグメンテーションが実行されたら、対応する体積を、セグメント化されたボクセルの数に画像ボクセルの体積を掛けた値として計算します(画像をDICOMファイルに変換するときに実行される補間を考慮します)。
- 129のXe換気スキャンをセグメント化することにより、手動または既存の多くの自動アプローチの1つを使用して、換気量を決定します33。
結果
図1 は、健康な人の代表的な換気と3面ローカライザーの画像を示しています。換気画像では、肺全体で高い 129Xe信号が観察され、この個人では換気障害は明らかではありません。
図2、 図3、 図4 は、罹患した個人の代表的な換気と解剖学的画像を示しています。
ディスカッション
上記の換気および解剖学的MRIアプローチは、実装のシンプルさを維持しながら、画質とSNRを最大化するように設計されています-これらのシーケンスプロトコルは、多核操作が有効になっていれば、一般にベンダー製品のパルスシーケンスから適応することができ、画像はスキャナーコンピュータ上で自動的に再構築されます。ここで説明する2Dアプローチの1つの欠点は、スライス選択的励起...
開示事項
著者のJ.F.M.、J.P.M.、およびY.M.S.は、Polarean, Inc.がサポートする臨床試験に参加しています。 著者のJ.F.M.、Y.M.S.は、Polarean, Inc.にコンサルティングサービスを提供しています(5000ドル未満)。著者J.P.M.がPolarean, Inc.から研究支援を受ける
謝辞
この研究は、米国国立衛生研究所(認可番号R01-CA172595-01、R01-HL132177、R01-HL167202、S10-OD018079、UL1-TR003015)およびシーメンスメディカルソリューションズから資金提供を受けました。
資料
| Name | Company | Catalog Number | Comments |
| 1.5T or 3T human MRI scanner | Siemens | MAGNETOM Symphony (1.5T) or Vida (3T); older models fine, as long as multinuclear option is/can be installed; scanners also available from GE and Philips | |
| 129Xe hyperpolarizer | Polarean | 9820 | |
| 129Xe MRI phantom | |||
| 129Xe MRI vest coil | Clinical MR Solutions | Also available from other vendors | |
| 129Xe polarization measurement station | Polarean | 2881 | |
| 1H MRI phantom | |||
| Coil file for 129Xe MRI vest coil | Also available from other vendors for their respective coils | ||
| ECG machine | |||
| Helium buffer gas | |||
| Interface box from coil to scanner | May be built into coil, but needs to be included separately if not | ||
| Liquid nitrogen | |||
| MRI-safe pulse oximeter | Philips | Expression MR200 | |
| Nitrogen buffer gas | |||
| PFT machine | |||
| Programming/image analysis software | MATLAB | R2023a | Various other options available |
| Pulse sequence design software | Siemens | IDEA software package; also available from GE and Philips for their respective scanners | |
| Scanner multinuclear option | Siemens | Scanner integrated hardware/software package; also available from GE and Philips for their respective scanners | |
| Tedlar gas sampling bags (500, 750, 1000, 1250, 1500 mL) | |||
| Xenon gas (129Xe isotopically enriched) |
参考文献
- Roos, J. E., McAdams, H. P., Kaushik, S. S., Driehuys, B. Hyperpolarized gas MRI: Technique and applications. Magn Reson Imaging Clin N Am. 23 (2), 217-229 (2015).
- Mugler, J. P., Altes, T. A. Hyperpolarized 129Xe MRI of the human lung. J Magn Reson Imaging. 37 (2), 313-331 (2013).
- Ebner, L., et al. The role of hyperpolarized 129xenon in MR imaging of pulmonary function. Eur J Radiol. 86, 343-352 (2017).
- He, M., Driehuys, B., Que, L. G., Huang, Y. C. T. Using hyperpolarized 129Xe MRI to quantify the pulmonary ventilation distribution. Acad Radiol. 23 (12), 1521-1531 (2016).
- Walkup, L. L., et al. Xenon-129 MRI detects ventilation deficits in paediatric stem cell transplant patients unable to perform spirometry. Eur Respir J. 53 (5), 1801779 (2019).
- Virgincar, R. S., et al. Quantitative analysis of hyperpolarized 129Xe ventilation imaging in healthy volunteers and subjects with chronic obstructive pulmonary disease. NMR Biomed. 26 (4), 424-435 (2013).
- Ebner, L., et al. Hyperpolarized 129Xenon magnetic resonance imaging to quantify regional ventilation differences in mild to moderate Asthma: A prospective comparison between semiautomated ventilation defect percentage calculation and pulmonary function tests. Invest Radiol. 52 (2), 120-127 (2017).
- Woodhouse, N., et al. Combined helium-3/proton magnetic resonance imaging measurement of ventilated lung volumes in smokers compared to never-smokers. J Magn Reson Imaging. 21 (4), 365-369 (2005).
- Mugler, J. P., et al. Simultaneous magnetic resonance imaging of ventilation distribution and gas uptake in the human lung using hyperpolarized xenon-129. Proc Natl Acad Sci U S A. 107 (50), 21707-21712 (2010).
- Qing, K., et al. Assessment of lung function in asthma and COPD using hyperpolarized 129Xe chemical shift saturation recovery spectroscopy and dissolved-phase MRI. NMR Biomed. 27 (12), 1490-1501 (2014).
- Cleveland, Z. I., et al. Hyperpolarized 129Xe MR imaging of alveolar gas uptake in humans. PLoS One. 5 (8), 12192 (2010).
- Wang, Z., et al. Using hyperpolarized 129Xe gas-exchange MRI to model the regional airspace, membrane, and capillary contributions to diffusing capacity. J Appl Physiol. 130 (5), 1398-1409 (2021).
- Guan, S., et al. 3D single-breath chemical shift imaging hyperpolarized Xe-129 MRI of healthy, CF, IPF, and COPD subjects. Tomography. 8 (5), 2574-2587 (2022).
- Ouriadov, A., et al. Lung morphometry using hyperpolarized (129) Xe apparent diffusion coefficient anisotropy in chronic obstructive pulmonary disease. Magn Reson Med. 70 (129), 1699-1706 (2013).
- Yablonskiy, D. A., Sukstanskii, A. L., Quirk, J. D., Woods, J. C., Conradi, M. S. Probing lung microstructure with hyperpolarized noble gas diffusion MRI: theoretical models and experimental results. Magn Reson Med. 71 (2), 486-505 (2014).
- Chan, H. F., Stewart, N. J., Norquay, G., Collier, G. J., Wild, J. M. 3D diffusion-weighted 129 Xe MRI for whole lung morphometry. Magn Reson Med. 79 (6), 2986-2995 (2018).
- Walkup, L. L., et al. tolerability and safety of pediatric hyperpolarized 129Xe magnetic resonance imaging in healthy volunteers and children with cystic fibrosis. Pediatr Radiol. 46 (12), 1651-1662 (2016).
- Driehuys, B., et al. Chronic obstructive pulmonary disease: safety and tolerability of hyperpolarized 129Xe MR imaging in healthy volunteers and patients. Radiology. 262 (1), 279-289 (2012).
- Myc, L., et al. Characterisation of gas exchange in COPD with dissolved-phase hyperpolarised xenon-129 MRI. Thorax. 76 (2), 178-181 (2021).
- Kaushik, S. S., et al. Measuring diffusion limitation with a perfusion-limited gas-Hyperpolarized 129Xe gas-transfer spectroscopy in patients with idiopathic pulmonary fibrosis. J Appl Physiol. 117 (6), 577-585 (2014).
- Dournes, G., et al. The clinical use of lung MRI in cystic fibrosis: What, now, how. Chest. 159 (6), 2205-2217 (2021).
- Thomen, R. P., et al. Hyperpolarized 129Xe for investigation of mild cystic fibrosis lung disease in pediatric patients. J Cyst Fibros. 16 (2), 275-282 (2017).
- Mammarappallil, J. G., Rankine, L., Wild, J. M., Driehuys, B. New developments in imaging idiopathic pulmonary fibrosis with hyperpolarized xenon magnetic resonance imaging. J Thorac Imaging. 34 (2), 136-150 (2019).
- Rankine, L. J., et al. 129Xenon gas exchange magnetic resonance imaging as a potential prognostic marker for progression of idiopathic pulmonary fibrosis. Ann Am Thorac. 17 (1), 121-125 (2020).
- Mata, J., et al. Evaluation of regional lung function in pulmonary fibrosis with xenon-129 MRI. Tomography. 7 (3), 452-465 (2021).
- Svenningsen, S., et al. Hyperpolarized (3) He and (129) Xe MRI: Differences in asthma before bronchodilation. J Magn Reson Imaging. 38 (3), 1521-1530 (2013).
- Stewart, N. J., et al. Comparison of 3He and 129Xe MRI for evaluation of lung microstructure and ventilation at 1.5T. J Magn Reson Imaging. 48 (3), 632-642 (2018).
- Hughes, P. J. C., et al. Assessment of the influence of lung inflation state on the quantitative parameters derived from hyperpolarized gas lung ventilation MRI in healthy volunteers. J Appl Physiol. 126 (1), 183-192 (2019).
- Polarean. . FDA Approves Polarean's XENOVIEWTM (xenon Xe 129 hyperpolarized) for use with MRI for the evaluation of lung ventilation. , (2022).
- Niedbalski, P. J., et al. Protocols for multi-site trials using hyperpolarized 129Xe MRI for imaging of ventilation, alveolar-airspace size, and gas exchange: A position paper from the 129Xe MRI clinical trials consortium. Magn Reson Med. 86 (6), 2966-2986 (2021).
- Bier, E. A., et al. A thermally polarized 129 Xe phantom for quality assurance in multi-center hyperpolarized gas MRI studies. Magn Reson Med. 82 (5), 1961-1968 (2019).
- He, M., et al. Dose and pulse sequence considerations for hyperpolarized 129Xe ventilation MRI. Magn Reson Imaging. 33 (7), 877-885 (2015).
- Tustison, N. J., et al. Image- versus histogram-based considerations in semantic segmentation of pulmonary hyperpolarized gas images. Magn Reson Med. 86 (5), 2822-2836 (2021).
- Tustison, N. J., et al. Convolutional neural networks with template-based data augmentation for functional lung image quantification. Acad Radiol. 26 (3), 412-423 (2019).
- Wild, J. M., et al. Comparison between 2D and 3D gradient-echo sequences for MRI of human lung ventilation with hyperpolarized 3He. Magn Reson Med. 52 (3), 673-678 (2004).
- Willmering, M. M., et al. Improved pulmonary 129 Xe ventilation imaging via 3D-spiral UTE MRI. Magn Reson Med. 84 (1), 312-320 (2020).
- Collier, G. J., et al. Single breath-held acquisition of coregistered 3D 129 Xe lung ventilation and anatomical proton images of the human lung with compressed sensing. Magn Reson Med. 82 (1), 342-347 (2019).
- Zha, W., et al. Semiautomated ventilation defect quantification in exercise-induced bronchoconstriction using hyperpolarized helium-3 magnetic resonance imaging: a repeatability study. Acad Radiol. 23 (9), 1104-1114 (2016).
- Ray, N., Acton, S. T., Altes, T. A., de Lange, E. E., Brookeman, J. R. Merging parametric active contours within homogeneous image regions for MRI-based lung segmentation. IEEE Trans Med Imaging. 22 (2), 189-199 (2003).
- Hughes, P. J. C., et al. Spatial fuzzy c-means thresholding for semiautomated calculation of percentage lung ventilated volume from hyperpolarized gas and 1 H MRI. J Magn Reson Imaging. 47 (3), 640-646 (2018).
- Tustison, N. J., et al. Ventilation-based segmentation of the lungs using hyperpolarized (3)He MRI. J Magn Reson Imaging. 34 (3), 831-841 (2011).
- Kanhere, N., et al. Correlation of lung clearance index with hyperpolarized 129Xe magnetic resonance imaging in pediatric subjects with cystic fibrosis. Am J Respir Crit Care Med. 196 (8), 1073-1075 (2017).
- Rayment, J. H., et al. Hyperpolarised 129Xe magnetic resonance imaging to monitor treatment response in children with cystic fibrosis. Eur Respir J. 53 (5), 1802188 (2019).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved