Method Article
眼窩骨折の3次元再構成
要約
軌道再建のための個別化医療は急速に発展しています。眼窩の繊細な性質のため、骨折再建後の小さな不一致は、視覚障害を引き起こす可能性があります。ここでは、軌道欠陥の仮想3D再構成のための3つの方法と、その適応症、および正しい再構成のための潜在的な落とし穴について説明します。
要約
眼窩骨折の再建は困難な場合があります。露出が限られていること、いくつかの壁の欠陥が関与していること、および可変の3次元(3D)解剖学的構造が、複雑なケースで優れた結果を達成することを困難にしています。眼窩欠損の再建に患者固有のインプラントを使用することは、大きな期待を示しています。それでも、このような場合には適切な仮想計画が重要であり、したがって、計画の構造とさまざまなオプションを理解することが不可欠です。このプロトコルでは、欠陥を再構築するための3つの方法を説明し、各方法の適応症について詳しく説明します。自動化されたコンピュータによる再構築は最も簡単な方法ですが、主に小さな欠陥に使用できます。骨折したセグメントの再配置は簡単で、骨折した壁の良好な解剖学的連続性をもたらしますが、粉砕されていない骨折が必要です。ミラーリングは、粉砕骨折で選択される方法です。この方法の欠点は、ミラーリング段階に続く広範な操作であるため、プランナーによる解剖学的構造と影響に対する高度な理解が必要であることです。方法の詳細な説明に続いて、再構築時に主な焦点となるべき解剖学的構造と見落とされている解剖学的構造が示されています。さらに、遭遇する落とし穴について説明し、議論し、それらを回避する方法も説明します。これらの方法は、社内で使用することも、外部に委託することもできますが、外科医が自分で計画を立てない場合でも、より良い結果を得るためには、それらを理解することが非常に重要です。
概要
3次元(3D)革命がピークを迎えています。私たちが使用している製品の多くは、3Dプリンターで作られています。医療では、この技術により、人為的ミス1を減らしながら優れた精度を実現できます。この品質は、精度が重要な外科分野で最も重要です。目は、機能的なニーズと美的知覚の両方にとって重要です2。軌道は7つの骨で構成される骨格腔であり、地球を保護します。骨の軌道は地球を保護し、支えています。神経、血管、筋肉、腺構造が含まれています。軌道の床は非常に薄く、ほとんどが上顎骨の軌道プロセスから構築されています。前外側では頬骨から構成され、後外側では眼窩床骨折3の重要なランドマークである口蓋骨から構成されている。内側眼窩壁は、前涙稜から眼窩頂点まで広がっています。パピラセア層は、内側壁の大部分を占めており、紙のように薄い骨で、簡単に骨折する可能性があります4。孤立した眼窩骨折は、すべての顔面骨折の4%〜16%を損ないます5。眼窩の骨折は、目の位置の変化を引き起こし、機能的な視覚障害と審美的障害の両方を引き起こす可能性があります6。骨の眼窩壁がわずかに動くだけでも、軌道体積と地球位置に大きな影響を与える可能性があります5。したがって、変位したまたは粉砕された眼窩壁を正確に再構築することが最も重要です。眼窩下神経の内側の眼窩底と内側壁はどちらも比較的薄く、眼窩への鈍的外傷4の間に容易に骨折する傾向があります。眼窩骨折の診断には、画像診断と身体検査が重要です。ほとんどの画像診断法には、コンピューター断層撮影(CT)の冠状切片が含まれます7。眼科医による損傷した眼窩の完全な評価が必要であり、視力、眼圧、眼球運動性、瞳孔検査、視野、細隙灯眼球検査、網膜検査、および外部検査が含まれます。この検査は、再建手術後にも実施する必要があります。過去には、眼窩欠損は骨移植片と後にチタンメッシュ7,8を使用して再建されました。経皮的または経結膜外科的アプローチを通じて骨移植片またはチタンメッシュを欠損に適合させることは、曝露が限られており、困難であったため、より正確な方法の必要性が生じました。チタンメッシュを事前に適応させるために3Dプリントモデルを使用して導入され9、続いて欠陥の正確な再構築のための患者特異的インプラント(PSI)が導入されました10。PSIは、整形外科、顎顔面外科、脳神経外科など、さまざまな外科分野でさまざまな目的で近年普及しています。骨折を減らすため、またはアブレーション手術の前にこの方法を使用することは、多くの場合簡単です。しかし、軌道上では、複雑な解剖学的構造と何度も粉砕された骨は、適切な再建を達成するために眼窩の解剖学的構造を深く理解する必要があります11。
最近、3D解析のための新しい方法を使用して、従来のアプローチとは対照的に、この方法の精度に関する研究が発表されました。その結果、PSIを再構成に使用すると、精度が2.7倍向上することが示されています。さらに、観察された長期的な合併症も少なかった。それでも、小さな間違いでさえ機能的および審美的な欠陥につながる可能性があることを認識することが重要です。したがって、軌道再構成11のすべての落とし穴に精通することが非常に重要です。この原稿では、軌道欠陥の仮想3D再構成に使用される3つの方法、それらの適応症、長所、短所について詳しく説明します。これにより、臨床医やエンジニアによる3D再構築のアウトソーシングを社内で行うだけでなく、監督することも可能になります。
プロトコル
このプロトコルは、Institutional Ethical Review Boardによって承認され、医療プロトコルと倫理に関するヘルシンキ宣言に従って実施されました。CT画像の使用について患者の同意が得られました
1. 軌道のセグメンテーション
注:このセクションは、D2Pソフトウェア(以下、セグメンテーションソフトウェアと呼びます)を使用して実行されます。
- 「 File」>「Add DICOM files 」をクリックして、患者の顔面骨CT画像DICOMファイルをソフトウェアにロードします(図2)。
注:DICOMスライスの厚さは1mm以上を推奨します。 - Coronal ビュー(右側の画面に表示)を選択し、[Add](追加)をクリックします(図3)。次の画面で [3D] をクリックして [Bone segmentation] インターフェースを開きます。
- 新しいマスクを作成します (セグメンテーション シーケンスの最初のステップ)。
- ボーンセグメンテーションインターフェースでは、3Dボリュームが左側の画面に表示され、冠状CTビューが右側に表示されます(図4)。下部ツールバーの左側にある Bone segmentation アイコンをクリックし、Thin bones を選択します。
- オービットと眼窩近傍領域の別々の領域をクリックし(これは左側のボリューム画面と右側のDICOM画面で実行できます)、選択した色(この例では緑)で完全なオービットが完全に定義されるまでクリックします(図5)。さまざまな DICOM 平面をスクロールして作成された [New Mask ] の精度を確認します。
注:不正確な選択が特定された場合は、元に戻す(Ctrl Z)し、この領域を別の空間位置で再選択できます。 細い骨 機能は、骨構造を検出するための最も低いしきい値を使用して、骨構造を軟組織から分離します。
- メッシュを作成します(セグメンテーションシーケンスの2番目のステップ)。最初の手順を完了して承認したら、ツールバーの [3D] をクリックします (図 6)。3Dモデル(メッシュ)の滑らかさとボイドがないことを十分に観察し、[File]>[Save > STL]をクリックして3DモデルをSTLファイルとして保存します(図7)。
注: 図8 と 図9 は、軌道床が粉砕されていない場合の追加のセグメンテーション方法である マルチスライス補間を示しています。 - 大きな粉砕骨折の場合は、前の手順に従って対側眼窩のモデルをセグメント化し、ミラーリング原理を実装することにより再建のガイドとして使用されます。
2. 軌道壁の再構築
注:このセクションは、Geomagic Freeform(以下、3D設計ソフトウェアと呼びます)を使用して実行されます。
- [ファイル]>[モデルのインポート]をクリックします。セグメンテーションシーケンスのステップ1.4でエクスポートしたSTLファイルを選択します。下部のツールバーの[詳細の追加]と[詳細の追加]をクリックします。次に、[Apply]をクリックします(補足図1)。
注:インポートされた作業モデルの表面は、滑らかさが増した( エッジシャープネスの値を低くする)非常に正確である必要があります。 - 骨折の解剖学的構造に基づいて、ステップ 2.3(自動再建)、2.4(解剖学的再配置)、および 2.5(ミラーリング)で説明されている次の 3 つの再建方法のいずれかを選択します。
- 自動再構築
注:これは、小さな欠陥や平坦で単調なトポグラフィーの領域に最適な方法です。- まず、欠陥の周囲の周囲の粘土の連続性を完全に実現します(補足図2)。破砕された床領域の周囲に小さな隙間が存在する場合 (白い矢印)、 粘土の追加 機能を使用してこれらの領域を手動で接続し、破砕周囲 (黒の矢印) の完全な連続性を実現します。
- [スムーズ] 機能を使用して、追加された粘土を滑らかにします。アクティブ化されたピースの New Mask を右クリックして、Clay Utilities/Copy to Mesh を選択します。
- メッシュツールを使用して、ギャップを自動的に埋めます(補足図3)。[Select Mesh Area] の下の軌道のメッシュ オブジェクトで、[なげなわ選択] ツールを使用して、フロア欠陥のマージンを選択します。
- キーボードの Delete キーを押します。 [メッシュの穴を埋める] を選択し、ボタンが非アクティブになるまで[ 埋める ]を回数だけクリックすると、床の欠陥が自動的に再作成されます。
- 最後のステップでは、メッシュを粘土に変換します。メッシュを右クリックし、[ Mesh Utilities] をクリックし、[ Copy to Clay] をクリックします。
- 解剖学的再配置
注:これは、破砕された床セグメントが全体のままで、元の地形の解剖学的構造を保持している場合に選択する方法です。- 2つの異なるSTL((i)軌道と(ii)粉砕されていない床セグメント)を異なるオブジェクトとしてインポートします(図8 および 図9)。
- セグメントを再配置します (補足図 4)。
- [Select/Move Clay] で [Reposition] ツールを選択し、[Move only] オプションの選択を解除します。解剖学的な無傷の境界線に合うように、床を手動で再配置します。
- または、断片化されたエッジの 1 つが正しい解剖学的位置に配置されている場合は、Select/Move Clay の Reposition origin ツールを使用します。
- [中心へ]をクリックし、トライアド(黒い矢印)をセグメントの解剖学的に正しいエッジにある回転の中心に移動します。「ピースを再配置」をクリックし、「回転のみ」を選択します。
- キーボードの Shift ボタンを押したまま、トライアドの中心を通ってピースを正しい解剖学的位置に回転させます。
注:解剖学的縮小により、欠陥は完全に完了する必要があります。それ以外の場合は、この方法を放棄し、次の再構築方法であるミラーリングを使用する必要があります。
- ミラーリング
注:これは、広範囲で粉砕された眼窩骨折で選択される方法です。- 2つの異なるSTLを異なるオブジェクトとしてインポートします:(i)フラクチャされた軌道と(ii)反対側の軌道。
- まず、無傷の軌道の鏡像を作成します。 ミラークレイ ツールを使用して、平面を内側に向けます( 補足図5Bの青い線)。 「Mirror Entire Piece and Preview」にチェックを入れ、「 Apply」をクリックします。
- 次に、ミラーリングされた軌道とフラクチャされた軌道を重ね合わせます(補足図6)。 [ピースの登録 ] ツールを使用して、ミラーされたオービットを [ソース ] として選択し、フラクチャされたオービットを [ターゲット] として選択します。
- ミラーされたオービット内の一意の解剖学的位置とフラクチャされたオービットの類似位置にマーカーを配置し、[ 適用 ]をクリックしてセグメントをスーパーインポーズします。「 自動 」をクリックして、最適な重ね合わせを行います。
注:重ね合わせられた鏡面軌道は、骨折した眼窩の解剖学的再構築のガイドとして機能します。
3. 再建された床面を基にした患者様専用のインプラント設計
注:このセクションは、3D設計ソフトウェアを使用して実行します。
- 軌道床面の準備(補足図7)
- [粘土を選択/移動]で、[原点を中央に再配置]>を選択します。座標系をミラー化された軌道床の中心に移動します。「回転のみ」を選択し、Z 軸を垂直に、X 軸を水平に、Y 軸を前後に配置します。
- Select/Move Clay で Reposition Piece を選択します。詳細設定の表示/非表示(Show/Hide Advanced Settings)を選択し、移動ステップ(Translate Step)を 0.8 mm に変更します。赤い長方形の矢印をクリックして、ミラー軌道を破砕軌道に沈め、破砕領域の無傷の境界が表示され始めるまで、ミラー軌道を亀裂軌道に沈めます。
- 緑色の長方形の下向きの矢印をもう一度クリックすると、ミラーリングされた軌道の床がさらに0.8mm沈みます。この深さはPSIの厚さと一致するため、元の床が再現されます。
- [Select/Move Clay] で [Select Clay] を選択し、[Lasso Select] ツールを使用します。床の解剖学的境界を選択します。[選択を反転] を選択し、残りを削除します。
注意: 床の境界を滑らかにするか、骨折した軌道の境界に合うように粘土を追加します。
- メッシュのアウトラインを作成します(補足図8)。
- オービット オブジェクトとフロア オブジェクトの両方を選択し、右クリックして[ ブール演算]または[新規として結合 ]を選択し、解剖学的に縮小された床とくぼんだ床を含むオービットの 1 つのオブジェクトを作成します。さらに時間で境界線を滑らかにします。
- 最終的なオブジェクトを複製します。右クリックして 「See Through」を選択し、「 Turn On」を選択します。 [カーブ]で [カーブを描画 ]を選択し、元のフラクチャ領域のすぐ周りでフォームのアウトラインを作成します。カーブはフラクチャされた軌道のエッジ上に置く必要があります。カーブは、新しく作成された床に載せることができるのは、骨の欠けている領域だけです。
- 輪郭が完全に描かれたら、[ 作成時に粘土に合わせる ] アイコンをクリックします。同様に、PSIのアンカーアームを作成します。
注:後縁は、後骨棚の上ではなく、連続して配置する必要があります(図1D)。メッシュの横方向の境界は、音の骨のエッジの上に載るように、欠陥を超えて最小限に拡張する必要があります。アンカリングアームを、下眼窩縁の明確に定義されたセグメント化された領域に配置します。重要なランドマークは常に避けることを忘れないでください。軌道への安全な解剖は、文献では31〜36mmの間で考えられていますが、ケースごとに調整された計画が推奨されます12,13。
- PSI を確定します (補足図 9)。
- [Detail Clay] で [Emboss With Curve] を選択し、距離を 0.8 mm から選択します。アウトラインで囲まれた領域の内側を選択し、[Raise] をクリックします。「粘土を追加」と「スムージング」を使用して、固定アームをインプラントの本体に接続します(補足図9B、黒矢印)。
- 複製されたオブジェクトから Boolean 関数と Remove From 関数を使用します。オブジェクトリストで、 Clay coarseness を右クリックして 0.1mmを選択します。 [スカルプト クレイ] で [Carve ] ツールを選択し、[ Tool Size ] を 2.1 mm に設定します。アンカーアームの最も遠い部分に固定穴を作成します。
- ツールサイズを1.5mmと1mmに設定して、PSIの残りの部分に排水穴を作成します。インプラントの端の近くに穴を開けないでください。Boolean と Remove From を実行して、最終的な PSI から元のフラクチャされた軌道を減算します。
注意: 固定穴は、手術室で使用されるネジシステムに適合する必要があります。直径1.5mmのネジを適合させるには、直径2.1mmの固定穴を使用してください。デザイン シーケンスの最後のステップでは、常に最終的な PSI から元のフラクチャされた軌道を差し引いて、術中に軌道上のメッシュのパッシブ シートを確保する必要があります。
- メッシュオブジェクトをSTLファイルとしてエクスポートし、最終的な製造プロセスに使用します。
結果
このプロトコルに記載されているすべての方法は、私たちの研究所で適用されました。このメソッドの簡単な適用を示すために、代表的なケースが提示されます。 図1 は、眼窩床骨折の症例を示しています。 図1A、B は、それぞれコロナCTと矢状CTの角度で眼窩床の変位を示しています。前後面と外側外側の両方で大きな変位があることに注目してください。外側と内側の棚が存在し、後部の棚は無傷ですが、非常に後方の位置にあります。
CTをセグメンテーションソフトウェアにアップロードしました(図2 および 図3)。次に、フラクチャーされた軌道(図4、 図5、 図6、 図7)と床面(図8 、 図9)のセグメンテーションを行い、2つのSTLファイルを作成しました。STLファイルを3D設計ソフトウェアにアップロードしました(補足図1)。小さなギャップが修正され、メッシュが作成されました(補足図2)。ギャップは、自動ギャップ充填を使用するのに十分なほど小さくありませんでした(補足図3)。フラクチャされたセグメントを正しい位置に再配置できませんでした。セグメントの両方のエッジがずれているため、回転のみの機能は不可能であることに注意してください (補足図 4)。粉が多すぎました。したがって、ミラーリング技術が必要でした(補足図5 および 補足図6)。再構成されたセグメントは、最終的なPSIが軌道空間に過剰に投影されるのを避けるために、劣った方向に移動されました(補足図7)。PSIの厚さは、市販のプレハブ軌道チタンプレートの厚さよりも大きいことを覚えておくことが重要です。PSIは、固定アームと排水穴を使用して作成されました(補足図8 および 補足図9)。アンカーアームの曲率は、術中にメッシュの単一の正確な空間位置を見つけるのに役立ちます。メッシュの術中の揺れは、不適切な位置決めや設計エラーを意味します。また、固定アームの設計では、眼窩下孔から遠ざけることを忘れないでください。豊富な排出穴は、眼窩内浮腫/血液蓄積を防ぐための設計の必須部分であり、眼窩コンパートメント症候群を発症するリスクをもたらします。
強制誘導試験の後、外科的処置には中足骨切開が含まれていました。これらの場合、経結膜切開も可能です。骨膜下解剖の結果、眼窩壁欠損が明らかになった。上顎洞に下方変位した眼窩内容物が上昇し、骨棚と下眼窩縁(固定腕)の正確な解剖学的一致に基づいて、PSIが明確な位置に配置されました。外科的切開を閉じる前に強制誘導試験を再度実施したが、眼球の動きに機械的な制限は示されなかった。さらに、解剖およびインプラント埋入後の眼の眼小垂下垂をチェックすることが重要です。骨膜と皮膚を縫合した。術後CTを実施しました。
図1C、D は、それぞれコロナCTと矢状CTビューでPSIを使用して再構成された軌道を示しています。PSIの配置を支えるために外側と内側の棚を使用し、後方の棚は非常に後方に配置されているため、後方の棚を避けていることに注意してください。その上に棚を配置すると、移動制限や軌道体積の変化が生じる可能性があります。したがって、PSIの後端は、棚と連続して横たわるように設計されました。
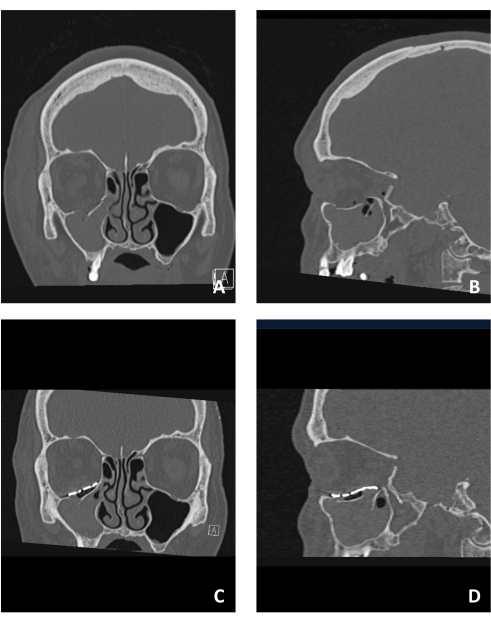
図1:眼窩床骨折に苦しむ患者の術前および術後の画像。 (A)変位した骨折セグメントによって観察された眼窩床骨折を示す術前冠状CTビュー。(B)同じ患者の矢状図で、下変位した骨折した眼窩床を示しています。(C)PSIを使用した床の再建を示す同じ患者の術後冠状CTビュー。PSI の優れた構造と位置に注目してください。(D)同じ患者の矢状ビュー。PSIを使用した床の解剖学的再構築は、床の後部領域に「怠惰なS」構造を示しています。 この図の拡大版を表示するには、ここをクリックしてください。

図 2: セグメンテーションのための CT のアップロード。 DICOMを挿入するには、 を押します フィレット > DICOMファイルの追加 ボタンをクリックして、3Dモデルをインポートしてセグメント化します。 この図の拡大版を表示するには、ここをクリックしてください。
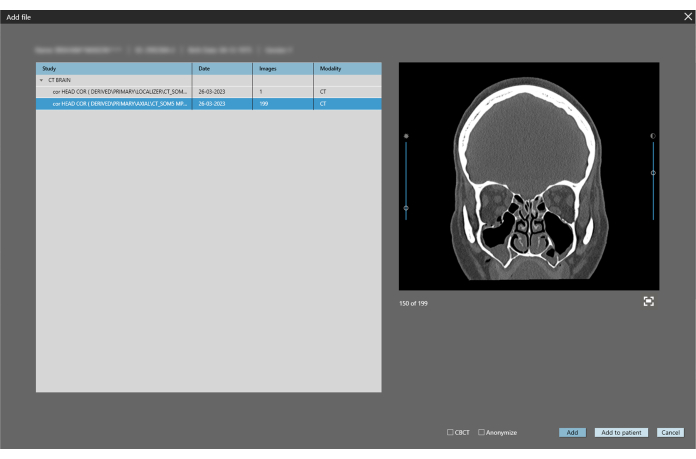
図3:適切な平面を選択します。 患者のCTの冠状多平面変形(MPR)は、スライス幅1mmで選択されます。 「追加 」ボタンをクリックします。 この図の拡大版を表示するには、ここをクリックしてください。
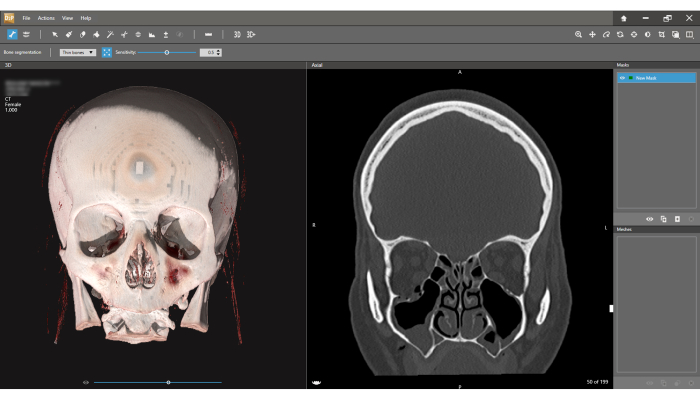
図4:ボーンセグメンテーションインターフェース。 左が3Dモデル、右が冠状CTビューです。ツールバーの Bone segmentation アイコンを押し、 Thin bones オプションを選択します。セグメンテーションプロセスの最初のステップは、新しいマスク(画面の右上隅)を定義することです。スライス幅は 1.000 mm (画面の左上隅) であることに注意してください。 この図の拡大版を表示するには、ここをクリックしてください。
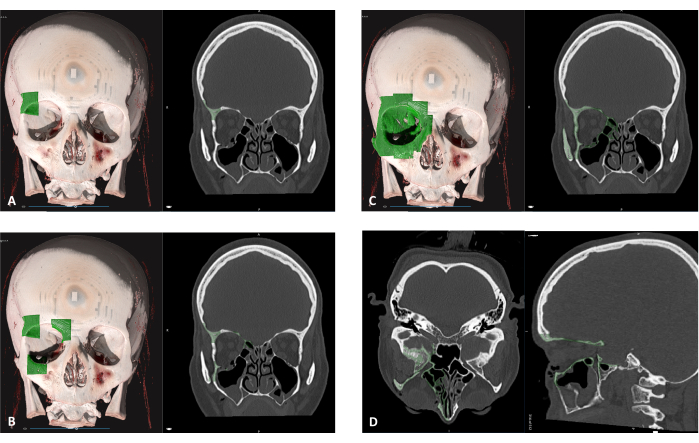
図 5: セグメンテーションの領域の定義 (A) 骨折した骨の軌道の任意の領域をクリックして、新しいマスク (緑の領域) の定義を開始します。(B)クリックするたびに、骨のセグメントのボリュームが追加されます。(C)全軌道がマークされるまで、さまざまな領域を選択し続けます。このプロセスは、3D ビューとスライス ビューの両方で実行できます。(D)次のステップに進む前に、眼窩のすべての骨部分が軸方向と矢状図で選択されていることを確認してください。 この図の拡大版を表示するには、ここをクリックしてください。
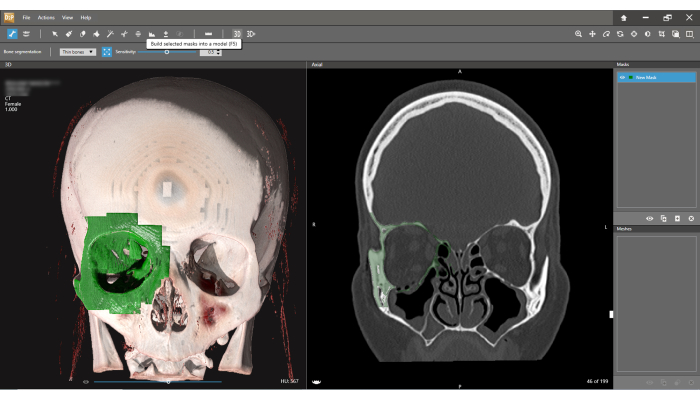
図 6: メッシュの作成。 ツールバーの 3D ボタンを選択します。選択したマスクは、メッシュとして定義されたモデルに組み込まれます。 この図の拡大版を表示するには、ここをクリックしてください。

図 7: メッシュの検査とエクスポート。 軌道の3Dモデル(メッシュ)が左側の画面に表示されます。 [ファイル]>[名前を付けて保存 ]を押し、[形式]で[STL]を選択します。軌道のSTLモデルがエクスポートされます。 この図の拡大版を表示するには、ここをクリックしてください。
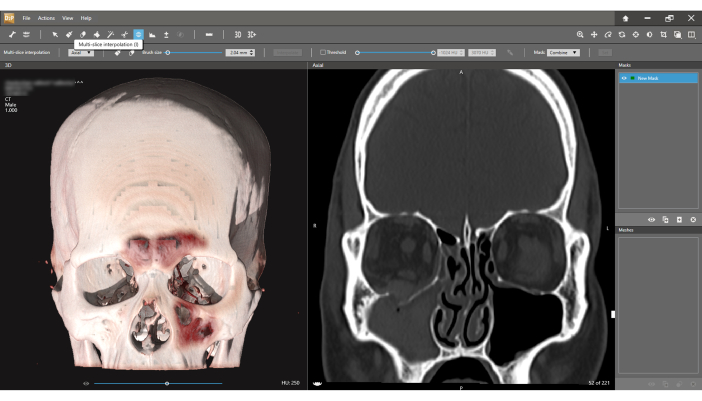
図8:マルチスライス補間セグメンテーション法。 床の破砕セグメントが粉砕されていない場合(右の冠状ビュー)、マルチスライス補間を使用して、このセグメントに別のメッシュが作成されます。 この図の拡大版を表示するには、ここをクリックしてください。
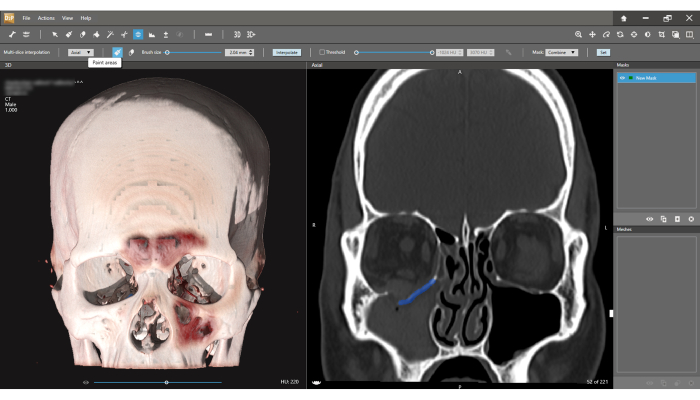
図 9: フラクチャされたセグメントを作成します。Multi-slice interpolation (マルチスライス補間) と Paint areas アイコンを使用して、冠状ビュー上の破砕されたセグメントをいくつかのランダムなスライスで選択することができます。次に、フラクチャされたセグメントを自動的に選択するための補間機能を使用して、セグメンテーションが実行されます。これで、床セグメントをSTLファイルとしてエクスポートできるようになりました。この図の拡大版を表示するには、ここをクリックしてください。
補足図1:STLを3D設計ソフトウェアにインポートします。 File > Import Modelをクリックし、図7でエクスポートしたSTLファイルを選択します。このファイルをダウンロードするには、ここをクリックしてください。
補足図2:粘土をメッシュに変えます。 まず、欠陥の周囲の周囲の完全な粘土の連続性が達成され、次に 粘土からメッシュへの変換 が実行されます。(A)破砕された床領域の周りの小さな隙間(白い矢印)、(B)これらの領域を手動で接続して、破断周囲の完全な連続性を実現します(黒い矢印)。(C)加えた粘土を滑らかにします。(D) 新しい メッシュを作成します。 このファイルをダウンロードするには、ここをクリックしてください。
補足図3:自動ギャップ充填。 (A)欠陥のマージンを選択します。(B)マージンの削除。(C,D)床が完全に再現されるまで穴を埋めます(D)。このファイルをダウンロードするには、ここをクリックしてください。
補足図4:解剖学的再配置シーケンス。 骨折したセグメントがワンピースとして変位した場合、解剖学的再配置が最も簡単で正確なオプションです。(A)軌道のSTLとフロアセグメントのSTLがインポートされ(補足図1)、フロアピースがアクティブ化されます(右クリック - アクティブ化)。(B)「粘土を選択して移動」で、「再配置」ツールが選択され、「移動のみ」オプションの選択が解除されます。(C)床は、解剖学的に無傷の境界に合うように手動で再配置されます。(D)断片化されたエッジの1つが正しい解剖学的位置に配置されている場合に、フラクチャされたセグメントを再配置する別の方法が可能です。この再配置方法では、回転の中心は空間に固定されます。このファイルをダウンロードするには、ここをクリックしてください。
補足図5:ミラーリング技術。 大きくて粉砕された軌道欠陥の場合、ミラーリング技術によりより正確な結果が得られます。(A)骨の大部分が欠けている右側の眼窩床。左の無傷の軌道はセグメント化されました。(B) ミラークレイ ツールを使用して、平面の位置を内側(青い線)に向けます。(C) ピース全体をミラーリング し、 プレビュー にチェックを入れてから 適用します。(D)左の無傷軌道の新しいミラーリングされたオブジェクト。 このファイルをダウンロードするには、ここをクリックしてください。
補足図6:ミラーリングされた軌道とフラクチャーされた軌道の重ね合わせ。 (A) [ピースの登録 ] ツールを使用して、ミラーリングされた軌道が ソース として選択され、フラクチャされた軌道が ターゲットとして選択されます。(B)マーカーは、ミラーリングされた軌道の一意の解剖学的位置とフラクチャーされた軌道の同様の位置に配置され、 次に[適用 ]をクリックしてセグメントを重ね合わせます。(C)最適な重ね合わせのために 自動 が選択されます。(D)重ね合わせられた鏡面軌道は、骨折した眼窩の解剖学的再構築のガイドとして機能します。 このファイルをダウンロードするには、ここをクリックしてください。
補足図7:軌道床の準備。 復元された床面は、垂直軸上で0.8mm押し下げられています。この垂直距離は、設計されたチタンメッシュの厚さと一致するため、メッシュが軌道の内側に侵入して体積が減少するのを防ぎます。(A) 「粘土の選択/移動」で、「 原点の再配置 」を選択し、「 中心へ」を選択します。座標系は、ミラー化された軌道床の中心に移動されます。 「回転のみ 」が選択され、Z軸が垂直に、X軸が水平に、Y軸が前後に配置されます(B)「 Select/MoveClay」では、「 Reposition Piece 」が選択されています。次に、 詳細設定の表示/非表示 と 移動ステップ を0.8mmに修正します。赤い長方形の矢印をクリックすると、ミラー軌道が破砕軌道に沈み込み、破砕領域の無傷の境界が表示され始めます。(C)緑色の長方形の下向きの矢印をもう一度クリックすると、ミラー軌道の床がさらに0.8mm沈みます。この深さはPSIの厚さと一致するため、元の床が再現されます。(D)「 粘土の選択/移動」で「 粘土の選択 」が選択され、 なげなわ選択ツール が使用されます。床の解剖学的周囲が選択されます。 「選択を反転 」が選択され、残りは削除されます。床の境界を滑らかにするか、破砕した軌道の境界に合うように粘土を追加します。 このファイルをダウンロードするには、ここをクリックしてください。
補足図 8: PSI を設計します。(A)オービットオブジェクトとフロアオブジェクトを選択し、右クリックしてブール演算/新規として結合を選択すると、解剖学的に縮小および陥没したフロアを含むオービットの単一のオブジェクトが作成されます。境界線は、さらにスムージングされます。(B)最終オブジェクトが複製され、右クリックして「See Through」が選択され、続いて「Turn On」が選択されます。(C) [カーブ]で[カーブを描画]が選択され、元のフラクチャ領域のすぐ周囲にアウトラインが作成されます。カーブはフラクチャされた軌道のエッジ上に置かれている必要があります。カーブは、新しく作成された床に載せることができるのは、骨の欠落している領域のみです(例:例:横方向の後端 - 黒の矢印)。アウトラインが完全に揃ったら、[作成時に粘土に合わせる]アイコンをクリックします。(D)同様に、PSIの固定アームが作成されます。このファイルをダウンロードするには、ここをクリックしてください。
補足図 9: PSI を確定します。 メッシュと固定アームはエンボス加工されてから接続されています。固定穴と水切り穴が作成されます。(A) ディテールクレイでは、 曲線付きエンボス が選択され、距離は0.8mmが選択されています。アウトラインで囲まれた領域の内側が選択され、[ 上げ] がクリックされます。(B) Add Clay と Smooth は、固定アームをインプラントの本体に接続するために使用されます(黒い矢印)。(C) Boolean 関数と Remove From 関数が複製されたオブジェクトに適用されます。(D)オブジェクトリストで、 粘土の粗さ を右クリックすると-0.1mmが選択されます。 [スカルプト クレイ] で [Carve ] ツールを選択し、[ Tool Size ] を 2.1 mm に設定します。アンカー アームの最も遠い部分に固定穴が作成されます。 ツールサイズは 1.5mmと1mmに設定され、PSIの残りの部分に排水穴を作成します-インプラントの端近くの穴は避けられます。最終的な患者専用インプラントが提示されます。 Boolean と Remove From は、最終的な PSI から元の骨折した軌道を差し引くために常に使用され、骨折した眼窩の骨端にインプラントの受動的な座を確保します。 このファイルをダウンロードするには、ここをクリックしてください。
ディスカッション
眼窩骨折再建術は、顎顔面外科医の最も重要でありながら繊細な仕事の1つです14。再建には、外部の小さな切開を通じて目の非常に敏感で目立つ器官の周りで作業することが含まれ、手術野の視界は部分的にしか見えません。この困難さのため、再建にPSIを使用すると、精度が大幅に向上し、罹患率を最小限に抑えることができます15。そうは言っても、正しい解剖学、すべての部品の3D再構成原理、PSIの特性とその影響、および手術中の適切な取り扱いについての理解が不十分なため、不適切な設計により、作成されたPSIを手術中に使用できなくなる可能性があります。これは簡単に回避できます16。
このプロトコルでは、さまざまな3D再構成方法について説明し、それらの適応について説明します。また、各方法の詳細な手順があり、PSIを設計する際に避けるべき落とし穴に重点を置いています。
眼窩骨折を再構築するための3つの方法が記載されている。最初の方法は、設計ソフトウェアの自動化を使用し、これまで適切な再構築のために小さな欠陥が必要であったため、あまり一般的ではありません。2つ目は解剖学的なリポジショニングで、適用可能な場合、設計者の経験と理解が少なくて済む一方で、非常に良い結果が得られます。3つ目は、最も一般的なミラーリング技術で、複雑な解剖学的構造、骨折特性、PSI特性、および各特定のケースを再構築するための主要な領域を高度に理解する必要があります。
この方法は、Krasovsky A et al.11で説明されているように、さまざまな軌道壁欠陥だけでなく、複数の壁欠陥にも適用できます。この方法は、最近獲得した骨折と、不適切に治癒した古い骨折の両方に使用できます。
私たちの研究所では、デザイナーは外科医でもあり、私たちの信念では、設計段階と手術中の両方で優れた結果をもたらします。しかし、このコンステレーションはこれまでのほとんどの研究所では不可能であるため、外科医とエンジニアの両方がこのプロトコルを使用して、この関係の反対側をよりよく理解し、落とし穴を回避し、より高いレベルの軌道再構築を達成することが求められています。
開示事項
著者は何も開示していません。
謝辞
何一つ
資料
| Name | Company | Catalog Number | Comments |
| D2P (DICOM to Print) | 3D systems | https://oqton.com/d2p/ | Segmentation software to create 3D stl files |
| Geomagic Freeform | 3D systems | https://oqton.com/freeform/ | Sculpted Engineering Design |
参考文献
- Prendergast, M. E., Burdick, J. A. Recent advances in enabling technologies in 3D printing for precision medicine. Adv Mater. 32 (13), 1902516 (2020).
- Rajantie, H., et al. Health-related quality of life in patients surgically treated for orbital blow-out fracture: a prospective study. Oral Maxillofac Surg. 25, 373-382 (2021).
- Som, P., Shugar, J., Brandwein, M. Anatomy and physiology of the sinonasal cavities. Head Neck Imaging. 3, 87-147 (2003).
- René, C. Update on orbital anatomy. Eye. 20 (10), 1119-1129 (2006).
- Nakamura, T., Gross, C. W. Facial fractures: analysis of five years of experience. Arch Otolaryngol. 97 (3), 288-290 (1973).
- Parsons, G. S., Mathog, R. H. Orbital wall and volume relationships. Arch Otolaryngol Head Neck Surg. 114 (7), 743-747 (1988).
- Ellis, E., Tan, Y. Assessment of internal orbital reconstructions for pure blowout fractures,cranial bone grafts versus titanium mesh. J Oral Maxillofac Surg. 61, 442 (2003).
- Emodi, O., Nseir, S., Shilo, D., Srouji, H., Rachmiel, A. Antral wall approach for reconstruction of orbital floor fractures using anterior maxillary sinus bone grafts. J Craniofac Surg. 29 (4), e421-e426 (2018).
- Blumer, M., et al. Customized titanium reconstruction of orbital fractures using a mirroring technique for virtual reconstruction and 3d model printing. J Oral Maxillofac Surg. 79 (1), 200.e201-200.e200 (2021).
- Blumer, M., Essig, H., Steigmiller, K., Wagner, M. E., Gander, T. Surgical outcomes of orbital fracture reconstruction using patient-specific implants. J Oral Maxillofac Surg. 79 (6), 1302-1312 (2021).
- Krasovsky, A., et al. Comparison of patient specific implant reconstruction vs conventional titanium mesh reconstruction of orbital fractures using a novel method. J Craniomaxillofac Surg. 52 (4), 491-502 (2024).
- Danko, I., Haug, R. H. An experimental investigation of the safe distance for internal orbital dissection. J Oral Maxillofac Surg. 56 (6), 749-752 (1998).
- Rontal, E., Rontal, M., Guilford, F. Surgical anatomy of the orbit. Ann Otol Rhinol Laryngol. 88, 382-386 (1979).
- Sigron, G. R., et al. Functional and cosmetic outcome after reconstruction of isolated, unilateral orbital floor fractures (blow-out fractures) with and without the support of 3d-printed orbital anatomical models. J Clin Med. 10 (16), 3509 (2021).
- Kotecha, S., Ferro, A., Harrison, P., Fan, K. Orbital reconstruction: a systematic review and meta-analysis evaluating the role of patient-specific implants. Oral Maxillofac Surg. 27 (2), 213-226 (2023).
- Stoor, P., et al. Rapid prototyped patient specific implants for reconstruction of orbital wall defects. J Craniomaxillofac Surg. 42 (8), 1644-1649 (2014).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved