13.10 : 속도 결정 단계
관련 반응 메커니즘
다단계 반응 메커니즘에서, 초등학교 단계 중 하나는 다른 단계보다 현저하게 느리게 진행됩니다. 이 가장 느린 단계는 속도 제한 단계(또는 속도 결정 단계)라고 합니다. 반응은 가장 느린 단계보다 빠르게 진행될 수 없으므로 속도 결정 단계는 전체 반응 속도를 제한합니다.
속도 결정 단계의 개념은 차선 폐쇄로 인한 짧은 트래픽 병목 현상으로 4 차선 고속도로의 비유에서 이해할 수 있습니다. 차량이 주행할 수 있는 전체 속도에 영향을 미치는 병목 현상과 마찬가지로 가장 느린 초등학교 단계는 순 반응 속도에 영향을 미칩니다.
요율법은 초등학교 반응에 대한 균형 잡힌 화학 방정식에서 직접 파생될 수 있다. 그러나, 이것은 대부분의 화학 반응에 대 한 경우, 어디 균형 된 방정식 종종 화학 시스템의 전반적인 변화를 나타냅니다., 다단계 반응 메커니즘에서 발생. 따라서, 속도법은 실험데이터로부터 결정되어야 하며, 반응메커니즘은 이후에 속도법에서 추론되어야 한다.
예를 들어 NO2 및 CO의 반응을 고려하십시오.
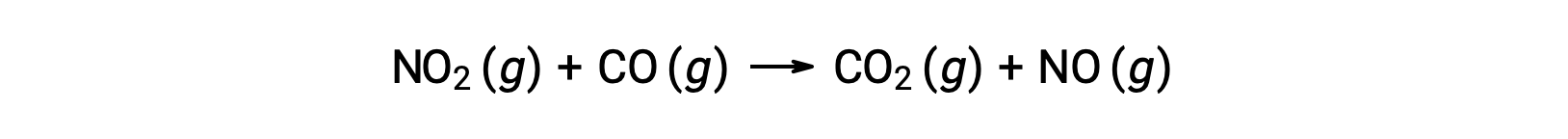
225 °C 이상의 온도에서이 반응에 대한 실험 속도 법은 다음과 같이 합니다.
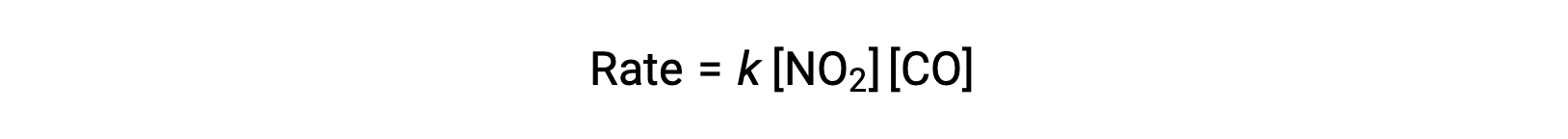
요금법에 따르면, CO에 대하여 NO2 및 1차 순위에 대하여 반응은 첫번째 순서입니다. 이것은 단단 이중 분자 기계장치와 일치하고, 이 반응 기계장치가 고온에서 이 화학 공정을 위해 유효할 수 있습니다.
그러나, 225°C 이하의온도에서, 반응은 NO2에대하여 제2 순서인 다른 비율 법에 의해 기술됩니다 :

이 속도 법은 단일 단계 메커니즘과 일치하지 않지만 다음 2 단계 메커니즘과 일치합니다.
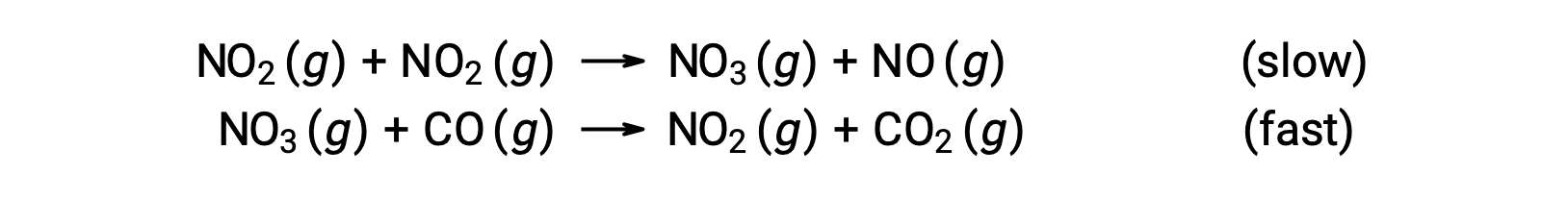
금리 결정(느린) 단계는 NO2 농도에 대한 2차 의존도를 나타내는 속도법을 부여하고, 두 개의 기본 방정식의 합은 전체적인 순반응을 제공한다.
일반적으로, 속도 결정(느린) 단계가 반응 메커니즘의 첫 번째 단계일 때, 전반적인 반응에 대한 속도법은 이 단계의 요율법과 동일하다. 그러나, 속도 결정 단계가 급속하게 가역적인 반응을 수반하는 초등학교 단계에 선행될 때, 전반적인 반응에 대한 비율법은 반응 중간자의 존재때문에 도출하기 어려울 수 있다.
이러한 경우, 전방 및 역공정의 비율이 같을 때 가역반응이 평형화된다는 개념을 활용할 수 있다.
예를 들어, NO가 중간종N2 O2를산출하기 위해 이질화되는 가역적인 초등반응을고려한다. 이 반응이 평형에있을 때 :
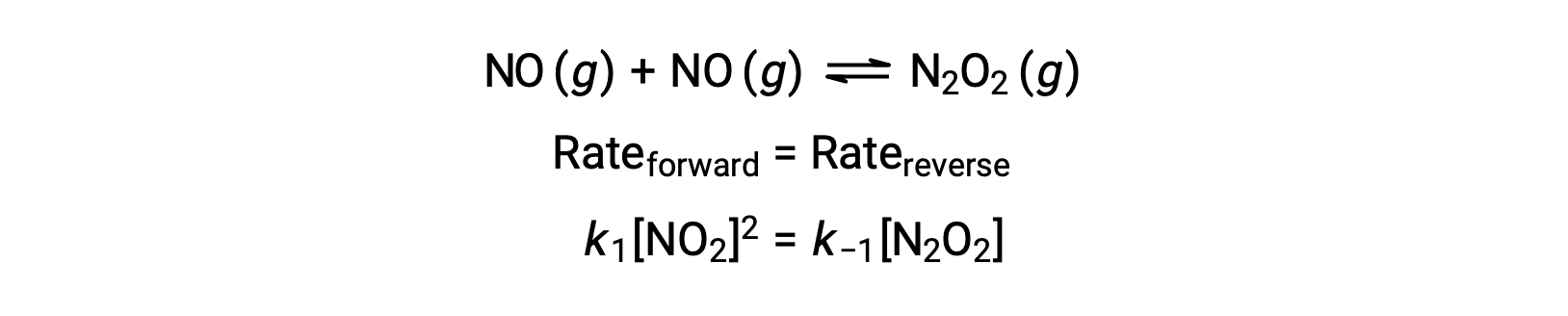
이러한 표현은 반응성 NO의 관점에서 중간의 농도를 표현하기 위해 재배열될 수 있다.
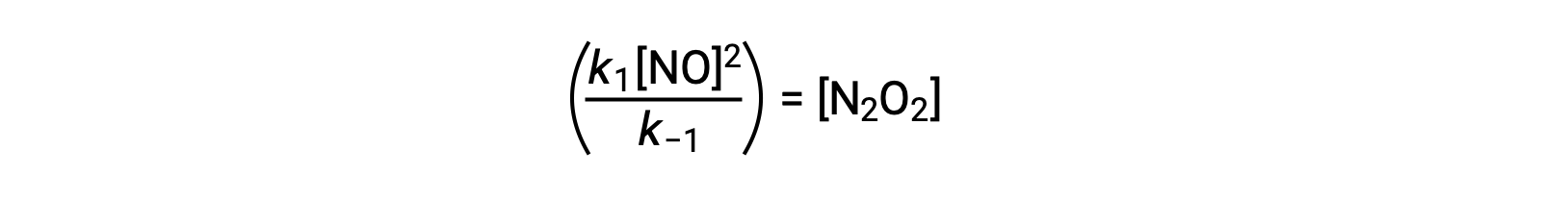
이 접근법은 반응 중간자가 있을 때 전반적인 반응에 대한 비율 법률을 공식화하는 데 활용될 수 있습니다.
반응 메커니즘에서 속도 법을 파생의 예
2단계 메커니즘이 제안된 질소 일산화질소와 분자 염소 사이의 반응을 고려하십시오.
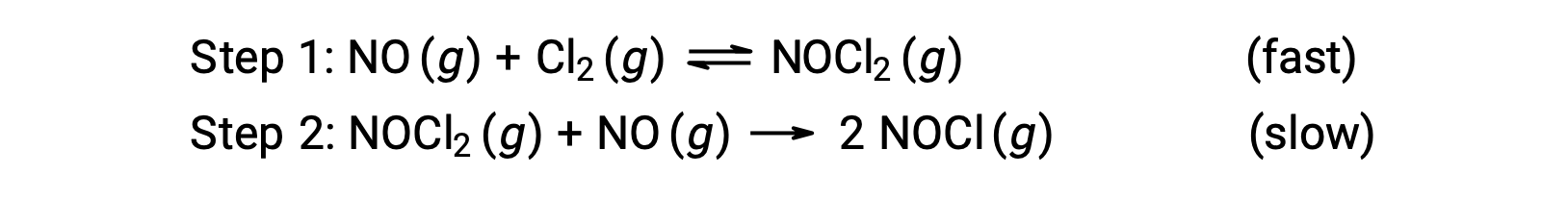
이 메커니즘은 방정식을 도출하고 전반적인 반응에 대한 속도 법을 예측하는 데 사용할 수 있습니다. 처음에는 두 가지 기본 반응을 추가함으로써 전반적인 반응에 대한 방정식이 얻어진다.
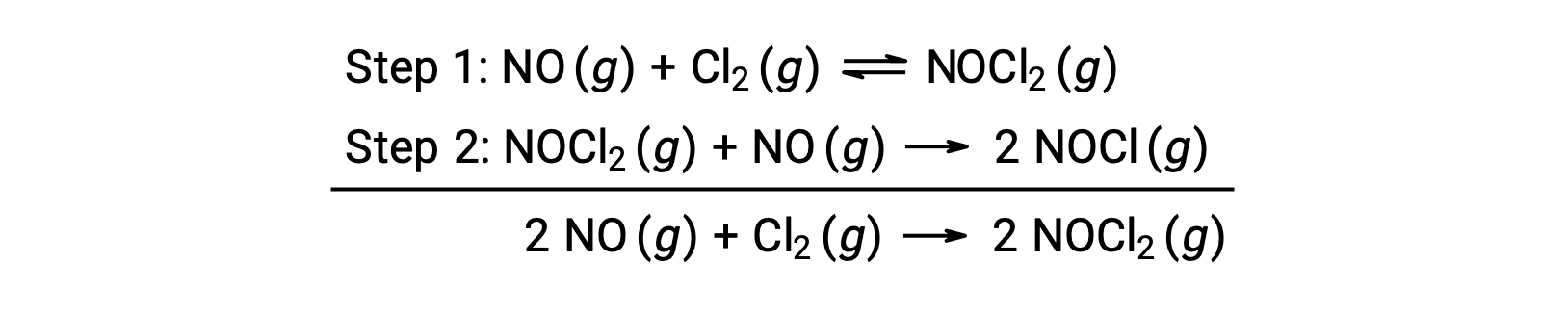
이 메커니즘에서 요율법을 도출하기 위해 두 가지 기본 단계에 대한 요금 법률이 작성됩니다.
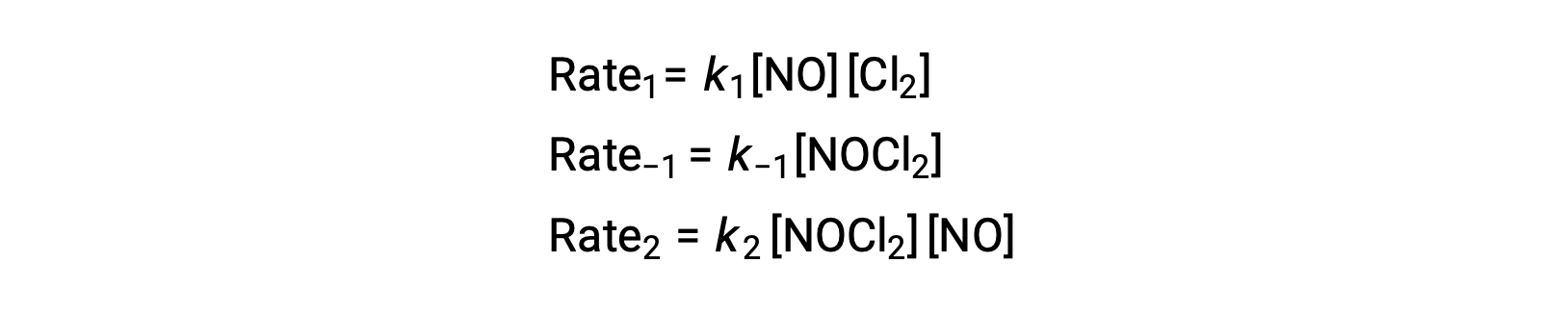
제안된 반응 메커니즘에 따르면 2단계는 속도 결정 단계이다. 따라서 전반적인 반응에 대한 요금법은 이 기본 단계의 요금법과 같아야 합니다. 그러나, 2단계의 속도법은 중간 종 농도,[NOCl2]를포함한다. 이를 수정하기 위해, 제1초단계의 요율법은 반응성 농도의 관점에서 중간 농도에 대한 표현을 도출하는 데 사용된다.
1단계가 평형에 있다고 가정합니다.
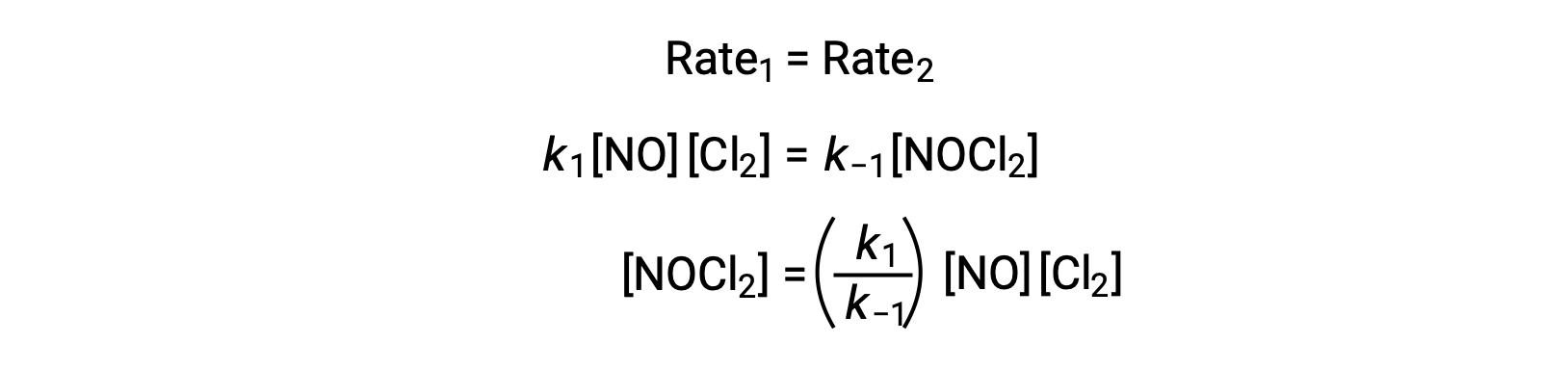
이 표현을 2단계 수익률에 대한 금리법으로 대체합니다.
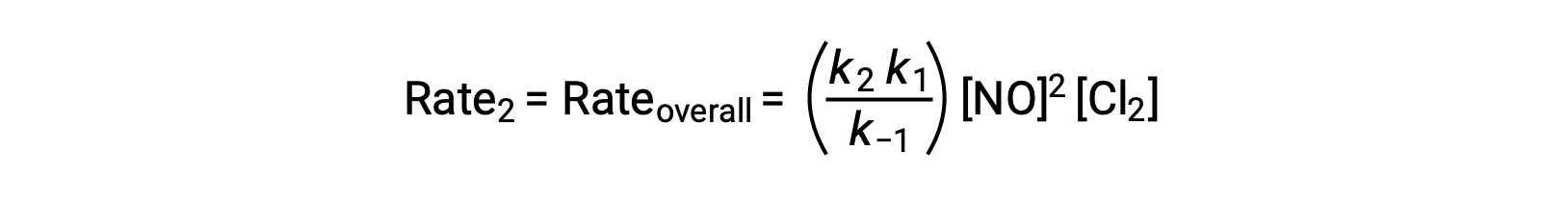
Tags
장에서 13:

Now Playing
13.10 : 속도 결정 단계
반응 속도론
31.8K Views

13.1 : 반응 속도
반응 속도론
51.5K Views

13.2 : 반응 속도 측정
반응 속도론
24.7K Views

13.3 : 농도와 속도 법칙
반응 속도론
30.2K Views

13.4 : 반응차수 계산
반응 속도론
55.2K Views

13.5 : 적분 속도 법칙: 시간에 의존하는 농도
반응 속도론
34.6K Views

13.6 : 반응의 반감기
반응 속도론
34.5K Views

13.7 : 반응 속도의 온도 의존성
반응 속도론
81.2K Views

13.8 : 아레니우스 플롯
반응 속도론
38.7K Views

13.9 : 반응 메커니즘
반응 속도론
25.5K Views

13.11 : 촉매
반응 속도론
26.7K Views

13.12 : 효소
반응 속도론
80.9K Views
Copyright © 2025 MyJoVE Corporation. 판권 소유