Method Article
전기 생리학을 바탕으로 솔리드 지원 막 소개
요약
여기에서 우리는 electrogenic 막 수송의 특성에 대한 응용 프로그램에 초점을 맞춘 견고한 지원 세포막에 따라 전기 생리학 방법을 제시한다.
초록
우리가 존재하는 전기 생리학 방법은 금 코팅 된 센서 칩 위에 포스파티딜콜린 단일 층에 화학적으로 흡착 octadecanethiol 층으로 구성된 고체 지원 막 (SSM)을 기반으로합니다. 이 어셈블리는 기준 전극, 염소화 실버 와이어를 포함하는 큐벳 시스템으로 마운트됩니다.
막 조각 또는 관심의 막 단백질을 포함 proteoliposomes의 흡착 후 빠른 솔루션 교환은 막 단백질의 수송 활동을 유도하는 데 사용됩니다. 단일 솔루션 교환 프로토콜 두 가지 솔루션을 하나의 비 활성화 한 활성화 솔루션이 필요합니다. 흐름은 패러데이 케이지 내에서 가압 공기 밸브와 배관 시스템에 의해 제어됩니다.
electrogenic 수송 활동의 속도론은 SSM과 proteoliposomes 또는 막 조각 사이의 용량 성 커플 링을 통해 얻을 수있다. 방법은, 그러므로, 오직 transien에게 얻을 수T 전류. 피크 전류는 고정 된 전송 작업을 나타냅니다. 시간에 따라 수송 전류는 회로 분석에 의해 재구성 할 수 있습니다.
이 방법은 특히 패치 클램프 또는 전압 클램프 방법으로 조사 할 수없는 세포 막에서 원핵 운송 또는 진핵 수송에 적합합니다.
서문
여기에서 우리는 electrogenic 막 단백질의 특성에 대한 확고한 지원 막 (SSM)에 따라 새로운 전기 생리학 방법을 보여줍니다.
고체 지지체는 유리 슬라이드, 센서 칩에 얇은 금 층으로 구성되어 있습니다. 친수성 금 표면 alcanethiol 시약의 티올 그룹을 바인딩하는 데 사용됩니다. 그 후, selfassembly 포스파티딜콜린의 monolyer의는 SSM의 형성이 완료됩니다.
막 단백질의 electrogenic 반응을 측정하기 proteoliposomes 또는 막 조각은 SSM (그림 1)에 흡착된다. 막과 SSM을 포함하는 단백질은 그 용량 성 결합 멤브레인 시스템을 형성한다. 따라서 단백질을 포함하는 막에 충전 전위는 SSM을 통해 용량 성 결합에 의해 감지 할 수 있습니다. 이 방법은 일시적으로 만 전류를 얻을 수 있습니다. 피크 전류는 고정 된 전송 작업을 나타냅니다. 시간에 따라 수송 잘라 내기rrents은 회로 분석에 의해 재구성 할 수 있습니다.
센서 칩은 큐벳 시스템 (그림 2)에 장착된다. 큐벳은 17 μL의 원통형 큐벳 볼륨이 (O-링과 그물 볼륨 마운트). 스프링 접촉 핀은 앰프 연락처를 만듭니다. 콘센트 커넥터는 주요 부분의 상단에 나사와 기준 전극, 염소화 실버 와이어를 전달합니다.
큐벳은 패러데이 케이지에 장착되어 있습니다. 그것은 빠른 솔루션 교환 (그림 3)에 대한 응답으로 막 단백질의 수송 활동을 유도하는 데 사용되는 유체 통로로 연결되어 있습니다. 단일 솔루션 교환 프로토콜 두 가지 솔루션을 하나의 비 활성화 한 활성화 솔루션이 필요합니다. 흐름은 인터페이스 박스에있는 컴퓨터 또는 수동 스위치를 밸브 제어 소프트웨어를 사용하여 압축 공기에 의해 제어됩니다.
프로토콜
1. SSM 기반의 전기 생리학에 대한 장치 설정
자세한 내용은 개략적 도면과 우리 큐벳의 사진을 포함하고 1, 2를 설정 우리의 기술 발행물의 두 가지에있다. 다른 솔루션 교환 구성과 흐름 프로토콜은 또한 우리의 방법 종이 2에 설명되어 있습니다.
다음에서 우리는 몇 가지 최근의 개선 및 비디오 프레 젠 테이션을위한 직접적인 관련이없는 기술적 인 세부 사항을 추가합니다.
밸브 제어 및 데이터 수집
인터페이스 박스는 상용 USB 디지털 출력 / 아날로그 입력 인터페이스 (NI USB 6009 내쇼날 인스트루먼트)와 밸브 드라이버가 포함되어 있습니다. 이 솔루션의 흐름을 제어 및 데이터 수집을 담당하고 있습니다. 밸브는 일반적으로 빠른 밸브 18까지의 전압으로 구동 V. 비디오에서 우리는 12 V 전원 공급 장치를 사용 할 수있는 스위칭, 그러나 12으로 구동 V. 있습니다.
밸브 드라이버 회로 보드는 4 개의 밸브를 조작 할 수 있습니다. 그것은 생물 물리학의 맥스 플랑크 연구소의 공장에서 제조되었다. 밸브는 전면 패널 스위치를 통해 컴퓨터 또는 수동으로 제어 할 수 있습니다. 후자는 청소 - 절차 및 플러시 편리합니다. 측정하는 동안, 인터페이스 박스는 밸브 제어 및 데이터 수집 소프트웨어 (SURFE 2 R 소프트웨어 IonGate 생명 과학)를 사용하여 컴퓨터 제어됩니다.
2. 준비
이 섹션에서는 SSM 기반의 전기 생리학 실험의 준비를위한 다양한 프로토콜이 언급되어 있습니다.
2.1 SSM의 형성 지질 솔루션 만들기
- 25 μL Octadecylamine (클로로포름 5 MG / ML)와 GLAS 유리 병에 375 μL Diphytanoylphosphatidylcholine을 (클로로포름 20 MG / ML) 섞는다.
- 회전 증발기 및 지속적인 질소 가스 유량 사용에 대한 클로로포름을 증발약 30 분.
- N-데칸의 500 μL로 흔들어 유리 병의 벽에서 지질을 제거합니다. 최종 지질 농도 1:60 (W / W) octadecylamine와 15 MG / ML입니다.
- 유리 저장 병에 대한 해결책을 전송합니다. -20 ° C.에서 지질 솔루션을 저장
기준 전극의 2.2 염소화
참조 전극 마모로 인해 일정한 간격으로 염화해야합니다.
- 염소 처리하기 전에 잘 사포를 사용하여 이전 silverchloride 층의 나머지 부분을 제거합니다.
- 1 M 염산 용액에 백금 전극과 함께 실버 와이어를 배치하고 0.5 mA에서 15 분간 chlorinate. 염소를 완료 한 후, 실버 와이어는 균일 한 어두운 회색 색상을 변경합니다.
폴리 아크릴 아마이드 젤 다리 2.3 준비
- 100 mM의 pH에서 KPI = 7, 100 mM의 KCl을 6를 포함하는 솔루션을 준비합니다%의 아크릴 아미드.
- 0.3 % APS (10 % 주식)을 추가하고 0.6 %는 TEMED 곧 피펫 솔루션을 섞는다.
- 즉시 용액을 혼합 한 후, 빈 젤 다리 용기에 혼합물의 30 μl를 주입 피펫을 사용합니다. 그것은 주입시 공기 방울을 방지하는 것이 중요합니다.
- 20 분의 배양 시간 동안 젤 중합.
- 중합 후 젤 다리 용액 (100 mM의 KPI pH가 7, 100 mM의 KCl을)에 저장됩니다. 젤 다리의 수명을 연장하기 위해 솔루션은 4 ° C.에 저장됩니다
측정 솔루션 2.4 준비
다른 구성의 솔루션을 교환 할 때 SSM과 용질의 강한 상호 작용으로 인해, 전기 아티팩트가 생성됩니다. 따라서 솔루션의 준비는 중요한 단계입니다. 솔루션 교환 아티팩트를 최소화하기 위해 솔루션의 준비 과정에서 다음과 같은 예방 조치를 취하십시오.
- 비 활성화하고 하나의 일괄 처리에서 솔루션을 활성화합니다, pH와 이온 강도를 조정합니다.
- 높은 소금 배경 솔루션 교환 아티팩트를 줄일 수 있습니다.
- 두 개의 볼륨으로 배치 솔루션을 나눕니다.
- 활성화 용액에 활성 화합물을 추가합니다. 가능한 한 유사한으로 삼투압과 두 솔루션의 이온 강도를 유지하기 위해 비 활성화 솔루션의 보상 화합물을 사용합니다.
- 솔루션은 4 ° C에 저장되어있는 경우, 온도도 작은 차이가 아티팩트를 생성 할 수 있기 때문에 모든 솔루션은 측정을 시작하기 전에 실내 온도에 도달해야합니다.
3. SSM 기반의 전기 생리학 실험
여기에서 우리는 SSM 기반의 전기 생리학 실험에 대한 일반적인 프로토콜을 제시한다.
3.1 SSM 설치 준비
SSM 설치를 사용하지 않을 때에는 튜브는 30 % 에탄올로 가득/ 물 솔루션 박테리아의 성장을 방지 할 수 있습니다.
- 큐벳을 설치하기 전에 튜브에서 에탄올을 제거하는 순수한 물 시스템을 씻으십시오. 물 컨테이너 에탄올 용기를 교체합니다. 높은 압력 (0.6-1.0 bar)를 물 20 ~ 30 ml의 시스템을 청소 사용.
- pH를 7.6 또는 비 활성화 솔루션을 100 mM의 KPI 버퍼를 사용하여 청소 절차를 반복합니다.
- 기포가 유체 시스템에 남아 있는지 확인합니다.
3.2 큐벳 장착
- 기준 전극에 O-링을 부착
- 스토리지 솔루션에서 젤 다리를 타고와 기준 전극을 연결합니다.
- 미리 기입 비 활성화 버퍼 콘센트 커넥터, O-링을 삽입하고 기준 전극 어셈블리를 완료하는 젤 다리를 연결합니다. 기포가 젤 다리와 출구 용액 흐름 경로의 교차점에 없는지 특별한주의를 기울입니다.
- cuve의 주요 부분을 Preassemble스프링 접촉 핀 (앰프에 연결), 유입 관 (터미널 밸브에 연결), O-링 (SSM에 대한 밀봉)하고 나사를 추가하여 테.
- 핀셋 사용하여 저장 용액 (에탄올 10 MM의 octadecanethiol)의 센서 칩을 꺼내.
- 피펫을 사용하여, 약에 남아있는 솔루션을 씻어. 순수 에탄올 5 ㎖.
- 질소 가스 하에서 전극을 건조.
- 입구 큐벳의 주요 부분의 구멍 수 있도록 큐벳의 기본 부분에 정확하게 센서 칩을 배치하는 것은 센서의 원형 활성 영역으로 전달됩니다.
- 센서 칩의 활성 영역 지질 용액 1 μL를 추가합니다. 금 층이 완전히 지질에 포함되어 있는지, 확인하십시오.
- 바로 지질의 솔루션을 추가 한 후, 미리 조립 된 주요 부분을 추가하여 큐벳을 닫습니다.
- 패러데이 케이지에 큐벳을 설치하기 전에 모든 표면이 완전히 건조되어 있는지 확인합니다.
- CONN터미널 밸브 스프링 접촉 핀과 입구 튜브 앰프 요법. 다음 패러데이 케이지 안에 나사 큐벳을 수정합니다.
- 큐벳의 상단에 콘센트 커넥터를 고정합니다. 마지막으로 콘센트 커넥터와 기준 전극에 전압 발생기 출구 튜브를 연결합니다.
- 즉시 설치 후 큐벳 0.6 바에서 버퍼 시스템을 씻는다. 이 자연 SSM 형성에 이르게한다.
3.3 측정 막 매개 변수
SSM의 품질을 확인하려면, 정전 용량 및 전도는 함수 발생기를 사용하여 측정하고 있습니다.
- 함수 발생기 사용하여 전도도를 측정하기 위해 mV에서 100 mV DC 전압을 적용합니다.
- 컨덕턴스를 계산 : 현재 붕괴 막 커패시터의 충전을 보여줍니다. 커패시터 후 완전히 측정 된 현재의 수익률에게 옴의 법칙을 사용하여 막 전도도가 청구됩니다. 단순함을 위해 우리는 CU를 사용rrent 1 초는 전압 후 전기 전도도 G = I / U.를 적용하여 산정
- 진폭과 커패시턴스를 측정하는 0.5 Hz의 주파수에서 최대 50 MV 피크 삼각형 AC 전압을 적용합니다.
- 용량 계산 결과 구형파 전류의 진폭은 커패시터의 충전 전류를 나타냅니다. 정전 용량 C는 전송 요금 같다 Q = ΔU = mV에서 100 mV로 나누어 IΔt. (나는 삼각형 전압의 차이가 현재의 긍정적 인 마이너스 음의 기울기이므로 ΔU 두 번 50 MV의인가 전압이다.)
- 반복적으로 막 약마다 10 분의 전기적 매개 변수를 모니터링 할 수 있습니다. 상수 값에 도달 할 때까지 30 ~ 40 분. 1-0.6에 대한 막대의 범위에서 높은 압력에서 KPI 버퍼와의 사이에 씻으십시오.
- SSM의 품질을 추정 : 최적의 매개 변수는 0.1-0.2 nS는 및 2-3.5 NF의 범위에 있습니다. 1 NF 아래 0.8 nS는 낮은 커패시턴스 위의 높은 전도성을 나타냅니다SSM이 제대로 형성되지 않습니다. 4 NF 위의 높은 용량은 활성 영역이 SSM에 의해 완전히 적용되지 않는 것을 의미합니다.
- 매개 변수가 최적의 범위 내에 있지 않은 경우, 멤브레인은 폐기되어야하며 다른 SSM은 갓 준비된 전극 칩을 사용하여, 준비.
솔루션 교환 아티팩트 3.4 검사
막 매개 변수를 검사 한 후, 측정 버퍼 용액 교환 유물에 대한 검사를해야한다.
- 유체 시스템에 각각의 솔루션 컨테이너를 삽입합니다.
- 수동 밸브를 사용하여 유체 시스템에서 공기 방울을 제거합니다.
- 데이터 수집 소프트웨어를 사용하면 실험에 사용할 흐름 프로토콜을 선택했다.
- 0.6 bar까지 압력을 조정하고 측정을 시작합니다.
- 떨어져 기계적 밸브 스위칭 유물에서 이상적으로 어떤 이슈 전류는 측정하지 않아야하거나 훨씬 SMA해야한다예상 단백질 교통 신호보다 ller의. 솔루션 교환 유물이 발견되면, 실험을 계속하기 전에 버퍼 조성물 및 / 또는 준비 절차를 최적화하려고합니다.
3.5 단백질 샘플을 추가
보통 proteoliposomes 또는 막 조각은 -80에서 냉동 저장됩니다 ° C.는 하나의 측정을 위해 약 30 μL의 나누어지는이 필요합니다.
- 비 활성화 솔루션 SSM을 씻어.
- 얼음에 단백질 샘플을 해동.
- 세 개의 10 초 초음파주기 얼음에 10 초 냉각 간격으로 교대된다. Proteoliposomes는 목욕 sonicator를 사용하여 초음파됩니다. 막 조각을위한 팁 sonicator이 (50W, 30 kHz에서 1 밀리미터 sonotrode 직경, 강도 20 %, 사이클 0.5)이 사용됩니다. 마지막 초음파 단계 후 얼음에 다시 샘플을 두지 않지만, 큐벳에 즉시 투입.
- 풀고 콘센트는 참조 전극 ASSE와 함께 커넥터를mbly.
- 피펫을 사용하여 단백질 시료 30 μl를 대기음 구멍 콘센트에 피펫 팁을 탑재.
- 폐기물 컨테이너에 비 활성화 경로에 수동 밸브를 열고 큐벳 볼륨으로 proteoliposomes을 주입. 센서 큐벳 볼륨으로 공기를 주입하지 않도록주의하십시오.
- 피펫 팁을 제거하기 전에, 추가 솔루션의 흐름을 방지하기 위해 수동 밸브를 닫습니다.
- proteoliposomes 1 ~ 2 시간의 배양 시간 동안 SSM에 흡착 할 수 있습니다. 그것은 하룻밤 배양하는 것도 가능합니다.
SSM 기반 실험의 3.6 일반 절차
- 4 ° C.에 저장하는 경우에, 시간 측정 버퍼를 따뜻하게 모든 측정 버퍼 유물을 피하기 위해 측정을 시작하기 전에 실내 온도에 있어야합니다.
- 솔루션을 변경하는 경우, 먼저 비 퍼징 조직으로 솔루션 컨테이너 내부에 튜브를 청소 한 다음 새 병을 삽입합니다.
- 측정을 시작하기 전에, 변경 절차에서 진화 할 수 기포를 제거하기 위해 수동 밸브를 사용합니다.
- 그냥 측정을 시작하기 전에 압력을 조정합니다. 우리는 정기적으로 우리의 특정 밸브와 튜브 구성이 약 1.0 ML / 초 유량을 산출 0.6 바의 압력을 사용합니다.
- 처음 몇 측정은 다른 후 바로 하나를 수행 할 수 있으며, 피크 전류가 일정하게 유지 될 때까지 거부해야한다. 솔루션은 pH가 다른 경우 적어도 3 분의 배양 시간은 측정을 시작하기 전에 proteoliposomes의 내부 산도를 조정하기 위해 필요합니다.
- 이제 세트까지 측정을위한 준비가되어 있습니다. 소음을 줄이기 위해 최소 3 측정이 이루어과 평균해야한다.
3.7 제어 측정
일련의 측정 중 신호 런은 단백질 분해 또는 흡착 손실로 인해 발생할 수 있습니다. 각각의 SSM 실험 내가해야런 컨트롤을 NCLUDE. 이 동일한 솔루션을 반복 측정하여 수행됩니다. 최소 런 컨트롤은 동일한 솔루션을 사용하여, 하나의 시작 부분에 측정하고 실험의 끝을 의미합니다.
우리는 당신이 실험에서 가장 높은 피크 진폭을 기대 조건 런 제어를 수행하는 것이 좋습니다. 이렇게하면 신호의 개요를 정량화 할 수 있습니다.
신호 런은 두 개요 컨트롤의 피크 진폭의 비교에 의해 정량화 할 수있다. 결과 백분율 값은 런의 선형 시간 의존성을 가정하여 측정 된 신호를 수정하는 데 사용할 수 있습니다.
3.8 아티팩트 컨트롤
가능하면 실험 후 관심 억제 단백질에 의해 결과를 확인하려고합니다. 나머지 신호는 아마도 솔루션 교환 유물이다. 신호는 측정 된 이슈를 수정해야합니다.
3.9
- 순수한 물 20 ~ 30 mL를 30 % 에탄올 / 물 20 ~ 30 ml의 시스템을 씻으십시오. 시스템을 사용하지 않을 때 에탄올 용액은 박테리아의 성장을 방지합니다.
- 이 세척 과정을 거친 후, 시스템에서 압력을 해제하고 모든 기기의 전원을 끄십시오.
- 패러데이 케이지에서 큐벳을 제거하고 분리. 큐벳의 모든 부분은 목욕 sonicator를 사용하여 필요한 경우, 물과 순수 에탄올로 세척 할 수 있습니다.
- 순수 에탄올 GLAS 비커에 센서 칩을 놓습니다. 목욕 sonicator를 사용하여 약 1 ~ 2 분 비커를 초음파 처리.
- 질소 가스 하에서 센서 칩을 말린다.
- 10 MM Octadecanthiol 에탄올 용액에 빛으로부터 멀리 센서 칩을 저장합니다. 약 30 분 배양 시간 이후 센서 칩은 재사용을위한 준비가되어 있습니다.
결과
지금까지, SSM 기반의 전기 생리학은 대부분 원핵 생물 유래의 20 개 이상의 운송, 예를 들면 MelB 3 NhaA 4 PUTP 5 (6 요약) 특성을 사용 하였다. 또한 세포 세포막에서 진핵 운송, 예를 들어 ClC7 7뿐만 아니라 이온 채널, 니코틴 아세틸 콜린 수용체 8 조사 된 예.
여기에서 우리는 5 9 LPR, 10시 레이스 지향의 아웃 85 % 이상 오른쪽으로 proteoliposomes를 사용하여 대장균에서 레이스 설탕 / H + cotransporter의 예 측정으로 제시한다. 우리는이 수송 단백질의 최소한의 운동 모델을 선도하는 주요 단계에 초점을 맞 춥니 다.
1. 야생형 레이스의 전기 생리학 특성
첫 번째 단계는 서로 다른의 pH 값을 측정하여 electrogenic 반응의 일반적인 특성이다 ( > 그림 4), 기질 농도 (그림 5)와 기판. 기술의 유효성을 검사하려면, 문학에 주어진 K M과는 PK 값이 재현되었다.
레이스의 pH 의존성은 두 개의 서로 다른 electrogenic 반응을 보여줍니다. pH가 5와 pH를 8.5 사이뿐만 아니라, 용량 성 결합 전류가 증가는 그것의 모양을 변경합니다. 산성 산도에 대해서만 빠른 electrogenic 반응이 남아있는 값 중에 알칼리 조건 하에서 정상 상태 전송이 관찰된다. 우리는 운송업자 전류 (그림 6) 재구성 회로 분석을 사용 빠른 electrogenic 반응에서 정상 상태 신호를 구별합니다.
pH가 7에서 monophasic 신호는 이상성됩니다. 또한이 두 가지 electrogenic 반응이 있다는 것을 나타냅니다. 전송 요금 (신호의 적분)로부터 추정, 두 반응은 약 6 % 및 전송주기의 총 electrogenicity의 94 %가있다.
electrogenic 반응 ove_step "> 2. 지정레이스의 반응주기의 특정 단계 두 electrogenic 반응을 지정하려면 E325A 레이스 변형 (그림 7)를 측정 하였다. 이 변종은 유당 교환을 보여 주지만 때문에 양성자 방출 억제의 모든 활성 전송 모드의 부족이다. 레이스 E325A의 신호는 빠른 과도을 대표하고 모든 측정의 pH 값에 대한 상수이다. 신호의 모양과 진폭은 산성 조건에서 레이스 야생형의 신호와 비슷합니다. 또한 우리는 용량 성 결합 시스템에서 측정 급속한 과도 전류에 대한 특징 감소 피크 전류, 후 작은 음의 위상을 관찰합니다. 유당 바인딩 및 릴리스 electrogenic 없기 때문에, 빠른 과도은 유당 바인딩을 다음 electrogenic 구조적 변화와 연관해야합니다.
그것은 양성자 방출 단계 속도 limiti 것으로 알려져있다유당 농도 구배 기반의 전송 모드에서 레이스 회전율 NG. 양성자 방출이 선호되기 때문에이 경우 우리는 알칼리성과 전송 속도의 증가를 기대하고 있습니다. 이것은 정상 상태 전송 레이스 야생형의 신호 상관 관계의 경우입니다. 또한 그것은 단지 내부 pH가 레이스의 정상 상태 전송 (게시되지 않은) 영향을 준다는 산도 기울기 측정하여 표시 할 수 있습니다. 따라서 큰 electrogenic 반응은 양성자 방출 단계에 할당 할 수 있습니다.
3. 운동 분석을위한 측정
전송 속도 켜고 electrogenic 반응의 확인 후 약 4.5 밀리의 높은 시간 해상도와 SSM 설치 프로그램을 사용하여 결정 하였다. 한 반응 신호를 지배 할 때,이 조건에서만 가능하다. 이 경우 속도 상수는 반복적 최소 자승 드를 사용하여 신호의 시간 해상도를 고려 과도 전류로부터 유도 될 수있다 컨볼 루션 알고리즘 (그림 8). 결정 속도 상수뿐만 아니라 제안 최소한의 운동 모델 (그림 9) 마지막으로 수송 동역학의 시뮬레이션에 사용 하였다. 시뮬레이션 곡선은 또한 운동 모델을 증명 SSM 데이터를 재현.

그림 1. SSM에 proteoliposomes의 흡착 형상. SSM은 센서 칩, 구조화 된 금 코팅 유리 슬라이드에 형성된다. 막 단백질의 electrogenic 반응을 측정하기 proteoliposomes 또는 막 조각은 SSM에 흡착되어 있습니다. 두 막은 용량 성 결합 시스템을 형성한다. 일시적으로 만 전류가 감지되는 이유입니다.
tp_upload/50230/50230fig2highres.jpg "/>
그림 2. SSM 큐벳은 센서 칩과 레퍼런스 전극을 수행합니다. 센서 칩은 큐벳베이스와 큐벳 머리 사이에 끼워 넣으면됩니다. 기준 전극은 폴리 아크릴 아마이드 젤 소금 교량 흐름 경로에서 격리됩니다.
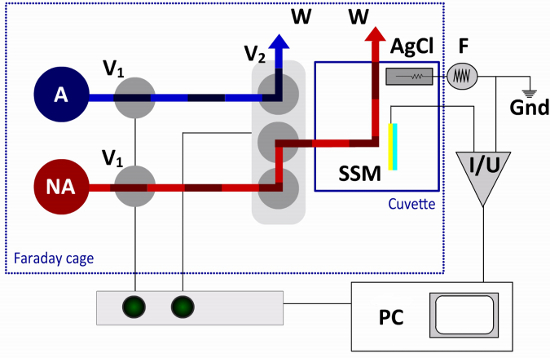
그림 3. SSM 설치 프로그램의 유체 통로 및 전기 회로. 단일 솔루션 교환 프로토콜에 하나의 비 활성화 (NA)와 하나의 활성화 (A) 솔루션이 필요합니다. 흐름은 두 개의 2 웨이 밸브 (V1)와 하나의 터미널 밸브 (V2)에 의해 제어됩니다. 비 활성화 및 활성화 솔루션과 터미널 밸브 스위치, 큐벳과 폐기물 용기 (W)에 다른 솔루션 솔루션 중 하나를 연출. 센서 칩 (SSM)는 증폭기 (I / U)에 연결되어 기준 전극 (AgCl을)은 외부 전기 회로에서 함수 발생기 (F)에 연결되어있는 동안. 컴퓨터 (PC)와 인터페이스 박스는 밸브 작동 및 데이터 수집에 사용됩니다.
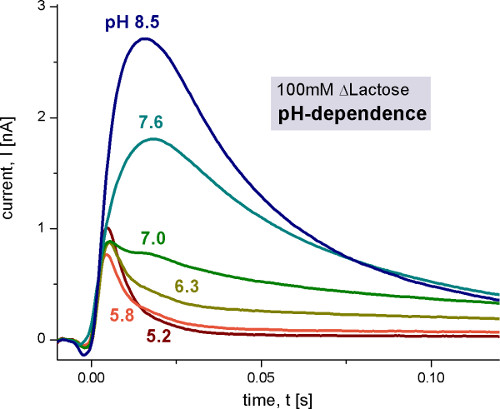
그림 4. 활성 솔루션은 100 MM의 유당을 포함하는 동안 다른 산도 값이 100 밀리미터 유당 농도 점프 후 야생형 레이스 proteoliposomes로 측정 과도 전류. 비 활성화 솔루션은 100 mM의 포도당이 포함되어 있습니다. 모든 솔루션은 1 ㎜의 DTT로 지정된 pH에서 100 MM의 칼륨 인산 버퍼에 준비되었다. 이있는 측정 조건에 대한 자세한 내용은 다음과 같은 그림 9와 10을 참조하십시오.
ftp_upload/50230/50230fig5highres.jpg "/>
그림 5. 평균 정규화 된 피크 전류는 서로 다른 농도의 pH 값에서 유당 농도 점프 후 야생형 레이스 proteoliposomes로 측정. K M 값은 하이퍼 볼릭 맞는로부터 얻을 수 있습니다.
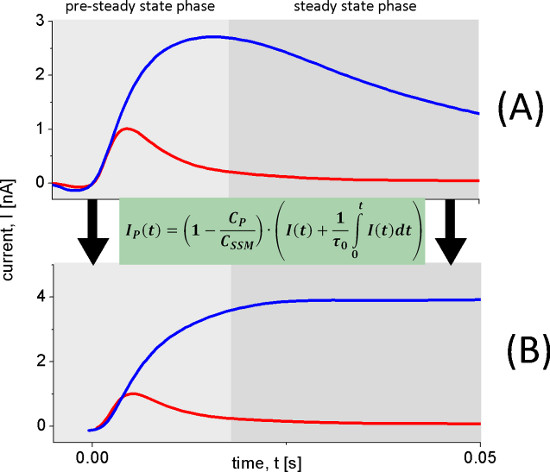
그림 6. 수송 전류의 재건. 과도 전류 (A) 수송 전류 (B)를 재구성하는 데 산도 8.5 (청색 트레이스)와 pH를 5.2 (적색 트레이스) 100 MM의 유당 농도 점프 후 야생형 레이스 proteoliposomes로 측정 하였다. pH가 5.2에서 빠른 electrogenic 반응이 발생하면서 pH에서 8.5 연속 매출이 관찰된다. 이것은 명확하게 복원 된 현재의 (B)에서 관찰된다.
files/ftp_upload/50230/50230fig7.jpg "고도 ="그림 7 "FO : 콘텐츠 너비 ="4 인치 "FO : SRC ="/ files/ftp_upload/50230/50230fig7highres.jpg "/>
그림 7. 과도 전류는 pH가 5.2에서 100 mM의 유당 농도 점프 후 E325A 레이스 proteoliposomes로 측정 하였다.이 모양의 변형은 전송주기의 양성자 방출 단계에서 억제하기 때문에 전송 부족합니다. 관찰 작은 음의 구성 요소는 용량 성 결합 시스템에서 측정 급속한 과도 전류에 대한 특성과 빠른 electrogenic 반응 후 막 용량의 방전에 의해 발생합니다. 그 시간 상수 π0은 시스템 (그림 1)의 커패시턴스와 컨덕턴스에 의해 결정됩니다.
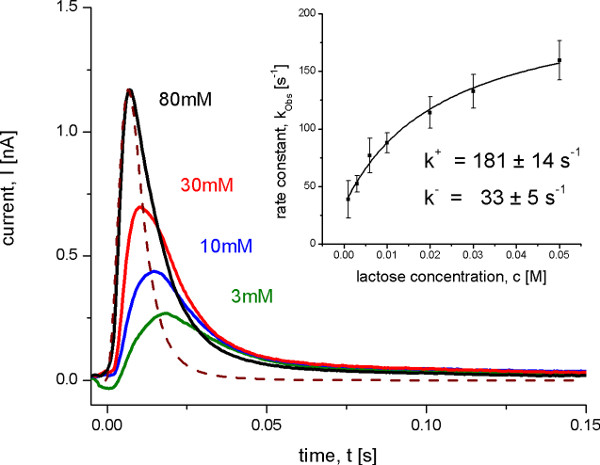
그림 8. 야생형 레이스 proteoliposomes로 측정 과도 전류는 afte를pH가 5.2에서 R 다른 유당 농도 이동합니다.이 조건없이 정상 상태 전송이 관찰하지만, 유당시 electrogenic 구조적 전환 바인딩입니다. 점선은 시스템의 시간 해상도를 나타내는 전달 함수를 보여줍니다. 삽입은 데이터 과장 적합은 관찰 속도 상수 kobs에서 속도 상수에 오프의 결정을 보여줍니다. 관찰 된 속도 상수는 반복적 최소 자승 디컨 볼 루션 알고리즘 10과 과도 전류로부터 결정 하였다.
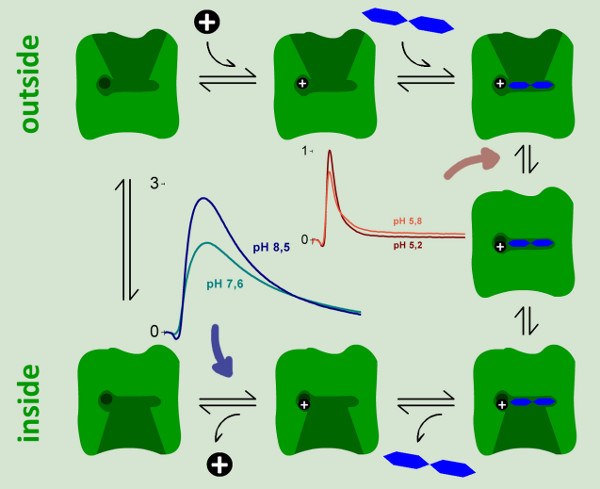
그림 9. 레이스. 두 electrogenic 단계의 반응주기 운동 모델을 식별 SSM 측정을 특징으로 할 수있다. 반응에서 총 책임 변위 ~ 94 %를 나타내는 강하게 electrogenic 반응주기는 중성과 기본의 pH 값에서 관찰된다. 그것은 양성자 방출 단계 (파란색 화살표)에 할당 할 수 있습니다. 야생형 레이스 지속적으로 매출이 억제 될 때 약하게 electrogenic 단계는 산성 pH에서 관찰된다. 우리는 반응주기의 총 책임 변위의 6 %를 나타냅니다 유당 바인딩시 electrogenic 구조적 전환이 반응으로 지정되어 있습니다.
토론
1. SSM 기반의 전기 생리학의 장점은 기존의 방법에 비해
SSM 기반의 전기 생리학은 전기 생리학 도구 상자의 유용한 도구로 자신을 증명하고있다. 그것은 규칙 전기 생리학, 즉 패치 클램프 및 전압 클램프 방법을 적용 할 수없는 경우에 특히 유용 외에도 몇 가지 드문 예외에서 세균 수송 때문에 박테리아의 작은 크기와 때문에 전압 클램프 또는 패치 클램프 방법을 사용하여 조사 할 수 없습니다 그들은 포유 동물 세포 나 난자에서 표현하기가 어렵습니다. 또한 생리학 관련 포유 동물 운송을 조사 할 수 있습니다. 이 경우 SSM 기반의 전기 생리학은 세포 세포막과 때문에 견고성 및 자동화에 대한 가능성의 약물 발견의 심사 응용 프로그램에 대한 운송을위한 매력적이다.
투명의 SSM-basedUsing 기존의 전기 생리학, 시간이 해결 특성orters가 도전합니다. 운송업자의 매출액은 낮기 때문에 '거대한 패치'또는 '전체 세포의 구성이 필요합니다, 솔루션 교환 실험에서 본질적으로 낮은 시간 해상도를 가지고있는. 합병증은 광분해 기판 릴리스를 사용하여 극복 할 수있다. 그러나 기판의 제한된 숫자는이 방법에 적합합니다. 여기에 SSM에서 빠른 솔루션 교환은 임의의 기판을 사용하여 높은 시간 해상도로 전기 생리학 연구를 수행 할 수있는 독특한 기회를 제공합니다.
2. 제한 사항 및 중요한 단계
패치 클램프 및 전압 클램프 기법과는 대조적으로, SSM 기반의 전기 생리학은 전위를 적용 할 수 없습니다. 수송 특성 따라서 막 잠재력에 의존하지 않는 모드를 수송하기 위하여 제한됩니다.
일반적으로, SSM 기반의 전기 생리학이 (electrogenic) 수송의 유형에 관한 아무런 제한이 없습니다. 그러나 전압 CL에게결합 단백질과 같은 세포 구성 요소는 단백질의 기능에 필요한 경우 앰프 나 패치 클램프 방법은 장점을 가지고 있습니다.
솔루션 교환이 큰 이슈 전류를 만드는 경우 제한이 발생할 수 있습니다. 기판 친 유성 화합물의 경우처럼 SSM과 강하게 상호 작용할 때 발생합니다. 아티팩트 컨트롤은 측정 된 신호를 수정하는 데 사용할 수 있습니다. 모든 측정 버퍼에서 더욱 높은 소금 배경 아티팩트를 줄일 수 있습니다. 그러나 경우에, 유물의 크기가 단백질 신호에 비교이고, 그 유물의 단백질 관련 신호를 분리하는 것은 거의 불가능하다. 다행히도, 높은 유물 최적화 된 솔루션 교환 예외적이다.
SSM 기반의 전기 생리학 실험의 성공적인 실현을위한 중요한 몇 가지 단계가 있습니다. 단백질 샘플의 준비는 가장 중요한 부분입니다. proteoliposomes를 사용하는 경우, 반드시 정찰titution 프로세스는 충분한 LPR의 깨끗하고 재생 가능한 샘플을 산출하고 수송이 올바른 방법으로 지향이다. 항체가 가능한 경우 LPR은 ELISA 실험에 의해 동결 골절 전자 현미경과 방향을 확인할 수 있습니다.
만 단백질 샘플을 배양 최적의 매개 변수를 보여줍니다 SSM을 사용합니다. 단백질의 주입은 또 다른 중요한 단계입니다. 초음파가 필수적이며, 기포 주입하는 동안 피해야한다. 기포 센서 칩에서 흡착 된 단백질 샘플을 제거하기 때문에 샘플 배양 한 후 측정 자체가 중요하다. 따라서 항상 솔루션을 변경 한 후 기포를 제거합니다. 그럼에도 불구하고 신호 런이 발생할 수 있습니다. 가능한 신호 런 문제를 해결하기 위해, 실험 기간 동안 런 컨트롤을 수행하는 것이 필수적입니다.
3. 특수 시스템
SSM-설정은 그 용도에 따라 변경 될 수 있습니다. 또한 t여기 완전히 다른, 고도로 전문화 된 설정입니다.
산도 기울기에 따라 예를 들어 비대칭 조건에서 단백질의 신호를 측정 할 수있는 가능성이 있습니다. 세 번째 해결책 내부와 proteoliposomes 외부 비대칭 버퍼 구성을 설정하려면, 휴식 솔루션 도입되어야하며이 두 Exchange 구성이 필요합니다. 여기에 비 활성화 및 휴식 솔루션 사이를 전환 추가로 세 방향 밸브가 필요합니다.
우리는 터미널 밸브를 부족하지만, 큐벳의 다른 유형을 사용하여 다른 흐름 경로를 개발 시스템의 시간 해상도를 증가시킵니다. 여기 활성화 및 비 활성화 솔루션의 접합 SSM 앞에 3mm, 큐벳 내부에 있습니다. 이 설정은 물론 빠른 전송 프로세스의 운동 분석에 적합합니다. 그것은 2 밀리 정도의 낮은 시간 해상도가 가능하다는 것을 보여 할 수 있습니다.
상업 Fully 자동화 시스템은 약물 검사에 대한 훨씬 더 높은 처리량을 목표로 사용할 수 있습니다. 이동식 장치 솔루션을 수집하고 표준의 microtiter 플레이트 형식의 96 - 웰 플레이트에서 센서 표면에 그들을 삽입합니다.
공개
관심 없음 충돌 선언하지 않습니다.
감사의 말
우리는 지원과 도움이 토론의 레이스 측정 및 E. 밤베르크에 공헌 J. 가르시아 CELMA, I 미르 노바와 R. Kaback 감사합니다.
자료
| Name | Company | Catalog Number | Comments |
| Materials | |||
| Waterbath Sonicator | Bandelin | RK 52 H | |
| Tip Sonicator | Hielscher Ultrasonics GmbH | UP50H | |
| 2-way valve | NResearch, West Caldwell, USA | NR225T011 | |
| Terminal valve | NResearch, West Caldwell, USA | NR225T031 | |
| Manometer | Greisinger electronics | GDH 14 AN | |
| Faraday cage | Max Planck Institute of Biophysics | ||
| Cuvette | Max Planck Institute of Biophysics | ||
| 100 ml solution containers | Kartell | 1623 | |
| O-rings | Seal Science Inc. | ||
| Oscilloscope | Tektronix | TDS 1002 | |
| Reference electrode | Max Planck Institute of Biophysics | ||
| Function generator | Max Planck Institute of Biophysics | ||
| Tubings | SAINT-GOBAIN Performance Plastics | AAC00006 | |
| Sensor chip | Fraunhofer Institut für Schicht und Oberflächentechnik | ||
| Interface box | Max Planck Institute of Biophysics | ||
| Amplifier | Keithley | 427 | |
| Manual cog | Vygon GmbH | 876 | |
| USB analog-to-digital converter | National Instruments | 6009 | |
| Regeants | |||
| 1,2‑Diphytanoyl-sn-glycero-3-Phosphatidylcholine | Avanti Polar Lipids, Inc. | 850356 | |
| Acrylamide/Bis-acrylamide | Sigma Aldrich | A3574 | |
| Ammonium persulfate | Sigma Aldrich | A3678 | |
| D-(+)-Glucose | Sigma Aldrich | G8270 | |
| Dithiothreitol | Sigma Aldrich | 43819 | |
| Ethanol absolut | VWR AnalaR NORMAPUR | 603-002-00-5 | |
| Natural E. coli lipids polar extract | Avanti Polar Lipids, Inc. | 100600 | for LacY reconstitution |
| n-Decane | Sigma Aldrich | D901 | |
| Octadecanethiol | Sigma Aldrich | O1858 | |
| Octadecylamine | Sigma Aldrich | 74750 | |
| Potassium chloride | Merck | 1049360500 | |
| Potassium phosphate dibasic | Sigma Aldrich | P3786 | |
| Potassium phosphate monobasic | Sigma Aldrich | P9791 | |
| Tetramethylethylenediamine | BIO RAD | 1610801 | |
| α-Lactose monohydrate | Sigma Aldrich | L8783 | |
참고문헌
- Seifert, K., Fendler, K., Bamberg, E. Charge transport by ion translocating membrane proteins on solid supported membranes. Biophys. J. 64, 384-391 (1993).
- Schulz, P., Garcia-Celma, J. J., Fendler, K. SSM-based electrophysiology. Methods. 46, 97-103 (2008).
- Garcia-Celma, J. J., et al. Rapid activation of the melibiose permease MelB immobilized on a solid-supported membrane. Langmuir. 24, 8119-8126 (2008).
- Mager, T., Rimon, A., Padan, E., Fendler, K. Transport mechanism and pH regulation of the Na+/H+ antiporter NhaA from Escherichia coli: an electrophysiological study. J. Biol. Chem. 286, 23570-23581 (2011).
- Zhou, A., et al. Charge translocation during cosubstrate binding in the Na+/proline transporter of E.coli. J. Mol. Biol. 343, 931-942 (2004).
- Ganea, C., Fendler, K. Bacterial transporters: charge translocation and mechanism. Biochim. Biophys. Acta. 1787, 706-713 (2009).
- Schulz, P., Werner, J., Stauber, T., Henriksen, K., Fendler, K. The G215R mutation in the Cl-/H+-antiporter ClC-7 found in ADO II osteopetrosis does not abolish function but causes a severe trafficking defect. PLoS ONE. 5, e12585 (2010).
- Schulz, P., Dueck, B., Mourot, A., Hatahet, L., Fendler, K. Measuring ion channels on solid supported membranes. Biophys. J. 97, 388-396 (2009).
- Garcia-Celma, J. J., Smirnova, I. N., Kaback, H. R., Fendler, K. Electrophysiological characterization of LacY. Proc. Natl. Acad. Sci. U.S.A. 106, 7373-7378 (2009).
- Garcia-Celma, J. J., Ploch, J., Smirnova, I., Kaback, H. R., Fendler, K. Delineating electrogenic reactions during lactose/H+ symport. Biochemistry. 49, 6115-6121 (2010).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유