JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
실험 방법 및 높은 Siderophile 요소 흠을 억제하는 프로토콜 : 높은 압력과 온도에서 금속 규산염 분할
요약
We present a procedure to determine the metal-silicate partitioning of siderophile elements, emphasizing techniques that suppress the formation of metal inclusions in experiments for the noble metals. The results of these experiments are used to demonstrate the effect of core-formation on the highly siderophile element composition of the mantle.
초록
Estimates of the primitive upper mantle (PUM) composition reveal a depletion in many of the siderophile (iron-loving) elements, thought to result from their extraction to the core during terrestrial accretion. Experiments to investigate the partitioning of these elements between metal and silicate melts suggest that the PUM composition is best matched if metal-silicate equilibrium occurred at high pressures and temperatures, in a deep magma ocean environment. The behavior of the most highly siderophile elements (HSEs) during this process however, has remained enigmatic. Silicate run-products from HSE solubility experiments are commonly contaminated by dispersed metal inclusions that hinder the measurement of element concentrations in the melt. The resulting uncertainty over the true solubility and metal-silicate partitioning of these elements has made it difficult to predict their expected depletion in PUM. Recently, several studies have employed changes to the experimental design used for high pressure and temperature solubility experiments in order to suppress the formation of metal inclusions. The addition of Au (Re, Os, Ir, Ru experiments) or elemental Si (Pt experiments) to the sample acts to alter either the geometry or rate of sample reduction respectively, in order to avoid transient metal oversaturation of the silicate melt. This contribution outlines procedures for using the piston-cylinder and multi-anvil apparatus to conduct solubility and metal-silicate partitioning experiments respectively. A protocol is also described for the synthesis of uncontaminated run-products from HSE solubility experiments in which the oxygen fugacity is similar to that during terrestrial core-formation. Time-resolved LA-ICP-MS spectra are presented as evidence for the absence of metal-inclusions in run-products from earlier studies, and also confirm that the technique may be extended to investigate Ru. Examples are also given of how these data may be applied.
서문
지상파 증가는 달의 형성 1, 2에 대한 책임을 생각 거대한 충격 단계에서 종료, chondritic 벌크 조성 행성 체 사이의 충돌의 시리즈로 발생한 것으로 생각된다. 충격에 의한 원시 지구와 수명이 짧은 동위 원소의 붕괴 난방 광범위한 용융 마그마 바다와 철 풍부한 금속의 용융이 내려 수 조밀 통해 연못의 형성을 야기하기에 충분했다. 마그마 바다의 바닥에 도달하면, 금속 용융은 유동 학적 경계, 실속 발생, 결국 성장 코어 2 고체 맨틀을 통해 내려 전에 최종 금속 규산염 평형을받을. 용융 금속과 같은 금속 실리케이트 상간 또한 화학 통신 맨틀의 중실 부 인해 대형 금속 다이아 퍼 (3)의 급속한 하강에 배제되는 것으로 생각된다 횡단. 금속 코어 및 규산염 녀 mant에 지구의이 차 분화6 - 제작은 모두 지구 물리학 및 지구 화학적 관찰 (4)에 의해 오늘 공개된다. 마그마 바다의 바닥에 금속 규산염 평형에 대한 설득력있는 조건을 산출하기 위해 이러한 관찰을 해석하지만, 실험 결과의 적절한 데이터베이스가 필요합니다.
프리미티브 상부 맨틀 (PUM)는 코어 형성 실리케이트 잔기를 갖는 가상의 저장이며 따라서 그 조성은 금속 규산염 평형 중에 미량 원소의 동작을 반영한다. 미량 원소는 그 화학적 친화도에 근거하여 코어 편 중에 용융 금속 규산염 사이에 분포된다. 금속 상에 대한 기본 요소의 크기는 금속 실리케이트 분배 계수에 의해 설명 될 수 있습니다 
 (1)
(1)
어디에  과
과 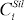 나는 금속 규산염 각각 녹아 원소의 농도를 나타낸다. 의 값
나는 금속 규산염 각각 녹아 원소의 농도를 나타낸다. 의 값 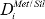 > 1 siderophile (철 사랑)의 행동과 그 <1 lithophile (바위 사랑) 동작을 나타냅니다. 요소를 siderophile PUM 조성 쇼의 추정은 일반적으로 지구의 대량 구성 6,8의 대표로 간주 구립 운석 7에 상대적으로 고갈된다. 이 고갈 핵심으로 siderophile 요소의 격리로 인해, 내화물 요소의 크기는 직접 값을 반영해야
> 1 siderophile (철 사랑)의 행동과 그 <1 lithophile (바위 사랑) 동작을 나타냅니다. 요소를 siderophile PUM 조성 쇼의 추정은 일반적으로 지구의 대량 구성 6,8의 대표로 간주 구립 운석 7에 상대적으로 고갈된다. 이 고갈 핵심으로 siderophile 요소의 격리로 인해, 내화물 요소의 크기는 직접 값을 반영해야 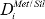 . 실험실 실험은 따라서의 값을 결정하고자
. 실험실 실험은 따라서의 값을 결정하고자 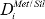 RA 이상압력 (P), 온도 (T)와 산소 분압 (f를 O 2) 마그마 바다의 기지에서 금속 분리와 관련된 조건의 NGE. T - -이 실험의 결과는 다음의 P 영역을 서술하기 위해 사용될 수있다 F의 O를 여러 siderophile 소자 PUM 풍부와 호환이 공간 (예를 들어, 9-11).
RA 이상압력 (P), 온도 (T)와 산소 분압 (f를 O 2) 마그마 바다의 기지에서 금속 분리와 관련된 조건의 NGE. T - -이 실험의 결과는 다음의 P 영역을 서술하기 위해 사용될 수있다 F의 O를 여러 siderophile 소자 PUM 풍부와 호환이 공간 (예를 들어, 9-11).
높은 압력과 마그마 바다 시나리오에 관련된 온도는 피스톤 실린더 또는 다중 모루 프레스를 사용하여 실험실에서 재현 할 수 있습니다. 피스톤 실린더 장치는 중간 압 (~ 2 GPA) 및 고온 (2573 ~ K)의 조건에 대한 액세스를 제공하지만, 대규모 샘플 볼륨과 용이하게 사용될 수있는 캡슐 재료의 다양성을 가능하게한다. 빠른 냉각 속도는 따라서 런 제품의 조직 해석을 단순화로 실리케이트 유리 조성물의 용융 범위의 소광을 허용한다.멀티 모루 장치는 일반적으로 작은 샘플 볼륨을 사용하지만 적절한 어셈블리 설계와 압력에 ~ 27 GPa의와 ~ 3,000 케이의 온도 이러한 방법의 사용은 적당히의 많은 파티션의 데이터를 허용하고 약간 요소가 될 siderophile있다을 달성 할 수있다 T 조건 - (P)의 넓은 범위에 걸쳐 모였다. 이들 데이터에 기초 PUM 조성물의 예측 모델이 정확한 값 의존하더라도 금속 규산염 평형 각각 ~ 초과 평균 압력 및 온도 조건에서 29 GPa 인 3000 K를 발생 시사한다. (예를 들면, V, CR) 2는 또한 공존 철, 위스 타이트에 의해 부과 된 그 아래 ~ 4-2 로그 단위에서 증가하는 동안 진화를 생각하는 f를 O (특정 산화 환원에 민감한 요소의 PUM의 풍요 로움에 대한 FeO의를 설명하기 위해 ) 상당 PT 조건 (철 위스 타이트 버퍼) 12.
비록 M의 PUM 풍부어떤 siderophile 요소가 깊은 마그마 바다의 바닥에 금속 규산염 평형에 의해 설명 될 수 있습니다, 그것은이 상황이 또한 가장 높은 siderophile 요소 (HSES)에 적용하는 경우 평가하기 어려운 입증했다. 낮은 압력 (P ~ 0.1 MPa의) 및 온도 (T <1673 K) 실험에 의해 표시 철 금속 HSES의 극단적 인 친 화성 규산 지구가 강하게 이러한 요소 고갈해야합니다 제안합니다. PUM위한 HSE 콘텐츠의 추정은, 그러나, (도 1) 콘드 라이트 만 적당한 공핍 대하여 나타낸다. 명백한 HSE 초과에 일반적으로 상정 솔루션은 지구가 핵심 형성 (13) 이후 chondritic 재료의 늦은 증가를 경험한다는 것이다. 이 늦은 인한이자 재료는 PUM와 혼합 HSE 농도를 상승하지만, 더 풍부한 요소에 무시할 영향을했을 것이다. 또는, HSES의 매우 낮은 자연 siderophile P로 나타낸 것이 제안되었다 - T 실험 코어 형성 14, 15 중에 존재하는 높은 PT 상태로 유지되지 않습니다. 이러한 가설을 검증하기 위하여, 실험은 적절한 조건에서 HSES의 용해도 및 금속 실리케이트 분할을 결정하기 위해 수행되어야한다. 그러나 많은 선행 연구에서 담금질 실행 제품의 규산염 부분의 오염, 실행 제품 분석을 복잡하고 금속과 규산염 용융물 사이 HSES에 대한 진정한 분배 계수를 가려있다.
HSES 자연에 적합한 농도 수준에 존재하는 파티션 실험에서, 철 금속에 대한 이러한 요소의 극단적 인 기본 설정은 규산염 용융 자신의 측정을 방지 할 수 있습니다. 이 문제를 회피하기 위해, 용해도 측정은 관심의 값 HSE에있는 규산염 용융물이 포화 만들어진다 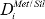 보리 소프의 등의 형식주의를 사용하여 계산등. (16). 환원 조건에서 수행 HSE 용해도 실험으로부터 담금질 실리케이트 런 제품, 그러나 종종 분산 HSE ± 철에 의한 오염에 대한 근거를 표시하는 17 개재물. 낮은 F 오에서 이러한 개재물의 가까운 편재에도 불구하고 태평양 표준시의 Ir, O를, 다시와의 Ru를 포함하는이 실험은, (예를 들어, 18-27), 자신의 조직 프레젠테이션의 연구 사이에 주목할만한 변화가있다; 예를 들어 22, 26 참조를 비교합니다. 이 개재물은 실험 28의 실행 조건에서 안정한 상을 형성 할 수있는 것으로 입증되었지만, 샘플 켄칭 될 때,이 개재물의 형성을 배제하는 것은 아니다. 개재물의 원점 주변 불확실성 분석 결과의 처리가 곤란하게하고, 감소 된 실리케이트 녹에 HSES의 진정한 용해도 이상 모호하게되었다. 포함이없는 실행 제품은 평가해야합니다어떤 연구는 정확한 용해 HSE 농도를 산출 분석 접근 방식을 채택하고있다. 31 - 환원 조건에서 금속 개재물의 형성을 억제하는데 상당한 진전 이제 샘플 디자인이 원료 (29)의 Au 또는 Si를 추가하여 기존의 연구에서 개정하는 피스톤 - 실린더 장치를 이용한 실험에서 입증되었다. 출발 물질에 금이나 원소의 Si 첨가는 각각의 실험 샘플 기하학 또는 F O 2 진화를 바꾼다. 이들 방법은 샘플에 확산 환원 대 HSE의 타이밍을 변경하여 금속 개재물 형성을 억제하도록 구성되며, 베넷 외. (31)에서 논의된다. 이러한 기계적으로 지원 평형 및 원심 분리 피스톤 실린더와 같은 내포물의 규산염 용융물을 정화하는 몇 가지 이전의 시도와는 달리, 본 프로토콜은 전문 appar없이 구현 될 수있다ATUS과 높은 PT 실험에 적합합니다.
보리 소프의 등의 형식주의를 사용하여 계산등. (16). 환원 조건에서 수행 HSE 용해도 실험으로부터 담금질 실리케이트 런 제품, 그러나 종종 분산 HSE ± 철에 의한 오염에 대한 근거를 표시하는 17 개재물. 낮은 F 오에서 이러한 개재물의 가까운 편재에도 불구하고 태평양 표준시의 Ir, O를, 다시와의 Ru를 포함하는이 실험은, (예를 들어, 18-27), 자신의 조직 프레젠테이션의 연구 사이에 주목할만한 변화가있다; 예를 들어 22, 26 참조를 비교합니다. 이 개재물은 실험 28의 실행 조건에서 안정한 상을 형성 할 수있는 것으로 입증되었지만, 샘플 켄칭 될 때,이 개재물의 형성을 배제하는 것은 아니다. 개재물의 원점 주변 불확실성 분석 결과의 처리가 곤란하게하고, 감소 된 실리케이트 녹에 HSES의 진정한 용해도 이상 모호하게되었다. 포함이없는 실행 제품은 평가해야합니다어떤 연구는 정확한 용해 HSE 농도를 산출 분석 접근 방식을 채택하고있다. 31 - 환원 조건에서 금속 개재물의 형성을 억제하는데 상당한 진전 이제 샘플 디자인이 원료 (29)의 Au 또는 Si를 추가하여 기존의 연구에서 개정하는 피스톤 - 실린더 장치를 이용한 실험에서 입증되었다. 출발 물질에 금이나 원소의 Si 첨가는 각각의 실험 샘플 기하학 또는 F O 2 진화를 바꾼다. 이들 방법은 샘플에 확산 환원 대 HSE의 타이밍을 변경하여 금속 개재물 형성을 억제하도록 구성되며, 베넷 외. (31)에서 논의된다. 이러한 기계적으로 지원 평형 및 원심 분리 피스톤 실린더와 같은 내포물의 규산염 용융물을 정화하는 몇 가지 이전의 시도와는 달리, 본 프로토콜은 전문 appar없이 구현 될 수있다ATUS과 높은 PT 실험에 적합합니다.
여기에 상세히 기재된 고온 (> 1873 K), 2 GPa의과 유사한 F의 O 2에서 규산염 용융물에 재현하여 OS,의 Ir, Ru로, Pt 및 Au로의 용해도를 결정하기 위해 피스톤 - 실린더 기반 접근법 철 위스 타이트 버퍼. 유사한 실험 설계의 응용 프로그램은 또한, 요구되는 위상 관계를 제공하는 특성을 습윤제, 다른 압력에서 HSE 실험에서 성공적인 증명할 수 있고 운동 관계는 선택 조건으로 유지. 그러나 기존 데이터는, 우리의 샘플 디자인은 깊은 마그마 바다에 해당하는 압력에서 성공 여부를 예측하기에 충분하다. 또한 윤곽 적당히 약간 siderophile 소자 (MSE와 각각 SSE) 멀티 앤빌 장치를 사용하여 분할을 결정하는 데 사용되는 일반적인 접근법이다. 높은 압력 HSES의 포함이없는 데이터 세트의 확장과 유사한 멀티 모루 방법을 채택 할 가능성이있다. 옷에테르, 이러한 절차는 코어 - 분리의 조건으로 지상파 증가의 단계 모두를 제한하는 수단을 제공한다.
프로토콜
출발 물질의 1)의 제조
- 합성 현무암
참고 : 현무암 조성물은 더 탈 중합 조성물로 출발 물질 규산염으로 사용, 피스톤 실린더 및 멀티 모루 실험에서 유리 해소하기 어렵거나 불가능 마그마 바다 시나리오에 더 관련이 있지만.- 철을 제외한 성분 산화물 또는 카보네이트 (칼슘 및 NA) 분말의 원하는 양을 계량하고, 마노 막자 사발에 추가 (표 1의 예를 참조). ~ 4g 체중의 Fe가없는 혼합물을 실험 양한 충분한 출발 물질을 제공한다.
- 이어서 분말 혼합물의 조성 및 입자 크기를 모두 균질화 아게이트 유봉을 이용하여 적어도 두 시간 동안 분쇄 침수 때까지 마노 모르타르에 에탄올을 추가한다.
참고 : 대지 출발 조성물의 균질성 사형 전자 MIC와 분말 혼합물의 펠렛을 가압 조사함으로써 확인할 수있다roscope는 에너지 분산 형 X 선 분광법에 의한 조성 분석에 장착. - 일단 완전히 균질화 ~ 20cm의 거리에서, 250 W의 가열 램프 아래에 박격포를 배치합니다. 분말 혼합물은 건조 후 20 ~ 60 분의 시간이 걸릴 수 있음, 알루미나 또는 멀 라이트 (알루미 노 - 실리케이트) 도가니 중 하나에 전송할 수 있습니다.
- 혼합물는 탄산, RT에서 상자로에 분말 혼합물과 도가니를 배치하고 3-5 시간에 걸쳐 1273 K로 램프. 1273 펀치 / N에로의 혼합물을 남겨주세요.
- 박스 퍼니스에서 탈 탄산 혼합물을 분리하고 RT로 냉각되도록. 일단 멋진, 무게 및 FeO의 또는 철 2 O 3 분말 (표 1 참조) 중 하나로 혼합물에 철을 추가합니다. 총 Fe 함유량을 유지하면서 철 2 O 3의 FeO의 비율을 변화 동일한 샘플의 마지막 F의 O이 변경 될 수있다. 환원 조건 더 액세스하려면, 모든 실험에서 (P)를 조사하기 위해T, 또한 혼합물에 ~ 0.5 ~ 2.0 중량 %의 Si를 추가합니다. 철 (±시)이 추가되면, 다시 마노 박격포와 유 봉 에탄올에서 분쇄 된 혼합물을 다시-균질화.
- 가열 램프하에 균질화 된 혼합물을 건조하고 쉘 바이알로 옮긴다. 준비가 될 때까지 데시 케이 터에 보관 샘플 캡슐을로드합니다.
- 금속 단계 : 다시, O를,의 Ir, Ru로 실험
- 고순도의 금속 분말을 사용하여, 금과 관심 HSE의 혼합물 : 1 중량 (RU 대 1 원자 질량의 차이를 고려하여 6) 의도 실험 재하여 OS, IR 또는 Ru로 조사하기 위해, 3을 제조 . ~ 500 mg 중량의 혼합물을 실험 양한 충분한 출발 물질을 제공한다.
- 흑연 도가니에 혼합물을 전송하고 흑연 뚜껑 커버. 이어서 ~ 5 분 동안 1473 K의 온도에서 상자로에 덮여 도가니를 배치했다. 노로부터 제거되면 조립체 COO를 가질 때까지 제 위치에 도가니 뚜껑을 남겨RT되었다.
주의 : 공기 오스뮴의 난방 독성 화합물의 산화 오스뮴의 형성의 원인이 될 수 있습니다. 오스뮴 금속은 CAS 번호 7440-04-2에 대한 MSDS (물질 안전 보건 자료)를 참조, 또한 알려진 피부 자극을 일으킬 수 있습니다.
주 :이 프로세스의 Au (융점 ~ 1337 K)를 용해하지 그러나 첨부 HSE 관심 HSE Au로의 껍질로 둘러싸여 금속 비드의 형성을 초래. - 흑연 도가니 금속 비드를 제거하고 그 긴 치수 ~ 1mm 측정 작은 조각으로 분할하는 면도날을 사용한다. 절단 후, 데시 케이 터에서 쉘 유리 병 및 저장소에 구슬을 배치합니다.
- 금속 단계 : 백금 실험
주 : 실험 편 인해 고온에서 Pt 및 Au로 완전 혼 화성에 금 코팅 비드 기법을 사용하여 수행 될 수 조사 (> 2042 K에서 0.1 MPa의 32). 이 편 물리적 껍질 의해 실험 동안 규산염 용융물로부터 분리된다 샘플 형상을 배제금의.- 혼합물 ~ 500 mg의 총을 1 중량 비율 철저히 1 편 및 IR의 금속 분말을 혼합한다. 철은 총 혼합물의 ~ 4 중량 %를 포함하도록 다음 ~ 금속 철 분말 20 mg을 추가.
- 작업대의 가장자리 테이프 (또는, 드릴 섕크, 드릴 블랭크 대신에 사용될 수있다) 빈 깨끗한 드릴 탁상 3 ~ 해당 MM 돌출 그래서. 드릴 빈의 돌출 끝에, 2-3mm ~의 내부 직경 4-6mm ~의 외부 직경, 석영 유리 튜브를 놓습니다.
- 유리관에 PtIrFe 혼합물을 놓고 그 위에 다른 드릴 공백을 삽입합니다. 두 드릴 블랭크 석영 유리 튜브의 내경보다하게는 0.1 mm보다 작은 직경을 가져야한다. 손으로 함께 드릴 보호 물을 밀어 금속 혼합물 콜드 프레스 (그림 2).
주의 : 콜드 프레스 공정 동안 과도한 힘의 사용은) 실리카 유리가 산산조각이 발생할 수 있습니다. - 알루미나 도가니에, 석영 유리관 내부에 여전히 초기 가압 분말을 넣어 가스 혼합 수직 튜브 노의 차가운 부분에서 중단. 1673 K로 가열로 온도를 상승하고 CO-CO 2 가스 혼합물을 사용하여, 철 위스 타이트 버퍼에 가까운 값으로 노 F의 O 2를 설정한다.
참고 : 주위 압력과 1673 K에서, 철 위스 타이트 버퍼가 1.93 × 10 -10 F O를 2 아빠 (33)에 해당한다. 비, 온도 및 F의 O 2를 혼합 CO-CO (2) 사이의 관계는 기준 (34)에서 찾을 수있다. 1673 K에서의 철 위스 타이트 버퍼 22.25 부피 % CO 2 및 77.75 부피 %의 CO를 포함하는 기체 혼합물을 사용한다.- 원하는 온도와 F O 2에 도달하면, 그 노 핫 스폿에 위치되도록, 알루미나 도가니를 낮추고 어닐링 가압 분말에 대한 O / N을 떠난다.
- cruc 제거ible 및 가스 혼합로에서 분말을 누르면하고 냉각 할 수 있습니다. 실리카 유리 튜브가 그대로이면, 튜브의 열처리 분말을 밀어 드릴 블랭크를 사용한다. 와이어 커터를 사용하여, 실험을 위해 선택된 샘플 캡슐 내에 맞도록 충분히 작은 조각으로 열처리 분말을 깰.
- 필요한 때까지 데시 케이 터에서 쉘 유리 병 및 저장소에 금속 조각을 전송합니다.
- 금속 단계 : 멀티 모루 실험
- 실험은 적당히 약간 siderophile 요소의 분할을 결정하기 위해, 동일한 비율로 철 금속 분말 합성 현무암 가루를 섞는다.
주 : 철의 일부는 Si를 <8 중량 % 포함하는 금속 부분의 통상적도록의 Fe-Si 합금으로서 첨가 될 수있다. 이 실험 F의 O 2가 낮게 유지 보장합니다. - 현무암 플러스 금속 혼합물에 금속 산화물 분말로 선택 미량 원소를 추가합니다. GR에 의해 출발 물질 균질화마노의 박격포와 유 봉 에탄올에서 inding. 요소에 따라 달라질 것이다 미량 첨가 원소의 정확한 양이 조사되고, 그러나, 수천 ppm의 2 중량 %의 공칭 농도 10,35 전형적인.
- 일단 균질화, 가열 램프하에 출발 물질 분말을 건조 할 때까지 필요한 데시 케이 터 내에서 쉘 바이알에 저장 한 다음을 전송할.
- 실험은 적당히 약간 siderophile 요소의 분할을 결정하기 위해, 동일한 비율로 철 금속 분말 합성 현무암 가루를 섞는다.
조립 부품 2. 준비
- 피스톤 실린더
주 : 피스톤 실린더 조립체는 마그네시아 압착 편을 이용한 흑연 저항 히터의 핫 스폿에지지되어 흑연 캡슐로 구성되어있다. 알루미나 피복 열전대는 시료의 상단에 온도를 모니터링하기 위해 조립체의 상부 부분을 통해 축 방향으로 위치된다. 노이어서 압력 매체 및 열 절연체 (36) 모두로 작동 된 BaCO3 세포에 의해 둘러싸여있다. 조립 치수가 제공된다도 3a. 실험 및 그 소스에 사용되는 예시적인 재료의 목록은 표 2에 제공된다.- 기계 재료를 (도 3a)을 시작으로 각각 고순도 흑연 마그네시아 봉 또는 관을 사용하여 중심 선반과 필요한 치수 캡슐 흑연, 흑연 단부 플러그 마그네시아지지 편.
주 : 실험 재, O가 및 IR을 조사하기 위해, HSE-FE 합금 캡슐 재료 29,30로서 흑연 대신 할 수있다. - 분말 원료에 대한 지시에 따라 동일한 방식으로 가열 램프하에 건조한 후, 실온에서 1 분 ~ 에탄올 흑연 캡슐 초음파 처리. 필요한 때까지 일단 건조, 건조기 또는 건조 오븐에서 쉘 유리 병 및 저장소에 캡슐을 전송합니다.
- 최소 8 시간 동안 상자로에서 1573 K에서 알루미나 멀 라이트 도가니 어닐링 하나의 마그네시아 지원 조각을 놓습니다. 어닐링 후, 조각 다음 저장소를 냉각 할 수 있도록건조 오븐 ~ 393 K. 유지
- 중량 비율 1 : 탄산 바륨 세포를 만들기 위해, 제 99 된 BaCO3 분말 및 사용 복사본 토너를 혼합한다. 혼합물의 7.4 그램의 최소 하나의 실험이 필요합니다. 코트 흑 연계 윤활제 건조 또는 PTFE 계 이형제 (표 2) 중 하나와 적절한 크기의 스틸 다이의 내부 부분 (된 BaCO3 슬리브의 치수는도 3a 참조).
- 스틸 다이 및 유압 프레스를 사용하여 ~ 250 MPa의에 혼합물의 콜드 프레스 3.7 G. 압축 해제하기 전에 1 분 동안 압력에서 혼합물을 남겨주세요. 이것은 17 mm의 높이로 슬리브를 제조한다. 두 소매는 각각의 조립이 필요합니다.
주 :이 셀 배열은 상술 29 일부 이전 연구에서 사용 - 31 번의 된 BaCO3 셀 적절한 크기의 다이가 사용할 수 제공 치환 될 수있다. - 에서 제거되면구동 오프 복사 토너 ~ 30 분간이 온도에서 보유 후, 상자 노에서 수 시간에 걸쳐 RT까지 923 K에서 슬리브를 가열함으로써, 다이. 복사 토너가 제거 된 후 오렌지에 검은 색에서 색의 변화를합니다. 오븐 ~ 393 K. 유지 건조에 어닐링 소매를 저장
- 기계 재료를 (도 3a)을 시작으로 각각 고순도 흑연 마그네시아 봉 또는 관을 사용하여 중심 선반과 필요한 치수 캡슐 흑연, 흑연 단부 플러그 마그네시아지지 편.
- 멀티 모루
주 : 멀티 앤빌 조립체 압착의 MgO 또는 알 2 O 3 필러 부재를 사용 원통형 흑연 히터 저항의 핫 스폿에 위치하는 샘플의 캡슐을 포함한다. 히터는 압력 매체 및 단열재 모두 역할을 소결 또는 주조 세라믹 면체 하나에 의해 둘러싸여있다. 열전쌍 어셈블리 설계에 따라 하나의 축 방향 또는 횡 방향으로 배치 될 수있다. 원하는 목적 및 P에 따라 멀티 모루 실험에 사용되는 다양한 크기와 어셈블리의 디자인이 있습니다 -. T 조건은 4 표시로 그림sembly 이전에 3.6 및 7.7 GPa의 35 금속 규산염 분할 실험을 수행하는 데 사용되는 디자인.- 피스톤 실린더 실험에 나타낸 바와 같이 동일한 방법으로 고순도 흑연 튜브의 캡슐 및 압착 마그네시아, 지르코니아 또는 슬리브를 준비한다. 필요한 치수는 그림 4a에 제공됩니다.
- 하드 해고 알루미나로드의 길이에서 알루미나 플러그를 확인합니다. 다음 손으로 필요한 길이로 막대를 고정, 그것은 파괴 될로드 점수 다이아몬드 파일을 사용 (치수도 4a 참조). 로드을 깨는 결과 모든 털을 제거 할 파일을 사용합니다. 실온에서 에탄올에 초음파를하여 플러그를 청소합니다.
- ㆍ MgO 계 캐스터 블이 부분을 이용하여 세라믹 18mm 팔면체 에지 길이 (OEL)로 팔면체를 준비하고 적절한 크기의 주형 (표 2 참조). 몰드 번째 요망 것과 동일한 두께로 시트에 의해 분리 8 절두 큐브를 보유 지그를 포함즉 개스킷 (37)을 미리 형성했다.
- 18mm (OEL)와 팔면체를 들어, 3mm 두꺼운 11 가장자리 길이 (TEL) 절단 MM 및 시트에 사용 큐브. 큐브와 시트 재료 알루미늄 또는 PVC를 사용합니다. 실리콘 그리스와 주조 세라믹 문의 모든 부품을 윤활, 금형을 조립합니다. 세라믹 혼합물에 대한 진입 점을 제공하기 위해 조립되지 않은 하나의 큐브를 남겨주세요.
- (100)에서 분말 세라믹 및 액체 활성화 결합 : 30 중량 비율을 철저하게 섞는다. 공기의 어떤 포획 된 포켓이 없는지 확인, 금형에 혼합물을 부어. 나머지 큐브를 넣고 혼합물이 적어도 2 시간 동안 설정할 수 있습니다. 각 면체는 ~ 세라믹 혼합물의 15g이 필요합니다.
- 일단 ~ 2 시간 동안 상자로에서 1,273-1,373 K에서 건조 후 393 K에서 오븐 어닐링에 ~ 1 일 탈수, 금형에서 면체를 제거, 설정합니다.
- 에 나타낸 면체 공기 중에서 실온으로 식힌 후, 7.3 mm 직경의 구멍을 뚫도 4b는 절연 슬리브, 흑연 히터 그리고 남은 샘플 성분을 수용한다.
- 준비가 될 때까지 ~ 393 K에서 건조 오븐에 보관 실험을 조립합니다.
구성 요소 3. 총회
- 피스톤 - 실린더 어셈블리의 실험
- 제 캡슐이 채워질 때까지 합성 현무암 분말을 첨가 한 다음 HSE 베어링 금속을 삽입하여 흑연 샘플 캡슐을로드. 중력 안정 장치의 사용은 실험 중에 전복에 대한 가능성을 최소화하고 기계적 작용을 통해 금속 위상의 분산을 방지하기위한 것이다.
- 캡슐 샘플을 보유하기위한 공동의 바닥에 건식 산화 마그네슘 분말을 소량 (일반적으로 <50 mg)을 놓는다. 이 구멍을 드릴 때 생성되는 테이퍼면을 평평하게하고 다시 캡슐을 깰 수 샘플 압축시 전단력을 감소시킨다.
- 이전에 미친 조립 모든도 3b에 도시 된 바와 같이 전자 부품.
- 하단 된 BaCO3 소매의 노출 끝을 통해 박의 작은 (~ 1.5 ㎜) 부분을 접는, 조립 30 μm의 두께 리드 호일의 조각을 감싸. (위) 및베이스 플러그도 3a에 도시 된 바와 같이 스틸 엔드 피스 (아래)와 함께, 12.7 mm 내경 텅스텐 카바이드로 압력 용기 조립체를 삽입한다.
참고 : 최종로드 피스톤 실린더 장치는 2 유압 램이있다. 낮은 램을 벌리고 다리는 텅스텐 카바이드 피스톤이 샘플의 바닥에 압력을 적용 할 수 있습니다. 상부 RAM 상부 샘플 표면의 위치를 고정하고 텅스텐 카바이드 코어 (38)에 추가적인 지원을 제공 압력 용기에 최종 하중을인가한다.도 3c는 대신 다리 토론토 대학 피스톤 실린더 장치를 나타낸다. -13 %의 마찰 보정 샘플 공칭 압력 사이의 차이를 고려하여 적용샘플 (39)에 의해 경험 D. - 유압 램 사이의 다리, 압력 용기 및베이스 플레이트를 놓습니다. 다음에 1.6 mm의 외경 4 홀 하드 소성 알루미나 튜브를 사용하여 C 형 열전대를 만든다. 알루미나 튜브는 상부 플레이트의 상면으로부터 돌출하는 튜브 ~ 1-2 mm의 허용하기에 충분히 긴 절단한다.
- 튜브에 인접한 구멍을 통해 두 와이어 조성 (표 2 참조) 피드 180도를 통해 끝을 켜고 선이 교차하도록 반대 구멍을 고정합니다. 접합이 직접 샘플 위에 있도록 상판 통해 어셈블리에 열전대를 삽입한다. 단부에서 노출 10-20 밀리미터 부를두고 유연한 테프론 튜브를 사용 열전쌍 와이어의 나머지를 절연 시키.
- 상판과 상부 램 사이의 장소에 필요한 금속 스페이서를 놓습니다. 조립시, 위치 일러 시트 양쪽 압력 용기 및 상기 사이조립 및 상부 램의 상단. 이들 시트는 전기 장치의 나머지 샘플 가열 회로를 격리.
- 멀티 모루 실험의 조립
- 상기 튜브에 인접한 구멍을 통해 와이어를 공급 모두 180을 통해 회전 단부와 대향하는 구멍들을 확보 4 홀 하드 소성 알루미나 튜브를 이용하여 C 형 열전대를 확인. 단부에서 노출 와이어 10-20 밀리미터 부를 남겨 짧은 알루미나 튜브의 길이 (~ 20mm) 한 다음 테플론 절연 재료로 전선의 나머지를 절연 시키.
- 그리고, 면체 지르코니아로 슬리브와 흑연 히터를 삽입도 4b에 나타낸 바와 같이 홈을 잘랐다. 면체의 상단에 열전대를 삽입하고 홈에 알루미나 덮여 팔을 놓습니다. 열전대 주변의 빈 공간을 채우고 건조 할 수 있도록 지르코니아 시멘트 (표 2 참조)를 사용합니다.
- 열전대 지성을 분리하기 위해서노출 된 전선이 덮여 때까지 흑연 캡슐에서, 면체의 기지에서 산화 마그네슘 분말을 추가합니다. 분말 미만 50 mg을 보통 노출 된 와이어를 포위하기에 충분하다. 산화 마그네슘 분말의 단단한 포장을 보장하기 위해, 루즈 파우더를 탐포하기 위해 드릴 빈을 사용합니다.
- 이전에 제조 된 샘플 재료로 흑연 캡슐을로드하고 개방 측면에서 면체에 배치합니다. 면체의 조립을 완료 알루미나 플러그를 삽입합니다.
- 화장실 큐브 (표 2)의 4 일 발사 - 나무, 큐브의 절단 된 모서리에 인접한 3면에 각각 하나의 짧은 길이를 접착제 폴리 비닐 아세테이트를 사용합니다. 각 발사 목재 조각. ~도 4에 도시 면체 크기, 길이 9.0 mm를하여 높이와 폭이 4.4 mm를 측정하고 각각의면에서 절단 된 가장자리 대향 사분면 발사 목재 조각을 배치한다.
- woode없이, 평면도에서 2 및 2 정사각형을 형성하는 네 큐브 조립N 개의 부착. 광장의 중앙을 향하도록 절단 된 모서리의 방향.
- 이 절단 된 모서리에 의해 지원 될 수 있도록, 큐브의 중심에 면체를 놓습니다. 그런 다음 각 열전대 무기가 광장의 반대 구석에서 나올 수 있도록 (그림 5A)
- 나무 조각과 조각이 더 나무 스페이서가없는 큐브 꼭대기에 나머지를 부착 보장, 중앙에 면체와 큐브를 형성하는 위치에 남아있는 화장실 큐브를 놓습니다.
- 시아 노 아크릴 레이트 형 접착제를 사용하여 조립 정육면체의 각면에 0.5 mm 두께의 시트 G10 (참조 : 표 2) ~ 정사각형 조각을 붙인다. 32mm의 화장실 큐브 ~ 55mm X 55mm를 측정 G10 시트를 사용합니다. 화장실 큐브의 두 저항 히터에 연락하여 전기 가열 회로의 일부를 형성 잘림이있다. 이 큐브에 문의 시트를 들어, 있도록 동박의 조각을 그림 (b)에 표시하고 배치 할이 좁은 (<1mm 폭) 슬릿을 잘라 나는T는 1, 2 단계 모루 사이의 접촉 지점을 제공합니다.
주 : 멀티 앤빌 장치 고정 링 내에 포함 앤빌의 2- 스테이지 시스템을 이용한다. 제 1 스테이지는 앤빌 중앙 캐비티를 형성하는 입방 6 이동식 웨지를 포함한다. 이 공동 세라믹 면체 (40)를 둘러싸고 절단 모서리 (두 번째 단계의 모루) 8 텅스텐 카바이드 큐브를 수용한다. 유압 프레스에 의해 제 1 스테이지에 적용 앤빌 수직 배향 력 따라서 시료의 준 정수압 압축을 초래하는 방식으로 팔면체에 전송된다. RAM 및 샘플 압력 오일 압력 사이의 관계는 (41)에 의해 설명 된 절차를 사용하여 여기에 설명 된 18mm OEL 캐스트 팔면체 조립체에 대해 조정할 수있다. - 마른 PTFE 윤활제를 사용하여 그림 6과 코트를에 표시된 치수 0.076 mm 두께의 마일 라 (Mylar)의 2 장을 잘라.
- 로 사전 절단 시트의 위치 하나(기지에서 직선) 링을 유지하고 자신이 0.076 mm 두께 일러와 함께 백업 및 PTFE 윤활제 (그림 5B)로 코팅되어 1 차 -stage의 모루,의 하위 집합 삽입합니다. 모루의 하부 세트를 실행 사이의 자리에 남아있을 수 있습니다. 1 단계 모루의 하부 세트로 조립 된 큐브를 놓고 압력 모듈을 종료 균형 열전쌍 와이어에 열전대 팔을 연결합니다.
- 고정 링에 2 차 사전 차단 마일 라 시트 (상단에 직선)를 놓고 마일 라 (Mylar) 백업 및 하부 세트와 동일한 방식으로 윤활해야 1 차 -stage의 모루의 상위 세트를 삽입합니다. 이러한 형태는 1 차 -stage 모루 번의 일러 시트 장치 (37)에 비해 30 % ~ 마찰에 의해 RAM 추력의 손실을 감소 고정 링 사이 일러 접촉 윤활 일러를 산출한다.
참고 : 두께와 일러 시트의 치수는 T에 따라 달라집니다압력 모듈의 그 정확한 디자인이 사용된다. 지구 물리학 연구소에서 사용 치수, 워싱턴의 카네기 연구소는 위의 그림 6에 설명한다.
4. 실험 실행하기
- 샘플을 100 K / 분의 속도로 필요한 압력, 열을 가져 일단 원하는 드웰 온도에 도달 할 때까지. 가열 단계 동안, 샘플 RAM 내의 오일은 오일 일정한 압력을 유지하기 위해 조절 될 필요가있다.
- 휴지 기간 후, 노의 전원을 절단하여 샘플을 급냉. 장치가 실온으로 냉각되면, 서서히 샘플을 압축 해제.
5. 실행 - 제품 분석
- 피스톤 실린더 실험에, 유압 램을 사용하여 압력 용기에서 최종 실험을 추출한다. 중장비 절단기 쌍 외부 흑연 캡슐 해제 조립체의 부분 (피스톤 cylind 삭제ER) 또는 샘플 캡슐과지지 편 (멀티 앤빌)를 포함하는 노.
- 에폭시의 샘플 마운트 (도 7a) (전형적으로 25.4 mm 직경의 원반을 형성한다). 320 내지 600 그릿 실리콘 카바이드 용지를 사용하여, 켄칭 규산염 용융물과 금속 상을 노출 샘플로 분쇄. ~ 0.3 내지 15 μm의 범위 그릿 크기 감소 알루미나 또는 다이아몬드 현탁액을 사용하여 노출 된 표면을 폴란드어.
- 카본 코트 연마 샘플 (42)의 표면 및 전자 프로브 마이크로 분석 (EPMA)에 의해 금속 실리케이트 런 제품의 주요 구성 요소를 분석한다. 거리 전자빔에서 알칼리 원소의 이동을 방지하기 위해 실리케이트 분석 디 포커스 (10 μm의) 빔 직경을 사용한다. 상기 프로토콜 생성 이전 샘플을 특성화하기 위해 사용 된 분석 조건으로 표준 참고 문헌에서 찾을 수있다 29 - 31, 35
참고 : investigat에 실험을 위해전자 MSE 및 SSE 분할은, EPMA들은 또한 충분한 농도로 존재 제공 트레이서 요소 분석에 적합한 증명할 수있다. - 주요 요소 분석에 이어, 0.3 μm의 알루미나 그리드를 사용하여, 탄소 피막을 제거한다. 런 제품의 미량 원소 함량을 결정하기 위해 레이저 어블 레이션을 유도 결합 플라즈마 질량 분광법 (LA-ICPMS)를 사용한다. 소개 LA-ICPMS에 의한 분석을 샘플링의 경우, 43 참조 참조하십시오.
주 : 칼슘 및 니켈 이전 HSE 용해도 연구 동위 성공적 유리 및 황화물 표준 물질을 각각 29, 30 모두를 이용하여 데이터를 줄이기 위해 내부 표준 물질로서 사용되어왔다. 모든 분석은 적어도 60 초 동안 절제 셀을 세척 한 다음 제거의 단일 패스가 선행되어야한다. 이 결과에 영향을주지 않는 실험 런 연마 제품에서 발생할 수있는 모든 표면 오염을 보장한다.
결과
규산이 낮은 F의 O 2에서 용융에서 실험에 다음 예제와 토론의 초점은 HSE의 용해도를 결정합니다. T - - 멀티 앤빌 실험 MSE 및 SSE 분할 데이터 P 제한하기 위하여 사용될 수있는 방법의 포괄적 인 예를 들어 F를 O 코어 금속 분리 2 조건을, 독자는 참조 9 칭한다 -. 11도 7B-D는 다시 표시 전형적인 실험 실행 제품에서 흩어?...
토론
여기에 설명 된 프로토콜을 사용하여 수행 포함없는 실험의 결과는 이전의 참조도 29의 (O를 · IR), 금 (Au), (30) (재), 금 (Au) 및 (31) (PT)의 문헌 데이터와 비교되었다. 백금은 포함이없는 실행 제품의 유용성을 입증에 가장 유익하다. 로우 F의 O 2 실행 실험을 위해, Ertel 외. (48)는 안정적으로 원점 개재물을 할당하므로 시분 LA-ICPMS 스펙트럼 최저 ?...
공개
저자가 공개하는 게 없다.
감사의 말
이 작품은 JMBNRB에게 수여 자연 과학 및 캐나다 장비, 검색 및 디스커버리 액셀러레이터 보조금 공학 연구위원회에 의해 지원되었다 워싱턴 포스트 박사 교제 프로그램의 카네기 연구소의 지원을 인정합니다. 스티븐 Elardo 또한 지구 물리학 연구소에서 피스톤 실린더 프레스로 촬영하기 전에 자신의 도움에 감사합니다.
자료
| Name | Company | Catalog Number | Comments |
| G10 Epoxy/Fiberglass Sheet | Accurate plastics, Inc. | GEES.020N.3648 | |
| Powdered starting materials- -Oxides, metals, carbonates | Alfa Aesar | Specific to desired experiment | |
| Castable 2-part MgO ceramic | Aremco | Ceramcast - 584 | |
| PTFE Dry Lubricant | Camie-Campbell | 2000 TFE-Coat | |
| Graphite resistance heaters | Carbone of America (Now owned by Mersen USA) | Custom Order | |
| Barium Carbonate | Chemical Products Corporation | Custom Order | Calcined free-flowing (CFF) grade |
| C-Type Thermocouple Wire (W26%Re, W5%Re) | Concept Alloys | ~0.25 mm diameter is suitable for most experiments | |
| Zirconia Cement | Cotronics; Resbond 940 2-part cement | Use 100 parts powder for every 25 to 28 parts activator | |
| Polyvinyl Acetate (PVA) Glue | e.g., Bostik | Often sold as 'white glue' | |
| Cyanoacrylate Glue | e.g., Krazy Glue/Loctite | ||
| Piston cylinder pressure vessel and WC piston | Hi-Quality Carbide Tooling Inc. | Custom Order | |
| Silica Glass Tubing | Quartz Plus | Custom Order | |
| Crushable ZrO2 tubes | Saint-Gobain | Custom Order | |
| Crushable MgO rods and tubes | Saint-Gobain | Custom Order | |
| WC cubes for multi-anvil experiments | Tungaloy | Custom Order | Cubes are grade-F WC alloy |
| Single hole alumina tube for multi-anvil thermocouple | Vesuvius McDanel | AXS071730-04-06 | |
| 4-hole alumina tube for piston cylinder thermocouple | Vesuvius McDanel | AXF1159--07-12 | |
| 4-hole alumina tube for multi-anvil thermocouple | Vesuvius McDanel | AXF1159-04-06 |
참고문헌
- Canup, R. M. Dynamics of Lunar Formation. Annual Review of Astronomy and Astrophysics. 42, 441-475 (2004).
- Rubie, D., Nimmo, F., Melosh, H. Formation of Earth’s core. Treatise on geophysics. 9, 51-90 (2007).
- Karato, S., Murthy, V. R. Core formation and chemical equilibrium in the Earth Physical considerations. Physics of the Earth and Planetary Interiors. 100, 61-79 (1997).
- Dziewonski, A. M., Anderson, D. L. Preliminary reference Earth model. Physics of the Earth and Planetary Interiors. 25 (4), 297-356 (1981).
- McDonough, W., Sun, S. The composition of the Earth. Chemical geology. 120 (3-4), 223-253 (1995).
- Palme, H., O’Neill, H. Cosmochemical estimates of mantle composition. Treatise on geochemistry. 2, 1-38 (2003).
- Fischer-Gödde, M., Becker, H., Wombacher, F. Rhodium, gold and other highly siderophile elements in orogenic peridotites and peridotite xenoliths. Chemical Geology. 280 (3-4), 365-383 (2011).
- Ringwood, A. E. Chemical evolution of the terrestrial planets. Geochimica et Cosmochimica Acta. 30, 41-104 (1966).
- Wood, B. J., Wade, J. Core formation and the oxidation state of the Earth. Earth and Planetary Science Letters. 236 (1-2), 78-95 (2005).
- Siebert, J., Corgne, A., Ryerson, F. Systematics of metal–silicate partitioning for many siderophile elements applied to Earth’s core formation. Geochimica et Cosmochimica Acta. 75 (6), 1451-1489 (2011).
- Righter, K. Prediction of metal–silicate partition coefficients for siderophile elements: an update and assessment of PT conditions for metal–silicate equilibrium during accretion of. Earth and Planetary Science Letters. 304 (1-2), 158-167 (2011).
- Wood, B. J., Walter, M. J., Wade, J. Accretion of the Earth and segregation of its core. Nature. 441 (7095), 825-833 (2006).
- Kimura, K. A. N., Lewis, R. O. Y. S., Anders, E. Distribution of gold and rhenium between nickel-iron and silicate melts: implications for the abundance of siderophile elements on the Earth and Moon. Geochimica et Cosmochimica Acta. 38, 683-701 (1974).
- Murthy, V. R. Early differentiation of the Earth and the problem of mantle siderophile elements: a new approach. Science. 253 (5017), 303-306 (1991).
- Righter, K., Humayun, M., Danielson, L. Partitioning of palladium at high pressures and temperatures during core formation. Nature Geoscience. 1 (5), 321-323 (2008).
- Borisov, A., Palme, H., Spettel, B. Solubility of palladium in silicate melts Implications for core formation in the Earth. Geochimica et Cosmochimica Acta. 58 (2), 705-716 (1994).
- Ertel, W., Dingwell, D. B., Sylvester, P. J. Siderophile elements in silicate melts — A review of the mechanically assisted equilibration technique and the nanonugget issue. Chemical Geology. 248 (3-4), 119-139 (2008).
- Borisov, A. L., Palme, H. The solubility of iridium in silicate melts: New data from experiments with lr10Pt90 alloys. Geochimica et Cosmochimica Acta. 59 (3), 481-485 (1995).
- Borisov, A., Palme, H. Experimental determination of Os metal/silicate partitioning. Neues Jahrbuch für Mineralogie - Abhandlungen. 172 (2-3), 347-356 (1998).
- Borisov, A., Palme, H. Experimental determination of the solubility of platinum in silicate melts. Geochimica et Cosmochimica Acta. 61 (20), 4349-4357 (1997).
- Ertel, W., O’Neill, H. S. C., Sylvester, P. J., Dingwell, D. B. Solubilities of Pt and Rh in a haplobasaltic silicate melt at 1300. C. Geochimica et Cosmochimica Acta. 63 (16), 2439-2449 (1999).
- Cottrell, E., Walker, D. Constraints on core formation from Pt partitioning in mafic silicate liquids at high temperatures. Geochimica et Cosmochimica Acta. 70 (6), 1565-1580 (2006).
- Yokoyama, T., Walker, D., Walker, R. J. Low osmium solubility in silicate at high pressures and temperatures. Earth and Planetary Science Letters. 279 (3-4), 165-173 (2009).
- Laurenz, V., Fonseca, O. C., Ballhaus, C., Peter, K., Heuser, A., Sylvester, P. J. The solubility of palladium and ruthenium in picritic melts: 2. The effect of sulfur. Geochimica et Cosmochimica Acta. 102, 172-183 (2013).
- Neill, H. S. C. Experimental petrochemisty of some highly siderophile elements at high temperatures, and some implications for core formation and the mantle’s early history. Chemical Geology. 120 (3-4), 255-273 (1995).
- Fortenfant, S. S., Dingwell, D. B., Ertel-Ingrisch, W., Capmas, F., Birck, J. L., Dalpé, C. Oxygen fugacity dependence of Os solubility in haplobasaltic melt. Geochimica et Cosmochimica Acta. 70 (3), 742-756 (2006).
- Ertel, W., O’Neill, H. S. C., Sylvester, P. J., Dingwell, D. B., Spettel, B. The solubility of rhenium in silicate melts: Implications for the geochemical properties of rhenium at high temperatures. Geochimica et Cosmochimica Acta. 65 (13), 2161-2170 (2001).
- Medard, E., Schmidt, M. W., Wahle, M., Keller, N. S., Gunther, D. Pt in Silicate Melts: Centrifuging Nanonuggets to Decipher Core Formation Processes. Lunar and Planetary Science Conference. , 3-4 (2010).
- Brenan, J., McDonough, W. Core formation and metal–silicate fractionation of osmium and iridium from gold. Nature Geoscience. 2 (11), 798-801 (2009).
- Bennett, N. R., Brenan, J. M. Controls on the solubility of rhenium in silicate melt: Implications for the osmium isotopic composition of Earth’s mantle. Earth and Planetary Science Letters. 361, 320-332 (2013).
- Bennett, N., Brenan, J., Koga, K. The solubility of platinum in silicate melt under reducing conditions: Results from experiments without metal inclusions. Geochimica et Cosmochimica Acta. 133, 422-442 (2014).
- Okamoto, H., Massalski, T. B. The Au-Pt ( Gold-Platinum ) System. Bulletin of Alloy Phase Diagrams. 6 (1), 46-55 (1985).
- Neill, H., Pownceby, M. Thermodynamic data from redox reactions at high temperatures. I. An experimental and theoretical assessment of the electrochemical method using stabilized zirconia. Contributions to Mineralogy and Petrology. 114 (3), 296-314 (1993).
- Deines, P., Nafziger, R., Ulmer, G., Woermann, E. . Temperature-oxygen fugacity tables for selected gas mixtures in the system CHO at one atmosphere total pressure. Bulletin of the Earth and Mineral Sciences Experiment Station. (88), (1974).
- Corgne, A., Keshav, S., Wood, B. J., McDonough, W. F., Fei, Y. Metal–silicate partitioning and constraints on core composition and oxygen fugacity during Earth accretion. Geochimica et Cosmochimica Acta. 72 (2), 574-589 (2008).
- Agee, C. B., Walker, D. Static compression and olivine flotation in ultrabasic silicate liquid. Journal of Geophysical Research. 93 (7), 3437-3449 (1988).
- Walker, D. Lubrication, gasketing, and precision in multianvil experiments. American Mineralogist. 76 (7-8), 1092-1100 (1991).
- Boyd, F., England, J. Apparatus for Phase-Equilibrium Measurements at Pressures up to 50 Kilobars and Temperatures up to 1750. C. Journal of Geophysical Research. 65 (2), 741-748 (1960).
- McDade, P., Wood, B. J., et al. Pressure corrections for a selection of piston-cylinder cell assemblies. Mineralogical Magazine. 66 (6), 1021-1028 (2002).
- Walker, D., Carpenter, M., Hitch, C. Some simplifications to multianvil devices for high pressure experiments. American Mineralogist. 75 (9-10), 1020-1028 (1990).
- Bertka, C. M., Fei, Y. Mineralogy of the Martian interior up to core-mantle boundary pressures. Journal of Geophysical Research. 102 (B3), 5251 (1997).
- Reed, S. J. B. . Electron Microprobe Analysis and Scanning Electron Microscopy in Geology. , (2005).
- Sylvester, P. J. . Laser Ablation ICP-MS in the Earth Sciences: Current Practices and Outstanding Issues. , (2008).
- Borisov, A., Walker, R. Os solubility in silicate melts: New efforts and results). American Mineralogist. 85 (7-8), 912-917 (2000).
- Borisov, A., Nachtweyh, K. Ru Solubility in Silicate Melts: Experimental Results in Oxidizing Region. Lunar and Planetary Science Conference. 77058, 1320 (1998).
- Borisov, A., Palme, H. Experimental determination of the solubility of Au in silicate melts. Mineralogy and Petrology. 56 (3-4), 297-312 (1996).
- Dunn, T. The Piston-Cylinder Apparatus. Short Course Handbook on Experiments at High Pressure and Applications to the Earth’s Mantle. , 39-94 (1993).
- Ertel, W., Walter, M., Drake, M., Sylvester, P. Experimental study of platinum solubility in silicate melt to 14GPa and 2273K: implications for accretion and core formation in Earth. Geochimica et Cosmochimica Acta. 70 (10), 2591-2602 (2006).
- Mann, U., Frost, D., Rubie, D. Partitioning of Ru. Rh, Pf, Re, Ir and Pt between liquid metal and silicate at high pressures and high temperatures-Implications for the origin of highly siderophile element concentrations in the Earth’s mantle. Geochimica et Cosmochimica Acta. 84, 593-613 (2012).
- Laurenz, V., Fonseca, R. O. C., Ballhaus, C., Sylvester, P. J. Solubility of palladium in picritic melts 1 . The effect of iron. Geochimica et Cosmochimica Acta. 74 (10), 2989-2998 (2010).
- Liu, Y., Ge, Y., Yu, D. Thermodynamic descriptions for Au–Fe and Na–Zn binary systems. Journal of Alloys and Compounds. 476 (1-2), 79-83 (2009).
- Rindone, G. E., Rhoads, J. L. The Colors of Platinum, Palladium, and Rhodium in Simple Glasses. Journal of the American Ceramic Society. 39 (5), 173-180 (1956).
- Akai, T., Nishii, J., Yamashita, M., Yamanaka, H. Chemical behavior of platinum-group metals in oxide glasses. Journal of Non-Crystalline Solids. 222 (Special Issue), 304-309 (1997).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유