JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
세포 이동의 양전자 방출 단층 촬영 이미징: 세포 방사선 표지 방법
요약
여기에 제시된 것은 바로 사용할 수 있는 방사성 표지 합성 [89 Zr]Zr-p-isothiocyanatobenzyl-desferrioxamine([89Zr]Zr-DBN)을 사용하여 양전자 방출 단층 촬영(PET) 방사성 동위원소, 89Zr(t1/2 78.4 h)로 세포를 방사성 표지하는 프로토콜입니다. [89Zr]Zr-DBN을 사용한 방사성 표지 세포는 투여 후 최대 7일 동안 PET를 사용하여 체내에서 투여된 방사성 표지 세포의 비침습적 추적 및 이미징을 가능하게 합니다.
초록
줄기세포 및 키메라 항원 수용체(CAR) T세포 치료제는 장기 재생을 위한 유망한 치료제이자 다양한 암에 대한 면역 요법으로 부상하고 있습니다. 이러한 분야에서 상당한 진전이 이루어졌음에도 불구하고 살아있는 시스템에서 투여된 치료 세포의 약동학 및 약력학을 더 잘 이해하기 위해서는 아직 더 많은 것을 배워야 합니다. 양전자 방출 단층 촬영(PET)을 사용한 세포의 비침습적 생체 내 추적을 위해 89Zr(t1/2 78.4h)을 사용하여 새로운 [89 Zr]Zr-p-isothiocyanatobenzyl-desferrioxamine([89Zr]Zr-DBN) 매개 세포 방사선 표지 방법이 개발되었습니다. 본 프로토콜은 중간엽 줄기세포, 계통 유도 심근세포, 간 재생 간세포, 백혈구, 흑색종 세포 및 수지상세포를 포함한 다양한 세포의 직접 방사선표지를 위한 [89Zr]Zr-DBN-매개 즉시 사용 가능한 방사선표지 합성을 기술한다. 개발된 방법론은 방사성 표지된 세포의 특성이나 기능에 영향을 미치지 않고 투여 후 최대 7일 동안 세포 이동에 대한 비침습적 PET 이미징을 가능하게 합니다. 또한, 이 프로토콜은 [89 Zr]Zr-DBN의 방사성 합성, [89 Zr]Zr-DBN의 생체적합성 제형, 방사성 표지를 위한 세포 준비, 그리고 마지막으로 세포의 성공적인 방사성 표지에 필요한 모든 복잡한 세부 사항을 포함하여 [89Zr]Zr-DBN을 사용한 세포의 방사성 표지를 위한 단계적 방법을 설명합니다.
서문
줄기세포와 키메라 항원 수용체(CAR) T세포 치료제는 심근부전1,2, 망막변성2, 황반변성2, 당뇨병2, 심근경색3,4,5, 암6,7,8,9 등 다양한 질병의 치료를 위해 활발히 연구되고 있다.10. 줄기세포 치료의 두 가지 그럴듯한 접근법 중 줄기세포를 질병 부위에 직접 생착시켜 치료적 반응을 일으키거나, 질병 부위에 부착하지 않고 질병 부위의 미세환경을 변화시켜 간접적인 치료적 반응을 일으킬 수 있다. 간접적인 치료적 반응은 질병을 복구하거나 치료할 수 있는 인자를 방출함으로써 질병 부위의 미세환경에 변화를 일으킬 수 있다5. 줄기 세포 치료의 이러한 접근 방식은 방사선 표지 줄기 세포의 비침습적 이미징으로 평가할 수 있습니다. 비침습적 영상은 질병 부위의 방사성 표지된 세포의 흡수와 치료 반응의 상관관계를 파악하여 직접 및 간접 치료 반응을 해독할 수 있습니다.
또한 CAR T-cell 6,7,8,9,10 및 수지상세포 면역요법 11,12를 이용하여 다양한 암을 치료하기 위한 면역세포 기반 치료제가 개발되고 있습니다. 기계학적으로 CAR T 세포 면역 요법 6,7,8,9,10에서 T 세포는 치료가 필요한 종양의 특정 항원에 결합하는 에피토프를 발현하도록 조작됩니다. 이렇게 조작된 CAR T세포는 투여 시 에피토프-항원 상호작용을 통해 종양 세포에 존재하는 특정 항원에 결합합니다. 결합 후 결합된 CAR T 세포는 활성화된 후 증식하여 사이토카인을 방출하는데, 이는 숙주의 면역 체계에 신호를 보내 특정 항원을 발현하는 종양을 공격하도록 합니다. 대조적으로, 수지상 세포 치료제(11,12)의 경우, 수지상 세포는 표면에 특정 암 항원을 제시하도록 조작된다. 이렇게 조작된 수지상세포는 투여될 때 림프절의 본거지이며 림프절의 T 세포에 결합합니다. T-세포는 투여된 수지상세포의 특정 암 항원에 결합하면 활성화/증식을 거쳐 특정 항원을 발현하는 종양에 대한 숙주의 면역 반응을 시작합니다. 따라서, 면역요법의 효능을 결정하기 위해 방사선 표지된 CAR T-세포 및 수지상세포를 이미징함으로써 투여된 CAR T-세포의 종양 부위(9,10)로의 이동(trafficking) 및 림프절(11,12)로의 수지상세포(homing)에 대한 평가가 가능하다. 또한 비침습적 세포 이동은 치료 가능성을 더 잘 이해하고, 직접 및 간접 치료 반응을 명확히 하고, 줄기 세포 및 면역 세포 기반 치료의 치료 반응을 예측 및 모니터링하는 데 도움이 될 수 있습니다.
광학 영상, 자기 공명 영상(MRI), 단일 광자 방출 컴퓨터 단층 촬영(SPECT) 및 양전자 방출 단층 촬영(PET)을 포함하여 세포 이동을 위한 다양한 이미징 양식이 3,4,9,10,12로 탐색되었습니다. 이러한 각 기술에는 고유한 장점과 단점이 있습니다. 이 중 PET는 정량적 특성과 높은 감도로 인해 가장 유망한 양식이며, 이는 이미징 기반 세포 매매 3,4,9,10에서 세포의 신뢰할 수 있는 정량화에 필수적입니다.
반감기가 78.4시간인 양전자 방출 방사성 동위원소 89Zr은 세포 표지에 적합합니다. 1주일 이상 세포 이동의 PET 이미징을 가능하게 하며 널리 사용되는 저에너지 의료용 사이클로트론 13,14,15,16,17에 의해 쉽게 생성됩니다. 또한, 적절하게 기능화된 p-이소티오시아나토벤질-데스페리옥사민(DFO-Bn-NCS) 킬레이터는 [89Zr]Zr-DBN 18,19,20,21,22,23,24 로도 알려진 89 Zr-표지 된, 즉시 사용 가능한 세포 표지 합성, [89Zr]Zr-p-이소티오시아나토벤질-데스페리옥사민의 합성을 위해 상업적으로 이용 가능합니다,25. [89Zr]Zr-DBN 매개 세포 표지의 원리는 세포막 단백질의 1차 아민과 [89Zr]Zr-DBN의 이소티오시아네이트(NCS) 부분 사이의 반응을 기반으로 하여 안정적인 공유 티오우레아 결합을 생성합니다.
[89Zr] Zr-DBN 기반 세포 표지 및 이미징은 줄기 세포 18,23,25, 수지상 세포18, 심장 줄기 세포19, 낙엽 기질 세포 20, 골수 유래 대식 세포 20, 말초 혈액 단핵 세포 20, Jurkat/CAR T 세포 21, 간세포22,24 및 백혈 구 25를 포함한 다양한 세포를 추적하기 위해 발표되었습니다. 다음 프로토콜은 [89Zr]Zr-DBN을 사용한 세포 방사선 표지 준비 및 세포 표지의 단계별 방법을 제공하고 특정 세포 유형에 대한 방사선 표지 프로토콜에서 필요할 수 있는 변경 사항을 설명합니다. 보다 명확성을 높이기 위해 여기에 제시된 세포 방사성 표지 방법은 4개의 섹션으로 나뉩니다. 첫 번째 섹션에서는 DFO-Bn-NCS로 89 Zr을 킬레이트하여 [89Zr]Zr-DBN을 제조하는 방법을 다룹니다. 두 번째 섹션에서는 세포 방사선 표지에 쉽게 사용할 수 있는 [89Zr]Zr-DBN의 생체 적합성 제형의 제조에 대해 설명합니다. 세 번째 섹션에서는 방사선 표지를 위한 세포의 전처리에 필요한 단계를 다룹니다. 세포의 전처리는 방사선 표지 중 세포 표면 단백질에 존재하는 일차 아민과 [89Zr]Zr-DBN의 반응을 방해하거나 경쟁할 수 있는 외부 단백질을 제거하기 위해 단백질이 없는 인산염 완충 식염수(PBS) 및 HEPES 완충 행크스 균형염 용액(H-HBSS)으로 세포를 세척하는 것을 포함합니다. 마지막 섹션에서는 세포의 실제 방사성 표지 및 품질 관리 분석과 관련된 단계를 제공합니다.
프로토콜
수지상세포와 흑색종세포를 상업적으로 수득하였다18. 간세포는 복강경 부분 간절제술 후 돼지의 간에서 분리하였다22,24. 줄기세포는 골수 흡인18,19,26으로부터 분리하였다. 지방 조직 유래 줄기 세포는 인간 세포 치료 실험실(Human Cellular Therapy Laboratory, Mayo Clinic Rochester23)에서 수득하였다. 인간 백혈구는 로체스터25에 있는 메이요 클리닉(Mayo Clinic)의 수혈 의학부(Division of Transfusion Medicine)로부터 받은 수집된 혈액으로부터 분리하였다. 방사선 표지에 사용되는 다양한 세포는 기관 동물 관리 및 사용 위원회, 메이요 클리닉 줄기 세포 연구 감독 소위원회, 수혈 의학 연구 위원회, 기관 생물 안전 위원회 및 방사선 안전 위원회에서 권장하는 지침에 따라 획득 및 사용되었습니다.
1. [ 89 Zr ]Zr-p-isothiocyanatobenzyl-desferrioxamine ([ 89Zr ]Zr-DBN)의 제조
타이밍 : ~ 160-220 분
참고 : [89 Zr] Zr-DBN의 제조를 위해 89 Zr을 [89 Zr] Zr- 인산 수소 ([89 Zr] Zr (HPO 4)2) 또는 [89Zr] Zr- 클로라이드 ([89Zr] ZrCl 4)의 형태로 분리하십시오.
- 확립된 하이드록사메이트 수지 기반 정제 방법13,17을 사용하여 모체 89 Y에서 89Zr을 분리합니다. 간단히 말해서, 먼저 ~100mg의 하이드록사메이트 수지로 컬럼을 준비한 다음 8.0mL의 순수 무수 아세토니트릴로 컬럼을 세척한 다음 5.0-6.0mL의 공기로 플러시하여 하이드록사메이트 수지를 활성화합니다. 그런 다음 15mL의 탈이온수로 컬럼을 세척한 다음 5.0-6.0mL의 공기로 다시 플러시한 다음 2.0mL의 0.50N HCl(미량 금속 기저 등급)을 통과시킨 다음 5.0-6.0mL의 공기로 추가로 플러시합니다. 다음으로, 89 Zr 및 89 Y를 모두 포함하는 용액을 히드 록사메이트 수지에로드하고 히드 록사 메이트 수지에서 결합되지 않은 89Y를 20 mL의 2.0 N HCl로 세척 한 다음 10 mL의 탈 이온수와 5.0-6.0 mL의 공기로 플러시합니다.
참고: 공기로 세척한 후 아래와 같이 89Zr의 용리를 수행할 수 있습니다.- [89Zr]Zr(HPO 4)2 형태로 89 Zr을 용출하기 위해 먼저 1.1 단계의 컬럼에 0.50mL의 1.2 M K 2 HPO 4/KH 2 PO 4 완충액(pH 3.5)을 첨가하고 30분 동안 컬럼에 그대로 두어 수지에서 [89 Zr]Zr(HPO 4)2로서 89Zr의 방출을 촉진합니다. 그런 다음 1.50mL의 1.2M K 2 HPO 4/KH2PO4 완충액(pH 3.5)을 추가로 사용하여 컬럼에서 89Zr을 용리합니다. [89Zr]Zr(HPO4)2를 용출한 후 그림 1과 같이 [89Zr]Zr(HPO4)2를 사용하여 [89Zr]Zr-DBN을 제조하기 위해 1.2, 1.2.1 및 1.2.2단계를 수행합니다.
- 89Zr을 [89 Zr]ZrCl4로 얻기 위해, 먼저 89 Zr을 [89Zr]Zr-옥살레이트로 용리시킨다.
- [89Zr]Zr-옥살레이트 형태로 89 Zr을 용출하기 위해 1.1 단계의 컬럼에 0.50mL의 1.0M 옥살산을 첨가하고 1분 동안 컬럼에 그대로 두어 수지에서 [89 Zr]-옥살레이트로서 89Zr의 방출을 촉진합니다. 그런 다음 컬럼에서 89Zr을 1.0M 옥살산 2.50mL(총 3.0mL)를 추가로 용리합니다17.
- Larenkov et al.14에 설명된 대로 음이온 교환 컬럼을 사용하여 [89 Zr]Zr-oxalate를 [89Zr]ZrCl4로 변환하려면 먼저 6.0mL 아세토니트릴로 세척한 다음 5.0-6.0mL의 공기로 세척하여 컬럼을 활성화합니다. 그런 다음 10.0mL의 식염수로 컬럼을 세척한 다음 5.0-6.0mL의 공기를 다시 세척합니다. 마지막으로 10.0mL의 탈이온수를 통과시킨 다음 5.0-6.0mL의 공기로 플러시합니다.
- [89Zr]Zr-oxalate가 포함된 3.0 mL 용액을 활성화된 음이온 교환 컬럼에 천천히 로드한 다음 5.0-6.0 mL의 공기를 플러시합니다. 그런 다음 89Zr이 로드된 컬럼을 50.0mL의 탈이온수로 세척하여 결합되지 않은 옥살산염 이온을 제거한 다음 5.0-6.0mL의 공기로 플러시합니다.
- [89Zr]ZrCl4 형태로 89 Zr을 용리하기 위해 0.10 mL의 1.0 N HCl을 컬럼에 첨가하고, 1.0분 동안 컬럼에 그대로 두어 89Zr의 방출을 수지에서 [89 Zr]ZrCl4로 촉진하고, 컬럼에서 89Zr을 1.0 N HCl 0.40 mL(총 0.5 mL)의 추가 0.40 mL로 용리합니다. 용출된 [89Zr]ZrCl4를 V자형 바이알에 넣고 질소 가스가 일정하게 흐르는 65°C의 가열 블록에 10-30분 동안 건조시킵니다. 건조 후 건조된 [89 Zr]ZrCl 4를 물에서 재구성하고 그림 1과 같이 [89 Zr]ZrCl4를 사용하여 [89Zr]Zr-DBN을 제조하기 위해 1.3 및 1.3.1단계를 따릅니다.
- 1.1.1 단계에서 1.2 M K 2 HPO 4 / KH2PO 4 (pH 3.5) (10-25 MBq)로 제조 된 ~ 120 μL의 [89Zr] Zr (HPO4) 2 μL를 취하고 용액을 중화하여 1.0 M HEPES-KOH (pH 7.5)의 ~ 100 μL 및 1.0 M K 2CO3 의 ~ 65 μL로 pH 7.5-8.0을 달성합니다.
- 89Zr의 다양한 겉보기 특이 활성을 갖는 상이한 89 Zr 제형에 대한 단계 1.2.2 또는 1.3.1에 대한 적절한 양의 DFO-Bn-NCS를 얻기 위해, DFO-Bn-NCS (7.5-15 μg)의 범위로 [89 Zr]Zr(HPO 4)2 또는 [89Zr]ZrCl4의 중화된 제형의 고정된 부피를 사용하여 일련의 킬레이트화 반응을 수행한다. [89Zr]Zr(HPO4)2의 경우, 37°C에서 ~550 rpm의 셰이커에서 60분 동안 킬레이트 반응을 배양합니다. 반면, [89Zr]ZrCl4의 경우 25°C에서 ~550rpm의 셰이커에서 30분 동안 킬레이트화 반응을 배양합니다. 배양 중 또는 배양 종료 시 침전물을 나타내는 킬레이트화 반응을 폐기하십시오. 배양 종료 시 아래 1.5단계에서 설명한 대로 각 킬레이트 반응에 대한 DFO-Bn-NCS의 킬레이트화 효율을 추정하기 위해 이동상으로 100mM 디에틸렌트리아민 펜타아세테이트(DTPA), pH 7.0을 사용하여 방사성 박막 크로마토그래피(rad-TLC)를 수행합니다.
참고: 킬레이트화 효율에 따라 [89 Zr]Zr(HPO 4)2 또는 [89Zr]ZrCl4의 중화된 제형에서 DFO-Bn-NCS의 침전을 일으키지 않고 ≥97% 킬레이트화 효율을 달성하는 데 필요한 1.2.2 또는 1.3.1단계에서 DFO-Bn-NCS의 최소량을 사용하십시오. 본원에서, [89Zr]Zr-DBN은 ≥97% 방사성화학적 순도로 합성하였다. - 무수 DMSO(3.76mg/mL)에서 신선한 5.0mM DFO-Bn-NCS를 준비하고 4.0μL의 5.0mM DFO-Bn-NCS(20nmol 또는 15μg)를 1.2단계에서 ~285μL의 중화된 [89Zr]Zr(HPO4)2 (10-25MBq)에 추가하고 피펫팅으로 용액을 혼합합니다. 킬레이트 혼합물의 최종 DMSO 농도를 총 부피의 2% 미만으로 유지하십시오.
- 89Zr의 다양한 겉보기 특이 활성을 갖는 상이한 89 Zr 제형에 대한 단계 1.2.2 또는 1.3.1에 대한 적절한 양의 DFO-Bn-NCS를 얻기 위해, DFO-Bn-NCS (7.5-15 μg)의 범위로 [89 Zr]Zr(HPO 4)2 또는 [89Zr]ZrCl4의 중화된 제형의 고정된 부피를 사용하여 일련의 킬레이트화 반응을 수행한다. [89Zr]Zr(HPO4)2의 경우, 37°C에서 ~550 rpm의 셰이커에서 60분 동안 킬레이트 반응을 배양합니다. 반면, [89Zr]ZrCl4의 경우 25°C에서 ~550rpm의 셰이커에서 30분 동안 킬레이트화 반응을 배양합니다. 배양 중 또는 배양 종료 시 침전물을 나타내는 킬레이트화 반응을 폐기하십시오. 배양 종료 시 아래 1.5단계에서 설명한 대로 각 킬레이트 반응에 대한 DFO-Bn-NCS의 킬레이트화 효율을 추정하기 위해 이동상으로 100mM 디에틸렌트리아민 펜타아세테이트(DTPA), pH 7.0을 사용하여 방사성 박막 크로마토그래피(rad-TLC)를 수행합니다.
- 1.1.2.4 단계에서 0.1 N HCl (40-80 MBq)로 공식화 된 [89Zr] ZrCl4 의 ~ 180 μL를 취하고 결과 용액을 중화하여 1.0 M Na2CO3 의 ~ 25 μL로 pH 7.5-8.0을 달성합니다.
- 무수 디메틸 설폭사이드(DMSO)(1.88mg/mL)에서 신선한 2.5mM DFO-Bn-NCS를 준비하고 4.0μL의 2.5mM DFO-Bn-NCS(10nmol 또는 7.5μg)를 1.3단계에서 중화된 [89Zr]ZrCl4(40-80MBq)의 ~205μL에 추가합니다. 피펫팅으로 용액을 혼합합니다. 킬레이트 혼합물의 최종 DMSO 농도를 총 부피의 2% 미만으로 유지하십시오.
- [89Zr]Zr(HPO 4)2의 경우 ~550 rpm의 셰이커에서 37°C에서 89 Zr의 킬레이트화를 60분 동안 진행하고, [89Zr]ZrCl4의 경우 ~550 rpm의 셰이커에서 25°C에서 30분 동안 4의 킬레이트화를 진행합니다.
- rad-TLC 이동 용매로 100mM DTPA(pH 7.0)를 사용하여 rad-TLC에 의한 89Zr킬레이트 효율을 측정합니다. [89Zr]Zr-DBN은 ~0.021-0.035의 R f를 나타내고, [89 Zr]ZrCl 4는 ~1.0의 R f를 나타내고, [89Zr]Zr(HPO4)2는 ~1.0의 R f를 나타낼 것으로 예상합니다. 방정식 (1)을 사용하여 킬레이트화 효율(%)을 계산합니다.
[89Zr]Zr-DBN을 형성하기 위해 DFO-NCS에 킬레이트화된 89 Zr의 백분율 = [ ([89 Zr]Zr - DBN의 Rf 에서의 방사능) / ([89 Zr]Zr - DBN의 Rf와 [89 Zr]Zr(HPO 4)2 또는 [89Zr]ZrCl4)의 Rf에서의 방사능의 합 ] × 100 (1)
참고: rad-TLC에 의해 결정된 세포 방사선 표지를 진행하기 위해 허용되는 89Zr 킬레이트화 효율은 ≥97%입니다. 제안된 ≥97%의 방사성 화학 순도 [89Zr]Zr-DBN은 현장에서 사용되는 다른 방사성 의약품에 대한 표준 방사성 화학 순도 요구 사항에 따라 설정되었습니다. 보충 그림 S1 및 보충 그림 S2에서 대표적인 rad-TLC를 참조하십시오.

그림 1: [89Zr]Zr-DBN 준비의 개략도. [89Zr] Zr-DBN의 제조를 위해 사전 공식화 된 [89 Zr] Zr (HPO 4) 2 또는 [89Zr] ZrCl4를 pH 7.5-8.0으로 중화합니다. 중화된 용액을 DFO-Bn-NCS로 배양합니다. rad-TLC에 의해 DFO-Bn-NCS에 대한 89Zr의 킬레이트화 효율을 확인하십시오. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
2. 세포 방사선 표지를 위한 [ 89Zr ]Zr-DBN의 생체 적합성 제형 (그림 2)
타이밍 : ~ 35 분
참고: 3단계에서 세포를 준비하는 데 걸리는 시간을 감안할 때 3~20분 배양을 위해 2단계 시작 약 30분 전에 3단계를 시작합니다. 이를 통해 4단계의 세포 방사성 표지는 2-3.2.2단계 완료 후 5~10분 이내에 시작할 수 있습니다.
- [89Zr]ZrCl4로부터 제조된 [89 Zr]Zr-DBN 제형의 경우, ~27.0 μL의 1.2 M K2HPO 4/KH2PO4 (pH 3.5) + ~23.0 μL의 1.0 M HEPES-KOH 완충액(pH 7.5)을 포함하는 세포 호환 혼합물 50.0 μL를 [89 Zr]Zr-DBN의 50.0 μL에 첨가한다. 실온(25°C)에서 ~30분 동안 [89Zr]Zr-DBN-세포 호환 혼합물을 배양합니다.
참고: [89 Zr]Zr(HPO4)2로 만든 [89Zr]Zr-DBN 제형은 세포의 방사선 표지에 생체 적합성이 있으며 2단계가 필요하지 않습니다.
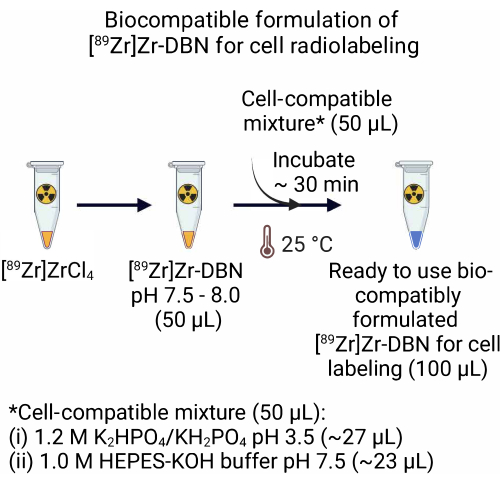
그림 2: 세포 방사성 표지를 위한 [89Zr]Zr-DBN의 생체 적합성 제형 준비. 방사성 표지 합성의 즉시 사용 가능한 생체 적합성 제형을 제조하기 위해 1.2 M K2HPO 4/KH2PO4 (pH 3.5) + 1.0 M HEPES-KOH를 포함하는 동일한 부피의 세포 호환 혼합물을 [89Zr]Zr-DBN의 동일한 부피에 첨가합니다. 25°C에서 ~30분 동안 배양합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
3. 방사성 표지를 위한 세포 준비
타이밍 : ~ 40-50 분
- 106 개의 부착 세포(줄기 세포, 흑색종 암 세포, 심혈관 줄기 세포, 수지상 세포 또는 간세포)를 × ~12개를 트립시화하고 15.0mL 원뿔형 원심분리 튜브에서 4°C에서 10분 동안 ~96 × g 의 세포를 원심분리합니다.
- 상층액을 폐기하고, 세포 펠릿을 ~500μL의 PBS에 재현탁시키고, 세포 현탁액을 1.5mL 미세 원심분리 튜브로 옮깁니다. 96°C에서 10분 동안 ~4× g 의 마이크로 원심분리기에서 세포를 원심분리합니다.
- 상층액을 버리고 세포 펠릿을 ~500μL의 H-HBSS에 재현탁시킵니다. 4°C에서 10분 동안 ~96× g 의 1.5mL 미세 원심분리기에서 세포를 원심분리합니다. 3.1.2단계를 한 번 더 반복하고 4.1.1단계로 진행합니다.
알림: H-HBSS는 0.01M HEPES(pH 8.0)의 Hanks 균형 소금 용액입니다.
- 인간 백혈구(혈액에서 갓 분리된 인간 백혈구)와 같은 비부착 세포의 경우, 트립신화를 건너뛰고 4°C에서 10분 동안 ~96×g의 1.5mL 미세 원심분리기에서 ~12 × 106 세포를 포함하는 세포 현탁액을 원심분리합니다.
- 상층액을 버리고, 세포 펠릿을 ~500μL의 PBS에 재현탁시키고, 4°C에서 10분 동안 ~96× g 의 1.5mL 미세 원심분리기에서 세포를 원심분리합니다.
- 상층액을 버리고 세포 펠릿을 ~500μL의 H-HBSS에 재현탁시킵니다. 4°C에서 10분 동안 ~96× g 의 1.5mL 미세 원심분리기에서 세포를 원심분리합니다. 3.2.2단계를 한 번 더 반복하고 4.1.1단계로 진행합니다.
4. 세포의 방사성 표지
타이밍 : ~ 125-155 분
- 세포 방사성 표지 시작(그림 3)
- 3.1.2단계 또는 3.2.2단계의 세포 현탁액을 사용하여 1.5mL 미세 원심분리 튜브에서 pH 7.5-8.0의 ~500μL의 H-HBSS에 약 ~6 × 106 개의 세포로 ~500μL 세포 현탁액을 준비합니다.
- 여기에 2단계에서 생체 적합성 제형화된 [89Zr]Zr-DBN의 ~100μL를 추가합니다.
- 방사성 표지를 위한 세포 배양(그림 4)
- ~500 μL로 설정된 마이크로피펫으로 위아래로 부드럽게 피펫팅하여 생체 적합성 제형[89 Zr]Zr-DBN과 세포 현탁액을 혼합합니다. 89Zr-동위원소16에 대해 489설정에서 방사능 선량 교정기를 사용하여 배양 튜브의 방사능량을 측정합니다.
- 세포 라벨링을 위해 25-37 °C에서 ~ 550 rpm의 셰이커에서 세포와 [89Zr] Zr-DBN 혼합물을 30-45 분 동안 배양합니다.
참고: 배양 온도는 표 1과 같이 방사선 표지에 사용되는 세포 유형에 따라 달라집니다. - 단계 4.2.2에서 배양 후, 갓 제조된 rad-TLC 용매(20mM 구연산나트륨[pH 4.9-5.1]:메탄올[1:1, V:V])를 사용하여 세포 방사성 표지 반응에서 rad-TLC를 수행합니다. rad-TLC 실행 후 방사성 표지된 세포에 대해 R f = ~0.73-0.81 및 Rf = ~0.01-0.02 부근에서 [89Zr]Zr-DBN 및 [89Zr]ZrCl4를 찾습니다. 방정식 (2)를 사용하여 Rf=~0.01-0.02에서 방사능의 백분율을 계산합니다.
Rf에서의 방사능 백분율 = ~0.01-0.02 = [ (R에서의 방사능 = ~0.01 - 0.02) / (Rf=~0.01 - 0.02 및 Rf= ~0.73 - 0.81에서의 방사능의 합) ] × 100 (2)
참고: Rf=~0.01-0.02 및 Rf = ~0.73-0.81에서 시각화된 피크를 이해하려면 보충 그림 S3의 백혈구 방사성 표지 반응에 대한 rad-TLC를 참조하십시오. - 별도의 1.5mL 미세 원심분리 튜브에서 pH 7.5-8.0에서 생체 적합성 제형의 [89Zr]Zr-DBN ~100μL를 ~500μL의 H-HBSS와 혼합하여 4.2.5단계에서 배경 보정을 위한 세포 없는 대조군으로 사용합니다. 4.2.2단계에서 사용한 것과 유사한 온도와 시간에서 배양한 후 rad-TLC를 수행합니다. rad-TLC 실행 후 Rf = ~0.73-0.81 부근에서 [89 Zr]Zr-DBN 및 [89Zr]ZrCl4를 찾습니다. 방정식 (3)을 사용하여 Rf = ~0.01-0.02에서 방사능의 백분율을 계산합니다.
Rf에서의 방사능 = ~0.01-0.02 = [ (R에서의 방사능 = ~0.01 - 0.02) / (Rf= ~0.01 - 0.02 및 Rf= ~0.73 - 0.81에서의 방사능의 합) ] × 100 (3)
참고: Rf = ~0.01-0.02 및 ~0.73-0.81에서 시각화된 피크를 이해하려면 보충 그림 S4의 무세포 제어 반응의 rad-TLC를 참조하십시오. - R f = ~0.01-0.02(단계 4.2.3의 rad-TLC)에서 R f = ~0.01-0.02(단계 4.2.3의 rad-TLC)에서의 방사능 백분율을 빼서 유효 세포 방사성 표지(%)를 계산합니다.
- 방사성 표지 및 세포 세척의 소광(그림 5)
- 단계 4.2.5에서 rad-TLC에 의한 방사성 표지 완료를 확인한 후, 표 1과 같이 ~600μL의 냉각된 세포에 적합한 완전 배지를 첨가하거나 H-HBSS를 첨가하여 방사성 표지 반응의 소멸을 수행합니다.
- 96°C에서 10분 동안 ~4× g 의 마이크로 원심분리기에서 세포를 원심분리합니다. 상층액을 버리십시오.
- 표 500과 같이 ~1μL의 냉각된 배지(Dulbecco's modified eagle medium(DMEM) + 10% 소 태아 혈청 + 5% 페니실린/스트렙토마이신 또는 Roswell Park Memorial Institute-1640(RPMI-1640) + 10% 소 태아 혈청 + 5% 페니실린/스트렙토마이신 또는 H-HBSS에 펠릿 세포를 부드럽게 재현탁시킵니다. ~500μL로 설정된 마이크로피펫으로 위아래로 부드럽게 피펫팅하여 세포 펠릿의 재현탁을 수행합니다.
- 96°C에서 10분 동안 ~4× g 의 마이크로 원심분리기에서 세포를 원심분리합니다.
- 4.3.2-4.3.4 단계를 두 번 반복하여 결합되지 않은 방사능을 씻어냅니다.
- 줄기 세포 또는 H-HBSS의 경우 DMEM + 10% 소 태아 혈청 + 5% 페니실린/스트렙토마이신이 있는 신선한 1.5mL 미세 원심분리 튜브로 펠릿을 옮기고 89Zr-동위원소16에 대해 489 설정에서 선량 보정기를 사용하여 세포 펠릿의 방사능을 측정합니다.
- 방정식 (4)를 사용하여 모든 세척 후의 최종 방사성 표지 효율을 계산합니다.
방사성 표지 효율 = [(4.3.6 단계에서 세포 펠릿의 붕괴 보정 방사능) / (4.2.1 단계에서 세포 펠릿 및 H-HBSS의 붕괴 보정 방사능) ] × 100 (4) - 방사성 표지된 세포의 품질을 보장하려면 먼저 방사성 표지된 세포의 최종 현탁액에 덩어리가 있는지 육안으로 검사합니다. 덩어리가 없으면 이 최종 일시 중단을 다음 단계로 진행합니다. 덩어리가 있지만 피펫팅이나 부드러운 흔들림으로 다시 부유할 수 있는 경우 그렇게 하고 육안 검사를 통과하므로 다음 단계로 진행합니다. 그러나 피펫팅이나 부드러운 흔들림으로 덩어리가 다시 부유하지 않으면 현탁액을 버리고 다시 시작하십시오.
- 육안 검사가 통과되면 방사성 표지 후 1시간 이내에 PBS에서 제조된 0.4% 트리판 블루 용액을 사용하여 트리판 블루 배제 생존도 테스트를 수행하고 방사성 표지된 세포의 세포 생존율을 평가하기 위한 세척 단계(4.3.3-4.3.7)를 수행합니다.
- 테스트를 수행하려면 방사성 표지된 세포와 표지되지 않은 세포 모두의 10.0μL 세포 현탁액에 0.4% 트리판 블루 용액 10.0μL를 추가하고 10.0μL로 설정된 마이크로피펫으로 트리판 블루 세포 현탁액을 위아래로 피펫팅하여 혼합합니다.
- 혈액 측정기에 ~10.0μL의 트리판 청색 세포 현탁액 혼합물을 로드하고 현미경으로 저배율로 또는 자동 세포 카운터를 사용하여 청색 염색 세포 수와 혈구계의 총 세포 수를 즉시 계산합니다. 방정식 (5)를 사용하여 생존 가능한 세포의 백분율을 계산합니다.
생존 가능한 세포의 백분율 = 100 - [(파란색 - 염색된 세포 수) / (총 세포 수)] × 100 (5)
- 표지되지 않은 세포와 비교하여 방사선 표지된 세포 현탁액에서 생존 가능한 세포의 비율에 변화가 없는 경우 방사선 표지된 세포를 사용하십시오. 생존 가능한 세포의 비율이 표지되지 않은 세포보다 작으면 방사성 표지된 세포를 폐기하십시오.
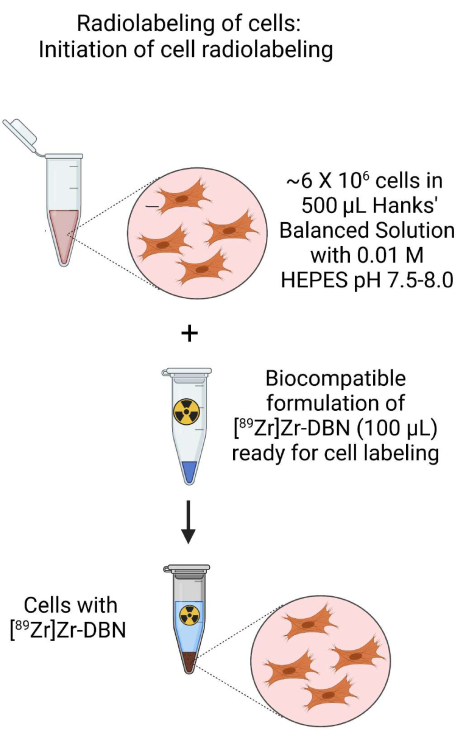
그림 3: 세포 방사성 표지 개시 개략도. HEPES 완충 Hanks 평형 염 용액에서 제조된 세포 현탁액에 생체 적합성 제형의 [89Zr]Zr-DBN을 첨가하여 세포의 방사성 표지를 시작합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
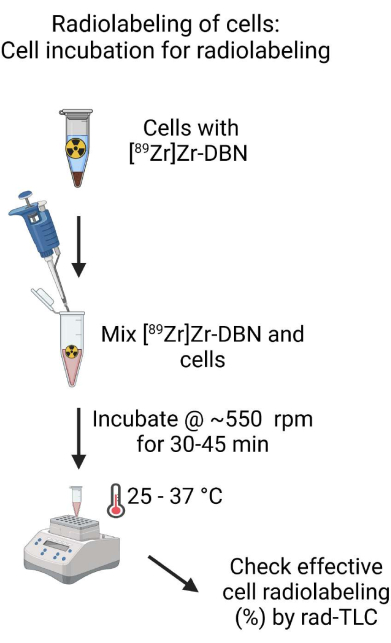
그림 4: 방사성 표지를 위한 세포 배양 개략도. 생체 적합성 제형의 [89Zr]Zr-DBN을 세포 현탁액과 완전히 혼합하고 세포 현탁액을 쉐이커의 온도 제어 가열 블록에서 30-60분 동안 배양합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
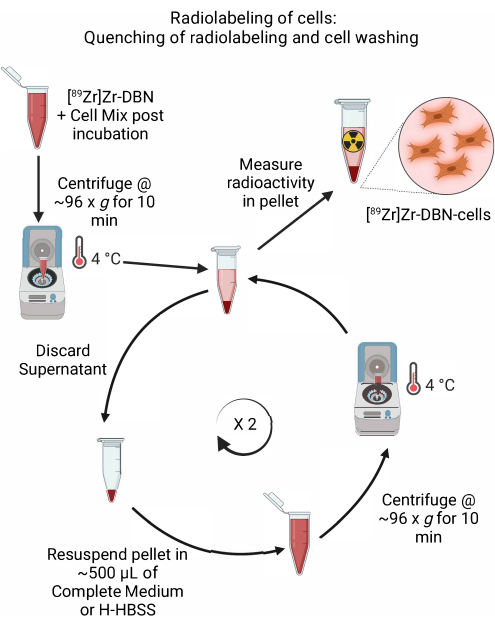
그림 5: 방사성 표지 및 세포 세척의 담금질 개략도. 냉각된 세포 배지 또는 H-HBSS를 첨가하여 세포의 방사성 표지를 소멸시킨 후 4°C에서 원심분리합니다. 세포 세척을 위해 상층액을 버리고 세포 펠릿을 ~500μL의 냉각 세포 배지 또는 H-HBSS에 재현탁시킵니다. 상층액을 버리고 세포 펠릿을 신선한 배지에 다시 현탁시키는 과정을 반복하여 결합되지 않은 방사성 표지 합성을 제거합니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
결과
본 논문에 제시된 대표적인 결과는 종전의 [89Zr]Zr-DBN 합성 및 세포 방사성 표지 연구 18,19,22,23,24,25에서 수집된 것이다. 간단히 말해서, 89Zr은 7.5-15 μg의 DFO-Bn-NCS를 사용하여 25-37 °C에서 30 ~ 60 분 내에 DFO-Bn-NCS와 성공적으로 복합화 될...
토론
다음은 효과적인 세포 방사선 표지를 위해 최적화가 필요한 프로토콜의 중요한 단계입니다. 프로토콜 단계 1.2 및 1.3에서 사용된 [89 Zr]Zr(HPO 4)2 또는 [89Zr]ZrCl 4의 부피에 따라 적절한 부피(마이크로리터)의 베이스를 사용해야 합니다. pH 7.5-8.0의 pH 범위를 달성하기 위해 [89 Zr]Zr(HPO 4)2의 중화에는 1.0M K 2 CO 3 용액을 사용하고 [89Zr] ZrCl4?...
공개
저자는 재정적 경쟁 이해관계가 없지만 이 기술의 발명자입니다(특허 # US20210330823A1).
감사의 말
이 연구는 NIH 5R21HL127389-02, NIH 4T32HL007111-39, NIH R01HL134664 및 DOE DE-SC0008947 보조금, 비엔나 국제원자력기구(International Atomic Energy Agency), 메이요 클리닉 핵의학과(Mayo Clinic Division of Nuclear Medicine), 방사선과, 미네소타주 로체스터(Rochester, MÓN)의 메이요 클리닉 재생 의학 센터(Mayo Clinic Center for Regenerative Medicine)의 지원을 받았습니다. 모든 피규어는 BioRender.com 를 사용하여 만들어졌습니다.
자료
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A996-4 | |
| Alpha Minimum Essential Medium | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 12571063 | |
| Anion exchange column | Macherey-Nagel, Inc., Düren, Germany | 731876 | Chromafix 30-PS-HCO3 SPE 45 mg cartridge |
| Conical centrifuge tubes (15 mL) | Corning Inc., Glendale, AZ, USA | 352096 | Falcon 15 mL high-clarity polypropylene (PP) conical centrifuge tubes |
| Dendritic cells | The American Type Culture Collection, Manassas, VA, USA | CRL-11904 | |
| DFO-Bn-NCS | Macrocyclics, Inc., Plano, TX, USA | B-705 | p-SCN-Bn-Deferoxamine |
| DMSO | Sigma-Aldrich, Inc., St. Louis, MO | 276855 | |
| Dose calibrator | Mirion Technologies (Capintec), Inc., Florham Park, NJ, USA | 5130-3234 | CRC -55tR Dose Calibrator |
| Dulbecco’s modified Eagle’s medium | The American Type Culture Collection, Manassas, VA, USA | 30-2002 | |
| Fetal Bovine Serum (FBS) | The American Type Culture Collection, Manassas, VA, USA | 30-2020 | |
| Hanks Balanced Salt solution (HBSS) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 14025092 | For preparation of H-HBSS |
| Hydrochloric Acid (trace metal basis grade) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A508P212 | |
| Melanoma cells | The American Type Culture Collection, Manassas, VA, USA | CRL-6475 | |
| Methanol | Sigma-Aldrich, Inc., St. Louis, MO | 34860 | |
| Microcentrifuge tube | Eppendorf, Hamburg, Germany | 30108442 | Protein LoBind microcentrifuge tube |
| Murine GM-CSF | R&D Systems, Inc., Minneapolis, MN USA | 415-ML-010 | |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 15140-122 | |
| Phosphate Buffered Saline without Ca2+ and Mg2+ | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 10010023 | For washing cells |
| Saline | Covidien LLC, Mansfield, MA, USA | 1020 | 0.9% Sterile Saline Solution |
| Shaker | Eppendorf, Hamburg, Germany | T1317 | Thermomixer |
| Silica gel-rad-TLC paper sheet | Agilent Technologies Inc., Santa Clara, CA, USA | SGI0001 | iTLC-SG |
참고문헌
- Bhawnani, N., et al. Effectiveness of stem cell therapies in improving clinical outcomes in patients with heart failure. Cureus. 13 (8), e17236 (2021).
- Zakrzewski, W., Dobrzynski, M., Szymonowicz, M., Rybak, Z. Stem cells: past, present, and future. Stem Cell Research & Therapy. 10 (1), 68 (2019).
- Bukhari, A. B., Dutta, S., De, A. Image guidance in stem cell therapeutics: unfolding the blindfold. Current Drug Targets. 16 (6), 658-671 (2015).
- Momeni, A., Neelamegham, S., Parashurama, N. Current challenges for the targeted delivery and molecular imaging of stem cells in animal models. Bioengineered. 8 (4), 316-324 (2017).
- Gnecchi, M., Zhang, Z., Ni, A., Dzau, V. J. Paracrine mechanisms in adult stem cell signaling and therapy. Circulation Research. 103 (11), 1204-1219 (2008).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L., Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death & Disease. 9 (3), 282 (2018).
- Zhang, Q., et al. CAR-T cell therapy in cancer: tribulations and road ahead. Journal of Immunology Research. 2020, 1924379 (2020).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69 (2021).
- Shao, F., et al. Radionuclide-based molecular imaging allows CAR-T cellular visualization and therapeutic monitoring. Theranostics. 11 (14), 6800-6817 (2021).
- Sakemura, R., Can, I., Siegler, E. L., Kenderian, S. S. In vivo CART cell imaging: Paving the way for success in CART cell therapy. Molecular Therapy Oncolytics. 20, 625-633 (2021).
- Wang, Y., et al. Dendritic cell biology and its role in tumor immunotherapy. Journal of Hematology & Oncology. 13 (1), 107 (2020).
- Bulte, J. W. M., Shakeri-Zadeh, A. In vivo MRI tracking of tumor vaccination and antigen presentation by dendritic cells. Molecular Imaging and Biology. 24 (2), 198-207 (2022).
- Holland, J. P., Sheh, Y., Lewis, J. S. Standardized methods for the production of high specific-activity zirconium-89. Nuclear Medicine and Biology. 36 (7), 729-739 (2009).
- Larenkov, A., et al. Preparation of zirconium-89 solutions for radiopharmaceutical purposes: interrelation between formulation, radiochemical purity, stability and biodistribution. Molecules. 24 (8), 1534 (2019).
- Pandey, M. K., et al. A new solid target design for the production of 89Zr and radiosynthesis of high molar activity [89Zr]Zr-DBN. American Journal of Nuclear Medicine and Molecular Imaging. 12 (1), 15-24 (2022).
- Pandey, M. K., et al. Improved production and processing of 89Zr using a solution target. Nuclear Medicine and Biology. 43 (1), 97-100 (2016).
- Pandey, M. K., Engelbrecht, H. P., Byrne, J. P., Packard, A. B., DeGrado, T. R. Production of 89Zr via the 89Y(p,n)89Zr reaction in aqueous solution: effect of solution composition on in-target chemistry. Nuclear Medicine and Biology. 41 (4), 309-316 (2014).
- Bansal, A., et al. Novel 89Zr cell labeling approach for PET-based cell trafficking studies. EJNMMI Research. 5, 19 (2015).
- Bansal, A., et al. 89Zr]Zr-DBN labeled cardiopoietic stem cells proficient for heart failure. Nuclear Medicine and Biology. 90-91, 23-30 (2020).
- Friberger, I., et al. Optimisation of the synthesis and cell labelling conditions for [89Zr]Zr-oxine and [89Zr]Zr-DFO-NCS: a direct in vitro comparison in cell types with distinct therapeutic applications. Molecular Imaging and Biology. 23 (6), 952-962 (2021).
- Lee, S. H., et al. Feasibility of real-time in vivo 89Zr-DFO-labeled CAR T-cell trafficking using PET imaging. PLoS One. 15 (1), e0223814 (2020).
- Nicolas, C. T., et al. Hepatocyte spheroids as an alternative to single cells for transplantation after ex vivo gene therapy in mice and pig models. Surgery. 164 (3), 473-481 (2018).
- Yang, B., et al. Tracking and therapeutic value of human adipose tissue-derived mesenchymal stem cell transplantation in reducing venous neointimal hyperplasia associated with arteriovenous fistula. Radiology. 279 (2), 513-522 (2016).
- Nicolas, C. T., et al. Ex vivo cell therapy by ectopic hepatocyte transplantation treats the porcine tyrosinemia model of acute liver failure. Molecular Therapy. Methods & Clinical Development. 18, 738-750 (2020).
- Bansal, A., Sharma, S., Klasen, B., Rosch, F., Pandey, M. K. Evaluation of different 89Zr-labeled synthons for direct labeling and tracking of white blood cells and stem cells in healthy athymic mice. Scientific Reports. 12 (1), 15646 (2022).
- Behfar, A., et al. Guided cardiopoiesis enhances therapeutic benefit of bone marrow human mesenchymal stem cells in chronic myocardial infarction. Journal of the American College of Cardiology. 56 (9), 721-734 (2010).
- Charoenphun, P., et al. 89Zr]oxinate4 for long-term in vivo cell tracking by positron emission tomography. European Journal of Nuclear Medicine and Molecular Imaging. 42 (2), 278-287 (2015).
- Sato, N., et al. In vivo tracking of adoptively transferred natural killer cells in rhesus macaques using 89zirconium-oxine cell labeling and PET imaging. Clinical Cancer Research. 26 (11), 2573-2581 (2020).
- Volpe, A., Pillarsetty, N. V. K., Lewis, J. S., Ponomarev, V. Applications of nuclear-based imaging in gene and cell therapy: probe considerations. Molecular Therapy Oncolytics. 20, 447-458 (2021).
- Fogli, L. K., et al. Challenges and next steps in the advancement of immunotherapy: summary of the 2018 and 2020 National Cancer Institute workshops on cell-based immunotherapy for solid tumors. Journal for Immunotherapy of Cancer. 9 (7), e003048 (2021).
- Li, X., Hacker, M. Molecular imaging in stem cell-based therapies of cardiac diseases. Advanced Drug Delivery Reviews. 120, 71-88 (2017).
- Puges, M., et al. Retrospective study comparing WBC scan and 18F-FDG PET/CT in patients with suspected prosthetic vascular graft infection. European Journal of Vascular and Endovascular Surgery. 57 (6), 876-884 (2019).
- Butterfield, L. H. Dendritic cells in cancer immunotherapy clinical trials: are we making progress. Frontiers in Immunology. 4, 454 (2013).
- de Vries, I. J. M., et al. Magnetic resonance tracking of dendritic cells in melanoma patients for monitoring of cellular therapy. Nature Biotechnology. 23 (11), 1407-1413 (2005).
- Gosmann, D., et al. Promise and challenges of clinical non-invasive T-cell tracking in the era of cancer immunotherapy. EJNMMI Research. 12 (1), 5 (2022).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유