É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Demonstrar os usos do Spectrometer Novel Força Gravitacional para esticar e Medida Proteínas fibrosas
Neste Artigo
Resumo
Este é um passo-a-passo mostrando o objetivo, funcionamento e resultados representativos do espectrômetro de força gravitacional romance.
Resumo
O estudo da estrutura macromolecular tornou-se crítica para a elucidação dos mecanismos moleculares e função. Existem vários bio-instrumentos limitada, mas importante, capaz de testar a dependência força de características estruturais em proteínas. Escala tem sido um parâmetro limitante sobre a precisão pesquisadores podem perscrutar o mundo nanomechanical de moléculas, tais como ácidos nucléicos, enzimas e proteínas motoras que executam o trabalho de sustentação da vida. Microscopia de força atômica (AFM) é bem afinado para determinar estruturas de proteínas nativas fibroso com uma resolução distância a par com microscopia eletrônica. No entanto, em estudos AFM força, as forças são tipicamente muito maior do que uma única molécula poderá ter 1, 2. Armadilhas ópticas (OT) são muito bons em determinar a distância relativa entre as esferas de presos e que pode dar forças muito pequenas 3. No entanto, eles não rendem precisa comprimentos absoluta das moléculas em estudo. Simulações moleculares fornecem informações de suporte para tais experiências, mas são limitados na capacidade de lidar com os mesmos grandes tamanhos moleculares, prazos longos, e convencer alguns pesquisadores, na ausência de outras evidências 2, 4.
A força gravitacional espectrómetro (GFS) preenche um nicho importante no arsenal de um investigador, oferecendo uma combinação única de habilidades. Este instrumento é capaz de gerar forças tipicamente com 98% ou maior precisão do intervalo femtonewton à gama nanonewton. As medições de distância atualmente são capazes de resolver o comprimento absoluto molecular até cinco nanômetros, e relativa distâncias par talão de separação com uma precisão semelhante a uma armadilha óptica. Além disso, o GFS pode determinar alongamento ou desenrolando onde a força está perto de equilíbrio, ou fornecer uma força de classificados de justapor contra qualquer medida mudanças estruturais. É ainda possível determinar quantas resíduos de aminoácidos estão envolvidos em eventos desenrolando sob cargas fisiológicas força 2. Ao contrário de outros métodos onde há força de calibração extenso que deve preceder qualquer ensaio, o GFS não requer calibração tal força 5. Complementando os pontos fortes de outros métodos, o GFS vai colmatar as lacunas na compreensão do nanomecânica de proteínas vitais e de outras macromoléculas.
Protocolo
Introdução ao GFS Novel Configuração
O GFS consiste de vários componentes essenciais: Um microscópio de luz comum, uma montagem equatorial, uma câmera e um computador [Figura 1]. A câmara de célula de fluxo selada que contém a amostra é também indispensável de acordo com o projeto GFS. O microscópio de luz é montado na montagem equatorial de modo que o escopo pode ser rodado em diferentes orientações no espaço. Esta capacidade permite que o vetor estático de gravidade para ser explorada de modo que as amostras podem ser dinamicamente orientada em relação ao vetor para que a força da gravidade pode transmitir cargas piconewton gama-força para as amostras. A câmera substitui a lente do microscópio de luz da ocular para que ele possa registrar as mudanças na orientação da amostra. Este dados brutos é digitalizado e manipulado pelo computador para interpretar os dados reais e em vigor medidas de distância. O fluxo de câmara selada foi concebido para permitir que todos os graus de liberdade no espaço sem perda de amostra. Na câmara reside a molécula da amostra que está preso perto de um terminal a um "ancorado" talão que é colada à superfície da câmara. O término oposto é amarrado a um "mobile" talão, que é livre a partir da superfície da câmara. É esta pérola móvel, livres no tampão de ensaio que podem ser postas em prática pela força gravitacional, assim, que se estende a molécula amarrados em cargas tão baixa força [Figura 2]. A amostra simplesmente parece um par de microesferas sob o microscópio, embora ele não ter alguma experiência para discernir o bem utilizável pares acoplados por seu apego a uma molécula de pares em que ambos os grânulos estão sentados na superfície do fluxo de câmaras. Uma modificação no sistema é a adição de uma plataforma flutuante que detém o GFS e está suspensa por molas. Nesta configuração, uma vez que a amostra foi rodada em uma posição onde a força gravitacional pode agir sobre a amostra, a plataforma e todos os seus componentes podem ser descartados contra a mola constante. Perto de queda livre, a força que age na esfera móvel é perto de zero e na extensão máxima das nascentes ", a força gravitacional é multiplicado em até duas vezes. Desta forma, uma resposta de força / distância classificados podem ser representados graficamente para medir o comportamento de uma única molécula com cargas força diferente.
1. Preparação de microesferas
- Submergir cerca de 10 mg de contas de vidro ou sílica em 0,04% 3-Aminopropyltriethoxysilane (corte com acetona) por dois minutos.
- Enxágüe com duas mudanças de água destilada duas vezes e centrifugar a pelota a 2000 xg por 5 minutos. Elimine o sobrenadante.
- Adicionar 5 mL de tampão de acoplamento (0,01 M piridina corte com água destilada duas vezes e ajustar o pH a 6,0), e agitar a mistura vigorosamente. Centrifugar como descrito acima. Repita este passo três vezes.
- Para bolo molhado de contas, adicione 2 mL de solução gluteraldehyde 5% (corte gluteraldehyde com tampão de acoplamento). Agite vigorosamente.
- Sob um capuz, gire mistura / gluteraldehyde talão por 3 horas à temperatura ambiente.
- Centrífuga como acima e aspirar o sobrenadante.
- Lave as contas em 5 mL de tampão de acoplamento, agitando-os vigorosamente e centrifugar e aspirar o sobrenadante. Repita isso três vezes mais.
- Adicionar cerca de 15 mL do anticorpo desejado para contas e agitar vigorosamente. As contas devem ser rodados durante 16-24 horas.
- Sob o capô, adicionar 5 mL de uma solução de resfriamento M glicina (glicina corte com água destilada duas vezes e ajustar o pH a 7,0). Agite vigorosamente esta mistura e rodar por 30 minutos.
- Centrífuga e aspirar o sobrenadante.
- Adicionar 5 mL de tampão de lavagem (0,01 M Tris, pH 7.0; azida de sódio a 0,1%, 0,1% BSA, 0,15 M NaCl; e 0,001 M EDTA). Agite vigorosamente este, centrífuga e aspirar o sobrenadante. Repita este passo três vezes.
- Alterar buffer para baixo teor de sal tampão (0,1 M KCl, 0,02 M imidazol; 5 mM MgCl 2; acertar a pH 7,0). Repita três vezes.
2. Anexo amostra para Microesferas
- Pegue uma pequena quantidade de contas preparados (cerca de 2 mL de cada bolo de contas no entanto, se há uma discrepância grande em diâmetro entre os lotes, é vantajoso usar em torno de uma relação de 08:01 de grandes para contas pequenas) e adicioná-los um tubo de microcentrífuga com tampão de ensaio. Reduzir a concentração de sua proteína para cerca de 5 mM, utilizando o tampão de ensaio. Prepare pelo menos um volume total de 400 mL, incluindo o buffer, a proteína, e as contas.
- Gire essa mistura em torno de 1 RPM por 3 horas (se a proteína está agitado demais, ele vai agregar e tornar-se inútil).
3. Preparação de slides Câmara
- Revestimento uma lâmina de microscópio com espessura de nitrocelulose 0,01% (em acetato de amilo). Deixe este slide secar por cerca de 10 minutos.
- Com um cortador de vidro afiada, corte tampa deslizante, de modo a fazer uma câmara. Isto requer quatro tiras de vidro.
- Use o fato deory borda do copo e ajuntá-lo através de uma mancha de graxa de vácuo em ambos os lados da borda.
- Tiras de graxa imprensa revestido em nitrocelulose seca coberta de slides para criar uma caixa na superfície da lâmina.
- Pipetar cerca de 2 mL de mistura do grânulo / proteína tocando pipeta na superfície de vidro dentro da caixa.
- Adicionar cerca de 2-40 mL de tampão sal dependendo de como grande da câmara é.
- Pressione uma lamínula em cima da caixa que já está revestida com graxa de vácuo para terminar a câmara selada e tampão.
- Deixe deslize sentar num lugar plano para que as contas tenham tempo suficiente para ancorá-los ao nitrocelulose.
4. GFS Aquisição de Dados
- Montagem de slides para GFS estágio
- Monitorar o que a câmera está gravando GFS e procure legítimo "pares talão", em que o micro é ligado pequena perto do equador da microesfera de grande porte.
- Quando um par potencial talão é encontrado, vá até a profundidade de foco para determinar se o "mobile" talão não está descansando na superfície da lâmina.
- Uma vez que um par adequado é identificado, note ângulo móvel talão é longe d max (d max = a distância máxima entre os centróides das microesferas acoplada). Mover o alcance em condições de adquirir vídeo.
- O ângulo de deslocação do GFS deve ser suficiente para gravar d min, d max, min e d, que poderíamos chamar de 25-90 graus, dependendo do comprimento da molécula.
- RECORDE como o par viaja d min para d max e volta para d min.
- É uma boa idéia para também gravar um filme do fundo para que ele possa ser subtraída posteriormente para análise.
- Se estiver executando uma queda GFS, mova o escopo de volta para d max e registrar a queda de pelo menos 60 frames por segundo. A parte crítica é a oscilação em primeiro lugar, mas longos períodos de gravação também pode ser usado para o estudo dinâmico.
5. GFS Análise de Dados
- Transformar vídeo bruto em digitalmente imagem "thresholded" e executar macro em ImageJ para determinar a posição do centróide de cada grânulo em cada quadro do vídeo. Este também é para o vídeo cair.
- Despejar o X, Y e dados da área de ImageJ em Excel e traçar os pontos.
- Se um bom par talão foi adquirida pelo vídeo, um corcunda perceptível no gráfico é indicativo das contas estar em suas mais próximo (d min) e no ápice do gráfico é a posição de d max.
- Usando estes dados, o raio de cada esfera deve ser determinada precisamente em ImageJ e toda esta informação é colocada na equação aninhada:
d = [(g sin α) 2 + (g cos α + d max - g) 2] 0,5
g = [d min 2 + b 2 r - (r a + r b) 2] 0,5 = r sin β b
c = d max - r a - g
(D = distância entre centróides; g = força de gravidade; α = o ângulo em graus paralelo à lente objetiva; r b = raio de móveis talão; r a = raio de ancorado talão; = ângulo β de ligação fora do eixo da o equador do cordão ancorado. - Usando o raio equipados do talão móveis, que também dá o seu volume, e dada a densidade da esfera, a força do talão móvel transmite na molécula pode ser calculado em piconewtons após a flutuação do solvente é subtraído. Este método mede a força sobre a molécula amarrado em piconewtons e calcula o comprimento molécula absoluta entre os anexos de anticorpos em nanômetros. F = V (db) a (F = força, V = volume, d = densidade da microesfera de vidro, a aceleração a = devido à gravidade, b = a densidade da água deslocada).
6. Resultados representativos:
Se a preparação do grânulo é feito corretamente, haverá agregação de talão mínimo, embora ainda possa haver um amontoado ocasionais talão. Quando vistos através do escopo, deve haver uma distribuição razoável de contas se emparelhado ou não na câmara.
É importante para minimizar vibrações, tanto quanto possível, para fazer isso uma mesa de ar, absorvendo choques especiais para pés de um tripé que sustenta uma montagem EQ, ou no sistema que utiliza molas podem ser usados para o isolamento de vibração.
Outra dica útil relativamente à câmara de fluxo selada é deixá-lo repousar durante cerca de cinco minutos em um nível de tabela depois de ter sido totalmente construído. Isso permite que qualquer grânulos maiores unattached a flutuar para baixo através do buffer e descanso na camada de nitrocelulose. Se o slide eram vez montado diretamente em cima da conclusão, o investigador teria sempre têm de lidar com contas, literalmente, voando pelo campo de visão, e se isso acontece durante a aquisição de vídeo que pode corromper ªexperiência e. Se isso for feito corretamente, a fuga de talão é significativamente minimizado e os resultados mais limpo vídeo.
Quando um par potencial talão é identificado pelo operador GFS, é útil para colocá-lo através de uma rotação preliminar para monitorar o comportamento do par. Raramente, o talão grande não é solidamente fixado sobre o slide. Se isso acontecer, não há nenhum uso em utilizar o par, pois é fundamental que a maior permanência do grânulo ancorada em uma posição fixa por toda a duração da aquisição. Se o par é estável e não apresenta "roll talão ancorada", então ele é adequado para a experimentação.
Um gráfico de distâncias de separação talão versus mudança no ângulo em relação à gravidade pode ser usado para avaliar os dados adquiridos. Um resultado bom representante mostraria pouca separação em um planalto e como o cordão móvel liberta-se do talão ancorado por causa da influência da gravidade, o gráfico vai mostrar mais a separação. Isso continua até que um pico legal é alcançado, que é chamado d max e para baixo a curva começa novamente retornando à base d min [Figura 1]. Em condições ideais, esta assinatura é simétrica. Um resultado não-representativa iria mostrar um gráfico com os padrões incoerentes não mostrando nenhuma d distintas min-max-d d padrão min, ou ele iria mostrar as separações que são ordens de magnitude muito alta para uma única molécula, indicando talvez houvesse um pedaço de poeira entre as contas, ou talvez que o talão móveis simplesmente não foi anexado a todos. O processo de encontrar o par, atirando-o, processá-lo e analisá-lo parar de muitos tem lacunas onde imprópria pares talão são abatidos fora. Então, se você chegar ao final de todo o processo e você tem um comprimento de molécula que é consistente com os resultados anteriores, pode-se ser muito confiante de que o par original talão é representativo e pode ser incluído nos resultados. Em um bom dia, cerca de metade do tiro pares de esferas pode ser tomada até se tornar um ponto de dados legítimos. Por exemplo, o comprimento da bobina enrolada de miosina entre MF20 e MF30 anticorpos, é conhecido com base em dados e EM AFM, dados para abordagem 100 nm 2,7,8,9. Se o resultado é várias vezes esse comprimento, a amostra agregada. Os resultados aqui apresentados são a partir de experimentos de rotação padrão GFS e demonstrar uma distância de 96 nm ± 5 nm, [Figura 2], que concorda em estreita colaboração com as medições do MF30 (que liga a N-terminal de miosina subfragment-2) e MF20 (que se liga na meromyosin luz) distância de separação de anticorpos sobre a miosina deduzida a partir dos valores da literatura [Figura 3].
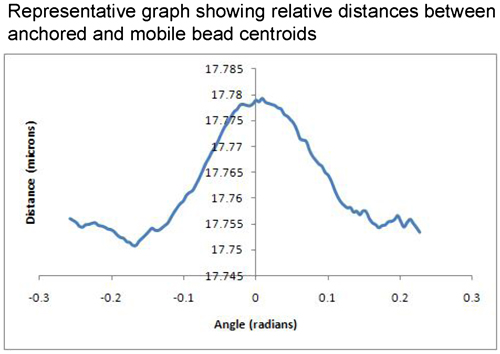
Figura 1. GFS configuração. Partes principais do GFS são rotulados.
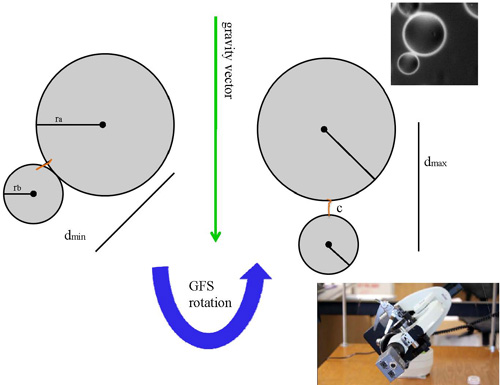
Figura 2. Esquemática do princípio GFS. Lado esquerdo mostra centróide de móveis talão a uma distância mínima de centróide de talão ancorado. Como GFS é girada, móveis talão alinha com o vetor de gravidade, que também é paralela com o eixo da molécula amarrados. Nesta posição, a distância entre os centróides das esferas móveis e ancorado é, no máximo. Canto superior direito mostra uma fatia representativa de um filme GFS. Parte inferior direita é uma imagem da rotação GFS passando.
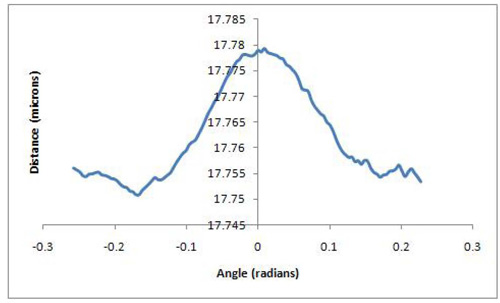
Figura 3 resultado Representante mostrando min d à esquerda do gráfico;. D max em uma separação relativa de 17,78 mícrons, e um retorno à d min em torno da linha de base de cerca de 17,75 microns de separação relativa entre as contas.
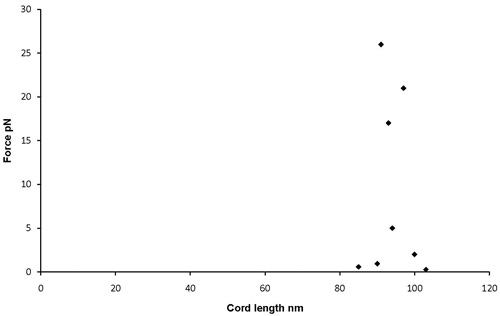
Figura 4. Resultado Representante do experimento de rotação GFS mostrando distância entre MF20 e MF30 anticorpos média 96 nm. Isso representa a duração aproximada de S2.
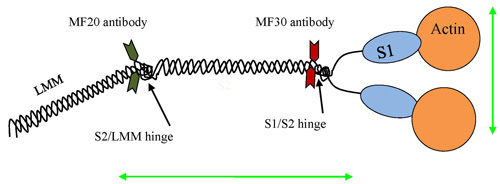
Figura 5. Miosina II dímero usado para mostrar anexos possível para uso com o GFS incluindo anticorpos e / ou anexos de actina. Possibilidades diferentes de fixação permite diferentes estratégias GFS para medir diferentes regiões, ou para aplicar força perpendicular ou paralelo ao domínio da haste do dímero miosina.
Access restricted. Please log in or start a trial to view this content.
Discussão
Ao converter um filme para uma representação digital thresholded, é crucial para a imagem thresholded para manter a mesma área em cada quadro do vídeo. Porque as contas em um par de esferas se movem independentemente um do outro, qualquer desvio nas áreas thresholded também pode causar as distâncias relativas entre os centróides das contas à deriva e introduzir erros significativos. Controlar a área limite reduzido o erro de cinco vezes nas medidas distância de 26 nm até 5 nm. Também é crucial para obter ...
Access restricted. Please log in or start a trial to view this content.
Divulgações
Agradecimentos
Este material é baseado num trabalho apoiado pela National Science Foundation, Grant No. 0842736.
Access restricted. Please log in or start a trial to view this content.
Materiais
| Name | Company | Catalog Number | Comments |
| 3-Aminopropyltriethoxysilane | Polysciences, Inc. | 919-30-2 | |
| Acetone | Fisher Scientific | A18P-4 | |
| Pyridine | Sigma-Aldrich | 110-86-1 | |
| Glutaraldehyde | Fisher Scientific | G7776 | |
| Glycine | Research Organics | BP381-1 | |
| Tris | Sigma-Aldrich | 9682T | |
| Sodium azide | Amresco | 71289 | |
| BSA | Sigma-Aldrich | AMR-0332-100G | |
| NaCl | Sigma-Aldrich | S7653 | |
| EDTA | MSI | E9884 | |
| Nitrocellulose | Sigma-Aldrich | 60443 | |
| N-N Dimethyl Formamide | Extracted from Large New | D4254 | |
| Rabbit skeletal myosin II | Zealand White Rabbits (7-8) | NA | |
| MF30 antibody (9-10) | Developmental Studies Hybridoma Bank | MF30 | |
| MF20 antibody (6) | Hybridoma Bank | MF20 | |
| Lab microscope | Boreal | WW57905M00 | |
| Equatorial mount | Celestron | CG-5 | |
| Digital video cam | Sony Corporation | XCDV60 | |
| Caliper release | Cabelas | IA-415482 | |
| Compression spring | Jones Spring Co. | 723 | |
| Extension spring | Jones Spring Co. | 770 | |
| ImageJ | National Institutes of Health | NA | |
| Fire-i drivers & application | Unibrain | 3.80 | |
| Excel | Microsoft | NA |
Referências
- Schwaiger, I., Sattler, C., Hostetter, D. R., Rief, M. The myosin coiled-coil is a truly elastic protein structure. Nat. Mater. 1, 232-235 (2002).
- Root, D. D., Yadavalli, V. M., Forbes, J. G., Wang, K. Coiled-coil nanomechanics and uncoiling and unfolding of the superhelix and alpha-helices of myosin. Biophysical Journal. 90, 2852-2866 (2006).
- Nishizaka, T., Miyata, H., Yoshikawa, H., Ishiwata, S., Kinosita, K. Unbinding force of a single motor molecule of muscle measured using optical tweezers. Nature. 377, 251-254 (1995).
- Gawalapu, R. K., Root, D. D. Fluorescence labeling and computational analysis of the strut of myosin's 50 kDa cleft. Arch. Biochem. Biophys. 456, 102-111 (2006).
- Kellermayer, M. S. Z. Visualizing and manipulating individual protein. Molecules Physiol. Meas. 26, R119-R153 (2005).
- Shimizu, T., Dennis, J. E., Masaki, T., Fischman, D. A. Axial arrangement of the myosin rod in vertebrate thick filaments: immunoelectron microscopy with a monoclonal antibody to light meromyosin. J. Cell Biol. 101, 1115-1123 (1985).
- Godfrey, J. E., Harrington, W. F. Self-association in the myosin system at high ionic strength. I. Sensitivity of the interaction to pH and ionic environment. Biochemistry. 9, 886-893 (1970).
- Root, D. D., Stewart, S., Xu, J. Dynamic docking of myosin and actin observed with resonance energy transfer. Biochemistry. 41, 1786-1794 (2002).
- Xu, J., Root, D. D. Conformational Selection during Weak Binding at the Actin and Myosin Interface. Biophys. J. 79, 1498-1510 (2000).
- Sattin, B. D., Pelling, A. E., Goh, M. C. DNA base pair resolution by single molecule force spectroscopy. Nucleic Acids Res. 32, 4876-4883 (2004).
Access restricted. Please log in or start a trial to view this content.
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados