Method Article
Especiação e biodisponibilidade Medidas de plutônio ambiental utilizando Difusão em Filmes Finos
Neste Artigo
Resumo
A técnica de gradientes difusivos em filmes finos (DGT) é proposto para estudos de especiação de plutónio. Este protocolo descreve experiências sondando o comportamento de difusão de Pu (IV) e Pu (V) na presença de matéria orgânica. DGTS implantados em uma mola karstic permitir a avaliação da biodisponibilidade de Pu.
Resumo
A captação biológica de plutônio (Pu) em ecossistemas aquáticos é particularmente preocupante uma vez que é um emissor de partículas alfa com meia-vida longa, que pode potencialmente contribuir para a exposição da biota e humanos. Os gradientes difusivos em fina técnica de filmes é introduzido aqui para medições in-situ de Pu biodisponibilidade e especiação. Uma célula de difusão construídos para experiências de laboratório com PU e o protocolo recentemente desenvolvidos permitem simular o comportamento ambiental de Pu em soluções modelo de várias composições químicas. Ajustamento dos estados de oxidação de Pu (IV) e Pu (V) descritas no presente protocolo é essencial, a fim de investigar a química redox complexa de plutónio no ambiente. A calibração da técnica e os resultados obtidos nas experiências laboratoriais permitem desenvolver um dispositivo DGT específico para medições in-situ Pu em águas doces. Medições de espectrometria de massa à base de Aceleradorde Pu acumulada por DGTS em uma mola cárstica permitiram determinar a biodisponibilidade de Pu em um ambiente de água doce mineral. A aplicação do presente protocolo para medições Pu usando dispositivos DGT tem um grande potencial para melhorar a nossa compreensão da especiação biológica ea transferência de Pu em ecossistemas aquáticos.
Introdução
O plutónio é um presente radionuclídeo artificial no meio ambiente como resultado da precipitação global, seguindo os testes com bombas nucleares e acidentes nucleares. A química redox de plutónio tem implicações importantes para a sua migração e dos ciclos biogeoquímicos nos sistemas aquáticos ambientais 1. O plutónio tem uma química complexa e pode existir em quatro estados de oxidação (III, IV, V, VI), ao mesmo tempo. Por conseguinte, a distribuição de espécies redox de plutónio em águas naturais é extremamente sensível ao ambiente químico local de 2,3. O estado de oxidação de plutônio também depende da origem da fonte - esta declaração ser mais relevante para ambientes contaminados e os locais de eliminação. Espécies de plutônio reduzidas (+ III e IV +) são encontrados predominantemente em ambientes anóxica e originárias de precipitação global e abastecido efluentes de resíduos, enquanto estados de oxidação mais elevados (+ V e VI +) pode ser encontrado entre os produtos de decaimento de outros actinidese em ambientes oxic 4.
A mobilidade eo comportamento ambiental de plutônio pode ser prevista em certa medida a partir da especiação redox. Plutónio sob + III + IV e estados de oxidação existe predominantemente em fase sólida e aumentou a capacidade de Sorb para colóides inorgânicos e ocorre naturalmente matéria orgânica (NOM) moléculas. O plutónio em + III + IV e os estados de oxidação é considerada como sendo menos móvel. Mais formas oxidadas solúveis de plutónio (+ V e VI +, sendo V + mais provável) 5 pode potencialmente contribuir para uma transferência biológica mais elevada para os organismos aquáticos, devido à maior mobilidade. No entanto, na presença de RNM, particularmente de ácido húmico, Pu (V) está a ser reduzida 17, deslocando o particionamento várias ordens de grandeza em favor da precipitação. Apesar do facto de a taxa de redução de Pu (V) para Pu (IV) é de 4 a 5 ordens de grandeza mais rápido do que a reacção inversa, remobilização de Pu (IV) sob condições oxidantes MAy também ter lugar uma. Dados experimentais recentes sobre sedimentos minerais modificados com Pu (IV), e submetidos a condições oxidantes naturais demonstraram que a concentração de Pu solúvel na fase aquosa, aumentou ao longo do tempo 1,6. Os autores explicam que por dessorção oxidativo de Pu (IV) e formação de Pu mais solúvel (V) e Pu espécies (VI). Oxidação de Pu (IV) pode também ocorrer devido a óxidos de manganês naturalmente encontradas 7. Estas observações são importantes para a modelagem de biodisponibilidade e avaliação dos riscos ambientais de eliminação de resíduos e sítios contaminados.
Os estudos sobre a biodisponibilidade e especiação de plutónio é uma tarefa desafiadora em laboratório e in-situ condições. Concentrações ambientais baixas, a variabilidade das espécies redox e as interações com colóides naturais tornam difícil para simular o comportamento biogeoquímico do plutónio. A técnica de gradientes difusivos em filmes finos (DGT) com base ema difusão de espécies livre de contaminantes e lábeis por meio de uma poliacrilamida (PAM) em gel é amplamente utilizado para medições ambientais de oligoelementos 8. Um amostrador DGT representa um dispositivo com três camadas feito de uma fase ligante (para a maioria dos metais vestigiais é a resina Chelex contido no gel PAM), camada de gel difusivo (gel de PAM de espessura variável) e uma membrana de filtro protector do gel e segurando o conjunto juntos. Filmes finos de gel de poliacrilamida, composta por 85% de água, permitir que as espécies complexas livres e instáveis para difundir mais rapidamente do que o plutônio obrigado a grandes moléculas NOM ou partículas coloidais naturais. Um set-up projetado para estudar a difusão de plutônio em filmes de gel PAM fina em condições de laboratório é chamado de célula de difusão 9.
A célula de difusão é um recipiente de dois compartimentos, onde dois compartimentos separados são interconectados por uma abertura de uma determinada superfície. A abertura, isto é, a janela entre as duas câmaras contains um disco de gel de difusão de uma dada espessura. Foi construída uma célula de Teflon com dois compartimentos de 100 ml e uma janela circular difusão 1,7 cm de diâmetro. Um compartimento é removível, o que facilita a montagem. Um sulco 0,5 cm de largura ao redor da janela esculpida a difusão no compartimento fixo serve para colocar o disco gel difusora. A profundidade do sulco deve ser semelhante à espessura do gel PAM destinado a ser utilizado. Nós escolher trabalhar com um gel de 0,39 mm de PAM, assim, a profundidade da ranhura na nossa célula de difusão é 0,39 mm. Uma imagem detalhada da célula de difusão é dada na Figura 1.
Quando uma solução contendo inicialmente plutónio é colocado em um compartimento (A), a difusão de espécies Pu vai estabelecer um gradiente de concentração do gel e irá começar a acumular-se no segundo compartimento (B), contendo inicialmente uma solução com a mesma composição química, sem Pu . A concentração inicial de espécies Pu no compartimento A é definido tal que permaNS constantes ou alterações muito pequenas (por 1% a 2%, no máximo) ao longo do experimento difusão. Determinação da quantidade de Pu difundida em função do tempo proporciona um meio para analisar a mobilidade das espécies Pu prevalecentes nas diferentes condições ambientais simuladas. A difusão em filmes finos fornece uma alternativa valiosa para estudos sobre a mobilidade Pu e especiação e pode ser aplicado com êxito em condições de campo 10. Pode-se substituir a célula de difusão por um amostrador passiva, fabricado com o gel difusivo PAM e resina Chelex como a fase ligante, que serve para acumular difundem espécies de PU. Tal amostrador pode ser exposta em condições de campo, - a quantidade de Pu acumulado na resina vai ser indicativa da especiação e a biodisponibilidade de Pu no respectivo ambiente de 10.
Neste trabalho, foi utilizada uma célula de difusão para investigar a mobilidade de Pu (IV) e (V) Pu espécies e suas interações com NOM em condições de laboratório. Furthermore, aplicamos grandes amostradores passivos DGT de uma superfície de 105 cm2 para estudar a biodisponibilidade de Pu em uma fonte cárstica da Swiss Jura Mountains (Rio Venoge), onde uma fração significativa de Pu foi encontrado nas partes intracelulares de musgos aquáticos em um trabalho anterior 11. Devido ao nível muito baixo de plutônio presente neste ambiente puro, foram utilizados espectrometria de massa (AMS) técnicas baseadas em aceleradores disponíveis no ETH Zurich para medir isótopos de plutónio.
Protocolo
1. O plutônio Tracer Preparação
- Pu (IV) preparação tracer
- A partir da solução stock de Pu Transferir uma alíquota apropriada contendo a quantidade desejada de PU para o experimento em um copo de vidro de 25 ml. Trabalhar com 10 Bq de Pu 239 de cada vez.
- Adicionar 1 ml de HNO 3 concentrado, 0,6 ml de 1 H H NaHSO4, 0,4 ml 2 SO 4 concentrado. Evapora-se até à secura sobre uma placa quente. Aquecer lentamente a 200 ° C no início, para evitar a projecção de ácido.
- Uma vez que nenhum líquido é deixado no recipiente, recozer o resíduo a 400 ° C - 500 ° C até que não há fumos brancos emanar. O resíduo é branca quando arrefecido e solúveis no tampão escolhido para a experiência.
Nota: Pu (IV) fonte preparado desta maneira pode ser armazenado a seco até vários meses 12.
- Preparação Pu (V) tracer 13
- Oxidação Pu
- Transferir uma alíquota do sto PuCK solução em um frasco de plástico de 20 ml de líquido de cintilação com uma tampa estanque. Trabalhar com 10 Bq de Pu 239 de cada vez. Adicionar 0,01 ml de 0,01 M de KMnO4 e deixar a mistura no escuro durante pelo menos 6 horas.
- Pu (VI) extracção
- Antes da extracção preparar uma solução de 0,5 M tenoiltrifluoroacetona (TTA) em ciclo-hexano e protegê-la da exposição à luz. Sempre preparar esta solução imediatamente antes de cada experiência.
- Adicionar à solução oxidada Pu 2 ml de 0,1 M CH3 COONa a pH 4,7 e 2 ml de 0,5 M tenoiltrifluoroacetona (TTA) em ciclo-hexano. Enrole a garrafa com uma folha de alumínio para manter a mistura reaccional no escuro, agitar durante 10 min. Separa-se a fase orgânica contendo Pu (VI) com uma pipeta de transferência e de um frasco de vidro limpo.
- Pu (VI) para Pu (V) fotoredução
- Deixar o frasco de vidro contendo Pu (VI) -TTA complexo em ciclo-hexano a luz ambiente durante 2 h.
- Pu (V) extracção
- Adicionar à luz exposta solução 1 ml de 0,1 M CH3 COONa a pH 4,7 e agita-se durante 5 min. Remover fase aquosa, contendo Pu (V). Determinar a concentração desta fonte por contagem de cintilação líquida, tendo uma alíquota de 100 ul.
Nota: Preparar Pu (V) soluções imediatamente antes de cada experiência uma vez que a estabilidade a longo prazo de Pu + V em estado de oxidação está a ser questionada.
- Adicionar à luz exposta solução 1 ml de 0,1 M CH3 COONa a pH 4,7 e agita-se durante 5 min. Remover fase aquosa, contendo Pu (V). Determinar a concentração desta fonte por contagem de cintilação líquida, tendo uma alíquota de 100 ul.
- Oxidação Pu
2. Preparação das soluções utilizadas nos experimentos
- Preparar soluções tamponadas
- Adicione solução 10 mM de MOPS (ácido 3- (N-morfolino) propanossulf único), tampão. Tome 200 ml desta solução e ajusta-se o pH desejado por adição gota a gota de HCl 0,1 M (pH 6,5 para utilização com Pu (IV) e pH 5,5 para utilização com Pu (V)).
- Preparar soluções para experimentos com Pu (IV)
- Solução A
- Dissolver Pu (IV) preparado no passo 1.1 em simililitros veral de 10 mM de MOPS solução tamponada a pH 6,5. Cuidadosamente lavar o copo com a mesma solução.
- Levar o volume a 72 ml com 10 mM de MOPS solução tamponada a pH 6,5. Verificar o pH e reajuste para 6,5 com NaOH 0,1 M. Transferir 72 ml desta solução para um copo limpo - esta é a solução (A) para ser introduzido no compartimento A da célula de difusão.
- Solução B
- Tomar 72 ml de 10 mM de MOPS a pH 6,5 solução tamponadas; adicionar 0,75 ml de 1 M de Na 2 SO 4. Verificar o pH, reajuste de 6,5, se necessário. Transferir 72 ml desta solução para um copo limpo - este é o «B» solução a ser introduzida no «B» do compartimento da célula de difusão.
- Preparar soluções com NOM
- Pesar 1,4 mg de fulvic liofilizado ou ácido húmico para obter uma concentração de 20 ppm e dissolvê-lo na «A» containi soluçãong Pu (IV). Preparar esta solução 24 h antes da experiência e para permitir o equilíbrio.
- Solução A
- Preparar soluções para experimentos com Pu (V)
- Solução A
- Dissolver Pu (V) obtido no passo 1.2.4 em 72 mL de 10 mM de MOPS a pH 5,5 solução tamponadas; adicionar 0,75 ml de 1 M de NaNO3. Verificar o pH e ajustar se necessário a 5,5. Transferir 72 ml desta solução para um copo limpo. Preparar a solução com Pu (V) imediatamente antes de experimentar.
- Solução B
- Tomar 72 ml de 10 mM de MOPS a pH 5,5 solução tamponadas; adicionar 0,75 ml de 1 M de NaNO3. Verificar o pH e ajustar se necessário a 5,5. Transferir 72 ml desta solução para um copo limpo.
- Preparar soluções com NOM
- Pesar 1,4 mg de fúlvico liofilizada ou ácido húmico para obter uma concentração de 20 ppm e dissolver no Uma solução contendo Pu (V). Deixar a solução durante 24 horaspara atingir o estado de equilíbrio entre Pu (IV) e (V) Pu espécies. Antes do experimento difusão executar uma extracção da fase líquida para determinar a fracção de Pu (V), tal como descrito na Secção 3.4.2.
- Solução A
3. experimentos de laboratório Difusão
- Prepare gel PAM
- Molhe uma bandeja de plástico com alguns ml de eletrólito (por exemplo, 10 mM NaNO 3), coloque a tira de gel PAM e expandir uniformemente sobre a superfície. Coloque cautelosamente um perfurador afiado de 2,7 cm de diâmetro sobre a superfície do gel. Evitar o deslizamento do punção sobre a superfície do gel.
- Use a iluminação focada local, se necessário, pode ajudar a visualizar o gel PAM transparente. Pressione o soco firmemente contra a superfície gel e solte uma vez que é cortado.
- Montagem da célula de difusão
- Posicione o disco de gel PAM com uma pinça na ranhura sobre a janela difusão de uma forma harmoniosa de rosto. Gire o parafuso de tal forma que o twO compartimentos da célula de difusão de manter unidas, entre si através do disco de gel de PAM.
- Mark A e B compartimentos da célula de difusão. Montagem da célula de difusão com o disco de gel imediatamente antes de cada experiência; não permitir que o gel seque.
- O lançamento de um experimento de difusão
- Lentamente, deitar as soluções A e B para os compartimentos correspondentes. Certifique-se de que ambas as soluções são derramadas com a mesma velocidade, de modo a fornecer um volume igual em cada um dos compartimentos em qualquer momento, de outra forma o gel difusora pode ser danificado.
- Inicie o cronômetro uma vez que as soluções estão na célula. Coloque os misturadores elétricos em miniatura sobre a célula de difusão. Nesta altura, a experiência de difusão é considerado iniciado.
- A recolha de amostras durante todo experimento difusão
- Retirar amostras de igual volume dentro de intervalos de tempo regulares a partir dos compartimentos A e B, simultaneamente, a fim de manter o volume constante durante todo o experiment.
- Tomar uma amostra 1,00 ml, simultaneamente, em cada um dos compartimentos imediatamente no início da experiência para determinar a concentração inicial Pu no compartimento de um.
- Use um intervalo de tempo de amostragem de 10 min em experimentos sem adição de NOM e 20 min para vários h em experimentos com ácido húmico. 2,00 ml alíquotas são suficientes para proporcionar uma boa sensibilidade para medições de alfa-espectrometria.
- Extracção em fase líquida de Pu (IV) e Pu (V)
- No final da experiência de difusão tomar separadamente 4 ml de amostras A e B os compartimentos em tubos de ensaio de plástico com tampas à prova de fugas. Acidifica-se amostras com 1 ml de HCl 2M.
- Adicionar 5 ml de 0,5 M de bis- (2-etil-hexil) fosfórico (HDEHP) solução em ciclo-hexano e agita-se tubos de ensaio vigorosamente durante 5 min. Deixar as amostras a fim de permitir a separação de fases. Remover a fase aquosa contendo Pu (V).
- Back-extração de Pu (IV)
- Back-extrato Pu (IV) a partir da fase orgânica restante com 5 mL de 5% (NH 4) 2 C 2 O 4.
- Retirar amostras de igual volume dentro de intervalos de tempo regulares a partir dos compartimentos A e B, simultaneamente, a fim de manter o volume constante durante todo o experiment.
Tratamento 4. Amostra
- Amostras de Spike com um padrão interno
- Pico amostras a serem analisadas com um traçador de rendimento. Use um pico de 1,00 ml de 242 Pu traçador de 25 MBq ml -1 concentração de actividade para medições de alfa-espectrometria.
- Oxidar matriz das amostras
- Evaporar amostras até à secura em uma chapa quente com 2,00 ml de HNO 3 concentrado.
5. separação radioquímica de Pu
- Ajuste Pu estado de oxidação
- Dissolve-se amostras secas a partir do ponto 4.2.1 em 5 ml de HNO 3 8 H, adicionar 20 mg de NaNO2, amostras de calor a 70 ° C durante 10 min. Esta etapa permite ajustar o estado de oxidação do Pu e + IV.
- Extracção em fase sólida de Pu
- Molhar uma resina de permuta aniónica em coluna quaternário à base de amina (tais como TEVA) com 1,5 mL de 8 M de HNO3. Use micro-colunas feitas de 1 ml ponta da pipeta com 100 mg da resina condicionada com 1,5 ml de 8 M de HNO3.
- Filtrar a solução de ponto 5.1.1 através da coluna de resina com taxa de fluxo de cerca de 1 ml min -1. Lavar o copo da amostra com 2 ml 8 M HNO3 três vezes e desmoronamentos de transferência para resina colunas.
- Elute Pu
- Lavar com 3 ml colunas 9 M de HCl. Elute Pu com 3 ml de solução 9 M HCl / 0,1 M HI. Evaporar eluatos na chapa quente. Trata-se com 2 ml de HNO 3 concentrado, evapora-se até à secura. Repita se necessário até que a cor do iodo marrom desaparece.
- Determinar a concentração nas amostras Pu por qualquer método disponível.
Nota. Para a gama de concentrações de 239 Pu utilizado neste protocolo alfa-espectrometria fornece uma boa sensibilidade. Prepare fontes de alfa-spectrometric contando por eletrodeposição em discos de aço inoxidável 14. Contagem de fontes no PIPS detector (450 mm 2) em um espectrómetro.
6. Análise dos Dados
- Plot difundido Pu versus tempo
- Traça-se a actividade de Pu (MBq) acumulada no compartimento B em função do tempo (min). Correta para o volume da amostra retirada durante a experiência de difusão: actividade acumulada de Pu (MBq) no tempo t é igual à concentração (mBq ml -1) determinado na amostra multiplicada pelo volume da solução (ml) na compartimento B no momento de amostragem (ver exemplo de folha de cálculo - Figura 2).
- Para traçar nos mesmos dados do gráfico de vários experimentos com diferentes concentrações Pu, as concentrações de uso normalizados para a concentração inicial de Pu compartimento A.
- Calcule o coeficiente de difusão
- Calcular coeficiente de difusão D (cm2 sec -1) das espécies de PU para cada experimento 10. Uso equação (1):
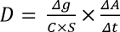 (1)
(1)
onde Δg é a espessura de gel de difusão (cm), C a concentração inicial Pu (MBq mL -1), S área de difusão (cm2), e A a actividade (MBq) de espécies Pu difundidos no compartimento B no momento t (seg). AA / Dt é o declive do gráfico linear de Pu difundida dentro do compartimento de B em função do tempo.
- Calcular coeficiente de difusão D (cm2 sec -1) das espécies de PU para cada experimento 10. Uso equação (1):
7. Estudos de Biodisponibilidade de Pu em Freshwaters naturais
- Prepare samplers DGT
- Molhar um tabuleiro de plástico com alguns ml de electrólito (por exemplo, 10 mM NaNO3), colocar a placa inferior (ver Figura 3) do dispositivo de amostragem DGT. Use a iluminação local, se necessário, pode ajudar a visualizar géis transparentes.
- Positiem uma tira de gel de resina Chelex seis centímetros × 22 centímetros e expandir de maneira uniforme sobre a superfície da placa. Colocar no topo da camada de gel de resina de uma tira de gel difusivo 6 cm × 22 cm PAM e expandir uniformemente sobre a superfície. Certifique-se de que os géis não são deslizantes e são posicionados de forma suave de rosto.
- Cobrir a camada de gel com uma difusivo 6 cm × 22 cm peça de uma membrana de filtro. Coloque a armação de cobertura do dispositivo de amostragem DGT (ver Figura 3) através da membrana filtrante e fechar o conjunto de pressionar ligeiramente o quadro nas bordas.
- Corte as partes que se estendem de gel com uma lanceta afiada, aberto e realinhar camadas de gel se necessário, até uma superfície de placa lisa é obtido. Fixe o conjunto com parafusos.
- Molhar os samplers DGT com alguns ml de eletrólito (por exemplo, 10 mM NaNO 3). Armazenar molhado em um saco plástico selado até várias semanas a 4-5 ° C.
- Implantação de DGTS em um corpo natural de água
- Leve o amostrador DGT para fora do saco de plástico. Corrigir samplers DGT no suporte como mostrado na Figura 4.
- Implante DGTS no corpo de água, quer suspendendo-os em uma corda forte ou a instalar num suporte vertical de uma forma estável para fornecer um fluxo constante de água tangencial ao longo da superfície da DGT. Implante dispositivos DGT nas águas doces para duas a três semanas, de modo a acumular o Pu numa concentração suficiente para as medições.
- Tratamento de DGTS recuperados
- Recuperar DGTS da água. Solte o conjunto, retire membrana de filtro e descarte. Retire a camada de gel superior (PAM gel difusora) e descarte.
- Transferir o gel de resina para um copo de vidro contendo 20 mL de 8 M de HNO3 e as amostras a serem analisadas pico com um traçador de rendimento. Use um pico de 1,00 ml de 242 Pu traçador de 0,25 MBq ml-1 (1,7 pg ml -1) para medições de concentração de actividade AMS. Depois de ter bem agitated, deixar amostras O / N para Pu eluição.
- Eluatos condição DGT
- Filtrar as soluções a partir das amostras de gel de resina; lavar os géis de resina restantes com 5 ml 8 M HNO3 e combinar washouts com amostras. Adiciona-se 20 mg de NaNO2 a cada amostra, aquecer as soluções a 70 ° C durante 10 min. Esta etapa permite ajustar o estado de oxidação do Pu e + IV.
- Extracção em fase sólida de Pu
- Molhar um cartucho de resina de permuta de aniões quaternários à base de amina com 10 mL de 8 M de HNO3. Passar as soluções de ponto 7.4.1 através do cartucho de resina de permuta com o caudal de cerca de 1 ml min -1. Lavar o copo com 5 ml de amostra 8 M HNO 3 três vezes e transferir os desmoronamentos de cartucho de resina de troca.
- Elute Pu
- Lavar com 10 ml de cartuchos 9 M de HCl. Eluir Pu com 15 ml de solução 9 M de HCl / 0,1 M HI. Evaporar fluido em uma placa quente. Tratar com 2 ml HNO 3 concentrado, eevaporam-se à secura. Repita se necessário até que a cor marrom iodo desapareceu completamente.
- Repetir separação radioquímica de Pu um a mais duas vezes maior se a purificação é necessária - dependendo do desempenho do sistema de detecção de Pu. Realizar a segunda e a terceira separações em micro-colunas feitas de 1 ml ponta da pipeta com 100 mg de resina de troca condicionados com 1,5 mL de 8 M de HNO3.
- Determinar a concentração nas amostras Pu. Use as técnicas de espectrometria de massa para medir 239 Pu por causa do baixo nível de plutónio no ambiente intocada.
Nota: Neste trabalho, usar o recurso AMS atento para análise dos actinídeos no Laboratório de Feixe de Íons Física no Instituto Federal Suíço de Tecnologia, em Zurique.
8. Análise dos Dados
- Calcular a concentração (DGT C em μBq ml -1) de biodisponível (lábil) Pu spECIES na água bruta a partir da quantidade de Pu acumulada pela DGT, durante o período de implementação. Uso equação (2):
 (2)
(2)
onde A é a actividade (μBq) de Pu acumulado na fase ligante, Δg a camada de difusão (gel de membrana de filtro +) Espessura (cm), D o coeficiente de difusão de Pu no gel PAM (cm 2 seg -1), S a área de difusão (cm2), e t o tempo de implantação (seg). - Compare C DGT de Pu determinado por DGTS com concentração Pu total na água bruta, bem como com outros dados disponíveis de especiação.
9. separação radioquímica para a Determinação do total Pu na água bruta
- Condição amostra de água
- Bombear água do corpo estudada de água através de uma membrana filtrante de 45 mm em uma plastic destinatário. Trabalhar com amostras de 10 a 50 L para medições AMS. Acidifica-se a água até pH 2 com HNO 3 imediatamente após a amostragem no local de amostragem antes do transporte para o laboratório.
- Precipitar Pu em hidróxidos de ferro
- No laboratório introduzir um agitador de topo no recipiente. Pico da amostra com Pu rendimento marcador. Use um pico de 1,00 ml de 242 Pu traçador de 0,25 MBq ml-1 (1,7 pg ml -1) para medições de concentração de actividade AMS.
- Adicionar FeCl3 · 6H 2 O levando cerca de 0,25 g por 10 L de amostra. Depois de ter agitado durante 30 min, precipitar os hidróxidos de ferro com NH4OH a pH 8.
- Em segundo lugar a precipitação de hidróxidos de ferro em Pu
- Decantar o sobrenadante da amostra de água do ponto 9.2.2. Recuperar o precipitado de hidróxidos de ferro em um copo de vidro de 2 L, lavar o recipiente com água deionizada e combinar as washouts com o SAMPle.
- Dissolve-se o precipitado em M ~ 100 mL de HCl 5, aquecer a 90 ° C para decompor os carbonatos. Filtrar se necessário, quando a solução é arrefecida. Re-precipitar hidróxidos de ferro com NH 4 OH a pH 8.
- Hidróxidos de ferro condição para análise
- Decantar o sobrenadante a partir da amostra do ponto 9.3.2. Recuperar o precipitado de hidróxido de ferro para um recipiente de centrifugação. Centrifugar, desprezar o sobrenadante. Lavar o precipitado com água desionizada. Repita 2-3 vezes.
- Dissolve-se o precipitado em 10 mL de 8 M de HNO 3, submeter-se a separação radioquímica de Pu, como descrito anteriormente nas secções de 7,4-7,6.
10. Preparar amostras para medições de AMS
- Precipitar Pu em hidróxidos de ferro
- Após a separação radioquímica, dissolver a amostra final em 0,5 ml de HCl 1 M, transferir a amostra com uma pipeta de plástico para um frasco de vidro de 2,5 ml. Lavar o twic amostra taçae com 0,5 ml de HCl 1 M, transferir o mesmo para lavagens frasco.
- Adicionar 0,5 ml de 2 mg ml-1 da solução de Fe3 + a proporcionar 1 mg de ferro. Precipitar os hidróxidos de ferro adicionando algumas gotas de NH 4 OH concentrado. Centrifuga-se e decanta-se o sobrenadante.
- Lavar o precipitado com água desionizada, de centrifugação e decanta-se o sobrenadante. Seca-se o precipitado sobre a placa quente a 90 ° C.
- Prepara-alvo para as medições AMS
- Asse os hidróxidos de precipitar a partir do ponto 10.1.3 em um forno para 2-3 horas a 650 ° C. Misture bem com 3-4 mg de pó de metal nióbio e prima em um suporte alvo Ti para medições AMS.
Nota: Nós medimos as amostras com o compacto (0,6 MV) sistema AMS "TANDY" no Instituto Federal Suíço de Tecnologia (ETH Zurich) sintonizado para medições de actinides 15,16.
- Asse os hidróxidos de precipitar a partir do ponto 10.1.3 em um forno para 2-3 horas a 650 ° C. Misture bem com 3-4 mg de pó de metal nióbio e prima em um suporte alvo Ti para medições AMS.
Resultados
Experimentos de difusão
Traçando as actividades de 239 Pu difundidos no compartimento da célula B da difusão em função do tempo dá uma representação visual do fluxo das 239 espécies Pu difundir através do gel de PAM. Os coeficientes de difusão calculados a partir destas parcelas de acordo com a equação 1 fornecem um meio adicional para comparar diferentes mobilidade de 239 Pu espécies redox em vários ambientes químicos, (Figura 2). A Figura 5 ilustra as experiências de difusão com Pu (IV) e Pu (IV) -pu (V) espécies mistas, respectivamente, nas tampão MOPS e na presença de 20 ppm de HA. Uma comparação destes lotes mostra que Pu (V) é significativamente mais móveis do Pu (IV) .Este é particularmente válido para Pu (IV) e Pu (V) quando HA (MW 5-40 kDa nas nossas experiências, caracterizado por o SI por Cusnir et ai.) 10 é adicionado como complexar moléculas. Pu (V) solut fonteion preparado de acordo com o protocolo descrito no presente documento contém espécies predominantemente Pu (V). Extracção da fase líquida com HDEHP no final da experiência de difusão nos MOPS solução tamponada encontrado 80% ± 10% de Pu (V). O rendimento químico desta extracção é de 80%. A solução com Pu (V) na presença de 20 ppm de HA foi equilibrada durante 24 h e Pu (V) na fracção desta solução modelo foi de 35% ± 10%.
Estudos sobre Pu biodisponibilidade em águas doces naturais
Vários dispositivos DGT construídas em nosso laboratório foram expostos com sucesso por períodos de duas a três semanas em uma mola cárstica do Jura montanhas suíças. Esta é uma fonte de água mineral com o pH da água na gama de 6,5-7,5, condutividade superior a 400 microsiemens por cm -1 e saturado com oxigénio. Estas experiências demonstraram boa aplicabilidade e robustez dos conjuntos de gel sem nenhum traço de biofouling, possivelmente também por causa de tele baixa temperatura da mola (7 ° C). DGTS recuperados após as implantações foram bem preservada, com camadas de gel intactas, conservando a forma inicial e aparência visual. Pu acumulada por DGTS foi analisada pela AMS. AMS oferece vantagens consideráveis sobre outras técnicas analíticas: é altamente sensível (para níveis sub-fg), e requer quantidade de amostra inicial muito inferior ao alfa-espectrometria ou técnicas de ICP-MS. Além disso, as interferências isobáricas moleculares, tais como o hidreto de urânio (238 UH), ou outras moléculas são eficientemente reprimido durante a medição AMS e não interfiram com a detecção 239 Pu. Por algumas razões técnicas (muito provavelmente uma contaminação com 239 Pu durante separações químicas), não fomos capazes de usar os dados para 239 Pu para as primeiras aplicações de DGTS no campo. No entanto, os resultados de 240 Pu foram imparcial. Assim, foi calculado o conteúdo de 239 Pu da medida 240 Pu, tendo 0,18 como Pu 240/239 relação atómica Pu para Fallout plutônio. Os resultados estão resumidos na Tabela 1.
239 concentrações Pu medidos em amostras de água a granel são semelhantes às concentrações reportados anteriormente para este aqüífero (1-7 μBq L -1) 11. Além disso, 239 concentrações Pu calculados a partir de medições da DGT são semelhantes dentro das incertezas de medição. Desde DGTS acumular únicas espécies livres e instáveis Pu, pode-se estimar a fração biodisponível de Pu nesta água. Os dados apresentados na Tabela 1 indicam que todas as 239 espécies Pu presentes na água são encontrados em grandes quantidades numa forma biodisponível. Este é um resultado interessante à luz de descobertas anteriores 11, que revelaram a acumulação predominante de 239 + 240 Pu na fracção intracelular dos musgos aquáticos crescimento em comparação com a mola 241 Am e 90 Sr. Os autores 11 sugerem que a maior mobilidade de Pu neste aquífero natural era devido à formação de um complexo de carbonato de Pu solúveis, possivelmente como uma forma plutonyl Pu (V), semelhante ao que ocorre naturalmente complexo de uranilo-carbonato. Água da mola Venoge é água dura, com alta concentração de carbonato e muito baixo teor de NOM (cerca de 1 ppm).
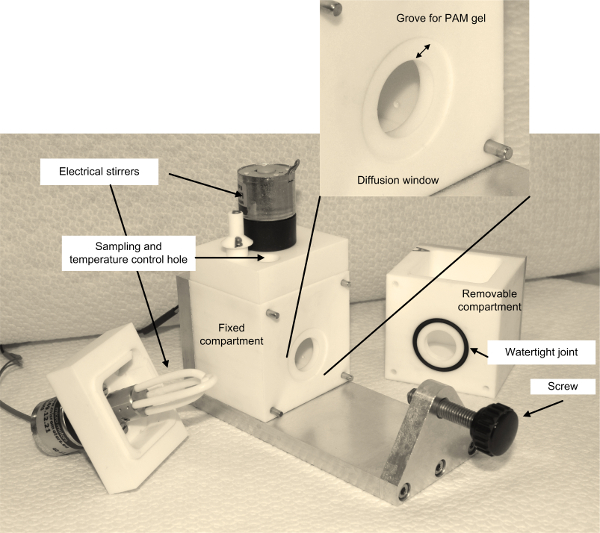
Figura 1. Difusão celular usado para experimentos em Pu difusão através do gel PAM. Os sulco 0,5 cm de espessura, a profundidade do sulco 0,39 milímetros. Por favor clique aqui para ver uma versão maior desta figura.
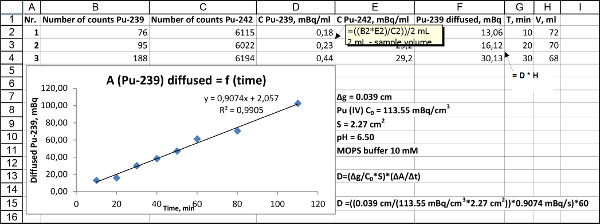
Figura 2. Snapshot da planilha do Excel usado para os cálculos do coeficiente de difusão. Por favor clique aqui para ver uma versão maior desta figura.

Figura 3. dispositivo de grande superfície DGT para medições de especiação Pu ambientais Os componentes do dispositivo DGT -. A placa de fundo ea armação de cobertura -. Retratada na esquerda, a montagem com furos equipe à direita Clique aqui para ver uma versão maior desta figura.

Figura 4. DGT dispositivos amostradores fixados no suporte (à esquerda) exposta no Venoge spring (à direita) para medições de biodisponibilidade Pu. Por favor clique aqui para ver uma versão maior desta figura.
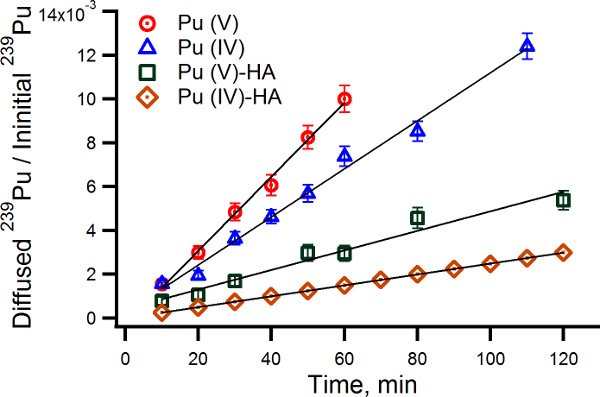
Figura 5. Lote de 239 a Pu difundido para dentro do compartimento B da célula de difusão em diferentes ambientes químicos. Os pontos de dados experimentais são dados para 239 Pu (IV) e 239 Pu (V), respectivamente, em tampão de MOPS, bem como para 239 Pu (IV) - Pu 239 (V) misturados entre espécies (35% ± 10% de Pu (V)), na presença de HA. A linha mostrada para 239 Pu (IV) -HA foi calculada utilizando um coeficiente de difusão de 0,50 x 10 -6 cm 2 s -1 10 previamente determinada. Os coeficientes de difusão calculados a partir da equação 1 são: Pu (IV) em tampão MOPS - 2,29 x 10 -6 cm 2 seg -1, Pu (V) em tampão MOPS - 3,50 x 10 -6 cm 2 seg -1, Pu (IV) - Pu (V) com HA - 0,92 x 10 -6 cm 2 s -1. De cima para baixo: Pu (V) em tampão MOPS (círculo aberto vermelho), Pu (IV) no tampão MOPS (azuis triângulos abertos), Pu (IV) - Pu (V) na presença de 20 ppm de HA (verde quadrados abertos), Pu (IV) na presença de 20 ppm de HA (losangos castanhos). Por favor clique aqui para ver uma versão maior desta figura.
| Tipo de amostra | Número de medições | 239 concentração Pu, μBq L -1 |
| Massa de água | 2 | 1,9 ± 0,55 |
| DGT 0,39 milímetros | 2 | 1,74 ± 0,9 |
| DGT 0,78 milímetros | 1 | 1,79 ± 0,9 |
Tabela 1. Os resultados representativos para 239 medições Pu por AMS em volume de água e amostradores DGT. 239 Pu na água bruta foi co-precipitado a partir de 20 L de água com hidróxidos de ferro, extraiu-se na resina de permuta específicos de actinídeos e medido pela AMS . 239 concentrações de PU para medições DGT calculados usando a equação 2 e coeficiente de difusão para Pu (IV). Incertezas para k = 2; U (95).
Discussão
A metodologia DGT descrito aqui para experimentos com Pu usando uma célula de difusão fornece uma abordagem confiável para vários estudos sobre Pu espécies redox e suas interações com moléculas orgânicas, partículas coloidais e sistemas ambientais simuladas. Outras aplicações de DGTS para medições ambientais de Pu vai contribuir para a nossa compreensão da biodisponibilidade e o destino deste radionuclídeo em ecossistemas aquáticos.
Experimentos de difusão Laboratório
A fim de realizar um experimento de difusão bem sucedida com conclusões significativas sobre a mobilidade Pu e interações sobre um ambiente químico específico, bem definidos e devem ser fornecidas condições controláveis. O ajuste de pu estados de oxidação antes da experiência é essencial para simplificar a interpretação dos dados, bem como para simular vários comportamentos bioquímicos das espécies redox Pu. A sensibilidade das espécies de Puvariações do pH faz buffer as soluções de uma obrigação. Atenção especial deve ser atraídos para as características de células de difusão e de configuração: o uso de material de polímero não-adsorvente Teflon evita adsorção nas paredes celulares e permite um conjunto robusto à prova de fugas, evitando a perda de Pu de difundir soluções durante o experimento.
A concentração Pu inicial a ser introduzido no compartimento A, bem como o intervalo de amostragem e o volume de cada amostra recolhida durante o ensaio de difusão depende do método analítico disponível no laboratório. Qualquer método analítico disponível pode ser utilizado para a determinação da concentração de Pu nas amostras a partir da célula de difusão, no entanto esta opção está estreitamente relacionada com a actividade inicial de Pu tomado para o experimento. 10 Bq de 239 Pu como recomendado neste protocolo (dando 100-140 MBq ml -1 ou ~ 2 × 10 -13 mol ml -1) são suficientes para proporcionar sensibilidade suficiente para measurementos por espectrometria alfa-e, geralmente, não apresentam problemas específicos para os regulamentos de protecção contra radiações. A concentração inicial de Pu pode ser reduzido se, outras técnicas analíticas, mais sensíveis estão disponíveis para a determinação Pu (por exemplo, espectrometria de massa). Intervalo de amostragem pode ser seleccionado para cada experiência de difusão em função da concentração inicial de Pu, e a taxa esperada de difusão através do gel de PAM. Apesar do facto de que as alíquotas de experiências de difusão não contêm outros radionuclidos de Pu, a presença de sais minerais e de o tampão de MOPS pode interferir com o procedimento analítico, reduzindo a eficiência e a precisão da análise quantitativa. Por isso, é preferível realizar a separação química de Pu sobre estas amostras.
A célula de difusão proporciona a melhor abordagem para o estudo da difusão em gel PAM vez que o gel é exposto directamente a uma solução bem agitada. Assim, os efeitos da bo difusivocamada undary (DBL) na superfície do gel são consideradas insignificantes. Boa agitação das soluções durante uma experiência de difusão é essencial, o que permite minimizar os efeitos DBL. Ao mesmo tempo, deve-se proceder com cuidado, a fim de não perturbar o gel PAM.
Os estudos de biodisponibilidade Pu em águas doces naturais
Os resultados produzidos por este protocolo mostra que a medição plutônio com dispositivos DGT fornece uma ferramenta eficiente para estudar a biodisponibilidade de plutónio em água doce. DGT produzir medições de concentração-tempo da média da espécie livre e lábil, as duas formas mais importantes para a captação biológica por organismos vivos. Além disso, a cinética da interacção de Pu com a matéria orgânica pode ser investigada através de géis de espessura diferente. O tempo necessário para as espécies de Pu-NOM de se difundir através do gel vai permitir que para os complexos mais lábeis para dissociar. Medições DGT pode ser complementado by técnicas de ultrafiltração, que produzem a percentagem de espécies coloidais Pu acima de um determinado tamanho (por exemplo, 8 kDa). Espécies coloidais Pu são geralmente considerados como espécies não biodisponível e fazem parte da fração Pu não mensurável usando DGT.
Neste ponto, os dispositivos DGT foram implantadas apenas em água doce de uma mola cárstica do Jura montanhas suíças. Baixas concentrações de Pu ambientais requerem uma implantação de longo prazo de dispositivos DGT, que podem encontrar desvantagens potenciais. A bio-incrustação da superfície do DGT representa uma desvantagem significativa, o aumento da espessura DBL e limitando assim o fluxo de Pu através do gel PAM. Encadernação fase dos DGTS expostas em águas marinhas ou águas de alta mineralização pode ser rapidamente saturado com outros metais traço, deturpar os dados para a acumulação de Pu. Determinação dos níveis de traço de Pu ambiental exige uma separação radioquímica completa e métodos analíticos muito sensíveis. Medição AMSs aplicadas neste protocolo não são amplamente disponíveis, mas pode ser substituída por outras técnicas de espectrometria de massa. No entanto, uma separação radioquímica rigorosa é necessária para eliminar a interferência isobárica 238 UH a partir de urânio que ocorre naturalmente.
A equação 2 mostra que o tamanho do dispositivo DGT é um parâmetro essencial que pode ser afinado para aumentar a quantidade de Pu acumulado durante um determinado tempo de implantação. Tiras de gel comerciais estão disponíveis apenas com uma superfície máxima de 6 cm x 22 cm. Portanto, a janela do amostrador DGT foi aumentada para 105 cm 2 (5 cm x 21 cm), tornando possível acumular suficiente de espécies de PU para os tempos de implantação relativamente curtos. A montagem de um tal amostrador DGT requer precisão e em especial consideração as propriedades de folhas de gel PAM ao manipular. É de fundamental importância para montar camadas de gel em um uniforme de rosto liso "sanduíche", a fim de fornecer uma homogers fluxo de espécies Pu da água bruta através do gel difusora. Bom fluxo de água na superfície do DGT é também um parâmetro importante, no entanto, é em grande parte determinada por condições de fluxo no aquífero. Recomenda-se a colocar os dispositivos para medições DGT Pu a cerca de 45 ° para a direcção do fluxo de água, a fim de proporcionar uma fonte de água constante e minimizar os efeitos da DBL.
Coeficiente de difusão utilizado na equação 2 deve ser corrigida, se a temperatura do corpo de água estudado é diferente da temperatura para a qual o coeficiente de difusão foi determinada. Os efeitos da temperatura sobre coeficientes de difusão são dadas pela equação de Stokes-Einstein (equação 3): 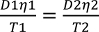 (3)
(3)
onde D 1 e D 2 são os coeficientes de difusão (cm2 s @ 1), η 1 e 2 são viscosidades η (mPa sec) de Water a temperaturas T 1 e T 2 (K), respectivamente.
Actualmente, não existe nenhum método para investigar Pu especiação em ambiente limpo, com excepção para os cálculos termodinâmicos com base em, por exemplo, pH e redox parâmetros. Estes parâmetros só estão disponíveis para as macro-componentes, tais como carbonatos, ferro ou manganês cátions. Assim, Pu especiação é derivado dessas espécies mensuráveis, mas não representa uma medida de "real". Aqui nós pensamos que a difusão em técnica fina película de gel PAM como apresentada neste artigo é um passo importante para a resolução do problema especiação Pu porque permite a medição in situ livres e espécies instáveis e, possivelmente, evidenciando espécies plutonyl. Embora apenas algumas medições DGT da Pu ambiental em águas doces foram realizadas até agora, os resultados obtidos são encorajadores para futuras aplicações da técnica DGT para Pu estudos de especiação e biodisponibilidade.Implantação de DGTS em águas orgânicos ricos potencialmente fornecer informações importantes sobre a mobilidade e as interações Pu na presença de moléculas de NOM. Resultados interessantes deve ser esperado a partir de medições da DGT em ambientes marinhos contaminados, como os mares costeiros ao redor da usina de reprocessamento nuclear de Sellafield e de Fukushima Daiichi usina nuclear danificada.
Divulgações
The authors have nothing to disclose.
Agradecimentos
This work was funded by the Swiss National Science Foundation (grant n° 200021-140230) and by the Swiss Federal Office of Public Health (PF and PS). We thank the Swiss Federal Office of Public Health for providing financial support for the open-access publication of this paper.
Materiais
| Name | Company | Catalog Number | Comments |
| 239Pu tracer | CEA | Source PU239-ELSC10 | |
| 242Pu tracer | LNSIRR | Source Pu242 N° 790 from Laboratory for National Standards of Ionizing Radiation of Russia | |
| 25 ml Beakers | |||
| Pipette | Socorex | ||
| Disposable plastic pipettes | Semadeni | ||
| 20 ml Plastic scintillation vial | Semadeni | ||
| Aluminium foil | |||
| Hot plate | |||
| Tweezers | |||
| Actinide exchange resin - TEVA - B | Triskem | TE-B50-A | |
| Actinide exchange resin - TEVA - R cartridges | Triskem | TE-R10-S | |
| 1 ml Pipette tips | Socorex | ||
| PAM gel strip 6×21 cm | DGT Research Ltd | 0.39 mm and 0.78 mm thickness / www.dgtresearch.com | |
| Chelex gel strip 6×21 cm | DGT Research Ltd | 0.40 mm thickness / www.dgtresearch.com | |
| Diffusion cell | Fabricated / in-house workshop | ||
| Ø 27 mm Punch | Fabricated / in-house workshop | ||
| Plastic tray | |||
| DGT set-up | Fabricated / in-house workshop | ||
| Membrane filter | PALL Corporation | HT-450 Tuffryn Polysulfone Membrane Disc Filter 0.45 μm / 145 μm thickness | |
| Nitric acid | Carlo Erba | 408025 | |
| Sulfuric acid | Sigma-Aldrich | 84720 | |
| Hydrocloric acid | Carlo Erba | 403981 | |
| Hydriodic acid | Merck | 100341 | |
| Potassium permanganate | Merck | 105082 | |
| Sodium hydrogen sulfate | Merck | 106352 | |
| Sodium sulfate | Merck | 106647 | |
| Sodium nitrate | Sigma-Aldrich | 31440 | |
| Sodium nitrite | Fluka | 71759 | |
| Sodium acetate | Merck | 106281 | |
| Ammonium oxalate | Fluka | 9900 | |
| Bis-(2-ethyl hexyl) phosphoric acid (HEDHP) | Merck | 177092 | |
| 2-thenoyltrifluoroacetone (TTA) | Fluka | 88300 | |
| MOPS buffer | Sigma-Aldrich | M9381 | MOPS sodium salt |
| Cyclohexane | Carlo Erba | ||
| Humic acid | Extracted from an organic-rich soil of an Alpine Valley, freeze-dried, MW 5-40 kDa | ||
| NH4OH | Carlo Erba | 419943 | |
| FeCl3·H2O | Sigma-Aldrich | 44944 |
Referências
- Kaplan, D. I., et al. Influence of oxidation states on plutonium mobility during long-term transport through an unsaturated subsurface environment. Environ. Sci. Technol. 38 (19), 5053-5058 (2004).
- Taylor, D. M. Environmental plutonium - Creation of the universe to twenty-first century mankind. Plutonium in the Environment. 1, 1-14 (2001).
- Maher, K., Bargar, J. R., Brown, G. E. Environmental Speciation of Actinides. Inorganic Chemistry. 52 (7), 3510-3532 (2013).
- Kurosaki, H., Kaplan, D. I., Clark, S. B. Impact of environmental curium on plutonium migration and isotopic signatures. Environ. Sci. Technol. 48 (23), 13985-13991 (2014).
- Orlandini, K. A., Penrose, W. R., Nelson, D. M. Pu(V) as the stable form of oxidized plutonium in natural-waters. Marine Chemistry. 18 (1), 49-57 (1986).
- Kaplan, D. I., et al. Eleven-year field study of Pu migration from Pu III, IV, and VI sources. Environ. Sci. Technol. 40 (2), 443-448 (2006).
- Morgenstern, A., Choppin, G. R. Kinetics of the oxidation of Pu(IV) by manganese dioxide. Radiochim. Acta. 90 (2), 69-74 (2002).
- Davison, W., Zhang, H. In-situ speciation measurements of trace components in natural-waters using thin-film gels. Nature. 367 (6463), 546-548 (1994).
- Zhang, H., Davison, W. Diffusional characteristics of hydrogels used in DGT and DET techniques. Anal. Chim. Acta. 398 (2-3), 329-340 (1999).
- Cusnir, R., Steinmann, P., Bochud, F., Froidevaux, P. A DGT Technique for Plutonium Bioavailability Measurements. Environ. Sci. Technol. 48 (18), 10829-10834 (2014).
- Froidevaux, P., Steinmann, P., Pourcelot, L. Long-Term and Long-Range Migration of Radioactive Fallout in a Karst System. Environ. Sci. Technol. 44 (22), 8479-8484 (2010).
- Bajo, S., Eikenberg, J. Preparation of a stable tracer solution of plutonium (IV). Radiochim. Acta. 91 (9), 495-497 (2003).
- Saito, A., Roberts, R. A., Choppin, G. R. Preparation of solutions of tracer level plutonium (V). Anal. Chem. 57 (1), 390-391 (1985).
- Bajo, S., Eikenberg, J. Electrodeposition of actinides for alpha-spectrometry. Journal of Radioanalytical and Nuclear Chemistry. 242 (3), 745-751 (1999).
- Dai, X. X., Christl, M., Kramer-Tremblay, S., Synal, H. A. Ultra-trace determination of plutonium in urine samples using a compact accelerator mass spectrometry system operating at 300 kV. Journal of Analytical Atomic Spectrometry. 27 (1), 126-130 (2012).
- Christl, M., et al. The ETH Zurich AMS facilities: Performance parameters and reference materials. Nuclear Instruments and Methods in Physics Research B. 294, 29-38 (2013).
- Blinova, O., et al. Redox interactions of Pu(V) in solutions containing different humic substances. Journal of Alloys and Compounds. 444, 486-490 (2007).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados